Изобретение относится к новой артроподицидной пестицидной композиции, содержащей в качестве активного ингредиента специальную пиретроидную комбинацию, производную фосфорной кислоты и при необходимости пиперонилбутилат и/или наполнители.
Изобретение относится к композиции, содержащей несколько активных ингредиентов по отношению к артроподам, и эта композиция содержит в качестве активного ингредиента пиретроиды и сложные фосфатные эфиры и, при необходимости, пиперонилбутилат, и наполнители и в качестве пиретроидного компонента эта композиция содержит 0,1-40 мас. циперметрина, состоящего на 40-100 мас. из 1R цис S и/или 1R трансS стереоизомера вне восьми возможных изомеров и находящихся по отношению к циперметриновому изомеру в соотношении 1:(1-99), эта композиция по меньшей мере содержит одну фосфорную кислоту, тиофосфорную кислоту или дитиофосфат, являющиеся токсичными по отношению к артроподам.
Одной из очевидных причин использования смеси активных ингредиентов является различная чувствительность отдельных насекомых по отношению к используемым химикатам. И часто оказывается дешевле, проще или более эффективно использовать соответствующим образом смешанные компоненты в форме одной единичной композиции. (I. stored Prod. Res, 1977, vol. 13.129-137; Pesric Sci, 1983.  385-398; Pestic Sci. 1983.
385-398; Pestic Sci. 1983.  373-384; IPPS 50 58237/1975/1973; 54 95730/1979/1978; 54 92625; 53 62830/1970/1976.
373-384; IPPS 50 58237/1975/1973; 54 95730/1979/1978; 54 92625; 53 62830/1970/1976.
Хорошо известно, что абсорбированные пиретроиды становятся неэффективными в организмах насекомых за счет различных механизмов. Один из этих методов устранения токсичности заключается в воздействии различных эстераз: путем расщепления сложной эфирной связи пиретроид подвергается гидролизу в нетоксичную молекулу. Сложные фосфатные эфиры ингибируют определенные вариации энзимов, метаболизирующих пиретроиды. Эстеразы являются различными по отношению к видам, специфическому характеру местного субстрата и к кинетическим параметрам. Поэтому ингибирующая активность конкретного ингибитора эстеразы является различной. В связи с этим в том случае, если на один вид эстеразы ингибитор оказывает воздействие, влияющее на метаболизм данного пиретроида, то нельзя сказать о возможном взаимодействии с другим видом или другой пиретроидной молекулой.
Так, например, инсектицид, такой как профенофос, эффективно ингибирующий энзимы, гидролизирующие перметрин, циперметрин, не оказывает влияния на активность пиретроидов, что было измерено на личинках Tribolium castaneum (Pestic. Biochem. Physiol. 1980,  81-85, Pestic. Sci. 1983
81-85, Pestic. Sci. 1983  367-372.
367-372.
Другим примером противоречивых результатов является то, что инсектицидный хлорпиринфос действует как синергетик флуцитрина и фенвалерата на Spodoptera littoralis, но он также действует как антагонист по отношению к токсичности циперметрина (BCPC Proceedings том 3: 943). По отношению к тем же самым видам монокротофос, профенофос, азинфос-метил и ацефат действуют как агенты-синергетики в широком диапазоне комбинаций вместе с циперметрином, фенвалератом и дельтаметрином.
Следующие комбинации являются исключениями:
фенвалерат + азинфос метил, дельтаметрин + азинфос метил и дельтаметрин + профенофос, в виде двойных смесей (Phytoparasitica 1986.  /2/:101), которые обладают аддитивным или антагонистичным взаимодействием. Синергизм может быть показан только при оральном применении активных ингредиентов, топические испытания не показали какого-либо результата.
/2/:101), которые обладают аддитивным или антагонистичным взаимодействием. Синергизм может быть показан только при оральном применении активных ингредиентов, топические испытания не показали какого-либо результата.
Что касается стойкости, то положительные результаты могут ожидаться при применении таких комбинаций, для которых активность индивидуальных компонентов характеризуется отрицательной взаимной корреляцией. Одной из наименее тщательно исследованных смесей является смесь, состоящая из фенвалерата и азинфос-метила и отрицательная взаимная корреляция по отношению к клещам вида Tetranychus urticae описывается в журнале Nature 1979  :298. Смесь двух активных ингредиентов в соотношении 1:1 приводит к высокой активности по отношению к клещам, устойчивым к воздействию (Pestic. Sci. 1980 11:600).
:298. Смесь двух активных ингредиентов в соотношении 1:1 приводит к высокой активности по отношению к клещам, устойчивым к воздействию (Pestic. Sci. 1980 11:600).
В соответствии с D BP 27 57 768 смеси, содержащие перметрин в качестве одного компонента и бромофозетил, хлорпирифос, бромфос, мелатион и диазинон, в качестве второго компонента, обладают антагонистическим взаимодействием в нормальных лабораторных условиях по отношению к домашним мухам (Musca domestica), но по отношению к сельскохозяйственным насекомым и устойчивым популяциям величина 50% летальной дозы имеет амплитуду на один порядок выше, что фактически свидетельствует о наличии синеpгистического эффекта. Что касается Christoneura occidentalis, принадлежащих к виду Lepidoptera, то хлорпирифос обладает синеpгистическим эффектом с дельтаметрином в соотношении 10:1, но действует как антагонист по отношению к перметрину и фенвалерату (I. Econ. Entomol. 1984,  16-22), в то время как на другие виды Lepidoptera (Ostrinia nubialis) комбинация из перметрина и хлорпирифоса демонстрирует значительный синергистический эффект в широком диапазоне комбинаций (I. Econ. Entomol, 1982
16-22), в то время как на другие виды Lepidoptera (Ostrinia nubialis) комбинация из перметрина и хлорпирифоса демонстрирует значительный синергистический эффект в широком диапазоне комбинаций (I. Econ. Entomol, 1982  28-30).
28-30).
В принципе может случиться так, что синергистический эффект может наблюдаться по отношению к чувствительному штамму и на уже устойчивом штамме может наблюдаться антагонизм. В качестве примера такого эффекта можно упомянуть взаимодействие циперметрина и монокротофоса по отношению к Spodopterа littoralis (Mod. Fac. Iandbouw. Rijksuniv. Cent, 50/2b, 1985 751).
Сокращение, используемое в таблице, приведенной в данном описании, представляет собой:
CIP циперметрин альфа-циано-3-феноксибензил-3-(2,2-дихлорвинил)-2,2-диме- тил-циклопропан -карбоксилат;
CHX "цинмикс" вне возможных изомеров циперметрина, в соотношении 40:60 из изомеров 1RцисS + 1SцисR 1RтрансS + 1S трансR;
TRX трансмикс вне возможных изомеров циперметрина; в соотношении 50:50 смесь 1RтрансS 1S трансR изомеров.
QUI хиналфос 0,0-диэтил-0-хиноксалин-2-ил фосфоротиоат;
DIA диазинон 0,0-диэтил-0-2-изопропил-6-метилпиримидин-4-ил фосфоротиоат;
TRIA триазофос 0,0-диэтил-0-1-фенил-1Н-1,2,4-триазол-3-ил фосфортиоат;
MET метидатион S-2,3-дигидро-5-метокси-2-оксо-1,3,4-тиадиазол-3-ил-метил- 0,0-диметил- фосфородитиоат;
HEPT гептенофос хлоробицикло- /3,2,0/гепта-2,6-диен-6-тилдиметил-фос- фат;
PHOS фозалон S-6-хлор-2,3-дигидро-2-оксобензоксазол-3-ил-метил-0,0-ди- этил-фосфородитиоат;
SF синергистический фактор
PBO пиперонил-бутилат.
Изобретение основано на знании того, что путем использования определенных типов стереоизомеров или смесей циперметрина, являющегося активным ингредиентом, что направление взаимодействия и его степень в значительной мере определяются стерической структурой исследуемого циперметрина. Было установлено, что путем обеспечения неизменным соотношения между комбинациями те же самые могут характеризоваться всеми формами взаимодействия, такими как синергизм, аддитивность или антагонизм в зависимости от того, какой стереоизомер циперметрина был использован.
Авторами не известны какие-либо публикации, касающиеся смеси, состоящей из пиретроида и сложного фосфатного эфира, в которых было бы исследовано взаимодействие пиретроидной комбинации со всеми возможными изомерами. Наши эксперименты представлены в примерах 1-4.
В примере 1 демонстрируется взаимодействие трех изомеров циперметрина и хиналфоса на домашнюю муху в комбинационных соотношениях 1-5. В зависимости от используемого изомера антагонистическое, аддитивное и синергистическое взаимодействия могут наблюдаться.
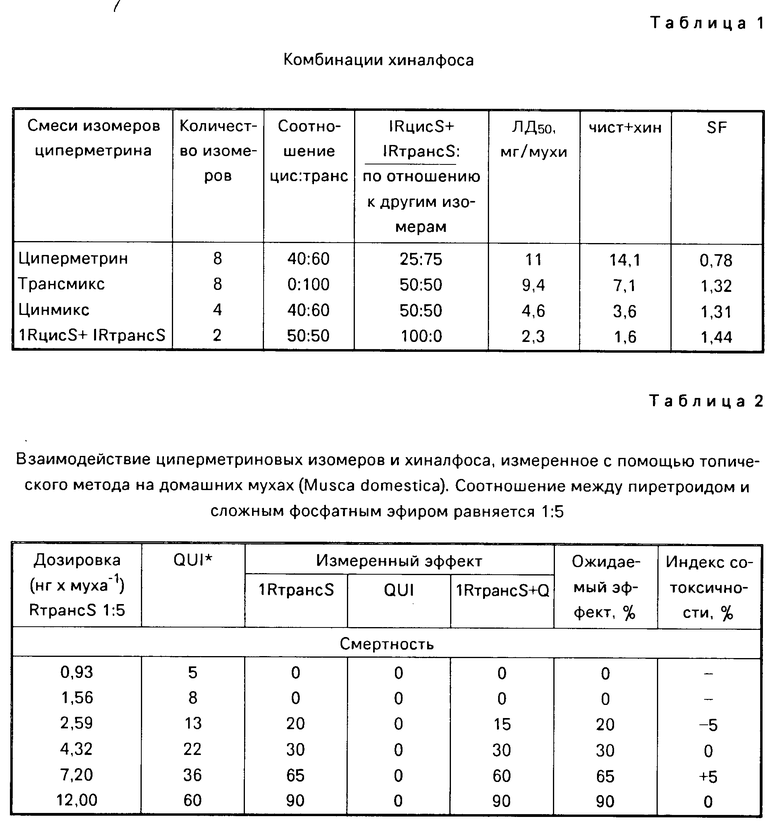
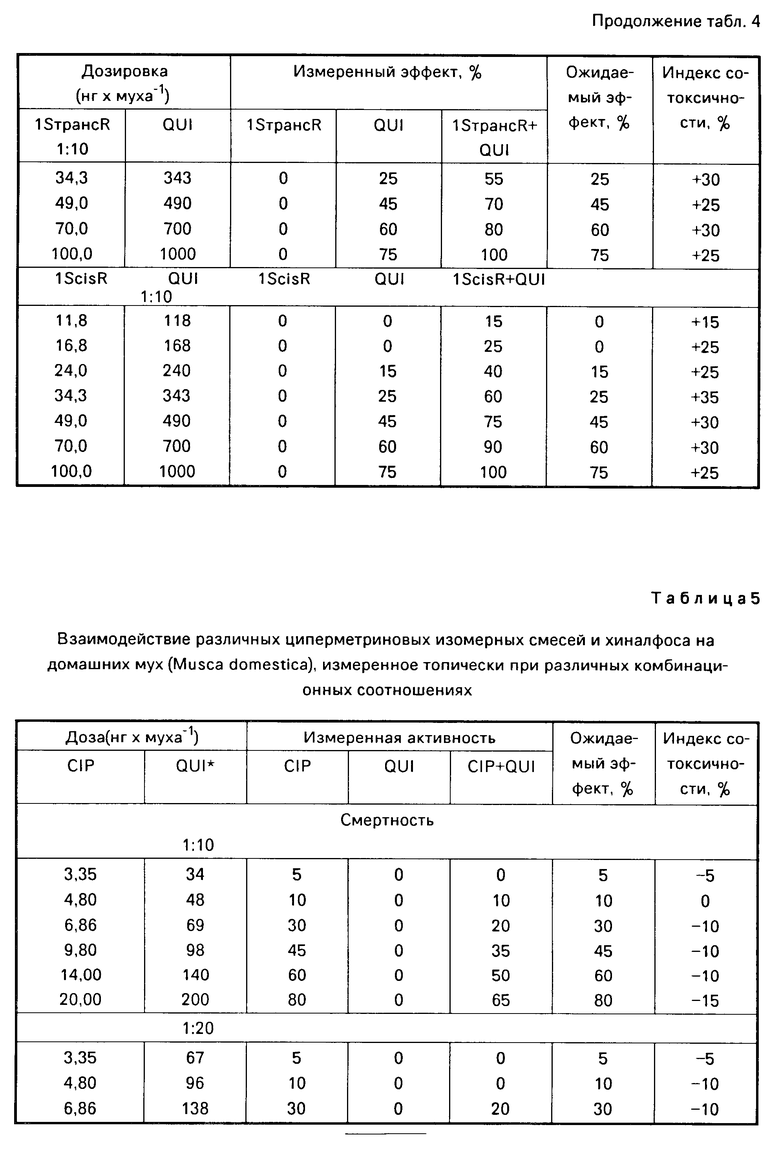
Путем изменения соотношения между изомером циперметрина и сложным фосфатным эфиром до 1:10 четыре изомера, подвергнутые раздельным испытаниям, действовали как синергистический агент по отношению к хиналфосу (см. табл. 4). Аналогичная тенденция может быть обнаружена в тех случаях, когда испытанию подвергаются цинмикс, содержащий 4 изомера, с хиналфосом: путем увеличения парциального отношения сложного фосфатного эфира антагонизм преобразуется в аддитивность и, начиная с парциального отношения, равного 1:10, превращается в синергизм. Циперметрин, содержащий 8 изомеров, ведет себя совершенно отличным образом, демонстрируя антагонистические действия при соотношениях 1:10 и 1:20 (пример 2). Некоторые смеси изомеров циперметрина, содержащие 8 изомеров, демонстрируют другие взаимодействия в тех случаях, когда они смешиваются с различными инсектицидами и акарицидами. При исследовании отдельных случаев авторами было показано, что в случае использования определенных изомеров циперметрина превосходные синергистические эффекты могут быть получены путем соответствующего выбора соотношений в комбинациях по сравнению с циперметрином, содержащим 8 изомеров. В соответствии с тестами, проведенными авторами изобретения, комбинациями, дающими особенно положительные результаты, являются те, в которых циперметриновый компонент состоит по меньшей мере из 40% 1RцисS и/или 1RтрансS изомеров. На основе данных, указанных в примере 2, была составлена табл. 1.
В соответствии с композициями, являющимися предметом изобретения, они содержат заданную смесь изомеров циперметрина и органический сложный фосфатный эфир в качестве инсектицида и при необходимости эти композиции содержат активатор, предназначенный для уничтожения артроподов, для ингибирования их развития и размножения, для нарушения их поведения и в конечном счете для предотвращения их отрицательной активности. Что касается пиретроида, то комбинация содержит циперметрин в количестве по меньшей мере равном 40% 1RцисS и 1RтрансS изомера и предпочтительно в соотношении между 1RцисS:1SцисR: 1RтрансS 1S трансR=20:20:30:30 40:40:10:10 и 1RтрансS:1SтрансR=40:60-100:0.
Комбинационное соотношение между изомером циперметрина и сложным фосфатным эфиром в композиции, являющейся предметом изобретения, может изменяться в диапазоне от 1:1 до 1:99, и предпочтительно в диапазоне от 1:10 до 1:99.
Композиция, являющаяся предметом изобретения, содержит в качестве фосфатного сложного эфира инсектициды и акарициды, предпочтительно фосфорные кислоты, тиофосфорные кислоты и дитиофосфорные кислоты. Некоторые примеры представлены далее в соответствии с классификацией имен Е-ISO, без их полных химических наименований.
Фосфорные кислоты: фосфамидон, гептенофос, тетрахлорвинфос, дихлорвос, трихлорфон, пропетамфос.
Тиофосфорные кислоты: паратион, метилпаратион, фенитротион, диазинон, триазофос, пиримифосэтил, пиримифосметил, деметон, мевинфос, хиналфос, фентион, бромофос, кумафос, этопроп, цианофос.
Дитиофосфаты: мелатион, мефосфолан, формотион, фентоат, фосмет, метидатион, фозалон, сульпрофос.
В особенности предпочтительными тиофосфорным кислотами являются соединения, выбранные из группы, включающей в себя хиналфос, диазинон, триазофос, и дитиофосфаты, из которых предпочтительными являются соединения, выбранные из группы, включающей в себя фозалон и метидатион, и предпочтительной фосфорной кислотой является гептенофос.
Преимуществом композиции, являющейся предметом изобретения, представляется то, что значительное синергистическое взаимодействие может быть достигнуто без изменения активности и уменьшение дозы может быть обеспечено по отношению к суммарно используемому количеству активного ингредиента. Тем самым проблемы, связанные с загрязнением окружающей среды, и затраты, связанные с защитой растений, могут быть уменьшены по сравнению с другими комбинациями сложных фосфатных эфиров, содержащих циперметрины, включающие в себя все изомеры.
Данный положительный эффект может быть объяснен за счет различного механизма активности компонентов, содержащихся в смеси. Характеризуемые высокой липидной растворимостью и быстрым активным контактом циперметриновые изомеры являются менее селективными и уничтожают всех артроподов, которые могут быть обнаружены на обрабатываемых площадях. В противоположность сложным фосфатным эфирам, которые в первую очередь уничтожают всех тех насекомых, которые используют сельскохозяйственные растения в качестве корма, их активность по отношению к полезным артроподам является более низкой.
Дозировка циперметрина может быть значительно уменьшена для композиции, являющейся предметом изобретения, благодаря синергистическому эффекту, хотя доза сложного фосфатного эфира является сама по себе сублетальной, нежелательные побочные воздействия пиретроидов на полезных паразитических насекомых являются сниженными. В целом сублетальные дозировки сложных фосфатных эфиров обнаруживают меньшее токсическое воздействие по отношению к полезным артроподам, поскольку они не подвергаются оральному отравлению или только косвенному воздействию.
В соответствии с изобретением такие комбинации являются предпочтительными для использования против сельскохозяйственных насекомых, которые содержат в качестве циперметринового активного ингредиента 1RцисS + 1SцисR: 1RтрансS + 1SтрансR зеркальные изомерные пары (антиподы) в соотношении 55: 45-25: 75. Также является предпочтительным, чтобы эта композиция содержала 5-50 мас. хиналфоса, диазинона и/или фозалона и 0-10 мас. пиперонилбутилата. В этих случаях предпочтительными являются эмульгируемые концентраты, содержащие в качестве одного носителя смесь ароматических растворителей, предпочтительно алкилбензолов, таких как, например, Solvesso 100, Solvesso 150.
Другой предпочтительной областью применения композиции, являющейся предметом настоящего изобретения, является использование ее для ветеринарии. Эти композиции предпочтительно должны содержать 1RтрансS и 1SтрансR зеркальные изомерные пары, от 5 до 50 мас. фозалона или от 5 до 50 мас. мелатиона, и от 0 до 10 мас. пиперонилбутилата. Композиции, предназначенные для ветеринарных целей, предпочтительно представляют собой эмульгируемые концентраты, содержащие в качестве наполнителя смесь ароматических растворителей, предпочтительно алкилбензолов, в соотношении 1:0,2 10 по отношению к общей массе активного ингредиента.
Композиции, являющиеся предметом изобретения, могут содержать: ионогенные поверхностно-активные вещества в качестве наполнителей, предпочтительно в количестве от 0,1 до 20 мас. кальциевой соли алкиларилсульфоната; неионогенные поверхностно-активные вещества предпочтительно в количестве 0,5-40 мас. алкилфенолполигликолевого простого эфира, содержащего 10 молей окиси этилена и/или от 0,5 до 40 мас. тристирилфенолэтоксилатов (EO=20), а также растворители, предпочтительно представляющие собой ксилол или смеси ароматических растворителей.
Эмульгируемые концентраты высокого качества могут быть получены в случае применения хиналфоса или, при необходимости, РВО комбинаций финалфоса в смесях ароматических растворителей. В некоторых случаях могут являться предпочтительными специальные смеси ароматических растворителей. В качестве поверхностно-активного вещества представляется предпочтительным использовать от 20 до 40 г/л кальциевой соли алкиларилсульфоната и также являются предпочтительными для использования в качестве неионогенного поверхностно-активного вещества от 50 до 100 г/л алкилфенолполигликолевые сложные эфиры, содержащие 10 молей окиси этилена и/или 10-100 г/л тристирилфенолэтоксилатов (ЕО= 20). Что касается композиций, содержащих фозалон, то ксилол может быть заменен смесью, состоящей из ароматических растворителей или специальными ароматическими растворителями, такими как Solvesso 100-150.
Прозрачные растворы могут быть получены в том случае, если активный ингредиент растворяется в ксилоле или в смеси, состоящей из ароматических растворителей, и в качестве сорастворителя может быть использован н-бутанол. Для получения прозрачного, растворимого в воде раствора композиции поверхностно-активных веществ, используемых для приготовления эмульгируемых концентратов, могут быть применены, но концентрация должна быть увеличена до 20-50 мас.
Что касается смесей ароматических растворителей, то предпочтительными являются такие смеси, которые приготовлены путем каталитической ароматизации бензола, в котором минимальная часть ароматических составляет до 75% и образуются практически чистые ароматические углеводородные фракции. Предпочтительным продуктом является такой, как, например, следующие:
Solvesso 100 (99% ароматических, 90% С9-алкилбензола)
Solvesso 150 (99% ароматических, 85% С10-алкилбензола)
Shellsol A, Aromasil H и Aromatol также являются предпочтительными.
П р и м е р 1. Эффективность инсектицидов и инсектицидных смесей была определена на самках домашних мух (Musca domestica) в возрасте 3-5 дней, выращенных в лабораторных условиях. Активные ингредиенты, использовавшиеся при проведении опытов, наносились, в виде капель, объемом 0,22 мл на спинную часть мух, которые находились под умеренным наркозом, выполненным с помощью СО2. В качестве растворителя были использованы норм. бутанол или 2-этоксиэтанол. Обработанные таким образом мухи помещались в плексиглазовые ящики и их кормление осуществлялось сахаром и водой.
Спустя 24 ч подсчитывалось количество погибших мух и это количество выражалось в процентах. Для каждой дозы испытаниям подвергалось 20 мух в 2-4 параллельных тестах. Эти тесты были повторены при 3-5 различных ситуациях.
Комбинированное взаимодействие приводится в соответствии к отношению ожидаемого эффекта, рассчитанного на основе активности компонентов, самих по себе, к измеренному эффекту. В том случае, если измеренный эффект превышает ожидавшийся эффект, то взаимодействие является синергистическим, если два эффекта являются одинаковыми, то взаимодействие является аддитивным, и если эффект взаимодействия является сниженным, то имеет место антагонистический эффект компонента. В этих примерах различия в ожидаемом и измеренном эффектах для каждой дозы, в процентах, характеризуются индексом сотоксичности. В соответствии с указанным выше положительная величина соответствует синергистической активности и отрицательная величина свидетельствует об антагонистической активности.
Данные, представленные в табл. 2, свидетельствуют о том, что определенные чистые изомеры циперметрина обладают различным взаимодействием с хиналфосом (при неизменном соотношении между ними, равным 1:5), зависящим от дозировки. Аддитивность (1RтрансS), антагонизм (1SтрансR) и синергизм (1RцисS) могут быть получены независимо от цис: транссоотношения или стерической структуры 1C- и альфа С-асимметричных атомов углерода.
В табл. 4 приведены данные, свидетельствующие о синергизме для комбинации различных циперметриновых изомеров с хиналфосом при соотношении 1:10, в то время как при соотношении 1:5 имеют место все формы взаимодействия (табл. 2,3).
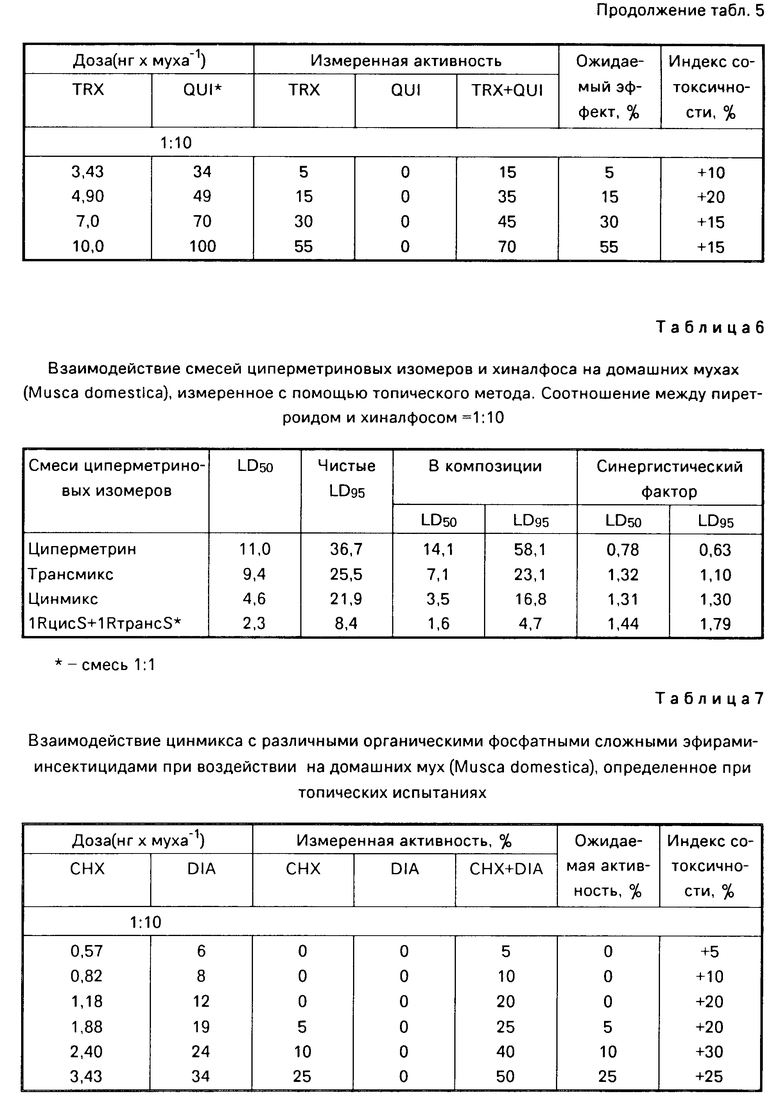
П р и м е р 2. Взаимодействие циперметрина, цинмикса, трансмикса и смеси циперметриновых изомеров 1RцисS + 1RтрансS в соотношении 1:1 с хиналфосом было исследовано с помощью методов, изложенных в примере 1. Полученные результаты суммированы в табл. 5 и эти результаты наглядно свидетельствуют о том, что в противоположность чистым циперметриновым изомерам цинмикс, трансмикс и смеси, состоящие из 1RцисS + 1RтрансS, в соотношении 1:1, обладают значительным синергистическим эффектом при соотношении 1:1 и выше между пиретроидом и сложным фосфатным эфиром. Смеси, состоящие из циперметрина, содержащего 8 изомеров, и хиналфоса, при соотношениях от 1:10 до 1:20, обладают антагонистическим эффектом.
Поскольку дозы хиналфоса в смесях вида 1:10 сами по себе представляются неэффективными, увеличение синергистического взаимодействия может быть осуществлено, если значения 50% летальных доз, измеренные только в смеси циперметриновых изомеров, будут разделены на значения 50% летальных доз, измеренных в композиции. В табл. 6 представлены данные, рассчитанные на основе данных, приведенных в табл. 4 с помощью вероятностного анализа (Финней, 1971).
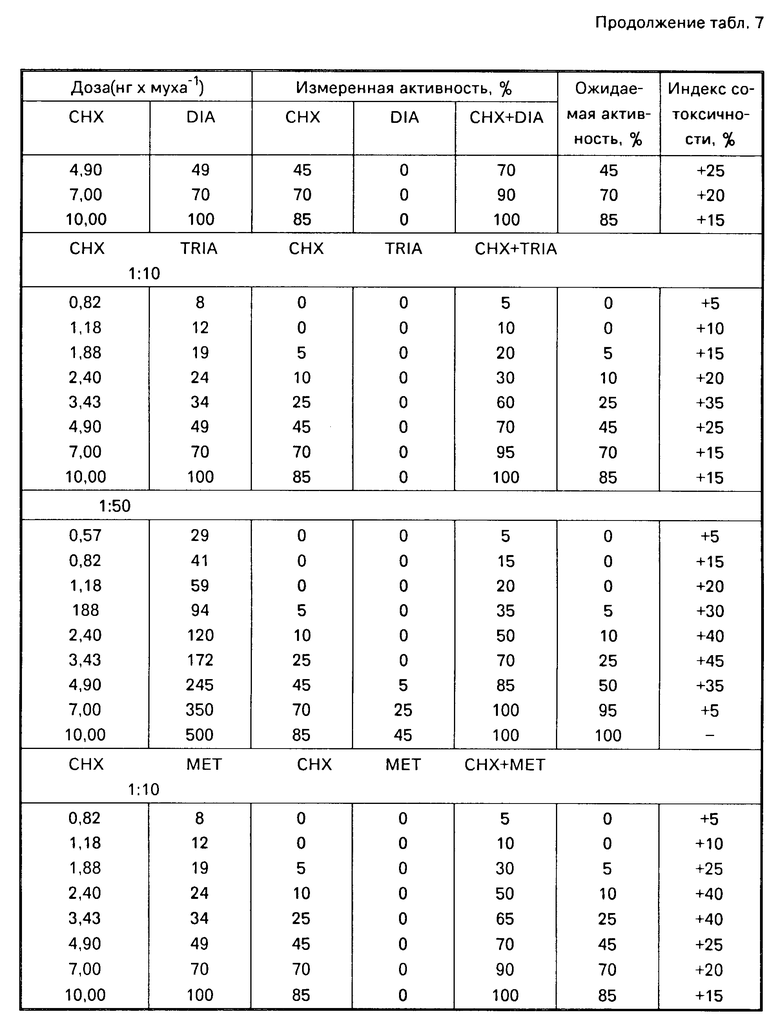
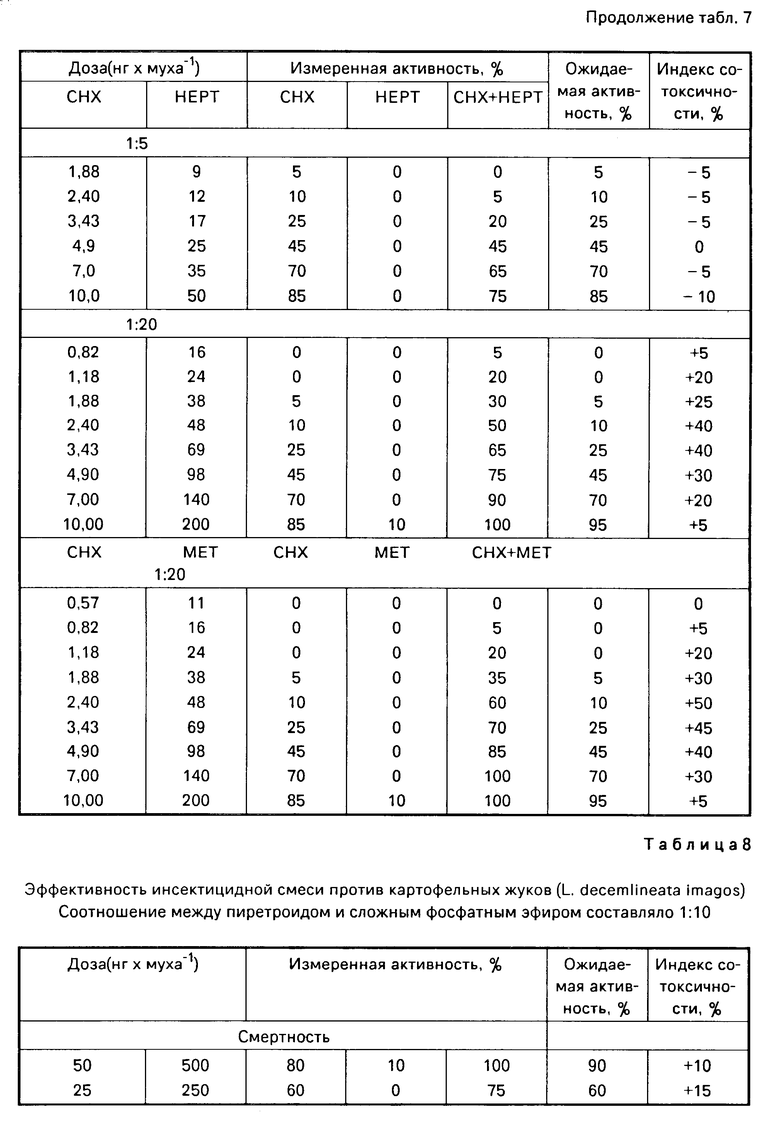
П р и м е р 3. Взаимодействие цинмикса и определенных типов сложных фосфатных эфиров было исследовано с помощью метода, использованного в примере 1, и полученные данные показывают, что синергистическая активность может иметь место при смешении цинмикса в соотношении 1:10 или при более высоком соотношении пиретроид сложный фосфатный эфир с диазиноном, триазофосом, метидатионом и гептенофосом.
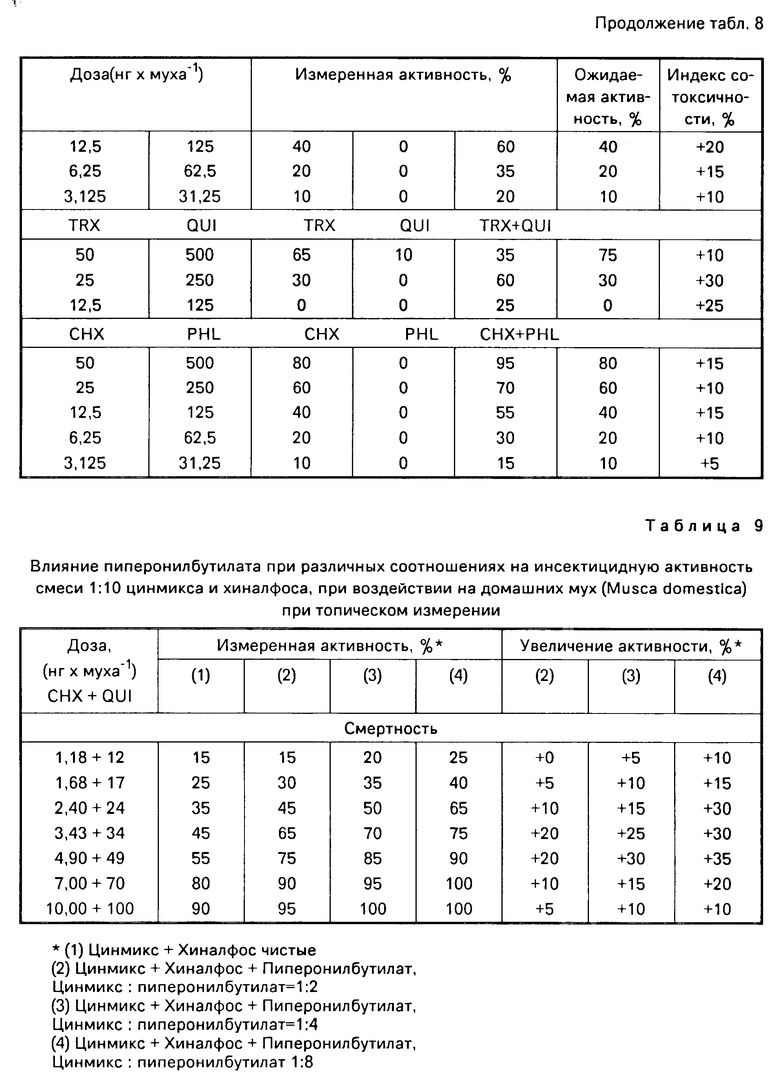
П р и м е р 4. Эффективность композиции, являющейся предметом настоящего изобретения, была определена применительно к картофельным жукам (L. decemlineata), собранным с участка свободной земли после выдерживания в условиях, аналогичных указанным в примере 1, и полученные результаты представлены далее в табл. 8.
П р и м е р 5. Активность пиперонилбутилата при различных дозах и цинмикса и хиналфоса при соотношении 1:10 была определена в соответствии с методикой, аналогичной указанной в примере 1 для инсектицидной активности. Полученные результаты показаны в приведенной далее табл. 9.
П р и м е р 6. 10 г цинмикса подвергались растворению в 475 г ксилола при 40оС при перемешивании. После дополнительного перемешивания производилось добавление к полученному ранее раствору кальциевой соли алкиларилсульфоната в количестве 35 г, а также смеси, состоящий из 80 г алкиларилфенолового полигликолевого простого эфира (10 ЕО). После полного растворения производили добавление 400 г хиналфоса в 50% ксилоле. Композиция, являющаяся предметом изобретения, давала стабильную эмульсию спустя 24 ч в воде Cipac D при концентрации 0,2 и 5 мас.
П р и м е р 7. К 80 г ксилола при 40оС производили добавление кальциевой соли алкиларилсульфоната в количестве 20 г и тристирилфенолэтоксилата (20ЕО) в количестве 90 г. Далее к полученному таким образом раствору добавляли 400 г пиперонилбутилата. В этой смеси далее медленно растворяли при перемешивании 10 г цинмикса. После полного растворения при перемешивании к полученному раствору производили добавление раствора, состоящего из 400 г хиналфоса в 50% ксилоле. Композиция, полученная в соответствии с настоящим примером, оставалась в форме стабильной эмульсии спустя два часа в воде Cipac D при концентрациях 0,2, 1, и 5 мас.
П р и м е р 8. К Solvesso 100, в количестве 725 г, производили добавление натриевой соли алкиларилсульфоната, в количестве 10 г и затем производили растворение добавленных 55 г алкилфенольного полигликолевого простого эфира (10ЕО). Далее к полученному таким образом раствору производили добавление, при 20оС, 200 г фозалона. Полученный таким образом раствор нагревался до 40оС и далее в нем растворялось 10 г цинмикса. В воде, имевшей жесткость 342 и 34,2 ппм при концентрациях 0,5 и 4 мас. устойчивость эмульсии была удовлетворительной при 20 и 30оС в течение 4 ч.
П р и м е р 9. В соответствии с этим примером 18 г кальциевой соли алкиларилсульфоната и 60 г алкилфенольного полигликолевого простого эфира (10 ЕО) подвергались растворению в 512 г Solvesso 150. Далее к полученному таким образом раствору при комнатной температуре производили добавление 400 г фозалона, а затем 10 г цинмикса растворяли при 40оС и добавляли к полученной смеси. Эта композиция позволила получить стабильную эмульсию при исследовании в течение двух часов в воде Cipac D при концентрации, равной 0,2%
П р и м е р 10. В соответствии с этим примером кальциевая соль алкиларилсульфоната в количестве 20 г, алкилфенольный полигликолиевый простой эфир (10 ЕО) в количестве 70 г и тристирилфенолэтоксилат (20 ЕО) в количестве 10 г подвергались растворению в 440 г Ароматола (Aromatol) смеси ароматических растворителей. Далее к полученному раствору при 20оС производили добавление 200 г фозалона. Далее к смеси при перемешивании производили добавление 250 г пиперонилбутилата. Затем при медленном перемешивании при 40оС производили добавление 10 г цинмикса. Стабильность эмульсии была определена с помощью метода Cipac, показавшего, что полученная эмульсия является устойчивой.
П р и м е р 11. В соответствии с этим примером кальциевая соль алкиларилсульфоната в количестве 15 г, алкилфенильный полигликолиевый простой эфир (15 ЕО) в количестве 20 г и тристирилфенолэтоксилат (20 ЕО) в количестве 70 г подвергались растворению в 85 г Ароматола (смеси органических растворителей). Далее к этому раствору производили добавление 400 г пиперонилбутилата, затем к полученной смеси при 40оС добавляли 400 г фозалона, а затем добавляли цинмикс в количестве 10 г. Стабильная эмульсия была получена в воде Cipac D при концентрациях 0,2, 1,0 и 5,0 спустя 30 мин и 20 ч.
П р и м е р 12. В соответствии с этим примером к хиналфосу в количестве 400 г, растворенному в 50% ксилоле, производили добавление кальциевой соли алкиларилсульфоната в количестве 10 г, алкилфенольного полигликолевого простого эфира (15 ЕО) в количестве 60 г, и тристирилфенолэтоксилата (20 ЕО) в количестве 20 г. При медленном перемешивании производилось растворение при 40оС цинмикса в количестве 10 г. После растворения производилось добавление пиперонилбутилата в количестве 400 г. При дополнительном перемешивании производилось добавление н-бутанола в количестве 20 и 80 г воды. Стабильность полученной эмульсии из прозрачного раствора, измеренная с помощью метода Cipac, была приемлемой.
П р и м е р 13. Пиперонилбутилат в количестве 200 г и Solvesso 100 в количестве 60 г подвергались перемешиванию. Далее к полученной таким образом смеси производилось добавление тристирилфенолэтоксилата (20 ЕО) в количестве 150 г, алкилфенольного полигликолиевого простого эфира (8 ЕО) в количестве 15 г и кальциевой соли алкиларилсульфоната в количестве 5 г. Далее производилось добавление при 20оС 200 г фозалона с последующим растворением в растворе при 40оС 10 г цинмикса. Полученный раствор охлаждался до 20оС и добавлялась смесь, состоящая из 50 г н-бутанола и 300 г воды. В результате была получена устойчивая эмульсия из прозрачного раствора в воде Cipac D в течение 14 ч при концентрациях 0,2, 1,0 мас.
П р и м е р 14. В соответствии с этим примером цинмикс в количестве 5 г подвергался растворению в 200 г хиналфоса в 50% ксилоле. В лабораторную сушилку с кипящим слоем загружалось 450 г Wessalon S (синтетическая кремневая кислота, имеющая большую удельную площадь поверхности). Двухслойный распылитель размещался в кипящем слое этой сушилки. При входной температуре 80оС на Weccalon S, находящемся в кипящем слое, производилось распыление раствора ксилола, содержащего хиналфос и цинмикс. Подача производилась со скоростью 300 мл/ч. После прекращения распыления ксилола он удалялся из Wessalon S потоком горячего воздуха.
После сушки смесь цинмикса и хиналфоса, нанесенная на носитель Wessalon S, выгружалась в лабораторный порошковый гомогенизатор, имеющий емкость 3 л. Далее производилось добавление в гомогенизатор 320 г нойбургского мела, 60 г дисперсогена А (Dispersogen A продукт конденсации нафталинсульфокислоты и формальдегида) и 20 г Netzer натриевой соли алитической сульфокислоты, и эти компоненты добавлялись в указанной последовательности. После того как добавление всех этих компонентов было завершено, процесс гомогенизации продолжался в течение 20 с. Полученная порошкообразная смесь была размельчена в воздушной мельнице с получением частиц размером 10 μм. Флотируемость по CIPAC: 86% время увлажнения 20 с.
П р и м е р 15. В соответствии с этим примером к раствору, содержащему 100 г хиналфоса в 50% ксилоле, производили добавление 5 г цинмикса. Этот ксилоловый раствор распылялся на 400 г носителя Wessalon S с использованием процесса в кипящем слое, описанного в примере 1. Сухая смесь выгружалась в лабораторный гомогенизатор, описанный в примере 1, в который затем вводились 465 г нейбургского мела, 60 г Дисперсогена А и 20 г Нетцера IS в указанной последовательности, и полученная смесь подвергалась гомогенизации. Полученная порошкообразная смесь затем размельчалась в воздушной мельнице до частиц размером менее 10 μм. Флотируемость по CIPAC: 82% время увлажнения 18 дней.
П р и м е р 16. В соответствии с этим примером в 100 г хиналфоса в 50% ксилоле производилось растворение 100 г пиперонилбутилата. Далее к полученному таким образом раствору производили добавление 5 г цинмикса и смесь подвергалась перемешиванию, полученный материал подвергался сушке. Полученный сухой премикс помещался в лабораторный гомогенизатор и при перемешивании производилось добавление 195 г нейбургского мела, 70 г Дисперсогена А и 30 г Нетцера IS. Полученный таким образом гомогенный продукт размельчался в воздушной мельнице. Флотируемость полученного продукта по CIPAC составила 85% время увлажнения 22 дня.
П р и м е р 17. В соответствии с этим примером 100 г раствора хиналфоса в 50% ксилоле растворялись с 50 г бутилата пиперонила. Далее при перемешивании производилось добавление 5 г цинмикса и процесс перемешивания продолжался до полного растворения. Полученный таким образом раствор ксилола наносился на 400 г носителя Wessalon S в сушилке с кипящим слоем, как было описано выше в примере 1, и сушился. Высушенная порошкообразная смесь смешивалась с нейбургским мелом в количестве 395 г, Дисперсогеном А в количестве 70 г и Нетцером IS в количестве 30 г в лабораторном гомогенизаторе. Полученный таким образом продукт подвергался размельчению. Флотируемость по CIPAC составила 83% время увлажнения 22 дня.
П р и м е р 18. В соответствии с этим примером цинмикс в количестве 5 г подвергался растворению в 150 мл смеси, состоящей из хлороформа и ксилола, в соотношении 1: 1. Далее производилось добавление фозалона. Полученный таким образом раствор разбрызгивался на 400 г носителя Wessalon S, с помощью процесса в кипящем слое, как было описано выше в примере 1, с последующим удалением ксилола и хлороформа путем сушки. Полученная сухая смесь подвергалась перемешиванию в лабораторном гомогенизаторе с нейбургским мелом в количестве 250 г, натрий лигнинсульфонатом в количестве 70 г и Atlox 4995, представляющим собой этоксилированный простой алкиловый эфир. Полученная таким образом гомогенная порошкообразная смесь подвергалась размельчению в воздушной мельнице с получением частиц размером менее 10 μм. Флотируемость полученного таким образом продукта в соответствии с CIPAC составила 95% время увлажнения 5 с.
П р и м е р 19. В соответствии с этим примером цинмикс в количестве 5 г и фозалон в количестве 50 г подвергались растворению в смеси, состоящей из ксилола и хлороформа, в количестве 75 мл, в соответствии с примером 5. После полного растворения полученный раствор наносился на носитель Wessalon S в количестве 400 г в установке с кипящим слоем и затем сушился. Полученная таким образом высушенная порошкообразная смесь загружалась в лабораторный гомогенизатор вместе с нейбургским мелом в количестве 390 г, натриевой солью лигнинсульфоната в количестве 60 г и Atlos 4995 в количестве 20 г. Порошкообразная смесь размельчалась после полной гомогенизации в воздушной мельнице. Флотируемость по CIPAC составила 95% время увлажнения 15 с.
П р и м е р 20. В соответствии с этим примером в смеси, состоящей из ксилола и хлороформа, в количестве 100 мл в соответствии с примером 5 производилось растворение цинмикса в количестве 5 г, пиперонилбутилата в количестве 100 г и фозалона в количестве 50 г. Полученный таким образом раствор наносился на носитель Wessalon S в количестве 450 г с помощью процесса в кипящем слое в соответствии с примером 1, и растворитель удалялся путем сушки. Полученная таким образом сухая смесь перемешивалась в лабораторном порошковом гомогенизаторе с нейбургским мелом в количестве 190 г, натриевой солью лигнинсульфоната в количестве 75 г и Atlox 4873 (этоксилированный простой алкильный эфир) в количестве 30 г. Полученная таким образом гомогенная порошкообразная смесь размельчалась в воздушной мельнице. Флотируемость полученного таким образом продукта в соответствии с CIPAC составила 86% время увлажнения 18 с.
П р и м е р 21. В смеси, состоящей из хлороформа и ксилола, в количестве 100 мл в соответствии с примером 5 производилось растворение цинминкса в количестве 5 г, пиперонилбутилата в количестве 50 г и фозалона в количестве 50 г. Полученный таким образом раствор наносился на носитель Wessalon S в количестве 400 г с помощью процесса в кипящем слое в соответствии с примером 1, растворитель удалялся путем сушки. Полученная таким образом безводная смесь смешивалась в порошковом лабораторном гомогенизаторе с нейбургским мелом в количестве 305 г, натриевой солью лигнинсульфоната в количестве 65 г и Atlox 4873 (этоксилированный алкильный простой эфир) в количестве 25 г. Полученная таким образом гомогенная порошкообразная смесь измельчалась в воздушной мельнице. Флотируемость полученного таким образом продукта в соответствии с CIPAC составила 89% время увлажнения равнялось 19 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ ДЛЯ ЗАЩИТЫ РАСТЕНИЙ ОТ ЧЛЕНИСТОНОГИХ ВРЕДИТЕЛЕЙ ДЛЯ УМО-ПРИМЕНЕНИЯ | 1989 |
|
RU2024225C1 |
| СИНЕРГЕТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВ ЧЛЕНИСТОНОГИХ | 1989 |
|
RU2069058C1 |
| МИКРОЭМУЛЬСИОННОЕ СРЕДСТВО ДЛЯ ЗАЩИТЫ РАСТЕНИЙ | 1989 |
|
RU2020819C1 |
| ЭМУЛЬГИРУЮЩИЙСЯ КОНЦЕНТРАТ ДЛЯ ЗАЩИТЫ РАСТЕНИЙ И ЭМУЛЬСИЯ ДЛЯ ОБРАБОТКИ РАСТЕНИЙ | 1989 |
|
RU2086125C1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСЕЙ ИЗОМЕРОВ ЦИПЕРМЕТРИНА | 1990 |
|
RU2045516C1 |
| ЛИОТРОПНАЯ ЖИДКОКРИСТАЛЛИЧЕСКАЯ КОМПОЗИЦИЯ | 1990 |
|
RU2045564C1 |
| ФУНГИЦИДНАЯ СИНЕРГИСТИЧЕСКАЯ КОМПОЗИЦИЯ | 1990 |
|
RU2012205C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОПАРГИЛАММОНИЙХЛОРИДА | 1994 |
|
RU2130450C1 |
| ФУНГИЦИДНАЯ СИНЕРГИТИЧЕСКАЯ КОМПОЗИЦИЯ | 1990 |
|
RU2091025C1 |
| ПРОИЗВОДНЫЕ 3,6-ДИЗАМЕЩЕННОГО 1,2,4,5-ТЕТРАЗИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ЛАРВИЦИДНО- И ОВИЦИДНО-АКТИВНАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ УМЕНЬШЕНИЯ КОЛИЧЕСТВА ЛИЧИНОК И ЯИЦ КЛЕЩЕЙ | 1994 |
|
RU2142949C1 |





Использование: в сельском хозяйстве, в частности в синеогических инсекцидных средствах защиты растений. Сущность изобретения: композиция содержит 5,5 31% активного начала, включающего а/ смесь изомеров циперметрина (IR цис S + IS цис R) (IR транс S + IS транс R) в соотношении 40 60 и б/ орозалон или хиналфос при массовом соотношении а б 1 (10 30), и остальное целевые добавки. 4 з. п. ф-лы, 10 табл.
Активный ингредиент 5,5 31,0
Целевые добавки Остальное
2. Композиция по п.1, отличающаяся тем, что она содержит 5 30 мас. хиналфоса, 0 40 мас. пиперонилбутоксида.
| СПОСОБ ПОЛУЧЕНИЯ БЕТУЛИНА | 1992 |
|
RU2074867C1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
Авторы
Даты
1995-10-10—Публикация
1988-11-17—Подача