Изобретение относится к биохимии и биотехнологии и может быть использовано для получения стабильных форм иммунобиологических препаратов.
Известен стабилизирующий состав, входящий в состав для иммуноферментного анализа (ИФА) [1] Состав реактива для ИФА включает конъюгат пероксидазы хрена, а стабилизатор содержит гентамицин, амикацин и тобрамицин.
Данный стабилизирующий состав оказывает лишь антибиотическое (противомикробное) действие и не влияет на термостабильность препарата в процессе его сушки и хранения.
Известно использование сахарозы, глюкозы и лактозы в качестве стабилизаторов при лиофилизации каталазы [2] где наблюдается 95%-ное сохранение активности.
Однако при использовании глюкозы и лактозы в качестве стабилизатора для получения конъюгата (КГ) БА:ПХ его активность снижается как при добавлении в раствор, так и после замораживания-оттаивания. При использовании в качестве стабилизатора сахарозы активность КГ БА:ПХ в ИФА сохраняется. После замораживания-оттаивания данного препарата в присутствии сахарозы сохраняется 50% его исходной активности.
Наиболее близким к изобретению техническим решением (прототипом) является стабилизирующий состав для получения лиофилизированных препаратов на основе КГ белка А и пероксидазы хрена [3] включающий сахарозу 5% бычий сывороточный альбумин (БСА) 0,6% и фосфатно-солевой буфер (ФСБ) остальное.
Этот стабилизатор снижает биологическую активность КГ в ИФА как при добавлении в раствор, так и на стадии лиофилизации, а также не обеспечивает сохранение биохимических свойств КГ в процессе длительного его хранения при положительных температурах.
Целью изобретения является снижение потерь биохимических свойств препарата в процессе лиофильного высушивания и последующего хранения при положительных температурах.
Цель достигается тем, что в качестве стабилизатора используется состав, состоящий из пептона, сахарозы и фосфатно-солевого буфера при следующем соотношении компонентов, мас. Пептон 4,0-12,0 Сахароза 1,3-6,0 Фосфатно-солевой буфер Остальное
Причем пептон и сахарозу вводят в состав в соотношении 2:1-4:1.
Новыми, отличительными от прототипа являются следующие существенные признаки предлагаемого состава. Состав дополнительно содержит пептон при следующих содержаниях компонентов, мас. Пептон 4,0-12,0 Сахароза 1,3-6,0 Фосфатно-солевой буфер Остальное
Причем пептон и сахарозу вводят в состав в соотношении 2:1-4:1.
Cравнение заявляемого способа с известными показывает, что отличительные от прототипа признаки проявляют новое, неизвестное ранее свойство, а именно полное сохранение активности КГ на стадии лиофилизации и увеличение срока его хранения при положительных температурах, что свидетельствует о соответствии предлагаемого технического решения критерию "существенные отличия" ("изобретательский уровень").
Такое сохранение активности КГ, возможно, обусловлено тем, что аминокислоты и короткие пептиды, находящиеся в свободном виде в составе пептона, имеют как гидрофильные, так и гидрофобные участки (эпитаксиальные поверхности белка А и пероксидазы хрена). Углеводы замещают молекулы воды у поверхности белков, сохраняя тем самым их конформацию в процессе удаления воды.
Стабилизирующий состав для получения лиофилизированных препаратов на основе КГ белка А и пероксидазы хрена (КГ БА:ПХ) готовится и используется следующим образом.
Компоненты стабилизатора (пептон, сахароза) растворяют в фосфатно-солевом буфере при комнатной температуре при перемешивании. Состав фильтруют через стеклянный фильтр, а затем через фильтр Millipor с размерами пор 0,45 мкм. Полученный раствор охлаждают во льду с последующим добавлением в него раствора КГ, достигая разбавления в 300-3000 раз в зависимости от титра КГ. Препарат разливают по 0,2 мл во флаконы объемом 5 мл. Замораживание препарата во флаконах производят при -60оС в течение 10 ч. Температура материала на стадии сублимации составляет (-30) (-35)оС, давление 3-5 Па, а досушивание осуществляют при конечной температуре 22оС в течение 3 ч. Общая продолжительность сушки КГ БА:ПХ со стабилизатором составляет 20 ч. По окончании лиофилизации флаконы укупоривают под вакуумом. Остаточную влажность препарата определяют по стандартной методике, которая составляет для всех экспериментальных образцов не более 3% Активность КГ БА:ПХ определяют до и после лиофилизации и в ходе хранения при температуре 4 и 37оС. В экспериментах использовали заявляемый стабилизирующий состав с разным процентным содержанием пептона и сахарозы и их соотношением в препарате. Активность КГ в ИФА определяют на тест-системе "Рекомбинант ВИЧ". ИФА проводят в соответствии с инструкцией на данную систему. На планшеты с иммобилизованным рекомбинантным антигеном сорбируют положительную и отрицательную сыворотки. После инкубации планшет промывают 5 раз, затем наносят КГ в растворе концентрата блокирующего раствора. После инкубации и промывки планшета в лунки вносили ортофенилендиамин и Н2О2. Реакцию останавливают 0,9 М серной кислоты, результаты регистрируют на 492 нм прибором Multiscan.
Примеры стабилизирующих составов приведены в табл.1.
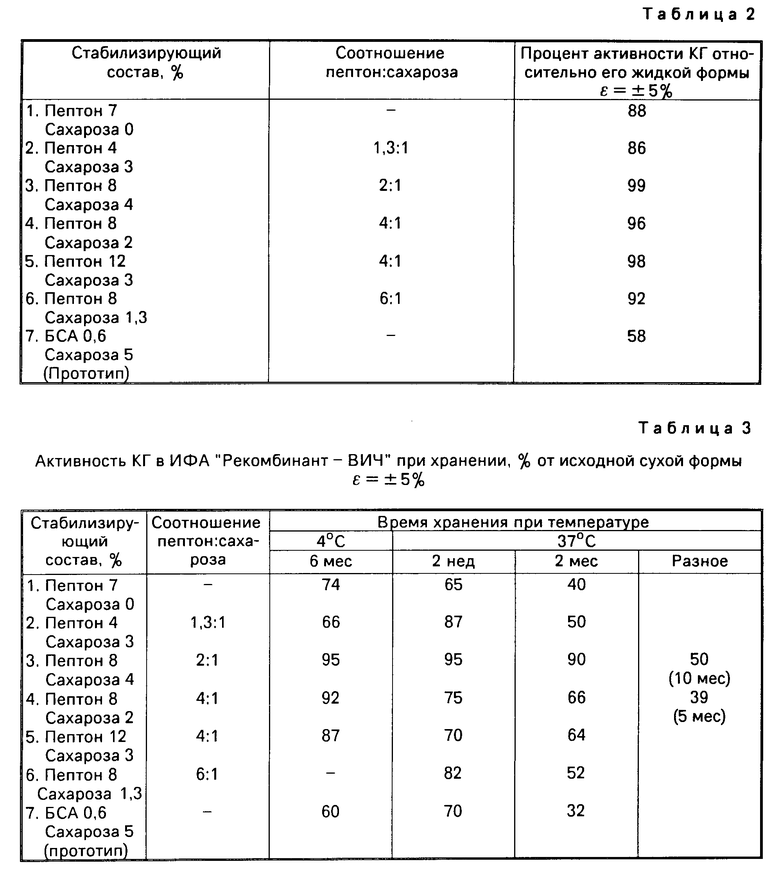
Сохранение активности КГ в ИФА "Рекомбинант ВИЧ" на стадии лиофилизации приведено в табл.2. Результаты показывают, что наиболее оптимальным является соотношение пептона и сахарозы 2:1-4:1, при которых потеря активности КГ составляет от 1 до 4% Результаты хранения КГ БА и ПХ с предлагаемым стабилизирующим составом приведены в табл.3. Эксперименты показывают, что при хранении КГ при температурах 4 и 37оС наиболее оптимальным также является соотношение пептона и сахарозы 2:1-4:1.
Следует отметить, что нижние границы концентраций пептона и сахарозы (соответственно 4 и 1,3) определяются минимальной концентрацией сухого остатка этих веществ, при которой препарат сохраняет после высушивания форму в виде таблетки. При этом суммарная концентрация этих веществ в исходном растворе не должна быть менее 5% Верхний предел концентрации пептона 12% ограничивается пределом его растворимости. Верхний предел концентрации сахарозы 6% определяется минимальным оптимальным соотношением пептон:сахароза 2:1 при максимальной концентрации пептона 12% Эксперименты показывают, что стабилизирующий эффект предлагаемого состава определяется в основном соотношением компонентов пептон:сахароза в пределах, указанных в заявке концентраций этих веществ.
Технико-экономическая эффективность предлагаемого технического решения состоит в следующем. Стабилизирующий состав на основе пептона и сахарозы (табл.2) позволяет лиофильно высушивать КГ БА и ПХ с потерей исходной активности на 1-4% при соотношении пептон: сахароза 2:1-4:1. Стабилизирующий состав по прототипу позволяет высушивать КГ Ба и ПХ с потерей исходной активности на 42% При хранении КГ БА и ПХ при 37оС в течение 2 мес (табл.3) предложенный стабилизирующий состав обеспечивает его активность на уровне 66-90% от исходной, а прототип на уровне 32% от исходной активности. Таким образом, по сравнению с прототипом предложенный стабилизирующий состав снижает потери биохимических свойств КГ БА и ПХ на порядок, а при последующем его хранении при положительных температурах потери биохимических свойств снижаются в 2-3 раза.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТАБИЛИЗИРУЮЩИЙ СОСТАВ ДЛЯ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННЫХ ПРЕПАРАТОВ НА ОСНОВЕ КОНЪЮГАТА АНТИИММУНОГЛОБУЛИНА G И ПЕРОКСИДАЗЫ ХРЕНА | 1996 |
|
RU2109290C1 |
| СТАБИЛИЗИРУЮЩИЙ СОСТАВ ДЛЯ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННЫХ ПОЛОЖИТЕЛЬНЫХ КОНТРОЛЬНЫХ СЫВОРОТОК, ИСПОЛЬЗУЕМЫХ В ТЕСТ-СИСТЕМАХ ДЛЯ ОПРЕДЕЛЕНИЯ СПЕЦИАЛЬНЫХ АНТИТЕЛ К ВИРУСАМ И МИКРООРГАНИЗМАМ | 1992 |
|
RU2011202C1 |
| СПОСОБ КОНСЕРВАЦИИ ИММУНОПЕРОКСИДАЗНОГО КОНЪЮГАТА | 2014 |
|
RU2549971C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ СТОЛБНЯЧНОГО АНТИТОКСИНА В ТВЕРДОФАЗНОМ ИММУНОФЕРМЕНТНОМ АНАЛИЗЕ | 1992 |
|
RU2113713C1 |
| Способ получения препарата вируса Марбург | 1991 |
|
SU1808012A3 |
| КОНЬЮГАТ ДЛЯ ИММУНОФЕРМЕНТНОГО АНАЛИЗА И СПОСОБ ИММУНОФЕРМЕНТНОГО АНАЛИЗА | 1992 |
|
RU2014610C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРЕПАРАТА КРОВЬ ГЕМОЛИЗИРОВАННАЯ | 2011 |
|
RU2455014C1 |
| ТЕСТ-СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К HBs-АНТИГЕНУ И БЛОКАТОР В ТЕСТ-СИСТЕМЕ | 2001 |
|
RU2206095C1 |
| ТЕСТ-СИСТЕМА ДЛЯ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНТИ-HBS В БИОЛОГИЧЕСКОМ ОБРАЗЦЕ | 2005 |
|
RU2290642C2 |
| СПОСОБ ЛИОФИЛЬНОЙ СУШКИ БИОПРЕПАРАТА | 1995 |
|
RU2111426C1 |
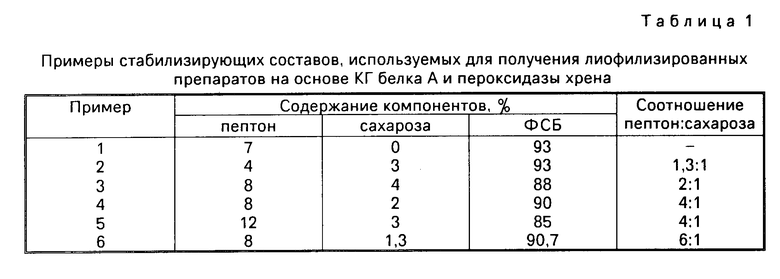
Использование: в стабилизирующем составе для получения лиофизилированных препаратов на основе конъюгата белка А и пероксидазы хрена. Сущность изобретения: состав пептон, сахарозу и фосфатно-солевой буфер при следующем соотношении компонентов, мас. пептон 4 12, сахароза 1,3 6, фосфатно-солевой буфер остальное, причем пептон и сахарозу вводят в состав в соотношении 21 41. Состав снижает потери биохимических свойств препарата в процессе лиофильного высушивания и последующего хранения при положительных температурах. 3 табл.
Пептон 4 12
Сахароза 1,3 6,0
Фосфатно-солевой буфер Остальное
2. Состав по п. 1, отличающийся тем, что содержит пептон и сахарозу в соотношении (2 1) (4 1).
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| Получение белка А, меченого пероксидазой хрена | |||
| - Фармакопейный комитет, 1988, с | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1995-10-20—Публикация
1991-09-12—Подача