Изобретение относится к вирусологической диагностике.
СПИД (синдром приобретенного иммунодефицита) представляет собой одну из основных угроз двадцатого столетия для здоровья людей. Вследствие его меняющейся биологической природы, способах распространения от индивидума к индивидуму, "скрытого" периода развития болезни, что делает затруднительным само его обнаружение, СПИД несомненно стоит в ряду эпидемиологических проблем, требующих беспрецедентных усилий. Несмотря на значительные затраты на повышение надежности диагностики СПИДа созданные к настоящему времени методики все еще недостаточно отвечают необходимым требованиям четкого контроля этой проблемы для любой группы населения (см. материалы рабочей группы, озаглавленные "Опыты испытания антител к НТLV-III, современные данные по отбору, лабораторному и эпидемиологическому коррелированию", под эгидой Центра лекарств и биологических средств FDA, Национальные институты здоровья и Центры контроля заболеваний, 31 июля 1985, Национальные Институты здоровья и Центры контроля заболеваний, 31 июля 1985, Национальный Институт здоровья, Бефезда, шт, Мэриланд; Budiansky S. Nature, 1985, 316, с. 96).
Существует несколько названий вируса иммунодефицита человека (НIV): для вируса HIV, выделенного в Пастеровском Институте (Париж, Франция), обозначением служит LAV, а для вируса HIV, выделенного в Национальном Институте здоровья, Бефезда, шт. Мэриланд, США, обозначением служит НTLV-III (лимфотропный вирус Т-клеток человека). В настоящем тексте вирус HIV часто будет называться в его общем смысле или же будет обозначаться как HTLV-III или LAV, или HIV. Термин HIV в настоящем описании включает другие вирусы, связанные с заражением СПИДом, независимо, выделены ли они или нет. Имеется в виду, что вирус НIV в единственном числе включает любой тип HIV независимо от его геномного содержания. Аналогично симптомы СПИД в общем виде будут называться, как включающие симптомы, вызываемые HIV (согласно вышеприведенному определению) РСК (родственный СПИДу комплекс), синдрома заболевания лимфатических узлов (СЗЛ) и другими вирусами, вызывающими по существу аналогичные клинические симптомы.
В настоящее время в лечебной практике наметились два подхода: иммунологический (создание вакцины) и непосредственная атака на сам вирус (противовирусная терапия). Поначалу создание вакцины казалось многообещающим, по крайней мере, теоретически, однако новые сведения о природе вируса в значительной степени ликвидировали эти ожидания. Дело в том что вирус легко подвергается мутации или изменению своей основной биохимической структуры, в результате чего определяющие вирусные антигенные "детерминанты", необходимые для эффективности вакцины, легко подвергаются мутации или изменению. Например, НТLV-III, выделенные в Калифорнии, Мэриланде и Англии, значительно отличаются друг от друга при тщательном анализе их геномного содержания. В результате проведенных исследований сделан вывод о том, что вакцинация против НIV не даст устойчивых длительных результатов в отличие от действительно положительных длительных результатов, достигаемых в случае большинства других вакцин, например, направленных против вируса полиомиелита, вируса кори и т. д.
При другом подходе к проблеме (непосредственная атака на вирус) учеными испытан ряд соединений, в том числе AZT, НРА-23, сурамин, рибавирин, интерферон, фаскарнет и т.д. Эти соединения включались в лабораторные или клинические исследования при ограниченных или неквалифицированных данных об их терапевтическом действии. Почти в каждом случае имеются свидетельства о высокой токсичности и/или неблагоприятных побочных эффектах (см. обзор, подготовленный Clark M. Newsweek, 5 августа 1985, с.71, а также Wallis G. Time, 12 августа 1985, с. 40-47. Ни одно из таких лекарств не является по существу новым и не способно быть селективно направлено против первопричины нарушений, а именно против мультипликации HIV в определенных клетках. К примеру, НРА-23 представляет собой комбинацию тяжелых металлов (отголосок применения в двадцатых годах в эпоху, предшествующую открытию пенициллина, мышьяка для лечения венерических заболеваний), сурамин по существу является противопаразитным средством (сонная болезнь) и фаскарнет является средством против вируса лишая. Последние два соединения могут ингибировать родственный НIV фермент, названный "обратимой транскриптазой", однако имеется недостаточно сведений, что такое ферментативное ингибирование приводит к значительному терапевтическому действию, или профилактике заболевания, или его облегчению. Применение АZT может быть связано с небольшим увеличением срока жизни жертв СПИДа, но сам по себе он в высшей степени токсичен и не уничтожает HIV (Yarchoan R. и др. Lancet, 15 марта 1986, с. 575, Chaisson R.E. и др. New England Journal of Medicine, 1986, т.315, с. 1611).
СПИД вызывает прогрессирующие нарушения в иммунной системе в результате заражения вирусом иммунодефицита человека (HIV). На ранних стадиях болезни ответственные за иммунитет клетки теряют свои свойства в результате потери Т-клеток (продуцируется тимусом), экспрессирующих так называемый Т4 антиген, т. е. ту часть Т-клеток, которая состоит в основном из фага-помощника и индуктора Т-клеток. Дефицит Т4 в клетках может привести к определенным видам дефицита в передающейся клетками иммуности, в том числе дефицита ЕУ (естественных клеток-убийц), АЛУ (активированных лимфокином клеток-убийц) и цитолитичных Т-клеток. При СПИДе отмечен также дефект лимфоцитов, происходящих из костного мозга.
СПИД является прогрессирующей болезнью, хотя время перехода от одной фазы к другой может меняться. Для фаз развития СПИДа существует классификация. Асимптоматические индивидуумы, зараженные НIV, иногда называются сероположительными ввиду присутствия в их крови антител к вирусу (Sarngadharan M. G. и др. Science, 1984, т. 224, с.506). Если у них не имеется других маркеров, их относят к пациентам ВР1-стадии согласно классификации Вальтера Рида (Redfild R.R. и др. New Ergland Journal of Medicine, 1986, т. 314, с. 131). Эту стадию также называют предРСК (РСК родственный спиду комплекс), хотя некоторые индивидуумы на этой стадии могут так и не показать характерного для РСК симптомологии. Некоторые из таких пациентов могут иметь симптомы заболевания лимфатических узлов (ВР2) и иметь дефицит Т-клеток (ВРЗ). После этого происходит уменьшение способности лимфоцитов претерпевать стимулируемую антигеном пролиферацию и стимулируемое антигеном образование гамма-интерферона и пациенты на такой ВР4-стадии начинают терять замедленную кожную гиперчувствительность. Пациенты на ВР5-стадии становятся обычно вялыми. Они подвержены заражению опоясывающим лишаем, афтозному стоматиту (молочнице) или проявляют симптомы РСК, которые включают продолжительные ознобы, потение по ночам, слабость, понос и/или потерю веса. Этот период РСК также характеризуется прогрессирующим падением иммунитета. Наконец, пациенты на ВР6-стадии подвержены любым инфекциям, т.е. речь идет об откровенном СПИДе или СПИДе в "полном расцвете", когда 50% пациентов умирает в течение 12 мес. (Murray H. W. и др. New England Journal of Medicine, 1984, т.310, с. 883).
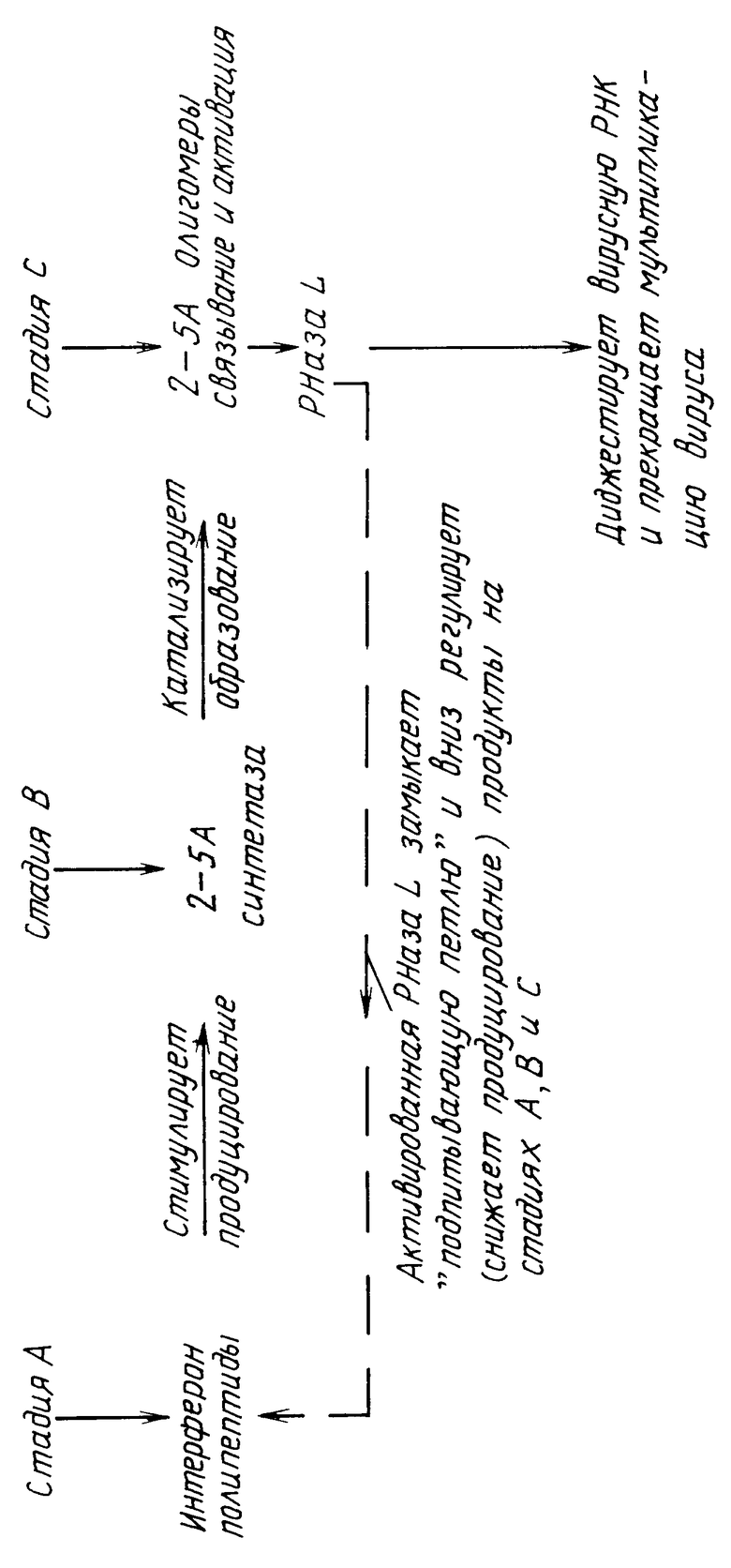
На чертеже показана схема образования 2'-5' олигаденилят-РНаза L.
Открыто вещество-ингибитор, выделяющееся или понуждаемое к выделению клетками, зараженными вирусами иммунодефицита человека. Этот ингибитор физически связан с ферментом РНазой L концевым продуктом на пути образования 2'-5'-олигаденилят-РНаза L, приводит к выходу из строя всей иммунной системы, что позволяет вирусам бесконтрольно размножаться. Описана техника идентификации таких ингибиторов либо непосредственно, либо косвенно по отсутствию РНазы L или неактивности РНазы L или присутствию ингибиторов промежуточных соединений на пути образования 2'-5' А-РНаза L, при этом ингибитор (ы) служит маркером для обнаружения присутствия HIV или родственных вирусов, дающих по существу такие же клинические симптомы. Также обсуждается прогнозирующее значение такого маркера с точки зрения развития в полном расцвете СПИДа у пациентов, в частности у пациентов, имеющих антитела к НIV в периферийной крови и тканях, включая кровь, фракции крови, клетки трансплантированных органов и клеточных экстрактах. Описаны методики активирования РНазы L и/или удаления, или дезактивации ингибирующего РНазу L вещества. Частью изобретения являются лечебные методы дезактивации ингибирующих PHазу L веществ (а) или вируса, направленного на такие ингибиторы. В изобретение включены способы получения антител к таким вирусам как in vivo, так и in vitro использованием в качестве антигена специфичного ингибитора PHазы L или вируса, направленного на ингибирование биохимических промежуточных соединений на пути образования 2'-5' А-РHаза L.
Изобретение включает использование дзРНК в фармацевтической композиции и способ активации PHазы L, удаления или дезактивации специфичного ингибитора РНазы L или вируса, направленного на ингибирование биохимических промежуточных веществ на пути образования 2'-5' А-РНаза L как у животных, так и человека. Композиция представляет собой сочетание дзРНК, предпочтительно неспаренной дзРНК, и лимфокина, такого как интерферон, или другого специфичного противовирусного средства, чье действие усиливается за счет выделения и сохранения зависящего от дзРНК пути образования 2'-5'А.
Рекомендуют, чтобы композиция содержала дзРНК и интерферон в отношении 0,01-1000 мк дзРНК на 0,1-100000 1RU интерферона.
Кроме того, изобретение включает способ придания устойчивости биологическим жидкостям или клеткам (предпочтительно жидкостям или клеткам человека) по отношению к вирусным инфекциям путем увеличения их сопротивляемости или путем смягчения действия инфекции НIV. Способ заключается в смешивании или контактировании указанных биологических жидкостей или клеток с эффективным количеством дзРНК, т.е. количеством дзРНК, ингибирующим НIV или активирующим РНазу L. Биологическая жидкость может представлять собой кровь человека или фракцию крови, например, предназначенную для переливания или диализа. Клетки могут происходить из намечаемой к пересадке кожи или трансплантируемого органа.
Кроме того, изобретение включает способ удаления или дезактивации веществ, ингибирующих образование РНазы L, из устройства для обработки парентеральных жидкостей или смягчения действия инфекции HIV из такого устройства. Способ заключается в контактировании указанного устройства с композицией, содержащей эффективное, ингибирующее НIV, активирующее РНазу L количество дзРНК.
Изобретение также включает лечебные методы и композиции, предназначенные для лечения пациентов, пораженных НIV, в том числе и пациентов с симптомами СПИДа, путем подавления или исключения специфичного к НIV ингибитора или вирус-направляемых ингибиторов промежуточных соединений на пути превращения 2'-5' А-РНаза L и/или активирования РНазы L. Композиция включает дзРНК и фармацев- тически приемлемый носитель или разбавитель. Изобретение включает также инструкции по использованию при лечении вызываемых ретровирусами или лимфотропным вирусом Т-клеток заболеваний, например СПИД, других вирусов человека, на чью мультипликацию будет действовать активация бездействующей РНазы L.
Ниже в виде примеров описаны лечебные способы селективного ингибирования вирусов человека, особенно НIV, без заметной токсичности к обычным клеткам: способы ингибирования, замедления или профилактики индивидуума от заражения НIV; способы профилактики или лечения родственного СПИДу комплекса и родственных СПИДу нарушений у человека; способы обработки биологических жидкостей, клеток и тканевых продуктов человека с целью предотвращения или фиксации инфекции или загрязнения НIV; а также способы коррекции определенных нарушений, связанных с НIV, в том числе потерю рецепторов интерферона на клетках в пределах иммунной системы, во всех случаях, основанных на сокращении или снижении уровня внутриклеточной 2'-5' А-синтетазы и дезактивации РНазы L и снижении или утрате внутриклеточных дзРНК в избранных клетках иммунной системы. Также описаны фармацевтические композиции, предназначенные для использования в перечисленных способах. В объем изобретения помимо лечения человека включено также и лечение животных.
Применение дзРНК приспособлено для коррекции специфичных нарушений, связанных с инфекцией НIV, в том числе утрата РНазы L и зависимых от дзРНК ферментов (например, протеинкиназы) на различных определяющих клетках в пределах иммунной системы, сокращение уменьшение внутриклеточной 2'-5' А-синтетазы в различных определяющих клетках в пределах иммунной, защищающей организм, системы и снижение или утрата внутриклеточной дзРНК и уменьшение или утрата биоактивных 2'-'5' А-олигомеров в различных решающих клетках в пределах иммунной, защищающей организм, системы.
Нарушения в клеточной "первой линии обороны" (пути образования 2'-5'-олигоаденилята) при СПИДе.
Различные исследования указывают на то, что путь образования 2'-5'-олигоаденилята (в медицинской литературе также называемый 2'-5' путем образования интерферона) при СПИДе нарушается. Такой путь образования является составной частью защитной системы организма от инфекций. При СПИДе и различных предшествующих ему состояниях, например РСК или СЗЛ (синдром заболевания лимфатических узлов), непосредственно участвующие на этом пути образования ферменты-факторы "включены" или активированы, и все же вирус СПИДа мультиплицируется. Например, уровень интерферона, как правило, повышен, также как повышен и уровень фермента 2'-5'-синтетазы. Однако механизм такого повышения, в частности неспособность системы, включенной, по меньшей мере, частично, ингибировать HIV, хоть до какой-то степени, оставался неизвестным до исследований, описанных ниже. В результате исследований идентифицирован ингибитор, который вторичен по отношению к инфекции НIV, и установлено, что этот ингибитор парализует противовирусный защитный механизм, противостоящий СПИДу в его полном развитии.
Об отсутствии или присутствии активированной РНазы L в цитоплазмических экстрактах моноядерных клеток периферийной крови (МКПК) пациентов делают вывод по способности образовывать специфичные продукты расщепления (СПР) из 28S и 18S рРНК согласно методикам Каriko K. и Ludwig J. Biochem Bilphys. Research Сommunica-tion, 1985, т. 128, с. 695, Wrescher D.H. и др. Nucleic Асid Research, 1981, т. 9, с. 1571. Рибосомная РНК (содержащая две молекулярные разновидности, обозначаемые как 28S и 18S) ведет себя аналогично вирусной РНК (например, НIV) по способности расщепляться под действием активированной рНазы, но только не дезактивированной РНазы. Активированная РНаза характеризуется тем, что в своей молекулярной структуре связана преимущественно с 2'-5'А-олигомерами и очень мало связана, если вообще связана, с ингибитором.
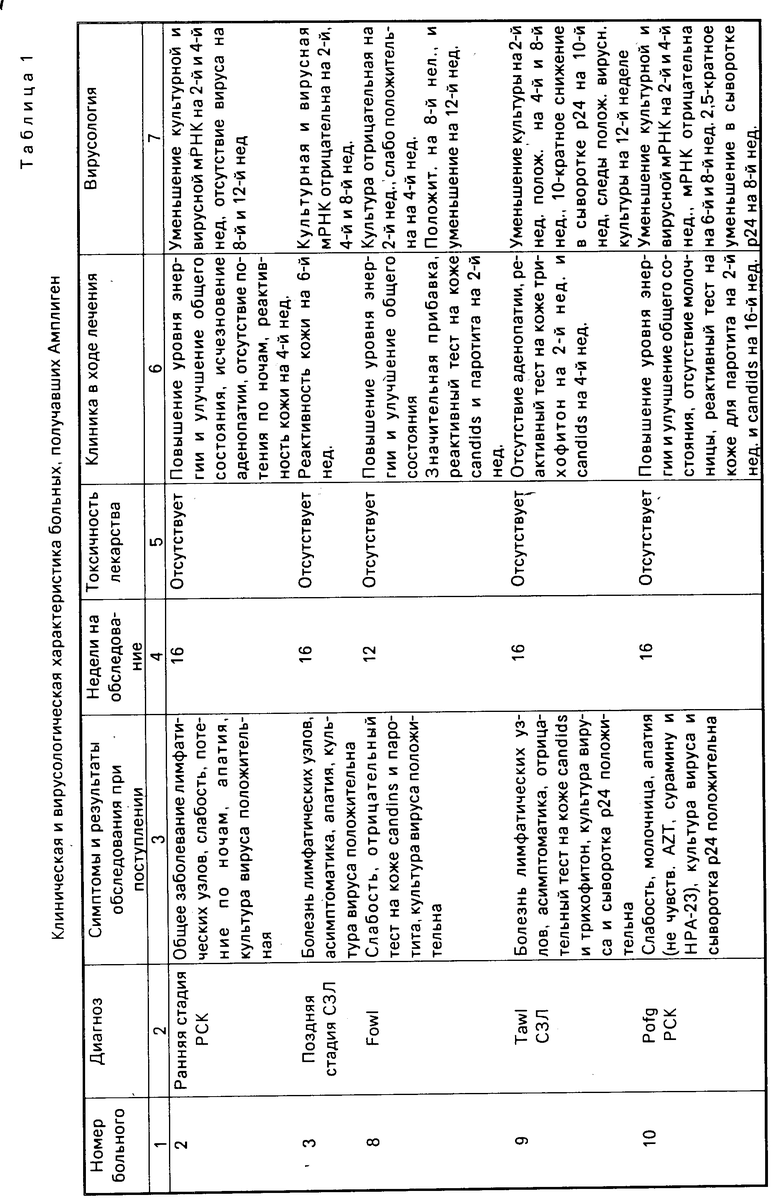
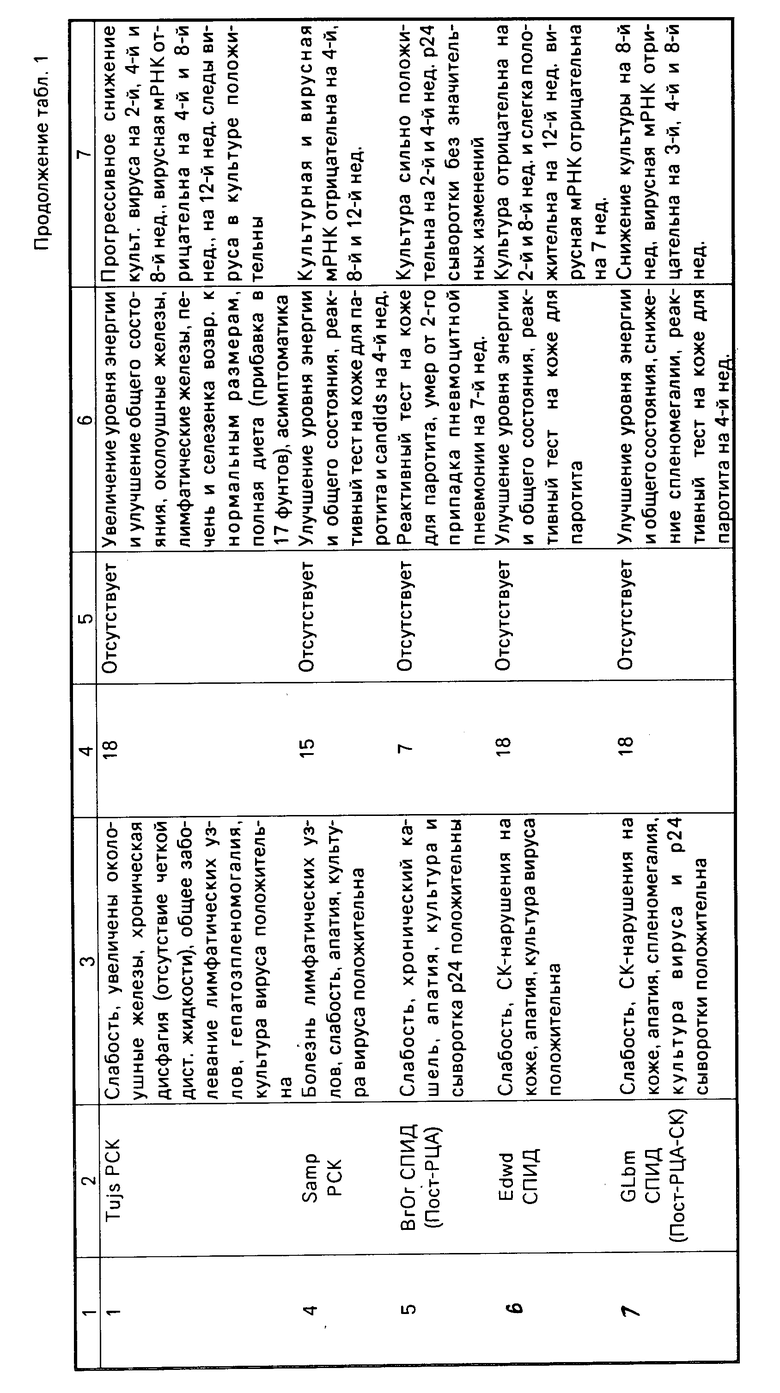
В табл.1 приведены обобщенные данные лечения 10 пациентов Амплигеном.
Экстракты клеток Н1929 (РНаза L минус), использованные в качестве источника рибосомной РНК, инкубируют 1 ч в отсутствие или присутствии цитоплазмических экстрактов МКПК здорового контрольного объекта или больных РСК и СПИД (каждый из которых получает свой кодировочный номер) перед лечением Амплигеном. Клетки Н1929 депозитированы в Американской Коллекции типовых культур.
До лечения экстракты от всех больных РСК-СПИДом также дают отсутствие активации (отсутствие СПР) даже при добавлении экзогенных биоактивных олигоаденилятов (2'5'-р3А3 (10-8 М), гели не приведены, что подтвердило невозможность присутствия даже следов молекул функциональной РНазы L в лимфоцитах больных до приема Амплигена. И наоборот, параллельно с лечением Амплигеном наблюдается прогрессирующая активация in vivo PНазы L: у больного 6 (РСК, на 8-й неделе и на 16-й неделе лечения); у больного 7 (СПИД, на 8-й неделе), а также различных больных по табл.1 (гели не приведены). Стрелками указаны положения специфичных продуктов расщепления (СПР) РНазы L. Только у пациента под номером 5 не удалось активировать РНазу L в результате приема дзРНК и, как и следовало ожидать, он умер от вторичных всевозможных инфекций.
Случай 1 биологический путь образования у нормальных индивидуумов, включая и перенесших инфекцию НIV.
Случай 2 СПИД и предшествующие ему заболевания, в том числе РСК, СЗЛ, асимтоматические НIV, сероположительные индивидуумы с прогрессирующей тенденцией к СПИДу и т.д. (см. чертеж): стадии А, В и G чрезмерно функциональны вследствие того, что РНаза 1 связана с ингибитором (стадия D нефункциональна) и не может закончить путь образования, поэтому путь образования не может быть соответствующим образом завершен из-за отсутствия "подпитывающего контроля", и НIV мультиплицируется даже при высоких концентрациях интерферона, 2-5 А-синтетазы и биоактивных олигомеров (особенно активны тримеры и тетрамеры 2-5 А).
Экспериментальные данные: впервые наблюдается присутствие в значительных концентрациях 2-5 а-олигомеров в лимфоцитах не получавших лечения больных по всему клиническому спектру СПИДа. Однако в отличие от нормальных индивидуумов РНаза L неактивна у больных РСКом и СПИДом, не получавших лечения. Если полученные от больных РСКом, СПИДом препараты РНазы L первоначально интенсивно промыть (перед испытанием), в том числе и трихлоруксусной кислотой (ТХК), в результате эти препараты РНазы L восстанавливают свою функциональность, т. е. они оказываются способы катализировать специфичное расщепление (на гелях обозначено как СПР) или макромолекулярную РНК, их следует считать активными. Опыты по восстановлению показали, что ингибитор РНазы L вымывается или обрывается, но если его добавить вновь, снова прерывает, иными словами ингибирует, реакции РНазы L.
Накопленные к настоящему времени данные указывают, что статус РНазы L (активной или неактивной) дает важный прогностический параметр для НIV и что специфическая обработка при участии двунитевых РНК может исправить характерные для НIV нарушения. Клинический спектр индивидуумов от асимптоматических носителей НIV (например, больной 8 по табл. 1) до ранних заболеваний (например, РСК или СЗЛ, больные 2, 3, 9, 10, 1 и 4) и СПИДа в полном расцвете подвергнут действию дзРНК с целью определения, можно ли заставить ингибитор освободить РНазу L, при этом ожидалось, что такое событие на молекулярном уровне может привести к понижению уровня HIV и многообещающим клиническим улучшениям. Индивидуумы (с примерной массой 60 кг) принимали дважды в неделю 50-250 мг специфичной дзРНК, названной Амплигеном. Известно, что 2'-5'-олиго А-синтетаза является зависимым от дзРНК ферментом, и была сочтена резонной возможность замещения ингибитора в РНазе L путем постепенного увеличения концентрации внутри клетки специфичных биоактивных 2'-5'-олигомеров использованием искусственной (синтетической) дзРНК.
Из табл.1 видно, как применение неспаренной дзРНК приводит к поразительному снижению уровня НIV в сыворотке крови подвергнутых лечению больных. Активирование РНазы L коррелируется с содержанием НIV и приводит к клиническим улучшениям. Спаренная дзРНК может оказаться приемлемой и дозировки могут быть достаточно низкими, чтобы избежать нежелательных реакций, таких как поли 1. Поли С (дзРНК приготовлена Lam pson). Там, где возможно применение более высоких дозировок, необходимость в применении неспаренной дзРНК будет гораздо большей.
Рекомендуют, чтобы дзРНК была способна давать необходимые высокие концентрации 2'-5' А-олигомеры для вытеснения ингибитора РHазы L без токсического действия, например вследствие ускоренной биодоступности структуры, приспособленной активировать продуцированные 2'-5'-олигомеров без побочных эффектов, или следствие сравнительно короткого периода полураспада после приема.
Неспаренная двунитевая РНК является известной формой макромолекулярной РНК (патент США N 4024222 и патент США N 4130641), в которой дестабилизацией двойной спирали не допускают базового спаривания. Неспаренная РНК хорошо известна своей способностью индуцировать интерферон, что указывает на механизм, не связанный с индуцированием интерферона.
Типичным лечебным воплощением неспаренной двунитевой РНК является синтетическая дзРНК, образованная комплексом полирибоинозиновой и полирибоцитидиловой-уридиловой кислоты, таким как rIn r (Cx, U или G)n, где x принимает значения от 4 до 29, например rIn r(C12U)n, далее называемая "Амплигеном". Исследованы многие полимерные дзРНК, по своему поведению аналогичные Амплигену. Ключевое лечебное преимущество неспаренных РНК по сравнению с другими формами природных и/или синтетических РНК заключается в их низкой токсичности по отношению к животным и человеку. Известны комплексы изРНК, на ранних стадиях образования способные запускать в действие различные связанные с интерфероном эффекты, однако токсичность таких соединений исключает какое-либо клиническое их применение для лечения рака или аналогичных нарушений (патент США N 3666646).
Описаны известные виды активности различных интерферонов, индукторов и дзРНК в недавно вышедших справочных изданиях, посвященных данному вопросу (противораковые и интерферонные средства. Под ред. R.M. Ottenbrite и G.И.Вutler, Марсель Деккер, Нью-Йорк, 1984, с. 301-319; Справочник экспериментальной фармакологии по интерферонам./Под ред. Р.Е.Соme и W.A.Carter, 1984, изд. Шпрингер-Ферлаг, Нью-Йорк и Гейдельберг, с. 533-555).
Как сейчас известно, дзРНК, например Амплиген, обладают терапевтической активностью против определенных опухолей человека, в частности рака почки. Хотя по существующему в настоящее время мнению дзРНК отводят роль только "индукторов интерферона", тем не менее дзРНК проявляют активность по отношению к определенным опухолям человека, полностью устойчивым к действию интерферона (заявка на Европейский патент N 83305426.5).
Описано ингибирование НIV в культуре клеток человека с помощью дзРНК при использовании Амплигена в качестве прототипа дзРНК (заявка на Европейский патент N 86306582.7, 1986).
Термин "неспаренная дзРНК" подразумевает, что водородные связи (укладка оснований) между противостоящими нитями дзРНК остаются сравнительно интактными, т. е. прерываются мене чем одной парой оснований на каждые 29 последовательных остатков оснований.
дзРНК может представлять собой комплекс полиинозината и полицитидилата с определенным отношением урациловых оснований или гуанидиновых оснований, например от 1 в 5 до 1 в 30 таких оснований (поли 1. поли (С4-29 х U или G). дзРНК может отвечать формуле Поли 1. Поли С, U, где соотношение С U примерно 13: 1 и коэффициенты осаждения как для Поли 1, так и для Поли С менее 9 и в пределах 2 единиц друг от друга, предпочтительно для обоих примерно 0,5 7,5.
дзРНК может отвечать общей формуле rIn (C12-13U)n. Другие приемлемые примеры дзРНК обсуждаются ниже.
Композиция может включать дзРНК и средство, помогающее ингибировать НIV, такое как лимфокин, например интерферон или итерлейкин, такой как IL-2. В табл. 2 приведены различные комбинации композиций. Недостаток РНазы L или недостаток другого аналогичного зависимого от дзРНК фермента виден в различных клетках больных СПИДом, в том числе Т-клетках, ЕУ-клетках, АЛУ-клетках, лимфоцитах и моноцитах (табл.2).
дзРНК может рассматриваться в качестве "базового биологического средства" для лечения и коррекции некоторых вызванных НIV нарушений. В табл.2 приведено семь специфичных для НIV дефектов или нарушений, которые приведены в сочетании с соответствующими потенциальными лечебными комбинациями дзРНК в смеси с другим лечебным средством или средствами.
Неспаренные дзРНК, рекомендуемые для использования в настоящем изобретении, основаны на сополинуклеотидах, выбранных среди поли (Сх, U) и поли (Сх, G), где х означает цифровой показатель, принимающий значения от 4 до 29, и являются неспаренными аналогами комплексов полирибоинозиновой и полирибоцитилиновой кислот, образованных модифицированием rIn rCn, введением неспаренных оснований (урацил или гуанидин) вдоль нити полирибоцитидилата (rCn). дзРНК может происходить из поли (I), поли (С) дзРНК модифицированием рибозильного скелета полирибоинозиновой кислоты (rIn), например путем включения 2'-0-метилрибозильных остатков. Такие неспаренные аналоги rIn rCn, из которых предпочтительны отвечающие общей формуле rI (С12, U)n, описаны Сarter и ТS'о в патентах США NN 4130641 и 4024222. Описанные из ДНК, как правило, приемлемы для использования согласно настоящему изобретению.
Специфичные примеры неспаренных дзРНК, предназначенных для использования в изобретении, включают
поли(1). поли(С4,U)
поли(1). поли(С7,U)
поли(1). поли(С13,U)
поли(1). поли(С22,U)
поли(1). поли(С20,G)
поли(1). поли(С29,G)
поли(1). поли(Ср)23G > р.
Фармацевтические композиции в соответствии с изобретением включают неспаренную дзРНК, возможно также интерферон или другие иммунные модуляторы (лимфокин) в смеси с фармацевтически приемлемым носителем или разбавителем. Фармацевтические композиции, рассматриваемые настоящим изобретением, включают композиции, приспособленные для парентерального введения в приемлемом фармацевтическом носителе.
Например, парентеральные растворы, суспензии или дисперсии могут быть приготовлены согласно известным фармацевтическим приемам со стерильной водой или несодержащей пирогенов водой в качестве растворителя/разбавителя также в смеси с физиологически приемлемыми солями.
Количество вводимой неспаренной дзРНК предпочтительно достаточно для достижения пиковой концентрации в крови от 0,01 мкг/мл дзРНК до 1000 мкг/мл в систематической системе кровообращения в точке, удаленной от места вливания, сразу же после введения. При сопутствующем введении интерферона его предпочтительно включают в количестве, которое приводит к уровню в 0,1-100000 IRU на миллилитр жидкости организма. Как правило, вводимое количество зависит от тяжести симптомов, в частности уровня доступной внутриклеточной биоактивной дзРНК, молекул 2'-5'олиго А или 2'-5' А-синтетазы и относительного уровня ингибирования РНазы L. В используемом здесь значении термин жидкость организма означает раствор сыворотки, витаминов и т.д. который циркулирует в организме больного известны и опубликованы в виде диаграмм и таблиц, которые доступны в обычном порядке. Средний объем жидкости в организме составляет примерно 5-6 л.
Изобретение иллюстрируется примерами использования дзРНК.
Неспаренную дзРНК, например Амплиген, приготовляют в виде водного раствора таким образом, что при добавлении к различным клеткам человека получают переходные концентрации жидкости (для промывания клеток) в 0,01-250 мкг/мл. Использован ряд клеток потенциальных мишеней для инфекции НIV. Действие Амплигена на инфекционность HIV показано в табл.3.
Ниже описан типичный эксперимент с Н-9 клетками лимфоидными клетками человека, которые могут быть остро или хронически инфицированы HIV. Клетки выращены в стандартных условиях (Metsuya и др. Science, 1984, т.226, с. 172) и анализируют несколько недель на предмет присутствия ферментов НIV или специфичных для НIV белков. Амплиген добавляют в различных концентрациях до, после или одновременно с добавлением вируса, тем самым имитируя различные клинические состояния. Проведен тщательный анализ числа клеток, морфологии и т.д. с целью определения, оказывает ли неспаренная дзРНК различное неспецифическое действие на рост лимфоидной клетки, как было описано Mitsuya, вместе с другими ингибиторами. Клетки в различные моменты эксперимента выделяют и исследуют с помощью ВЭЖХ (высокоэффективной жидкостной хроматографии) на присутствие 2'-5'-А-олигомеров по известной методике (Lee и др. Bilchemistry, 1985, т. 24, с. 551). Определенные А-олигомеры, присутствующие в природе, придают клеткам устойчивость к вирусам, однако ранее не было описано и не предполагалось, что испытуемое соединение (синтезированное человеком) может точно вводить в действие такую природную реакцию селективно, тем самым усиливая природный защитный механизм против вирусов в целом и, в частности, против HIV.
Эксперимент А проведен при 25-кратном превышении вируса (выраженного в виде инфекционных единиц) по сравнению с клетками-мишенями, в то время как эксперимент В проведен при 10-кратном превышении клеток-мишеней (обозначены как Н-9 клетки) по сравнению с вирусом. Процент положительных клеток приведен по отношению к клеткам, которые экспрессируют маркеры НIV, обозначенные как р24 и р19 на основании иммунофлуоресцентного анализа; обратная транскриптаза означает вирусный фермент, определенный в клеточном центрифугате по стандартной методике, и обозначена как гА/dT. Одновременно проводят подсчет клеток: клетки мультиплицируются с нормальными скоростями роста при всех испытанных концентрациях Амплигена (вплоть до 300 мкг/мл). В экспериментах А и В Амплиген (50 мкг/мл) добавляют на первый день. ВЭЖХ-анализ показал (на 3-7-й день в опытах А и В) специфичное смещение в распределении 2'-5'-олигомера таким образом, что олигомеры в более высоким молекулярным весом (менее противовирусные) смещены к олигомерам с более низким молекулярным весом (более противовирусные), вносящим вклад в селективное и сильное подавление НIV. Одновременное определение РНазы L (фиг.1) указывает на восстановление РНазы L при последовательной обработке дзРНК.
Аналогичные опыты проведены и с другими различными клетками человека, являющимися потенциальными in vivo мишенями для НIV. В этих опытах использованы клетки, функционально определенные как EУ-клетки (естественные клетки-убийцы), Т-клетки фага-помощника, Т-клетки подавителя, моноядерные клетки и т. д. Во всех случаях неспаренная дзРНК в различных концентрациях оказывалась способной селективно прекращать и/или предотвращать мультипликацию HIV без какого-либо воздействия на рост и созревание нормальных клеток (табл. 2). Пролиферацию Т-клеток в культуре устанавливают стандартным добавлением 1L-2 фактора, т.е. хорошо известным в биологии клетки способом. Селективное подавление НIV с помощью неспаренной дзРНК устойчиво связано со специфичным смещением или усилением в распределении 2'-5'-олигомера, что установлено ВЭЖХ-анализом.
В соответствующих биохимических процессах дзРНК участвует в нисходящем направлении или в местах, отдаленных от мест биохимических нарушений индивидуумов группы риска (активно инфицированных или неинфицированных НIV), тем самым восстанавливает нормальную способность противостоять вирусам.
дзРНК очень эффективно воспринимается клетками, вследствие чего не требует интактных рецепторов интерферона. Кроме того, неспаренная дзРНК также существует в виде биоактивных фрагментов, что ускоряет внутриклеточное усвоение и распределение. Таким образом, дзРНК обладает потенциалом, позволяющим легко преодолеть барьер между кровью и мозгом, который может служить остаточным резервуаром НIV у отдельных индивидуумов.
Как правило, используемая в изобретения дзРНК имеет размеры молекулы, аналогичные тем, что приведены в виде примеров в патентах США NN 4024222 и 4130641, однако дзРНК с более низким молекулярным весом, получаемые в виде фрагментов родственных молекул, тоже эффективны. Такие фрагменты могут составлять, например, от половины до одной десятой размера типичного материала дзРНК, описанного ранее.
дзРНК активирует 2'-5' А-полимеразы и промотирует синтез 500-кратного прироста активных противовирусных олигонуклеотидов по сравнению с применяемым отдельно интерфероном (дзРНК дает до 250 наномолей 2'-5'-олиго А в 1,6 х 108 клетках, в то время как 200 ед./мл интерферона дают только 0,5 наномолей 2'-5'-олиго А).
Аналогичное явление наблюдалось в ЕУ-клетках индивидуумов с риском заболеть СПИДом или с явными признаками СПИДа. Аналогичная ситуация существует по отношению к уровню активности естественных клеток-убийц больных РСК-СПИДом. Однако гораздо меньше известно о механизме регуляции ЕУ-клеток. Больные РСК-СПИДом и здоровые члены группы риска часто обладают слабой способностью к иммунноконтролю (функциональные ЕУ- и Т-лимфоциты) и не могут быть реактивированы интерфероном. Амплиген действует в стороне от блока болезни и способен активировать цитотоксичные лимфоциты.

Использование: в вирусологической диагностике. Сущность изобретения: для определения HIV у пациента отбирают пробу лимфоидных клеток и с ними ставят биологический тест на налие РНазыL. По наличию РНазыL судят о присутствии HIV в пробе. 3 табл. 1 ил.
СПОСОБ ОПРЕДЕЛЕНИЯ HIV, включающий отбор биологического материала с последующей постановкой биологического теста, отличающийся тем, что, с целью повышения надежности определения, в качестве биологического материала используют лимфоидные клетки, а биологический тест ставят на наличие активированной РНазы L.
| Puthey et al | |||
| Science, 1986, v 234, р.1392-1395. |
Авторы
Даты
1995-11-27—Публикация
1988-03-03—Подача