Изобретение относится к новым дифенилметилпиперазиновым производным, в частности к новым дифенилметилпиперазиновым производным, обладающим эффектом ингибирования по отношению к гиперсокращению и гиперудлинению сердечной мышцы и защищающим эффектом в отношении некроза сердечной мышцы, не сопровождаясь при этом кардиодепрессантным действием.
Кроме того, изобретение относится к лекарственным препаратам, содержащим упомянутые выше новые дифенилметилпиперазиновые производные в качестве эффективных ингредиентов, которые воздействуют на систему кровообращения, в частности, лекарственным препаратам, содержащим новые дифенилметилпиперазиновые производные в качестве эффективных ингредиентов, ингибирующих некроз сердечной мышцы и препятствующих гиперсокращениям и гипернапряжениям миокарда, защищающих от некроза миокарда, не сопровождаясь при этом кардиодепрессантным эффектом, и к лекарственным средствам, содержащим те же самые ингредиенты, и используемым для лечения и предотвращения острого инфаркта миокарда.
Современное повышение средства возраста населения сопровождалось увеличением количества заболеваний кровеносной системы, таких, как артериальная гипертония, стенокардия и инфаркт миокарда. В частности, имелось множество проявлений острого инфаркта миокарда с летальным исходом. До сих пор, причина такого острого инфаркта миокарда относилась к закупорке, возникающей вследствие тромба или коронарного спазма коронарной артерии, которая осуществляет питание сердца. Однако, в последнее время, Капеко и др. выдвинули предположение нового механизма острого инфаркта миокарда, согласно которому у пациентов с сердечным инфарктом миокарда обнаруживается два вида некроза, статическое омертвление клеток (SD) и кинетическое омертвление клеток (KD), при этом KD является основной причиной острого инфаркта миокарда. (Journal of Tokyl Womer's Medical College, 52, 1443, 1982). Кроме того, Копеко с сотрудниками, используя кроликов для создания модели острого инфаркта миокарда, описали инфаркт, вызванный KD, при использовании кальциевых антагонистов для ингибирования его симптомов (японская патентная заявка N Sho 61-40651). Кроме того, за последнее время им удалось создать модель острого инфаркта миокарда, вызванного КD, в Zangendorff in vitro системе, аналогично тому, как это было установлено в системе in vivo. Однако, некоторые из этих Са антагонистов оказывали сильный кардиодепрессантный эффект, и надо полагать, желательным является создание соединений, выявляющих слабый кардиодепрессантный эффект при сильном ингибирующем воздействии на KD.
Объектом изобретения является создание соединений, обладающих вышеупомянутым KD-ингибирующим эффектом, не сопровождающимся кардиодепрессантным воздействием, и создание лекарственных препаратов, содержащих эти соединения в качестве эффективных ингредиентов для ингибирования некроза сердечной мышцы и течения и предотвращения острого инфаркта миокарда.
Цель изобретения создание не только новых дифенилметилпиперазиновых производных, обладающих KD-ингибирующим эффектом, не сопровождающимся каким-либо кардиодепрессантным действием, в частности новых дифенилметилпиперазиновых производных, имеющих конкретные замещающие группы, и их фармацевтически приемлемых солей, но также и создание лекарственных препаратов для ингибирования некроза сердечной мышцы и для лечения и предотвращения острого инфаркта миокарда, и в этих лекарственных препаратах в качестве эффективного ингредиента содержатся вышеназванные новые дифенилметилпиперазиновые производные, имеющие конкретные замещающие группы, и их фармацевтические приемлемые соли.
А именно, соединениями изобретения являются дифенилметилпиперазиновые производные, характеризующиеся химическим строением, представленным следующей формулой I: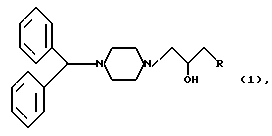
где R представляет собой 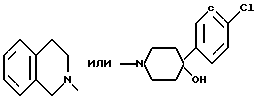
или их фармацевтически приемлемые соли.
К тому же, лекарственные препараты изобретения для ингибирования некроза сердечной мышцы и для лечения и предотвращения острого инфаркта миокарда содержат в качестве эффективного ингредиента один или несколько дифенилметилпиперазиновых производных, имеющих химическое строение, представленное формулой I выше или их фармацевтически приемлемые соли.
Новые дифенилметилпиперазиновые производные изобретения характеризуются сильным эффектом, предотвращающим некроз сердечной мышцы, не сопровождающимся кардиодепрессантным эффектом, и могут использоваться в качестве прекрасных ингибиторов некроза сердечной мышцы и прекрасного лекарства для лечения и предотвращения острого инфаркта миокарда. Следовательно, изобретение дает прекрасный ингибитор некроза сердечной мышцы и прекрасное лекарственное средство для лечения и предотвращения острого инфаркта миокарда.
Способность создавать сильное ингибирующее действие по отношению к некрозу сердечной мышцы, не сопровождающееся кардиодепрессантным действием, представляет собой новое свойство, раскрываемое в новых дифенилметилпиперазиновых производных данного изобретения.
Из формулы I можно увидеть: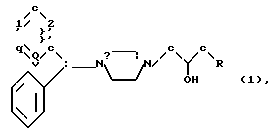
где R представляет собой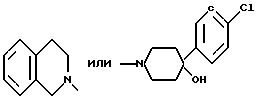
что соединение изобретения имеет основные атомы азота и оно, таким образом, способно образовывать кислотно-аддитивную соль в этом месте. Кислота, использованная для образования кислотно-аддитивной соли, может быть выбрана из фармацевтически приемлемых кислот. Следовательно, фармацевтически приемлемые соли соединения, изображенного в формуле I, также подпадают под охват соединений изобретения. Соли могут, например, включать неорганические кислые соли, такие, как гидрохлорид, сульфат, нитрат, фосфор или подобные им, и органические кислые соли, такие, как цитраты, малеаты, фумараты, адипаты, бензоаты, сукцинаты, ацетаты, тартраты, соли яблочной кислоты или подобные им.
Дифенилметилпиперазиновые производные формулы I изобретения и их фармацевтически приемлемые соли могут быть получены различными путями, например, в соответствии со схемой реакции А или В, при условии, что R в формуле реакции имеет то же значение, что и определенное в формуле I изобретения.
Способ А. Процесс получения представляется следующим образом.
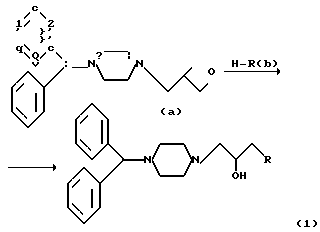
В вышеприведенном способе А аминное соединение формулы (b) является следующим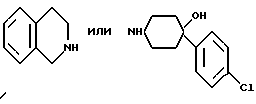
В процессе получения в соответствии со способом А в качестве исходного эпоксидного соединения (формула (а)) используется 1-(дифенилметил)-4-[1-(2,3-эпокси)пропил] пиперазин, а в качестве исходного аминного соединения используется тетрагидроизохинолин или 1-(4-хлорфенил-4-гидрокси)пиперидин (формула (b)).
В процессе получения в соответствии со способом А эпоксидное соединение 1-(дифенилметил)-4-[1-(2,3-эпокси)пропил]пиперазин (формула (а)) нагревается с аминным соединением 1,2,3,4-тетрагидроизохинолином или [4-(4-хлорфенил)-4-гидрокси]пиперидином в о-дихлорбензоле при нагревании с обратным холодильником в течение 1-4 ч, образуя соединение формулы I.
В процессе получения в соответствии со способом А, если в качестве аминного соединения формулы (b) используется 1,2,3,4-тетрагидроизохинолин, полученное таким образом соединение формулы I представляет собой 1-[2-(1,2,3,4-тетрагидро)изохинолинил] -3-[1-(4-дифенилметил)пиперазинил] -2-пропанол.
Кроме того, в соответствии с методом получения по способу А, если в качестве аминного соединения формулы (b) используется 4-(4-хлорфенил)-4-гидроксипиперидин, полученное таким образом соединение формулы I представляет собой 1-[1-(4-дифенилметил)пиперазинил]-3-[1-4-(4-хлорфенил)-4-гидрокси пиперазинил]-2-пропанол.
В обоих приведенных выше случаях соединения формулы I, которые получаются по методу получения в соответствии со способом А, могут быть выделены и очищены стандартными способами.
В процессе получения в соответствии со способом А исходное вещество формулы (а) может быть получено стандартными методами, относящимися к получению эпоксидных соединений.
Типичными способами получения вещества формулы (а) являются способы, детально описанные в следующих экспериментальных примерах. Основной реакцией является следующая.
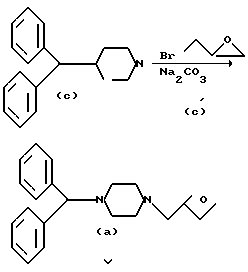
В приведенной выше схеме реакции, 1-(дифенилметил)пиперазин (формула (с)) взаимодействует с реагентом эпибромгидрином (формула (с')) в присутствии карбоната натрия в инертном растворителе с образованием соединения формулы (а).
Способ В. Процесс получения представляет собой следующую реакцию.
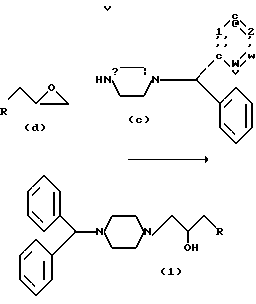
В методе получения в соответствии со способом В эпоксидное соединение формулы (d) нагревается с дифенилметилпиперазином формулы (с) в о-дихлорбензоле с обратным холодильником в течение от 1 до 4 ч с образованием соединения формулы I. Продукт реакции может быть выделен и очищен стандартными методами, как было упомянуто выше.
В методе получения в соответствии со способом В, если R в эпоксидном соединении представляет собой 1,2,3,4-тетрагидроизохинолинильную группу, эпоксидное соединение представляет собой 2-[1-(2,3-эпокси)пропил]-1,2,3,4-тетрагидроизохинолин, а полученный таким образом продукт реакции представляет собой 1-[2-(1,2,3,4-тетрагидро)изохинолинил] -3-[1-(4-дифенилметил)пиперазинил] -2-пропанол. Также, в методе получения по способу В, если R в эпоксидном соединении представляет собой 1-[4-(4-хлорфенил)-4-гидрокси] пиперазинильную группу, эпоксидное соединение является 1-[1-(2,3-эпокси)пропил] -4-(4-хлорфенил)-4-гидроксипиперидином и полученным таким образом продуктом реакции является 1-[1-(4-дифенилметил)пиперазинил]-3-[1-[4-(4-хлорфенил)-4-гидрокси]пиперидинил] пропанол.
Исходное вещество формулы (d) может быть синтезировано тем же способом, что и в формуле (а) способа А.
Полученные таким образом дифенилметилпиперазиновые производные могут быть с использованием стандартных способов превращены в форму различных, упомянутых выше солей.
Дифенилметилпиперазиновые производные формулы I изобретения и фармацевтически приемлемые соли обладают KD-ингибирующим эффектом и могут быть использованы в качестве лекарственных средств при лечении сосудистых заболеваний. В частности, производные могут быть полезными в качестве лекарственных препаратов для анти-миокардиального некроза, лекарственных средств для предотвращения и ингибирования некроза сердечной мышцы и лекарственных препаратов для лечения и предотвращения острого инфаркта миокарда.
Ингибитор для некроза сердечной мышцы и лекарственный препарат для лечения и предотвращения острого миокарда изобретения содержит в качестве эффективного ингредиента один или несколько соединений формулы I и их фармацевтически приемлемые соли.
В том случае, когда соединения изобретения используются в качестве лекарственных препаратов для ингибирования или предотвращения некроза сердечной мышцы или лекарственных средств для лечения или предотвращения острого инфаркта миокарда, их дозировка меняется в зависимости от степени заболевания, веса пациента, способа приема и т.п. и конкретно не ограничивается. Обычно, соединения могут приниматься орально или парентально (например, внутривенно) приблизительно один раз в день в количестве от 10 мг до 1,000 мг/д для взрослого человека (средний вес 60 кг). Формы для приема могут включать, например, порошок, parvule, гранулы, таблетки, капсулы, инъекции и т. п. Кроме того, препараты могут быть изготовлены с использованием стандартного носителя или разбавителя в соответствии с общепринятыми способами.
Экспериментальный пример 1.
1-(дифенилметил)пиперазин (10,0 г) растворяли в ацетонитриле (50 мл) и добавляли карбонат натрия (6,5 г) и эпибромгидрин (6,8 г) к раствору и нагревали с обратным холодильником в течение 2,5 ч. После фильтрования полученной соли, фильтрат концентрировали при пониженном давлении. Остаток очищали на силикагелевой хроматографической колонке (Waco Gel С-200, 200 г) и элюировали смесью растворителей хлороформ (99 частей) + метанол (1 часть) с образованием 1-(дифенилметил)-4-(1-(2,3-эпокси)пропил)пиперазина (5,9 г).
Спектр ядерного магнитного резонанса:
1Н-ЯМР (СДС13, 500 мГц) δ: 2,30-2,80 (12Н, м); 3,06-3,10 (1Н, м); 4,23 (1Н, с); 7,16 (2Н, т, J 7,3 Гц); 7,25 (4Н, т, J 7,3 Гц); 7,40 (4Н, д, J 7,3 Гц).
Экспериментальный пример 2.
1,2,3,4-тетрагидроизохинолин (25,0 г) растворялся в ацетонитриле (100 мл) и к раствору добавлялись карбонат натрия (40,0 г) и эпибромгидрин (31,0 г) и нагревались с обратным холодильником в течение 4 ч. После фильтрования образовавшейся соли, фильтрат концентрировался при пониженном давлении. Остаток очищался на хроматографической колонке с силикагелем (Waco Gel С-200, 500 г) и элюировался смесью растворителей из хлороформа (99 частей) + метанола (1 часть), образуя 2-[1-(2,3-эпокси)пропил]-1,2,3,4-тетрагидроизохинолин (15,6 г).
Спектр ядерного магнитного резонанса:
1Н-ЯМР (СДС12, 100 мГц) d: 2,36-2,60 (2Н, м); 2,73-3,03 (6Н, м); 3,09-3,29 (1Н, м); 3,65 (1Н, д, J 14,9 Гц); 3,83 (1H, д, J 14,9 Гц); 6,94-7,20 (4Н, м).
Экспериментальный пример 3.
1-(дифенилметил)-4-(1-(2,3-эпокси)пропил)пиперазин (3,0 г) и 4-(4-хлорфенил)-4-гидроксипиперидин (2,5 г) растворялись в о-дихлорбензоле (20 мл) и нагревались с обратным холодильником в течение 2,5 ч. После охлаждения продукт очищался на силикагелевой хроматографической колонке (Waco Gel С-200, 100 г), образуя 1-[1-(4-дифенилметил)пипаризинил]-3-[1-4-(4-хлорфенил)-4-гидрокси)пиперидинил]-2-пропанол (соединение I, 4,6 г).
Инфракрасный абсорбционный спектр:
ИКСmax (см-1) KBr: 3300, 2950, 2650, 1620, 1450, 1100, 910, 830, 750, 710 (для гидрохлорида).
Спектр ядерного магнитного резонанса.
1Н-ЯМР (СДС13, 500 МГц) d 1,50-1,90 (4Н, м), 2,01-2,21 (2Н, м), 2,30-2,55 (10Н, м), 2,80-2,98 (2Н, м), 3,87-3,93 (1Н, м), 4,22 (1Н, с), 7,16 (2Н, т. J 7,3 Гц), 7,26 (4Н, т, J 7,3 Гц), 7,30 (2Н, д, J 8,5 Гц), 7,40 (4Н, д, J 7,3 Гц), 7,42 (2Н, д, J 8,5 Гц).
FD Масс-спектр (ионизация).
FD-MS (m/z): 519, 521 (M+).
Экспериментальный пример 4.
2-[1-(2,3-эпокси)пропил] -1,2,3,4-тетрагидроизохинолин (3,0 г) и 1(дифенилметил)пиперазин (4,4 г) растворялись в о-дихлорбензоле (20 мл) и нагревались с обратным холодильником в течение 2,5 ч. После охлаждения продукт очищался на силикагелевой хроматографической колонке (Waco Gel С-200, 150 г), образуя 1-[2-(1,2,3,4-тетрагидро)изохинолинил]-3-[1-(4-дифенилметил)пиперазинил] -2-пропанол (соединение 2, 6,0 г).
Инфракрасный абсорбционный спектр.
ИКСmax (см-1) Kbr: 3400, 3000, 2550, 1620, 1450, 1080, 920, 760, 710 (для гидрохлорида).
Спектр ядерного магнитного резонанса.
1Н-ЯМР (СДС13, 100 МГц) d 2,30-2,60 (12Н, м), 2,75-2,95 (4Н, м), 3,62-3,80 (2Н, м), 3,92-4,03 (1Н, м), 4,21 (1Н, с), 7,00-7,51 (14Н, м).
FD масс спектр.
FD-MS (m/z): 441 (М+).
Фармакологическое испытание.
Методика испытания (1).
Было выделено сердце крысы мужской особи, весом от 300 до 380 г, и осуществлялась перфузия под давлением в 80 см, измеряемым водомером, в соответствии с методом Лангендорфа. Бикарбонатный раствор Krebs-Henseleit (37oC, pH 7,4), содержащий 11 мМ глюкозы, оксигенировался смесью газа, состоящего из 95% O2 + 5% CO2. Кроме того, сердце подвергалось компульсивно стимулированию действием электростимулятора при 330 сокращений/мин. После стабилизации в течение 10 мин, была осуществлена перфузия в течение 10 мин с использованием раствора Krebs-Henseleit, содержащего 5,5 мМ кальция в виде кальциевого отложения, в котором растворялось испытуемое соединение. После этого, в перфузат было добавлено 1,5 мл водного раствора, содержащего 0,1 мг адреналина в качестве пускового лекарственного средства, и, спустя 1 мин, было добавлено 1 мл водного раствора, содержащего 10 мг кофеина. Спустя еще 2 мин, сердце было извлечено с тем, чтобы поместить его в раствор формальдегида. Сердце было зафиксировано в формальдегидном растворе и затем было разрезано в горизонтальном направлении с промежутками в 3 мм. Каждый из разрезанных блоков обезвоживался, обезжиривался и помещался в парафин, в надлежащем виде, и затем, был разрезан на слои толщиною от 3 до 4 мкм. Нарезанные образцы для приготовления препарата были помещены железо-гематоксилиновой краской по методу Heidenhain. С помощью оптического микроскопа производилось пять степеней оценки (-, ±, +, ++, +++) на основе степени некроза сердечной мышцы. Место, в котором отношение некроза сердечной мышцы к поперечному сечению левого желудочка сердца составляет не более, чем 5% т.е. (-) и (±), обозначалось как наличие эффекта ингибирования некроза сердечной мышцы.
Методика испытания (2).
Сердце крысы мужской особи весом от 300 до 380 г было выделено и подвергалось перфузии под давлением 80 см, измеряемым водомером, в соответствии с методом Лангендорфа в тех же условиях, что и в методике испытания (1). Латексный баллончик был вставлен в левый желудочек сердца и был использован для измерения как давления в левом желудочке, так и частоты сердечных сокращений. В этих условиях, когда функция сердца стабилизовалась, в течение 10 мин осуществлялась перфузия с использованием перфузата, содержащего соединение, подлежащее испытанию, и производилась регистрация изменения сердечной функции. Величина частоты сердечных сокращений (HR) x давление левого желудочка служило оценкой при выявлении сердечной функции.
Результаты испытания.
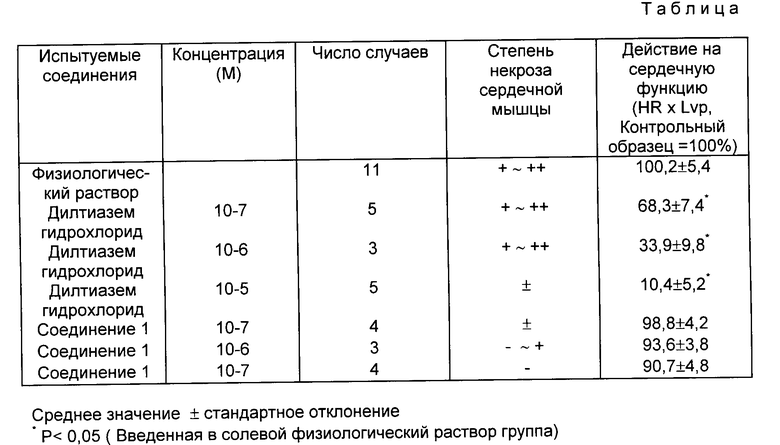
Результаты испытаний по методика (1) и (2) показаны в таблице.
Из колонки, показывающей степень некроза сердечной мышцы в таблице, можно видеть, что соединения 1 и 2 характеризуются более сильным эффектом ингибирования некроза ткани сердечной мышцы по сравнению с дилтиазем гидрохлоридом (торговая марка: Herbesser). Кроме того, из колонки, показывающей в таблице действие на сердечную функцию, даже при дозах, значительно больших для ингибирования некроза сердечной мышцы, соединения 1 и 2 имеют значительно меньшее воздействие на сердце и в качестве активного ингредиента лекарственных препаратов для защиты сердечной мышцы является эффективными в ингибировании и предотвращении некроза сердечной мышцы и лечении и предотвращении острого инфаркта миокарда. Действие на сердечную функцию в таблице.
Промышленная применимость.
Соединения изобретения являются новыми дифенилметилпиперазиновыми производными, обладающими эффектом ингибирования гиперсокращений и гипернапряжений миокарда и защищающими от некроза сердечной мышцы, не вызывая при этом кардиодепрессантного эффекта. Например, в качестве лечебных лекарственных препаратов эти соединения являются значительно более эффективными при лечении и предотвращении острого инфаркта миокарда по сравнению с предшествующими лекарственными средствами для лечения и предотвращения указанных болезней, и представляют собой прекрасный ингибитор некроза сердечной мышцы, который является эффективным в ингибировании и предотвращении некроза сердечной мышцы.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНОЕ 1,4-БЕНЗОТИАЗЕПИНА | 1991 |
|
RU2089550C1 |
| ПРИМЕНЕНИЕ МОКСОНИДИНА ДЛЯ ЛЕЧЕНИЯ ПОСТИНФАРКТНЫХ СОСТОЯНИЙ | 2000 |
|
RU2261097C2 |
| Кардиопротекторная фармацевтическая субстанция и способ ее получения | 2016 |
|
RU2629772C1 |
| ТЕТРАГИДРОИЗОХИНОЛИНКАРБАМАТЫ 1,2,3,3А,8,8А-ГЕКСАГИДРО-1,3А-8-ТРИМЕТИЛПИРРОЛО (2,3-B)ИНДОЛА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ АЦЕТИЛХОЛИНЭСТЕРАЗЫ | 1990 |
|
RU2124516C1 |
| ПРОИЗВОДНОЕ ДИГИДРОИНДОЛИЗИНОНА | 2015 |
|
RU2707887C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 1,2,3,4-ТЕТРАГИДРОИЗОХИНОЛИНА | 2005 |
|
RU2378257C2 |
| ПРОИЗВОДНЫЕ ЦИННАМОИЛ-ПИПЕРАЗИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ PAR-1 | 2007 |
|
RU2440997C2 |
| КОМБИНАЦИЯ, СОДЕРЖАЩАЯ АНТАГОНИСТ РЕЦЕПТОРА АНГИОТЕНЗИНА II И ЭПОКСИСТЕРОИДНЫЙ АНТАГОНИСТ РЕЦЕПТОРА АЛЬДОСТЕРОНА | 1996 |
|
RU2166330C2 |
| СОЕДИНЕНИЯ ГЕКСЕНОНА И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНСКИХ ЦЕЛЯХ | 2011 |
|
RU2553668C2 |
| ПРИМЕНЕНИЕ ТАЛИПОРФИНА ИЛИ ЕГО ПРОИЗВОДНЫХ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ СЕРДЦА, А ТАКЖЕ ИХ ПОЛУЧЕНИЕ | 2001 |
|
RU2350326C2 |
Использование: в медицине, в качестве препаратов, обладающих эффектом ингибирования по отношению к гиперсокращению и гиперудлинению сердечной мышцы и защищающим эффектом в отношении некроза сердечной мышцы. Описываются дифенилметилпиперазиновые производные формулы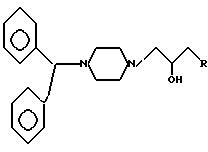
где R - группа формулы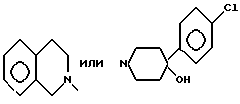
Реагент 1: 1-(дифенилметил)-4-[1-(2,3-эпокси)пропил]гиперазин; реагент 2: 1,2,3,4-тетрагидроизохинолин или [4-(4-хлорфенил)-4-гидрокси]пиперидин. Условия реакции: при нагревании, в о-дихлорбензоле. 1 табл.
Дифенилметилпиперазиновые производные следующей формулы: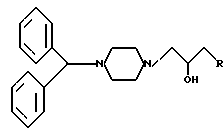
где R -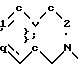
или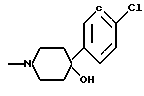
или их фармацевтически приемлемая соль.
| Способ получения пластических масс | 1927 |
|
SU10398A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Патент США N 4382934, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1997-09-27—Публикация
1991-07-10—Подача