Изобретение относится к электроаналитической химии и может быть использовано при определении микроколичеств мышьяка (III) в природных и сточных водах, пищевой и сельскохозяйственной продукции.
Известен способ определения мышьяка (III) на вращающемся стеклоуглеродном электроде (марка СУ-2000) (Васильев А.М., Темердашев З.А., Шмальц В.В.// Тез.докл. Всероссийская конференция по анализу окружающей среды "Экоаналититка-94"), Краснодар, 1994, с.42). В основе определения использовалась способность мышьяка (III) осаждаться на поверхность стеклоуглеродного электрода, модифицированную ионами меди (II). Определены оптимальные условия определения и установлены оптимальные концентрации Cu2+ (1•10-5 моль/л), вводимые при определении различных диапазонов концентраций мышьяка (III).
Известен способ определения мышьяка (III) на стеклоуглеродном электроде в присутствии ионов меди (II) (Anodic-stripping voltamperometric determination of arsenic at a copper-coated glassy-carbon electrode (S.Jaya, T.Prasada Rao and G.Prabhakara Pao// Talanta, vol.34, N 6, p.574-576, 1987). Интервал линейности наблюдается в пределах 7,5-750 мкг/л. Потенциал электролиза составляет - 0,6 B. В присутствии не менее 8•10-5 моль/л меди (II) регистрируют аналитический сигнал при потенциале +0,36 B. Время накопления 2 мин. Фон - 2M хлорная кислота (HClO4). Общий объем анализируемого раствора составляет 50 мл.
Целью настоящего изобретения является увеличение чувствительности определения мышьяка (III).
Указанная цель достигается тем, что концентрирование мышьяка (III) проводят на поверхности стеклоуглеродного электрода, покрытого золотом. В растворе до 3,0 М соляной кислоты осаждают мышьяк на поверхности электрода в интервале потенциалов -0,40-(-0,45)B в течение 1-10 мин, после чего регистрируют производную анодного тока по времени при линейной развертке потенциала. Нижний предел обнаружения мышьяка составляет 0,5 мкг/л.
Для установления оптимальных условий определения мышьяка (III) изучалась зависимость максимума производной анодного тока по времени от потенциала, времени электролиза и концентрации соляной кислоты.
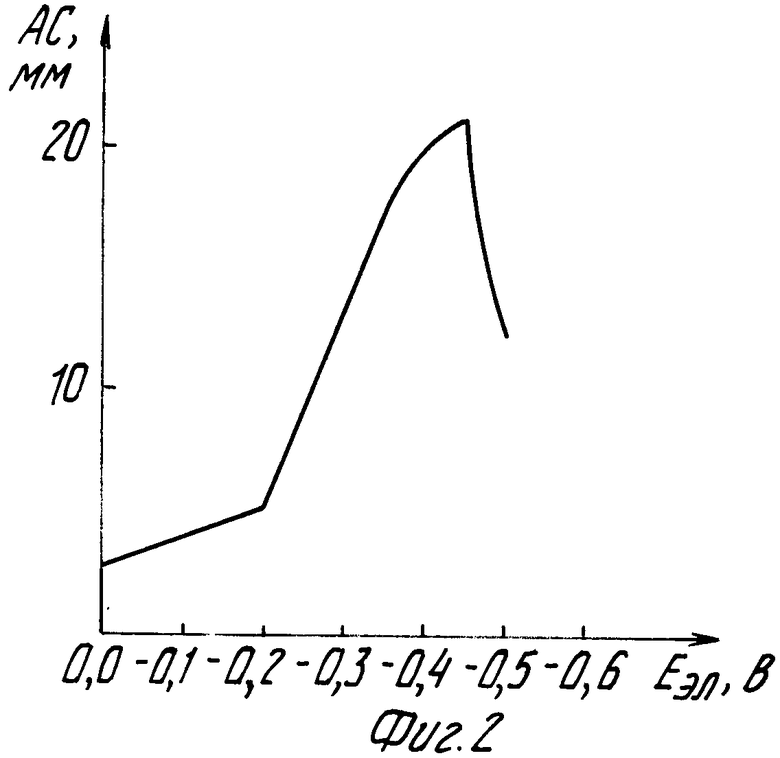
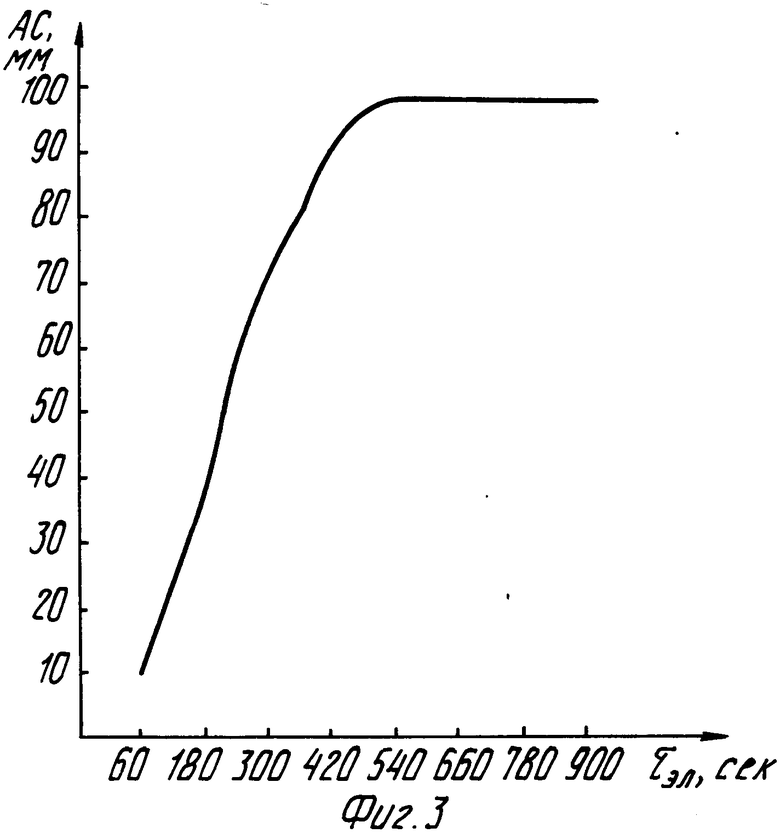
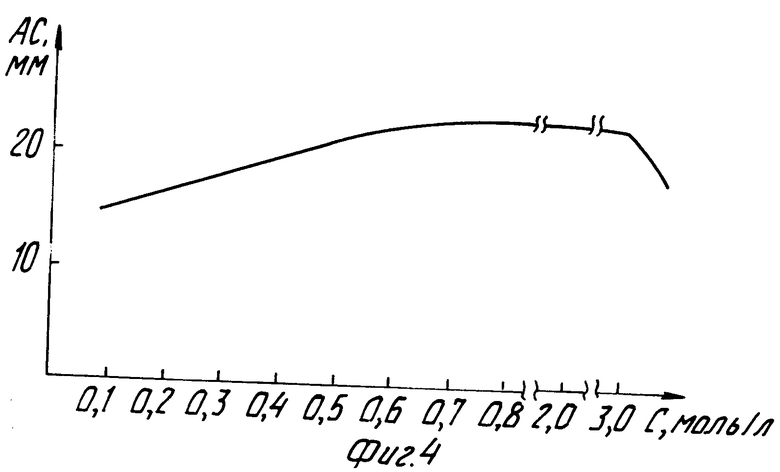
На фиг.1 представлены производные анодного тока по времени в растворах с разным содержанием мышьяка (III); на фиг.2 - зависимость аналитического сигнала As(III) от потенциала электролиза; на фиг.3 - зависимость аналитического сигнала As(III) от времени электролиза; на фиг.4 - зависимость аналитического сигнала As(III) от концентрации соляной кислоты.
Представленные на фиг.1 производные анодного тока по времени зарегистрированы в растворе 0,2 М HCl (1), содержащем 0,5 мкг/л (2); 1 мкг/л (3); 2 мкг/л (4); 4 мкг/л (5); 8 мкг/л (6) мышьяка (III), в интервале потенциалов от -0,4 до +0,6 В в течение 4 мин при скорости изменения потенциала 0,05 В/с в постоянно-токовом режиме с дифференцированием в 3-х электродной ячейке. Содержание мышьяка определяют методом калибровочной прямой (Ю.С.Ляликов //М. : Химия, 1974). Видно, что с увеличением концентрации ионов мышьяка (III) аналитический сигнал растет (фиг.1).
При изучении зависимости аналитического сигнала от одного из параметров (потенциала, времени и концентрации соляной кислоты) два других оставались постоянными. Стеклоуглеродный электрод, покрытый золотом, погружали в электролизер с раствором 0,2 М HCl, содержащем 7 мкг/л мышьяка (III), проводили электролиз в течение 4 мин при разных постоянных потенциалах в интервале 0,0-(-0,5) В и регистрировали производные анодного тока по времени. Измеряли величину максимума производной анодного тока по времени в зависимости от потенциала электролиза. Как видно из фиг.2 максимум производной анодного тока по времени увеличивается линейно с ростом отрицательного потенциала электролиза в интервале от -0,20 до (-0,45)В. В области потенциалов электролиза -0,4-(-0,45)В наблюдается максимальное значение аналитического сигнала. В случае проведения электролиза при потенциале -0,45-(-0,50) B величина аналитического сигнала уменьшается (фиг.2). Поэтому при определении мышьяка (III) оптимальным является проведение его накопления на электроде в интервале потенциалов -0,40-(-0,45)В.
При выбранном потенциале электролиза (-0,40-(-0,45) В стеклоуглеродный электрод, покрытый золотом, погружали в раствор 0,2 М HCl, содержащий 7 мкг/л мышьяка (III). Концентрирование As (III) проводили в интервале от 1 до 15 мин с одновременной регистрацией производного анодного тока по времени. Как видно из фиг.3, начиная от 1 до 10 мин, аналитический сигнал увеличивается с ростом продолжительности электролиза (фиг.3). При осаждении мышьяка (III) в течение более 10 мин величина аналитического сигнала практически не изменяется. Это обуславливает проведение электролиза в течение 1-10 мин.
Как видно из фиг.4, величины аналитических сигналов в растворе до 3,0 М HCl изменяются незначительно. Это обуславливает определение мышьяка (III) при концентрации соляной кислоты от 0,1 M до 3,0 М. При концентрациях больших 3,0 М наблюдается разрушение поверхности стеклоуглерода, покрытого золотом.
Таким образом, оптимальными условиями определения мышьяка (III) является концентрирование его на поверхности стеклоуглеродного электрода, покрытого золотом в растворе до 3,0 М HCl в интервале потенциала -0,4-(-0,45) В в течение 1-10 мин. Перечисленные условия являются существенными отличительными признаками.
Пример. Стеклоуглеродный электрод, покрытый золотом, погружают в электролизер с раствором 0,2 М HCl, содержащий 5 мкг/л мышьяка (III), и концентрируют его при потенциале -0,4 В в течение 4 мин при перемешивании раствора. Через 20 с регистрируют производную анодного тока по времени при линейной развертке потенциала в интервале -0,4-(+0,6) В и измеряют величину максимума анодного тока мышьяка (III). Содержание мышьяка (III) определяют методом калибровочной прямой. Получили значения: 4,8; 5,0; 5,1; 5,2 (мкг/л As(III)).
При определении мышьяка (III) использовался стандартный образец состава раствора соли мышьяка (ГСОРМ -13) ГСО 3397-86 с массовой концентрацией ионов 0,1 мг/мл.
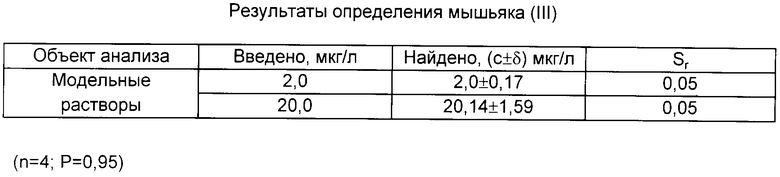
Правильность разработанного способа определения мышьяка (III) проверена с использованием метода добавок стандартного раствора способом введено - найдено, результат которого представлен в таблице.
Преимущество предлагаемого способа по сравнению с прототипом состоит в снижении (в 15 раз) предела обнаружения мышьяка (III) (предел обнаружения мышьяка составляет 0,5 мкг/л по сравнению с пределом обнаружения мышьяка в прототипе 7,5 мкг/л).
Изобретение относится к электроаналитической химии, а именно к способу определения мышьяка (III), включающему концентрирование мышьяка на поверхности стеклоуглеродного электрода в растворе кислоты с последующей регистрацией аналитического сигнала, при этом концентрирование мышьяка (III) проводят на поверхности стеклоуглеродного электрода, покрытого золотом, в растворе до 3,0 M в интервале потенциалов -0,40-(-0,45)B в течение 1-10 мин с последующей регистрацией производной анодного тока по времени при линейной развертке потенциала. 1 табл., 4 ил.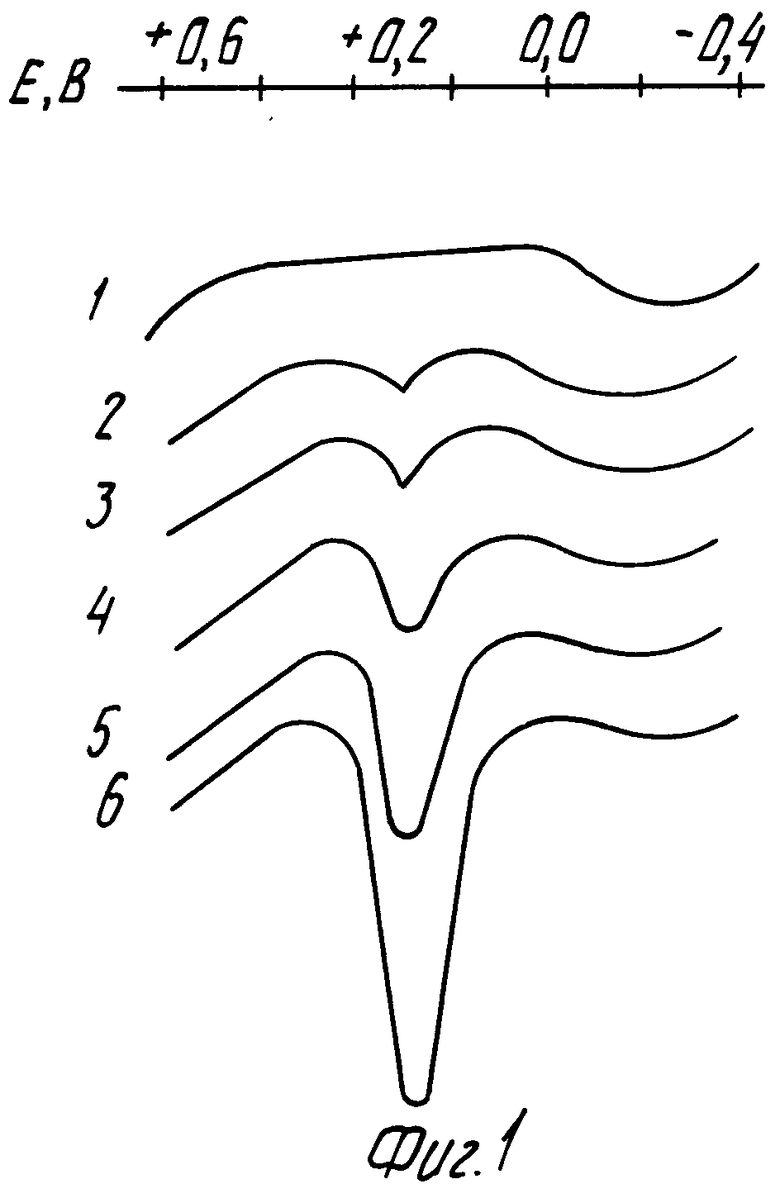
Способ определения мышьяка (III), включающий концентрирование мышьяка на поверхности стеклоуглеродного электрода в растворе кислоты с последующей регистрацией аналитического сигнала, отличающийся тем, что концентрирование мышьяка (III) проводят на поверхности стеклоуглеродного электрода, покрытого золотом, в растворе до 3,0 М в интервале потенциалов (-0,40) (-0,45) В в течение 1 10 мин с последующей регистрацией производной анодного тока по времени при линейной развертке потенциала.
| Anodic-stripping voltammetric determination of arsenic at a copper-coated glassy-carbon electrode | |||
| C.Jaya, T | |||
| Prasada Rao and G | |||
| Prabhakara Rao | |||
| Talanta, 1987, vol | |||
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| Приспособление для обучения правильному ведению смычка на смычковых инструментах | 1924 |
|
SU574A1 |
Авторы
Даты
1998-02-20—Публикация
1996-10-09—Подача