Изобретение относится к медицине, касается получения протективного гликопротеина возбудителя мелиоидоза, который может быть использован в качестве компонента для создания вакцин.
Известны различные способы выделения антигенных комплексов из возбудителей рода Pseudomonas, обладающих протективными свойствами.
Известен способ получения фильтратов бульонных культур возбудителя мелиоидоза. Обезвреженные формалином препараты обладают слабой иммуногенностью (Nigg C., Heckly R.G., Colling M. Toxin produced by Malleomyces pseudomallei//Proc.Soc.Exp.Biol.Med.-1955, -v.89, -p.17-20).
Известен способ получения антигенных комплексов оболочек из микробных клеток P.pseudomallei, обладающих некоторыми протективными свойствами. Способ включает получение клеточных стенок путем дифференциального центрифугирования взвеси клеток после их механической дезинтеграции, а также выделение белково-муреинового комплекса водно-фенольной экстракцией при 70oC (С.М. Фарбер. Диссертация "Сравнительная характеристика оболочек возбудителей сапа и мелиоидоза". Волгоград, 1979, с. 119-125).
Известен способ получения антигенных фракций для приготовления вакцин из возбудителей патогенных микроорганизмов, в том числе и Pseudomonas mallei. Иммуногенную фракцию получают из микроорганизмов после разрушения их методами замораживания - оттаивания либо ультразвуковой обработки. После центрифугирования взвеси клеток супернатант подвергают гель-фильтрации через колонку с Сефадексом C-200 (Andre Alme Dodin. Фр. патент 7406983 (2262533), 1975 "Procede de preparation d'une fraction antigenique utilisable en particulier pour is vaccination contra ie cholera).
В известных аналогах иммуногенные препараты представляют собой смесь различных антигенов, проявляющих протективный эффект.
Наиболее близким решением является способ получения протективного антигена из микробных клеток P.pseudomallei (прототип - Dodin M.A. Les antigens vaccinants. -Bordeaux Med/ 1979, 5, p. 229-301).
В прототипе автор выделяет поверхностные антигены липопротеиновой природы из клеток, высушенных ацетоном, обрабатывая их ультразвуком с частотой 500 кГц. После центрифугирования экстракт подвергают гель-фильтрации на колонке с сефадексом G-200. Выделенная антигенная высокомолекулярная фракция W1+2 обладает выраженным протективным эффектом. При вакцинировании 30 дельфинов его иммуногенность составила более 75%.
Анализ условий способа получения иммуногенного препарата в прототипе показывает, что для гомогенизации микробных клеток используют жесткий режим их разрушения. Проведенные нами исследования по влиянию различных режимов обработки клеток на выход поверхностных антигенов выявляют, что ультразвуковая обработка способствует более интенсивному разрушению антигенных структур, вследствие чего в экстракте обнаруживаются биомолекулы с большим разбросом по молекулярной массе с преобладанием низкомолекулярных компонентов.
Кроме того, гель-фильтрацией материала через сефадекс G-200 можно выделить только суммарный препарат, состоящий из биомолекул с мол. массой 400000-800000 Дальтон, т. е. затруднена возможность получения материала с высокой степенью гомогенности.
Целью изобретения является разработка технологии выделения гликопротеиновой фракции поверхностного антигенного комплекса возбудителя мелиоидоза, сохраняющей и проявляющей протективный эффект.
Поставленная цель достигается тем, что микроорганизмы типичного штамма возбудителя мелиоидоза австралийского серовара культивируют на целлофановой пленке, помещенной на поверхность плотной питательной среды, стерилизуют, получают водно-солевой экстракт растворимых антигенов. Супернатант отделяют центрифугированием и далее подвергают фракционированию последовательно гель-фильтрацией на носителе "Toypearl "HW-60F" и ионообменной хроматографией на DEAE сефадексе A-50.
Для получения гликопротеиновой фракции возбудителя мелиоидоза штамм P. pseudomallei 111 культивируют на целлофановой пленке, расположенной на поверхности плотной питательной среды в течение двух суток при 37oC. Бактериальную массу смывают 0,15 М раствором хлористого натрия и инактивируют ацетоном, охлажденным до -20oC. Микробные клетки отделяют фильтрованием через бумажный фильтр при атмосферном давлении, трижды промывают ацетоном, охлажденным до -20oC, и высушивают при комнатной температуре.
Водно-солевой экстракт готовят гомогенизацией 2%-ной вес/объем взвеси микробных клеток в забуференном фосфатами физиологическом растворе pH 7,2 при интенсивном перемешивании с использованием стеклянных бус d = 6 мм (20 бус на 50 мл взвеси) в течение двух суток (12 ч при 20oC и 36 ч инкубирование при 4oC) на шуттеле "Laboratory Shake" (Польша) в режиме работы прибора: амплитуда - 9, обороты - 150. Клетки осаждают центрифугированием при 10000 в течение 1 ч при 4oC. Супернатант, содержащий поверхностные растворимые антигены, далее подвергают гель-хроматографии на колонке с носителем "Toypearl" HW-60F" фирмы "Toyo Soda" (Япония). Фракционирование осуществляют забуференным фосфатами 0,3 М раствором хлористого натрия pH 7,2, содержащим 0,02% азида натрия. Скорость прохождения буферного раствора 90-120 мл/ч при температуре 8-12oC. Детекцию фракций осуществляют с помощью проточного спектрофотометра при длине волны 280 нм.
Фракции, содержащие протективный гликопротеин, выявляют реакцией иммунодиффузии в геле и иммуноэлектрофорезом с использованием козлиных гипериммунных сывороток, полученных к высушенным ацетоном клеткам P.pseudomallei. Гликопротеиновый антиген в иммуноэлектрофорезе проявляется в виде одной линии преципитата, расположенной в электронейтральной области электрофореграммы.
Фракции, содержащие гликопротеин, объединяют, концентрируют под азотом в ячейке "Amicon" с использованием фильтра PM-10 cd = 43 мм фирмы "Diaflo" (Ирландия) и диализуют против 0,05 М трис-HCl буферного раствора pH 7,7 в течение 24 ч с трехкратной сменой буфера. Затем материал наносят на колонку, заполненную DEAE-сефадексом A-50 в CL-форме, и проводят ионообменную хроматографию с использованием в качестве стартового буфера 0,05 М трис-HCl pH 7,7. Элюирование фракций проводят с использованием линейного градиента концентрацией NaCl от 0 до 1 М.
В результате элюции выделяют фракцию, содержащую протективный гликопротеин. По химическому составу полученная антигенная фракция представляет собой гликопротеин с весовым соотношением белка к углеводу 1:6 (анализ белка по Lowry, углевода по Dubois).
Количество выделяемого гликопротеина варьирует в пределах 0,7-1,5% от весового количества исходных микробных клеток и зависит от методов выращивания возбудителя мелиоидоза и способов гомогенизации его микробных клеток.
Таким образом, благодаря предлагаемому способу получен иммуногенный гликопротеин возбудителя мелиоидоза, проявляющий протективные свойства при заражении лабораторных животных вирулентными штаммами P.pseudomallei. Препарат может быть использован в качестве компонента мелиоидозной вакцины.
Пример 1. Подбор оптимального метода культивирования возбудителя мелиоидоза.
С целью получения максимального количества поверхностных антигенов в процессе роста P.pseudomallei исследуют два способа культивирования микробных клеток. По первому - используют традиционный метод получения бакмассы, заключающийся в выращивании микроорганизмов на мясо-пептонном агаре с 5% глицерина, pH 6,8 при 37oC в течение 24-48 ч. По второму методу односуточную бульонную культуру P.pseudomallei 111 в объеме 20 мл засевают на поверхность стерильной целлофановой пленки, покрывающей агар с толщиной слоя 3 см. Усилия инкубирования аналогичны первому способу. Далее бактериальную массу смывают 0,15 М раствором NaCl, сушат и инактивируют ацетоном, охлажденным до -20oC.
Выход гликопротеиновой антигенной фракции при использовании второго метода культивирования увеличивается в 1,5-2 раза.
Пример 2. Изучение различных методов получения водно-солевых экстрактов P.pseudomallei.
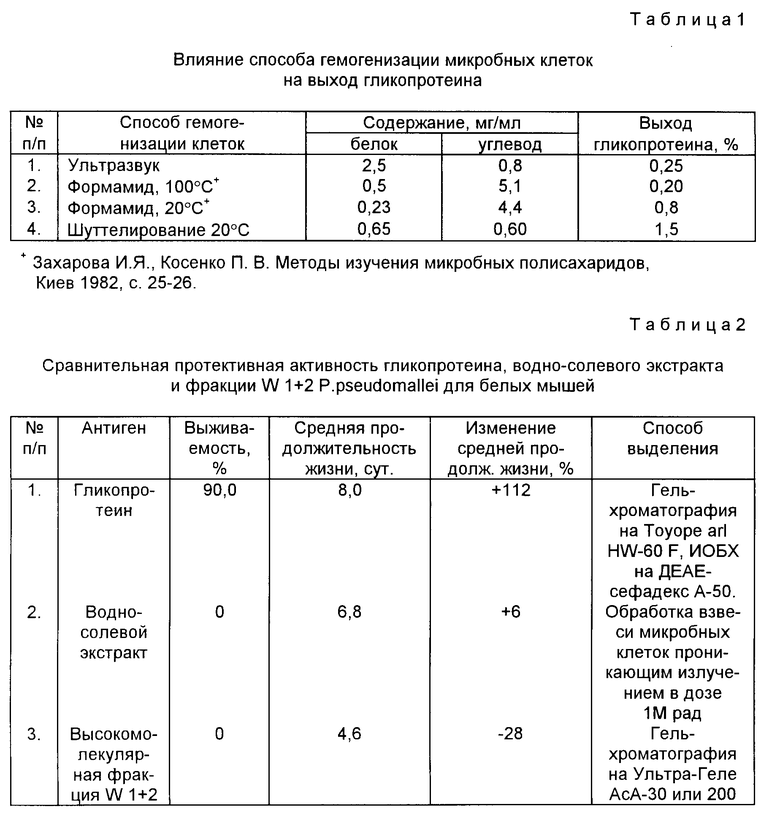
Для выделения протективного гликопротеина P.pseudomallei используют экстракты, полученные при различных методах гомогенизации микробных клеток, а именно ультразвуковой обработкой биомассы в фосфатно-солевом буфере, формамидной экстракцией при 20 и 100oC, шуттелированием микробной взвеси в забуференном физрастворе в присутствии стеклянных бус при 20oC. В табл. 1 представлены данные по химическому составу экстрактов, полученных различными методами.
Из данных табл. 1 видно, что максимальное количество гликопротеина получают при мягких щадящих условиях гомогенизации микробных клеток.
Пример 3. Подбор носителя и условий элюирования при гель-хроматографическом разделении водно-солевого экстракта P.pseudomallei.
Возможность эффективного разделения водно-солевого экстракта методом гель-хроматографии изучают на носителях "ToyopearI" HW-55, 60, 65F", fine фирмы "Toyo Soda" (Япония).
Для разделения используют хроматографические колонки размерами 2,8 х 70 см и 1,6 х 60 см. Элюирование фракций осуществляют различными растворами: дистиллированной водой, 1/3 М фосфатным буфером, pH 7,0, содержащим 0,2 М NaCl, 0,025 М трис-HCl буфером, pH 7,5, содержащим 0,3 М NaCl, и забуференным фосфатами физиологическим раствором, содержащим 0,3 М HCl и 0,02% азида натрия, pH 7,2.
Скорость элюирования на колонке 2,8 х 70 см составляет 80-120 мл/ч. Детекцию отобранных фракций осуществляют при длине волны 226 и 280 нм.
Оптимальное разделение водно-солевого экстракта было достигнуто на хроматографической колонке 2,8 х 70 см, заполненной носителем "Toyopearl "HW-60F", при нанесении от 3 до 10 мл 0,1-0,2% водно-солевого экстракта. В качестве элюента удовлетворительным является использование забуференного фосфатами физиологического раствора, pH 7,2, содержащего 0,3 М NaCl и 0,02% азида натрия.
Разделение на пять пиков поглощения достигают при скорости потока элюента 110 мл/ч. Первый пик профиля элюции содержит протективный антиген. Фракции первого пика объединяют, концентрируют под азотом на ячейке "Amicon" с фильтром pM-10 и диализуют против 0,05 М трис-HCl pH 7,7 буферного раствора в течение 24 ч при температуре 12oC с трехкратной сменой буфера для последующего разделения ионообменной хроматографией.
Пример 4. Подбор ионообменника и условий элюирования при ионообменном выделении протективного антигена (гликопротеина).
В качестве ионообменников для эффективного выделения протективного гликопротеина используют различные анионообменники: DEAE-сефадекс A-25 и A-50 в различных формах.
Учитывая специфичность протективного антигена, состоящего из значительного количества углеводного компонента и представляющего по молекулярной массе крупную биоструктуру, в качестве ионообменника использование DEAE-сефадекса A-50 в хлор-форме. Подбор значений pH для стартового буферного раствора от 7,5 до 8, предающего антигенному экстракту отрицательный заряд, обнаружил, что оптимальной величиной pH является 7,7. При этом значении pH достигают как определенной сорбции наносимого материала, так и успешного его элюирования при добавлении различных количеств хлористого натрия.
Для выделения протективного гликопротеина применяют хроматографическую колонку размерами 2,5 х 30 см, заполненную DEAE-сефадексом A-50 в хлор-форме, уравновешенным 0,05 М трис-HCl буферным раствором pH 7,7.
Антигенный препарат, выделенный гель-фильтрацией, после диализа в уравновешивающем буфере наносят на колонку и элюируют 0,05 М трис-HCl буферным раствором в градиенте концентраций NaCl от 0 до 1 М в течение 24 ч со скоростью 40 мл/ч при температуре 12oC.
Протективный гликопротеин обнаруживают во фракциях первого пика профиля элюции с помощью козлиной иммунной сыворотки. Фракции объединяют, концентрируют, диализуют против дистиллированной воды, лиофилизируют и используют для иммунизации лабораторных животных.
Выход протективного гликопротеина составляет 1,5% от весового количества исходных сухих микробных клеток. В сухом веществе гликопротеина весовое соотношение белка к углеводу составляет 1:6.
В аналитическом иммуноэлектрофорезе в геле агарозы протективный гликопротеин при тестировании его иммунными козлиными сыворотками широкой направленности к высушенным ацетоном микробным клеткам P.pseudomallei проявляется в виде отдельной электронейтральной дуги преципитата.
Пример 5. Изучение протективных свойств гликопротеина Pseudomonas pseudomallei.
Протективные свойства выделенного гликопротеинового антигена исследуют на двух видах лабораторных животных: белых мышах и белых крысах. Белым мышам выделенный гликопротеин вводят внутримышечно в дозе 20,0 мкг (по сухому весу) с неполным адъювантом Фрейнда, двухкратно, через 14 сут. Через 21 сут после второго цикла иммунизации животных заражают внутрибрюшинно дозой микробных клеток в 30 ЛД50 высоковирулентного штамма P.pseudomallei 100. Наблюдение за животными ведут в течение 36 дней.
Эксперимент на белых крысах проводят в аналогичных условиях за исключением того, что иммунизирующая доза протективного гликопротеина составляет 100 мкг на животное, а заражающая доза 13 ЛД50.
Высокомолекулярную фракцию W 1 + 2 - получают в условиях способа-прототипа.
Данные, полученные в ходе эксперимента, представлены в табл. 2 и 3.
Данные табл. 2 показывают, что иммунизация мышей предлагаемым гликопротеином приводит к 90%-ной выживаемости животных при 100%-ной гибели животных при использовании водно-солевого экстракта или фракции W 1 + 2. Средняя продолжительность жизни животных за наблюдаемый период увеличивается на 142%.
Испытания на белых крысах (табл. 3) показывают, что предлагаемая гликопротеиновая фракция способствует выживанию 60% взятых животных и увеличению их продолжительности жизни на 70,6%.
Иммунизация животных высокомолекулярной фракцией W 1 + 2, полученной в условиях эксперимента способа-прототипа, приводит к выживанию только 17% и увеличению средней продолжительности жизни на 15%.
Применение водно-солевого экстракта показывает его полную неэффективность для защиты животных, исключая увеличение продолжительности жизни животных лишь на 19%.
Таким образом, благодаря предложенному способу выделения антигенных фракций из вирулентного штамма P.pseudomallei 111 был выделен протективный гликопротеин с достаточной степенью чистоты. В лиофилизированном препарате весовое соотношение белка к углеводу составляет 1:6. Гликопротеин представляет собой электронейтральную биомолекулу и обладает иммуногенными свойствами.
Изучение протективных свойств полученного гликопротеина на таких лабораторных животных, как белые мыши и крысы, показывает выраженный эффект их защиты при заражении вирулентным штаммом P.pseudomallei 100.
Эти результаты позволяют рассматривать выделенный гликопротеин, как перспективный компонент для создания мелиоидозной вакцины.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КАПСУЛЬНОГО АНТИГЕНА ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА, ОБЛАДАЮЩЕГО АНТИФАГОЦИТАРНОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2255762C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОПРОТЕАЗ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 1995 |
|
RU2088663C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS. MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ ПОВЕРХНОСТНОМУ АНТИГЕНУ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 1997 |
|
RU2116344C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАПСУЛЬНОГО ВЕЩЕСТВА ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2001 |
|
RU2231364C2 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ КОМПОНЕНТУ КАПСУЛОПОДОБНОЙ СУБСТАНЦИИ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 1997 |
|
RU2117042C1 |
| СПОСОБ ВЫДЕЛЕНИЯ БЕЛКА 39 кДа НАРУЖНОЙ МЕМБРАНЫ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2002 |
|
RU2208445C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ УРОВНЯ ИММУНОГЕННОСТИ КАПСУЛЬНЫХ АНТИГЕНОВ BURKHOLDERIA MALLEI | 2005 |
|
RU2293993C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЛЕГОЧНОГО МЕЛИОИДОЗА | 1999 |
|
RU2157538C1 |
| СПОСОБ ДИФФЕРЕНЦИРОВАНИЯ ПАТОГЕННЫХ ОТ НЕПАТОГЕННЫХ БУРКХОЛЬДЕРИЙ | 2008 |
|
RU2378360C1 |
| СПОСОБ ИММУНОПРОФИЛАКТИКИ ЭКСПЕРИМЕНТАЛЬНОГО МЕЛИОИДОЗА ИНКАПСУЛИРОВАННЫМИ АНТИГЕНАМИ Burkholderia pseudomallei | 2008 |
|
RU2373955C1 |
Изобретение относится к медицине и касается получения гликопротеинового антигена PS. psendomallei, пригодного для изучения биологии мелиоидозного микроба и использования в качестве перспективного компонента для создания мелиоидозной вакцины. Сущность способа заключается в том, что для выделения гликопротеиновой фракции используют двухсуточную культуру вирулентного штамма PS.psludomallei австралийского серовара, выращенную на целлофановой пленке, расположенной на поверхности плотной питательной среды. Культуру обезвреживают ацетоном, получают из нее водно-солевой экстракт гомогенизацией 2%-ной взвеси микробных клеток в щадящих условиях. Далее гомогенат подвергают последовательному фракционированию методом гельфильтрации на носителе "Toyopearl "HW-60F" рН 7,2 и ионообменной хроматографии на DЕAЕ-сефадексе А-50, рН 7,7. В качестве элюента при этом используют 0,05 М трис-HCl буферного раствора в диапазоне концентраций хлористого натрия от 0 до 1 М. Выделенный гликопротеин представляет собой гликопротеин, состоящий из белка и углевода в соотношении 1 : 6, в иммуноэлектрофорезе выявляется в виде линии преципитата электронейтральной электрофореграммы. При заражении предварительно иммунизированных гликопротеином белых мышей и крыс вирулентными штаммами PS. psendomallei достигают значительного протективного эффекта. 3 табл.
Способ получения протективного гликопротеина возбудителя мелиоидоза, включающий культивирование микроорганизмов, получение водно-солевого экстракта, гель-фильтрацию, ионообменную хроматографию, отличающийся тем, что для получения протективного гликопротеина используют типичный штамм возбудителя мелиоидоза австралийского серовара, выращиваемый на целлофановой пленке, помещенной на поверхность плотной питательной среды, получают водно-солевой экстракт гомогенизацией 1 - 3%-ной взвеси микробных клеток при 20 - 30oС, который далее подвергают последовательно гельфильтрации с использованием носителя "Toyopearl "HW - 60F" и буферных растворов рН 7 - 7,5 ионообменной хроматографии на ДЕАЕ-сефадексе А-50 с применением в качестве элюента 0,05 М трис - НСl буферного раствора рН 7,7 с использованием линейного градиента в диапазоне концентраций хлористого натрия 0 - 1 М.
| Dodin M.A | |||
| Zes antigens vaccinants | |||
| - Bordeaux Med | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
Авторы
Даты
1998-04-27—Публикация
1996-06-06—Подача