Изобретение относится к медицине и касается выделения мажорного белка 39 кДа наружной мембраны (НМ) возбудителя мелиоидоза (Burkholderia pseudomallei), ассоциированного с вирулентностью этого опасного микроорганизма, и который может использоваться при создании специфических иммунодиагностических и иммунопрофилактических средств.
Известны различные способы выделения белков НМ грамотрицательных микроорганизмов, в том числе возбудителя мелиоидоза. Так, описан способ выделения белков из наружной мембраны Vibrio cholerae при помощи экстракции саркозилом, тритоном и ультрацентрифугирования с последующей ионообменной хроматографией. Полученные фракции содержали группу протеинов, в том числе и белок 38 кДа, который был очищен методом FPLC (fast protein liquid chromatography) (Chakrabarti S. , Chaudhuri K., Sen K,, Das J. Porins of Vibrio cholerae: purification and characterization of Omp U // J. Bacteriol. - 1996. - Vol. 178. - P.524-530). Однако данный способ получения белка 38 кДа является достаточно сложным и трудоемким.
Для Pseudomonas syringae описаны методы выделения биополимеров наружной мембраны при помощи водной, солевой и детергентной экстакции. В результате проведенных манипуляций была получена ассоциация белковых фракций, включающая в себя ряд протеинов различной молекулярной массы (м.м.), что само по себе не является способом выделения отдельных белков наружной мембраны (Mykhalskyij L. О., Ovod V.V., Gvozdiak R.I. Isolation and partial characteristics of biopolymers in the outer membrane of Pseudomonas syringae II Ukr Biokhim Zh. - 1990. - Vol.62. - P.40-47).
Известен также способ выделения белков наружной мембраны Psendomonas aerugimosa, которые изолировали при помощи экстракции клеток тритоном, этилендиаминтетрауксусной кислотой (ЭДТА) и лизоцимом. При этом были получены белки наружной мембраны и нековалентно связанный с пептидогликаном протеин (Hancock R.E., Irvin R.Т., Costerton J.W., Carey A.M. Pseudomonas aerugimosa outer membrane: peptidoglycan-associated proteins // J. Bacteriol. - 1981. - Vol. 145.- P.628-631). Однако и в этом случае способ не предполагает выделения очищенного мономерного мембранного биополимера.
Описан способ выделения мембранных белков из дезинтегрированной на Х-прессе биомассу В. pseudomallei методом дифференциального растворения препаратов в ионных и неионных детергентах и ультрацентрифугирования. Гель-хроматография полученного препарата НМ позволила фракционировать его на три составляющие, в которых были обнаружены порядка 10 групп белков (Гулько Л.Б. , Вейко В. П., Калачев И.Я. Определение белкового спектра фракций наружных мембран бактерий Burkholderia pseudomallei II В сб.: Проблемы медицинской и экологической биотехнологии. - Оболенск. -1999. - С.50). Однако в данном случае получали комплексный препарат белков наружной мембраны, содержащий достаточно значительную группу биополимеров.
Наиболее близким решением является способ выделения олигомерного белка 110 кДа НМ возбудителя мелиоидоза, ассоциированного с пептидогликаном (Gotoh N. , White N.J., Chaowagul W., Woods D.E. Isolation and characterization of the outer-membrane proteins of Burkholderia (Pseudomonas) pseudomallei. // Microbiology. - 1994. - Vol.140. - P.797-805).
В прототипе авторами предложена технология получения высокополимерного белка 110 кДа, заключающаяся в центрифугировании лизата биомассы возбудителя мелиоидоза в градиенте плотности сахарозы (70, 58, 52, 48, 40 и 30%) с последующей гель-фильтрацией полученной фракции на Sephacryl S-200 и ионообменной хроматографии на CM-Sepharose. Приготовленный таким образом препарат представлял в ДСН-ПААГе достаточно гомогенный биополимер с м.м. 110 кДа, который при нагревании до 95oС диссоциировал как минимум на четыре протеина, основным из которых являлся мономер 38 кДа. Полученный белок 110 кДа позволяет проводить экспериментальное конструирование синтетических мембран с целью изучения их проницаемости для низкомолекулярных углеводов. Однако авторами не выделены в чистом виде мономерные белки НМ В. pseudomаllei, что не позволяет оценить их иммунобиологические свойства, создать средства иммунохимической идентификации и специфической профилактики.
В то же время, для расшифровки функциональной значимости мембранных биополимеров в реализации вирулентных и иммуногенных свойств необходима эффективная технология выделения очищенных мономерных белков НМ возбудителя мелиоидоза. Кроме того, для аналитических целей следует иметь специфические иммунодиагностические тест-системы детекции этих белков.
Целью изобретения является выделение белка 39 кДа - основного мажорного компонента НМ, ассоциированного с вирулентностью возбудителя мелиоидоза.
Цель достигается тем, что односуточную бактериальную культуру смывают с пластин агара раствором, содержащим 10 mM Трис-НСl рН 8,0, 1,5 mM ЭДТА, 0,3 М сахарозы, добавляют мертиолат натрия до 1:10000 и подвергают 3 циклам замораживания и оттаивания, после чего клеточную суспензию обрабатывают ультразвуком (60 Вт) 6-кратно по 30 с на льду. Дезинтеграт дважды центрифугируют в течение 15 мин при 1500 g. Полученный супернатант дважды центрифугируют в течение 2 ч при 100000 g и 10oС, ресуспедируя его в растворе 10 mM Трис-HCI рН 8,0 и 1,5 mM ЭДТА. Полученный осадок ресуспендируют в минимальном объеме бидистилированной воды и центрифугируют при 100000 g и 10oС 2,5 ч в ступенчатом градиенте плотности сахарозы, приготовленном в 10 mM Трис-HCl рН 8,0, 1,5 mM ЭДТА: 5,0 мл 55%; 9,0 мл 43%; 8,0 мл 35%; 5,0 мл 19% сахарозы. Отбирают нижнюю фракцию в интерфазе градиента плотности сахарозы 43-55%, представляющую собой смесь белков НМ. Дальнейшее фракционирование протеинов с помощью гель-хроматографии на колонке 25х750 мм с TSK HW-60F (Toyopearl) и элюента: 0,5 М раствора NaCl с 0,05 М Трис-НСl рН 8,0 и 2% ДСН позволяет выделить фракцию, содержащую в основном белок 39 кДа. Использование препаративного электрофореза в 10% ДСН-ПААГ с последующей электроэлюцией позволяет выделить очищенный белок 39 кДа.
Полученный таким образом мажорный белок 39 кДа НМ возбудителя мелиоидоза представляет собой высокоочищенный протеин, пригодный для изучения иммунобиологических свойств и разработки средств его специфической идентификации.
Пример 1. Подбор методов и условий выделения очищенного белка 39 кДа.
Используют односуточную агаровую культуру типичного штамма возбудителя мелиоидоза, выращенную при 37oС на среде, содержащей кислотный гидролизат казеина и дрожжевой экстракт, которая по своим ростовым качествам не уступает средам фирмы "Difco". Выращивание культуры в течение двух и трех суток не используют, в связи с весьма сильным аутолизом микробных клеток. Биомассу смывают раствором 10 mM Трис-НСl рН 8,0 и 0,3 М сахарозы, в котором для лучшей элиминации надмембранного материала клетки добавляют 1,5 mM ЭДТА. С целью достаточно щадящей дезинтеграции бактериальные клетки вначале подвергают 3-кратному замораживанию и оттаиванию с последующей сонификацией при 60 Вт 6-кратно в течение 60 с на льду. Клеточные оболочки выделяют из дезинтеграта путем центрифугирования (дважды) при 1500 g в течение 15 мин (10oС), после чего супернатант дважды подвергают ультрацентрифугированию при 100000 g и 10oС в течение 2,5 ч, что позволяет получить комплексный препарат мембран, не содержащий крупные клеточные фрагменты. С целью фракционирования мембран применяют центрифугирование в ступенчатом градиенте плотности сахарозы (55, 43, 35, 19%) при 100000 g и 10oС в течение 2,5 ч. Данный методический прием позволяет более эффективно изолировать мажорные белки НМ в интервале градиента плотности 43-55%. Дальнейшее фракционирование протеинов осуществляют с помощью гель-хроматографии на колонке 25х750 мм с TSK HW-60 F (Toyopearl) и элюента: 0,5 М раствора NaCl с 0,05 М Трис-НСl рН 8,0 и 2% ДСН. Матрица данного носителя позволяет применять указанный активный детергент без ограничений. По данным электрофореза в ДСН-ПААГ белок 39 кДа обнаруживается как в первом, так и во втором пике профиля элюции, однако, в последнем случае содержится минимальное количество контаминирующих белков 42 и 27 кДа, что позволяет эффективно использовать препаративный электрофорез в 10% ДСН-ПААГ и электроэлюцию для выделения очищенного белка 39 кДа НМ возбудителя мелиоидоза (фиг.1).
Пример 2. Диссоциация высокомолекулярных белков наружной мембраны В. pseeudomallei, ассоциированных с пептидогликаном.
С целью оценки участия белка 39 кДа в формировании высокополимерного олигомера наружной мембраны возбудителя мелиоидоза препарат, содержащий белки наружной мембраны, и связанный с ними пептидогликан, подвергают температурной обработке в течение 5 мин при 95oС в присутствие ДСН и 2-меркаптоэтанола. В ДСН-ПААГ электрофорезе выявляют, что крупные мембранные биополимеры, находящиеся в зоне старта, отчетливо диссоциируют на ряд белков, одним из которых является мажорный белок 39 кДа и, следовательно, является мономерным протеином олигомера 120 кДа (фиг.2).
Пример 3. Экспрессия белка 39 кДа в зависимости от уровня вирулентности возбудителя мелиоидоза.
Для выяснения корреляции уровня вирулентности и экспрессии протеина 39 кДа используют типичные вирулентные штаммы В. pseudomallei, a также культуры, пассированные на чувствительных к мелиоидозу животных (золотистые хомячки) и полученные в лабораторных условиях с резко сниженной вирулентностью. Проводят сравнительное изучение белкового состава клеточных оболочек указанных вариантов возбудителя мелиоидоза с помощью ДСН-ПААГ электрофореза. Анализ электрофореграмм позволяет сделать заключение о наличии прямой корреляции экспрессии белка наружной мембраны 39 кДа и уровнем вирулентности возбудителя мелиоидоза, т.е. чем выше уровень вирулентности, тем выше продукция протеина 39 кДа (фиг.3).
Пример 4. Протективные свойства белка 39 кДа при экспериментальном мелиоидозе.
Для оценки иммуногенных свойств протеина 39 кДА используют иммунизацию им чувствительных к мелиоидозу лабораторных животных (золотистых хомячков и белых мышей) в дозе 15 мкг однократно, подкожно. Через 14 сут производят заражение высоковирулентным штаммом В. pseudomallei 100 в дозе 30 LD50. Учет результатов опыта проводят через 30 сут. Статистическая обработка полученных результатов свидетельствует, что белок 39 к Да наружной мембраны возбудителя мелиоидоза позволяет выжить до 10% взятых в опыт лабораторных животных в сравнении с контрольной группой при экспериментальном мелиоидозе.
Пример 5. Дифференциация вирулентных и авирулентных штаммов возбудителя мелиоидоза с помощью иммунной сыворотки к белку 39 кДа.
Антисыворотку с активностью в реакции иммунодиффузии в геле не менее чем 1: 32 добавляют к 15 мл расплавленного и остуженного до 45oС 1% агара "Difco", приготовленного на 0,15 М растворе NaCl, в количестве 0,25 мл. Тщательно перемешивают и выливают в чашку Петри, расположенную строго горизонтально. В сформировавшемся геле вырезают лунки диаметром 2,5-3,0 мм и заполняют их равными объемами бактериальных ультразвуковых дезинтегратов (60 Вт по 60 с трехкратно на льду), приготовленных из взвеси высушенных ацетоном микробных клеток (10 мг/мл) исследуемых штаммов. Через 24-36 ч учитывают результаты иммунодиффузии. Дезинтеграты вирулентных штаммов с монорецепторной сывороткой к белку 39 кДа формируют четкие округлые зоны преципитата различных размеров, у авирулентных культур эти зоны практически отсутствуют.
Полученный таким образом мажорный белок 39 кДа НМ возбудителя мелиоидоза представляет собой высокоочищенный протеин, ассоциированный с вирулентностью и пригодный для изучения его иммунобиологических свойств, разработки эффективных специфических идентификационных иммунологических тест-систем и конструирования иммунопрофилактических препаратов.


Изобретение относится к медицине и описывает способ выделения мембранного белка 39 кДа возбудителя мелиоидоза (Burkholderia pseudomallei). Выделение белка 39 kDa включает этапы выращивания бактерий, смыва биомассы, обработки клеточной суспензии ультразвуком на льду, центрифугирования дезинтеграта при 1500 g, двукратного центрифугирования при 100000 для выделения суммарного препарата клеточных мембран, центрифугирования препарата клеточных мембран на ступенчатом градиенте плотности сахарозы (55%, 43%, 35%, 19%) при 100000 g для изоляции наружной мембраны (НМ), последующей гель-хроматографии HM на TSK HW-60F (Toyopearl), препаративного электрофореза I пика элюции и электроэлюции белка 39 кДа. Изобретение обеспечивает получение мажорного белка 39 кДа НМ В.pseudomallei, представляющего собой высокоочищенный протеин, полностью сохраняющий антигенную активность и пригодный для изучения его иммунобиологических свойств, разработки эффективных специфических идентификационных иммунологических тест-систем и конструирования иммунопрофилактических препаратов. 3 ил.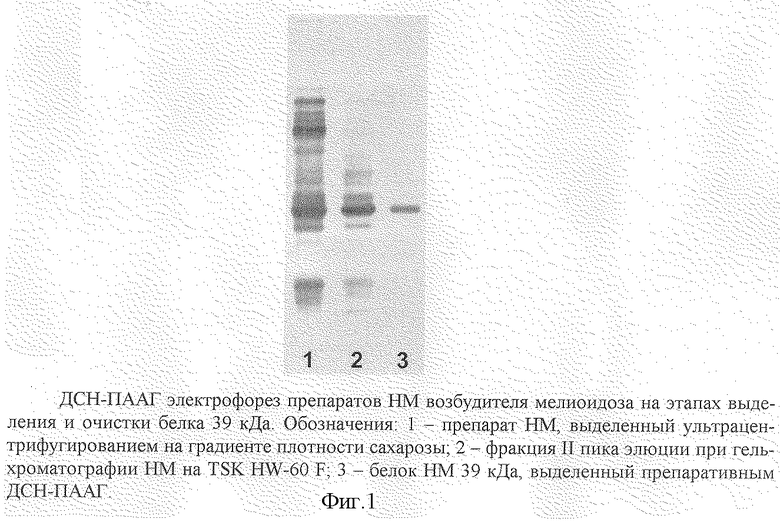
Способ выделения белка 39 кДа наружной мембраны возбудителя мелиоидоза, включающий выращивание бактериальной массы в течение 24 ч и выделение протеина, отличающийся тем, что смыв биомассы производят смесью ингредиентов, содержащей 10 mM Трис-HCl рН 8,0, 1,5 mM ЭДТА, 0,3 М сахарозы, добавляют мертиолат натрия до 1 : 10000 и подвергают 3 циклам замораживания и оттаивания, после чего клеточную суспензию обрабатывают ультразвуком (60 Вт) 6-кратно по 30 с на льду, дезинтеграт центрифугируют в течение 15 мин при 1500 g и 2 ч при 100000 g (10oС), ресуспендируя осадок в растворе 10 mМ Трис-HCl рН 8,0 с 1,5 mМ ЭДТА и бидистилированной воды с последующим центрифугированием при 100000 g и 10oС 2,5 ч в ступенчатом градиенте плотности сахарозы, приготовленном в 10 mМ Трис-HCl рН 8,0, 1,5 mМ ЭДТА: 5,0 мл 55%; 9,0 мл 43%; 8,0 мл 35%; 5,0 мл 19% сахарозы, фракцию, изолированную в диапазоне 35-55% плотности сахарозы, хроматографируют на колонке с TSK HW-60F (Toyopearl) 0,5 М раствором NaCl с 0,5 М Трис-HCl рН 8,0 и 2% ДСН, после чего проводят препаративный электрофорез в 10% ДСН-ПААГе с последующей электроэлюцией белка 39 кДа.
| Gotov N | |||
| et al | |||
| Microbiology | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| Способ закалки пил | 1915 |
|
SU140A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛАТЕКСНОГО ДИАГНОСТИКУМА | 1991 |
|
RU2012888C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЛЕГОЧНОГО МЕЛИОИДОЗА | 1999 |
|
RU2157538C1 |
Авторы
Даты
2003-07-20—Публикация
2002-02-20—Подача