Изобретение относится к области нефтехимического синтеза, в частности к способу получения транс-5,6-ди(замещенных)-1,9-декадиенов общей формулы I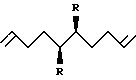 .
.
где
R - C4H9, C5H11, PhCH2, 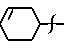 .
.
Указанные углеводороды могут найти применение в качестве исходного сырья для получения полимерных материалов, растворителей, компонентов моторных топлив и присадок, биологически активных препаратов, а кислородсодержащие производные (эпоксиды, кетоны) в лакокрасочной промышленности.
Известен способ получения замещенных α,ω - непредельных декатриенов, например 1-фенил-1,4E, 9-декатриена [1] совместно с 4-фенил-1,7-циклодекадиеном, заключающийся во взаимодействии бутадиена (350 г) со стиролом (бутадиен:стирол ≈ 2:1) в присутствии трехкомпонентного катализатора, состоящего из Ni(acac)2 (6,18 г), Et2AlOEt (6,3 г) и три-0-гидроксибифенилфосфита (12,9 г) в 100 мл циклооктадиена. Реакцию проводят в стальных автоклавах при температуре 80oС под давлением 60 атм. В результате образуется 1-фенил-1,4E, 9-декатриен (73,1%) и 4-фенил-1,7-циклодекадиен (4,3%). Недостатком способа является необходимость работы с пожаро- и взрывоопасным газообразным исходным реагентом (бутадиен) под давлением (60 атм) при сравнительно высокой температуре (≈ 80oС).
Известен способ получения замещенных α,ω - непредельных декатриенов, например 1-фенил-1,4E, 9-декатриена [2] совместно с 1,4,9-декатриеном и циклическими олигомерами бутадиена (4-винилциклогексен, циклооктадиен, циклододекатриен), заключающийся во взаимодействии бутадиена (100 г) со стиролом (бутадиен: стирол ≈ 2:1) в присутствии 3,9 ммоль CO и двухкомпонентного катализатора, состоящего из Ni (acac)2 (3,9 ммоль) и Et3Al (19,5 ммоль) в 25 мл бензола. Реакцию проводят в стальных автоклавах под давлением при температуре ≈ 80oС. В результате образуется сложная смесь углеводородов, состоящая из 1,4,9-декатриена, 1-фенил-1,4E,9-декатриена и циклических олигомеров (4-винилциклогексен, циклооктадиен, циклододекатриен). Недостатком способа является низкая селективность реакции. Наряду с замещенным α,ω - непредельным декатриеном образуются линейные и циклические олигомеры бутадиена (1,4,9-декатриен, 4-винилциклогексен, циклооктадиен, циклододекатриен). Процесс обладает повышенной пожароопасностью, т.к. необходимо работать с газообразным исходным реагентом (бутадиен) под давлением при температуре ≈ 80oС. Кроме того, известный способ не позволяет получать транс-5,6-диалкил(арил, алкенил)-1,9-декатриены.
Таким образом, в литературе совершенно отсутствуют сведения по регио-и стереоселективному синтезу транс-5,6-диакил(арил,алкенил)-1,9-декатриенов.
Целью изобретения является разработка нового способа регио- и стереоселективного синтеза транс-5,6-диалкил(арил,алкенил)-1,9- декатриенов.
Поставленная цель достигается взаимодействием α - олефинов (1-гексен. 1-гептен, 4-винилциклогекс-1-ен, аллилбензол) с этилалюминийдихлоридом (EtAlCl2) и металлическим магнием, взятых в мольном соотношении Mg : EtAlCl2:  = 10:(10-12):(20-22), преимущественно 10:11:21, в присутствии катализатора тетрахлорида циркония (ZrCl4) в количестве 3 - 6 мол.% по отношению к металлическому магнию, предпочтительно 5 мол.%, в атмосфере аргона при комнатной температуре (22 - 23oС) и нормальном давлении в ТГФ при перемешивании в течение 8 ч с последующим добавлением эквимолярного по отношению к EtAlCl2 количества бутиллития (BuLi) при температуре от -5 до 0oС однохлористой меди (CuCl) в количестве 2 - 4 мол.% по отношению к металлическому магнию, предпочтительно 3 мол.%, и аллилхлорида
= 10:(10-12):(20-22), преимущественно 10:11:21, в присутствии катализатора тетрахлорида циркония (ZrCl4) в количестве 3 - 6 мол.% по отношению к металлическому магнию, предпочтительно 5 мол.%, в атмосфере аргона при комнатной температуре (22 - 23oС) и нормальном давлении в ТГФ при перемешивании в течение 8 ч с последующим добавлением эквимолярного по отношению к EtAlCl2 количества бутиллития (BuLi) при температуре от -5 до 0oС однохлористой меди (CuCl) в количестве 2 - 4 мол.% по отношению к металлическому магнию, предпочтительно 3 мол.%, и аллилхлорида 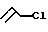 в четырехкратном избытке по отношению к EtAlCl2 (
в четырехкратном избытке по отношению к EtAlCl2 ( 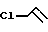 : EtAlCl2 = 4:1) с перемешиванием при комнатной температуре (22 - 23oС) 4 - 6 ч. Получают транс-5,6-диалкил-(арил, алкенил)1,9- декадиены с выходами 61 - 88%. Реакция протекает по схеме
: EtAlCl2 = 4:1) с перемешиванием при комнатной температуре (22 - 23oС) 4 - 6 ч. Получают транс-5,6-диалкил-(арил, алкенил)1,9- декадиены с выходами 61 - 88%. Реакция протекает по схеме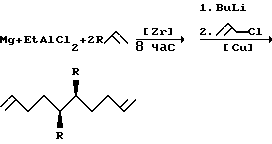 .
.
Проведение указанной реакции в присутствии катализатора ZrCl4 или CuCl больше соответственно 6 или 4 мол.% не приводит к существенному увеличению выхода целевых продуктов. Использование катализатора ZrCl4 или CuCl меньше соответственно 3 или 2 мол.% по отношению к металлическому магнию снижает выход дизамещенных α,ω - диенов, что связано с уменьшением реакционных центров. Опыты проводили при комнатной температуре (22 - 23oС). При более высокой температуре (например, 50oС) увеличивается содержание продуктов уплотнения, при меньшей температуре (например, 0oС) снижается скорость реакции.
Без катализатора ZrCl4 реакция не идет, без CuCl выход целевого продукта не превышает 15%. Не удается получить транс-5,6-диалкил(арил,алкенил)-1,9-декадиены без EtAlCl2 или его замены на другие алюминийорганические соединения, например AlEt3, i - Bu3Al, i - Bu2AlH.
Существенные отличия предлагаемого способа от известного: в известном способе используются в качестве исходных реагентов бутадиен, стирол и газообразная окись углерода, реакция протекает под давлением при повышенной температуре в присутствии фосфинового комплекса никеля. В предлагаемом способе реакция протекает в присутствии металлического Mg, α - олефинов, EtAlCl2, циркониевого и медного катализатора без давления при комнатной температуре.
Преимущество предлагаемого способа состоит в том, что предлагаемый способ в отличие от известных позволяет получать с высокой регио- и стереоселективностью транс-5,6-диалкил(арил,алкенил)-1,9-декадиены.
Пример 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 11 ммоль EtAlCl2 в 20 мл ТГФ, 10 ммоль магния (порошок), 21 ммоль 1-гексена и 0,5 ммоля ZrCl4, перемешивают 8 ч при комнатной температуре (22 - 23oС), добавляют 11 ммоль BuLi в гексане, затем при температуре от -5 до 0oС CuCl (0,3 ммоль) и аллилхлорид в количестве 44 ммоля. Реакционную массу перемешивают 5 ч при комнатной температуре, обрабатывают водой, выделяют транс-5,6-дибутил-1,9-декадиен с выходом 81%.
Спектральные характеристики транс-5,6-дибутил-1,9-декадиена:
ИК-спектр ( ν, см-1): 3095, 2985, 2940, 2870, 1640, 1470, 1010, 930.
Спектр ПРМ ( δ , м.д.): 0,89 т (6H, CH3), 1,23 м (18H, CH, CH2), 1,84 - 2,18 м (4H, CH2), 4,88 - 6,02 м (6H, олефиновые). М+ 250.
Спектр ЯМР13C ( δ , м.д.):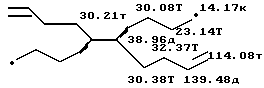 .
.
Другие примеры, подтверждающие способ, приведены в таблице.
Все опыты проводили при комнатной температуре (22 - 23oС) в ТГФ. В других растворителях (диоксан, эфир, гексан, бензол, циклогексан) выход целевых продуктов резко снижался.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ТРЕО-5,6-ДИЗАМЕЩЕННЫХ ГЕПТ-1-ЕНОВ И ТРЕО-5,6-ДИЗАМЕЩЕННЫХ ДЕКА-1,9-ДИЕНОВ | 1994 |
|
RU2109717C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНС-5,6-ДИ (ЗАМЕЩЕННЫХ)-ГЕПТ-1-ЕНОВ | 1993 |
|
RU2100337C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4,5-ДИАЛКИЛ(ФЕНИЛ)-1,4Z,9-ДЕКАТРИЕНОВ | 1995 |
|
RU2145319C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНС-1,2-ДИ(ЗАМЕЩЕННЫХ)-ЦИКЛОБУТАНОВ | 1993 |
|
RU2109719C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНС-3,4-ДИ(ЗАМЕЩЕННЫХ)-ТЕТРАГИДРОТИОФЕНОВ | 1993 |
|
RU2109740C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2-ДИАЛКИЛ(ФЕНИЛ)-ЦИКЛОБУТ-1-ЕНОВ | 1995 |
|
RU2106333C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(Н-БУТИЛ)-2-МАГНИЙ(Н-БУТИЛ)[60]ФУЛЛЕРЕНОВ | 1998 |
|
RU2136687C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ХЛОР-2-АЛЮМАБИЦИКЛО(3.2.2) НОНАНА | 1998 |
|
RU2139880C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-ЭТИЛ-2,3-ДИАЛКИЛ(ФЕНИЛ)АЛЮМАЦИКЛОПРОПЕНОВ, 1-ЭТИЛ-2,3-ДИАЛКИЛ(ФЕНИЛ)АЛЮМАЦИКЛОПЕНТ-2-ЕНОВ И 1-ЭТИЛ-2,3,4,5-ТЕТРААЛКИЛАЛЮМАЦИКЛОПЕНТАДИЕНОВ | 1999 |
|
RU2160269C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-(АЛКОКСИ)-2,3-ДИАЛКИЛ(ФЕНИЛ)АЛЮМАЦИКЛОПРОПЕНОВ, 1-(АЛКОКСИ)-2,3-ДИАЛКИЛ(ФЕНИЛ)АЛЮМАЦИКЛОПЕНТ-2-ЕНОВ И 1-(АЛКОКСИ)-2,3,4,5-ТЕТРААЛКИЛАЛЮМАЦИКЛОПЕНТАДИЕНОВ | 1999 |
|
RU2160268C2 |
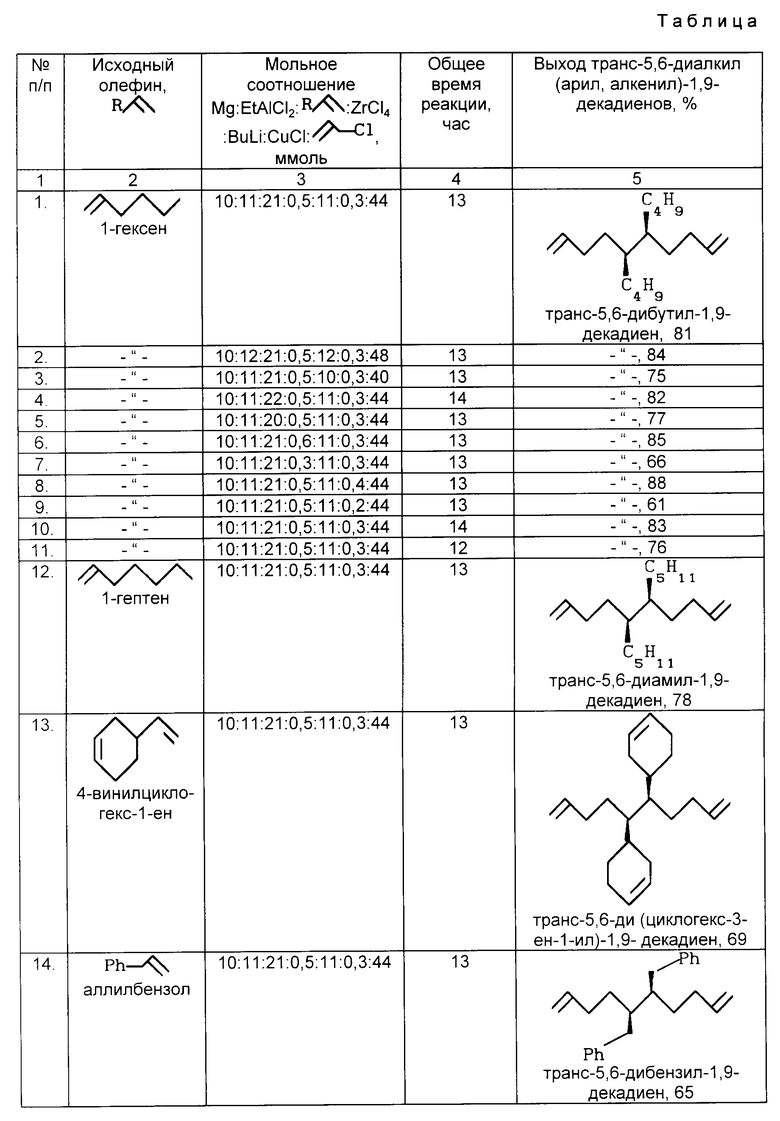
Изобретение относится к нефтехимическому синтезу, конкретно к способу получения транс-5,6-диалкил (арил, алкенил)-1,9-декадиенов, которые могут найти применение в качестве исходного сырья для получения полимерных материалов, растворителей, компонентов моторных топлив и присадок, биологически активных препаратов и т.д. Транс-5,6-диалкил (арил, алкенил)-1,9-декадиены получают путем взаимодействия 1-гептен, 1-гексен, 4-винилциклогексен-1-ен, аллилбензола с этилалюминийхлоридом и металлическим магнием в молярном соотношении, равном 20 - 22 : 10 - 12 : 10, в присутствии катализатора тетрахлорида циркония в количестве 3 - 6 мол.% по отношению к металлическому магнию в атмосфере аргона при комнатной температуре и нормальном давлении в среде тетрагидрофурана при перемешивании в течение 8 ч с последующим последовательным добавлением эквимолярного по отношению к EtAlCl2 количества бутиллития при температуре от -5o до 0oС, однохлористой меди в количестве 2 - 4 мол. % по отношению к металлическому магнию, аллилхлорида в четырехкратном избытке по отношению к EtAlCl2 и перемешиванием при комнатной температуре в течение 4 - 6 ч. Выход 80 - 88%. 1 табл.
Способ получения транс-5,6-ди(замещенных)-1,9- декадиенов общей формулы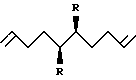
где R - бутил, амил, бензил, циклогексенил,
отличающийся тем, что 1-гексен, 1-гептен, 4-винилциклогекс-1-ен или аллилбензол подвергают взаимодействию с этилалюминийдихлоридом и металлическим магнием в молярном соотношении 20 - 22 : 10 - 12 : 10 в присутствии катализатора тетрахлорида циркония в количестве 3 - 6 мол.% по отношению к металлическому магнию в атмосфере аргона при комнатной температуре и нормальном давлении в среде тетрагидрофурана при перемешивании в течение 8 ч, с последующим последовательным добавлением эквимолярного по отношению к EtAlCl2 количества бутиллития при температуре от 5 до 0oС, однохлористой меди в количестве 2 - 4 мол.% по отношению к металлическому магнию, аллилхлорида в четырехкратном избытке по отношению к EtAlCl2 и перемешиванием при комнатной температуре в течение 4 - 6 ч.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Полуавтоматическая линия безотходной заготовки арматурных стержней | 1976 |
|
SU630046A1 |
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Патент США, N 3390195, кл | |||
| Аппарат для предохранения паровых котлов, экономайзеров, кипятильников и т.п. приборов от разъедания воздухом, растворенным в питательной воде | 1918 |
|
SU585A1 |
Авторы
Даты
1998-04-27—Публикация
1993-07-16—Подача