Изобретение относится к синергетическим фармацевтическим противовирусным комбинациям нуклеозидных производных, фармацевтическим композициям, содержащим вышеупомянутые комбинации и их использованию в медицинской терапии, в частности к способам лечения или профилактики вирусных инфекций, в частности ретровирусных инфекций.
Синдром приобретенного иммунодефицита (СПИД) является иммуноподавляющим или иммунодеструктивным заболеванием, которое является причиной предрасположенности организма человека в смертельным условно-патогенным инфекциям. Если быть более точным, то СПИД связан с прогрессирующим снижением содержания T-клеток, в частности тех из них, которые являются помощниками-индукторами, несущими маркер поверхности ОКТ4.
Вирус иммунодефицита человека (ВИЧ) был воспроизводимо выделен из пациентов, страдающих СПИДом или имеющих симптомы, которые часто предшествуют СПИДу. Вирус ВИЧ является цитопатогенным и проявляется в большинстве случаев в результате инфицирования и разрушения T-клеток, несущих ОКТ4-маркер. В настоящее время известно, что, вообще говоря, ВИЧ является этиологическим агентом СПИДа.
Со времени открытия того факта, что ВИЧ является этиологическим агентом СПИДа, были сделаны многочисленные предложения относительно анти-ВИЧ-химиотерапевтических агентов, которые могут оказаться эффективными при лечении пациентов, страдающих СПИДом. Так, например, в Европейском патентном описании N 0382526 предложены анти-ВИЧ замещенные 1,3-оксатиоланы. В патентном описании США N 4724232 и Европейском патентном описании N 0196185 предложен 3'-азидо-3'-деокситимидин (который получил санкцию на применение под названием зидовудин) и его использование при лечении СПИДа.
В этом патентном описании заявитель устанавливает, что 1-[2-(гидроксиметил)-1,3-оксатиолан-5-ил] -5-фторцитозин в комбинации с 3'-азидо-3'-деокситимидином /зидовудином/ позволяет получить неожиданно значительно более высокую анти-ВИЧ-активность этих соединений. Применение 1-[2-(гидроксиметил)-1,3-оксатиолан-5-ил] -5-фторцитозина вместе с зидовудином обеспечивает синергетический рост анти-ВИЧ-активности по сравнению с анти-ВИЧ-активностями каждого отдельного соединения.
В соответствии с первым отличительным свойством настоящего изобретения предлагается комбинация /a/ 1-[2-(гдроксиметил)-1,3-оксатиолан-5-ил]-5-фторцитозина формулы (I):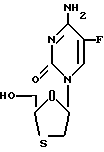 ,
,
или его физиологически функционального производного и
/b/ 3'-азидо-3'-деокситимидина /зидовудина/ формулы (II):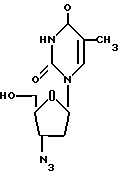 , или его физиологически функционального производного, причем компоненты (a) и (b) этой комбинации используются вместе так, что обеспечивается синергетический противовирусный эффект. Термин "синергетический противовирусный эффект", используемый в соответствии с настоящим изобретением, относится к противовирусному действию, которое выше ожидаемых чисто аддитивных эффектов отдельных компонентов (a) и (b) этой комбинации.
, или его физиологически функционального производного, причем компоненты (a) и (b) этой комбинации используются вместе так, что обеспечивается синергетический противовирусный эффект. Термин "синергетический противовирусный эффект", используемый в соответствии с настоящим изобретением, относится к противовирусному действию, которое выше ожидаемых чисто аддитивных эффектов отдельных компонентов (a) и (b) этой комбинации.
Необходимо отметить, что соединение формулы (I) содержит два хиральных центра и, следовательно, оно существует в форме двух пар оптических изомеров /т. е. энантиомеров/ и их смесей, включающих рацемические смеси. Соединение формулы (I) может быть либо цис-, либо транс-изомером или из смесями. Каждый цис- и транс-изомер может существовать в форме одного из двух энантиомеров или их смесей, включая рацемические смеси.
Все такие изомеры и смеси их, включая рацемические смеси, содержатся в области притязаний настоящего заявителя, которая также включает таутомерные формы соединений формул (I) и (II). В предпочтительном варианте используют цис-изомеры соединения формулы (I).
Под термином "физиологически функциональное производное" подразумевается приемлемая с фармацевтической точки зрения соль, сложный эфир или соль сложного эфира "базисного" соединения формулы (I) или (II), приемлемый с фармацевтической точки зрения амид соединения формулы (I) или любое другое соединение, которое после применения к пациенту способно превращаться /непосредственно или косвенно/ в "базисное" соединение или его активный метаболит или остаток.
Предпочтительные сложные эфиры в соответствии с изобретением включают сложные эфиры карбоновых кислот, в которых некарбониловая составляющая сложного эфира выбирается из линейного или разветвленного алкила, например н-пропила, третичн.-бутила, н-бутила, алкоксиалкила (например, метоксиметила), аралкила (например, бензила), арилоксиалкила (например, феноксиметила) и арила (например, фенила); сложные эфиры сульфонатов такие, как алкил- или аралкилсульфонил (например, метансульфонил); сложные эфиры аминокислот (например, L-валил или L-изолеуцил); сложные эфиры дикарбоновых кислот (например, полусукцинат); сложные эфиры моно-, ди- или трифосфатов. Сложные эфиры фосфатов могут быть, кроме того, этерифицированы, например, при помощи C1-20 спирта или его химически активного производного, или при помощи 2,3-ди(C6-24)ацил глицерина.
Любая алкиловая составляющая, содержащаяся в таких сложных эфирах, в предпочтительном варианте содержит от 1 до 18 атомов углерода, в частности 1-4 атома углерода. Любая ариловая составляющая, содержащаяся в таких сложных эфирах, в предпочтительном варианте содержит фенильную группу, необязательно замещенную, например, галогеном, C1-4 алкилом, C1-4 алкокси или нитро.
Приемлемые с фармацевтической точки зрения амиды соединения формулы (I) включают такие производные, в которых группа амино цитозина содержится в форме амида, например NHCOR, в котором R является C1-6 алкилом или арилом (например, фенилом, необязательно замещенным галогеном, C1-4 алкилом, C1-4 алкокси, нитро или гидроксилом).
Примеры приемлемых с фармацевтической точки зрения солей включают основные соли, например, полученные из соответствующего основания, такого как щелочной металл (например, натрий), соли щелочноземельных металлов (например, магний), аммония и NX
Примеры вирусных инфекций и связанных с ними клинических заболеваний, которые могут быть вылечены или предотвращены в соответствии с настоящим изобретением, включают человеческие ретровирусные инфекции, такие как вирус иммунодефицита человека /ВИЧ/, например ВИЧ-1 или ВИЧ-2, и лимфотропный вирус Т-клеток человека ЛВТЧ, например ЛВТЧ-I или ЛВТЧ-II-инфекции. Комбинации, являющиеся предметом изобретения, особенно эффективны при лечении СПИДа и связанных с ним клинических заболеваний, таких как комплекс, связанный со СПИДом /КСС/, прогрессирующая общая лимфаденопатия /ПОЛ/, нейрологические заболевания, связанные со СПИДом, такие как рассеянный склероз или тропический парапарез, анти-ВИЧ антитело-положительные и ВИЧ-положительные заболевания, такие как тромбоцитопенический акроангиотромбоз. Комбинации, являющиеся предметом изобретения, можно также использовать при лечении псориазов. Комбинации, являющиеся предметом изобретения, как было установлено, особенно эффективны при лечении бессимптомных инфекций или заболеваний, вызываеых или связанных с человеческими ретровирусами.
В соответствии со вторым отличительным свойством изобретения предлагаются комбинации, которые были уже описаны выше, для использования в медицинской терапии, в частности для лечения или профилактики для лечения или профилактики любой из вышеупомянутых вирусных инфекций или заболеваний, в частности ВИЧ-инфекций, включая СПИД.
Изобретение, кроме того, включает способ получения комбинаций, описанных выше, который содержит соединение вместе компонентов (a) и (b) комбинации в медикаменте, чтобы получить синергетический противовирусный эффект.
В соответствии с еще одним аспектом предлагается способ применения комбинации изобретения для получения медикамента для лечения любой из указанных вирусных инфекций или заболеваний.
Кроме того, в соответствии с изобретением предлагается способ лечения или профилактики вирусных инфекций (в частности, ВИЧ-инфекций) у млекопитающих (включая человека), который содержит применение к вышеупомянутому млекопитающему эффективного количества комбинации, описанной выше. Должно быть ясно, что в соответствии с изобретением компоненты (a) и (b) комбинации, могут быть применены одновременно или последовательно. Однако в последнем случае эти компоненты применяют в течение достаточно короткого промежутка времени, чтобы гарантировать достижение синергетического противовирусного эффекта.
Кроме того, в соответствии с изобретением предлагается способ усиления у млекопитающих (включая человека), страдающих вирусной инфекцией, противовирусной активности компонентов (a) и (b) комбинации при котором применяют к вышеупомянутому млекопитающему эффективное синергетическое количество компонента (a) одновременно, заранее или после применения компонента (b).
Преимущество комбинации изобретения заключается в том, что оно позволяет добиться улучшенной противовирусной эффективности при определенной дозе одной из противовирусных компонент (по сравнению с использованием только этой компоненты), при этом улучшается терапевтический показатель компоненты. Так, например, эту комбинацию можно использовать для лечения заболеваний, которые в противном случае потребовали бы относительно больших доз противовирусной компоненты, при которых могут возникать проблемы с токсичностью. Более низкие дозы этой комбинации могут обеспечить большее удобство для пациента и более высокую гибкость.
Комбинации изобретения могут быть применены к млекопитающему известным способом. Как указано выше, компоненты (a) и (b) могут быть применены одновременно (например, в единой фармацевтической форме) или отдельно (например, в отдельных фармацевтических формах). В общем случае эти комбинации могут быть применены местным, стоматическим, прямокишечным или парентеральным (например, внутривенным, подкожным или внутримышечным) способами. Должно быть ясно, что эти приемы могут варьироваться в зависимости, например, от серьезности заболевания, подлежащего лечению, и состояния пациента.
Должно быть также ясно, что несмотря на то, что в общем случае должна существовать оптимальная пропорция компонент, которая обеспечивает максимальное усилие, даже исчезающе малое количество одной компоненты будет достаточно, чтобы усилить эффект другой до некоторой степени, и поэтому любая пропорция двух усиливающих компонент будет все-таки обладать целевым синергетическим эффектом. Однако наибольшую синергию в общем случае отмечали, когда эти две компоненты содержатся в конкретных пропорциях.
Оптимальные молярные пропорции зидовудина к 1-[2-(гидроксиметил)-1,3-оксатиолан-5-ил] -5-фторицитозину или их соответствующих физиологически функциональных производных для использования в соответствии с изобретением изменяются в области от 1:1 до 1:600, в предпочтительном варианте от 1:10 до 1:250, а в самом предпочтительном варианте 1:25.
В дальнейшем компоненты комбинации именуются как "активные ингредиенты".
Дозировка комбинации будет зависеть от заболевания, подлежащего лечению, и других клинических факторов, таких как масса и состояние пациента, способ применения этих компонентов комбинаций. Примеры областей доз и пропорций компонентов приведены ниже.
В общем случае, соответствующая доза комбинации настоящего изобретения в пересчете на общую массу компонентов (a) и (b) будет изменяться в области от 3 до 120 мг на 1 кг массы тела пациента в день, в предпочтительном варианте в области от 6 до 90 мг на 1 кг массы тела в день, а в наиболее предпочтительном варианте в области от 15 до 60 мг на 1 кг массы тела в день. Желательная дозировка в предпочтительном варианте состоит из двух, трех, четырех, пяти, шести и более поддоз, применяемых через соответствующие промежутки времени в течение дня. Эти поддозы могут быть применены в форме единичной дозы, например, содержащей от 10 до 1500 мг, в предпочтительно варианте от 20 до 1000 мг, а в самом предпочтительном варианте от 50 до 700 мг активных ингредиентов на форму единичной дозы.
Несмотря на то, что активные ингредиенты могут применяться отдельно, в предпочтительном варианте они содержатся в виде фармацевтических форм. Фармацевтические формы, являющиеся предметом изобретения, содержат комбинацию в соответствии с изобретением вместе с одним или несколькими, приемлемыми с фармацевтической точки зрения, носителями или наполнителями, а также необязательно другие терапевтические агенты. Когда отдельные компоненты этой комбинации применяют раздельно, они в общем случае каждый отдельно содержится в виде фармацевтической формы. Ссылки, которые делаются ниже на формы, относятся, если не указано противное, к формам, содержащим либо эту комбинацию, либо ее компоненту. К этим формам относятся такие формы, которые предназначены для стоматического, прямокишечного, носового, местного (включая, через кожу, трансбуккальный и подъязычный методы), влагалищного или парентерального (включая подкожный, внутримышечный, внутривенный и внутрикожный) применения. Эти формы могут иметь форму единичной дозы и могут быть получены при помощи любого приема, известного в области фармацевтики. Такие приемы включают стадию соединения вместе активных ингредиентов с носителем, который состоит из одного или нескольких дополнительных ингредиентов.
В общем случае, эти формы получают при помощи равномерного и тщательного соединения вместе активных ингредиентов с жидкими носителями или тонко измельченными твердыми носителями, или теми и другими, а затем, если это необходимо, продукту придают ту или иную форму.
Формы, являющиеся предметом изобретения, предназначенные для стоматического применения, могут находится в виде дискретных единиц, таких как капсулы, крахмальные капсулы или таблетки, каждая из которых содержит заранее определенное количество активных ингредиентов; в виде порошка или гранул; в виде раствора или суспензии в водной или неводной жидкости; в виде жидкой эмульсии масло в воде, или жидкой эмульсии вода в масле. Активный ингредиент может также содержаться в форме шариков, лекарственной кашки или пасты.
Таблетка может быть получена при помощи прессовки или формования, необязательно с одним или несколькими дополнительными ингредиентами. Прессованные таблетки могут быть получены при помощи прессовки в соответствующем средстве активных ингредиентов в свободно-текущей форме, такой как порошок или гранулы, необязательно смешанных со связывающим агентом (например, повидоном, желатином, оксипропилметил целлюлозой), смазочным материалом, инертным разбавителем, консервирующим агентом, разрыхляющим агентом (например, натрий гликоллат крахмала, сшитый повидон, сшитая натрий карбоксиметил целлюлоза), поверхностно-активным или диспергирующим агентом, формованные таблетки могут быть изготовлены при помощи формования смеси порошкообразного соединения, увлажненной инертным жидким разбавителем, при помощи соответствующего средства. Таблетки могут быть покрыты или на них может быть нанесено рефление, им могут быть приданы формы, обеспечивающие медленное или контролируемое высвобождение активных ингредиентов, используя при этом, например, оксипропилметил целлюлозу в различных пропорциях, чтобы обеспечить целевой профиль высвобождения. Таблетки могут быть снабжены "кишечным" покрытием, чтобы обеспечить высвобождение в кишечнике, а не в желудке.
Формы, предназначенные для местного применения во рту, включают лепешки, содержащие активные ингредиенты во вкусной основе, в общем случае в сахарозе и акации или трагаканте; пастилки, содержащие активный ингредиент в инертной основе, такой как желатин и глицерин, или сахароза и акация, и жидкости для полоскания рта, содержащие активный ингредиент в соответствующем жидком носителе. Формы для прямокишечного применения могут иметь вид суппозитория на соответствующей основе, содержащей, например, кокосовое масло или салицилат.
Местное применение может быть также обеспечено посредством трансдермального ионтофорезного средства.
Формы, предназначенные для применения через влагалище, включают пессарии, тампоны, кремы, гели, пасты, пены или распыляющие средства, содержащие в дополнение к активному ингредиенту такие носители, применение которых в этой области известно.
Формы, предназначенные для парентерального применения, включают водные и неводные, изотонные стерильные растворы для инъекций, которые могут содержать анти-оксиданты, буферные растворы, бактериостаты и растворенные вещества, которые придают форме изотонность относительно крови пациента; водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты и загущающие агенты; липосомы или другие системы в форме микрочастиц, которые предназначены для доставки соединения к компонентам крови или к одному или нескольким органам. Эти формы могут иметь вид контейнера с одной или несколькими дозами, например ампулы и пузырьки, и они могут быть сохранены в условиях сушки вымораживанием /лиофилизации/, требующих только добавление стерильного жидкого носителя, например воды для инъекций, непосредственно перед использованием. "Неподготовленные" растворы и суспензии для инъекций могут быть получены из стерильных порошков, гранул и таблеток тех типов, что были описаны ранее.
Предпочтительными формами единичных доз являются те, что содержат ежедневную дозу или ежедневную поддозу активных ингредиентов, о чем речь шла выше, или соответствующие ее доли.
Необходимо иметь в виду, что в дополнение к тем ингредиентам, что были перечислены выше, формы, являющиеся предметом изобретения, могут включать другие агенты, известные в этой области техники, имеющие отношение к типу рассматриваемой формы, например те, что используют при стоматическом применении, могут включать такие дополнительные агенты, как вкусовые агенты, загущающие агенты и ароматизирующие агенты.
Соединения комбинации настоящего изобретения могут быть получены при помощи известной процедуры. Зидовудин может быть получен, например, как это описано в патенте США N 4724232. Зидовудин может быть также получен от фирмы Aldrich Chemical Co., Milwauree, kI 53233, USA.
1-[2-(Гидроксиметил)1,3-оксатиолан-5-ил]-5-фторцитозин может быть получен, например, в результате:
a) взаимодействия необязательно замещенного 5-фторцитозина с 1,3-оксатиоланом формулы /IIIA/: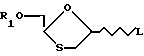
в которой R1 является водородом или защищающей окси группой, а L - замещаемая группа; или
b) взаимодействия соединения формулы /IIIB/: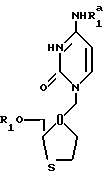
/в которой R1 уже был определен выше, а R
c) взаимодействия соединения формулы /IIIC/: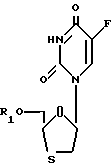
/в которой R1 уже был определен выше/ с агентом, позволяющим превратить оксо-группу в 4-позиции урацилового кольца в амино-группу; любые оставшиеся защищающие группы должны быть удалены, чтобы получить целевой продукт.
Что касается процедуры a), то окси-защищающая группа включает такие защищающие группы, как ацил (например, ацетил), арилацил (например, бензоил или замещенный бензоил), тритил или монометокситритил, бензил или замещенный бензил, триалкилсилил (например, диметил-третичн.-бутилсилил) или дифенилметилсилил. Соединение 5-фторцитозина может быть защищено силилом, например триметилсилиловыми группами. Такие группы могут быть удалены при помощи известных приемов. Замещаемая группа L является замещаемой группой, тип которой хорошо известен в области химии нуклеозидов, например галоген, такой как хлор или бром, алкокси такой, как метокси или этокси, или ацил такой, как ацетил или бензоил.
Реакция в процедуре a) может быть осуществлена в органическом растворителе (например, 1,2-дихлорэтане или ацетонитриле) в присутствии кислоты Льюиса, такой как хлорид четырехвалентного олова или триметилсилилтрифлат.
Соединения формулы /IIIA/ могут быть получены из соответствующим образом защищенного 2-гидроксиацетальдегида формулы (IV):
R1OCH2CHO,
в которой R1 уже был определен выше, как это описано в Can. Y. Research. , т. 8, с. 129 /1933/ и Европейском патентном описании N 0382526. Реакция соединений формулы IV с меркаптоацеталем HSCH2CH(OR)2, в котором R является C1-4 алкокси, таким как HSCH2CH(OC2H5)2, известна в этой области техники /Chem. Ber., т. 85, с. 924 - 932 /1952/ / и дает соединения формулы IIIA, в которой L является OR /алкокси/, например, метокси или этокси. В качестве альтернативы соединения формулы IIIA, в которой L является алкокси, могут быть превращены в соединения формулы IIIA, в которой L является галогеном или ацилом, при помощи приемов, известных в области химии углеводов.
Соединения формулы IV могут быть получены из 1,2-O-изопропилиден глицерина при помощи введения R1 (например, трехзамещенного силила, бензила или тритила) и удаления группы изопропилидена слабой кислотой (например, водным раствором муравьиной или уксусной кислоты) или бромидом цинка в ацетонитриле с последующим окислением группы спирта водным раствором периодата.
Что касается процедуры b), то 5-фтор-заместитель может быть введен при помощи известного в этой области техники приема /M.Y. Robins и др./ В кн. Nucleic Aсid Chemistry, Part 2, редакторы L.B. Townsend и R.S. Tipson, изд. Y. Kiley and sons, New-York, с. 895 - 900 /1978/ и ссылки, приведенные здесь; R. Dusohinsky,/ В кн. Nucleic Aсid Chemistry, Part I, редакторы L.B. Towsend и R. S. Tipson изд. Y. Wiley and sons, с. 43 - 46 /1978/ и ссылки, приведенные здесь/. Фторирующим агентом может быть, например, триметилгипофторит во фтортрихлорметане.
Что касается процедуры c), то соединение формулы /IIIC/ в предпочтительном варианте обрабатывают 1,2,4-триазолом, в предпочтительном варианте вместе с 4-хлорфенил дихлорфосфатом, чтобы получить соответствующее соединение 4-(1,2,4-триазолила), которое затем превращают в целевое соединение 4-амино (цитидина) в результате взаимодействия, например, с метанолом.
Исходные материалы формулы IIIB и IIIC могут быть получены, например, в результате взаимодействия соответствующего /необязательно защищенного/ основания соединения формулы IIIA при помощи той же процедуры, что описана в пункте a). 5-Фторурацил и 5-фторцитозин могут быть получены от фирмы Aldrich Chemical Co., Milwaure, WI 53233, USA.
Разделение /±/-цис-и /±/-транс-изомеров формулы (I), например, в защищенной форме может быть осуществлено при помощи хроматографии на силикагеле со смесью органических растворителей, таких как этил ацетат/метанол, этил ацетат/гексан или дихлорметан/метанол. Любая защищающая группа может быть затем удалена с использованием соответствующего реагента для каждой группы.
Сложные эфиры компонент-соединений формул I и II могут быть получены известным приемом в результате взаимодействия с соответствующим этерифицирующим агентом, таким как галид или ангидрид кислоты. Соединения формул I и II или их сложные эфиры могут быть превращены в их приемлемые с фармацевтической точки зрения соли в результате обработки соответствующим основанием. Сложный эфир или соль компоненты-соединения могут быть превращены в базовое соединение при помощи гидролиза.
Приемлемые с фармацевтической точки зрения амиды соединения формулы (I) могут быть получены, например, в результате взаимодействия с соответствующим ацилирующим агентом, например галидом или ангидридом кислоты, предназначенным для ацилирования 5'-OH и 4-NH2 групп. Ациловая группа может быть затем удалена селективно из одной или другой 5'-OH и 4-NH2 групп. Например, в результате обработки диацилированного соединения при кислотных условиях, например кислоте Льюиса, такой как бромид цинка в метаноле, удаляют 4N-ациловую группу, чтобы получить соответствующий 5'-OH сложный эфир в то время, как в результате обработки диацилированного соединения при щелочных условиях, например, метилатом натрия удаляют 5'-OH ациловую группу, чтобы получить соответствующий 4N-амид. Ациловые группы могут быть также удалены селективно в результате обработки производимыми промышленностью ферментами эстеразы и липазы, например эстеразой печени свиньи или липазы поджелудочной железы, или при помощи обработки в соответствии с процедурами, описанными в патентном описании США N 5071983. Соединение формулы (I) может быть превращено в его приемлемую с фармацевтической точки зрения соль в соответствии с известными приемами, например, в результате обработки соответствующим основанием.
Приводимые ниже примеры предназначены только для иллюстрации и их не следует рассматривать в качестве ограничений изобретения. Термин "активный ингредиент" обозначает смесь компонент зидовудина и цис-1-[2-(гидроксиметил)-1,3-оксатиолан-5-ил]-5-фторцитозина в молярном отношении 1 : 25.
Пример 1. Форма в виде таблетки.
Следующие формы A, B и С получали при помощи влажной грануляции ингредиентов с раствором повидона с последующим добавлением стеарата магния и прессовки.
Форма A (мг/таблетку)
Активный ингредиент - 250
Лактоза /Фармакопея Великобритании/ - 210
Повидон /Фармакопея Великобритании/ - 15
Натрий гликоллат крахмала - 20
Стеарат магния - 5
Всего - 500
Форма B (мг/таблетку)
Активный ингредиент - 250
Лактоза /Фармакопея Великобритании/ - 150
Авицел PH 101 - 60
Повидон /Фармакопея Великобритании/ - 15
Натрий гликоллат крахмала - 20
Стеарат магния - 5
Всего - 500
Форма C (мг/таблетку)
Активный ингредиент - 250
Лактоза /Фармакопея Великобритании/ - 200
Крахмал - 50
Повидон - 5
Стеарат магния - 4
Всего - 359
Следующие формы D и E получали при помощи непосредственной прессовки смешанных ингредиентов. Лактоза в форме E имеет тип для непосредственной прессовки /фирма Dairy Crest - "Zeparox"/.
Форма D (мг/таблетку)
Активный ингредиент - 250
Предварительно желатинизированный крахмал NF15 - 150
Всего - 400
Форма E (мг/таблетку)
Активный ингредиент - 250
Лактоза /Фармакопея Великобритании/ - 150
Авицел - 100
Всего - 500
Форма F (форма для регулируемого высвобождения).
Форму получали при помощи влажной грануляции ингредиентов с раствором повидона с последующим добавлением стеарата магния и прессовки (мг/таблетку)
Активный ингредиент - 500
Оксипропилметилцеллюлоза /типа Methocel K4M Premium/ - 112
Лактоза /Фармакопея Великобритании/ - 53
Повидон /Фармакопея Великобритании/ - 28
Стеарат магния - 7
Всего - 700
Высвобождение лекарственного препарата имеет место в течение периода в примерно 6 - 8 ч и завершается спустя 12 ч.
Пример 2. Капсулы.
Форма A
Капсулу получали при помощи смешения ингредиентов формы D в примере 1 и заполнения смесью желатиновой капсулы, состоящей из двух твердых частей. Форму B (см. ниже) получали аналогичным образом.
Форма B (мг/капсулу)
Активный ингредиент - 250
Лактоза /Фармакопея Великобритании/ - 143
Натрий гликоллат крахмала - 25
Стеарат магния - 2
Всего - 420
Форма C (мг/капсулу)
Активный ингредиент - 250
Макрогель 4000 /Фармакопея Великобритании/ - 350
Всего - 600
Капсулы формы C получали при помощи плавления Макрогеля 4000 /Фармакопея Великобритании/, диспергирования в расплаве активного ингредиента и заполнения расплавом жесткой желатиновой капсулы, состоящей из двух частей.
Форма D (мг/капсулу)
Активный ингредиент - 250
Лецитин - 100
Арахисовое масло - 100
Всего - 450
Капсулы формы D получали при помощи диспергирования активного ингредиента в лецитине и арахисовом масле и заполнения дисперсией мягких, эластичных желатиновых капсул.
Форма E /Капсула с регулируемым высвобождением/.
Следующую форму капсулы с регулируемым высвобождением получали при помощи экструзии ингредиентов a, b и c, используя экструдер, затем осуществляли грануляцию материала после экструзии и сушку. Высушенные гранулы затем покрывали контролирующей высвобождение мембраной /d/ и ими заполняли жесткие желатиновые капсулы, состоящие из двух частей (мг/капсулу).
/a/ Активный ингредиент - 250
/b/ Микрокристаллическая целлюлоза - 125
/c/ Лактоза /Фармакопея Великобритании/ - 125
/d/ Этил целлюлоза - 13
Всего - 513
Пример 3. Форма для инъекций.
Форма A (мг).
Активный ингредиент - 200
0,1 М раствор хлористоводородной кислоты или 0,1 М раствор гидрата окиси натрия, сколько нужно до pH - 4,0-7,0
Стерильная вода - До 10 мл
Активный ингредиент растворяли в большей части воды /35 - 40oC/ и pH обеспечивали на уровне между 4,0 и 7,0 при помощи хлористоводородной кислоты или гидрата окиси натрия по необходимости. Затем порцию доводили до объема при помощи воды, а затем фильтровали через стерильный микропористый фильтр в стерильную емкостью 10 мл желтую стеклянную ампулу /типа I/ и закрывали в стерильных условиях.
Форма B.
Активный ингредиент - 125 мг
Стерильный, не содержащий пирогенов раствор фосфата, pH 7, в качестве буфера - До 25 мл
Пример 4. Внутримышечная инъекция.
Активный ингредиент - 200 мг
Бензиловый спирт - 0,10 г
Гликофурол 75 - 1,45 г
Вода для инъекции - До 3,00 мл
Активный ингредиент растворяли в гликофуроле. Затем добавляли бензиловый спирт, получали раствор и добавляли воду до 3 мл. Затем смесь фильтровали через стерильный микропористый фильтр и плотно закрывали в стерильные емкостью 3 мл желтые стеклянные ампулы (типа I).
Пример 5. Сироп
Активный ингредиент - 250 мг
Раствор сорбита - 1,50 г
Глицерин - 2,00 г
Бензоат натрия - 0,005 г
Вкусовой агент, peach 17.42.3169 - 0,0125 мл
Очищенная вода - До 5,00 мл
Активный ингредиент растворяли в смеси глицерина и большей части очищенной воды. Затем в раствор добавляли водный раствор бензоата натрия, добавляли раствор сорбита и вкусовой агент. Объем доводили до необходимого с использованием очищенной воды и тщательно перемешивали.
Пример 6. Суппозиторий (мг/капсулу суппозитория)
Активный ингредиент - 250
Твердый жир, Фармакопея Великобритании (Witepson H15 - фирма Dynamit Nobel) - 1770
Всего - 2020
Одну пятую жира Witepson H15 плавили в чашке, снабженной паровой рубашкой, при температуре максимум 45oC. Активный ингредиент просеивали через сито 200 μm и добавляли в расплавленную основу при перемешивании, используя средство Silverson, снабженное отсекающей головкой, до тех пор, пока не будет получена однородная дисперсия. Поддерживая смесь при температуре 45oC, в суспензию добавляли оставшийся Witepson H15 и перемешивали, чтобы обеспечить однородную смесь. Полную суспензию пропускали через сито из нержавеющей стали с размером отверстий 250 μm и при непрерывном перемешивании давали возможность остыть до 40oC. При температуре от 38 до 40oC 2,02 г смеси заполняли соответствующие 2 мл пластические формы. Суппозиториям давали возможность охладиться до комнатной температуры.
Пример 7. Пессарии (мг/пессарий)
Активный ингредиент - 250
Безводная декстроза - 380
Картофельный крахмал - 363
Стеарат магния - 7
Всего - 1000
Указанные выше ингредиенты непосредственно смешивали, а пессарии получали при помощи прямой прессовки полученной в результате смеси.
Пример 8. Получение 1-[2-(гидроксиметил)-1,3-оксатиолан-5-ил]-5-фторцитозина.
Метод А. Получали /±/-цис и /±/-транс 2-бензоилоксиметил-5-/ N4-ацетилцитозин-1-ил/-1,3-оксатиолан и разделяли на /±/-цис и /±/-транс изомеры, как это описано в Европейском патентном /EP/ описании N 0382526. /±/-Цис изомер подвергали фторированию с использованием трифторметил гипофторита во фтортрихлорметане /CCl3F/ и хлороформе при температуре -78oC в соответствии с процедурой Робинса и др. /Robins и др. Nuсleic Acid Chemistry, Part 2, c. 895 - 900 /1978/. N4-Ацетил и 2-бензоил группы удаляли диметиламином в этаноле, а продукт, /±/-цис-1-2-оксиметил(-1,3-оксатиолан-5-ил)-5-фторцитозин, выделяли.
Метод B. (±)-цис и (±)-транс-2-бензоилоксиметил-5-(урацил-1-ил)-1,3-оксатиолан получали, как это описано в EP N 0382526. После депротекции 2-гидроксильной группы при помощи насыщенного метанолового раствора аммиака изомеры разделяли на силикагеле, используя EtOAc/MeOH в качестве элюента /EP N 0382526/. (±)-Цис-изомер взаимодействовал с уксусным ангидридом в пиридине при комнатной температуре, чтобы получить 2-ацетат. Растворитель удаляли под вакуумом при температуре < 30oC. Затем 2-ацетат растворяли в CHCl3 и промывали водным бикарбонатом. Отделившийся органический слой сушили, а CHCl3 выпаривали под вакуумом. (±)-цис-2-ацетилоксиметил-5-(урацил-1-ил)-1,3-оксатиолан подвергали фторированию, как это описано выше /метод A/, с использованием процедуры Робинса и др. Превращение 5-F-урацилового основания в 5-F-цитозиновое основание осуществляли при помощи получения производного 4-(1,2,4-триазол-1-ила) в соответствии с процедурами, описанными в C.B.Reece, y. Chem.Soc., Perkins I, с.1171/1984/ и W. L. Sung, Nucleic Acids Res, т.9, с.6139 /1981/, используя 1,2,4-триазол и 2 эквивалента 4-хлорфенилдихлорфосфата в сухом пиридине при окружающей температуре. После этого превращения осуществляли взаимодействие с метанолом, предварительно насыщенным аммиаком, при 0oC, а 2-ацетат подвергали гидролизу, чтобы получить /±/-цис-1-/2-оксиметил/-1,3-оксатиолан-5-ил/-5-фторцитозин.
Противовирусная активность.
Комбинации, являющиеся предметом настоящего изобретения, испытывали на анти-ВИЧ-активность на ВИЧ-инфицированных клетках МТ4, как это описано в статье Averett, D.R., y. Virol. Methods, т.23, с.263 - 276 /1989/. Эти клетки подвергали воздействию ВИЧ в течение одного часа перед добавлением противовирусной компоненты. Эти компоненты испытывали в последовательности 2,5-кратных разбавлений. Спустя пять дней при инкубировании при температуре 37oC определяли количество клеток. Вычисляли ингибирование индуцированного ВИЧ цитопатического действия, а синергетический эффект определяли с использованием F I C-точек, как это описано у Elion, Singer и Hitchings, J. Biol. Chem., т.208, с.477 /1954/.
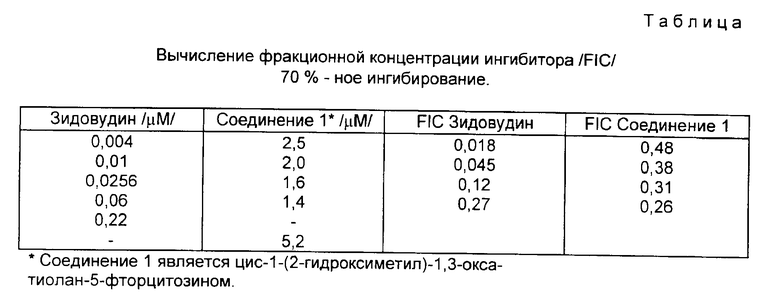
Фракционные концентрации ингибитора /FIC/зидовудина и цис-1-[2-(оксиметил)-1,3-оксатиолан-5-ил] -5-фторцитозина вычисляли по методу Elion и др. (см. таблицу).
Эти значения могут быть представлены в виде графика, из которого можно установить, что комбинация цис-1-[2-(гидроксиметил)-1,3-оксатиолан-5-ил]-5-фторцитозина и зидовудина обладает сильным синергетическим эффектом.
Изобретение относится к синергетическим фармацевтическим комбинациям 1-[2-(гидроксиметил)-1,3-оксатиолан-5-ил]-5-фторцитозина или его производных и 3'-азидо-3'-деокси-тимидина или его производных, а также к их использованию в медицинской терапии, в частности при лечении или профилактике ВИЧ-инфекции. Преимущество комбинации в том, что ее противовирусные компоненты могут быть использованы в более низких дозах. 3 с. и 4 з.п.ф-лы, 1 табл.
| Способ получения нуклеозида или его фармацевтически приемлемых солей | 1984 |
|
SU1442076A3 |
| 5 @ -Фосфонаты 3 @ -азидо-2 @ ,3 @ -дидезоксинуклеозидов, являющиеся специфическими ингибиторами вируса СПИД в культуре лимфоцитов человека Н9/ШВ | 1987 |
|
SU1548182A1 |
| ОПТИЧЕСКАЯ СИСТЕМА ДЛЯ ФОТОГРАФИРОВАНИЯ СЛЕДОВ ЧАСТИЦ В ЦИЛИНДРИЧЕСКИХ ПУЗЫРЬКОВЫХ КАМЕРАХ | 0 |
|
SU196185A1 |
| КЛАПАН ЦЕНТРАЛИЗОВАННОЙ СИСТЕМЫ ПОДКАЧКИ ШИН ТРАНСПОРТНОГО СРЕДСТВА | 0 |
|
SU382526A1 |
Авторы
Даты
1998-05-20—Публикация
1992-03-05—Подача