Изобретение относится к производству углерода, предпочтительно, нитевидного и водорода из углеводородов. Нитевидный углерод образуется в виде клубка нитей, имеющих диаметр в несколько сот ангстрем и длиной до нескольких микрон. Благодаря наличию высокодисперсных частиц никеля и железа нитевидный углерод имеет ферромагнитные свойства и может быть использован для получения ферромагнитных чернил, графитовых пигментов для копирования, синтетических и природных каучуков и пластиков. Наряду с этим, углеродный материал может быть использован как при выплавке сталей, так и в качестве восстановителя в порошковой металлургии.
Известно несколько катализаторов и способов получения углерода и водорода:
1. Разложением метана в присутствии массивного металлического катализатора (Fe, Co, Ni) при 650 - 720oC [1].
2. Разложением углеводородных газов на поверхности железосодержащего катализатора при 850 - 900oC под давлением 1 - 35 атм [2].
3. Разложением метана или других углеводородов на поверхности брикетированной сажи с никелем или сажи с железом при температурах ниже точки разложения этих соединений [3].
4. Разложением метана на поверхности Ni/Al2O3 или Ni/MgO катализаторов при 500 - 550oC [4].
5. Разложением метана на поверхности Ni-Cu/Al2O3 или Ni-Cu/MgO катализаторов при температурах 560 - 650oC [5].
По достигаемому положительному эффекту наиболее совершенным является катализатор и способ получения углерода и водорода, который и выбран за прототип [5].
По прототипу катализатор имеет состав, мас.%: 70 - 90 оксида никеля с 2 - 16 оксида меди и 8 - 14 гидроксида алюминия или магния. Способ приготовления катализатора включает механохимическую активацию двойной смеси оксидов никеля и меди, а затем тройной смеси никеля и меди с гидроксидом алюминия или магния в планетарной центробежной мельнице с последующим восстановлением смеси водородом при нагревании до температуры реакции разложения метана. Способ получения углерода и водорода состоит в пропускании метана над вышеуказанными катализаторами при 560 - 650oC и атмосферном давлении.
Основными недостатками рассматриваемого катализатора и способа получения углерода и водорода являются:
1. Относительно невысокие общие выходы углерода и водорода на грамм восстановленного катализатора.
2. Стабильность работы катализатора и, соответственно, выходы углерода и водорода резко снижаются при увеличении рабочей температуры выше 650oC, а при 560 - 650oC метан разлагается на углерод и водород не полностью, разложение ограничено константой равновесия. Степень превращения 20 - 60%, т.е. значительная часть метана не используется. На выходе из реактора получается метано-водородная смесь, что затрудняет ее дальнейшее использование.
3. Невозможно перерабатывать метано-водородные смеси с содержанием в них водорода больше 60 - 70%.
Изобретение решает задачу повышения выхода углерода и водорода и увеличения степени использования метана.
Задача решается использованием катализатора состава, мас.%: 69 - 74 оксида никеля, 9,5 - 12 оксида меди, 9,5 - 12 гидроксида алюминия и 2 - 12 оксида железа и следующим способом получения углерода и водорода из метана:
1) восстановление катализатора водородом во время нагрева до температуры реакции 651 - 800oC;
2) замена водорода на метан и проведение реакции разложения до полного прекращения;
3) охлаждение реактора в токе метана или инертного газа до комнатной температуры.
Отличительными признаками предлагаемого катализатора является его состав, включающий, мас.%: 69 - 74 оксида никеля, 9,5 - 12 оксида меди, 9,5 - 12 гидроксида алюминия и 2 - 12 оксида железа. Выбор состава катализатора продиктован соображениями достижения максимального выхода углерода и водорода из метана при повышении степени использования метана. Оказалось, что этого можно достигнуть, если к составу катализатора из прототипа добавить оксид железа.
Отличительными признаками предлагаемого способа получения углерода и водорода из метана являются: состав катализатора и температура проведения процесса. Выбор температурного интервала проведения реакции определяется тем, что при температурах ниже 651oC резко снижается скорость реакции, уменьшается степень разложения метана из-за термодинамических ограничений, падает выход продукта, а использование температур выше 800oC не увеличивает выход углерода и водорода и оказывается невыгодным с энергетической точки зрения.
Неизвестна заявляемая совокупность признаков, приводящая к увеличению выхода углерода и водорода при одновременном повышении степени использования метана, поэтому предлагаемый катализатор и способ получения углерода и водорода можно классифицировать как соответствующий критерию "изобретательский уровень".
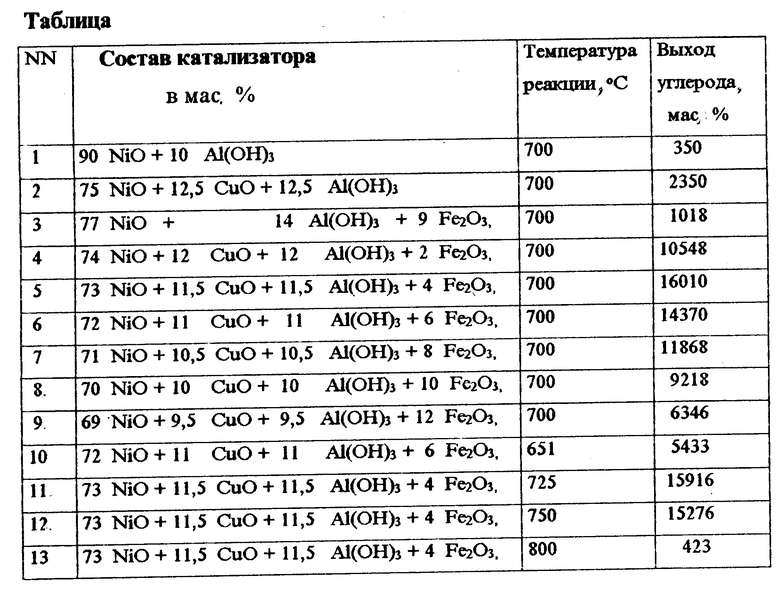
Сущность изобретения иллюстрируется следующими примерами и подтверждается данными, приведенными в таблице.
Примеры 1 - 3 приведены для сравнения.
Пример 1. Катализатор, состоящий из 90 мас.% NiO и 10 мас.% Al(OH)3 и полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0046 г загружают в проточный реактор с весами Мак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 700oC. Затем водород заменяют на метан и проводят реакцию разложения при 700oC в течение 1,5 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 350 мас.% по отношению к весу восстановленного катализатора.
Пример 2. Катализатор, состоящий из 75 мас.% NiO, 12,5 мас.% CuO и 12,5 мас. % Al(OH)3 и полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0039 г загружают в проточный реактор с весами Мак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 700oC. Затем водород заменяют на метан и проводят реакцию разложения при 700oC в течение 1,5 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 2350 мас.% по отношению к весу восстановленного катализатора.
Пример 3. Катализатор, состоящий из 77 мас.% NiO, 14 мас.% Al(OH)3 и 9 мас. % Fe2O3, полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0031 г загружают в проточный реактор с весами Мак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 700oC. Затем водород заменяют на метан и проводят реакцию разложения при 700oC в течение 3 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 1018 мас.% по отношению к весу восстановленного катализатора.
Примеры 4 - 13 иллюстрируют сущность изобретения.
Пример 4. Катализатор, состоящий из 74 мас.% NiO, 12 мас.% CuO, 12 мас.% Al(OH)3 и 2 мас. % Fe2O3, полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0029 г загружают в проточный реактор с весами Мак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 700oC. Затем водород заменяют на метан и проводят реакцию разложения при 700oC в течение 5 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 10548 мас.% по отношению к весу восстановленного катализатора.
Пример 5. Аналогичен примеру 4, отличается только составом катализатора 73 мас. % NiO, 11,5 мас.% CuO, 11,5 мас.% Al(OH)3 и 4 мас.% Fe2O3. Привес катализатора за счет углерода составил 16010 мас.% по отношению к весу восстановленного катализатора.
Пример 6. Аналогичен примеру 4, отличается только составом катализатора 72 мас. % NiO, 11 мас.% CuO, 11 мас.% Al(OH)3 и 6 мас.% Fe2O3. Привес катализатора за счет углерода составил 14370 мас.% по отношению к весу восстановленного катализатора.
Пример 7. Аналогичен примеру 4, отличается только составом катализатора 71 мас. % NiO, 10,5 мас.% CuO, 10,5 мас.% Al(OH)3 и 8 мас.% Fe2O3. Привес катализатора за счет углерода составил 11868 мас.% по отношению к весу восстановленного катализатора.
Пример 8. Аналогичен примеру 4, отличается только составом катализатора 70 мас.% NiO, 10 мас.% CuO, 10 мас.% Al(OH)3 и 10 мас.% Fe2O3. Привес катализатора за счет углерода составил 9218 мас.% по отношению к весу восстановленного катализатора.
Пример 9. Аналогичен примеру 4, отличается только составом катализатора 69 мас. % NiO, 9,5 мас.% CuO, 9,5 мас.% Al(OH)3 и 12 мас.% Fe2O3. Привес катализатора за счет углерода составил 6346 мас.% по отношению к весу восстановленного катализатора.
Пример 10. Катализатор, состоящий из 72 мас.% NiO, 11 мас.% CuO, 11 мас. % Al(OH)3 и 6 мас.% Fe2O3, полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0033 г загружают в проточный реактор с весами Бак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 651oC. Затем водород заменяют на метан и проводят реакцию разложения при 651oC в течение 4 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 5433 мас. % по отношению к весу восстановленного катализатора.
Пример 11. Катализатор, состоящий из 73 мас.% NiO, 11,5 мас.% CuO, 11,5 мас.% Al(OH)3 и 4 мас.% Fe2O3, полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0023 г загружают в проточный реактор с весами Мак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 725oC. Затем водород заменяют на метан и проводят реакцию разложения при 725oC в течение 3 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 15916 мас.% по отношению к весу восстановленного катализатора.
Пример 12. Катализатор, состоящий из 73 мас. NiO, 11,5 мас.% CuO, 11,5 мас.% Al(OH)3 и 4 мас.% Fe2O3, полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0023 г загружают в проточный реактор с весами Мак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 750oC. Затем водород заменяют на метан и проводят реакцию разложения при 750oC в течение 3 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 15276 мас.% по отношению к весу восстановленного катализатора.
Пример 13. Катализатор, состоящий из 73 мас.% NiO, 11,5 мас.% CuO, 11,5 мас.% Al(OH)3 и 4 мас.% Fe2O3, полученный 30 мин механохимической активацией в планетарной центробежной мельнице, в количестве 0,0034 г загружают в проточный реактор с весами Мак-Бена, нагревают в течение 30 - 35 мин в потоке водорода 20 л/ч до температуры 800oC. Затем водород заменяют на метан и проводят реакцию разложения при 800oC в течение 3 ч и расходе метана 3 л/ч. Привес катализатора за счет углерода составил 423 мас.% по отношению к весу восстановленного катализатора.
Как видно из описания примеров и таблицы предлагаемое изобретение позволяет получать нитевидный углерод и водород из метана и может найти промышленное применение в утилизации газовых углеводородных выбросов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕРОДНОГО МАТЕРИАЛА И ВОДОРОДА | 1994 |
|
RU2086502C1 |
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕРОДНОГО МАТЕРИАЛА И ВОДОРОДА | 1993 |
|
RU2071932C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И ПРОЦЕСС ПОЛУЧЕНИЯ ФЕРРОМАГНИТНОГО ГРАФИТИРОВАННОГО УГЛЕРОДА И ВОДОРОДА | 1992 |
|
RU2042425C1 |
| СПОСОБ ОБЕЗВРЕЖИВАНИЯ ХЛОРСОДЕРЖАЩИХ УГЛЕВОДОРОДОВ | 1995 |
|
RU2093228C1 |
| МЕТАЛЛУГЛЕРОДНЫЙ КАТАЛИЗАТОР | 1994 |
|
RU2096083C1 |
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕРОДНЫХ НАНОТРУБОК | 1998 |
|
RU2146648C1 |
| КАТАЛИЗАТОР ДЛЯ СЕЛЕКТИВНОГО ГИДРИРОВАНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2087187C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА И ВОЛОКНИСТОГО УГЛЕРОДА | 2004 |
|
RU2284962C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРОВ | 1997 |
|
RU2126718C1 |
| СПОСОБ ПРЯМОГО ВЫДЕЛЕНИЯ ЭЛЕМЕНТНОЙ СЕРЫ ИЗ СЕРОВОДОРОДСОДЕРЖАЩИХ ГАЗОВ И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1998 |
|
RU2142906C1 |
Изобретение относится к производству углерода, предпочтительно нитевидного, и водорода из углеводородов. Сущность изобретения: катализатор содержит, мас.%: оксид никеля - 69 - 74; оксид меди - 9,5 - 12; гидроксид алюминия - 9,5 - 12 и оксид железа - 2 - 12. Указанный катализатор позволяет при 651 - 800oC перерабатывать метан или метановодородные смеси с 70 - 80% степенью использования. 2 с. и 1 з.п. ф-лы, 1 табл.
NiO - 69,0 - 74,0
CuO - 9,5 - 12,0
Al(OH)3 - 9,5 - 12,0
Fe2O3 - 2,0 - 12,0
2. Способ получения углерода и водорода, включающий разложение метана на никельсодержащем катализаторе при повышенной температуре, отличающийся тем, что в качестве катализатора используют смесь оксидов никеля, меди, железа и гидроксида алюминия, восстановленную водородом при нагревании до 651 - 800oC, при следующем соотношении компонентов, мас.%:
NiO - 69,0 - 74,0
CuO - 9,5 - 12,0
Al(OH)3 - 9,5 - 12,0
Fe2O3 - 2,0 - 12,0
3. Способ по п.2, отличающийся тем, что разложение метана ведут при 651 - 800oC.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Robertson S.D., Carbon formation from pyrolysis over some transition metal surfaces | |||
| Nature and properties of the carbon formed | |||
| Кинематографический аппарат | 1923 |
|
SU1970A1 |
| Станок для нарезания зубьев на гребнях | 1921 |
|
SU365A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| SU, авторское свидетельство, 380714, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| SU, патент, 43587, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| RU, патент, 1828066, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| RU, патент, 2042425, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1998-08-10—Публикация
1997-03-12—Подача