Изобретение относится к новым производным 1,4-диазепина и их фармакологически приемлемым солям, способу их получения и фармацевтического применения. Соединения и их соли обладают прекрасной лечебной активностью.
В последнее время фактор активации тромбоцитов (далее сокращенно ФАТ) привлек особое внимание, и в настоящее время прояснена его связь с различными заболеваниями. Считается, что ФАТ принимает участие не только в воспалительных процессах, но также и при коуглопатии потребления, эндотоксическом шоке, астме, язвах и отторжениях во время трансплантации органов. Кроме того, внимание к нему было привлечено и в качестве медиатора, проявляющемся в одной из аллергических реакций.
В этих обстоятельствах проведены исследования, направленные на соединения с анти-ФАТ активностью. Например, в выложенной заявке на патент Япония N 63-33382 в качестве соединений с анти-ФАТ действием предложены производные 1,4-диазепина. Однако удовлетворительного средства с анти-ФАТ активностью, пригодного, в частности, для лечения аллергических заболеваний, таких как астма, до сего времени не было предложено.
Соответственно, нами продолжены долгосрочные исследования производных 1,4-диазепина, обладающих не только прекрасной анти-ФАТ активностью, но также и увеличенным сроком проявления активности.
Нами были проведены долгосрочные интенсивные исследования с целью достижения вышеуказанной цели, в результате чего мы обнаружили, что этой цели отвечают производные 1,4-диазепина, определение которым дается ниже, или их фармакологически приемлемые соли. Настоящее изобретение совершено на основе указанных результатов.
Изобретение представляет производные триазола (1,4) диазепина общей формулы I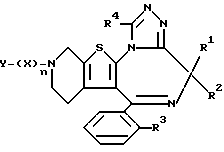
или их фармацевтически приемлемые соли, в которой R1 и R2 являются одинаковыми или различными и представляют атом водорода или низший алкил,
R3 представляет атом галогена,
R4 представляет низший алкил,
n означает 1, когда X представляет собой группу формулы: 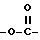 , группу формулы:
, группу формулы: 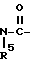 , где R5 означает атом водорода или низший алкил, или группу формулы:
, где R5 означает атом водорода или низший алкил, или группу формулы: 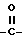 , и Y означает (C3-C6)циклоалкильную группу, возможно замещенную метильной группой или возможно замещенную в первом положении этинильной группой; или (C3-C6)циклоалкил(C1-C2)алкильную группу; или (C3-C6)алкинильную группу, возможно замещенную фенильной группой; или группу формулы:
, и Y означает (C3-C6)циклоалкильную группу, возможно замещенную метильной группой или возможно замещенную в первом положении этинильной группой; или (C3-C6)циклоалкил(C1-C2)алкильную группу; или (C3-C6)алкинильную группу, возможно замещенную фенильной группой; или группу формулы: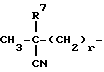
где R7 - водород или метил, r равно 0 или 1; группу формулы: NC(CH2)p, где p целое число от 1 до 5; или группу формулы: 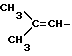 ; или группу формулы: A(CH2)q, где A представляет группу, выбранную из пиридильной группы, тетрагидропиранильной группы, морфолиногруппы и имидазолильной группы, и q целое число от 0 до 2; или группу формулы:
; или группу формулы: A(CH2)q, где A представляет группу, выбранную из пиридильной группы, тетрагидропиранильной группы, морфолиногруппы и имидазолильной группы, и q целое число от 0 до 2; или группу формулы: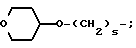
где S целое число от 1 до 2;
или фенилэтинильную группу; или группу формулы: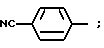
или группу формулы: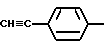
или группу формулы: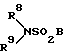
где R8 и R9 одинаковые или разные и представляют водород или низший алкил, или пиридилметил, или циклогексил, или R8 и R9 вместе с атомом азота образуют пиперидиновое, имидазолиновое или морфолиновое кольцо, и B представляет фениленовую или (C1-C3)алкиленовую группу; или группу формулы: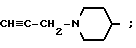
или группу формулы: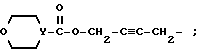
или группу формулы: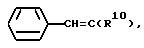
где R10 водород или метил;
или группу формулы: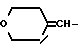
или фенил(C1-C2)алкильную группу, возможно замещенную в фенильном кольце галогеном;
или группу формулы: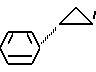 ;
;
или группу формулы: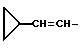 ;
;
или группу формулы: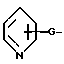 ,
,
в которой G - CH=CH- , или -SCH2-;
или, когда X представляет собой группу формулы: 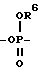 ,
,
где R6 означает низший алкил, Y представляет (C2-C7)алкильную группу,
или n означает 0, когда Y означает (C3-C6)алкинильную группу.
Предпочтительными соединениями формулы I и их фармацевтически приемлемыми солями являются соединения, в которых R3 означает хлор, R1 - водород и R4 метил, и
когда R2 означает водород, то Y - X означает группу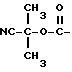 ;
;
или группу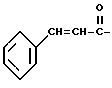 ;
;
или группу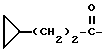 ;
;
или группу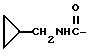 ;
;
или группу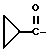 ;
;
или группу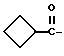 ;
;
или группу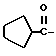 ;
;
или когда R2 означает метил, то Y - X означает группу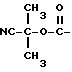
или группу 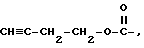
или группу 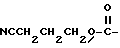 , или
, или
группу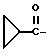 .
.
Кроме того, изобретение представляет производные триазоло[1,4]диазепина общей формулы II: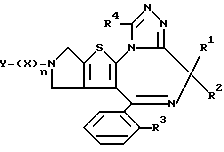 ,
,
или его фармацевтически приемлемые соли, где R1 и R2 являются атомами водорода, R3 представляет атом галогена, R4 представляет низший алкил, X представляет группу формулы: 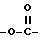 , или группу формулы
, или группу формулы 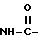 ,
,
Y представляет (C3-C6)циклоалкил(C1-C2) алкильную группу, или (C3-C6)алкинильную группу, или группу формулы: 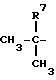 ,
,
где R7 - метил,
или группу формулы NC(CH2)p, где P целое число от 1 до 3, или группу формулы A(CH2)q, где A представляет группу, выбранную из пиридильной, тетрагидропиранальной, морфолильной и морфолинокарбонильной групп, q целое число от 0 до 2, или (C2-C7)алкильную группу, или фенил(C1-C2)алкильную группу, возможно замещенную в фенильном кольце на атом галогена, нитро- или трифторметильную группу.
Изобретением представлены также производные триазоло[1,4]диазепина общей формулы III: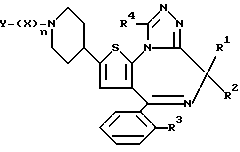
или их фармацевтически приемлемые соли, где R1 и R2 являются атомами водорода, R3 представляет атом галогена, R4 представляет низший алкил,
когда n равно 1, X представляет группу 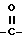 или
или 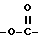 , Y представляет (C3-C6)циклоалкильную группу или (C3-C6)алкильную группу, или группу формулы: NC(CH2)p, где P целое число от 1 до 3, или группу формулы: A(CH2)q, где A представляет группу, выбранную из пиридильной, имидазолильной, тиенильной, тетрагидропиранильной и морфолильной групп, q - целое число от 0 до 3, или фенилэтинильную группу, или (C2-C7)алкильную группу, или фенил(C1-C2)алкильную группу, возможно замещенную в фенильном кольце на атом галогена, или (C1-C2)алкокси(C1-C2)алкильную группу, или X представляет группу
, Y представляет (C3-C6)циклоалкильную группу или (C3-C6)алкильную группу, или группу формулы: NC(CH2)p, где P целое число от 1 до 3, или группу формулы: A(CH2)q, где A представляет группу, выбранную из пиридильной, имидазолильной, тиенильной, тетрагидропиранильной и морфолильной групп, q - целое число от 0 до 3, или фенилэтинильную группу, или (C2-C7)алкильную группу, или фенил(C1-C2)алкильную группу, возможно замещенную в фенильном кольце на атом галогена, или (C1-C2)алкокси(C1-C2)алкильную группу, или X представляет группу 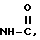 и Y - группу
и Y - группу 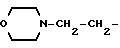 , или когда n равно 0, Y представляет (C3-C6)алкинильную группу, (C1-C2)алкокси(C1-C2)алкильную группу, диметиламиносульфонильную или тиофенсульфонильную группу.
, или когда n равно 0, Y представляет (C3-C6)алкинильную группу, (C1-C2)алкокси(C1-C2)алкильную группу, диметиламиносульфонильную или тиофенсульфонильную группу.
Изобретением раскрывается способ применения вышеохарактеризованных соединений и их солей. Согласно изобретению фармацевтическая композиция содержит фармакологически эффективное количество соединения или его соли по вышеприведенному определению, а также фармакологически приемлемый носитель. Способ лечения заболевания, против которого эффективно проявление анти-ФАТ активности, заключается во введении фармакологически эффективного количества соединения изобретения или его соли. Этим заболеванием является аллергическое заболевание, такое как астма.
Производные 1,4-диазепина общей формулы (I) обладает хорошей ингибирующей ФАТ эффективностью и устойчивостью при высокой безопасности.
Соответственно, цель изобретения заключается в создании производных 1,4-диазепина или их фармакологически приемлемых солей, обладающих хорошим анти-ФАТ действием. Другая цель изобретения заключается в создании способа получения таких производных. И еще одна цель изобретения заключается в получении содержащего такие производные средства.
В настоящем изобретении предпочтительными являются соединения следующего химического строения: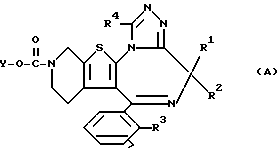
где R1, R2, R3, R4 и Y соответственно принимают вышеуказанные значения;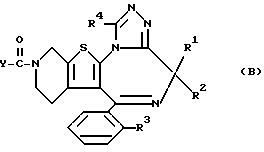
где R1, R2, R3, R4 и Y соответственно принимают вышеуказанные значения;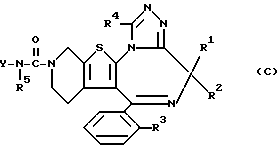
где R1, R2, R3, R4, R5 и Y принимают соответственно вышеуказанные значения.
Что касается значений R1 и R2 в соединении группы (I) изобретения, то наиболее предпочтительно, если R1 - атом водорода и R2 - низший алкил, в частности метил. Вышеуказанное отражено нижеследующей общей формулой: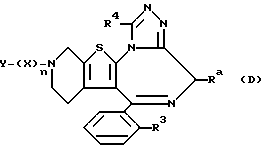
где Rа представляет низший алкил.
Наиболее предпочтительной группой соединений, в которых Rа - метил, являются соединения нижеследующей общей формулы: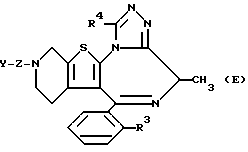
где Y, R3 и R4 принимают вышеуказанные значения, Z представляет группу формул 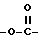 или
или 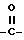 .
.
Соединения формулы (E) и в особенности те соединения, в которых метил находится в диазепиновом цикле, проявляют неожиданно лучшую анти-ФАТ активность по сравнению с известным производным 1,4-диазепина, о чем речь пойдет ниже.
Применяемые в настоящем изобретении фармакологически приемлемые соли - это обычные неядовитые соли, например: неорганические соли, такие как хлоргидраты, бромгидраты, сульфаты, фосфаты и т.п., органические соли, такие как ацетаты, малеаты, сукцинаты, метансульфонаты и т.п., а также соли аминокислот, таких как альгинин, аспаратиновая кислота, глутаминовая кислота и т.п.
Соединения изобретения имеют в молекуле асимметрический атом углерода и могут существовать в виде различных пространственных изомеров. В практике изобретения отдельные изомеры и их смеси все охватываются объемом изобретения. К примеру, соединение формулы (D), приведенной выше, имеет асимметрический атом углерода, связанный с Rа (если Rа - метил), вследствие чего имеет стереоизомеры. Изомеры могут быть выделены обычными препаративными способами.
Кроме того, отдельные соединения могут образовывать гидраты, которые также охватываются объемом изобретения.
Соединения изобретения синтезируют по обычным методикам, типичные примеры которых приведены ниже.
Препаративный способ 1
Для получения соединений формулы (I), в которых X представлен формулой: 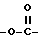 , или формулой:
, или формулой: 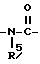 , и n = 1, синтез осуществляют по следующей схеме реакции:
, и n = 1, синтез осуществляют по следующей схеме реакции: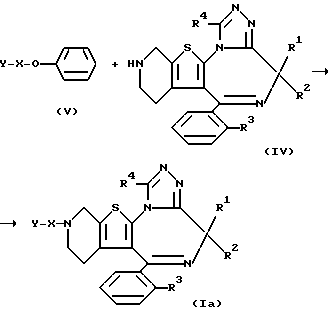
где X, n, Y, R1, R2, R3 и R4 принимают соответственно вышеуказанные значения.
Соединение формулы (IV) конденсируют с соединением формулы (V) и получают соединение формулы (Ia), являющееся одним из целевых соединений.
Реакцию проводят обычным образом без растворителя или в инертном в условиях реакции растворителе, выбранном из хлороформа, тетрагидрофурана, диэтилового эфира, ацетона, бензола, толуола и диметилформамида. Температура реакции от комнатной до 150oC, наиболее предпочтительно 100 - 130oC.
В вышеприведенной схеме реакции соединение формулы (V), применяемое в качестве исходного продукта, синтезируют, например, согласно нижеследующей схеме реакции: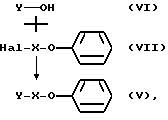
где Y, X и n принимают соответственно вышеуказанные значения и Hal представляет атом галоида.
В вышеприведенной схеме реакции соединение общей формулы (VI) конденсируют с галоидпроизводным общей формулы (VII) и получают соединение общей формулы (V).
Реакцию рекомендуется проводить в присутствии оснований, в том числе аминов, таких как триэтиламин, пиридин и т.п., гидридов щелочных металлов, таких как гидрид натрия, гидрид калия и т.п., гидроксидов щелочных металлов, таких как гидроксид калия, гидроксид натрия и т.п.
Реакция может быть проведена без растворителя или в растворителе. Примеры растворителей включают: простые эфиры, такие как тетрагидрофуран, диоксан и т.п., галоидпроизводные, такие как хлористый метилен, хлороформ и т. п., ароматические соединения, такие как бензол, толуол, ксилол и т.п. и другие соединения, такие как диметилформамид, диметилсульфоксид и т.п.
Препаративный способ 2
Синтез соединений, в которых X представлен формулой 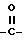 и n = 1, проводят по следующей схеме реакции:
и n = 1, проводят по следующей схеме реакции: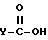
или реакционноспособное производное этой кислоты (VIII)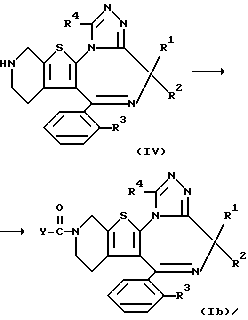
Если подробнее, то карбоновую кислоту общей формулы (VIII) или ее реакционноспособное производное конденсируют с соединением общей формулы (IV) и получают соединение общей формулы (IB), являющееся одним из целевых соединений.
Конденсацию проводят обычным образом. Реакционноспособные производные кислоты включают: галоидангидриды кислоты, такие как хлорангидриды, бромангидриды и т. п.; азиды кислоты; N-гидроксибензотриазольное производное; активные сложные эфиры, такие как N-гидроксисукцинамид; симметричные ангидриды кислот; смешанные ангидриды со щелочными карбонатами, п-толуолсульфокислотой и т.п.
Реакцию проводят при нагревании без растворителя или в растворителе, не принимающем участия в реакции, например бензоле, толуоле, ксилоле, тетрагидрофуране, хлороформе, четыреххлористом углероде, диметилформамиде и т.п., с осуществлением, к примеру, дегалоидирования. Лучшие результаты достигаются при проведении реакции в присутствии неорганических солей, таких как гидрокарбонат натрия, карбонат калия, каустическая сода и т.п., или органических оснований, таких как триэтиламин, пиридин, пиримидин, диэтиланилин и т.п.
При использовании свободных кислот лучшие результаты достигаются в присутствии конденсирующего средства, такого как 1,1'-карбонилдиимидазол, дициклогексилкарбодиимид и т.п.
Препаративный способ 3
Синтез соединений, в которых X представлен формулой 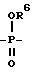 и n = 1, осуществляют по следующей схеме реакции:
и n = 1, осуществляют по следующей схеме реакции: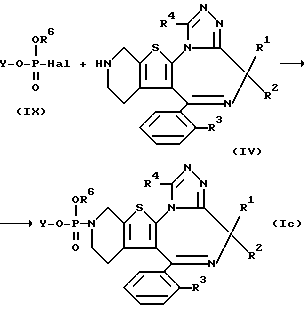
где Y, R1, R2, R3, R4 и R6 принимают соответственно вышеуказанные значения и Hal представляет атом галоида.
Галоидпроизводное формулы (IX) и соединение общей формулы (IV) вступают в реакцию с образованием целевого соединения формулы (Ic).
Реакция относится к реакции дегидрогалоидирования и ее проводят обычным путем при нагревании без растворителя или в растворителе, не принимающем участия в реакции и выбранном, например, из бензола, толуола, ксилола, тетрагидрофурана, хлороформа, четыреххлористого углерода и диметилформамида. Лучшие результаты достигаются в присутствии неорганических солей, таких как гидрокарбонат натрия, карбонат калия, карбонат натрия и каустическая сода, или органических оснований, таких как триэтиламин, пиридин, пиримидин, диэтиланилин и т.п.
Препаративный способ 4
Для синтеза соединений формулы (I), где n = 0, используют следующую схему реакции: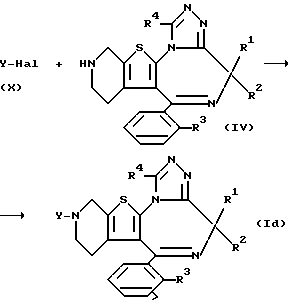
где Y, R1, R2, R3 и R4 принимают соответственно вышеуказанные значения и Hal представляет атом галоида.
Галоидпроизводное формулы (X) вступает в реакцию с соединением общей формулы (IV) с образованием целевого соединения формулы (Id).
Реакция относится к реакции дегалоидирования и ее проводят обычным путем при нагревании без растворителя или в растворителе, не принимающем участия в реакции и выбранном из бензола, толуола, ксилола, тетрагидрофурана, хлороформа, четыреххлористого углерода и диметилформамида. Лучшие результаты достигаются при проведении реакции в присутствии неорганических солей, таких как гидрокарбонат натрия, карбонат калия, карбонат натрия и каустическая сода, или органических оснований, таких как триэтиламин, пиридин, пиримидин, диэтиланилин и т.п.
Исходное соединение формулы (IV), применяемое в вышеприведенных препаративных способах 1 - 4, может быть синтезировано согласно следующей методике.
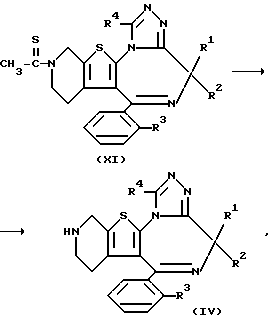
где R1, R2, R3 и R4 принимают соответственно вышеприведенные значения.
Согласно приведенной схеме тиоамид формулы (XI) подвергают гидролизу с получением соединения общей формулы (IV).
Гидролиз проводят по обычной методике, в которой соединение общей формулы (IV) может быть получено при нагревании в присутствии, например, гидроксида натрия, гидроксида калия, этоксида натрия, метоксида натрия и т.п. В реакции может быть использован растворитель, такой как метиловый спирт, этиловый спирт и т.п., тетрагидрофуран, диметоксиэтан или водный растворитель.
В случае вышеуказанного исходного соединения формулы (IV), в котором R1 - водород, R2 - метил и R4 - метил, препаративный способ его получения может быть отражен следующей конкретной схемой (см. фиг. 1 - 3).
На фиг. 3 знаком "*" отмечен асимметрический атом углерода и формула (XX) представляет соответствующий энантиомер.
Ниже вкратце иллюстрируется каждая из вышеприведенных стадий.
(Первая стадия)
2-Бромпропионилбромид формулы (XIII) по обычной методике конденсируют с соединением общей формулы (XII) и получают соединение общей формулы (XIV).
Реакцию проводят в двухфазной системе (в условиях реакции Шоттен-Баума) органического растворителя, такого как, например, толуол, бензол, ксилол и т. п., в присутствии либо гидроксида щелочного металла, такого как гидроксид натрия, гидроксид калия и т.п., либо основания, такого как гидрокарбонат натрия, гидрокарбонат калия и т.п.
Или же реакция может быть проведена в присутствии основания, в том числе амина, такого как триэтиламин, пиридин и т.п., гидроксида щелочного металла, такого как гидроксид натрия, гидроксид калия и т.п., или гидрида щелочного металла, такого как гидрид натрия, гидрид калия и т.п., в растворителе, не принимающем участия в реакции, таком как, например, дихлорметан, дихлорэтан, тетрагидрофуран, толуол, бензол, ксилол, диметилформамид и т.п.
(Вторая стадия)
На этой стадии через соединение общей формулы (XIV) по обычной методике пропускают газообразный аммиак и получают соединение общей формулы (XV).
Реакцию рекомендуется проводить в интервале низких температур, например при 30 - 100oC.
Реакцию проводят без растворителя или в растворителе, не принимающем участия в реакции и выбранном из простых эфиров, таких как тетрагидрофуран, диоксан и т.п., этилацетата, хлороформа, метанола, этанола, пиридина и дихлорэтана.
(Третья стадия)
На данной стадии осуществляют дегидратацию соединения общей формулы (XV) по обычной методике с его циклизацией и образованием соединения общей формулы (XVI).
Одна из методик описывается более детально. Соединение растворяют в соответствующем растворителе, не принимающем участия в реакции, таком как, например, бензол, толуол, ксилол, пиридин и т.п., и к раствору добавляют эквивалент кислотного катализатора, такого как уксусная кислота, силикагель и т.п. Реакционную систему нагревают с удалением образующейся воды с помощью обезвоживающего средства или насадки Дина-Старка.
(Четвертая стадия)
На этой стадии проводят реакцию между пентасульфидом фосфора и соединением общей формулы (XVI) с получением соединения общей формулы (XVII).
Реакцию проводят в растворителе, таком как пиридин, диметоксиэтан, диглимы, тетрагидрофуран, толуол, бензол, ксилол и т.п. Реагентом может служить азид из пентасульфида фосфора, реактив Лаусона, (2,4-бис(4-метоксифенил)-1,3-дитиа-2,4-дифосфетан-2,4-дисульфид). В некоторых случаях реакцию проводят в присутствии основания, такого как гидрокарбонат натрия.
(Пятая стадия)
На этой стадии осуществляют реакцию ацетогидразида с соединением общей формулы (XVII) с его циклизацией и образованием соединения общей формулы (XVIII).
Реакцию проводят нагреванием ацетогидразида в растворителе, не принимающем участия в реакции, таком как, например, диоксан, диметоксиэтан, диглимы и т.п., или в отсутствие растворителя. Или же проводят реакцию гидразингидрата в растворителе, таком как метанол или этанол, и полученный гидразид вводят в реакцию с этил орто-ацетатом и получают целевой продукт. Еще в одном варианте может быть осуществлена реакция гидразида с ацетилхлоридом или уксусным ангидридом и затем проводят дегидратацию полученного продукта с получением соединения формулы (XVIII).
(Шестая стадия)
На этой стадии проводят по обычной методике гидролиз соединения общей формулы (XVIII) и получают соединение общей формулы (XIX).
Осуществляют реакцию по известным методикам, например нагреванием в присутствии гидроксида калия, гидроксида натрия, этоксида натрия, метоксида натрия, этоксида калия, метоксида калия и т.п., с получением в результате соединения общей формулы (XIX).
В реакции может быть использован растворитель, в том числе спиртовой растворитель, такой как метиловый спирт или этиловый спирт, тетрагидрофуран, диметоксиэтан или водные растворители.
Конкретный пример получения соединения общей формулы (XIX) использованием вышеприведенного ряда превращений иллюстрируется препаративным примером (см. ниже), где R3 - атом хлора.
Соединения общей формулы (XIX) являются новыми соединениями, играющими важную роль в качестве промежуточных продуктов для получения конечных соединений с хорошей анти-ФАТ активностью. Более конкретно, конечное соединение, полученное на основе промежуточного соединения (т.е. соединения общей формулы (I), где R1 - атом водорода и R2 - метил), проявляет неожиданно высокую анти-ФАТ активность по сравнению с известными производными 1,4-диазепина. В этом смысле соединения общей формулы (IV), в которых R1 - атом водорода и R2 - низший алкил, в частности метил, являются очень ценными промежуточными продуктами.
Промежуточные соединения обладают асимметрическим атомом углерода, вследствие чего существуют в виде оптических изомеров. В практике изобретения d1-изомеры при желании могут быть разделены на оптически активные продукты.
Разделение может быть осуществлено на стадии получения соединения общей формулы (XV) с применением для разделения оптического разделяющего средства, такого как: (+) или (-)-винная кислота, (+) или (-)-камфорная кислота, (+) или (-)-дибензоилвинная кислота, (+) или (-)-10-камфорсульфоновая кислота, (+) или (-)-миндальная кислота и т.п. Или же на стадии получения соединений общей формулы (IV) или (XIX) разделение может быть осуществлено применением оптического разделяющего средства, такого как дибензоил-D-винная кислота или дибензоил-L-винная кислота. И еще в одном варианте разделение возможно на стадии получения соединений общих формул (XV), (XIX) или (IV) применением колонки для разделения оптических изомеров, такой как, например, колонка с хиральным полиамидом на силикагеле в ВЭЖХ (высокоэффективная жидкостная хроматография) с элюированием смесью тетрагидрофуран-гексан.
Другие соединения, отличные от описанных в способах их получения, могут быть получены аналогичным путем, но на основе других исходных продуктов.
Экспериментальный пример
Испытание на связывание ФАТ-рецептора с тромбоцитами человека
(Методика)
Тромбоциты отбирают обычным путем у здоровых людей и суспендируют до концентрации 108 тромбоцитов/460 мкл в связующем буфере (10 мМ фосфатного солевого буфера (pH 7) с 0,1% (мас./об.) АБС (альбумина бычьей сыворотки) и 0,9 мМ CaCl2). Тромбоциты (108) в 460 мкл буфера переносят в полипропиленовые пробирки и предварительно инкубируют с испытуемым соединением (20 мкл) после центрифугирования в течение 6 мин при 37oC. Затем в пробирки добавляют 20 мкл раствора связующего буфера с 3Н-ФАТ (конечная концентрация 3Н-ФАТ 0,6 нМ) и инкубируют 6 минут. Реакцию связывания прекращают добавлением 3 мл охлажденного льдом промывного раствора (солевой раствор, содержащий 0,1% (мас. /об.) АБС). Тромбоциты отделяют вакуумным фильтрованием на стеклянных фильтрах (Wharman GF/C). После высушивания стеклянного фильтра с помощью сцинтиллятора с жидкостным сцинтиллирующим счетчиком измеряют радиоактивность фильтра.
Процент ингибирования подсчитывают по нижеприведенному уравнению и последующей интерполяцией полученных результатов получают значения ИК (ингибирующей концентрации).

где связывание - радиоактивность связывания в отсутствие холодного ФАТ или испытуемых соединений;
неспецифичное связывание - радиоактивность связывания в присутствии 10-5 М ФАТ.
Полученные результаты приведены в таблице.
Неспецифичное связывание - радиоактивность (dpm) после инкубирования с 10-5 М ФАТ.
Полученные результаты приведены в таблице.
Знаком "*" обозначен асимметрический атом углерода и знаком "(+)" и "(-)" указаны направления удельного вращения.
Из таблицы очевидно, что соединения изобретения обладают анти-ФАТ активностью. Более того, найдено, что соединения обладают повышенной и более продолжительной анти-ФАТ активностью при большей безопасности по сравнению с известными соединениями. Таким образом, настоящее изобретение обладает большими достоинствами.
Соответственно, соединения изобретения будут эффективны для лечения и профилактики заболеваний, передаваемых ФАТ.
Типичные заболевания, по отношению к которым соединения применимы в качестве лечебных и профилактических средств, включают: аллергические заболевания, астму, тромбоз, церебральную апоплексию (внутримозговое кровоизлияние, внутримозговой тромбоз), инфаркт миокарда (стенокардия), синдром коагулопатии потребления человека (СГП), тромбофлебиты, гломерулярный гепатит, анафилактический шок, шок от кровотечения и т.п. соединения изобретения будут особенно полезными в качестве противоаллергических средств и противоастматических средств.
При введении этих соединений в качестве анти-ФАТ средств они могут быть использованы в пероральных дозировках в виде таблеток, порошков, гранул, капсул, сиропов и т.п. Или же они могут быть использованы в парентеральных дозировках в виде свеч, инъекций, внешнего лекарственного средства или капельного внутреннего вливания. В случае изобретения соединения рекомендуется применять в качестве перорального средства.
Дозировки могут зависеть от вида заболевания, его тяжести и возраста больного. В случае перорального введения соединения применяют в дозировках 0,001 - 10 мг/кг, предпочтительно 0,01 - 0,5 мг/кг.
Препараты для перорального или парентерального введения могут быть изготовлены применением обычных фармацевтически приемлемых добавок. Для получения растворов для инъекций или капельного внутривенного вливания к основному компоненту добавляют при необходимости модификаторы pH, буферные растворы, стабилизаторы и солюбилизаторы. Смесь может быть высушена вымораживанием при необходимости с получением инъекций для подкожного, внутримышечного или внутривенного введения или для капельного внутривенного вливания.
Ниже представлены данные по острой токсичности, полученные при испытании на крысах соединения примера 77, LD50 (мг/кг):
Орально - Внутривенно
самцы
1000 - 2000 - 120 - 240
самки
612 - 120 - 240
Ниже приведены типичные примеры изобретения, которые не следует рассматривать как ограничивающие его.
В числе приведенных ниже примеров: (A) примеры 1 - 77 и препаративные примеры 1 - 29; (B) примеры 78 - 104 и препаративные примеры 30 - 34; (C) примеры 105 - 120 и препаративные примеры 35 - 43; (D) примеры 121 - 137 и препаративные примеры 44 - 52.
Необходимо отметить, что получение исходных соединений или веществ описывается в виде препаративных примеров.
ПРИМЕР 1
6-(2-Хлорфенил)-3-(1-циано-1-метилэтоксикарбонил)-11-метил-2,3,4,5- тетрагидро-8Н-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин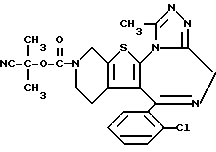
(1) Синтез 1-циано-1-метилэтилфенилкарбоната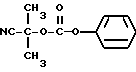
При охлаждении льдом к 0,85 г (10 ммолей) циангидрина ацетона в пиридине (20 мл) по каплям прибавляют 1,4 г (9 ммолей) фенилхлорформата, после чего перемешивают 30 минут. После завершения реакции растворитель отгоняют с получением остатка, который растворяют в хлороформе и промывают 1 н. соляной кислотой, насыщенным водным раствором бикарбоната натрия и сушат над сульфатом магния. Полученный продукт очищают колоночной хроматографией на силикагеле с элюированием смесью этилацетат - н-гексан (1:49) и получают с количественным выходом целевое соединение в виде бесцветного твердого вещества.
(2) Синтез 6-(2-хлорфенил)-3-(1-циано-1-метилэтоксикарбонил)-11-метил-2,3,4,5-тетрагидро- 8Н-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепина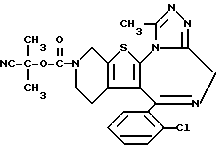
В хлороформе растворяют 0,5 г 1-циано-1-метилэтилфенилкарбоната и 0,15 г 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8Н-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло[4,3-a] [1,4]диазепина, хорошо перемешивают, после чего растворитель отгоняют. Полученную смесь перемешивают в бане при 120oC 1 час. После охлаждения и очистки колоночной хроматографией на силикагеле с элюированием смесью хлороформ - этанол (99:1) получают 0,18 г целевого продукта в виде аморфного вещества.
1Н-ЯМР (90 МГц, CDCl3) 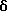 : 1,77 (6H, с), 1,8-2,2 (2H, м), 2,68 (3H, с), 3,1-3,6 (2H, м), 4,22 (1H, м), 4,50-4,88 (2H, м), 5,6 (1H, м), 7,35 (4H, м).
: 1,77 (6H, с), 1,8-2,2 (2H, м), 2,68 (3H, с), 3,1-3,6 (2H, м), 4,22 (1H, м), 4,50-4,88 (2H, м), 5,6 (1H, м), 7,35 (4H, м).
FABMS (M+H+) m/z: 481
ПРИМЕР 2
6-(2-Хлорфенил)-3-(3-цианопропоксикарбонил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин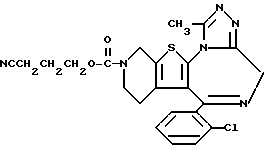
(1) Синтез 3-цианопропилфенилкарбоната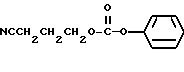
При охлаждении льдом к 0,85 г 4-гидроксибутиронитрила и 1,5 г пиридина в хлороформе (20 мл) по каплям прибавляют 1,5 г фенилхлорформата, после чего перемешивают 30 минут. После завершения реакции реакционную смесь промывают насыщенным водным раствором бикарбоната натрия и сушат над сульфатом магния. Затем растворитель отгоняют и очисткой остатка на колонке с силикагелем с элюированием смесью этилацетат - н-гексан (3:17) получают 1,2 г целевого соединения.
(2) Синтез 6-(2-хлорфенил)-3-(3-цианопропоксикарбонил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепина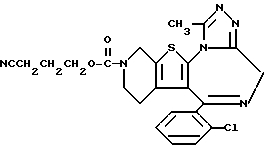
В хлороформе растворяют 0,11 г 1-цианопропилфенилкарбоната и 0,13 г 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f] [1,2,4] триазоло[4,3-a] [1,4] диазепина, хорошо перемешивают, после чего растворитель отгоняют. Полученную смесь перемешивают 1 час в бане при 110oC, затем охлаждают и после очистки хроматографией на колонке с силикагелем с элюированием смесью хлороформ - этанол (49:1) получают 0,1 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 1,41-1,80 (м, 2H), 1,80-2,17 (м, 2H), 2,22-2,52 (м, 2H), 2,6 (с, 3H), 2,80-5,76 (м, 6H), 4,2 (т, J = 7 Гц, 2H), 7,3 (м, 4H).
FABMS (M+H+) m/z: 481
ПРИМЕР 3
3-(3-Бутинилоксикарбонил)-6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин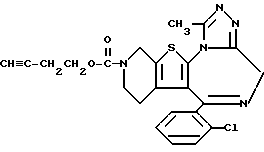
(1) Синтез 3-бутилфенилкарбоната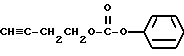
При охлаждении льдом к 0,7 г 3-бутин-1-ола и 1,5 г пиридина в дихлорметане (20 мл) по каплям прибавляют 1,7 г фенилхлорформата и перемешивают 30 минут. После завершения реакции реакционную смесь промывают насыщенным водным раствором бикарбоната натрия и сушат над сульфатом магния. Затем растворитель отгоняют и после очистки колоночной хроматографией на силикагеле с элюированием смесью этилацетат - н-гексан (1:49) с количественным выходом получают целевое соединение в виде бесцветного масла.
(2) Синтез 3-(3-бутинилоксикарбонил)-6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепина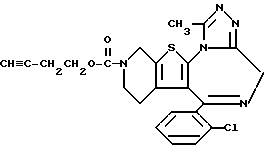
В хлороформе растворяют 0,1 г 3-бутинилфенилкарбоната и 0,18 г 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепина хорошо перемешивают, после чего растворитель отгоняют. Полученную смесь перемешивают 1 час при 110oC. После охлаждения и очистки колоночной хроматографией на силикагеле с элюированием смесью хлороформ - этанол (99:1) получают 0,17 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) 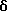 : 1,60 - 2,16 (м, 2H), 1,94 (с, 3H), 2,5 ( дв. т, J = 2 Гц, 7 Гц, 2H), 2,66 (с, 3H), 2,86 - 5,74 (м, 6H), 4,17 (т, J = 7 Гц, 2H), 7,29 (м, 4H).
: 1,60 - 2,16 (м, 2H), 1,94 (с, 3H), 2,5 ( дв. т, J = 2 Гц, 7 Гц, 2H), 2,66 (с, 3H), 2,86 - 5,74 (м, 6H), 4,17 (т, J = 7 Гц, 2H), 7,29 (м, 4H).
MS m/z (Pos. Gab): 466 (M + H+).
ПРИМЕР 4
6-(2-Хлорфенил)-3-(2-цианоэтиламинокарбонил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин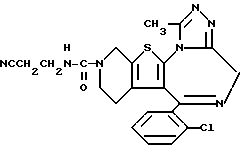
(1) Синтез N-(2-цианоэтил)карбамата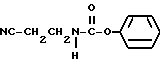
При охлаждении льдом к 0,7 г 3-аминопропионитрила и 1,2 г триэтиламина в дихлорэтане (20 мл) по каплям прибавляют 1,4 г фенилхлорформата и перемешивают 30 минут. После завершения реакции смесь промывают насыщенным водным раствором бикарбоната натрия и сушат над сульфатом магния. После отгонки растворителя и очистки колоночной хроматографией на силикагеле с элюированием смесью этилацетат - н-гексан (1:9) получают 1,3 г целевого соединения.
(2) Синтез 6-(2-Хлорфенил)-3-(2-цианоэтиламинокарбонил)-11-метил-2,3,4,5-тетрагидро- 8Н-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепина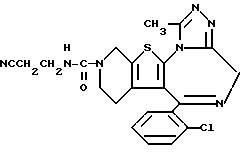
В хлороформе растворяют 0,09 г N-(2-цианоэтил)карбамата и 0,18 г 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло[4,3-a] [1,4] диазепина, хорошо перемешивают, после чего растворитель отгоняют. Полученную смесь перемешивают 1 час при 140oC. После охлаждения очисткой колоночной хроматографией на силикагеле с элюированием смесью хлороформ - метанол (19:1) получают 0,12 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 1,45 - 2,23 (м, 2H), 2,6 (т, J = 7 Гц, 2H), 2,64 (с, 3H), 2,80 - 5,69 (м, 9H), 7,29 (м, 4H).
MS m/z (Pos. Fab): 466 (M + H)+.
ПРИМЕР 5
6-(2-Хлорфенил)-11-метил-3-(2-пропинил)-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин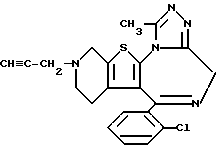
К раствору 0,12 г 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепина в диметилформамиде (20 мл) при комнатной температуре добавляют гидрид натрия (30 мг 60%) и перемешивают 1 час при 60oC. При комнатной температуре добавляют 60 мг 3-бромпропина и реакционную смесь перемешивают 1 час при 60oC. После охлаждения в реакционную смесь добавляют воду, экстрагируют этилацетатом и сушат над сульфатом магния. Удалением растворителя и очисткой колоночной хроматографией на силикагеле с элюированием смесью хлороформ - метанол (98,5: 1,5) получают 20 мг целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 1,52 - 2,12 (м, 2H), 2,25 (т, J = 2 Гц, 1H), 2,16 - 2,84 (м, 2H), 2,66 (с, 2H), 3,45 (д, J = 2 Гц, 2H). 3,74 (м, 2H), 3,9 - 4,4, 5,20 - 5,76 (2м, 2H), 7,27 (м, 2H).
MS m/z: 407.
ПРИМЕР 6
6-(2-Хлорфенил)-11-метил-3-циклопропанкарбонил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин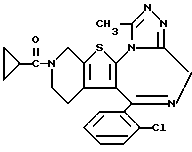
В 4 мл N,N-диметилформамида растворяют 90 мг циклопропанкарбонилхлорида и к полученному раствору по каплям при -60oC добавляют раствор 150 мг 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f] [1,2,4] триазоло[4,3-a] [1,4] диазепина в 6 мл N,N-диметилформамида и 210 мг триэтиламина и смесь перемешивают 30 минут. После отгонки растворителя добавляют насыщенный водный раствор бикарбоната натрия, экстрагируют хлороформом и сушат над сульфатом магния. После фильтрования, отгонки растворителя и очистки полученного остатка колоночной хроматографией на силикагеле с элюированием смесью MeOH - CH2Cl2 (1:99) получают 140 мг (выход 79%) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,4 - 1,3 (м, 4H), 1,4 - 2,7 (м, 3H), 2,67 (с, 3H), 2,8 - 5,8 (м, 6H), 7,1 - 7,6 (м, 4H).
Ms m/z (Pos. Fab.): 438 (M + H)+.
ПРИМЕР 7
6-(2-Хлорфенил)-3-циклопропанкарбонил-8,11-диметил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин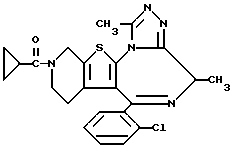
В 4 мл N, N-диметилформамида растворяют 100 мг 6-(2-хлорфенил)-3-циклопропанкарбонил-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло[4,3-a] [1,4]диазепина, к полученному раствору добавляют 54 мг гидрида натрия (55%) и 0,5 мл метилбромида и смесь перемешивают 1 час при комнатной температуре. Реакцию прекращают добавлением воды и раствор нейтрализуют уксусной кислотой. Затем растворитель отгоняют при пониженном давлении и полученный остаток экстрагируют 20 мл дихлорметана. Полученный раствор сушат над безводным сульфатом магния, растворитель удаляют и после очистки колоночной хроматографией на силикагеле (400 меш, 10 г) получают заглавное соединение.
1H-ЯМР (90 МГц, CDCl3) 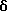 : 0,55 - 1,15 (м, 4H), 1,45 - 2,50 (м, 3H), 2,1 (д, J = 6,8 Гц, 3H), 2,66 (с, 3H), 2,8 - 4,8 (м, 3H), 4,26 (к, J = 6,8 Гц, 1H), 4,8 - 5,2 (м, 1H), 7,05 - 7,65 (м, 4H).
: 0,55 - 1,15 (м, 4H), 1,45 - 2,50 (м, 3H), 2,1 (д, J = 6,8 Гц, 3H), 2,66 (с, 3H), 2,8 - 4,8 (м, 3H), 4,26 (к, J = 6,8 Гц, 1H), 4,8 - 5,2 (м, 1H), 7,05 - 7,65 (м, 4H).
Ms m/z (Pos. Fab.): 452 (M + H)+.
ПРИМЕР 8
6-(2-Хлорфенил)-3-циннамоил-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин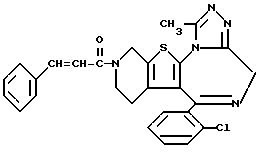
В 8 мл N,N-диметилформамида растворяют 80 мг циннамоилхлорида и к полученному раствору по каплям прибавляют 4 мл раствора 120 мг 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4] триазоло[4,3-a][1,4]диазепина и 160 мг триэтиламина в N,N-диметилформамиде и смесь перемешивают. После отгонки растворителя добавляют насыщенный водный раствор бикарбоната натрия, экстрагируют хлороформом, сушат над безводным сульфатом магния, фильтруют, растворитель отгоняют и после очистки остатка колоночной хроматографией на силикагеле с элюированием смесью MeOH - CH2Cl2 (1:99) получают 11 мг (68%) заглавного соединения.
MS m/z (Pos. Fab.): 500 (M + H)+.
ПРИМЕР 9
6-(2-Хлорфенил)-3-циклобутанкарбонил-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин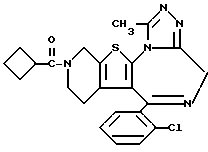
В 8 мл N,N-диметилформамида растворяют 50 мг циклобутанкарбоновой кислоты, 70 мг моногидрата 1-гидроксибензотриазола и 150 мг 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4] диазепина, при охлаждении льдом добавляют 100 мг N,N'-дициклогексилкарбодиимида, после чего перемешивают 10 минут при той же температуре и сутки при 4oC. Затем после перемешивания еще 1 час при комнатной температуре нерастворимое вещество отфильтровывают и растворитель отгоняют. Добавляют насыщенный водный раствор бикарбоната натрия, после чего экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор отфильтровывают, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью MeOH - CH2Cl2 (1:99) получают 180 мг (98%) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,5 (м, 9H), 2,67 (с, 3H), 2,8 - 5,9 (м, 6H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. Fab.): 452 (M + H)+.
ПРИМЕР 10
6-(2-Хлорфенил)-3-диэтилфосфоро-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин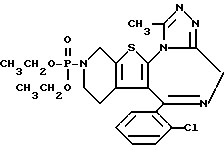
В 5 мл тетрагидрофурана и 1 мл триэтиламина растворяют 100 мг 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло[4,3-a] [1,4]диазепина, к полученному раствору добавляют 100 мг диэтилхлорфосфата и смесь перемешивают 1 час при комнатной температуре. Реакционный раствор прибавляют к насыщенному водному раствору бикарбоната натрия, экстрагируют этилацетатом и сушат над безводным сульфатом магния. Растворитель удаляют при пониженном давлении и очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием смесью CH3OH:CH2Cl2 (5:95) получают 100 мг (72%) целевого соединения.
MS (FAB): 506 (M + H)+.
1H-ЯМР (90 МГц, ): 1,28 (т, J = 8, 6H), 1,44 - 2,20 (м, 2H), 2,69 (с, 3H), 3,7 - 4,6 (м, 9H), 5,33 - 5,72 (м, 1H), 7,12 - 7,48 (м, 5H).
ПРИМЕР 11
3-(3-Бутинилоксикарбонил)-6-(2-хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин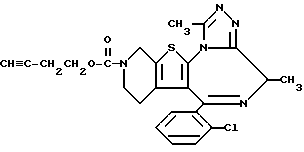
К раствору 57 мг 3-(3-бутинилоксикарбонил)-6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4] диазепина в диметилформамиде (2 мл) добавляют 28 мг гидрида натрия (55%,) и 0,2 мл метилбромида и перемешивают 1 час при комнатной температуре.
Для прекращения реакции добавляют воду и раствор нейтрализуют уксусной кислотой. Растворитель отгоняют при пониженном давлении и полученный остаток экстрагируют 10 мл дихлорметилена и затем 20 мл дихлорметилена. Раствор сушат над сульфатом магния, растворитель удаляют и после очистки колоночной хроматографией на силикагеле (400 меш, 10 г) с элюированием смесью метанол - дихлорметан (1:99) получают 24 мг целевого соединения.
1H-ЯМР (90 МГц, CDCl3): 7,4 (5H, Ar), 4,9 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,5 (1H, J = 18 Гц, N-CH2(C-2)), 4,2 (1H, м, C8-H), 4,1 (2H, т, J = 8 Гц, O-CH2), 2,7 (3H, с), 2,5 (2H, дв. т, J = 1,7 Гц, ≡ -CH2), 2,1 (3H, д, J = 7 Гц, CH CH3), 3 - 2 (5H, м).
ПРИМЕР 12
6-(2-Хлорфенил)-8,11-диметил-3-(3-цианопропоксикарбонил)-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин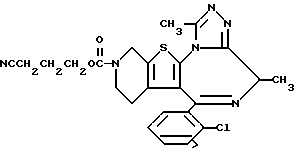
К раствору 62 мг 6-(2-хлорфенил)-3-(3-цианопропоксикарбонил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4] диазепина в 2 мл диметилформамида при комнатной температуре добавляют 34 мг гидрида натрия (55%) и 0,2 мл метилбромида и смесь перемешивают 1 час при комнатной температуре. Для прекращения реакции к раствору добавляют воду и нейтрализуют уксусной кислотой. Растворитель отгоняют при пониженном давлении и полученный остаток экстрагируют 10 мл дихлорметилена и затем 20 мл дихлорметилена. Раствор сушат над сульфатом магния, растворитель удаляют и после очистки колоночной хроматографией на силикагеле (400 меш, 10 г) с элюированием смесью метанол - дихлорметан (1:99) получают 21 мг целевого соединения.
1H-ЯМР (90 МГц, CDCl3): 7,4 (2H, Ar), 4,9 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,5 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,2 (1H, м, C8-H), 4,1 (2H, т, J = 8 Гц, O-CH2), 2,7 (3H, с), 2,4 (3H, д, J = 7 Гц), 2,1 (3H, д, J = 7 Гц, CHCH3), 3 - 2 (6H, м).
ПРИМЕР 13
6-(2-Хлорфенил)-8,8-диэтил-3-(3-цианопропоксикарбонил)-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4] триазоло[4,3-a] [1,4]диазепин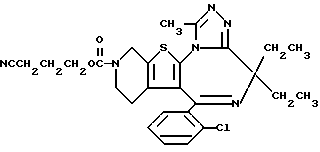
К раствору 69 мг 6-(2-хлорфенил)-3-(3-цианопропоксикарбонил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4] диазепина в 2 мл диметилформамида при комнатной температуре добавляют 10 мг гидрида натрия (55%) и 0,03 мл метилбромида и перемешивают 2 часа при комнатной температуре.
Тонкослойной хроматографией выявлено присутствие исходного соединения и двух новых продуктов, а именно: моноэтилпроизводного и диэтилпроизводного. Поэтому добавляют 10 мг гидрида натрия и 0,03 мл этилбромида, перемешивают еще 2 часа, после чего для прекращения реакции к раствору добавляют воду и нейтрализуют уксусной кислотой. Растворитель отгоняют при пониженном давлении и полученный остаток экстрагируют 10 мл дихлорметилена и затем 20 мл дихлорметилена. Раствор сушат над сульфатом магния, растворитель удаляют и после очистки колоночной хроматографией на силикагеле (400 меш, 13 г) с элюированием смесью метанол - дихлорметан (1:99) получают 41 мг целевого соединения.
1H-ЯМР (90 МГц, CDCl3): 7,4 (5H, Ar), 4,9 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,5 (1H, J = 18 Гц, N-CH2(C-2)), 4,1 (2H, т, J = 8 Гц, O-CH2), 2,7 (3H, с, CH3), 2,0 - 2,7 (10H, м), 1,3 (6H, т, J = 7 Гц, CH2CH3).
ПРИМЕР 14
3-(3-Бутинилоксикарбонил)-6-(2-хлорфенил)-8,8-диэтил-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин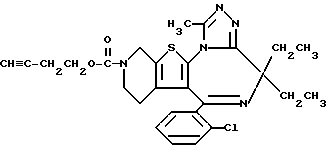
Воспроизведена общая методика примера 12 использованием 65 г 3-(3-бутинилоксикарбонил)-6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепина. Получено 23 мг целевого продукта.
1H-ЯМР (90 МГц, CDCl3): 7,4 (5H, Ar), 4,9 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,5 (1H, J = 18 Гц, N-CH2(C-2)), 4,1 (2H, т, J = 8 Гц, O-CH2), 2,7 (3H, с, CH3), 2,0 - 2,7 (8H, м, CH2CH3 и CH2CH3), 1,3 (6H, т, J = 7 Гц, CH2CH3).
ПРИМЕР 15
6-(2-Хлорфенил)-3-(1-циано-1-метилэтоксикарбонил)-7,11-диметил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин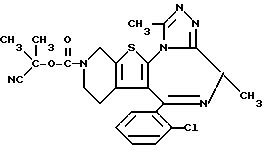
К раствору 1,12 г соединения примера 1 в N,N-диметилформамиде (3 мл) при охлаждении льдом добавляют 0,24 г гидрида натрия (60%) и перемешивают 30 минут. Затем к раствору добавляют 0,37 мг метилбромида, перемешивают 30 минут при охлаждении льдом и 1 час при комнатной температуре. После завершения реакции добавляют воду, экстрагируют хлороформом и сушат сульфатом магния. Полученный после фильтрования и концентрирования остаток очищают колоночной хроматографией на силикагеле с элюированием смесью хлороформ - метанол (99:1) и получают 0,19 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,76 (с, 6H), 1,8 - 2,2 (м, 2H), 2,1 (д, 3H), 2,66 (с, 3H), 3,0 - 3,9 (м, 2H), 4,24 (к, 1H), 4,3 - 4,9 (м, 2H), 7,35 (м, 4H).
FABMS (M + H+) m/z: 495.
ПРИМЕРЫ 16 - 71
По методике вышеприведенного примера получены следующие соединения.
ПРИМЕР 16
6-(2-Хлорфенил)-3-(1-циано-1-метилэтоксикарбонил)-8,8,11-триметил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин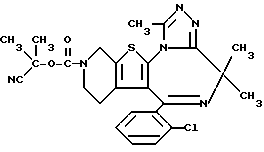
1H-ЯМР (90 МГц, CDCl3) δ: 1,8 (с, 6H), 2,8 (с, 3H), 3,1 (с, 3H), 3,0 - 3,9 (м, 4H), 3,8 (с, 3H), 4,4 - 4,9 (м, 2H), 7,4 (м, 4H).
ПРИМЕР 17
6-(2-Хлорфенил)-3-циклопропилметиламинокарбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин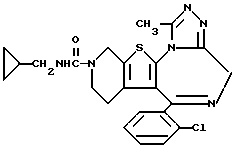
1H-ЯМР (90 МГц, CDCl3) δ: 0,04 - 0,32 (м, 2H), 0,36 - 0,60 (м, 2H), 0,70 - 1,16 (м, 1H), 1,52 - 2,17 (м, 2H), 2,66 (с, 3H), 2,84 - 5,85 (м, 7H), 3,04 (дв. д, J = 6 Гц, 7 Гц, 2H), 7,32 (м, 4H).
FABMS (M + N+) m/z: 467.
ПРИМЕР 18
6-(2-Хлорфенил)-3-(1-этинилциклогексиламинокарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин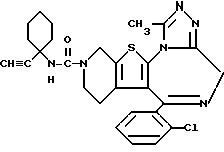
1H-ЯМР (90 МГц, CDCl3) δ: 1,12 - 2,24 (м, 12H), 2,37 (с, 1H), 2,80 - 5,76 (м, 7H), 7,29 (м, 4H).
FABMS (M + N+) m/z: 519.
ПРИМЕР 19
6-(2-Хлорфенил)-3-(5-цианопентиламинокарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин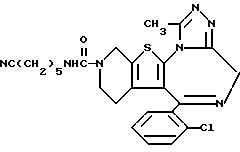
1H-ЯМР (90 МГц, CDCl3) δ: 1,28 - 2,16 (м, 8H), 2,32 (т, J = 7 Гц, 2H), 2,81 - 5,68 (м, 9H), 7,29 (м, 4H).
FABMS (M + H+) m/z: 508.
ПРИМЕР 20
6-(2-Хлорфенил)-3-(4-цианофениламинокарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин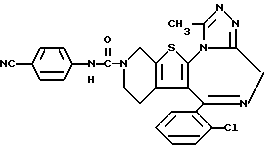
1H-ЯМР (90 МГц, CDCl3) δ: 1,55 - 2,18 (м, 2H), 2,67 (с, 3H), 3,8 - 5,7 (м, 6H), 7,32 (м, 4H), 7,47 (м, 4H), 8,4 (уш., с, 1H).
FABMS (M + H+) m/z: 514.
ПРИМЕР 21
6-(2-Хлорфенил)-3-(3-цианофениламинокарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин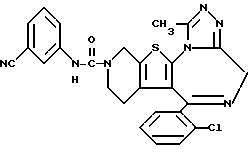
1H-ЯМР (90 МГц, CDCl3) δ: 1,43 - 2,17 (м, 2H), 2,63 (с, 3H), 3,04 - 5,68 (м, 6H), 7,05 - 7,72 (м, 8H).
FABMS (M + H+) m/z: 514.
ПРИМЕР 22
6-(2-Хлорфенил)-3-(3-этинилфениламинокарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин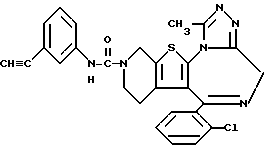
1H-ЯМР (90 МГц, CDCl3) 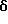 : 1,4 - 2,4 (м, 2H), 2,66 (с, 3H), 3,01 (с, 1H), 3,05 - 5,08 (м, 6H), 6,64 (уш. с, 1H), 6,88 - 7,48 (м, 8H ).
: 1,4 - 2,4 (м, 2H), 2,66 (с, 3H), 3,01 (с, 1H), 3,05 - 5,08 (м, 6H), 6,64 (уш. с, 1H), 6,88 - 7,48 (м, 8H ).
FABMS (M + H+) m/z: 513.
ПРИМЕР 23
6-(2-Хлорфенил)-11-метил-3-(морфолин-4-ил)карбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин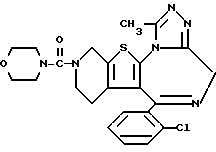
1H-ЯМР (90 МГц, CDCl3) δ: 1,32 - 2,44 (м, 2H), 2,66 (с, 3H), 2,92 - 5,8 (м, 6H), 3,21 (т, J = 6 Гц, 4H), 3,63 (т, J = 6 Гц, 4H), 7,29 (м, 4H).
FABMS (M + H+) m/z: 483.
ПРИМЕР 24
6-(2-Хлорфенил)-3-(1-этинилциклопентиламинокарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин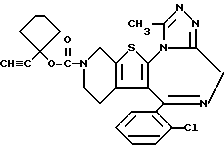
1H-ЯМР (90 МГц, CDCl3) δ: 1,40 - 2,44 (м, 10H), 2,56 (с, 1H), 2,67 (с, 3H), 2,9 - 5,8 (м, 6H), 7,29 (м, 4H).
FABMS (M + H+) m/z : 506.
ПРИМЕР 25
6-(2-Хлорфенил)-11-метил-3-(фенилэтинилкарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин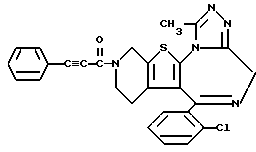
1H-ЯМР (90 МГц, CDCl3) δ: 1,67 - 2,40 (м, 2H), 2,68 (с, 3H), 3,04 - 5,80 (м, 6H), 7,12 - 7,60 (м, 9H).
FABMS (M + H+) m/z: 498.
ПРИМЕР 26
6-(2-Хлорфенил)-3-(1,1-диметил-2-пропинилоксикарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин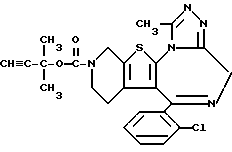
1H-ЯМР (90 МГц, CDCl3) δ: 1,40 - 2,18 (м, 2H), 1,68 (с, 6H), 2,53 (с, 1H), 2,67 (с, 3H), 2,90 - 5,76 (м, 6H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 480.
ПРИМЕР 27
6-(2-Хлорфенил)-11-метил-3-(1-метил-2-пропинилоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин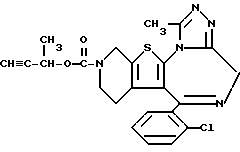
1H-ЯМР (90 МГц, CDCl3) 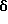 : 1,38 - 2,32 (м, 2H), 1,5 (д, J = 7 Гц, 3H), 2,45 (д, J = 2 Гц, 1H), 2,66 (с, 3H), 2,88 - 5,70 (м, 6H), 5,34 (дв. к, J = 2 Гц, 7 Гц, 1H), 7,29 (м, 4H).
: 1,38 - 2,32 (м, 2H), 1,5 (д, J = 7 Гц, 3H), 2,45 (д, J = 2 Гц, 1H), 2,66 (с, 3H), 2,88 - 5,70 (м, 6H), 5,34 (дв. к, J = 2 Гц, 7 Гц, 1H), 7,29 (м, 4H).
FABMS (M + H+) m/z: 466.
ПРИМЕР 28
6-(2-Хлорфенил)-11-метил-3-(1-метил-3-бутинилоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин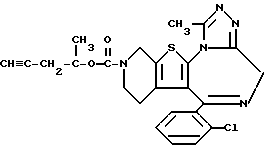
1H-ЯМР (90 МГц, CDCl3) δ: 1,3 (д, J = 7 Гц, 3H), 1,5 - 2,6 (м, 5H), 2,66 (с, 3H), 2,88 - 5,72 (м, 7H), 7,29 (м, 4H).
FABMS (M + H+) m/z: 480.
ПРИМЕР 29
6-(2-Хлорфенил)-11-метил-3-(2-пентинилоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин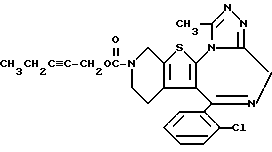
1H-ЯМР (90 МГц, CDCl3) δ: 1,13 (д, J = 7 Гц, 3H), 1,54 - 2,36 (м, 2H), 2,25 (тр. к, J = 2 Гц, 7 Гц, 2H), 2,67 (с, 3H), 2,84 - 5,76 (м, 6H), 4,66 (т, J = 2 Гц, 2H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 480.
ПРИМЕР 30
6-(2-Хлорфенил)-11-метил-3-(3-пентинилоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин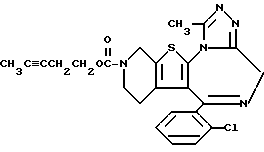
1H-ЯМР (90 МГц, CDCl3) δ: 1,5 - 2,2 (м, 2H), 1,74 (т, J = 2 Гц, 3H), 2,42 (м, 2H), 2,66 (с, 3H), 2,9 - 5,7 (м, 6H), 4,11 (т, J = 7 Гц, 2H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 480.
ПРИМЕР 31
6-(2-Хлорфенил)-3-[2-(имидазол-1-ил)этоксикарбонил] -11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин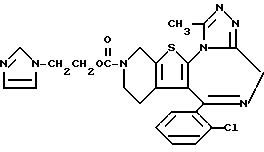
1H-ЯМР (90 МГц, CDCl3) δ: 1,50 - 2,19 (м, 2H), 2,66 (с, 3H), 2,8 - 5,8 (м, 10H), 6,70 - 6,92 (м, 1H), 6,92 - 7,06 (м, 1H), 7,12 - 7,54 (м, 1H), 7,30 (м, 4H).
FABMS (M + H+) m/z: 508.
ПРИМЕР 32
6-(2-Хлорфенил)-11-метил-3-(2,3,5,6-тетрагидропиран-4-ил)оксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин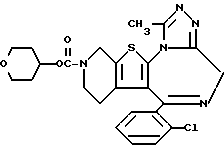
1H-ЯМР (90 МГц, CDCl3) 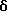 : 1,40 - 2,12 (м, 6H), 2,67 (с, 3H), 2,84 - 5,68 (м, 11H), 7,29 (м, 4H).
: 1,40 - 2,12 (м, 6H), 2,67 (с, 3H), 2,84 - 5,68 (м, 11H), 7,29 (м, 4H).
FABMS (M + H+) m/z: 498.
ПРИМЕР 33
6-(2-Хлорфенил)-3-[5-гексинилоксикарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин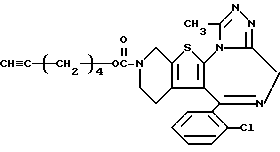
1H-ЯМР (90 МГц, CDCl3) δ: 1,20 - 2,32 (м, 6H), 1,94 (т, J = 2 Гц, 1H), 2,21 (дв. т, J = 2 Гц, 7 Гц, 2H), 2,66 (с, 3H), 2,84 - 5,76 (м, 6H), 7,28 (м, 4H).
FABMS (M + H+) m/z: 494.
ПРИМЕР 34
6-(2-Хлорфенил)-3-(3-циано-1-оксопропил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин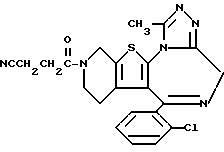
1H-ЯМР (90 МГц, CDCl3) δ: 1,16 - 2,38 (м, 2H), 2,42 - 2,79 (м, 4H), 2,67 (с, 3H), 3,20 - 5,72 (м, 6H), 7,31 (м, 4H).
FABMS (M + H+) m/z: 451.
ПРИМЕР 35
6-(2-Хлорфенил)-3-(2-циано-1-оксоэтил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин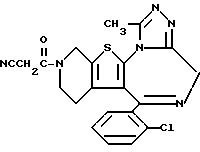
1H-ЯМР (90 МГц, CDCl3) δ: 1,60 - 2,35 (м, 2H), 2,66 (с, 3H), 3,20 - 5,76 (м, 8H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 437.
ПРИМЕР 36
6-(2-Хлорфенил)-3-(3-цианопропоксикарбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин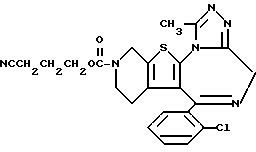
1H-ЯМР (90 МГц, CDCl3) δ: 1,41 - 1,80 (м, 2H), 1,80 - 2,17 (м, 2H), 2,22 - 2,52 (м, 2H), 2,66 (с, 3H), 2,86 - 5,76 (м, 6H), 4,2 (т, J = 7 Гц, 2H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 481.
ПРИМЕР 37
6-(2-Хлорфенил)-11-метил-3-(1-оксо-4-пентинил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин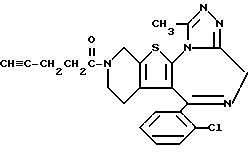
1H-ЯМР (90 МГц, CDCl3) 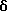 : 1,54 - 2,18 (м, 2H), 1,96 (м, 1H), 2,44 - 2,65 (м, 4H), 2,71 (с, 3H), 2,88 - 5,76 (м, 6H), 7,42 (м, 4H).
: 1,54 - 2,18 (м, 2H), 1,96 (м, 1H), 2,44 - 2,65 (м, 4H), 2,71 (с, 3H), 2,88 - 5,76 (м, 6H), 7,42 (м, 4H).
FABMS (M + H+) m/z: 450.
ПРИМЕР 38
6-(2-Хлорфенил)-11-метил-3-(1-пропаргилпиперидин-4-ил)оксикарбонил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин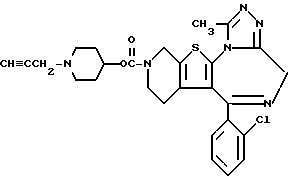
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,9 (м, 11H), 2,25 (т, 1H), 2,7 (с, 3H), 3,3 (д, 2H), 3,0 - 3,9 (м, 2H), 4,0 - 4,9 (м, 1 + 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FD): 535.
ПРИМЕР 39
6-(2-Хлорфенил)-3-циклогексилоксикарбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин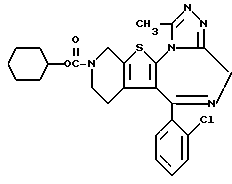
1H-ЯМР (90 МГц, CDCl3) δ: 1,2 - 2,3 (м, 12H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 4,0 - 4,8 (м, 1 + 1 + 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FAB): 496.
ПРИМЕР 40
6-(2-Хлорфенил)-3-циклогексилэтоксикарбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин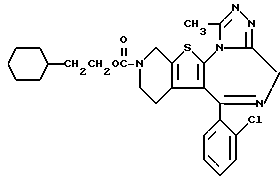
1H-ЯМР (90 МГц, CDCl3) δ: 0,6 - 2,7 (м, 17H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 4,0 - 4,4 (м, 1 + 2H), 4,4 - 4,8 (м, 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FAB): 538.
ПРИМЕР 41
6-(2-Хлорфенил)-3-циклопропилметоксикарбонил-11-метил 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин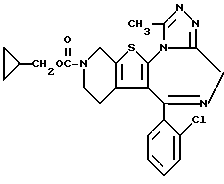
1H-ЯМР (90 МГц, CDCl3) 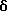 : 0,2 - 2,0 (м, 2H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 3,8 - 4,0 (д, 2H), 4,4 - 4,8 (м, 1 + 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
: 0,2 - 2,0 (м, 2H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 3,8 - 4,0 (д, 2H), 4,4 - 4,8 (м, 1 + 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FAB): 468.
ПРИМЕР 42
6-(2-Хлорфенил)-3-циклогексилметоксикарбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин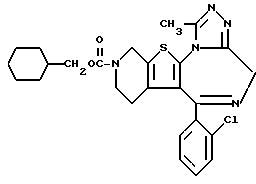
1H-ЯМР (90 МГц, CDCl3) δ: 0,8 - 2,2 (м, 13H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 3,7 - 4,0 (д, 2H), 4,1 - 4,8 (м, 1 + 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FAB): 510.
ПРИМЕР 43
6-(2-Хлорфенил)-11-метил-3-(4-пиридилкарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин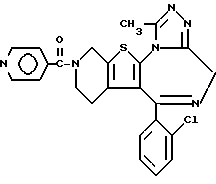
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,5 (м, 2H), 2,67 (с, 3H), 3,10 - 3,75 (м, 2H), 3,9 - 5,8 (м, 4H), 7,0 - 7,7 (м, 6H), 8,4 - 8,8 (м, 2H).
MS m/z (Pos. FAB): 475.
ПРИМЕР 44
6-(2-Хлорфенил)-3-циклогексилметилкарбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин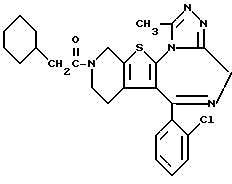
1H-ЯМР (90 МГц, CDCl3) δ: 0,6 - 2,4 (м, 13H), 2,16 (д, J = 6,5 Гц, 2H), 2,67 (с, 3H), 2,8 - 5,9 (м, 6H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 494 (M + H)+.
ПРИМЕР 45
6-(2-Хлорфенил)-3-циклогексанкарбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин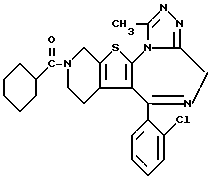
1H-ЯМР (90 МГц, CDCl3) 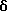 : 0,7 - 2,7 (м, 13H), 2,67 (с, 3H), 2,8 - 5,8 (м, 6H), 7,1 - 7,4 (м, 4H).
: 0,7 - 2,7 (м, 13H), 2,67 (с, 3H), 2,8 - 5,8 (м, 6H), 7,1 - 7,4 (м, 4H).
MS m/z (Pos. FAB): 480 (M + H)+.
ПРИМЕР 46
6-(2-Хлорфенил)-11-метил-3-(3-пиридилкарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин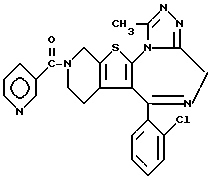
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,6 (м, 2H), 2,66 (с, 3H), 2,8 - 6,0 (м, 6H), 7,1 - 8,0 (м, 6H), 8,4 - 8,8 (м, 2H).
MS m/z (Pos. FAB): 475 (M + H)+.
ПРИМЕР 47
3-[4'-(Морфолин-4-илсульфонил)фениламинокарбонил] -6-(2-хлорфенил)- 11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин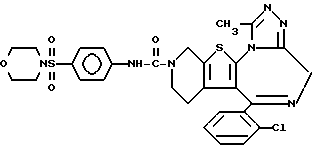
1H-ЯМР (90 МГц, CDCl3) δ: 1,8 - 2,2 (м, 4H), 2,63 (с, 3H), 2,80 - 3,08 (м, 4H), 3,24 - 3,90 (м, 9H), 4,6 - 4,9 (м, 2H), 7,20 - 7,42 (м, 4H), 7,45 - 7,68 (м, 4H), 7,75 (уш. полоса, 1H).
MS: m/z 638.
ПРИМЕР 48
6-[4'-(N-Пиперидиносульфонил)фениламинокарбонил] -6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин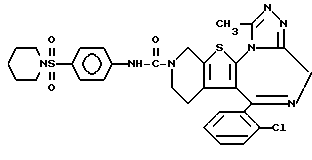
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 - 2,3 (м, 10H), 2,64 (с, 3H), 2,75 - 3,10 (м, 4H), 3,3 - 4,3 (м, 2H), 4,60 - 4,92 (м, 2H), 7,15 - 7,40 (м, 4H), 7,42 - 7,60 (м, 4H) 7,72 (уш. полоса, 1H).
MS: m/z 636.
ПРИМЕР 49
3-[4'-(N-Имидазоилсульфонил)фениламинокарбонил] -6-(2-хлорфенил)- 11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин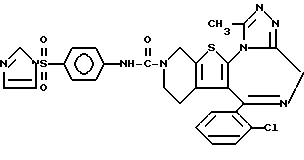
1H-ЯМР (90 МГц, CDCl3) δ: 1,6 - 2,4 (м, 4H), 2,7 (с, 3H), 3,75 - 4,30 (м, 2H), 4,4 - 5,0 (м, 2H), 7,0 - 7,5 (м, 12H).
MS: m/z 619.
ПРИМЕР 50
3-[4'-(Сульфамоил)фениламинокарбонил] -6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин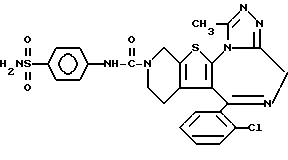
1H-ЯМР (90 МГц, CDCl3) 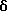 : 1,4 - 2,2 (м, 4H), 2,62 (с, 3H), 3,6 - 4,4 (м, 2H), 5,1 - 5,5 (м, 2H), 7,1 (с, 2H), 7,3 - 7,6 (м, 4H), 7,62 (AB к, 4H, J = 9 Гц) 8,95 (с, 1H).
: 1,4 - 2,2 (м, 4H), 2,62 (с, 3H), 3,6 - 4,4 (м, 2H), 5,1 - 5,5 (м, 2H), 7,1 (с, 2H), 7,3 - 7,6 (м, 4H), 7,62 (AB к, 4H, J = 9 Гц) 8,95 (с, 1H).
MS: m/z 568.
ПРИМЕР 51
3-[4'-(N, N'-Диэтиламиносульфонил)фениламинокарбонил] -6-(2-хлорфенил)- 11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин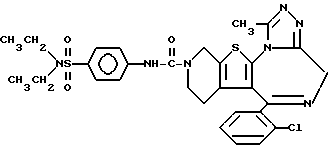
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 (т, 6H, J = 7,2 Гц), 1,7 - 2,3 (м, 4H), 2,62 (с, 3H), 3,16 (к, 4H, J = 7,2 Гц), 3,4 - 4,2 (м, 2H), 3,55 - 3,60 (м, 2H), 7,18 - 7,40 (м, 4H), 7,54 (AB к, 4H, J = 9 Гц), 7,7 (с, 1H).
MS: m/z 624.
ПРИМЕР 52
3-[4'-(N'-Циклогексиламиносульфонил)фениламинокарбонил]-6-(2-хлорфенил)- 11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин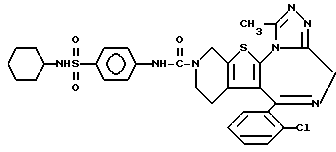
1H-ЯМР (90 МГц, CDCl3) δ: 0,8 - 2,2 (м, 14H), 2,64 (с, 3H), 2,8 - 4,3 (м, 3H), 4,6 - 4,3 (м, 3H), 4,6 - 4,9 (м, 2H), 5,05 (д, 1H, J = 7,2 Гц), 7,2 - 7,4 (м, 4H), 7,56 (AB к, 4H, J = 9 Гц), 7,76 (с, 1H).
MS: m/z 650.
ПРИМЕР 53
3-[4'-(2''-Пиридилметиламиносульфонил)фениламинокарбонил] -6-(2-хлорфенил)- 11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4] триазоло[4,3-a][1,4]диазепин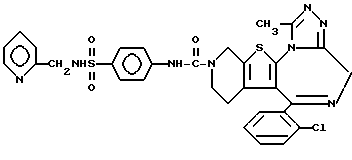
1H-ЯМР (90 МГц, CDCl3) δ: 1,6 - 2,2 (м, 4H), 2,72 (с, 3H), 3,6 - 4,5 (м, 6H), 6,50 - 6,72 (м, 2H), 7,0 - 7,7 (м, 11H), 8,11 - 8,28 (м, 1H).
MS: m/z 659.
ПРИМЕР 54
3-[3-(N-Пиперидиносульфонил)пропилоксикарбонил] -6-(2-хлорфенил)- 11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5] тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин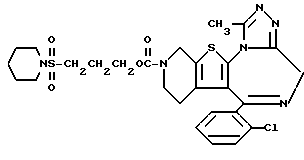
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,3 (м, 12H), 2,7 (с, 3H), 2,95 (т, 2H, J = 7,2 Гц), 3,1 - 3,4 (м, 4H), 3,5 - 4,2 (м, 2H), 4,22 (т, 2H, J = 7,2 Гц), 4,42 - 4,82 (м, 2H), 7,2 - 7,5 (м, 4H).
MS: m/z 603.
ПРИМЕР 55
3-[3-(N-Морфолиносульфонил)пропилоксикарбонил] -6-(2-хлорфенил)- 11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло[4,3-a][1,4]диазепин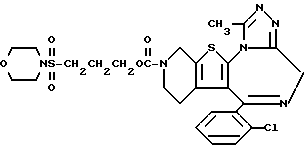
1H-ЯМР (90 МГц, CDCl3) 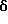 : 1,6 - 2,4 (м, 6H), 2,7 (с, 3H), 2,98 (т, 2H, J = 7,2 Гц), 3,6 - 3,9 (м, 4H), 2,8 - 4,4 (м, 2H), 4,22 (т, 2H, J = 7,2 Гц), 4,40 - 4,84 (м, 2H), 7,2 - 7,5 (м, 4H).
: 1,6 - 2,4 (м, 6H), 2,7 (с, 3H), 2,98 (т, 2H, J = 7,2 Гц), 3,6 - 3,9 (м, 4H), 2,8 - 4,4 (м, 2H), 4,22 (т, 2H, J = 7,2 Гц), 4,40 - 4,84 (м, 2H), 7,2 - 7,5 (м, 4H).
MS: m/z 605.
ПРИМЕР 56
3-[4'-(N-Морфолиносульфонил)фенилоксикарбонил] -6-(2-хлорфенил)- 11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло[4,3-a][1,4]диазепин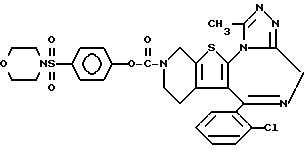
1H-ЯМР (90 МГц, CDCl3) δ: 1,6 - 2,4 (м, 4H), 2,74 (с, 3H), 2,8 - 3,1 (м, 4H), 3,6 - 3,8 (м, 4H), 3,1 - 5,1 (м, 4H), 4,9 - 7,6 (м, 8H).
MS: m/z 639.
ПРИМЕР 57
6-(2-Хлорфенил)-3-(2-цианоэтилметиламино)карбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин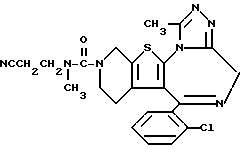
1H-ЯМР (90 МГц, CDCl3) δ: 1,57 - 2,22 (м, 2H), 2,61 (т, J = 7 Гц, 2H), 2,67 (с, 3H), 2,94 (с, 3H), 3,0 - 5,8 (м, 6H), 3,43 (т, J = 7 Гц, 2H), 7,31 (м, 4H).
FABMS (M+ H+) m/z: 480.
ПРИМЕР 58
6-(2-Хлорфенил)-3-(1-этинил-1-циклогексилокси-1-карбонил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин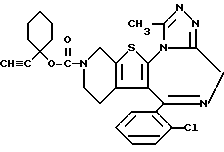
1H-ЯМР (90 МГц, CDCl3) δ: 1,04 - 2,35 (м, 12H), 2,59 (с, 1H), 2,67 (с, 3H), 2,78 - 5,78 (м, 6H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 520.
ПРИМЕР 59
6-(2-Хлорфенил)-11-метил-3-(1-фенил-2-пропинилоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин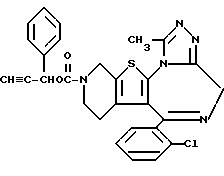
1H-ЯМР (90 МГц, CDCl3) δ: 1,63 - 2,30 (м, 2H), 2,57 (д, J = 2 Гц, 1H), 2,65 (с, 3H), 2,97 - 5,71 (м, 6H), 6,35 (д, J = 2 Гц, 1H), 7,11 - 7,64 (м, 9H).
FABMS (M + H+) m/z: 528.
ПРИМЕР 60
6-(2-Хлорфенил)-3-(2-цианоэтокси)карбонил-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин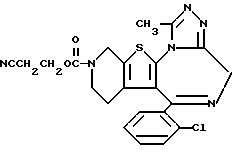
1H-ЯМР (90 МГц, CDCl3) 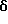 : 1,40 - 2,34 (м, 2H), 2,66 (с, 3H), 2,7 ( т, J = 7 Гц, 2H), 2,79 - 5,76 (м, 6H), 4,28 (т, J = 7 Гц, 2H), 7,3 (м, 4H).
: 1,40 - 2,34 (м, 2H), 2,66 (с, 3H), 2,7 ( т, J = 7 Гц, 2H), 2,79 - 5,76 (м, 6H), 4,28 (т, J = 7 Гц, 2H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 467.
ПРИМЕР 61
6-(2-Хлорфенил)-11-метил-3-(2-пропинил)аминокарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин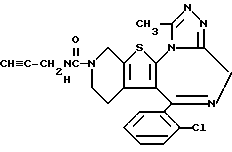
1H-ЯМР (90 МГц, CDCl3) δ: 1,56 - 2,08 (м, 2H), 2,19 (д, J = 2 Гц, 1H), 2,65 (с, 3H), 2,96 - 5,70 (дв. д, J = 2 Гц, 7 Гц, 6H), 3,98 (дв. д, J = 2 Гц, 7 Гц, 2H), 4,83 (т, J = 7 Гц, 1H), 7,28 (м, 4H).
FABMS (M + H+) m/z: 451.
ПРИМЕР 62
3-(2-Бутинилоксикарбонил)-6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин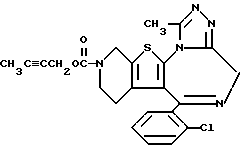
1H-ЯМР (90 МГц, CDCl3) δ: 1,43 - 2,15 (м, 2H), 1,84 (т, J = 2 Гц, 3H), 2,66 (с, 3H), 2,80 - 5,74 (м, 6H), 4,64 (к, J = 2 Гц, 2H), 7,3 (м, 4H).
FABMS (M + H+) m/z: 466.
ПРИМЕР 63
6-(2-Хлорфенил)-11-метил-3-[2-(2-пиридил)этиламинокарбонил] - 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин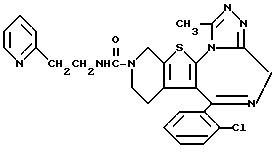
1H-ЯМР (90 МГц, CDCl3) δ: 1,46 - 2,25 (м, 2H), 2,65 (с, 3H), 2,76 - 5,76 (м, 6H), 2,92 (т, J = 7 Гц, 2H), 3,42 - 3,68 (м, 2H), 5,95 - 6,24 (м, 1H), 6,93 - 7,39 (м, 6H), 7,4 - 7,66 (м, 1H), 8,25 - 8,40 (м, 1H).
MS m/z: 517.
ПРИМЕР 64
6-(2-Хлорфенил)-3-[2-(морфолин-4-ил)этиламинокарбонил] -11-метил- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин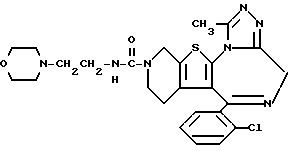
1H-ЯМР (90 МГц, CDCl3) δ: 1,54 - 2,20 (м, 2H), 2,30 - 2,58 (м, 6H), 2,67 (с, 3H), 2,88 - 5,80 (м, 6H), 3,17 - 3,42 (м, 2H), 3,55 - 3,74 (м, 4H), 5,03 - 5,19 (м, 1H), 7,3 (м, 4H).
MS m/z: 525.
ПРИМЕР 65
6-(2-Хлорфенил)-3-[4-(морфолин-4-илкарбонилокси)-2-бутинилоксикарбонил]- 11-метил-2,3,4,5-тетрагидро- 8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин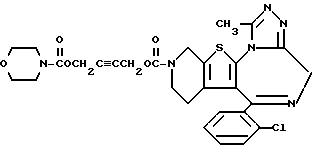
1H-ЯМР (90 МГц, CDCl3) 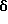 : 1,55 - 2,28 (м, 2H), 2,66 (с, 3H), 2,87 - 5,75 (м, 6H), 3,34 - 3,54 (м, 4H), 3,54 - 3,72 (м, 4H), 4,75 (с, 4H), 7,3 (м, 4H).
: 1,55 - 2,28 (м, 2H), 2,66 (с, 3H), 2,87 - 5,75 (м, 6H), 3,34 - 3,54 (м, 4H), 3,54 - 3,72 (м, 4H), 4,75 (с, 4H), 7,3 (м, 4H).
MS m/z: 594.
ПРИМЕР 66
6-(2-Хлорфенил)-11-метил-3-[4-(пиридин-2-илметиламинокарбонилокси)- 2-бутинилоксикарбонил] -2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин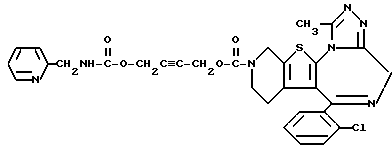
1H-ЯМР (90 МГц, CDCl3) δ: 1,6 - 2,2 (м, 2H), 2,7 (с, 3H), 3,00 - 5,75 (м, 6H), 4,46 (д, J = 5 Гц, 2H), 4,72 (с, 4H), 5,90 - 6,20 (м, 1H), 7,1 - 7,6 (м, 6H), 7,5 - 7,9 (м, 1H), 8,40 - 8,70 (м, 1H).
MS m/z: 615.
ПРИМЕР 67
6-(2-Хлорфенил)-11-метил-3-(4-пентинилоксикарбонил)-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин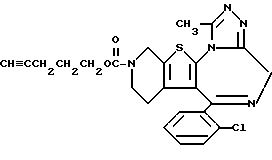
1H-ЯМР (90 МГц, CDCl3) δ: 1,52 - 2,08 (м, 4H), 1,92 (т, J = 2 Гц, 1H), 2,08 - 2,40 (м, 2H), 2,66 (с, 3H), 2,84 - 5,72 (м, 6H), 4,17 (т, J = 7 Гц, 2H), 7,29 (м, 4H).
MS m/z: 479.
ПРИМЕР 68
6-(2-Хлорфенил)-11-метил-3-(2-пропинилоксикарбонил)-2,3,4,5-тетрагидро- 8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин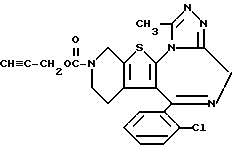
1H-ЯМР (90 МГц, CDCl3) δ: 1,68 - 2,15 (м, 2H), 2,5 (т, J = 3 Гц, 1H), 2,62 (с, 3H), 2,85 - 5,79 (м, 6H), 4,65 (д, J = 3 Гц, 2H), 7,4 (м, 4H).
MS m/z: 451.
ПРИМЕР 69
6-(2-Хлорфенил)-11-метил-3-[2-(пиридин-2-ил)этоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин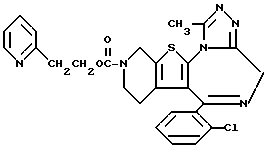
1H-ЯМР (90 МГц, CDCl3) δ: 1,64 - 2,25 (м, 2H), 2,50 - 5,74 (м, 6H), 2,71 (с, 3H), 2,9 (т, J = 7 Гц, 2H), 3,91 (т, J = 7 Гц, 2H), 6,86 - 7,80 (м, 7H), 8,36 - 8,76 (м, 1H).
MS m/z: 518.
ПРИМЕР 70
6-(2-Хлорфенил)-11-метил-3-[(тетрагидропиран-2-ил)метоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин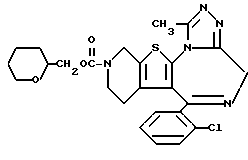
1H-ЯМР (90 МГц, CDCl3) 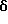 : 1,12 - 2,32 (м, 8H), 2,66 (с, 3H), 2,92 - 5,72 (м, 11H), 7,3 (м, 4H).
: 1,12 - 2,32 (м, 8H), 2,66 (с, 3H), 2,92 - 5,72 (м, 11H), 7,3 (м, 4H).
MS m/z: 499.
ПРИМЕР 71
6-(2-Хлорфенил)-11-метил-3-[2-(морфолин-2-ил)этоксикарбонил)- 2,3,4,5-тетрагидро- 8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин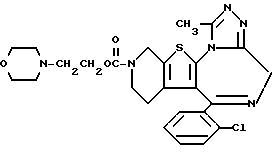
1H-ЯМР (90 МГц, CDCl3) δ: 1,54 - 2,24 (м, 2H), 2,36 - 2,64 (м, 6H), 2,68 (с, 3H), 3,04 - 5,84 (м, 6H), 3,52 - 3,80 (м, 4H), 4,24 (т, J = 7 Гц, 2H), 7,39 (м, 4H).
MS m/z: 526.
Препаративный пример 1
6-Ацетил-2-(2-бромпропиониламино)-3-(2-хлорбензоил)-4,5,6,7- тетрагидротиено[2,3-c]пиридин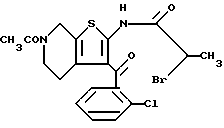
К 600 г 2-амино-3-(2-хлорбензоил)-6-ацетил-4,5,6,7-тетрагидротиено[2,3-c] пиридина добавляют 13,3 г толуола и 3,66 литра воды, затем добавляют 301 г гидрокарбоната натрия и к полученному раствору при 60oC по каплям прибавляют 301 мл 2-бромпропионилбромида. Добавляют еще 170 г гидрокарбоната натрия и 170 мл 2-бромпропионилбромида для завершения реакции. После охлаждения до комнатной температуры добавляют 500 г гидрокарбоната натрия и органическую фазу отделяют. Водную фазу дважды экстрагируют этилацетатом, соединяют с органической фазой, промывают водой и сушат над безводным сульфатом магния. Растворитель отгоняют при пониженном давлении и после промывания полученного твердого остатка эфиром получают 800 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 1,7 - 2,4 (м, 2H), 1,99 (д, J = 2 Гц, 2H), 2,06 и 2,12 (оба с, всего 3H), 3,25 - 3,7 (м, 2H), 4,41 (к, J = 7,2 Гц, 1H), 4,4 - 4,8 (м, 2H), 7 - 7,5 (м, 4H).
Препаративный пример 1
6-Ацетил-2-(2-аминопропиониламино)-3-(2-хлорбензоил)-4,5,6,7- тетрагидротиено[2,3-c]пиридин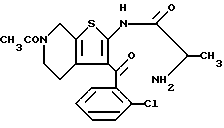
(Способ A)
В 0,72 литра дихлорэтана и 1,08 литра этилацетата растворяют 841 г 6-ацетил-2-(2-бромпропиониламино)-3-(2-хлорбензоил)-4,5,6,7- тетрагидротиено[2,3-c] пиридина и при -10oC пропускают газообразный аммиак. Полученную смесь нагревают в автоклаве 1 час при 100oC. После завершения реакции избыток аммиака удаляют и реакционную смесь переносят при охлаждении льдом в 3 н. соляную кислоту. После экстрагирования этилацетатом водную фазу нейтрализуют насыщенным водным раствором карбоната натрия и затем неоднократно экстрагируют хлороформом. Полученную органическую фазу промывают насыщенным солевым раствором, сушат над безводным сульфатом магния и после отгонки растворителя при пониженном давлении получают 636,8 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 1,48 (д, J = 6,8 Гц, 3H), 1,6 - 2,3 (м, 4H), 2,07 и 2,12 (два с, всего 3H), 3,25 - 4,00 (м, 3H), 4,35 - 4,75 (м, 2H), 7,0 - 7,6 (м, 4H).
(Способ B)
В 150 мл хлороформа при комнатной температуре растворяют 10 г 2-амино-3-(2-хлорбензоил)-6-ацетил-4,5,6,7-тетрагидротиено[2,3-c]пиридина и к полученному раствору понемногу в течение часа прибавляют при комнатной температуре и перемешивании 17 г хлоргидрата аланилхлорида. После завершения реакции к смеси добавляют 150 мл воды и перемешивают 30 минут. Водную фазу отделяют. Раствор в хлороформе с целью экстрагирования обрабатывают 150 мл воды. Обе водные фазы объединяют, промывают хлороформом, нейтрализуют бикарбонатом натрия и экстрагируют хлороформом. Растворитель удаляют при пониженном давлении и получают 10,1 г соединения в виде желтого порошка.
Препаративный пример 3
8-Ацетил-5-(2-хлорфенил)-3-метил-6,7,8,9-тетрагидро-1H, 3H-пиридо[4',3': 4,5]тиено[3,2-f][1,4]диазепин-2-он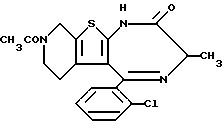
В 2,3 литра толуола, 637 мл пиридина и 94,3 мл уксусной кислоты растворяют 636,8 г 6-ацетил-2-(2-аминопропиониламино)-3-(2-хлорбензоил)-4,5,6,7- тетрагидротиено[2,3-c] пиридина и кипятят с обратным холодильником в течение дня и ночи с удалением воды из реакционной системы. После удаления растворителя добавляют бензол, охлаждают и после фильтрования получают 300 г целевого продукта в виде кристаллов.
1H-ЯМР (90 МГц, CDCl3) δ: 1,3 - 2,6 (м, 2H), 1,76 (д, J = 6,8 Гц, 3H), 2,06 и 2,12 (два с, всего 3H), 2,8 - 4,1 (м, 2H), 3,87 (к, J = 6,8 Гц, 1H), 4,1 - 5,1 (м, 2H), 7,1 - 7,5 (м, 4H), 9,0 - 9,5 (уш. с, 1H).
Препаративный пример 4
3-Метил-5-(2-хлорфенил)-8-тиоацетил-6,7,8,9-тетрагидро-1H, 3H-пиридо[4', 3': 4,5]тиено[3,2-f][1,4]диазепин-2-тион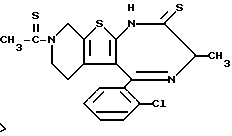
В 3 литрах диметоксиэтана растворяют 288 г 3-метил-5-(2-хлорфенил)-8-ацетил-6,7,8,9-тетрагидро-1H, 3H-пиридо[4', 3': 4,5]тиено[3,2-f][1,4]диазепин-2-она, добавляют 186 г гидрокарбоната натрия и 364 г пентасульфида фосфора и кипятят с обратным холодильником 3 часа. Реакционную смесь фильтруют через целит и растворитель отгоняют при пониженном давлении. К полученному остатку в небольших количествах добавляют метанол и дихлорметан с целью последующей адсорбции на силикагеле и после высушивания и очистки колоночной хроматографией с элюированием смесью дихлорметан - метанол (98:2) получают 300 г целевого соединения.
Препаративный пример 5
6-(2-Хлорфенил)-3-тиоацетил-8,11-диметил-2,3,4,5-тетрагидро-8H, -пиридо[4',3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин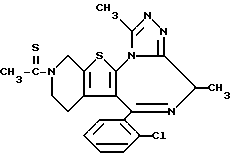
В 70 мл диоксана растворяют 4,81 г 3-метил-5-(2-хлорфенил)-8-тиоацетил-6,7,8,9-тетрагидро-1H, 3H-пиридо[4', 3': 4,5]тиено[3,2-f][1,4]диазепин-2-тиона, к полученному раствору добавляют 660 мг ацетогидразида и смесь нагревают при 100oC. После охлаждения смесь концентрируют при пониженном давлении и очисткой полученного остатка колоночной хроматографией с элюированием смесью дихлорметан - этанол (98:2) получают 750 г целевого соединения.
Препаративный пример 6
6-(2-Хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5] тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин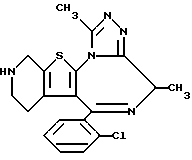
В 1 литре метанола растворяют 281 г 6-(2-хлорфенил)-8,11-диметил-3-тиоацетил-2,3,4,5-тетрагидро-8H-пиридо[4',3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4] диазепина, к полученному раствору добавляют 0,81 литра 4н. гидроксида натрия и нагревают до кипения с обратным холодильником. После охлаждения реакционную смесь подсаливают и экстрагируют хлороформом, после чего растворитель отгоняют при пониженном давлении. Очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (95:5) получают 142 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 - 2,3 (м, 3H), 2,1 (д, J = 6,8 Гц, 3H), 2,45 - 3,3 (м, 2H), 2,66 (с, 3H), 3,85 - 4,10 (м, 2H), 4,26 (к, J = 6,8 Гц, 1H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 384 (M + H)+.
Препаративный пример 7
(-)-6-(2-Хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин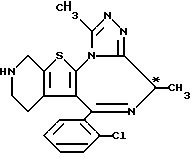
В 980 мл этанола при нагревании растворяют 86 г (±)-6-(2-хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5] тиено[3,2-f][1,2,4] триазоло[4,3-a][1,4]диазепина и 45,86 г дибензоил-D-тартрата и оставляют при комнатной температуре. Образовавшиеся кристаллы отфильтровывают, промывают эфиром, после действием разбавленного водного раствора бикарбоната натрия и двукратной экстракцией дихлорметаном переводят в свободное состояние. Полученную органическую фазу промывают насыщенным солевым раствором, сушат над безводным сульфатом магния и после отгонки растворителя при пониженном давлении получают 11 г целевого соединения.
Кроме того, фильтрат, от которого фильтрованием был отделен тартрат, подвергают вышеописанной обработке с получением в результате 11,3 г целевого соединения.
[α]
Препаративный пример 8
(+)-6-(2-Хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин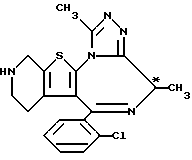
По методике препаративного примера 7, но использованием дибензоил-1-винной кислоты получают целевое соединение.
[α]
ПРИМЕР 72
(+)-6-(2-Хлорфенил)-3-(1-циано-1-метилэтоксикарбонил)-8,11-диметил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a] [1,4]диазепин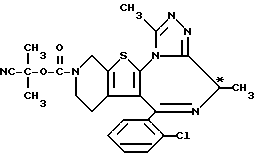
В дихлорметане растворяют 5 г (-)-6-(2-хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепина, к раствору добавляют 5 г 1-циано-1-метилэтилфенилкарбоната и смесь нагревают 4 часа при 100oC с отгонкой растворителя. После завершения реакции полученный остаток очищают колоночной хроматографией с элюированием смесью хлороформ - метанол (99:1) и получают 2,7 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) 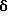 : 1,76 (с, 6H), 1,8 - 2,2 (м, 2H), 2,1 (д, 3H), 2,66 (с, 3H), 3,0 - 3,9 (м, 2H), 4,24 (к, 1H), 4,3 - 4,9 (м, 2H), 7,35 (м, 4H).
: 1,76 (с, 6H), 1,8 - 2,2 (м, 2H), 2,1 (д, 3H), 2,66 (с, 3H), 3,0 - 3,9 (м, 2H), 4,24 (к, 1H), 4,3 - 4,9 (м, 2H), 7,35 (м, 4H).
FABMS (M + N)+ 481.
[α]
ПРИМЕР 73
(+)-3-(3-Бутинилоксикарбонил)-6-(2-хлорфенил)-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин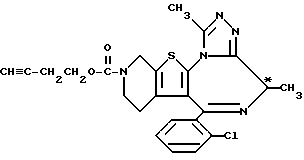
В дихлорметане растворяют 5 г (-)-6-(2-хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4] диазепина, к раствору добавляют 5 г 3-бутинилфенилкарбоната и смесь нагревают 4 часа при 110oC с отгонкой растворителя. После завершения реакции полученный остаток очищают колоночной хроматографией с элюированием смесью дихлорметан - метанол (99:1) и получают 1,6 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 7,4 (5H, Ar), 4,9 (д, 1H, J = 18 Гц,N-CH2(C-2)), 4,5 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,2 (1H, м, C8-H), 4,1 (2H, т, J = 8 Гц, O-CH2), 2,7 (3H, с), 2,5 (2H, дв. т, J = 1 Гц, 7 Гц, ≡ -CH2), 2,1 (3H, д, J = 7 Гц, CHCH3), 3,0 - 2,0 (5H, м).
[α]
ПРИМЕР 74
(+)-6-(2-Хлорфенил)-3-циклопропанкарбонил-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4',3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин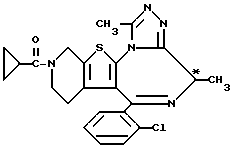
В 70 мл дихлорметана растворяют 5 г (-)-6-(2-хлорфенил)-8,11-диметил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4] диазепина, к раствору добавляют 1,42 г триэтиламина и при охлаждении льдом по каплям прибавляют 1,44 г циклопропанкарбонилхлорида. После завершения реакции реакционную смесь промывают насыщенным водным раствором бикарбоната натрия, затем насыщенным солевым раствором, сушат над безводным сульфатом магния и затем растворитель отгоняют при пониженном давлении. Очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (98:2) и получают 4,2 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,55 - 1,15 (м, 4H), 1,45 - 2,50 (м, 3H), 2,1 (д, J = 6,8 Гц, 3H), 2,66 (с, 3H), 2,8 - 4,8 (м, 3H), 4,26 (к, J = 6,8 Гц, 1H), 4,8 - 5,2 (м, 1H), 7,05 - 7,65 (м, 4H ).
MS m/z (Pos. Fab): 452 (M + H)+.
[α]
[α]
Другие способы получения соединений в вышеприведенных примерах показаны ниже.
Препаративный пример 9
1-(Циано-1-метилэтоксикарбонил)-4-гидроксипиперидин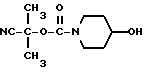
Смесь 50 г 1-циано-1-метилэтилфенилкарбоната и 25 г 4-гидроксипиперидина нагревают при 130o. После завершения реакции полученный продукт очищают колоночной хроматографией на силикагеле с элюированием смесью гексан - этилацетат (1:1 - 1:2 - 0:1) и получают 50,5 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,26 - 2,10 (м, 5H), 1,8 (с, 6H), 2,96 - 3,35 (м, 2H), 3,60 - 4,15 (м, 3H).
Препаративный пример 10
1-(циано-1-метилэтоксикарбонил)-4-пиперидон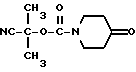
К раствору 4,15 мл оксалилхлорида в дихлорметане (50 мл) при -78oC по каплям прибавляют 5,06 мл диметилсульфоксида и затем 5,05 г 1-(1-циано-1-метилэтоксикарбонил)-4-гидроксипиперидина. После перемешивания при той же температуре 1 час добавляют 16,57 мл триэтиламина и перемешивание продолжают 1 час при комнатной температуре. Реакционную смесь фильтруют, промывают водой, сушат над безводным сульфатом магния, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - н-гексан (1:9) получают 3,9 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,8 (с, 6H), 2,48 (т, J = 7 Гц, 4H), 3,74 (т, J = 7 Гц, 4H).
Препаративный пример 11
2-Амино-3-(2-хлорбензоил)-6-(1-циано-1-метилэтоксикарбонил)- 4,5,6,7-тетрагидротиено[2,3-c]пиридин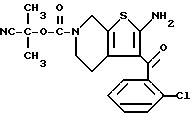
К смеси 3,9 г соединения препаративного примера 10, 0,6 г серы, 3,3 г 2-хлорцианоацетофенона и 20 мл N,N-диметилформамида прибавляют при 40oC 1,6 мл триэтиламина и все перемешивают 3 часа при 60oC. По окончании реакции растворитель испаряют досуха и промыванием остатка этилацетатом получают 5 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) 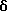 : 1,60 - 1,95 (м, 2H), 1,75 (с, 6H), 3,4 (м, 2H), 4,32 (м, 2H), 7,1 - 7,5 (м, 6H).
: 1,60 - 1,95 (м, 2H), 1,75 (с, 6H), 3,4 (м, 2H), 4,32 (м, 2H), 7,1 - 7,5 (м, 6H).
Препаративный пример 12
2-(2-Бромпропиониламино-3-(2-хлорбензоил)-6-(1-циано-1-метилэтоксикарбонил)- 4,5,6,7-тетрагидротиено[2,3-c]пиридин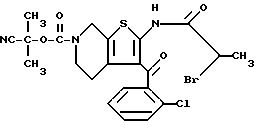
К смеси 5 г соединения препаративного примера 11, 2,1 г гидроксикарбоната натрия, 50 мл воды и 200 мл толуола прибавляют при 60oC по каплям 4,6 г 2-бромпропионилбромида. После завершения реакции добавляют этилацетат, водную фазу отделяют, органическую фазу промывают насыщенным солевым раствором, сушат над безводным сульфатом магния и после отгонки растворителя получают 6 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,76 (с, 6H), 1,88 (м, 2H), 2,0 (д, J = 7 Гц, 3H), 3,24 - 3,60 (м, 2H), 4,20 - 4,68 (м, 2H), 4,62 (к, J = 7 Гц, 1H), 7,0 - 7,5 (м, 4H).
Препаративный пример 13
2-(2-Аминопропиониламино)-3-(2-хлорбензоил)-6-(1-циано-1-метилэтоксикарбонил) -5,6,7,8-тетрагидротиено[2,3-c]пиридин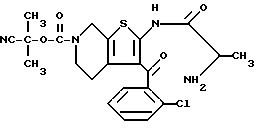
В 50 мл этилацетата растворяют 6 г соединения препаративного примера 12 и раствор насыщают 2 часа при -20oC аммиаком, после чего нагревают 5 часов при 100oC в запаянной пробирке. После завершения реакции продукт реакции экстрагируют 2н. соляной кислотой, полученную водную фазу нейтрализуют гидрокарбонатом натрия, насыщают затем хлористым натрием и экстрагируют хлороформом. После высушивания над безводным сульфатом магния и отгонки растворителя получают 0,7 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,51 (д, J = 7 Гц, 3H), 1,50 - 2,04 (м, 2H), 1,78 (с, 6H), 3,28 - 3,60 (м, 2H), 3,62 - 3,96 (м, 1H), 4,5 (м, 2H), 7,20 - 7,54 (м, 4H).
Препаративный пример 14
3-Метил-5-(2-хлорфенил)-8-(1-циано-1-метилэтоксикарбонил) -6,7,8,9-тетрагидро-1H,3H-пиридо[4',3':4,5]тиено[2,3-e][1,4]диазепин-2- он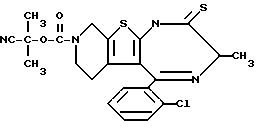
Смесь 0,4 г соединения препаративного примера 13, 0,7 г пентасульфида фосфора, 0,4 г гидрокарбоната натрия и 40 мл 1,2-диметоксиэтана кипятят с обратным холодильником 2 часа. После завершения реакции растворитель отгоняют, к остатку добавляют метанол, нерастворимое вещество отфильтровывают, фильтрат концентрируют. Очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью хлороформ - метанол (99:1) получают 0,3 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,5 - 2,0 (м, 2H), 1,76 (с, 6H), 1,92 (д, J = 7 Гц, 3H), 3,0 - 4,0 (м, 2H), 4,0 - 4,3 (м, 1H), 4,3 - 5,0 (м, 2H), 7,1 - 7,6 (м, 4H).
ПРИМЕР 75
3-(1-Циано-1-метилэтоксикарбонил)-(2-хлорфенил)-8,11-диметил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин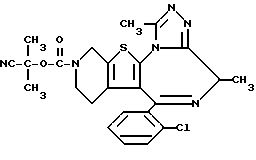
В 20 мл 1,4-диоксана растворяют 0,3 г соединения препаративного примера 14 и 0,3 г ацетогидразида и кипятят с обратным холодильником 3 часа. По окончании реакции растворитель отгоняют и очисткой остатка колоночной хроматографией с элюированием смесью хлороформ - метанол (99:1) получают 0,2 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,76 (с, 6H), 1,8 - 2,2 (м, 2H), 2,10 (д, 3H), 2,66 (с, 3H), 3,0 - 3,9 (м, 2H), 4,24 (к, 1H), 4,3 - 4,9 (м, 2H), 7,35 (м, 4H).
Препаративный пример 15
N-(3-Бутинилоксикарбонил)-4-гидроксипиперидин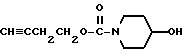
3-Бутинилфенилкарбонат (10 г) и 5,8 г 4-гидроксипиперидина нагревают без растворителя 30 минут при 100oC. После завершения реакции очисткой колоночной хроматографией на силикагеле с элюированием смесью гексан - этилацетат (1:1 - 1:2) получают 10,6 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,16 - 2,10 (м, 5H) 1,98 (т, J = 2 Гц, 1H), 1,42 (дв. т, J = 2 Гц, 7 Гц, 2H), 2,9 - 3,5 (м, 2H), 3,6 - 4,1 (м, 3H), 4,15 (т, J = 7 Гц, 2H).
Препаративный пример 16
N-(3-Бутинилоксикарбонил)-4-пиперидон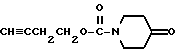
Смешивают 25 мл оксалилхлорида и 500 мл дихлорметана и к смеси постепенно по каплям в токе азота при температуре от -50oC до -70oC прибавляют 41 мл диметилсульфоксида, после чего к реакционной смеси по каплям прибавляют раствор N-(3-бутинилоксикарбонил)-5-гидроксипиперидина (10,3 г) в 50 мл дихлорметана. Наконец, по каплям прибавляют 120 мл триэтиламина и температуру медленно повышают до комнатной. Реакционную смесь переносят в насыщенный солевой раствор, трижды экстрагируют дихлорметаном и сушат над безводным сульфатом магния. Растворитель отгоняют при пониженном давлении и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью гексан - этилацетат (3:1) получают 8,9 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) 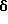 : 2,0 (т, J = 2 Гц, 1H), 2,3 - 2,8 (м, 6H), 3,76 (т, J = 7 Гц, 4H), 4,21 (т, J = 7 Гц, 2H).
: 2,0 (т, J = 2 Гц, 1H), 2,3 - 2,8 (м, 6H), 3,76 (т, J = 7 Гц, 4H), 4,21 (т, J = 7 Гц, 2H).
Препаративный пример 17
2-Амино-3-(2-хлорбензоил)-6-(3-бутинилоксикарбонил)-4,5,6,7- тетрагидротиено[2,3-c]пиридин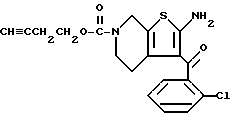
В 25 мл диметилформамида растворяют 7,4 г N-(3-бутинилоксикарбонил)-4-пиперидона, 1,21 г серы и 61,5 г 2-хлорцианоацетофенона, затем добавляют 3,5 мл триэтиламина и перемешивают 1 час при 60oC. По окончании реакции очисткой продукта колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 11,2 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,64 - 1,90 (м, 2H), 1,96 (т, J = 2 Гц, 1H), 2,3 - 2,7 (т, J = 2 Гц, 7 Гц, 2H), 3,4 (т, J = 7 Гц, 2H), 4,14 (т, J = 7 Гц, 2H), 4,3 - 4,5 (м, 2H), 7,0 - 7,5 (м, 6H).
Препаративный пример 18
2-(2-Бромпропиониламино)-3-(2-хлорбензоил)-6-(3-бутинилоксикарбонил) -4,5,6,7-тетрагидротиено[2,3-c]пиридин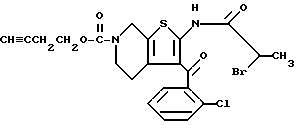
В 20 мл диоксана растворяют 1,35 г 2-амино-(2-хлорфенил)-6-(3-бутинилоксикарбонил)-4,5,6,7- тетрагидротиено[2,3-c]пиридина, к раствору добавляют 0,33 г пиридина, после чего при 0oC по каплям прибавляют 0,9 г 2-бромпропионилбромида. По окончании реакции реакционную смесь переносят в воду, экстрагируют дихлорметаном, сушат над безводным сульфатом магния, растворитель отгоняют при пониженном давлении и после очистки остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - гексан (1:1 - 1:0) получают 1,19 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 2,02 (т, J = 7 Гц, 3H), 1,7 - 2,2 (м, 3H), 3,5 (дв. т, J = 2 Гц, 7 Гц, 2H), 3,44 (т, J = 7 Гц, 2H), 4,16 (т, J = 7 Гц, 2H), 4,4 - 4,8 (м, 3H), 7,0 - 7,5 (м, 5H).
Препаративный пример 19
2-(2-Аминопропиониламино)-3-(2-хлорбензоил)-6-(3-бутинилоксикарбонил) -4,5,6,7-тетрагидротиено[2,3-c]пиридин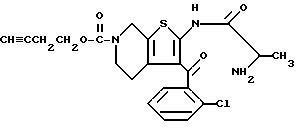
В 36 мл этилацетата растворяют 1,16 г 2-(2-бромпропионил)-3-(2-хлорбензоил)-6-(3-бутинилоксикарбонил)-4,5,6,7- тетрагидротиено[2,3-c]пиридина, раствор при охлаждении насыщают газообразным аммиаком, после чего нагревают при 100oC в запаянной пробирке. По окончании реакции продукт охлаждают, добавляют 50 мл этилацетата, промывают 1н. соляной кислотой, водную фазу нейтрализуют водным раствором карбоната натрия и экстрагируют хлороформом. Полученную органическую фазу сушат над безводным сульфатом магния, растворитель отгоняют при пониженном давлении и после очистки остатка колоночной хроматографией на силикагеле с элюированием дихлорметаном получают 0,36 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,5 (т, J = 7 Гц, 3H), 1,6 - 1,8 (уш. с, 2H), 1,8 - 2,1 (м, 3H), 2,52 (дв. т, J = 2 Гц, 7 Гц, 2H), 3,44 (т, J = 7 Гц, 2H), 3,76 (к, J = 7 Гц, 1H), 4,16 (т, J = 7 Гц, 2H), 4,50 - 4,64 (м, 2H), 7,1 - 7,7 (м, 5H).
Препаративный пример 20
3-Метил-5-(2-хлорфенил)-8-(3-бутинилоксикарбонил)-6,7,8,9- тетрагидро-1H,3H-пиридо[4',3':4,5]тиено[3,2-f][1,4]диазепин-2-он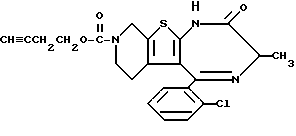
В 10 мл толуола и 0,8 мл пиридина растворяют 0,36 г 2-(2-аминопропиониламино)-3-(2-хлорбензоил)-6-(3-бутинилоксикарбонил)-4,5,6,7- тетрагидротиено[2,3-c]пиридина, к раствору добавляют 0,18 мл уксусной кислоты и кипятят с обратным холодильником с удалением воды. После завершения реакции толуол отгоняют при пониженном давлении, к отгоняемой реакционной смеси добавляют дихлорметан, затем промывают водой и сушат над безводным сульфатом магния. Отгонкой при пониженном давлении растворителя и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (100:0 - 97:3) получают 0,22 г заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,76 (д, J = 7 Гц, 3H), 1,6 - 2,2 (м, 3H), 2,5 (дв. т, J = 2 Гц, 7 Гц, 2H), 2,9 - 4,0 (м, 2H), 3,86 (к, J = 7 Гц, 1H), 4,17 (т, J = 7 Гц, 2H), 4,3 - 4,9 (м, 2H), 7,0 - 7,6 (м, 5H).
Препаративный пример 21
3-Метил-5-(2-хлорфенил)-8-(3-бутинилоксикарбонил)-6,7,8,9- тетрагидро-1H,3H-пиридо[4',3':4,5]тиено[3,2-f][1,4]диазепин-2-тион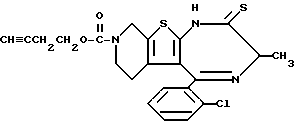
В 10 мл диметоксиэтана растворяют 0,21 г 3-метил-5-(2-хлорфенил)-8-(3-бутинилоксикарбонил)-6,7,8,9- тетрагидро-1H,3H-пиридо[4',3':4,5]тиено[3,2-f] [1,4] диазепин-2-она, к раствору добавляют 0,11 г гидрокарбоната натрия и 0,22 г пентасульфида фосфора и все нагревают 3 часа при 80oC. После окончания реакции добавляют дихлорметан и метанол, смесь отфильтровывают, к фильтрату добавляют силикагель и растворитель испаряют досуха. Колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 0,15 г очищенного целевого соединения.
1H-ЯМР (90 МГц, CDCl3) 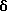 : 1,12 - 2,00 (м, 2H), 1,73 (д, J = 7 Гц, 3H), 2,12 (т, J = 2 Гц, 1H), 2,4 (дв. т, J = 2 Гц, 7 Гц, 2H), 2,64 - 3,80 (м, 2H), 4,01 (к, J = 7 Гц, 1H), 4,02 (т, J = 7 Гц, 2H), 4,10 - 4,76 (м, 2H), 7,28 (м, 2H).
: 1,12 - 2,00 (м, 2H), 1,73 (д, J = 7 Гц, 3H), 2,12 (т, J = 2 Гц, 1H), 2,4 (дв. т, J = 2 Гц, 7 Гц, 2H), 2,64 - 3,80 (м, 2H), 4,01 (к, J = 7 Гц, 1H), 4,02 (т, J = 7 Гц, 2H), 4,10 - 4,76 (м, 2H), 7,28 (м, 2H).
ПРИМЕР 76
3-(3-Бутинилоксикарбонил)-6-(2-хлорфенил)-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,4]триазоло[4,3-a][1,4]диазепин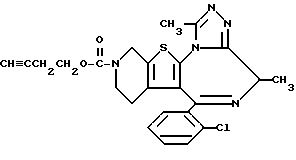
К 150 мг 3-метил-5-(2-хлорфенил)-8-(3-бутинилоксикарбонил)-6,7,8,9- тетрагидро-1H, 3H-пиридо[4', 3':4,5]тиено[3,2-f][1,4]диазепин-2-тиона добавляют 100 мг ацетогидразида, затем добавляют 2 мл диоксана и все нагревают 3 часа при 130oC с отгонкой растворителя. После завершения реакции очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (98:2) получают 80 мг целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 7,5 (4H, Ar), 4,9 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,5 (1H, д, J = 18 Гц, N-CH2(C-2)), 4,2 (1H, м, C8-H), 4,1 (2H, т, J = 8 Гц, O-CH2), 2,7 (3H, с), 2,5 (2H, дв. т, J = 1 Гц, 7 Гц, ≡ -CH2), 2,1 (3H, д, J = 7 Гц, CHCH), 3 - 2 (5H, м).
Препаративный пример 22
1-Циклопропанкарбонил-4-гидроксипиперидин
В 400 мл дихлорметана растворяют 20 г 4-гидроксипиперидина, к раствору добавляют 24 г триэтиламина, после чего при -60oC добавляют раствор 20,7 г циклопропанкарбонилхлорида в 100 мл дихлорметана. По окончании реакции реакционную смесь экстрагируют хлороформом в отсутствие соли, сушат над сульфатом магния и растворитель отгоняют при пониженном давлении. Очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием дихлорметаном получают 32 г (96%) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,55 - 1,55 (м, 4H), 1,15 - 2,15 (м, 5H), 2,4 (уш. с, 1H), 2,80 - 3,55 (м, 2H), 3,65 - 4,30 (м, 3H).
Препаративный пример 23
1-Циклопропанкарбонил-4-пиперидон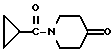
В 500 мл дихлорэтана растворяют 66 г оксалилхлорида, к раствору при -67oC по каплям прибавляют 61 г диметилсульфоксида, затем при той же температуре прибавляют раствор 44 г 1-циклопропанкарбонил-4-гидроксипиперидина по каплям и, наконец, при -67oC добавляют 131 г триэтиламина, после чего температуру повышают до комнатной. Образовавшуюся соль отфильтровывают, фильтрат концентрируют, к концентрату добавляют воду, экстрагируют этилацетатом и сушат над безводным сульфатом магния. Кроме того, водную фазу экстрагируют хлороформом и экстракт высушивают. Растворитель отгоняют при пониженном давлении и очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (3:7) получают 33 г (76%) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,65 - 1,20 (м, 4H), 1,6 - 2,0 (м, 1H), 2,49 (т, J = 6,1 Гц, 4H), 3,91 (т, J = 6,1 Гц, 4H).
Препаративный пример 24
2-Амино-3-(2-хлорбензоил)-6-циклопропанкарбонил-4,5,6,7- тетрагидротиено[2,3-c]пиридин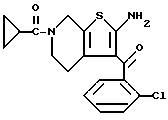
В 330 мл N,N-диметилформамида растворяют 33 г 1-циклопропанкарбонил-4-пиперидона, 6,3 г серы и 25,5 г 2-хлорцианоацетофенона и затем при 60oC добавляют 20 г триэтиламина. По окончании реакции растворитель отгоняют при пониженном давлении, к полученному остатку для его кристаллизации добавляют метанол, кристаллы отфильтровывают и после промывания метанолом получают 49,4 г (69%) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,55 - 1,15 (м, 4H), 1,4 - 2,0 (м, 3H), 3,35 - 3,75 (м, 2H), 4,3 - 4,7 (м, 2H), 7,0 - 7,7 (м, 4H).
Препаративный пример 25
2-(2-Бромпропиониламино)-3-(2-хлорбензоил)-6-циклопропанкарбонил- 4,5,6,7-тетрагидротиено[2,3-c]пиридин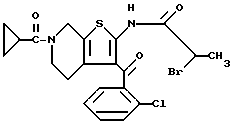
К 21,83 г 2-амино-3-(2-хлорбензоил)-6-циклопропанкарбонил)-4,5,6,7- тетрагидротиено[2,3-c]пиридина добавляют 450 мл толуола и 150 мл воды, затем добавляют 10,16 г гидрокарбоната натрия и при нагревании до 50 - 60oC добавляют 9,5 г 2-бромпропионилбромида. Для завершения реакции дополнительно добавляют водный раствор гидрокарбоната натрия (10,6 г гидрокарбоната натрия в 150 мл воды) и 5 мл 2-бромпропионилбромида. После окончания реакции добавляют этилацетат, реакционную смесь промывают один раз насыщенным солевым раствором, сушат над безводным сульфатом магния и после отгонки растворителя при пониженном давлении получают 29,9 г (количественный выход) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,55 - 1,20 (м, 4H), 1,6 - 2,2 (м, 3H), 1,99 (д, J = 7,2 Гц, 3H), 3,35 - 3,80 (м, 2H), 4,45 - 4,85 (м, 2H), 4,61 (к, J = 7,2 Гц, 1H), 7,0 - 7,6 (м, 4H).
Препаративный пример 26
2-(2-Аминопропиониламино)-3-(2-хлорбензоил)-6-циклопропанкарбонил-4,5,6,7- тетрагидротиено[2,3-c]пиридин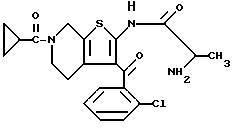
В 65 мл 1,2-дихлорэтана и 65 мл этилацетата растворяют 23,04 г 2-(2-бромпропиониламино)-3-(2-хлорбензоил)-6-циклопропанкарбонил-4,5,6,7- тетрагидротиено[2,3-c]пиридина и в полученный раствор пропускают газообразный аммиак 1 час при -15oC, после чего раствор помещают в запаянную ампулу и нагревают 2 часа при 100oC. Для завершения реакции через раствор вновь пропускают 30 минут при -15oC аммиак, после чего в запаянной ампуле нагревают еще 1,5 часа при 110oC. После охлаждения льдом реакционную смесь переносят в охлаждаемую льдом 2 н. соляную кислоту, добавляют этилацетат и водную фазу отделяют. К водной фазе добавляют при охлаждении льдом карбонат натрия с установлением pH 8, после чего экстрагируют хлороформом в обессоленных условиях. Экстракт промывают насыщенным солевым раствором, сушат над безводным сульфатом магния, фильтруют и после концентрирования получают 12,97 г (выход 64%) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,45 - 1,20 (м, 4H), 1,48 (д, J = 7,2 Гц, 3H), 1,4 - 2,4 (м, 3H), 3,35 - 3,85 (м, 2H), 3,74 (к, J = 7,2 Гц, 1H), 4,45 - 4,85 (м, 2H), 7,0 - 7,7 (м, 4H).
Препаративный пример 27
5-(2-Хлорфенил)-8-циклопропанкарбонил-3-метил-6,7,8,9- тетрагидро-1H, 3H-пиридо[4',3':4,5]тиено[3,2-f][1,4]диазепин-2-он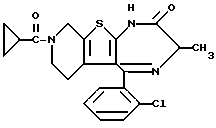
В 260 мл толуола и 90 мл пиридина растворяют 12,95 г 2-(2-аминопропиониламино)-3-(2-хлорбензоил)-6-циклопропанкарбонил-4,5,6,7- тетрагидротиено[2,3-c] пиридина, к раствору добавляют 5,4 г уксусной кислоты и кипятят с обратным холодильником 5 часов. После отгонки растворителя добавляют бензол и фильтрованием образовавшихся кристаллов получают 2,96 г целевого соединения. Колоночной хроматографией маточного раствора на силикагеле с элюированием смесью этилацетат-гексан (4:6) получают 3,84 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,50 - 1,25 (м, 4H), 1,3 - 2,3 (м, 3H), 1,75 (д, J = 6,5 Гц, 3H), 2,80 - 5,25 (м, 5H), 7,00 - 7,65 (м, 4H).
Препаративный пример 28
5-(2-Хлорфенил)-8-циклопропантиокарбонил-3-метил-6,7,8,9- тетрагидро-1H, 3H-пиридо[4',3':4,5]тиено[3,2-f][1,4]-диазепин-2-тион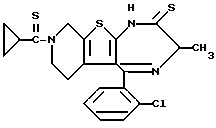
В 60 мл 1,2-диметоксиэтана суспендируют 2,92 г 5-(2-хлорфенил)-8-циклопропанкарбонил-3-метил-6,7,8,9- тетрагидро-1H, 3H-пиридо[4', 3': 4,5]тиено[3,2-f] [1,4] диазепин-2-она, к суспензии добавляют 1,78 г гидрокарбоната натрия и 3,92 г пентасульфида фосфора и кипятят с обратным холодильником 4 часа. Реакционную смесь фильтруют через целит, фильтровальный пирог тщательно промывают 30% смесью метанол - дихлорметан и промывной раствор объединяют с фильтратом. Объединенный фильтрат концентрируют и очисткой концентрата колоночной хроматографией на силикагеле с элюированием дихлорметаном получают 1,03 г целевого соединения (выход 33%).
1H-ЯМР (90 МГц, 10% CD3OD- CDCl3) δ: 0,80 - 1,55 (м, 4H), 1,60 - 2,75 (м, 3H), 2,0 (д, J = 6,1 Гц, 3H), 3,2 - 5,2 и 5,6 - 6,2 (оба м, всего 5H), 7,2 - 7,8 (м, 4H).
MS m/z (Pos. FAB): 446 (M+H)+.
Препаративный пример 29
6-(2-Хлорфенил)-3-циклопропантиокарбонил-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин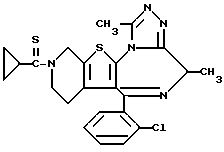
В 40 мл диоксана растворяют 1 г 5-(2-хлорфенил)-8-циклопропантиокарбонил-3-метил-6,7,8,9- тетрагидро-1H, 3H-пиридо[4', 3': 4,5]тиено[3,2-f][1,4] диазепин-2-тиона, к раствору добавляют 0,17 г ацетогидразида и все перемешивают 10 часов при 90oC и 1 час при 120oC. Дополнительно добавляют 0,17 г ацетогидразида и для завершения реакции перемешивают еще 1 час при 120oC. После отгонки растворителя и очистки остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 280 мг (выход 27:) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,75 - 1,75 (м, 4H), 1,75 - 2,60 (м, 3H), 2,1 (д, J = 6,8 Гц, 3H), 2,67 (с, 3H), 3,2 - 4,6 (м, 2H), 4,26 (к, J = 6,8 Гц, 1H), 4,65 - 5,40 и 5,55 - 6,0 (два м, всего 2H), 7,00 - 7,65 (м, 4H).
ПРИМЕР 77
6-(2-Хлорфенил)-3-циклопропанкарбонил-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4',3': 4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин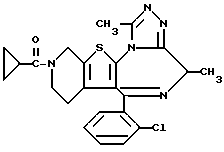
В 10 мл дихлорметана растворяют 100 мг 6-(2-хлорфенил)-3-циклопропантиокарбонил-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло [4,3-a][1,4]диазепина, к раствору добавляют 10 мл 4н. соляной кислоты, после чего прибавляют при перемешивании 1 мл водного раствора, содержащего 30 мг нитрита натрия. К охлажденному льдом раствору добавляют карбонат натрия с установлением pH 8, затем экстрагируют дихлорметаном, промывают насыщенным солевым раствором, сушат над безводным сульфатом магния, фильтруют, концентрируют и очисткой концентрата колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 69,9 мг (72%) целевого соединения.
1H-ЯМР (90 МГц, CDCl3) 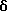 : 0,55 - 1,15 (м, 4H), 1,45 - 2,5 (м, 3H), 2,1 (д, J = 6,8 Гц, 3H), 2,66 (с, 3H), 2,8 - 4,8 (м, 3H), 4,26 (к, J = 6,8 Гц, 1H), 4,8 - 5,2 (м, 1H), 7,05 - 7,65 (м, 4H).
: 0,55 - 1,15 (м, 4H), 1,45 - 2,5 (м, 3H), 2,1 (д, J = 6,8 Гц, 3H), 2,66 (с, 3H), 2,8 - 4,8 (м, 3H), 4,26 (к, J = 6,8 Гц, 1H), 4,8 - 5,2 (м, 1H), 7,05 - 7,65 (м, 4H).
MS m/z (Pos. FAB: 452 (M + H)+.
ПРИМЕР 78
3-[2-(Тетрагидропиран-4-ил)оксиэтил] оксикарбонил-6-(2-хлорфенил)- 11-метил-2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин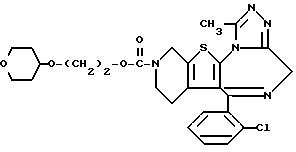
1H-ЯМР (90 МГц, CDCl3) δ: 1,3 - 2,4 (м, 6H), 2,68 (с, 3H), 2,8 - 5,7 (м, 15H), 7,20 - 7,54 (м, 4H).
ПРИМЕР 79
6-(2-Хлорфенил)-3-циклогексилэтоксикарбонил-11-метил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин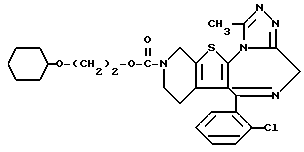
1H-ЯМР (90 МГц, CDCl3) δ: 0,6 - 2,3 (м, 15H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 4,0 - 4,4 (м, 1 + 2H), 4,4 - 4,8 (м, 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FAB: 524.
ПРИМЕР 80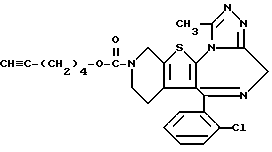
1H-ЯМР (90 МГц, CDCl3) δ: 1,20 - 2,32 (м, 6H), 1,94 (т, J = 2 Гц, 1H), 2,21 (дв. т, J = 2 Гц, 7 Гц, 2H), 2,66 (с, 3H), 2,84 - 5,76 (м, 6H), 4,08 (т, J = 7 Гц, 2H), 7,28 (м, 4H).
MS m/z (Pos. FAB: 495 (M+H)+.
ПРИМЕР 81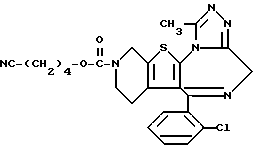
1H-ЯМР (90 МГц, CDCl3) δ: 1,40 - 2,21 (м, 6H), 2,37 (т, J = 7 Гц, 2H), 2,67 (с, 3H), 2,92 - 5,80 (м, 6H), 4,11 (т, J = 7 Гц, 2H), 7,31 (м, 4H).
MS m/z (Pos. FAB): 494 (M + H+).
Пример 82
6-(2-Хлорфенил)-3-(1-цианоэтокси)карбонил-11-метил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин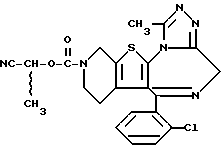
1H-ЯМР (90 МГц, CDCl3) 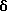 : 1,7 (т, J = 7 Гц, 3H), 1,75 (м, 1H), 2,15 (м, 1H), 2,69 (с, 3H), 3,25 (м, 1H), 3,85 (м, 1H), 4,2 (м, 1H), 4,53 (м, 1H), 4,85 (м, 1H), 5,43 (м, 1H), 5,65 (м, 1H), 7,23 - 7,65 (м, 4H).
: 1,7 (т, J = 7 Гц, 3H), 1,75 (м, 1H), 2,15 (м, 1H), 2,69 (с, 3H), 3,25 (м, 1H), 3,85 (м, 1H), 4,2 (м, 1H), 4,53 (м, 1H), 4,85 (м, 1H), 5,43 (м, 1H), 5,65 (м, 1H), 7,23 - 7,65 (м, 4H).
MS m/z (Pos. FAB): 467 (M+).
ПРИМЕР 83
6-(2-Хлорфенил)-3-циклобутилоксикарбонил-11-метил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин
1H-ЯМР (90 МГц, CDCl3) δ: 1,5 - 2,5 (м, 8H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 4,0 - 4,9 (м, 1 + 1 + 2H), 5,4 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FAB): 468
ПРИМЕР 84
6-(2-Хлорфенил)-3-(2-метил-3-цианопропилокси)карбонил-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a] [1,4]диазепин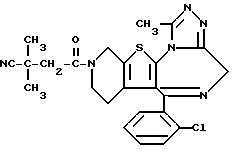
1H-ЯМР (90 МГц, CDCl3) δ: 1,35 (с, 3H), 1,45 (м, 3H), 1,75 (м, 1H), 2,12 (с, 1H), 2,7 (с, 3H), 3,25 (м, 1H), 3,9 (м, 1H), 4,08 (с, 2H), 4,22 (м, 1H), 4,55 (м, 1H), 4,56 (м, 1H), 5,62 (м, 1H), 7,30 - 7,45 (м, 4H).
MS m/z (Pos. FAB): 495 (M+).
ПРИМЕР 85
6-(2-Хлорфенил)-11-метил-3-(2-метилциклогексилоксикарбонил)- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин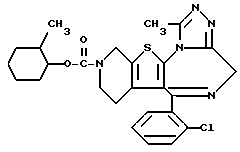
6-(2-Хлорфенил)-11-метил-3-(3-метилциклогексилоксикарбонил)- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин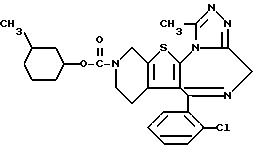
6-(2-Хлорфенил)-11-метил-3-(4-метилциклогексилоксикарбонил)- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин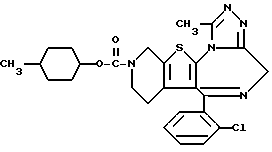
Вышеприведенные соединения имеют одинаковые значения в ЯМР-спектрах, приведенные ниже.
1H-ЯМР (90 МГц, CDCl3) δ: 0,7 - 1,0 (д, 3H), 1,0 - 2,2 (м, 11H), 2,7 (с, 3H), 3,0 - 4,0 (м, 2H), 4,0 - 4,9 (м, 1 + 1 + 2H), 5,3 - 5,8 (м, 1H), 7,4 (м, 4H).
MS m/z (Pos. FAB): 510.
Препаративный пример 30
3-Циклопропилпропионовая кислота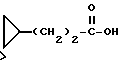
К 5,06 г этилового эфира 3-циклопропилакриловой кислоты добавляют 100 мл метанола, 100 мл тетрагидрофурана и 2 г 10% палладия на угле (содержит 50% воды), после чего в течение суток гидрируют при нормальной температуре и нормальном давлении. Катализатор отфильтровывают, растворитель отгоняют, к остатку добавляют 20 мл метанола, 20 мл тетрагидрофурана, 10 мл воды и 7 г гидроксида натрия и смесь перемешивают 3,5 часа при 80oC. После отгонки растворителя добавляют воду и промывают этилацетатом. К полученной водной фазе добавляют при охлаждении льдом водный раствор хлористоводородной кислоты до pH 3, затем экстрагируют хлороформом без добавления соли и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием дихлорметаном получают 1,8 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,65 - 1,10 (м, 2H), 1,10 - 1,85 (м, 5H), 2,33 (т, J = 7,2 Гц, 2H), 8,9 (уш. с, 1H).
ПРИМЕР 86
6-(2-Хлорфенил)-3-(3-циклопропил)пропионил-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин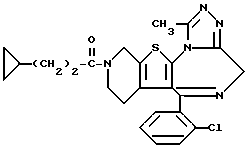
В 8 мл N,N-диметилформамида растворяют 50 мг 3-циклопропилпропионовой кислоты, 120 мг 6-(2-хлорфенил)-11-метил-2,3,4,5-тетрагидро-8H-пиридо[4',3': 4,5] тиено [3,2-f] [1,2,4] триазоло[4,3-a][1,4]диазепина и 60 г моногидрата 1-гидроксибензотриазола и к полученной смеси при охлаждении льдом добавляют 80 мг N,N'-дициклогексилкарбодиимида. После перемешивания в течение 10 минут смесь продолжают перемешивать сутки при 4oC. Затем перемешивают 1 час при комнатной температуре, растворитель отгоняют, к остатку от перегонки добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагель с элюированием смесью дихлорметан - метанол (1:99) получают 110 мг целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,70 - 1,05 (м, 3H), 1,05 - 2,40 (м, 6H), 2,27 (т, J = 7 Гц, 2H), 2,67 (с, 3H), 2,8 - 5,9 (м, 6H), 7,10 - 7,55 (м, 4H).
MS m/z (Pos. FAB)
ПРИМЕР 87
6-(2-Хлорфенил)-3-циннамоил-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин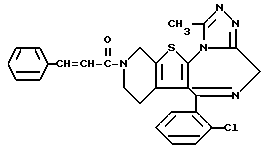
В 8 мл N,N-диметилформамида растворяют 80 мг циннамоилхлорида, к раствору добавляют 4 мл раствора 120 мг 6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепина и 160 мг триэтиламина в N,N-диметилформамиде (-60oC, по каплям) и все перемешивают в тех же условиях 30 минут. После отгонки растворителя добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор отфильтровывают, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью метанол - дихлорметан (1:99) получают 110 мг (68%) заглавного соединения.
1H-ЯМР (CDCl3) δ: 1,2 - 2,6 (м, 2H), 2,48 (с, 3H), 2,8 - 5,9 (м, 6H), 6,74 (т, J = 15,1 Гц, 1H), 7,1 - 7,7 (м, 9H), 7,64 (т, J = 15,1 Гц, 1H).
MS m/z (Pos. FAB): 500 (M + H)+.
ПРИМЕР 88
6-(2-Хлорфенил)-11-метил-3-(2-метилциклопропанкарбонил)- 2,3,4,5-тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин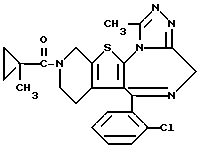
В 8 мл N,N-диметилформамида растворяют 50 мг 2-метилциклопропанкарбоновой кислоты, 130 мг 6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4]триазоло [4,3-a][1,4]диазепина и 70 мг моногидрата 1-гидроксибензотриазола, к раствору при охлаждении льдом добавляют 90 мг N,N'-дициклогексилкарбодиимида и все перемешивают 10 минут. Перемешивание продолжают сутки при 4oC и еще 1 час при комнатной температуре. После отгонки растворителя добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и после очистки полученного остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 120 мг (76%) целевого соединения.
1H-ЯМР (CDCl3) δ: 0,40 - 0,72 (м, 1H), 0,72 - 1,00 (м, 1H), 1,26 (с, 3H), 1,4 - 2,4 (м, 2H), 2,68 (с, 3H), 2,9 - 5,9 (м, 6H), 7,1 - 7,7 (м, 4H).
MS m/z (Pos. FAB): 452 (M + H)+.
ПРИМЕР 89
6-(2-Хлорфенил)-11-метил-3-фенилацетил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин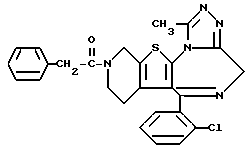
В 4 мл N,N-диметилформамида растворяют 120 мг 6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a] [1,4] диазепина и 160 мг триэтиламина и полученный раствор по каплям при -60oC прибавляют к раствору 60 мг хлорангидрида фенилуксусной кислоты в 5 мл N, N-диметилформамида. После окончания реакции растворитель отгоняют, к остатку добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 110 мг (69%) целевого соединения.
1H-ЯМР (CDCl3) δ: 1,0 - 2,6 (м, 2H), 2,61 и 2,66 (оба с, всего 3H), 2,8 - 6,0 (м, 6H), 3,69 и 3,77 (оба уш. с, всего 2H), 6,8 - 7,7 (м, 9H).
MS m/z (Pos. FAB): 488 (M + H)+.
ПРИМЕР 90
6-(2-Хлорфенил)-11-метил-3-(3-метилкротоноил)- 2,3,4,5-тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин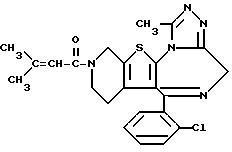
В 4 мл N,N-диметилформамида растворяют 120 мг 6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a] [1,4] диазепина и 160 мг триэтиламино и полученный раствор прибавляют при -60oC к раствору хлорангидрида 3-метилкротоновой кислоты (50 мг) в 5 мл N, N-диметилформамида. После завершения реакции растворитель отгоняют, к остатку добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 130 мг целевого соединения.
1H-ЯМР (CDCl3) 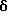 : 1,0 - 2,5 (м, 8H), 2,7 (с, 3H), 2,8 - 5,9 (м, 6H), 6,73 (уш. с, 1H), 7,1 - 7,6 (м, 4H).
: 1,0 - 2,5 (м, 8H), 2,7 (с, 3H), 2,8 - 5,9 (м, 6H), 6,73 (уш. с, 1H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 452 (M + H)+.
ПРИМЕР 91
6-(2-Хлорфенил)-11-метил-3-((транс)-2-фенилциклопропанкарбонил)- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a] [1,4]диазепин
В 12 мл N,N-диметилформамида растворяют 70 мг транс-2-фенил-1-циклопропанкарбоновой кислоты, 120 мг 6-(2-хлорфенил)-11-метил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепина и 60 мг моногидрата 1-гидроксибензотриазола и к полученному раствору при охлаждении льдом прибавляют 80 мг N,N'-дициклогексилкарбодиимида. После перемешивания в течение 10 минут смесь перемешивают сутки при 4oC и еще 1 час при комнатной температуре. Растворитель отгоняют, к остатку добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Сульфат отфильтровывают, растворитель отгоняют и очисткой полученного остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 160 мг целевого соединения.
1H-ЯМР (CDCl3) δ: 1,4 - 2,8 (м, 6H), 2,66 (с, 3H), 2,8 - 5,8 (м, 6H), 6,5 - 7,7 (м, 6H).
MS m/z (Pos. FAB): 514 (M + H)+.
ПРИМЕР 92
6-(2-Хлорфенил)-11-метил-3-(α-метилциннамоил)-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин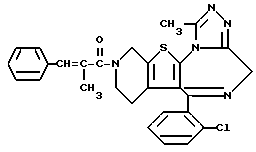
1H-ЯМР (CDCl3) δ: 1,7 - 2,5 (м, 2H), 2,14 (д, J = 4 Гц, 3H), 2,72 (с, 3H), 2,8 - 5,9 (м, 6H), 6,87 (к, J = 4 Гц, 1H), 7,0 - 7,7 (м, 9H).
MS m/z (Pos. FAB)
ПРИМЕР 93
6-(2-Хлорфенил)-11-метил-3-(4-пиридилтио)ацетил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин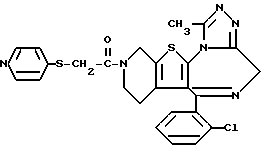
1H-ЯМР (CD3OD-CDCl3) δ: 1,4 - 2,6 (м, 2H), 2,68 (с, 3H), 2,8 - 5,9 (м, 6H), 3,82 (уш. с, 2H), 7,05 - 7,6 (м, 6H), 8,1 - 8,6 (м, 2H).
MS m/z (Pos. FAB): 521 (M + H)+.
ПРИМЕР 94
6-(2-Хлорфенил)-11-метил-3-(3-фенилпропионил)-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин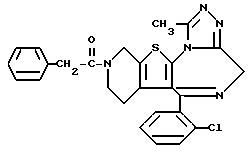
1H-ЯМР (CDCl3) δ: 1,0 - 2,3 (м, 4H), 2,66 (с, 3H), 2,65 - 3,15 (м, 2H), 2,8 - 5,9 (м, 6H), 6,65 - 7,65 (м, 9H).
MS m/z (Pos. FAB): 502 (M + H)+.
ПРИМЕР 95
6-(2-Хлорфенил)-11-метил-3-[3-(3-пиридил)акрилоил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин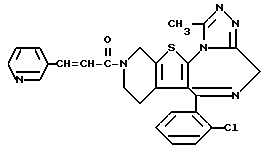
1H-ЯМР (CDCl3) 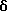 : 1,5 - 2,5 (м, 2H), 2,68 (с, 3H), 3,0 - 5,8 (м, 6H), 6,83 (уш. д, J = 15,5 Гц, 1H), 7,15 - 7,90 (м, 6H), 7,6 (д, J = 15,5 Гц, 1H), 8,3 - 8,5 (м, 1H), 8,64 (уш. с, 1H).
: 1,5 - 2,5 (м, 2H), 2,68 (с, 3H), 3,0 - 5,8 (м, 6H), 6,83 (уш. д, J = 15,5 Гц, 1H), 7,15 - 7,90 (м, 6H), 7,6 (д, J = 15,5 Гц, 1H), 8,3 - 8,5 (м, 1H), 8,64 (уш. с, 1H).
MS m/z (Pos. FAB): 501 (M + H)+.
ПРИМЕР 96
6-(2-Хлорфенил)-3-(3-циклогексилпропионил)-11-метил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин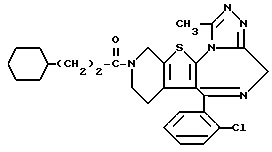
1H-ЯМР (CDCl3) δ: 0,6 - 2,5 (м, 15H), 2,28 (уш. т, J = 8 Гц, 2H), 2,66 (с, 3H), 2,8 - 5,9 (м, 6H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 508 (M + H)+.
ПРИМЕР 97
6-(2-Хлорфенил)-3-(4-фторфенил)ацетил-11-метил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин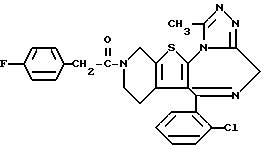
1H-ЯМР (CDCl3) δ: 1,0 - 2,4 (м, 2H), 2,66 (с, 3H), 2,8 - 5,9 (м, 6H), 3,65 (уш. с, 2H), 6,65 - 7,60 (м, 8H).
MS m/z (Pos. FAB): 506 (M + H)+.
ПРИМЕР 98
6-(2-Хлорфенил)-3-(4-цианобутаноил)-11 -метил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин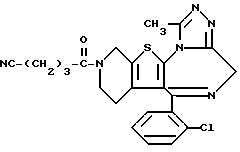
1H-ЯМР (CDCl3) δ: 1,4 - 2,3 (м, 4H), 2,30 - 2,65 (м, 4H), 2,67 (с, 3H), 2,8 - 5,8 (м, 6H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 465 (M + H)+.
Препаративный пример 31
Этиловый эфир тетрагидропиран-Δ4,a-уксусной кислоты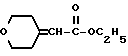
При охлаждении льдом к раствору 6,72 г (30 ммолей) диэтилфосфоэтилацетата в 100 мл диметилформамида добавляют 1,2 г (30 ммолей) гидрида натрия и перемешивают 10 минут. Затем к смеси при охлаждении льдом добавляют 2,5 г (25 ммолей) тетрагидро-4H-пиран-4-она, температуру повышают до комнатной и перемешивание продолжают 2 часа при 80oC. После окончания реакции добавляют этилацетат, промывают насыщенным солевым раствором и сушат над сульфатом магния. Раствор концентрируют при пониженном давлении и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью гексан - этилацетат (9:1) получают 4,2 г целевого продукта в виде светло-желтого маслянистого вещества.
1H-ЯМР (CDCl3) δ: 1,3 (т, J = 7,2 Гц, 3H), 2,0 - 2,3 (м, 2H), 3,0 (уш. с, 2H), 3,8 (т, J = 5,4 Гц, 2H), 4,0 - 4,3 (м, 2H), 4,1 (к, J = 7,2 Гц, 2H).
Препаративный пример 32
Этиловый эфир 4-тетрагидропиранилуксусной кислоты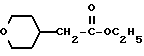
В 50 мл метанола растворяют 2 г этилового эфира тетрагидропиран-Δ4,a-уксусной кислоты, к раствору добавляют 10% палладий на угле и смесь гидрируют 3 часа. После фильтрования катализатора и концентрирования при пониженном давлении реакционной смеси получают 1,6 г целевого продукта.
1H-ЯМР (CDCl3) δ: 1,1 - 2,3 (м, 7H), 1,3 (т, J = 7,2 Гц, 3H), 3,2 - 3,6 (тр. д, J = 12,6 Гц, 2,9 Гц, 2H), 3,8 - 4,3 (м, 2H), 4,1 (к, J = 7,2 Гц, 2H).
Препаративный пример 33
4-Тетрагидропиранилуксусная кислота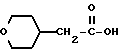
К 0,9 г этилового эфира 4-тетрагидропиранилуксусной кислоты добавляют 20 мл метанола, 10 мл воды и 1 г гидроксида натрия и перемешивают 1 час при 80oC. Растворитель отгоняют, к остатку добавляют воду, после промывания этилацетатом подкисляют водным раствором хлористоводородной кислоты до pH 3, экстрагируют хлороформом без добавления соли и сушат над безводным сульфатом магния. Раствор фильтруют и после отгонки растворителя получают 0,87 г сырого целевого продукта.
1H-ЯМР (CDCl3) 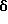 : 1,0 - 2,4 (м, 5H), 2,28 (уш. д, J = 6,5 Гц, 2H), 3,37 (тр. д, J = 11,5 Гц, 2,9 Гц, 2H), 3,7 - 4,1 (м, 2H), 7,85 (уш. с, 1H).
: 1,0 - 2,4 (м, 5H), 2,28 (уш. д, J = 6,5 Гц, 2H), 3,37 (тр. д, J = 11,5 Гц, 2,9 Гц, 2H), 3,7 - 4,1 (м, 2H), 7,85 (уш. с, 1H).
ПРИМЕР 99
6-(2-Хлорфенил)-11-метил-3-(тетрагидропиран-4-ил)ацетил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин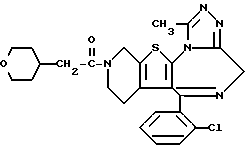
1H-ЯМР (CD3OD-CDCl3) δ: 0,9 - 2,4 (м, 9H), 2,67 (с, 3H), 2,8 - 5,9 (м, 10H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 496 (M+H)+.
Препаративный пример 34
Тетрагидропиран-Δ4,a-уксусная кислота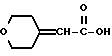
К 0,8 г этилового эфира тетрагидропиран- Δ4,a-уксусной кислоты добавляют 20 мл метанола, 10 мл воды и 1 г гидроксида натрия и смесь перемешивают 2 часа при 80oC. После отгонки растворителя к смеси добавляют воду и промывают этилацетатом. Водную фазу подкисляют соляной кислотой до кислой реакции, после чего экстрагируют этилацетатом в условиях, исключающих образование соли, и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и после очистки полученного остатка колоночной хроматографией на силикагеле с элюированием дихлорметаном получают 0,17 г (25%) целевого продукта.
1H-ЯМР (CD3OD-CDCl3) δ: 2,34 (уш. т, J = 5,4 Гц, 2H), 2,98 (уш. т, J = 5,4 Гц, 2H), 3,50 - 3,95 (м, 4H), 5,66 (уш. с, 1H), 8,45 (уш. с, 1H).
ПРИМЕР 100
6-(2-Хлорфенил)-11-метил-3-(тетрагидропиран-Δ4,a-ацетил)-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин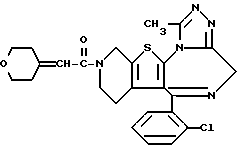
1H-ЯМР (CDCl3) δ: 1,4 - 2,5 (м, 2H), 2,10 - 2,41 (м, 2H), 2,41 - 2,80 (м, 2H), 2,67 (с, 3H), 2,8 - 5,9 (м, 6H), 3,45 - 3,90 (м, 4H), 5,72 (уш. с, 1H), 7,15 - 7,50 (м, 6H).
MS m/z (Pos. FAB): 494 (M + H)+.
ПРИМЕР 101
6-(2-Хлорфенил)-3-[(транс)-3-циклопропилакрилоил] -11-метил-2,3,4,5- тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин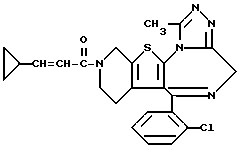
1H-ЯМР (CDCl3) δ: 0,40 - 1,15 (м, 4H), 1,2 - 2,6 (м, 3H), 2,66 (с, 3H), 2,8 - 6,0 (м, 6H), 6,13 (д, J = 21,6 Гц, 1H), 6,25 (дв. д, J = 21,6 Гц, 14,4 Гц, 1H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 464 (M+H)+.
ПРИМЕР 102
6-(2-Хлорфенил)-3-[(транс)-3-циклопропилакрилоил] -8,11-метил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,4]диазепин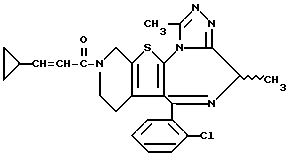
(1) Получение этилового эфира транс-3-циклопропилакриловой кислоты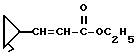
В 300 мл N,N-диметилформамида растворяют 38,38 г этилового эфира диэтилфосфоноуксусной кислоты, к раствору добавляют при 0oC 6,85 г гидрида натрия (60%), перемешивают 30 минут при комнатной температуре и при 0oC по каплям прибавляют 10 г циклопропанальдегида. После перемешивания 2 часа при комнатной температуре добавляют ледяную воду, затем экстрагируют эфиром, промывают водой и сушат над безводным сульфатом магния. Раствор фильтруют и очисткой концентрированного остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (2:98) получают 11,18 г (60%) заглавного соединения в виде транс-изомера.
1H-ЯМР (CDCl3) δ: 0,4 - 1,1 (м, 4H), 1,26 (т, J = 7,2 Гц, 3H), 1,3 - 1,8 (м, 1H), 4,13 (к, J = 7,2 Гц, 2H), 5,82 (д, J = 15,5 Гц, 1H), 6,37 (дв. д, J = 15,5 Гц, 10,1 Гц, 1H).
(2) Получение транс-3-циклопропилакриловой кислоты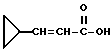
К полученному вышеприведенном способом этиловому эфиру транс-3-циклопропилакриловой кислоты (11,18 г) добавляют 100 мл метанола, 50 мл воды и 1 г гидроксида натрия и нагревают 1,5 часа при 80oC. После концентрирования для создания кислой среды добавляют концентрированную соляную кислоту, затем экстрагируют хлороформом, промывают насыщенным солевым раствором и сушат над безводным сульфатом магния. Сульфат отфильтровывают и после концентрирования получают 8,82 г (99%) целевого продукта.
1H-ЯМР (CDCl3) δ: 0,3 - 1,2 (м, 4H), 1,2 - 1,9 (м, 1H), 5,83 (д, J = 15,1 Гц, 1H), 6,47 (дв. д, J = 15,1 Гц, 6,5 Гц, 1H), 9,06 (уш. с, 1H).
(3) 6-(2-Хлорфенил)-3-[(транс)-3-циклопропилакрилоил] -8,11-диметил- 2,3,4,5-тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a] [1,4]диазепин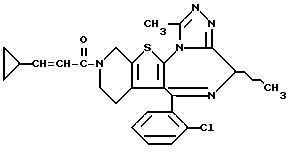
В 12 мл N,N-диметилформамида растворяют 90 мг транс-3-циклопропилакриловой кислоты, 120 мг моногидрата 1-гидроксибензотриазола и 240 мг 6-(2-хлорфенил)-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4', 3': 4,5]тиено[3,2-f] [1,2,4]триазоло [4,3-a][1,4]диазепина, к полученному раствору при охлаждении льдом добавляют 160 мг 1,3-дициклогексилкарбодиимида, после чего перемешивают 9 часов при 4oC и 1 час при комнатной температуре. После концентрирования добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, фильтрат концентрируют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью метанол - дихлорметан (1:99) получают 240 мг (выход 80%) целевого соединения.
1H-ЯМР (CDCl3) δ: 0,4 - 1,1 (м, 4H), 1,35 - 2,00 (м, 2H), 2,0 - 2,6 (м, 1H), 2,09 (д, J = 6,8 Гц, 3H), 2,65 (с, 3H), 2,8 - 4,1 (м, 2H), 4,1 - 5,3 (м, 2H), 4,26 (к, J = 6,8 Гц, 1H), 6,15 (дв. д, J = 19,8 Гц, 1H), 6,31 (дв. д, J = 19,8 Гц, 15,1 Гц, 1H), 7,10 - 7,55 (м, 4H).
MS m/z (Pos. FAB): 478 (M + N) +.
ПРИМЕР 103
6-(2-Хлорфенил)-3-циклобутанкарбонил-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин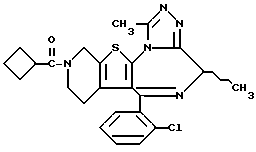
В 8 мл N,N-диметилформамида растворяют 40 мг циклобутанкарбоновой кислоты и 120 мг 6-(2-хлорфенил)-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4', 3': 4,5] тиено[3,2-f] [1,2,4] триазоло [4,3-a][1,4]диазепина и к полученному раствору при охлаждении льдом добавляют 80 мг 1,3-дициклогексилкарбодиимида, после чего перемешивают 9 часов при 4oC и 1 час при комнатной температуре. После концентрирования добавляют насыщенный водный раствор гидрокарбоната натрия, затем экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, концентрируют и очисткой концентрата колоночной хроматографией на силикагеле с элюированием смесью метанол - дихлорметан (1: 99) получают 120 мг (выход 82%) целевого соединения.
1H-ЯМР (CDCl3) δ: 1,2 - 2,8 (м, 8H), 2,09 (д, J = 6,8 Гц, 3H), 2,65 (с, 3H), 2,85 - 3,80 (м, 3H), 3,8 - 4,6 (м, 2H), 4,25 (к, J = 6,8 Гц, 1H), 4,8 - 5,3 (м, 1H), 7,0 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 466 (M+H)+.
ПРИМЕР 104
6-(2-Хлорфенил)-3-циклопентанкарбонил-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепин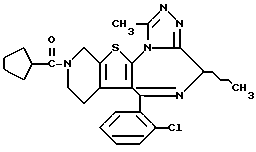
В 8 мл N, N-диметилформамида растворяют 50 мг циклопентанкарбоновой кислоты и 120 мг 6-(2-хлорфенил)-8,11-диметил-2,3,4,5- тетрагидро-8H-пиридо[4',3':4,5]тиено[3,2-f][1,2,4]триазоло [4,3-a][1,4]диазепина и к полученному раствору при охлаждении льдом добавляют 80 мг 1,3-дициклогексилкарбодиимида, после чего перемешивают 9 часов при 4oC и затем 1 час при комнатной температуре. После концентрирования добавляют насыщенный водный раствор гидрокарбоната натрия, затем экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, концентрируют и очисткой концентрата колоночной хроматографией на силикагеле с элюированием смесью метанол - дихлорметан (1:99) получают 110 мг (73%) целевого соединения.
1H-ЯМР (CDCl3) δ: 1,1 - 2,1 (м, 8H), 2,1 (д, J = 6,8 Гц, 3H), 2,1 - 3,1 (м, 1H), 2,66 (с, 3H), 3,1 - 4,0 (м, 2H), 4,0 - 5,3 (м, 2H), 4,26 (к, J = 6,8 Гц, 1H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 480 (M+H)+.
Препаративный пример 35
N-(Бензилоксикарбонил)-3-пирролидинол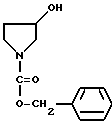
В 500 мл хлороформа растворяют 30 г 3-пирролидинола, к раствору добавляют 53 мл триэтиламина и затем при комнатной температуре по каплям постепенно прибавляют 52 мл бензилоксикарбонилхлорида. По окончании реакции реакционную смесь переносят в воду и экстрагируют хлороформом. Растворитель отгоняют при пониженном давлении и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью гексанэтилацетат получают 70,67 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 1,7 - 2,1 (м, 2H), 2,8 - 3,2 (м, 3H), 3,2 - 3,7 (м, 4H), 4,2 - 4,5 (м, 1H), 5,1 (с, 2H), 7,3 (с, 5H).
Препаративный пример 36
N-(Бензилоксикарбонил)-3-пирролидон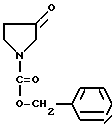
К раствору 150 мл хлорангидрида щавелевой кислоты в 2 литрах дихлорметилена постепенно в токе аргона при температуре от -70oC до -50oC прибавляют 245 мл диметилсульфоксида, затем по каплям прибавляют раствор 70,67 г N-(бензилоксикарбонил)-3-пирролидинола и после прибавления по каплям 720 мл триэтиламина температуру смеси повышают до комнатной. После окончания реакции реакционную смесь выливают в воду, экстрагируют дихлорметиленом, после чего растворитель отгоняют при пониженном давлении. Очисткой остатка колоночной хроматографией с элюированием смесью гексан - этилацетат получают 65,55 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 2,6 (т, J = 7,5 Гц, 2H), 3,7 - 4,0 (м, 4H), 5,12 (с, 2H), 7,3 (с, 5H).
Препаративный пример 37
2-Амино-3-(2-хлорбензоил)-5-бензилоксикарбонил-4,6- дигидротиено[2,3-c] пиррол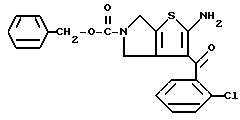
В 300 мл диметилформамида растворяют соединение препаративного примера 36 (66,55 г), 54,3 г 2-хлорцианоацетофенона и 9,9 г серы, к раствору добавляют 45 мл триэтиламина и смесь нагревают 2 часа при 60oC. По окончании реакции растворитель отгоняют при пониженном давлении и очисткой остатка колоночной хроматографией с элюированием смесью гексан - этилацетат получают 68,4 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 3,4 - 3,9 (м, 2H), 4,3 - 4,6 (м, 2H), 4,98 и 5,02 (оба с, всего 2H), 7,0 - 7,6 (м, 11H).
Препаративный пример 38
2-Бромацетиламино-3-(2-хлорбензоил)-5-бензилоксикарбонил-4,6-дигидротиено [2,3-c]пиррол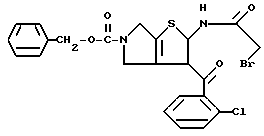
К смеси 600 мл толуола и 150 мл воды добавляют 68,4 г соединения препаративного примера 37, затем добавляют 33,5 г гидрокарбоната натрия, после чего при 60oC по каплям прибавляют 25 мл бромацетилбромида. По окончании реакции реакционную смесь выливают в дихлорметилен, промывают водой, растворитель отгоняют при пониженном давлении и полученный остаток применяют без дополнительной очистки в последующей реакции.
1H-ЯМР (90 МГц, CDCl3) δ: 3,50 - 3,95 (м, 2H), 4,08 (с, 2H), 4,3 - 4,7 (м, 2H), 5,03 и 5,07 (оба с, всего 2H), 7,0 - 7,6 (м, 10H).
Препаративный пример 39
2-Аминоацетиламино-3-(2-хлорбензоил)-5-бензилоксикарбонил- 4,6-дигидротиено [2,3-c]пиррол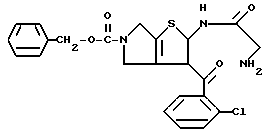
Соединение препаративного примера 38 растворяют в 3,5 литра этилацетата и раствор насыщают 8 часов газообразным аммиаком. Нерастворимые неорганические вещества отфильтровывают, полученный фильтрат разгоняют при пониженном давлении с удалением растворителя и фильтрованием образовавшихся кристаллов получают 41,9 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 3,3 - 3,9 (м, 4H), 4,4 - 4,7 (м, 2H), 5,02 и 5,06 (оба с, всего 2H), 7,0 - 7,5 (м, 11H).
Препаративный пример 40
5-(2-Хлорфенил)-7-бензилоксикарбонил- 6,8-дигидро-1H, 3H-пирроло[4',3': 4,5]тиено[3,2-f][1,4]диазепин-2-он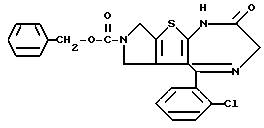
В смеси 250 мл бензола и 500 мл пиридина растворяют 38,5 г соединения препаративного примера 39, к раствору добавляют 5,2 мл уксусной кислоты и смесь нагревают при 120oC с удалением из системы образующейся воды. По окончании реакции реакционную смесь концентрируют при пониженном давлении и очисткой остатка колоночной хроматографией с элюированием смесью гексан - этилацетат получают 21 г целевого продукта.
1H-ЯМР (90 МГц, CDCl3) δ: 3,6 - 3,9 (м, 2H), 4,42 (с, 2H), 4,3 - 4,7 (м, 2H), 5,06 (с, 2H), 7,0 - 7,5 (м, 10H).
Препаративный пример 41
5-(2-Хлорфенил)-7-бензилоксикарбонил- 6,8-дигидро-1H, 3H-пирроло[4',3': 4,5]тиено[3,2-f][1,4]диазепин-2-тион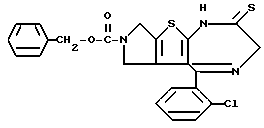
В 300 мл толуола растворяют 13,7 г соединения препаративного примера 40, к раствору добавляют реактив Ронсона [2,4-бис(4-метоксифенил)-1,3-дитиа-2,4-дифосфетан-2,4-дисульфид] и все нагревают 15 минут при 80oC. По окончании реакции растворитель отгоняют при пониженном давлении и очисткой остатка колоночной хроматографией с элюированием смесью гексан - этилацетат получают 9,3 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) 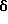 : 3,5 - 3,9 (м, 2H), 4,3 - 4,7 (м, 4H), 5,00 и 5,06 (оба с, всего 2H), 6,9 - 7,5 (м, 10H).
: 3,5 - 3,9 (м, 2H), 4,3 - 4,7 (м, 4H), 5,00 и 5,06 (оба с, всего 2H), 6,9 - 7,5 (м, 10H).
Препаративный пример 42
3-Бензилоксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f][1,2,4]триазоло[4,3-a] [1,4]диазепин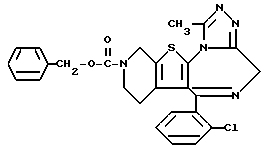
К 10,2 г соединения препаративного примера 41 добавляют 250 мл метанола, затем добавляют 4,8 мг моногидрата гидразина и все перемешивают 1 час при комнатной температуре. По окончании реакции осадок гидразида отфильтровывают, добавляют к нему 200 мл триэтил орто-ацетата и нагревают 40 минут при 80oC. По окончании реакции реакционную смесь концентрируют при пониженном давлении и очисткой концентрата колоночной хроматографией с элюированием смесью бензол - ацетат получают 7,39 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 2,7 (с, 3H), 3,6 - 3,9 (м, 2H), 4,6 - 4,8 (м, 2H), 4,8 - 5,0 (м, 2H), 5,05 и 5,09 (оба с, всего 2H), 7,0 - 7,5 (м, 9H).
Препаративный пример 43
3H-5-(2-Хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4', 3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин
К 3 мл дихлорметилена добавляют 0,23 г соединения препаративного примера 42, затем добавляют 0,7 мл иодтриметилсилана и перемешивают при комнатной температуре. По окончании реакции добавляют метанол, растворитель отгоняют при пониженном давлении и очисткой остатка колоночной хроматографией с элюированием смесью дихлорметилен - метанол - аммиак получают 0,1 г целевого соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 2,7 (с, 3H), 3,6 - 3,9 (м, 2H), 4,5 - 4,7 (м, 2H), 4,8 - 5,1 (м, 2H), 7,0 - 7,6 (м, 4H).
ПРИМЕР 105
3-(2'-Цианоэтил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин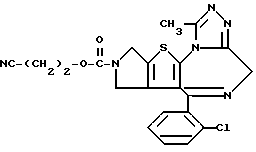
1H-ЯМР (CDCl3) δ: 2,67 (т, J = 7 Гц, 1H), 2,75 (т, J = 7 Гц, 1H), 2,75 (с, 3H), 3,64 - 3,90 (м, 2H), 4,25 (т, J = 7 Гц, 1H), 4,31 (т, J = 7 Гц, 1H), 4,64 - 4,82 (м, 2H), 4,80 - 5,12 (м, 2H), 7,26 - 7,46 (м, 4H).
MS m/z: 453.
ПРИМЕР 106
3-(3'-Бутинил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин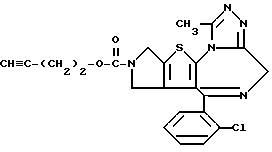
1H-ЯМР (CDCl3) δ: 2,0 (т, J = 7 Гц, 1H), 2,46 (дв. т, J = 7 Гц, 2 Гц, 1H), 2,55 (с, 3H), 2,75 (с, 3H), 3,60 - 3,75 (м, 2H), 4,14 (т, J = 7 Гц, 1H), 4,2 (т, J = 7 Гц, 1H), 4,60 - 4,85 (м, 2H), 4,75 - 5,10 (м, 2H), 7,10 - 7,54 (м, 4H).
MS m/z: 452.
ПРИМЕР 107
3-[2-(Морфолин-4-ил)этил] оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4', 3': 4,5] тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4] диазепин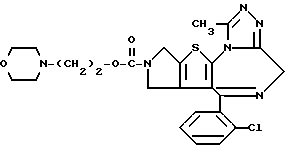
1H-ЯМР (CDCl3)  : 2,20 - 2,85 (м, 6H), 2,76 (с, 3H), 3,5 - 3,9 (м, 6H), 4,2 (т, J = 7 Гц, 1H), 4,28 (т, J = 7 Гц, 1H), 4,55 - 4,80 (м, 2H), 4,80 - 5,15 (м, 2H), 7,20 - 7,55 (м, 4H).
: 2,20 - 2,85 (м, 6H), 2,76 (с, 3H), 3,5 - 3,9 (м, 6H), 4,2 (т, J = 7 Гц, 1H), 4,28 (т, J = 7 Гц, 1H), 4,55 - 4,80 (м, 2H), 4,80 - 5,15 (м, 2H), 7,20 - 7,55 (м, 4H).
MS m/z: 513.
ПРИМЕР 108
3-(3-Пиридилэтил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин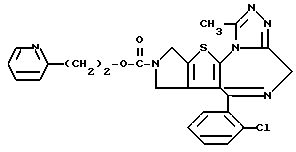
1H-ЯМР (CDCl3) δ: 2,72 (с, 3H), 3,04 (т, J = 7 Гц, 1H), 3,12 (т, J = 7 Гц, 1H), 3,48 - 3,85 (м, 2H), 4,30 - 4,80 (м, 4H), 4,70 - 5,18 (м, 2H), 4,70 - 5,18 (м, 2H), 6,95 - 7,70 (м, 7H), 8,40 - 8,56 (м, 1H).
MS m/z: 505.
ПРИМЕР 109
3-(Тетрагидропиран-4-ил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4', 3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин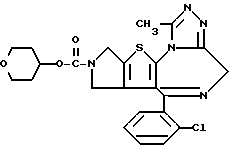
1H-ЯМР (CDCl3) δ: 1,4 - 2,3 (м, 4H), 2,74 (с, 3H), 3,32 - 4,05 (м, 7H), 4,60 - 5,08 (м, 4H), 7,20 - 7,56 (м, 4H).
MS m/z: 484.
ПРИМЕР 110
3-(3'-Бутин-2-ил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин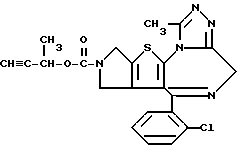
1H-ЯМР (CDCl3) δ: 1,54 (д, J = 7 Гц, 3H), 2,48 (д, J = 2 Гц, 1H), 2,72 (с, 3H), 3,60 - 3,86 (м, 2H), 4,60 - 4,82 (м, 2H), 4,78 - 5,10 (м, 2H), 5,18 - 5,46 (м, 1H), 7,12 - 7,54 (м, 4H).
MS m/z: 452.
ПРИМЕР 111
3-(3'-Морфолино-3'-оксопропил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H,7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4] диазепин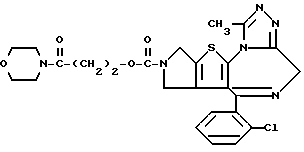
1H-ЯМР (CDCl3) δ: 2,50 - 2,83 (м, 2H), 2,72 (с, 3H), 3,32 - 3,85 (м, 10H), 4,34 (т, J = 7 Гц, 1H), 4,4 (т, J = 7 Гц, 1H), 4,52 - 4,80 (м, 2H), 4,72 - 5,10 (м, 2H), 7,20 - 7,52 (м, 4H).
ПРИМЕР 112
3-Циклогексилметилоксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин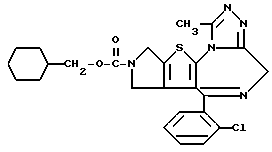
1H-ЯМР (CDCl3) 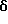 : 0,68 - 1,96 (м, 11H), 2,75 (с, 3H), 3,56 - 4,00 (м, 4H), 4,65 - 4,80 (м, 2H), 4,82 - 5,18 (м, 2H), 7,20 - 7,58 (м, 4H).
: 0,68 - 1,96 (м, 11H), 2,75 (с, 3H), 3,56 - 4,00 (м, 4H), 4,65 - 4,80 (м, 2H), 4,82 - 5,18 (м, 2H), 7,20 - 7,58 (м, 4H).
MS m/z: 496.
ПРИМЕР 113
3-Бензиламинокарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин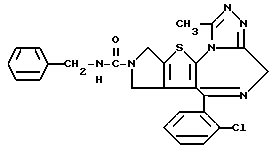
1H-ЯМР (CDCl3) δ: 2,68 (с, 3H), 3,60 - 3,94 (м, 2H), 4,36 (д, J = 5,4 Гц, 2H), 4,50 - 5,08 (м, 4H), 7,04 - 7,50 (м, 10H).
MS m/z: 489.
ПРИМЕР 114
3-(н-Гексил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин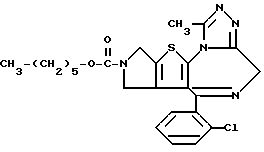
1H-ЯМР (CDCl3) δ: 0,75 - 1,04 (м, 3H), 1,1 - 1,8 (м, 8H), 2,72 (с, 3H), 3,54 - 3,84 (м, 2H), 4,02 (т, J = 7 Гц, 1H), 4,08 (т, J = 7 Гц, 1H), 4,58 - 4,80 (м, 2H), 4,78 - 5,10 (м, 2H), 7,20 - 7,48 (м, 4H).
MS m/z: 484.
ПРИМЕР 115
3-Фенэтилоксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин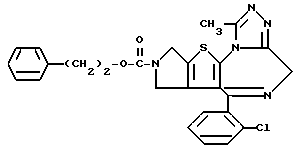
1H-ЯМР (CDCl3) δ: 2,72 (с, 3H), 2,86 (т, J = 7 Гц, 1H), 2,94 (т, J = 7 Гц, 1H), 3,55 - 3,84 (м, 2H), 4,24 (т, J = 7 Гц, 1H), 4,3 (т, J = 7 Гц, 1H), 4,50 - 4,75 (м, 2H), 4,78 - 5,10 (м, 2H), 6,98 - 7,50 (м, 9H).
MS m/z: 504.
ПРИМЕР 116
3-(4'-Хлорбензил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин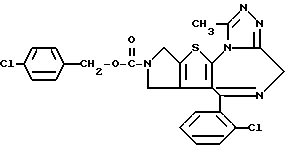
1H-ЯМР (CDCl3) δ: 2,72 (с, 3H), 3,60 - 3,92 (м, 2H), 4,6 - 4,8 (м, 2H), 4,80 - 5,04 (м, 2H), 5,08 (с, 2H), 7,26 (АВк, J = 6 Гц, 4H), 7,10 - 7,46 (м, 4H).
MS m/z: 524.
ПРИМЕР 117
3-(1'-Циано-1'-метилэтил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4', 3': 4,5] тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4] диазепин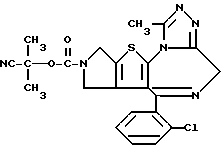
1H-ЯМР (CDCl3)  : 1,52 (с, 3H), 1,8 (c, 3H), 2,72 (c, 3H), 2,72 (c, 3H), 3,50 - 3,86 (м, 2H), 4,56 - 4,76 (м, 2H), 4,78 - 5,10 (м, 2H), 7,20 - 7,45 (м, 4H).
: 1,52 (с, 3H), 1,8 (c, 3H), 2,72 (c, 3H), 2,72 (c, 3H), 3,50 - 3,86 (м, 2H), 4,56 - 4,76 (м, 2H), 4,78 - 5,10 (м, 2H), 7,20 - 7,45 (м, 4H).
MS m/z: 467.
ПРИМЕР 118
3-(3'-Hитробензил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин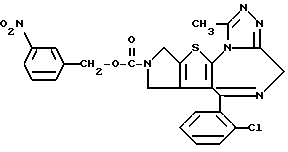
1H-ЯМР (CDCl3) δ: 2,72 (с, 3H), 3,66 - 3,88 (м, 2H), 4,67 - 4,82 (м, 2H), 4,82 - 5,08 (м, 2H), 5,18 (д, J = 2,8 Гц), 7,20 - 7,72 (м, 6H), 7,96 - 8,24 (м, 2H).
MS m/z: 535.
ПРИМЕР 119
3-(4'-Трифторметилбензил)оксикарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4', 3': 4,5] тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4] диазепин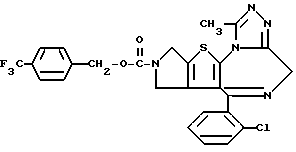
1H-ЯМР (CDCl3) δ: 2,76 (с, 3H), 3,70 - 3,92 (м, 2H), 4,70 - 4,86 (м, 2H), 4,88 - 5,10 (м, 2H), 5,22 (с, 2H), 7,25 - 7,60 (м, 4H), 7,56 (АВ к, J = 7 Гц, 4H).
MS m/z: 558.
ПРИМЕР 120
3-(2'-Цианоэтил)аминокарбонил-5-(2-хлорфенил)-10-метил- 2,4-дигидро-2H, 7H-пирроло[4',3':4,5]тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин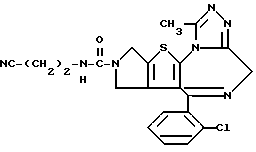
1H-ЯМР (CDCl3) δ: 2,6 (т, J = 7 Гц, 2H), 2,7 (с, 3H), 3,4 (т, J = 7 Гц, 1H), 3,46 (т, J = 7 Гц, 1H), 4,58 - 4,80 (м, 2H), 4,8 - 5,1 (м, 2H), 5,30 - 5,58 (м, 1H), 7,2 - 7,5 (м, 4H).
MS m/z: 452.
Препаративный пример 44
1-Бензилоксикарбонил-4-(2-гидроксиэтил)пиперидин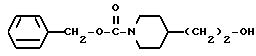
В 480 мл воды растворяют 50 г 4-пиперидинэтанола и 49,2 г гидрокарбоната натрия, к раствору при охлаждении льдом по каплям прибавляют 55,2 мл бензилоксикарбонилхлорида, после чего перемешивают в тех же условиях 1 час. Затем реакционную смесь экстрагируют хлороформом, сушат над безводным сульфатом магния, сульфат отфильтровывают, растворитель отгоняют и после очистки остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (30:70) получают 66 г (65%) заглавного соединения.
1H-ЯМР (CDCl3) δ: 0,75 - 1,85 (м, 7H), 2,5 - 3,0 (м, 2H), 3,4 - 3,8 (м, 2H), 3,9 - 4,3 (м, 2H), 5,11 (с, 2H), 7,1 - 7,4 (м, 5H).
Препаративный пример 45
1-Бензилоксикарбонил-4-(формилметил)пиперидин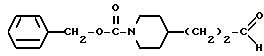 R
R
В одном литре дихлорметана растворяют 159 г хлорангидрида щавелевой кислоты, к раствору при -67oC по каплям прибавляют 195,8 г диметилсульфоксида и перемешивают 30 минут. Затем при -67oC по каплям прибавляют 66 г 1-бензилоксикарбонил-4-(2-гидроксиэтил)пиперидина в 200 мл дихлорметана и, наконец, при той же температуре по каплям прибавляют 380 г триэтиламина, после чего перемешивают 1 час. После отгонки растворителя добавляют этилацетат, нерастворимые вещества отфильтровывают, фильтрат промывают водой, сушат над безводным сульфатом магния, фильтруют и растворитель отгоняют. Очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (20:80) получают 55 г (84%) заглавного соединения.
1H-ЯМР (90 МГц: CDCl3) δ: 0,80 - 1,85 (м, 4H), 1,85 - 2,45 (м, 1H), 2,36 (дв. д, J = 6,1 Гц, 1,8 Гц, 2H), 2,5 - 3,0 (м, 2H), 3,90 - 4,35 (м, 2H), 5,07 (с, 2H), 7,1 - 7,5 (м, 5H), 9,67 (т, J = 1,8 Гц, 1H).
Препаративный пример 46
2-Амино-5-[4-(1-бензилоксикарбонил)пиперидил]-3-(2-хлорбензоил)тиофен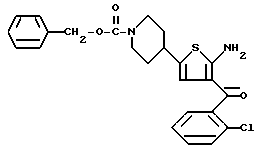
В 250 мл N,N-диметилформамида суспендируют 55 г 1-бензилоксикарбонил-4-(формилметил)пиперидина, 6,75 г серы и 38,87 г 2-хлорцианоацетофенона, к суспензии при 40oC прибавляют 7,75 г триэтиламина и перемешивают 1,5 часа. После отгонки растворителя добавляют этилацетат, промывают водой и затем насыщенным солевым раствором, сушат над сульфатом магния, фильтруют и растворитель отгоняют. Очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (30:70) получают 67,9 г (выход 76%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) 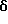 : 1,15 - 2,10 (м, 4H), 3,40 - 4,05 (м, 3H), 3,95 - 4,35 (м, 2H), 5,06 (с, 2H), 6,04 (уш. с, 1H), 6,94 (уш. с, 2H), 7,10 - 7,55 (м, 9H).
: 1,15 - 2,10 (м, 4H), 3,40 - 4,05 (м, 3H), 3,95 - 4,35 (м, 2H), 5,06 (с, 2H), 6,04 (уш. с, 1H), 6,94 (уш. с, 2H), 7,10 - 7,55 (м, 9H).
Препаративный пример 47
2-[4-(1-Бензилоксикарбонил)пиперидил]-5-(бромацетиламино)-4- (2-хлорбензоил)тиофен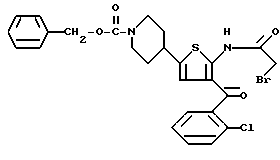
К соединению препаративного примера 46 (67,9 г) добавляют 1,5 литра толуола, 350 мл воды и 27 г гидрокарбоната натрия, затем при 60oC добавляют 48,61 г бромангидрида бромуксусной кислоты. По окончании реакции добавляют этилацетат, органическую фазу отделяют, промывают насыщенным солевым раствором и сушат над безводным сульфатом магния. Раствор фильтруют и после отгонки растворителя получают заглавное соединение.
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 - 2,2 (м, 4H), 2,55 - 3,05 (м, 3H), 4,07 (с, 2H), 4,00 - 4,45 (м, 2H), 5,06 (с, 2H), 6,36 (уш. с, 1H), 7,1 - 7,6 (м, 9H), 12,47 (уш. с, 1H).
Препаративный пример 48
2-(Аминоацетиламино)-5-[4-(1-бензилоксикарбонил)пиперидил] -3- (2-хлорбензоил)тиофен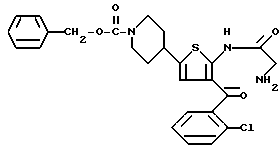
Ко всему количеству соединения препаративного примера 47 добавляют 2 литра этилацетата, в раствор при перемешивании и комнатной температуре 3 часа пропускают газообразный аммиак, после чего перемешивание продолжают еще 12 часов. После пропускания в течение 30 минут газообразного азота органическую фазу отделяют с исключением образования соли, образовавшуюся водную фазу экстрагируют с исключением образования соли. Обе органические фазы сушат над безводным сульфатом магния, раствор фильтруют и после отгонки растворителя получают заглавное соединение.
1H-ЯМР (90 МГц, CDCl3) δ: 1,10 - 2,15 (м, 4H), 2,50 - 3,05 (м, 3H), 4,61 (уш. с, 2H), 3,9 - 4,4 (м, 2H), 5,06 (с, 2H), 6,32 (уш. с, 1H), 7,1 - 7,6 (м, 9H).
Препаративный пример 49
2-[4-(1-Бензилоксикарбонил)пиперидил] -4-(2-хлорфенил)тиено [3,2-f][1,4] диазепин-7-он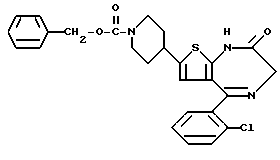
Ко всему количеству соединения препаративного примера 48 добавляют 600 мл бензола, 1,5 литра пиридина и 9,6 г уксусной кислоты, после чего смесь кипятят с удалением из системы воды. После отгонки растворителя очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (60:40) получают 61,21 г заглавного соединения (полный выход на всех трех стадиях 77%).
1H-ЯМР (90 МГц, CDCl3) δ: 1,00 - 2,15 (м, 4H), 2,35 - 3,00 (м, 3H), 3,9 - 4,4 (м, 2H), 4,43 (м, 2H), 5,07 (с, 2H), 6,16 (уш. с, 1H), 7,05 - 7,55 (м, 9H), 8,93 (уш. с, 1H).
Препаративный пример 50
2-[4-(1-Бензилоксикарбонил)пиперидил] -4-(2-хлорфенил)тиено [3,2-f][1,4] диазепин-7-тион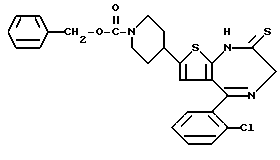
Смесь 61,21 г соединения препаративного примера 49, 13,53 г гидрокарбоната натрия и 27,54 г пентасульфида фосфора суспендируют в 1 литре 1,2-диметоксиэтана и перемешивают 1,5 часа при 80oC. Реакционную смесь фильтруют через целитовую мембрану, образовавшийся фильтрованльный пирог промывают смесью хлороформа с метанолом (≈7:3), промывной раствор объединяют с фильтратом, растворитель отгоняют и очисткой остатка колоночной хроматографией с элюированием дихлорметаном, содержащим 2 - 8% метанола, получают 62,6 г (99%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,15 - 2,10 (м, 4H), 2,5 - 3,1 (м, 3H), 3,95 - 4,45 (м, 2H), 4,83 (уш. с, 2H), 5,07 (уш. с, 2H), 6,18 (уш. с, 1H), 7,0 - 7,6 (м, 9H).
Препаративный пример 51
2-[4-(1-Бензилоксикарбонил)пиперидил] -4-(2-хлорфенил)-9-метил-6H-тиено [3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин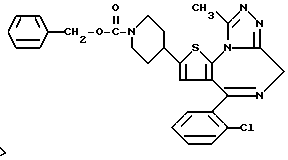
В 3,5 литра метанола суспендируют 62,6 г соединения препаративного примера 50, к суспензии добавляют 33,5 г моногидрата гидразина, после чего перемешивают 1 час при комнатной температуре и 1 час при 80oC. После удаления растворителя отгонкой и очистки остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (98:2) получают 21,5 г (33%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,2 - 2,2 (м, 4H), 2,60 - 3,05 (м, 3H), 2,67 (с, 2H), 4,0 - 4,4 (м, 2H), 4,88 (уш. с, 2H), 5,07 (уш. с, 2H), 6,34 (уш. с, 1H), 7,1 - 7,5 (м, 9H).
Препаративный пример 52
4-(2-Хлорфенил)-9-метил-2-(4-пиперидил)-6H-тиено [3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин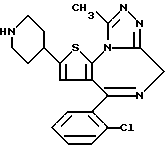
В 140 мл дихлорметана растворяют 6,65 г соединения препаративного примера 51, к раствору в токе азота добавляют 17 мл триметилсилилиодида и перемешивают 25 минут в токе азота. После охлаждения добавляют 40 мл метанола, затем растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол - триэтиламин (94,5: 5:0,5) получают 4,45 г (90%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,10 - 2,05 (м, 4H), 2,35 - 3,20 (м, 5H), 2,6 (с, 3H), 4,77 (уш. с, 2H), 6,37 (уш. с, 1H), 7,2 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 398 (M + H)+.
ПРИМЕР 121
4-(2-Хлорфенил)-9-метил-2-[4-(1-фенилпропиолилпиперидил)] -6H -тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин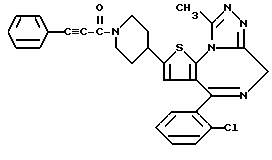
Смесь 50 мг фенилпропиоловой кислоты, 110 мг производного пиперидина препаративного примера 52 и 50 мг 1-гидроксибензотриазола растворяют в 8 мл N, N-диметилформамида, к раствору при охлаждении льдом прибавляют 70 мг N, N'-дициклогексилкарбодиимида, после чего перемешивают сутки при 4oC и затем 1 час при комнатной температуре. После отгонки растворителя к остатку добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 130 мг (89%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,4 (м, 4H), 2,55 - 3,50 (м, 3H), 2,68 (с, 3H), 4,35 - 4,90 (м, 2H), 4,88 (уш. с, 2H), 6,37 (уш. с, 1H), 7,05 - 7,65 (м, 8H).
MS m/z (Pos. FAB): 526 (M + H)+.
ПРИМЕР 122
4-(2-Хлорфенил)-2-[4-{ 1-(3-цианопропионил)пиперидил} ]-9-метил-6H -тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин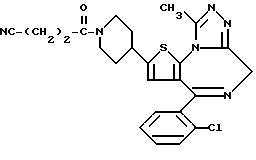
К 1 г метилового эфира 3-цианопропионовой кислоты добавляют 10 мл метанола, 1 мл воды и 1,34 г карбоната калия и перемешивают 2 часа при 60oC. После отгонки растворителя добавляют хлороформ, нерастворимые вещества отфильтровывают и промывают хлороформом. К кристаллам добавляют метанол, нерастворимые вещества отфильтровывают и после отгонки растворителя получают 1,31 г калиевой соли 3-цианопропионовой кислоты в смеси с неорганической солью.
В 10 мл N,N-диметилформамида растворяют 100 мг вышеполученной смеси, 150 мг производного пиперидина препаративного примера 52 и моногидрат 1-гидроксибензотриазола (80 мг), после чего при охлаждении льдом прибавляют 80 мг N,N'-дициклогексилкарбодиимида и перемешивают сутки при 4oC и 4 часа при комнатной температуре. После отгонки растворителя добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой остатка на колонке с силикагелем с элюированием смесью дихлорметан - метанол (99:1) получают 140 мг (выход 78%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 - 2,3 (м, 4H), 2,67 (с, 3H), 2,4 - 3,4 (м, 3H), 3,5 - 4,2 (м, 2H), 4,4 - 5,9 (м, 1H), 4,88 (уш. с, 2H), 6,35 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 479 (M + H)+.
ПРИМЕР 123
4-(2-Хлорфенил)-9-метил-2-[4-(1-морфолиноацетилпиперидил)] -6H-тиено [3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин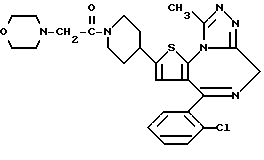
В 4 мл N,N-диметилформамида растворяют 150 мг производного пиперидина препаративного примера 52 и 150 мг триэтиламина и полученный раствор при -60oC прибавляют по каплям к раствору 60 мг хлорацетилхлорида в 4 мл N,N-диметилформамида. По окончании реакции добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, из фильтрата отгоняют только хлороформ, к остатку добавляют 40 мг морфолина и 100 мг карбоната калия и перемешивают 1,5 часа при 60oC. После отгонки растворителя добавляют воду, экстрагируют хлороформом и сушат над безводным сульфатом магния. Экстракт фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (98:2) получают 130 мг заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) 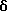 : 1,20 - 2,25 (м, 4H), 2,30 - 2,65 (м, 4H), 2,68 (с, 3H), 2,65 - 3,40 (м, 5H), 3,5 - 3,8 (м, 4H), 3,95 - 4,36 (м, 1H), 4,36 - 4,90 (м, 1H), 4,89 (с, 2H), 6,35 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
: 1,20 - 2,25 (м, 4H), 2,30 - 2,65 (м, 4H), 2,68 (с, 3H), 2,65 - 3,40 (м, 5H), 3,5 - 3,8 (м, 4H), 3,95 - 4,36 (м, 1H), 4,36 - 4,90 (м, 1H), 4,89 (с, 2H), 6,35 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 525 (M + H)+.
ПРИМЕР 124
4-(2-Хлорфенил)-9-метил-2-[4-{ 1-(4-пентиноил)пиперидил} ] -6H-тиено [3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин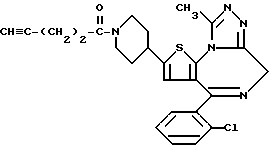
В 10 мл N,N-диметилформамида растворяют 40 мг 4-пентиновой кислоты, 150 мг производного пиперидина препаративного примера 52 и 60 мг моногидрата 1-гидроксибензотриазола, после чего при охлаждении льдом добавляют 80 мг N, N'-дициклогексилкарбодиимида и перемешивают сутки при 4oC и 6 часов при комнатной температуре. После отгонки растворителя добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 140 мг (78%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,3 - 2,3 (м, 5H), 2,3 - 2,7 (м, 4H), 2,5 - 3,4 (м, 3H), 2,67 (с, 3H), 3,65 - 4,15 (м, 1H), 4,4 - 5,0 (м, 1H), 4,88 (уш. с, 2H), 6,35 (уш. с, 1H), 7,05 - 7,60 (м, 4H).
MS m/z (Pos. FAB): 478 (M + H)+.
ПРИМЕР 125
2-[4-{ 1-(4-Бромфенилацетил)пиперидил}]-4-(2-хлорфенил)-9-метил-6H-тиено [3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин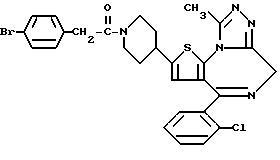
Воспроизведена методика примера 121, но с использованием 4-бромфенилуксусной кислоты.
1H-ЯМР (90 МГц, CDCl3) δ: 1,15 - 2,20 (м, 4H), 2,49 - 3,30 (м, 5H), 2,87 (с, 3H), 3,55 - 4,10 (м, 1H), 4,45 - 5,00 (м, 1H), 4,88 (уш. с, 2H), 6,34 (уш. с, 1H), 6,60 - 7,11 (м, 4H), 7,11 - 7,60 (м, 4H).
MS m/z (Pos. FAB): 596 [(M + H)+, Cl = 35, Br = 81].
ПРИМЕР 126
4-(2-Хлорфенил)-2-[4-(1-цианоацетилпиперидил)] -9-метил-6H-тиено [3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин
Воспроизведена методика примера 121, но с использованием цианоуксусной кислоты.
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,4 (м, 4H), 2,45 - 3,55 (м, 3H), 2,67 (с, 3H), 3,47 (с, 2H), 3,55 - 4,00 (м, 1H), 4,4 - 4,9 (м, 1H), 4,87 (уш. с, 2H), 6,37 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 465 (M + H)+.
ПРИМЕР 127
4-(2-Хлорфенил)-9-метил-2-[4-[{ 4-(2-тиенил)пропионил} пиперидил] ]-6H-тиено [3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин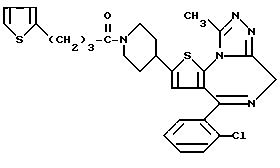
Воспроизведена методика примера 121, но с использованием 4-(2-тиенил)бутановой кислоты.
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 - 2,2 (м, 6H), 2,40 - 3,32 (м, 3H), 2,67 (с, 3H), 3,32 - 4,45 (м, 4H), 4,45 - 5,05 (м, 2H), 4,88 (уш. с, 2H), 6,32 (уш. с, 1H), 6,95 - 7,60 (м, 7H).
MS m/z (Pos. FAB): 550 (M + H)+.
ПРИМЕР 128
4-(2-Хлорфенил)-2-[4-(1-циклопропанкарбонилпиперидил)] -9-метил-тиено [3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин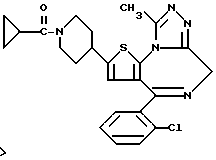
В 5 мл N,N-диметилформамила растворяют 700 мг производного пиперидина препаративного примера 52 и 900 мг триэтиламина и к полученному раствору при -60oC по каплям прибавляют раствор 650 мг 3-бромпропионилхлорида в 10 мл N, N-диметилформамида. После отгонки растворителя добавляют насыщенный водный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и после очистки остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 400 мг (49%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,60 - 1,15 (м, 4H), 1,20 - 2,25 (м, 5H), 2,4 - 3,5 (м, 3H), 2,68 (с, 3H), 3,7 - 5,0 (м, 2H), 4,89 (уш. с, 2H), 6,36 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
ПРИМЕР 129
4-(2-Хлорфенил)-9-метил-2-[4-(1-пентаноил)пиперидил] -6H-тиено [3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин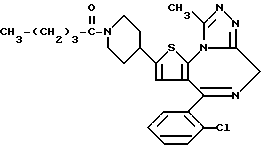
Воспроизведена методика примера 121, но при использовании хлорангидрида валериановой кислоты.
1H-ЯМР (90 МГц, CDCl3) δ: 0,91 (т, J = 6,5 Гц, 3H), 1,1 - 2,3 (м, 3H), 2,31 (т, J = 7,2 Гц, 2H), 2,67 (с, 3H), 2,5 - 3,4 (м, 3H), 3,7 - 4,2 (м, 1H), 4,45 - 5,00 (м, 1H), 4,88 (уш. с, 2H), 6,35 (уш. с, 2H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 482 (M + N)+.
ПРИМЕР 130
4-(2-Хлорфенил)-9-метил-2-[4-(1-октаноил)пиперидил] -6H-тиено [3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин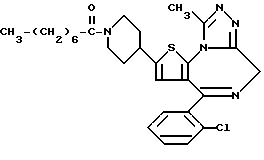
Воспроизведена методика примера 121, но при использовании октаноилхлорида.
1H-ЯМР (90 МГц, CDCl3) δ: 0,7 - 1,1 (м, 3H), 1,1 - 2,5 (м, 14H), 2,31 (т, J = 7,5 Гц, 2H), 2,68 (с, 3H), 2,50 - 3,35 (м, 3H), 3,70 - 4,15 (м, 1H), 4,45 - 5,0 (м, 1H), 4,88 (уш. с, 2H), 6,35 (уш. с, 2H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 524 (M + H)+.
ПРИМЕР 131
4-(2-Хлорфенил)-2-[4-(1-метоксиацетилпиперидил]-9-метил-6H-тиено [3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин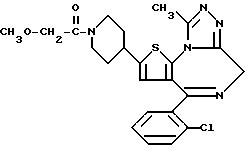
Соединение синтезировано по методике примера 121, но при использовании хлорангидрида метоксиуксусной кислоты.
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 2,3 (м, 4H), 2,4 - 3,2 (м, 3H), 2,68 (с, 3H), 3,39 (с, 3H), 3,7 - 4,2 (м, 1H), 4,06 (с, 2H), 4,4 - 4,9 (м, 1H), 4,89 (м, 1H), 6,36 (уш. с, 1H), 7,10 - 7,55 (м, 4H).
MS m/z (Pos. FAB): 470 (M + H)+.
Препаративный пример 53
2-Морфолиноэтилфенилкарбонат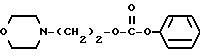
В 40 мл дихлорэтана растворяют 2 г 4-(2-гидроксиэтил)морфолина и 3,6 г пиридина, затем к раствору при охлаждении льдом по каплям прибавляют 5,97 г фенилхлорформата и перемешивают в тех же условиях 30 минут. Добавляют насыщенный водный раствор гидрокарбоната натрия, органическую фазу отделяют, водную фазу экстрагируют и экстракт объединяют с органической фазой, затем промывают насыщенным солевым раствором и сушат над безводным сульфатом магния, Раствор фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (3:70) получают 3,39 г (89%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 2,35 - 2,70 (м, 4H), 2,69 (т, J = 6,1 Гц, 2H), 3,55 - 3,85 (м, 4H), 4,34 (м, 4H), 4,34 (т, J = 6,1 Гц, 2H), 6,95 - 7,50 (м, 4H).
ПРИМЕР 132
4-(2-Хлорфенил)-9-метил-2-[4-(2-морфолиноэтилоксикарбонил)пиперидил] - 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин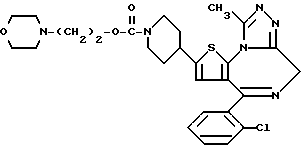
В 6 мл хлороформа растворяют 170 мг производного пиперидина препаративного примера 52 и 290 мг 2-морфолиноэтилфенилкарбоната и полученный раствор упаривают при перемешивании и 80oC досуха. Снова добавляют хлороформ и упаривание досуха повторяют дважды или трижды, добиваясь полноты реакции. Полученный продукт подвергают колоночной хроматографии на силикагеле с элюированием смесью дихлорметан - метанол (97:3), к полученным фракциям добавляют дихлорметан, из которых декантированием отделяют нерастворимые вещества. После отгонки дихлорметана вновь в небольшом количестве добавляют дихлорметан и снова отделяют нерастворимые вещества, после чего в результате отгонки дихлорметана получают 170 мг заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,2 - 2,2 (м, 4H), 2,25 - 3,15 (м, 7H), 2,54 (т, J = 6,1 Гц, 2H), 2,68 (с, 3H), 3,55 (м, 4H), 3,95 - 4,45 (м, 2H), 4,18 (т, J = 6,1 Гц, 2H), 4,89 (уш. с, 2H), 6,36 (уш. с, 1H), 7,10 - 7,55 (м, 4H).
MS m/z (Pos. FAB): 555 (M + H)+.
Препаративный пример 54
2-Цианоэтилфенилкарбонат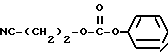
Соединение синтезировано по методике препаративного примера 53.
1H-ЯМР (90 МГц, CDCl3) δ: 4,83 (с, 2H), 6,9 - 7,5 (м, 5H).
ПРИМЕР 133
4-(2-Хлорфенил)-2-[4-{ 1-(2-цианоэтилоксикарбонил)пиперидил}]- 9-метил-6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин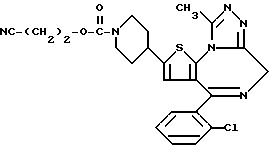
В 5 мл хлороформа растворяют 150 мг производного пиперидина препаративного примера 52 и 180 мг 2-цианоэтилфенилкарбоната и полученный раствор упаривают досуха при перемешивании нагреванием от комнатной температуры до 110oC. Операцию с добавлением хлороформа и упариванием досуха при перемешивании повторяют до полного завершения реакции. Очисткой полученного продукта колоночной хроматографией на силикагеле с элюированием дихлорметаном получают 90 мг заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,3 - 2,2 (м, 4H), 2,5 - 3,2 (м, 3H), 2,68 (с, 3H), 2,69 (т, J = 6,1 Гц, 2H), 3,90 - 4,45 (м, 2H), 4,25 (т, J = 6,1 Гц, 2H), 4,88 (уш. с, 2H), 6,36 (уш. с, 1H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 495 (M + H)+.
ПРИМЕР 134
4-(2-Хлорфенил)-2-[4-(1-цианометилоксикарбонил)пиперидил] -9-метил- 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин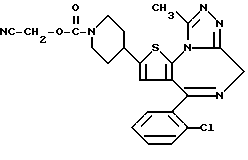
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 - 2,4 (м, 4H), 2,6 - 3,3 (м, 3H), 2,68 (с, 3H), 3,9 - 4,5 (м, 2H), 4,89 (уш. с, 2H), 6,36 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 481 (M + H)+.
ПРИМЕР 135
4-(2-Хлорфенил)-2-[4-{ 1-(3-цианопропилоксикарбонил)пиперидил} ] - 9-метил-6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин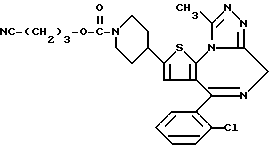
1H-ЯМР (90 МГц, CDCl3) δ: 1,1 - 2,3 (м, 6H), 2,42 (т, J = 6,8 Гц, 2H), 2,68 (с, 3H), 2,6 - 3,3 (м, 3H), 3,85 - 4,45 (м, 2H), 4,16 (т, J = 5,8 Гц, 2H), 4,48 (уш. с, 2H), 6,35 (уш. с, 1H), 7,10 - 7,55 (м, 4H).
MS m/z (Pos. FAB): 509 (M + H)+.
ПРИМЕР 136
2-[4-{ 1-(3-Бутинилоксикарбонил)пиперидил} ] -4-(2-хлорфенил)- 9-метил-6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин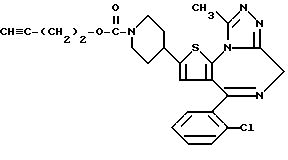
1H-ЯМР (90 МГц, CDCl3) 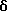 : 1,2 - 2,2 (м, 4H), 1,96 (т, J = 2,9 Гц, 1H), 2,30 - 3,15 (м, 3H), 2,51 (тр. д, J = 6,8 Гц, 2,9 Гц, 2H), 2,68 (с, 3H), 3,9 - 4,5 (м, 2H), 4,15 (т, J = 6,8 Гц, 2H), 4,89 (уш. с, 2H), 6,35 (уш. с, 1H), 7,1 - 7,6 (м, 4H).
: 1,2 - 2,2 (м, 4H), 1,96 (т, J = 2,9 Гц, 1H), 2,30 - 3,15 (м, 3H), 2,51 (тр. д, J = 6,8 Гц, 2,9 Гц, 2H), 2,68 (с, 3H), 3,9 - 4,5 (м, 2H), 4,15 (т, J = 6,8 Гц, 2H), 4,89 (уш. с, 2H), 6,35 (уш. с, 1H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 494 (M + H)+.
ПРИМЕР 137
2-[4-(1-Бутоксикарбонил)пиперидил] -4-(2-Хлорфенил)- 9-метил-6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин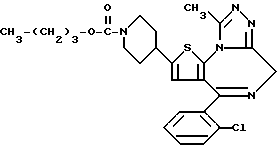
1H-ЯМР (90 МГц, CDCl3) δ: 0,92 (т, J = 6,1 Гц, 3H), 1,1 - 2,2 (м, 8H), 2,68 (с, 3H), 2,50 - 3,15 (м, 3H), 3,9 - 4,4 (т, J = 6,5 Гц, 2H), 4,88 (уш. с, 2H), 6,35 (уш. с, 1H), 7,10 - 7,55 (м, 4H).
MS m/z (Pos. FAB): 498 (M + H)+.
Препаративный пример 55
2-Бромэтил трет-бутилдиметилсилиловый эфир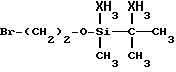
В 40 мл N,N-диметилформамида растворяют 2 г этиленбромгидрина и 2,4 г имидазола и к полученному раствору при комнатной температуре прибавляют 2,65 г трет-бутилдиметилсилилхлорида. После окончания реакции добавляют бензол, после чего промывают водой и водным раствором гидрокарбоната натрия, сушат над безводным сульфатом магния, фильтруют и после отгонки растворителя получают 3,6 г (выход 94%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 0,13 (с, 6H), 0,94 (с, 9H), 3,38 (т, J = 6,5 Гц, 2H), 3,88 (т, J = 6,5 Гц, 2H).
Препаративный пример 56
1-(2-Гидроксиэтил)имидазол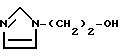
В 70 мл N,N-диметилформамида растворяют 3,56 г 2-бромэтил трет-бутилдиметилсилилового эфира и 1,97 г имидазола, затем к раствору добавляют 4 г карбоната калия и перемешивают 2 часа 40 минут при 90oC. После отгонки растворителя добавляют этилацетат, промывают водой и сушат над безводным сульфатом магния. Раствор фильтруют и после отгонки растворителя полученный остаток растворяют в тетрагидрофуране и к полученному раствору прибавляют 12,6 мл раствора тетрабутиламмонийфторида (1 М раствор в тетрагидрофуране) и перемешивают при комнатной температуре. По окончании реакции растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием дихлорметаном получают 0,59 г (35%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 3,28 (уш. с, 1H), 3,6 - 4,2 (м, 4H), 6,84 (уш. с, 1H), 7,28 (уш. с, 1H).
Препаративный пример 57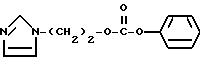
Соединение синтезировано из соединения препаративного примера 56 по методике препаративного примера 53.
ПРИМЕР 138
4-(2-Хлорфенил)-2-[4-[1-{ 2-(1-имидазоил)этилоксикарбонил} пиперидил] ]- 9-метил-6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин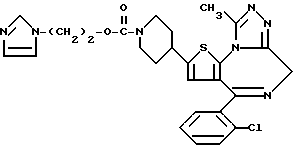
1H-ЯМР (90 МГц, CDCl3) δ: 1,2 - 2,2 (м, 4H), 2,4 - 3,1 (м, 3H), 3,9 - 4,5 (м, 6H), 4,87 (уш. с, 2H) 6,36 (уш. с, 1H), 7,1 - 7,6 (м, 4H), 7,42 (уш. с, 1H).
MS m/z (Pos. FAB): 536 (M + H)+.
ПРИМЕР 139
4-(2-Хлорфенил)-9-метил-2-[4-{ 1-тетрагидропиран-4-ил-оксикарбонил) пиперидил}]-6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин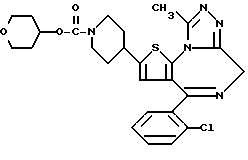
1H-ЯМР (90 МГц, CDCl3) δ: 1,0 - 2,2 (м, 8H), 2,5 - 3,2 (м, 3H), 2,68 (с, 3H), 3,25 - 3,67 (м, 2H), 3,67 - 4,00 (м, 2H), 4,00 - 4,39 (м, 2H), 4,50 - 5,05 (м, 1H), 4,88 (с, 2H), 6,35 (уш. с, 1H), 7,05 - 7,55 (м, 4H).
MS m/z (Pos. FAB): 526 (M + H)+.
Препаративный пример 58
Фенил 3-фенилпропилкарбонат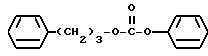
Соединение получено с выходом 70% по методике препаративного примера 53.
1H-ЯМР (90 МГц, CDCl3) δ: 1,80 - 2,25 (м, 2H), 2,74 (дв. д, J = 9 Гц, 6,5 Гц, 2H), 4,23 (д, J = 6,5 Гц, 2H), 6,95 - 7,55 (м, 10H).
ПРИМЕР 140
4-(2-Хлорфенил)-9-метил-2-[{ 1-(3-фенилпропилоксикарбонил)пиперидил} ] - 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин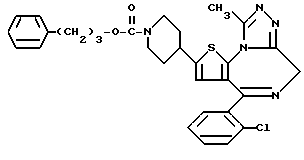
1H-ЯМР (90 МГц, CDCl3) 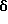 : 1,0 - 2,2 (м, 6H), 2,4 - 3,2 (м, 5H), 2,68 (с, 3H), 3,8 - 4,4 (м, 2H), 4,07 (т, J = 6,5 Гц, 2H), 4,87 (уш. с, 2H), 6,36 (уш. с, 1H), 6,7 - 7,6 (м, 9H).
: 1,0 - 2,2 (м, 6H), 2,4 - 3,2 (м, 5H), 2,68 (с, 3H), 3,8 - 4,4 (м, 2H), 4,07 (т, J = 6,5 Гц, 2H), 4,87 (уш. с, 2H), 6,36 (уш. с, 1H), 6,7 - 7,6 (м, 9H).
MS m/z (Pos. FAB): 560 (M + H)+.
ПРИМЕР 141
4-(2-Хлорфенил)-9-метил-2-[4-{1-(2-морфолиноэтиламинокарбонил)пиперидил} ]- 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин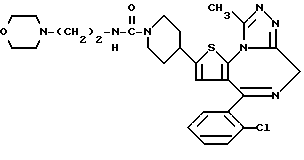
В 4 мл хлороформа растворяют 170 мг производного пиперидина препаративного примера 52 и 210 мг 4-[2-(фенилоксикарбонил)этил]морфолина и полученный раствор упаривают досуха при 80oC и перемешивании. Добавление хлороформа и упаривание досуха повторяют дважды с завершением в результате реакции. Продукт реакции подвергают колоночной хроматографии на силикагеле с элюированием смесью дихлорметан - метанол (95:5). К полученной фракции в небольшом количестве добавляют дихлорметан и нерастворимые продукты удаляют при декантации. После отгонки дихлорметана снова добавляют небольшое количество дихлорметана и снова удаляют нерастворимые вещества, но фильтрованием. После отгонки дихлорметана получают 160 мг заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,00 - 2,25 (м, 4H), 2,25 - 3,10 (м, 9H), 2,67 (с, 3H), 3,1 - 3,5 (м, 2H), 3,50 - 3,85 (м, 4H), 3,85 - 4,20 (м, 3H), 4,88 (уш. с, 2H), 6,35 (уш. с, 1H), 7,1 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 554 (M + H)+.
Препаративный пример 59
4-(Фенилоксикарбонил)морфолин
Соединение синтезировано по методике препаративного примера 53 и очищено колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (5:95).
1H-ЯМР (90 МГц, CDCl3) δ: 3,4 - 3,9 (м, 8H), 6,9 - 7,5 (м, 5H).
ПРИМЕР 142
4-(2-Хлорфенил)-9-метил-2-[4-(1-морфолинокарбонилпиперидил)] - 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин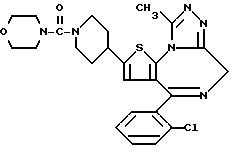
К 180 мг производного пиперидина препаративного примера 52 и 250 мг 4-(фенилоксикарбонил)морфолина добавляют 5 мл хлороформа, после чего температуру повышают от комнатной до 130oC при перемешивании и испаряют в течение 12 часов досуха. Продукт подвергают колоночной хроматографии на силикагеле с элюированием дихлорметаном и получают 38,8 мг заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,2 - 2,4 (м, 4H), 2,6 - 3,2 (м, 3H), 2,68 (с, 3H), 3,00 - 3,45 (м, 4H), 3,45 - 3,95 (м, 6H), 4,88 (уш. с, 2H), 6,36 (уш. с, 1H), 7,05 - 7,50 (м, 4H).
Препаративный пример 60
2-Этоксиэтил-п-толуолсульфокислота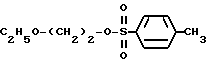
В 40 мл пиридина растворяют 2 г 2-этоксиэтанола, к раствору при охлаждении льдом прибавляют 5,66 г п-толуолсульфонилхлорида, после чего температуру повышают. Добавляют этилацетат, промывают водой и насыщенным водным раствором гидрокарбоната натрия, сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и после очистки остатка колоночной хроматографией на силикагеле с элюированием смесью этилацетат - гексан (5: 95) получают 3,69 г (56%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,12 (т, J = 7,2 Гц, 3H), 2,42 (с, 3H), 3,42 (к, J = 7,2 Гц, 2H), 3,4 - 3,7 (м, 2H), 4,0 - 4,2 (м, 2H), 7,26 (уш. д, J = 8,3 Гц, 2H), 7,73 (уш. д, J = 8,3 Гц, 2H).
ПРИМЕР 143
4-(2-Хлорфенил)-2-[4-{ 1-(2-этоксиэтил)пиперидил} ] -9-метил- 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин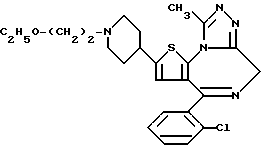
В 5 мл N,N-диметилформамида растворяют 150 мг производного пиперидина препаративного примера 52 и 140 мг 2-этоксиэтил п-толуолсульфоната, к раствору прибавляют 100 мг карбоната калия, после чего перемешивают 2 часа при 90oC. После отгонки растворителя добавляют воду, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют, растворитель отгоняют и очисткой остатка колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол получают 130 мг (68%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ: 1,2 (т, J = 7,2 Гц, 3H), 1,5 - 2,4 (м, 6H), 2,4 - 3,0 (м, 1H), 2,64 (т, J = 6,1 Гц, 2H), 2,71 (с, 2H), 2,80 - 3,25 (м, 2H), 3,51 (к, J = 7,2 Гц, 2H), 3,59 (т, J = 6,1 Гц, 2H), 4,95 (уш. с, 2H), 6,44 (уш. с, 1H), 7,2 - 7,6 (м, 4H).
MS m/z (Pos. FAB): 470 (M + H)+.
Препаративный пример 61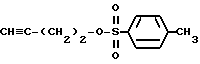
Соединение получено по методике препаративного примера 60 с выходом 70%.
1H-ЯМР (90 МГц, CDCl3) 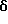 : 1,95 (т, J = 2,9 Гц, 1H), 2,27 (с, 3H), 2,53 (тр. д, J = 7,2 Гц, 2,9 Гц, 2H), 4,06 (т, J = 7,2 Гц, 2H), 7,25 (уш. д, J = 8,3 Гц, 2H), 7,73 (уш. д, J = 8,3 Гц, 2H).
: 1,95 (т, J = 2,9 Гц, 1H), 2,27 (с, 3H), 2,53 (тр. д, J = 7,2 Гц, 2,9 Гц, 2H), 4,06 (т, J = 7,2 Гц, 2H), 7,25 (уш. д, J = 8,3 Гц, 2H), 7,73 (уш. д, J = 8,3 Гц, 2H).
ПРИМЕР 144
2-[4-{ 1-(3-Бутинил)пиперидил}]-4-(2-хлорфенил)-9-метил- 6H-тиено[3,2-f] [1,2,4]триазоло[4,3-a][1,4]диазепин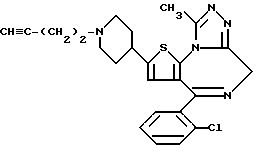
1H-ЯМР (90 МГц, CDCl3) δ: 1,4 - 3,0 (м, 11H), 1,97 (т, J = 2,5 Гц, 1H), 2,68 (с, 3H), 2,8 - 3,2 (м, 2H), 4,88 (уш. с, 2H), 6,35 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 450 (M + H)+.
ПРИМЕР 145
4-(2-Хлорфенил)-4-[1-(диметиламиносульфонил)пиперидил] -9-метил- 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин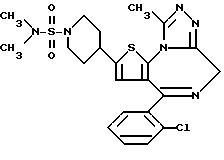
В 3 мл N,N-диметилформамида растворяют 100 мг производного пиперидина препаративного примера 52 и 80 мг триэтиламина и к полученному раствору при -60oC по каплям прибавляют раствор 50 мг диметилсульфамоилхлорида в 5 мл N, N-диметилформамида. Поскольку исходные соединения остаются непрореагировавшими в больших количествах, при комнатной температуре добавляют триэтиламин и диметилсульфамоилхлорид до исчезновения исходных соединений. После отгонки растворителя добавляют насыщенный раствор гидрокарбоната натрия, экстрагируют хлороформом и сушат над безводным сульфатом магния. Раствор фильтруют и после очистки колоночной хроматографией на силикагеле с элюированием смесью дихлорметан - метанол (99:1) получают 90 мг (71%) заглавного соединения.
1H-ЯМР (90 МГц, CDCl3) δ : 1,5 - 2,2 (м, 4H), 2,5 - 3,1 (м, 3H), 2,68 (с, 3H), 2,8 (с, 6H), 3,55 - 3,90 (м, 2H), 4,89 (уш. с, 2H), 6,32 (уш. с, 1H), 7,1 - 7,5 (м, 4H).
MS m/z (Pos. FAB): 505 (M+N)+.
ПРИМЕР 146
4-(2-Хлорфенил)-9-метил-2-[4-{ 1-(2-тиофенсульфонил)пиперидил}]- 6H-тиено[3,2-f][1,2,4]триазоло[4,3-a][1,4]диазепин
1H-ЯМР (90 МГц, CDCl3) δ: 1,5 - 2,3 (м, 4H), 2,30 - 2,95 (м, 1H), 2,44 (тр. д, J = 12,2 Гц, 3,6 Гц, 2H), 2,67 (с, 3H), 3,65 - 4,15 (м, 2H), 4,88 (уш. с, 2H), 6,33 (уш. с, 1H), 6,8 - 7,7 (м, 7H).
MS m/z (Pos. FAB).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ НАПРАВЛЕННОЙ ДЕГРАДАЦИИ БЕЛКА | 2020 |
|
RU2820673C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2716136C2 |
| ПРОИЗВОДНЫЕ ДИФЕНИЛА, ПРОИЗВОДНОЕ ФЕНИЛПИПЕРАЗИНА И СПОСОБ ЛЕЧЕНИЯ | 1995 |
|
RU2125051C1 |
| СОЕДИНЕНИЕ, ОБЛАДАЮЩЕЕ ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2809763C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЯ | 2002 |
|
RU2358733C2 |
| ПРОИЗВОДНЫЕ ПИРИДАЗИНОНА И ТРИАЗИНОНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ | 2001 |
|
RU2279428C2 |
| ПРОИЗВОДНЫЕ АНТРАНИЛОВОЙ КИСЛОТЫ ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ИХ ОСНОВЕ | 1994 |
|
RU2128644C1 |
| ПРОИЗВОДНЫЕ КОНДЕНСИРОВАННЫХ ПОЛИЦИКЛИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2167877C2 |
| АЗОТСОДЕРЖАЩИЕ КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОДУКЦИИ БЕТА-АМИЛОИДА | 2010 |
|
RU2515976C2 |
| ИНГИБИТОРЫ АКТИВНОСТИ АКТ | 2010 |
|
RU2579513C2 |
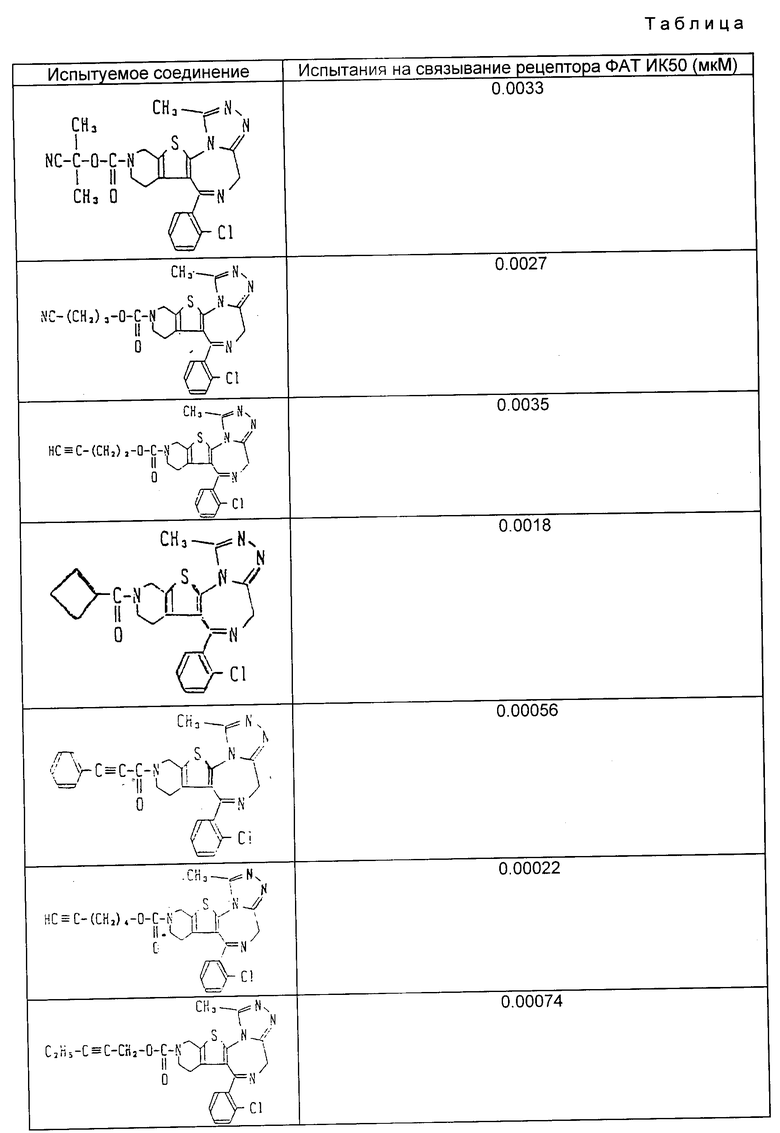
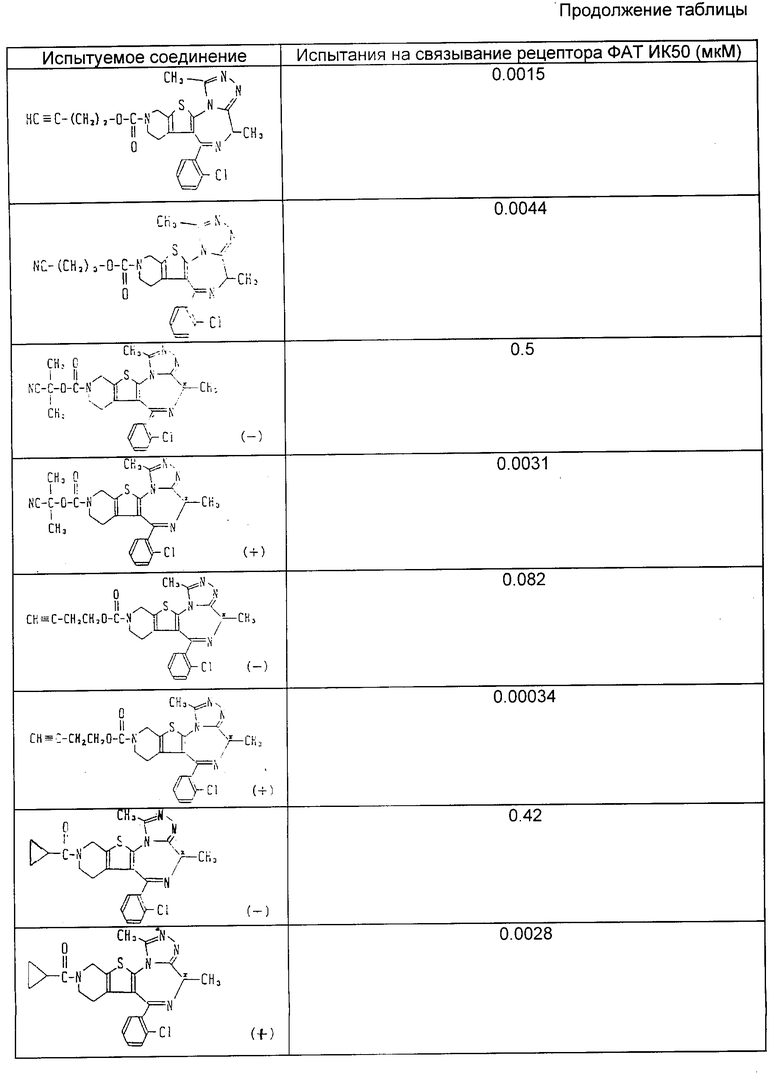
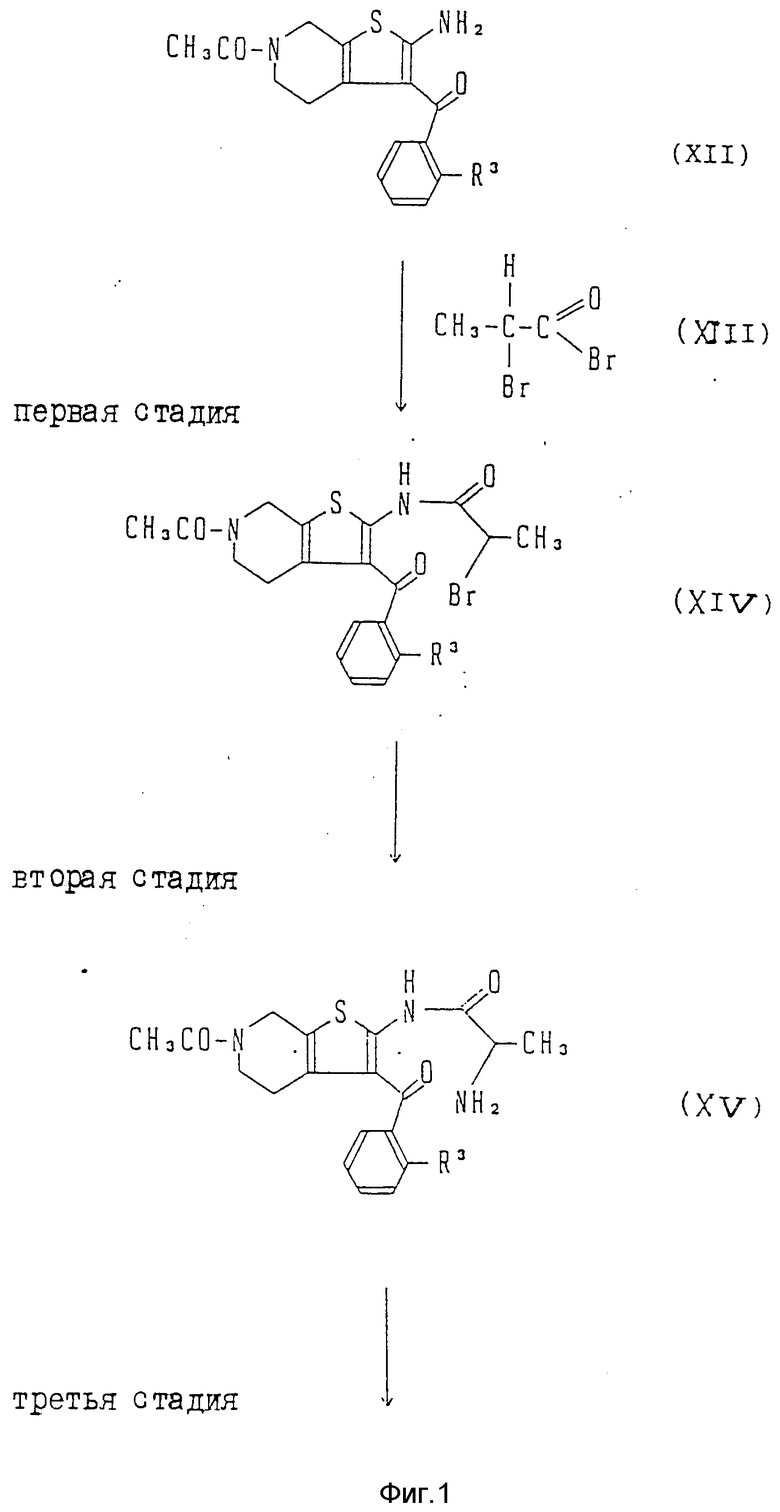
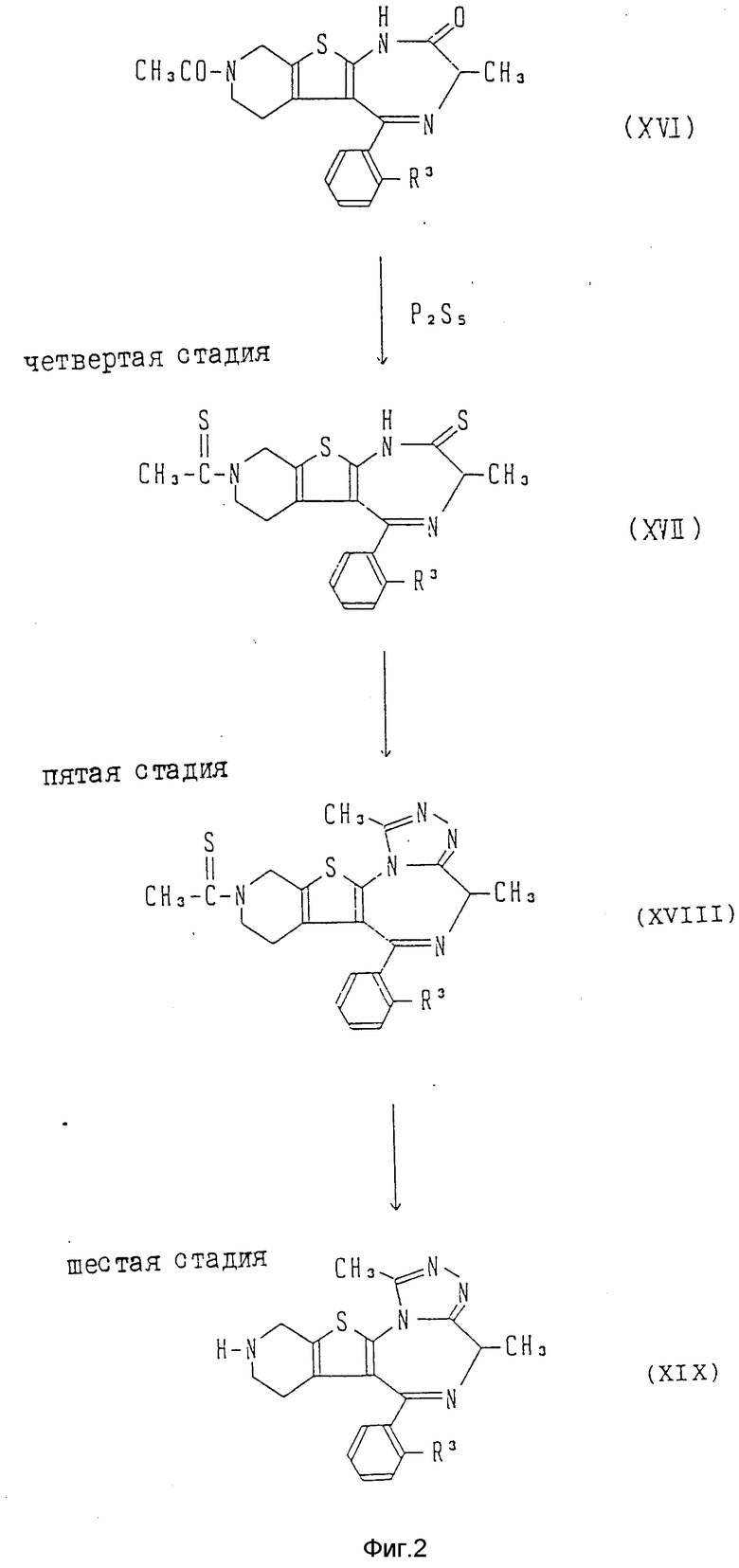
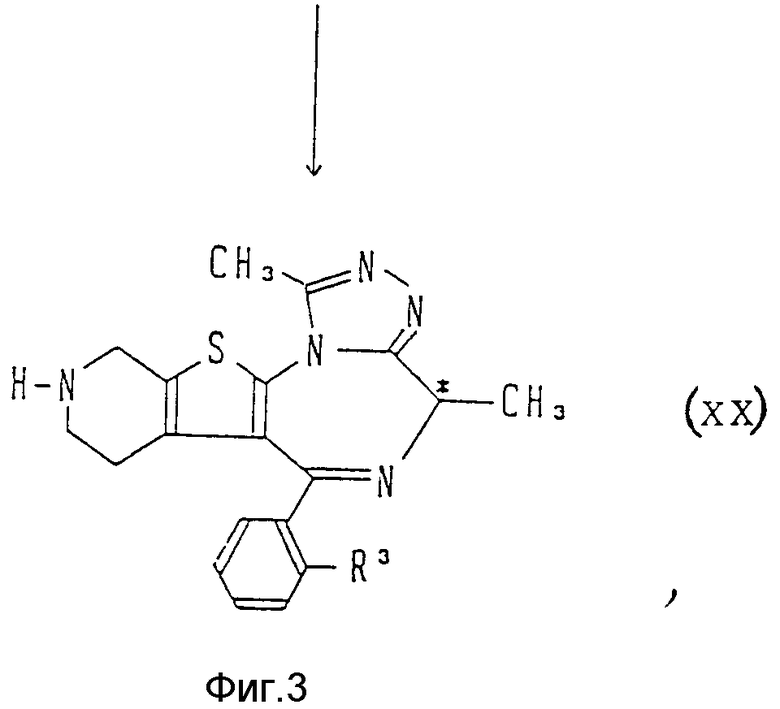
Сущность: производные триазоло-1,4-диазепина формулы I - III и их фармакологические соли, где R1 и R2 - H или алкил, R3 - галоген, R4 - низший алкил, X - группа формул -OCO-, - NR5CO-, где R5 - H или низший алкил, -CO-, или другие группы и Y - циклоалкил, циклоалкилалкил, алкинил или другие группы. Производные диазепина I - III проявляют подавляющее фактор активации тромбоцитов действие с увеличенным сроком проявления этой активности. 7 с. и 4 з.п.ф-лы, 1 табл., 3 ил.
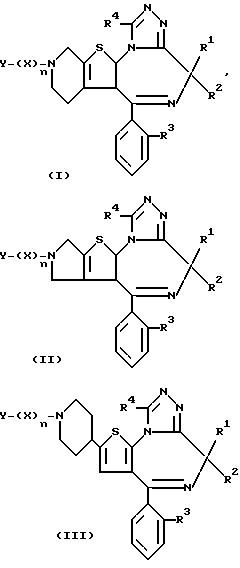 \
\
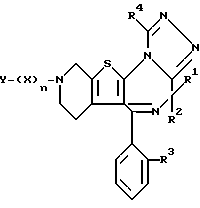
или их фармацевтически приемлемые соли,
где R1 и R2 - одинаковые или различные, атом водорода или низший алкил;
R3 - атом галогена;
R4 - низший алкил;
n = 1, когда Х - группа формулы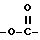
группа формулы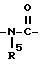
где R5 - атом водорода или низший алкил, или группа формулы 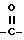
Y - С3 - С6-циклоалкильная группа, возможно замещенная метильной группой или возможно замещенную в первом положении этинильной группой, или С3 - С6-циклоалкил-С1 - С2-алкильная группа или С3 - С6-алкинильная группа, возможно замещенная фенильной группой, группа формулы 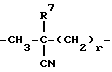
где R7 - водород или метил;
r = 0 или 1,
группа формулы
NC(CH2)p,
где p - целое число от 1 до 5;
или группа формулы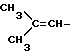
или группа формулы
A(CH2)q,
где А - группа, выбранная из пиридильной группы, тетрагидропиранильной группы, морфолиногруппы и имидазолильной группы;
q - целое число от 0 до 2;
или группа формулы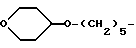
где s - целое число от 1 до 2,
или фенилэтинильная группа, или группа формулы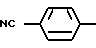
или группа формулы 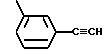
или группа формулы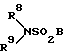
где R8 и R9 - одинаковые или различные водород или низший алкил, или пиридилметил, или циклогексил, или R8 и R9 вместе с атомом азота образуют пиперидиновое, имидазолиновое или морфолиновое кольцо;
В - фениленовая или С1 - С3-алкиленовая группа,
или группа формулы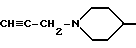
или группа формулы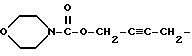
или группа формулы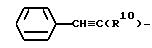
где R10 - или метил,
или группа формулы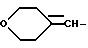
или фенил - С1 - С2-алкильная группа, возможно замещенная в фенильном кольце галогеном, или группа формулы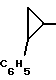
или группа формулы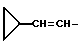
или группа формулы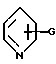
где G - СН=СН- или -SСН2-;
или, когда Х представляет собой группу формулы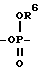
где R6 - низший алкил;
Y - С2 - С7-алкильная группа,
или n = 0, когда Y - С3 - С6-алкинильная группа.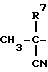
где R7 - водород или метил, С3 - С6-алкинильная группа или С3 - С6-циклоалкил-С1 - С2-алкильная группа.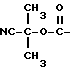
или группа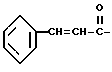
или группа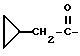
или группа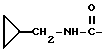
или группа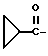
или группа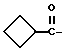
или группа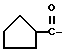
или когда R2 - метил, то Y - X - группа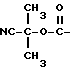
или группа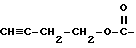
или группа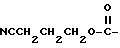
или группа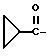 .
.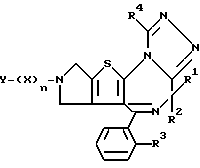
или их фармацевтически приемлемые соли,
где R1 и R2 - атомы водорода;
R3 - атом галогена;
R4 - низший алкил;
X - группа формулы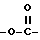
или группа формулы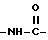
Y - С3 - С6-циклоалкил-С1 - С2-алкильная группа, или С3 - С6-алкинильная группа, или группа формулы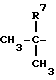
где R7 - метил,
или группа формулы
NC(CH2)p,
где p - целое число от 1 до 3,
или группа формулы
A(CH2)q,
A - группа, выбранная из пиридильной, тетрагидропиранальной, морфолильной или морфолинокарбонильной групп;
q - целое число от 0 до 2,
или С2 - С7-алкильная группа или фенил-С1 - С2-алкильная группа, возможно замещенная в фенильном кольце на атом галогена, нитро- или трифторметильная группа.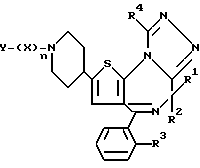
или их фармацевтически приемлемые соли,
где R1 и R2 - атомы водорода;
R3 - атом галогена;
R4 - низший алкил;
когда n = 1, X - группа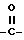
или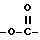
Y - С3 - С6-циклоалкильная группа или С3 - С6-алкильная группа,
или группа формулы
NC(CH2)p,
где p - целое число от 1 до 3,
или группа формулы
A(CH2)q,
где A - группа, выбранная из пиридильной, имидазолильной, тиенильной, тетрагидропиранильной и морфолильной групп;
q - целое число от 0 до 3,
или фенилэтинильная группа, или С2 - С7-алкильная группа, или фенил-С1 - С2-алкильная группа, возможно замещенная в фенильном кольце на атом галогена, или С1 - С2-алкокси-С1 - С2-алкильная групп, или X - группа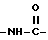
Y - группа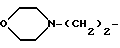
или когда n = 0, Y - С3 - С6-алкинильная группа, С1 - С2-алкокси-С1 - С2-алкильная группа, диметиламиносульфонильная или тиофенсульфонильная группа.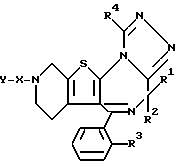
где X - группа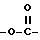
или группа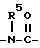
R1, R2, R3, R4, R5 и Y имеют значения, определенные в п.1,
отличающийся тем, что производное триазоло [1,4] диазепина общей формулы IV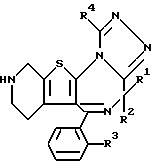
где R1, R2, R3 и R4 имеют значения, определенные в п.1,
подвергают взаимодействию с соединением общей формулы V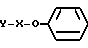
где X и Y имеют указанные значения.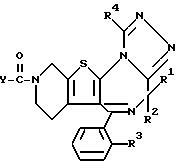
где R1, R2, R3, R4 и Y имеют значения, определенные в п.1,
отличающийся тем, что производное триазоло [1,4] диазепина формулы IV подвергают взаимодействию с соединением формулы VIII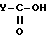
где Y имеет указанные значения,
или его реакционноспособным производным.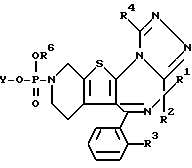
где R1, R2, R3, R4 и R6 имеют значения, определленные в п.1;
Y - С2 - С7-алкинильная группа,
отличающийся тем, что производное триазоло [1,4] диазепина общей формулы IV подвергают взаимодействию с соединением общей формулы IX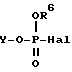
где R5 и Y имеют указанные значения;
Hal - атом галогена.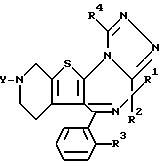
где R1, R2, R3 и R4 имеют значения, определенные в п.1;
Y - С3 - С6-алкинильная группа,
отличающийся тем, что производное триазоло [1,4] диазепина общей формулы IV подвергают взаимодействию с соединением общей формулы X
Y - Hal,
где Y и Hal имеют указанные значения.
Приоритет по пунктам:
31.10.88 по пп.1, 2, 7 - 11;
16.12.88 по п.1;
24.11.88 по п.1;
28.12.88 по п.1.
| DE 3724031 A1, 28.01.88 | |||
| ПОДБОРЩИК-КОПНИТЕЛЬ | 0 |
|
SU254245A1 |
| ПРИСПОСОБЛЕНИЕ К ПРОВОЛОКООБВЯЗЫВАЮЩЕЙ МАШИНЕ ДЛЯ ПОДГИБА УЗЛА ОБВЯЗКИ ПАКЕТА | 0 |
|
SU268242A1 |
| 0 |
|
SU194416A1 | |
| EP 0230942 A2, 17.01.87 | |||
| УСТРОЙСТВО ДЛЯ ФОРМИРОВАНИЯ ВЗРЫВНОЙ ВОЛНЫ В ЗАРЯДЕ ВЗРЫВЧАТОГО ВЕЩЕСТВА | 2013 |
|
RU2531678C1 |
| DE 3502392 A1, 31.07.86 | |||
| DE 3701344 A1, 23.07.87. | |||
Авторы
Даты
1998-08-20—Публикация
1989-10-30—Подача