Изобретение относится к борьбе с нематодами, паразитирующими на растениях, главным образом к способу борьбы с корневыми цистообразующими нематодами. Изобретение также касается придания устойчивости к нематодам растениям большого числа видов, чувствительным к корневым цистообразующим нематодам, например растениям картофеля (Solanum tuberosum).
Цистообразующие нематоды (особенно Heterodera и Globodera spp) являются основными вредителями большинства сельскохозяйственных культур. Они вызывают прямые потери урожая, а также косвенные потери, например из-за затрат на пестициды и неоптимального использования севооборота. Картофельные цистообразующие нематоды (Globodera rostochiensis и Globodera pallida) являются основными вредителями картофеля в Соединенном Королевстве, многих других районах Европы и в других основных областях возделывания картофеля. Heterodera glycines (цистообразующая нематода оси) при возделывании сои наносит экономический ущерб, который может превышать 500 миллионов долларов в год только в США. Heterodera schachtii (цистообразующая нематода свеклы) является главной проблемой для возделывающих сахарную свеклу в Европе и США. Heterodera avenae (цистообразующая нематода хлебных злаков) представляет собой всемирную экономическую проблему.
Экономически значимые плотности цистообразующих нематод обычно вызывают задержки в росте сельскохозяйственных растений. Их корневая система меньше, чем у незараженных растений, что приводит к появлению на листьях симптомов минеральной недостаточности и увеличивает опасность увядания в засушливых почвенных условиях. Потери урожая зависит от плотности цистообразующих нематод в посадках и в некоторых случаях могут достигать существенно более 50% для таких культур, как картофель и соя.
До недавнего времени борьба с нематодами растений проводилась путем использования химических препаратов с нематоцидной активностью, а также с использованием соответствующих агротехнических приемов и путем возделывания устойчивых сортов. Все это может быть применено в интегрированной форме. Нематоциды принадлежат к наиболее неприемлемым химическим веществам, широко применяемым для защиты сельскохозяйственных растений. Например, Алдикарб (Aldicarb) и продукты его распада высокотоксичны для млекопитающих и загрязняют почвенные воды. В итоге правительства некоторых штатов США ввели ограничения на использование этого нематоцида. В Нидерландах проводится политика сокращения применения нематоцидов со сроком использования более 5 лет. Сельскохозяйственные меры борьбы с нематодами не являются идеальным решением, т.к. такие меры, как смена культур, обуславливают скрытые потери, которые неприемлемы для тех, кто выращивает специализированные монокультуры или лишь несколько экономических альтернативных культур.
Устойчивость растения к нематодам может быть вызвана неспособностью последних размножаться на генотипе видов растений-хозяев, и может иметь место доминантный, полудоминантный или рецессивный тип наследования, основанный на одном или нескольких генах растения. Однако их коммерческая ценность для селекционера растений и фермера ограничена. Например, у картофеля могут быть различные источники устойчивости, обуславливающие разделение популяций в Европе, как в случае с одиночным доминантным геном H1, обуславливающим устойчивость к G. rostochiensis (Ro1 и Ro4), но не к другим формам этого вида (Ro2, Ro3 и Ro5).
Сорт Maris Piper экспрессирует H1 и широко используется в Соединенном Королевстве против G.rostochiensis, но его использование совпало с повышенным преобладанием G. pallida, способной размножаться при наличии H1. Проблема, обуславливаемая патотипами, преодолевающими устойчивость, существует и в случае других цистообразующих нематод, источники устойчивости к которым известны. В некоторых случаях источники устойчивости являются полигенными, что создает дополнительные трудности для селекционера растений. Кроме того, устойчивость у некоторых сортов является по своей природе скорее количественной, нежели качественной, и поэтому в ответ на частое использование таких культур со временем может произойти усиленное размножение.
В последнее время все большее распространение получают генно-инженерные подходы к защите растений от болезней и вредителей, в том числе и от нематод. Так, известен (EP 0352052 A3 (A 01 N 63/02)) способ борьбы с нематодами, включающий в себя встраивание в геном растений гена Bacillus thuringiensis, кодирующего токсин, который обладает нематоцидной активностью. При этом указанный ген экспрессируется в растении конститутивно, в результате чего в указанном растении создается и поддерживается определенный уровень чужеродного для него продукта (токсина), что может оказывать определенное отрицательное действие как на само растение, так и на его потребителей.
Предлагаемым изобретением решается задача создания способа борьбы с нематодами, при котором продукт, обеспечивающий устойчивость растения к нематодам, начинает продуцироваться именно при заражении паразитом и продуцируется специфично в кормовой зоне наметод.
Эта задача решается тем, что предложен способ борьбы с нематодами, отличающийся тем, что осуществляют следующие стадии:
(а) идентифицирует ген, который индуцируется в успешно зараженном нематодой растении;
(б) получают конструкцию, объединяя промоторный участок данного гена с другой областью, кодирующей продукт, нарушающий жизнедеятельность нематод или предотвращающий инфицирование растения нематодами;
(в) трансформируют растение указанной конструкцией с получением растения, устойчивого к нематодам.
Целесообразно на стадии (а) идентифицировать ген, который индуцируется в растении в зоне кормления нематод.
Поверхность раздела между растением и патогеном является ключевым местом в определении чувствительности или устойчивости к инвазии. В ходе ранних детерминирующих стадий инвазионного процесса поверхность раздела ограничивается очень малым количеством растительных клеток в месте инфекции. Позднейшая редифференцировка существующих растительных клеток формирует синцитий, которым питается животное. Синцитий индуцируется личинками второй стадии после их перемещения в корни хозяина, возможно, в ответ на выделения животного в первичные кормовые клетки. Если растение чувствительно, то синцитий увеличивается в объеме и поддерживается в течение всего периода питания нематоды. В случае с самками этот период может длиться несколько недель. Клеточная биология синцития подробно описана.
В кормовой зоне цистообразующей нематоды экспрессируются гены, являющиеся специфичной частью чувствительности к нападению нематод. Идентификация этих генов может быть проведена с помощью полимеразной цепной реакции (ПЦР).
Целесообразно ген, индуцируемый в зоне кормления нематод, идентифицировать следующим образом:
(а) получают библиотеки кДНК зараженных и незараженных растений;
(б) сравнивают полученные библиотеки кДНК зараженных и незараженных растений;
(в) выявляют клон кДНК, содержащий ген, индуцируемый в зоне кормления нематод,
(г) используют данный клон кДНК для идентификации соответствующего гена в растении.
Идентифицированные таким образом гены могут быть использованы для прямого выделения в ходе нападения нематоды веществ, токсичных либо для растительной клетки, либо для нематод, специфично в кормовой зоне. Специфичное выделение таких веществ дает возможность использовать соединения, которые в случае их конструктивной экспрессии в растении могли бы ослабить рост растения или привести к неприемлемому токсикологическому вреду. Диапазон таких соединений известен и для их применения согласно изобретению пригодны стандартные биотехнологические методики.
Соответствующие нематодспецифичные гены могут быть найдены у широкого ряда растений, что позволяет защитить любую культуру, с которой возможны генетические манипуляции для экспрессии промоторов генов, характерных для кормовой зоны и соединенных с последовательностями, способными нарушать размножение нематод. В качестве примеров можно привести картофель, томаты, сахарную свеклу и табак.
Известно также, что развитие синцития сходно для множества цистообразующих нематод. Поэтому использование специфично включающегося гена универсально для всех цистообразующих нематод. К ним относятся, например, Globodera pallida и Globodera rostochiensis (картофельные цистообразующие нематоды), Heterodera glycines (цистообразующие нематоды сои), Heterodera shachtii (цистообразующая нематода свеклы), Heterodera avenae (цистообразующая нематода хлебных злаков), Heterodera oryzae (рисовая цистообразующая нематода) и Giobodera tabacom (табачная цистообразующая нематода).
В настоящем описании термин "ген" относится к последовательности ДНК, которая включает в себя: (1) верхние (5') регуляторные сигналы, включая промотор, (2) кодирующую область, определяющую продукт, белок или РНК гена, и (3) нижние (3') области, включая сигналы терминации транскрипции и полиаденилирования, (4) ассоциированные с ними последовательности, необходимые для эффективной и специфичной экспрессии.
Термин "промотор" относится к области последовательности ДНК, включающей необходимые сигналы для эффективной экспрессии кодирующей последовательности. Это могут быть, например, последовательности, с которыми связывается РНК-полимераза, и области, с которыми связываются другие регуляторные белки, а также области, участвующие в контроле трансляции белка, и кодирующая последовательность.
Целесообразно на стадии (б) промоторный участок объединять с областью, кодирующей продукт, вызывающий гибель клетки, способной редифференцироваться для образования кормовой зоны.
Предпочтительно указанный продукт представляет собой ДНКазу, РНКазу, протеиназу, токсичный белок, токсичный пептид, продукт, обуславливающий мультигенный токсический синдром, или антисмысловую РНК редифференцирующихся клеток.
Под мультигенным токсическим синдромом понимают ситуацию, при которой промотор может экспрессировать белок или пептид, остающийся в неактивной форме до активизации белком, который продуцируется геном, соединенным с другой промоторной последовательностью, специфичной для кормовой зоны. Продукт первого гена A может быть неактивным до тех пор, пока не образует под действием продукта второго гена в новый продукт A', который является активным токсином или протеазой. В другом случае, A может быть неактивным без B, так что только молекулы A-B активны.
Антисмысловая РНК включает в себя один или несколько генов антисмысловой РНК, аналогичных генам, специфичным для кормовой зоны. Другими словами, промотор может быть использован для регуляции образования своей собственной антисмысловой РНК. Это сильно снижает уровень нормального продукта. И наоборот, промотор может быть использован для управления экспрессией антисмысловой РНК для общих клеток генов, таких как АТФ-синтетаза, необходимых для жизнеспособности клетки.
Целесообразно на стадии (б) промоторный участок объединять с областью, кодирующей продукт, оказывающий летальное или сублетальное действие на нематод.
Предпочтительно указанный продукт представляет собой токсичный для нематоды белок, антитело, нарушающее процесс питания нематод, или токсичный для нематод полипептид.
Примерами потенциально пригодных генов, которые могут быть использованы при реализации настоящего изобретения, являются:
(а) белковый токсин Bacillus thuringiensis (или сходного с ним организма), обладающий антинематодной активностью;
(б) ген токсичного для метода белка (заявка на патент Великобритании 9104617.7);
(в) антитело, нарушающее питание путем воздействия на глотание или переваривание пищи подобно одному из антител, описанных для соевой цистообразующей нематоды, включая действующие против спинной глоточной железы (Atkinson et al. , 1988 Annals of Applied Biology 112, 459-469), используя известные (Hiatt, A. , Cafferkey, R.C. & Bowdish, K. 1989 Production of Antibodies in Transgenic Plants Nature, 342, 76-78) процедуры для трансгенной экспрессии антител в растениях;
(г) белок или пептид типа нейропептида, оказывающий токсичное действие на питающихся цистообразующих нематод после заглатывания ими пищи.
Следует принять во внимание, что уровень устойчивости к нематоде не должен быть абсолютным, но должен в общем обеспечивать уровень, хозяйственно или экономически значительный для данного растения.
Изобретение предусматривает также создание средств, обеспечивающих устойчивость к нематоде, локализованную в зоне ее питания или рядом с ней. Этим устраняется необходимость для растения продуцировать антинематодные продукты конститутивно. Этим ограничивается любое вредное для растения действие, которое может возникнуть при конститутивной экспрессии. Многие культуры могут быть защищены от цистообразующих нематод с помощью данного изобретения, и, таким образом, являются возможными объектами генетического манипулирования с целью экспрессии промоторов генов, специфичных для синцития, соединенных с последовательностями, которые нарушают редифференцировку растительных клеток в синцитий или экспрессируют в синцитии продукты антинематодных генов. Это касается культур, поражающихся такими цистообразующими нематодами, как Globodera pallida и Globodera rostochiensis (картофельные цистообразующие нематоды), Heterodera giycines (цистообразующая нематода сои), Heterodera shachtii (cвекловичная цистообразующая нематода), Heterodera avenae (цистообразующая нематода хлебных злаков), Heterodera carotae (цистообразующая нематода моркови), Heterodera oryzae (цистообразующая нематода риса) и Globodera tabacum (табачная цистообразующая нематода). В качестве примеров культур, которые могут быть защищены от цистообразующих нематод благодаря данному изобретению, можно привести картофель, томаты, сою, сахарную свеклу, рапс, пшеницу, рожь, ячмень, овес, рис, морковь, капусту и табак.
На фиг. 1 показана зона кормления нематод, индуцированная корневой узловой нематодой в трансформированном растении табака.
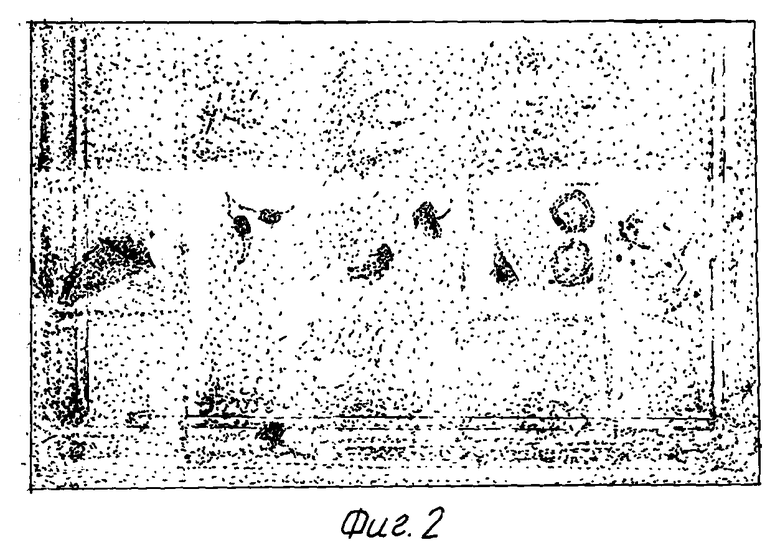
На фиг. 2 показаны образцы ткани, взятые из различных частей целого трансформированного растения табака.
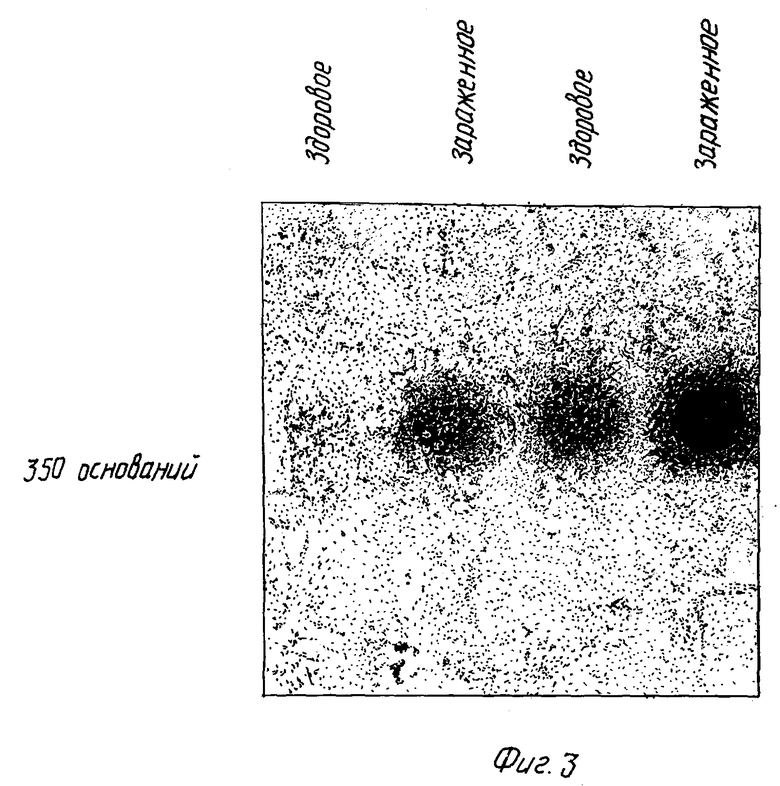
На фиг. 3 представлены результаты нозерн-блоттинга проб, полученных из здоровых и пораженных нематодами растений томатов и сахарной свеклы.
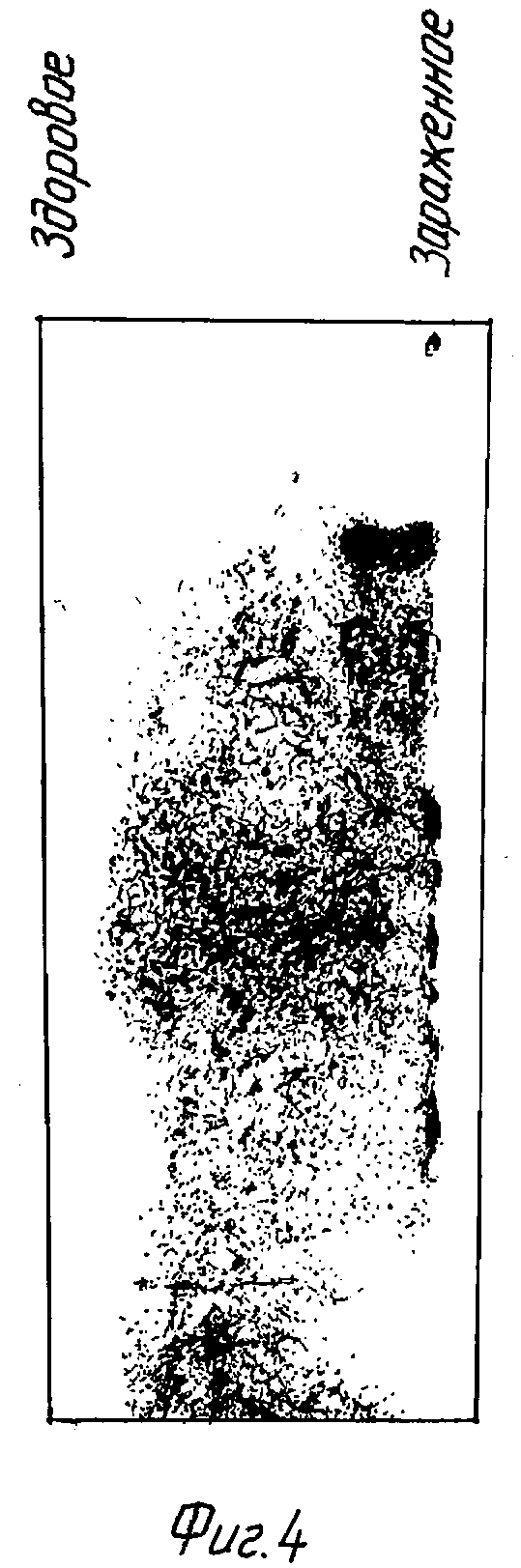
На фиг. 4 представлены результаты нозерн-блоттинга проб, полученных из здоровых и пораженных наматодой растений картофеля.
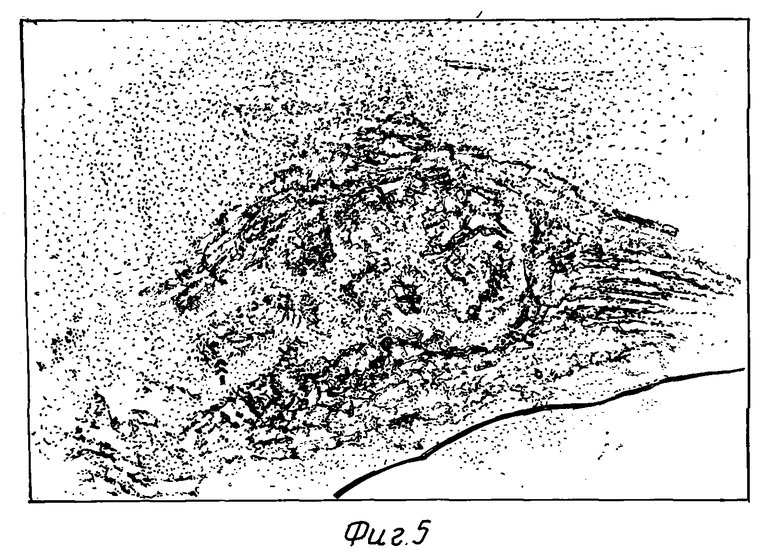
На фиг. 5 показан криосрез трансгенного корня A.thaliana.
На фиг. 6 показана зона кормления, индуцированная цистообразующей нематодой в трансформированном растении A.thaliana.
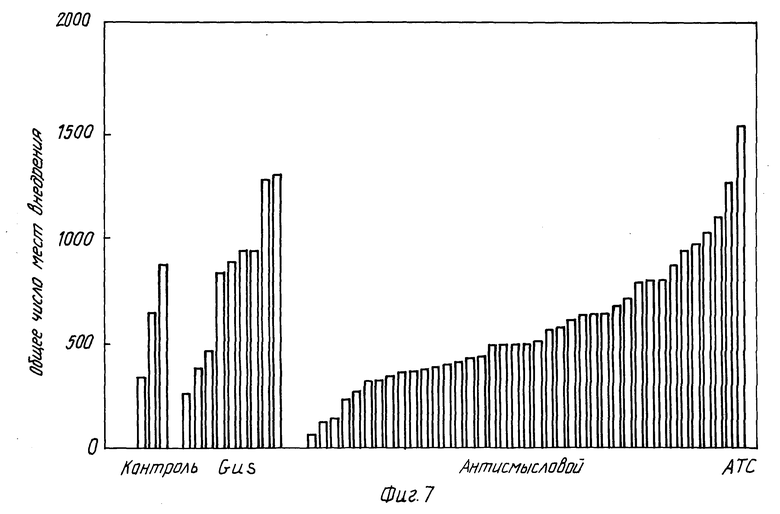
Фиг. 7 представляет собой гистограмму, демонстрирующую общее число мест внедрения нематоды для растений табака, трансформированных смысловой и антисмысловой последовательностью GUS.
Ниже изобретение поясняется примерами, которые, однако, не ограничивают его объема.
Первый пример касается способов, использованных для идентификации, характеристики и манипулирования генами картофеля с целью создания устойчивого трансгенного растения картофеля.
Пример 1
Этот пример описывает использование сорта картофеля, чувствительного к Globodera rostochiensis, патотип Ro2, для определения генов, экспрессирующихся в зоне питания нематоды. В разделах 1 - 5 предлагаются методики получения зараженной корневой ткани. Небольшие количества локально зараженных тканей дали количества РНК (раздел 6), наиболее удобные для конструирования библиотеки кДНК с помощью ПЦР-амплификации (разделы 7.1 - 7.4). Выделение клонов кДНК, специфичных для питающих клеток, проводилось с помощью дифференциальной гибридизации с пробами кДНК из зараженных и незараженных тканей (раздел 7.5). ДНК положительных клонов кДНК была секвенирована (раздел 10), и вставки использовались как пробы на следующих этапах. Проверка временной и пространственной экспрессии генов была проведена с помощью нозерн-анализа (раздел 8) с использованием разных тканей растения и разного времени заражения. Дальнейшая локализация экспрессии гена проводилась гибридизацией in situ (раздел 12). Геномные клоны, соответствующие кДНК клонам, специфичным для питающих клеток, выделялись из библиотеки геномной ДНК (раздел 11). Промоторы идентифицировались секвенированием ДНК (раздел 11) для создания конструкций, пригодных для создания трансгенных растений картофеля, обладающих устойчивостью к нематоде (раздел 13) локально в кормовой зоне.
1. Растительный материал
Solanum tuberosum, сорт Maris Piper (шотландский семенной картофель, класс A) проращивался 24 дня (Kosack K.E., Atkinson H.J., Bowles D.J. 1990. Changes in abundance of translatable mRNA species in potato roots and leaves following root invasion by cyst-nematode G. rostochiensis pathotypes. Physiol. Mol. Plant Pathol.). Индивидуальные побеги отрезались после выращивания в мешках, либо для выращивания в горшках использовались целые клубни.
2. Нематоды
Популяция цист Globodera rostochiensis, патотипы Ro1 и Ro2, содержались в сухих условиях при 4oC. Цисты замачивались в водопроводной воде на 7 дней при 4oC. Добавлялся диффузат из корней картофеля Shepherd A.M., 1986. In: Southey J.F. (ed) Laboratory methods for work with plant and soil nematodes: MAFF reference book 402, 6th edn.), и личинки выводились через 4 - 7 дней при комнатной температуре.
3. Заражение
Материал в мешках. Индивидуальные побеги помещались в готовые мешки (Northup-King, Миннесота). Полоски бумаги Whatman GFA размером 1 х 0,5 см помещались под кончики индивидуальных корней. 50 червей в 10 мл корневого диффузата наносились на каждый кончик корня, который затем покрывался второй полоской GFA. Фильтровальная бумага GFA удалялась через 24 ч после инокуляции для синхронизации заражения. Основание отрезалось, и мешки промывались водопроводной водой.
Материал в горшках. Проросшие клубни выращивались в горшках (25 см) в почве с невылупившимися цистами в количестве, достаточном для получения популяции в 50 яиц на грамм почвы.
Контрольные (неинокулированные) мешки и горшки содержались в тех же условиях, но без цист.
4. Условия выращивания
Зараженные растения картофеля выращивались в режиме 16 часов освещения при 22oC и 6 часов темноты при 18oC.
5. Сбор материала и анализ
Выращенные в мешках ткани собирали на 4-й, 7-й, 15-й и 24-й дни после инвазии. Обесцвеченные локально зараженные корни вырезались прямо в конверты из фольги в жидком азоте. Ткани корня, соседние с зоной заражения, также вырезались и замораживались отдельно.
Ткани, выращенные в горшках, собирались через 26 дней после заражения патотипом Ro2. Вылупившиеся самки и цисты удалялись тонкой кистью и локально зараженные ткани вырезались в жидком азоте в индивидуальные пакеты из фольги.
6. Выделение тотальной РНК
Ткани в пакетах из фольги дробили пестиком в порошок и хранили при -70oC. Размолотые ткани (12 мг) переносили в предварительно охлажденные в жидком азоте одноразовые пластиковые пробирки Sarstedt (на 20 мл), затем добавляли 0,5 мл смеси фенол/CH3Cl/изоамиловый спирт (25:24:1) и 0,5 мл буфера GuHCl (8M гуанидин-HCl), 20 мM МЭС (4-морфолино-этанол-сульфоновая кислота), 20 мМ Na2ЭДТА, доведенного до pH=7 с использованием NaOH, и 2-меркаптоэтанол, добавленный в количестве, достаточном для получения концентрации 50 нМ, непосредственно перед применением). Пока пробирки оттаивали во льду, ткани гомогенизировались 15 ударами смесителя Polytron (Kinematica, Швейцария). Водную фазу реэкстрагировали фенолом более трех раз перед осаждением в течение ночи при -20oC после добавления 0,2 объема 1M уксусной кислоты и 0,7 объема холодного 96%-ного этанола. РНК, собранная центрифугированием примерно при 13000 g в течение 15 мин в микроцентрифуге, промывалась в 400 мкл 3М раствора ацетата натрия (pH=5,5) при 4oC, затем в 70%-ном холодном этаноле перед окончательным растворением в 30 - 50 мкл воды, обработанной DEPC, и хранилась при -70oC.
7. Конструирование библиотеки кДНК с помощью ПЦР
7.1 Синтез кДНК
1 мкг тотальной РНК из корней картофеля, собранных через 26 дней после заражения G. rostochiensis, патотип Ro2, денатурировался в течение 5 мин в водяной бане при 70oC и затем быстро охлаждался во льду. Проба этой РНК добавлялась в реакционную смесь, состоящую из 4 мкл 5 х AMVRT буфера (250 мМ Трис-HCl (pH= 8,3), 250 мМ KCl, 50 мМ MgCl2, 5 мМ DDT, 5 мМ ЭДТА, 50 мг/мл бычьего сывороточного альбумина), 2 uл олигонуклеотида (дТ17, 100 мкг/мл), 2 мкл смеси дНТФ (по 10 мМ АТФ, дЦТФ, дГТФ, дТТФ), 1 мкл 10 мМ раствора спермидин-HCl, 1 мкл 80 мМ раствора пирофосфата натрия и 125 единиц плацентарного ингибитора рибонуклеазы человека (HPRNI). 10 единиц обратной транскриптазы вируса птичьей миелобластомы (AMV) добавлялись для доведения конечного реакционного объема до 20 мкл перед инкубацией его при 42oC в течение 1 ч. Реакция прерывалась добавлением 20 мкл 0,1 М раствора NaCl, 40 мМ ЭДТА. Размер и количество продуктов определяли проведением параллельной реакции, содержащей 50 мкКи дЦТФ, меченный 32P (3000 Ки/ммоль). Меченые продукты реакции фракционировались в щелочном геле, с которого затем делали авторадиографические снимки. Вся масса меченых продуктов была в пределах от 200 до 2000 т. п.о., с четко различимыми крупными продуктами.
Олиго-дТ-праймер удалялся избирательной преципитацией. 0,5 мкг поли I поли C (Pharmacia) и 3 мкг 10%-ного (масс./об.) раствора СТАВ добавлялись в реакционную смесь перед центрифугированием в микроцентрифуге при комнатной температуре в течение 20 мин. Супернатант осторожно удалялся, и осадок ресуспендировался в 14 мкл 1М раствора NaCl, к которому добавили 25 мкл H2O и 1 мкл 10%-ного раствора СТАВ, и проба снова осаждалась микроцентрифугированием. Осадок окончательно ресуспендировался в 10 мкл 1М раствора NaCl и осаждался в 2,7 объеме этанола в течение ночи при -20oC. Осадок промывался в 70%-ном этаноле и растворялся в 7 мкл H2O. Реакцию дГ-наращивания проводили, добавив в пробу: 4 мкл 5 х буфера для наращивания (1М какодилата калия, 125 мМ Трис-HCl, pH 7,2), 1 мкл 2 мМ раствора ДТТ, 2 мкл 5 мМ раствора хлорида кобальта, 5 мкл 20 М раствора дГТФ и 25 единиц терминальной трансферазы (Boehringer) - и инкубируя смесь при 37oC 20 мин; для прекращения реакции добавляли 4 мкл 100 мМ раствора ЭТДА и 2 мкл 12 М раствора NaCl. Избыточные нуклеотиды удалялись добавлением 1 мкл 10%-ного (масса/объем) раствора СТАВ и микроцентрифугированием при 4oC в течение 20 мин. Осадок растворялся в 10 мкл 1 М раствора NaCl перед добавлением 0,25 мкг гликогена и 30 мкл холодного этанола и переосаждался в течение ночи при -20oC. После промывки в 70%-ном этаноле осадок растворялся в 20 мкл 50 мМ раствора NaOH, 2 мМ раствора ЭДТА и инкубировался 60 мин при 65oC для гидролиза РНК. кДНК снова осаждалась этанолом, промывалась, и осадок растворялся в 20 мкл H2O.
7.2. ПЦР амплификация
ПЦР амплификация первой цепи кДНК с гомополимерным хвостом проводилась с использованием затравок:
A (олиго-дТ17-Not I); ГЦГГЦЦГЦТТТТТТТТТТТТТТТТ, B (олиго-дЦ14-EcoRI); ААГГААТТЦЦЦЦЦЦЦЦЦЦЦЦЦЦ.
Реакционные смеси для ПЦР содержали 10 мкл 10 х ПЦР буфера (100 мМ Трис-HCl, pH = 8,3 500 мМ KCl, 40 мМ MgCl2, 0,1% желатина), 10 мкл 10 х смеси дНТФ (по 5 мМ дАТФ, дЦТФ, дГТФ, дТТФ), 100 пикомолей затравки B, 2 единицы Taq-полимеразы и 1-10 нг кДНК с олиго-(дГ) хвостом в общем реакционном объеме 20 мкл, сверху покрытом 20 мкл минерального масла. Режим термических циклов был следующим: 1 цикл 96oC, 2 мин, для денатурации продуктов; 96oC, 2 мин, 58oC, 2 мин, 72oC, 3 мин для синтеза второй цепи; 1 цикл (96oC, 2 мин, 40oC, 2 мин, 72oC, 2 мин) для получения хорошей затравки с олиго-(дТ) конца; 15 циклов (96oC, 2 мин, 58oC, 2 мин, 72oC, 3 мин) для амплификации продуктов. Реакционная смесь разделялась электрофоретически в NuSieve GTG LMP (FMC Bioproducts) геле с использованием лидерной ДНК в 123 т.п. о. как маркера для определения размеров, участки геля, соответствующие классам размерами меньше 500, от 500 до 1500, от 1500 до 2000 и более 2000 п.о. были вырезаны, и ДНК была выделена из геля путем замораживания при -20oC и последующего центрифугирования в микроцентрифуге в течение 10 мин в фильтры Spin-X (Costar). ПЦР-продукты были блот-гибридизированы по Саузерну с 3 клонами, которые, как было известно, конститутивно экспрессировались в корнях картофеля. Пробы кДНК длинных и коротких, а также имеющих высокое или малое относительное содержание транскриптов гибридизовались с продуктами ПЦР, демонстрируя четкое наличие различных с библиотекой транскриптов.
7.3. Создание библиотеки
Выделенная ДНК (более 200 п.о.) разрезалась с помощью EcoRI и NotI и лигировалась с ДНК лямбда-ZAP, а затем упаковывалась in vitro с помощью смеси Stratagene Giga Plus для упаковки согласно прилагаемой инструкции. Библиотека встраивалась в E.coli, штамм XL1-Blue, с использованием чашек LB с 1%-ным верхним агаром, содержащем 12,5 мМ IPTG и 6,25 мг/мл X-гала (X-gal).
7.4. Анализ библиотеки
Качество библиотеки кДНК, сделанной с помощью ПЦР, анализировалось двумя способами. (1) Примерно 96% бляшек оказалось рекомбинантными, что было показано с помощью инсерционной инактивации альфа-комплементации бета-галактозидазы. (2) Бляшки, отобранные случайным образом в ПЦР буфер и амплифицированные с использованием затравок, комплементарных М13, имели, как было показано, одиночные инсерции от 230 до 1000 п.о. со средним размером инсерции 470 п.о.
7.5. Дифференциальный скрининг
Библиотека дала 3,5 • 105 рекомбинантных фагов, 6 • 104 из которых были подвергнуты скринингу с использованием проб, меченных 32P-дЦТФ и синтезированных как первая цепь кДНК для 10 мкл тотальной РНК, выделенной из зараженных корневых тканей, собранных через 26 дней после инвазии Ro2, или из здоровых корней того же возраста (Gurr S.J., McPherson M.J. 1991. PCR-based cDNA library construction. In: McPherson V.J., Quirke P., Taylor G.R. (eds) Polymerase chain reaction: A practical approach. IRL Press at Oxford University Press, Oxford). Невключившийся изотоп удалялся осаждением с помощью ацетата аммония, и пробы доводились до получения гибридизационной жидкости, эквивалентной по числу отсчетов на микрограмм кДНК на миллилитр, после подсчета жидкостной сцинтилляции. Осуществлялся сбор бляшек в двух вариантах, и ДНК бляшек денатурировалась в растворе NaOH (0,5М) и NaCl (1,5М), нейтрализовалась в 1,5, 0,5 М Трис-HCl (pH = 7,2) и 1 мМ ЭДТА и высушивалась (80oC, 2 ч). Фильтры прегибридизовались отдельно в "здоровых" и "зараженных" прегибридизационных жидкостях, содержащих 5х SSPE, 6% ПЭГ 6000, 0,5% Marvel (сухое снятое молоко), 1% SDS, 0,1% пирофосфата натрия и 250 мкг/мл обработанной ультразвуком и денатурированной ДНК спермы сельди, при 65oC в течение 6 ч. Гибридизация проводилась при 65oC в течение 24 ч после добавления соответствующей пробы первой цепи, меченной радиоактивным изотопом. После гибридизации фильтры отмывались последовательно в растворе 5х SSC, 0,1% SDS, затем в растворе 1х SSC, 0,1% SDS при 65oC, дважды по 20 мин в каждом растворе. Блоты экспонировались на рентгеновскую пленку с использованием усиливающих экранов при -70oC. Бляшки, которые гибридизовались с 26-дневной пробой Ro2, но не со здоровой 26-дневной пробой, очищались до однородности двумя дополнительными циклами скрининга.
8. Нозерн- и Саузерн-гибридизация и приготовление проб
РНК массой по 10 мкг на дорожку разделялась в 0,6 М формальдегидагарозном геле при напряжении 7,5 Всм-1. Гель фотографировался и промывался дважды по 20 мин в растворе 10х SSC и переносился на мембрану Hybond-N (Amerisham) раствором 10х SSC. Фильтры высушивались (80oC, 2 ч) и прегибридизовались в течение 12 ч при 42oC в смеси, содержащей 50% формамида, 5x SSC, 1x раствор Денхардта, 100 мкг/мл ДНК спермы сельди и 250 мМ фосфатного буфера (pH = 6,5). Гибридизация проводилась в свежем прегибридизационном буфере, включающем 2-4 пробы pPSR (25 нг), меченые 32P-гексапраймером (Feinberg A.P. & Vogelstein B. 1983. Nucleic Acids Research, 14, 2229) при 42oC в течение 24 ч. Фильтры промывались последовательно в растворе 5x SSC, 0,1% SDC при 42oC, затем в растворе 2x SSC, 0,1% SDS при 42oC и окончательно в растворе 2x SSC 0,1% SDS при 65oC. Блоты экспонировались на рентгеновскую пленку с усиливающими экранами при -70oC. Инсерция PMR1 готовилась путем отбора одиночной очищенной бляшки в ПЦР буфере и амплифицировалась с использованием комплементарных затравок M13 согласно (Gussow D. & Clackson T. 1989. Nucleic Acids Research 17, 4000).
Геномная ДНК готовилась из ядер, выделенных из молодых листьев картофеля (сорт Maris Piper) согласно (Jofuku K.D. & Goldberg R.B. 1989. In Plant Molecular Biology: A practical Approach (ed C.S. Shaw)pp 37-66). Высокомолекулярная ДНК фракционировалась по размеру в 0,6%-ном агарозном геле после обработки ее рестрикционными ферментами. Для анализа экспрессии генов в растении РНК выделялась из стеблей, черешков, листьев, цветков и корней как зараженных, так и незараженных растений. Для анализа раневого ответа растительные корни или листья давили и выделяли РНК из обработанных тканей через определенный промежуток времени (3, 6, 9 и 12 ч после обработки). Пробы сравнивались с помощью нозерн-гибридизации с РНК, выделенной из зараженных нематодой корней. Гели отмывали, денатурировали и переносили на мембрану Hybond-N (Sambrook J., Fritsch E.F. & Maniatis T. 1989. Molecular Cloning: A laboratory manual, 2nd edn., Cold Spring Harbour Press). Фильтр высушивался (80oC, 2 ч) и прегибридизовался в течение 6 ч при 65oC в прегибридизационной жидкости, как описано для дифференциального скрининга бляшек. Гомологичная гибридизация и условия отмывки были теми же, что и в случае фильтров для нозерн-гибридизации. Гетерологичная гибридизация проводилась при 56oC, фильтры отмывались в растворе 5x SSC при 65oC.
9. Вырезание последовательности из лямбда-ZAP и очистка плазмиды
Плазмида pBlue из клона PMR1, содержащего вставку, последовательность которой соответствует одной из формул 1-8, вырезалась из положительно гибридизующегося клона лямбда-ZAP и освобождалась согласно (Stratagene manual). Плазмидная ДНК очищалась центрифугированием в градиенте плотности хлоридав цезия (Davis L.G., Dibner M.D., Batey J.F. 1986. Basic methods in molecular biology. Elsevier Science Publishers, New York).
Последовательности формул 1-8
ГЦЦЦАААЦТТТЦЦГГТГТАЦТЦЦТТГТЦЦТТГТТТТТТГТАГТЦТТТТАЦЦТАТЦЦААЦАААААТ ТТЦТЦГЦЦААААААГГГТТАТААЦАЦЦГЦГАТАААГЦТЦТТАААТААТГ
(формула 1)
ААЦАТЦГГГТЦЦААГАГАГГААААГГЦАЦГААГААТГГАЦААТТТТАЦЦААААГЦАТТТЦЦТТАГ ГЦТЦАТАААГЦАТТТТАААЦЦЦЦГАТГЦТГТТГТТГТТТТГААГГ
(формула 2)
ГТАТЦЦАЦГЦЦТЦТГААТАГЦАЦАГАААЦАГАГТЦТАЦААГААААГЦАЦАЦАТАТТТТТГЦАГТТ ГГАГАААТААЦГАГЦЦАТТГТААТТГНЦГГТТЦТААГННТЦГААГЦГАТЦААААТТАААТТАААГТТАГЦААЦГГ
(формула 3)
ЦАТГАЦГАТГГАЦААААТЦАТТГАГГААЦТГГАТААЦАЦЦГННЦГГЦТГЦЦГГГГЦТГГЦГААТЦ ТГТГГГТНЦЦГЦЦААТТЦГТААЦЦГТАТЦГАТАТГЦТЦТЦААЦЦГГЦАТТАААА
(формула 4)
ЦАГЦАТТАЦАЦТГГЦЦЦАГГТГЦАГТАЦАГЦАТГТГГГТГАЦГНГГАААНАНННЦЦТГГТАЦТТТ ТЦГГААЦТАТГЦАЦАЦЦГГЦТГЦТАТЦАААГЦЦТГААГГЦЦТГЦАТА
(формула 5)
ГТЦГЦТАЦЦТТТЦГГГАЦГЦААТАЦЦГТАТТГЦТГЦГЦТТЦЦАГАГАГТЦАЦЦТАЦЦГЦТТТГААТГАЦ
(формула 6)
ГЦГЦЦГЦГГЦАЦАТЦГГГГГЦТЦГГНГГЦТАЦГГЦТАЦГГАГГТТГЦАЦААЦТТГЦГГАЦГЦАААТАААЦГЦГЦААЦААТЦГГ
(формула 7)
ЦГТГАГТЦАГТНАГТЦГТАТТАЦААТТЦАЦТГГЦЦГТЦГТТТТАЦААЦГТЦГТЦГТГАЦТГГГАА АЦЦЦ
(формула 8)
где А - аденин,
Ц - цитозин,
Т - тимин,
Г - гуанин,
Н - любой нуклеотид.
10. Анализ последовательности
Секвенирование плазмидной ДНК, денатурированной щелочью, проводилось согласно (Manufacturers protocols for Sequenase (Version 2.0) reactions (United States Biochemical Corp.)). Данные по секвенированию сравнивались с базами данных EMBL и GenBank (выпуск 23) с использованием программы QUICKN, использующей алгоритм Липмана и Пирсона (Lipman D.J.K., Pearson W.R. 1985. Rapid and sensitive protein similarity searches. Science, 227: 1435-1441) и введенной в операционную систему VMS компьютера VAX 11/750.
11. Выделение геномного клона
Библиотека геномной ДНК на основе лямбда EMBL3 была сконструирована путем частичной рестрикции геномной ДНК сорта Maris Piper рестриктазой EcoI согласно (Sambrook J., Fritsch E.F & Maniatis T. 1989. Molecular Cloning: A laboratory manual, 2nd edn., Cold Spring Harbour Press). Библиотека анализировалась путем перепечатки примерно 1,8 • 105 клонов, приготовления перенесенных на фильтры дуплицированных бляшек, прегибридизации, а затем гибридизации и отмывки, как описано выше в разделе 7.5, за исключением того, что проба была приготовлена путем мечения гексапраймером инсерционной ДНК и ее ПЦР амплификации (Gussow D., Clackson T. 1989. Direct clone characterization from plaques and colonies by the polymerase chain reaction. Nucleic Acids Res. 17:10) из кДНК клонов, pPMR1, pRMR2 или pPMR3.
Позитивно гибридизующиеся клоны, выделенные после трех циклов гибридизационного скрининга, были в дальнейшем охарактеризованы с помощью рестрикционного анализа и секвенирования ДНК (Sambrook J., Fritsch E.F. & Maniatis T. 1989. Molecular Cloning: A laboratory manual, 2nd edn., Cold Spring Harbour Press) для локализации промоторных последовательностей.
12. Гибридизация in situ
Ткани зараженных и незараженных корней заливались парафином, резались, прегибридизовались и затем гибридизовались со смысловыми антисмысловыми пробами pPMR1, pPMR2 и pPMR3 согласно (Jackson D. In: Molecular Plant Pathology: A Practical Approach (ed. S.J. Gurr, M.J. McPherson and D.J. Bowles IRL Press, Oxford, 1991).
13. Получение и регенерация трансгенных растений
Трансгенные растения картофеля были получены с помощью способов, описанных (Harch et al. 1985. Science, 227, 1229-1231), с использованием штамма GV3 101 Agrobacterium, содержащего плазмиду pGV3850, несущую промоторы, специфичные для кормовых клеток и слитые с соответствующим дисруптивным геном, выбранным из генов, перечисленных во вводной части настоящего описания, при этом до проверки на устойчивость к нематодам были регенерированы ростки.
Пример 2
В этом примере описывается реализация способа по изобретению на растениях табака, томатов, сахарной свеклы и Arabidopsis thaliana.
1. Некоторое количество кДНК, индуцированных нематодами, было выделено из инфицированных Meloidogyne javanica (корневая узловая нематода) растений табака путем скринирования библиотеки кДНК. Ассоциированный с одной из этих кДНК протомор был выделен и соединен с репортерной последовательностью GUS, помещенной в Т-ДНК бинарного вектора; эта конструкция была использована для получения трансформированных корней табака путем сокультивирования с Agrobacterium rhizogenes. На прилагаемой фиг. 1 показана специфическая экспрессия (голубая окраска) репортерной последовательности GUS в зоне кормления нематод под управлением указанного промотора в корнях трансформированного таким образом растения табака. Нематода в зоне кормления окрашена красной краской. Та же самая конструкция была использована для трансформации целых растений табака путем сокультивирования с A.tumefaciens. На фиг. 2 показаны образцы, взятые из различных частей целого трансформированного растения табака, причем голубая окраска обнаруживается только на зараженных нематодой образцах корней.
Упомянутый выше промотор был соединен с барназой рибонуклеазой из Bacillus amyloliquefaciencs. Этой конструкцией трансформировали табак, используя A. tumefaciens. Трансформированные таким образом целые растения табака заражали затем M.javanica. Было определено, что среднее число мест внедрения нематоды на растение для контрольных растений табака, трансформированных GUS, было равно примерно 800, в то время как для двух независимо трансформированных растений табака, трансформацию которых осуществили согласно изобретению, число мест внедрения не растение было равно для одного из растений - 350, для другого - 10.
Эта методология была повторена с тем исключением, что индуцируемый нематодой промотор был соединен с кодирующей последовательностью гена, экспрессирующегоcя в зоне кормления нематоды, в антисмысловой ориентации. На фиг. 7 прямоугольные полоски обозначают общее число мест внедрения нематоды на растения для растений табака, трансформированных указанной антисмысловой последовательностью, растений табака, трансформированных контрольной GUS последовательностью, и нетрансформированных контрольных растений табака. На фиг. 7 легко увидеть, что некоторые из растений, трансформированных антисмысловой последовательностью, обнаруживают значительно более низкое количество мест внедрения по сравнению с контрольными популяциями. Такие устойчивые к нематодам представители этой популяции (трансформированной антисмысловой последовательностью) могут, конечно, быть использованы в стандартных процедурах скрещивания для получения большого числа индивидуальных устойивых к нематодам растений.
2. Тот ген, для которого была обнаружена экспрессия его промотора специфически в зоне кормления нематод при заражении корневой узловой нематодой в табаке (см. фиг. 1 и 2), также индуцируется в кормовых зонах других видов нематод и других видов растений. На фиг. 3 показан Нозерн-блот, демонстрирующий, что количество мРНК этого гена увеличено (т.е. этот ген индуцировался) как при заражении цистообразующей нематодой (Heterodera schactii) сахарной свеклы (Beta vulgaris), так и заражении корневой узловой нематодой (M. javanica) томатов (Lycospersicon esculentum). Таким образом, Нозерн-блот показывает, что гены, выделенные с использованием способа по изобретению, являются пригодными для создания устойчивости к широкому кругу корневых узловых и цистообразующих нематод во многих видах растений.
На фиг. 4 показан Нозерн-блот гена, индуцированного в картофеле в кормовой зоне цистообразующей нематоды картофеля Globodera rostochiensis. Это является дальнейшим подтверждением общей применимости данного способа.
Индуцированный нематодой ген был идентифицирован в Arabidopsis thaliana, и на фиг. 5 показана криосекция трансгенного корня A.thaliana со специфической экспрессией репортерной последовательности GUS в гигантской клетке в ответ на заражение Meloidogyne. На фиг. 6 показана специфическая экспрессия конструкции промотор/GUS в зоне кормления в ответ на заражение A.thaliana цистообразующей нематодой H.schactii.
Гены из растений одного вида могут точно экспрессироваться пространственно и по времени в растении другого вида, даже если эти виды принадлежат к разным семействам. Благодаря сходству в физиологии и патологии образования синцития и жизненных циклов цистообразующих нематод на ряде растений из разных семейств, ген, экспрессирующийся в синцитии одного растения, будет точно экспрессироваться при введении его в другие виды растений.
Подтверждение этого было получено с помощью идентификации эквивалентных генов в других видах растений. Рестрицированные геномные ДНК табака, томата и сахарной свеклы гибридизовались с pPMR1 (согласно методам раздела 8). Во всех вариантах кросс-гибридизация показала наличие в этих растениях эквивалентных генов. Конструкция, содержащая ген, представленный pPMR1, может, таким образом, управлять точно локализованной экспрессией подходящего антинематодного гена в ряде сельскохозяйственных растений. Эти эксперименты также позволяют создать способ выделения эквивалентных генов из других видов растений для экспрессии в них антинематодного защитного механизма.
Изобретение относится к сельскому хозяйству, в частности к способам борьбы с корневыми, цистообразующими нематодами, паразитирующими на растениях. Способ борьбы с нематодами предусматривает идентификацию гена, индуцируемого в успешно зараженном растении путем заражения этого растения нематодой, модификацию гена для придания растению устойчивости к нематодам и трансформацию растения модифицированным геном с последующим получением растения, устойчивого к нематодам. Способ может быть универсальным при защите от цистообразующих нематод, так как основан на использовании генов, являющихся специфичной частью чувствительности к нападению нематод. 8 з.п. ф-лы, 7 ил.
Приоритет по признакам:
19.04.91 - признаки: антитело, нарушающее процесс питания нематод по п.7 и признак томатов, сои, сахарной свеклы, рапса, пшеницы, ржи, ячменя, риса, моркови и капусты по п.9;
10.09.90 - остальные пункты формулы и остальные признаки пп.7 и 9.
| ПРЯМОЗУБАЯ ЦИЛИНДРИЧЕСКАЯ ПЕРЕДАЧА | 0 |
|
SU352052A1 |
Авторы
Даты
1999-04-27—Публикация
1991-09-10—Подача