Изобретение относится к области фармакологии и биологии, может быть использовано при разработке новых лекарственных препаратов, обладающих активностью стимулятора памяти, а также в медицине.
Известны пептиды - фрагменты адренокортикотропного гормона (АКТГ), обладающие активностью стимулятора памяти. Фрагменты АКТГ(4-10) (формулы Met-Glu-His-Phe-Arg-Trp-Glu), АКТГ(5-10) (формулы Glu-His-Rhe-Arg-Trp-Gly) и АКТГ(4-7) (формулы Met-Glu-His-Phe) способны стимулировать память животных; наиболее активным из этих фрагментов является АКТГ(4-10) (De Wied D. Neuropeptides in learning and memory processes, Behavioural Brain Research (1997), v. 87, p. 83-90; Виноградов В.М., Медведев В.Н., Гречко А.Т., Бахарев В. Д. , Пономарева-Степная М.А. Влияние на поведенческую активность крыс нейропептидов - фрагментов АКТГ и вазопрессина. Физиологический журнал СССР, (1980), т. 66, с. 409-415) [1, 2]. Однако известные природные фрагменты АКТГ обладают физиологической активностью недостаточно высокого уровня и длительность их эффектов невелика, что затрудняет их использование в медицине.
Известен синтетический аналог АКТГ(4-10) - гептапептид Семакс (формулы Met-Glu-His-Phe-Pro-Gly-Pro), являющийся стимулятором памяти пролонгированного действия (патент СССР N 939440, C 07 C 103/52, 1981 г.) [3].
В настоящее время Семакс используется в качестве субстанции для приготовления лекарственного средства (Патент РФ N 2045958, A 61 K 37/02, 1994 г. ) [4].
Задачей, решаемой настоящим изобретением, явилось получение нового стимулятора памяти пептидной природы, обладающего высокой биологической активностью.
Задача решается тем, что гексапептид формулы Glu-His-Phe-Pro-Gly-Pro рекомендуется как соединение, обладающее выраженной активностью стимулятора памяти.
Ниже приведены примеры реализации изобретения.
Пример 1. Синтез заявляемого гексапептида осуществляли поэтапно - трипептиды Glu-His-Phe и Pro-Gly-Pro синтезировали путем ступенчатого наращивания, начиная с N-концевого дипептида. Целевой продукт получали присоединением трипептида Pro-Gly-Pro к C-концу последовательности Glu-His-Phe. Для синтеза гексапептида Glu-His-Phe-Pro-Gly-Pro использовали производные L-аминокислот. Упаривание растворов проводили на вакуумном испарителе при 40oC. Температуры плавления, определенные на столике для плавления Boetiys, даны без исправления. Индивидуальность полученных соединений проверяли с помощью ТСХ на пластинках с силикагелем фирмы Silufol (СФР).
Приведены хроматографические подвижности (Rf) в системах растворителей: бутанол: уксусная кислота:вода (4:1:1) - (1); этилацетат:ацетон:50% уксусная кислота: вода (2: 1:1) - (2); бензол:этанол (8:2) - (3); хлороформ:метанол: аммиак (7:2,5:0,5) - (4); хлороформ:метанол:аммиак (6:4:1) - (5); хлороформ: метанол:уксусная кислота (42:7:1) - (6); ацетон:бензол:уксусная кислота (50: 100:1) - (7); хлороформ:метанол (9:1) - (8); гексан:ацетон (3:2) - (9); метанол - (10).
Вещества обнаружили в УФ-свете с помощью нингидрина, реагентов Бартона, Паули и Рейнделя-Хоппе, о-толидина в среде хлора. Удельное вращение определяли на поляриметре марки "A1-ЕПО".
Проверку гомогенности пептида проводили в помощью высокоэффективной жидкостной хроматографии. Все растворители абсолютировали. Точки плавления не корректировали.
Принятые сокращения:
Z - бензилоксикарбонильная группа (КБЗ)
ДМФА - диметилформамид
ТЭА - триэтиламин
OMe - метиловый эфир
Obzl - бензиловый эфир
OBut - трет-бутиловый эфир
OEt - этиловый эфир
Boc - трет-бутилоксикарбонил
ТСХ - тонкослойная хроматография
ТФУ - трифторуксусная кислота
I.1. Z-Glu(OBut)-His-OMe. В колбе N1 13.5 г (40 ммол) Z-Glu(OBut)-OH растворяли в 50 мл хлористого метилена, охлаждали до +50oC и добавляли 5.6 мл (40 ммол) ТЭА. Реакционный раствор охлаждали до (-25) - (-30)oC. При этой температуре прибавляли из пипетки 5.30 мл (40 ммоль) изобутилового эфира хлормуравьиной кислоты. Температуру реакции удерживали в интервале (-18) - (-20)oC в течение 20 мин. Одновременно в колбе N2 готовили раствор 12.1 г (50 ммоль) 2•HClHis-OMe в 70 мл хлороформа, содержащего 14 мл (100 ммоль) ТЭА, и для полного растворения нагревали до 60oC. Раствор охлаждали до -25oC и после образования смешанного ангидрида глутаминовой кислоты в колбе N1 ее содержимое приливали сразу к раствору эфира в колбе N2. Температура реакционной смеси повышается до -10oC, эту температуру поддерживали 1 час, затем раствор оставляли на 1 час в холодильнике и выдерживали при 20oC еще в течение 3-х часов. Реакционный раствор упаривали, добавляли 300 мл этилацетата, полученный раствор промывали 3 раза по 30 мл H2O, 3 раза по 30 мл 10% Na2CO3, 3 раза по 30 мл H2O, 1 раз насыщенным раствором NaCl. Органический слой высушивали над MgSO4, фильтровали и упаривали. При упаривании выпадает осадок, который отфильтровывали, промывали на фильтре гексаном, сушили в вакууме. Остаток растирали с гексаном, отфильтровывали, сушили.
Выход - 18.36 г (94%). Т.пл. 98-100oC; [α]
Rf - 0.213(1), 0.64(2), 0.495(3), 0.428(6).
I.2. Z-Glu(OBut)-HisN2H3. 18 г (37 ммоль) Z-Glu(OBut)-His-OMe растворяли в 25 мл метанола и добавляли 6.9 мл (138 ммоль) гидразин-гидрата, перемешивали на мешалке при 20oC 72 часа. Реакционную смесь упаривали. Кристаллизовали из 50% метанола, выпавший осадок промывали на фильтре небольшим количеством воды и эфиром, сушили в вакууме над P2O5/KOH.
Выход - 13.7 г (76%). Т.пл. 145-147oC; [α]
Rf - 0.484(2), 0.206(3), 0.94(5), 0.114(6).
I.3. Z-Glu(OBut)-His-Phe-OMe. К охлажденному до -20oC раствору 8.8 г (18 ммоль) Z-Glu(OBut)-HisN2H3 50 мл ДМФА добавляли 15.5 мл (4 экв.) раствора хлористого водорода в этилацетате, 2.14 (18 ммоль) трет-бутилнитрита и перемешивали 30 мин при -5oC. Реакционную смесь охлаждали до -40oC и прибавляли охлажденный до -10oC раствор 4.34 г (18.9 ммоль) гидрохлорида метилового эфира фенилаланина в 30 мл ДМФА и 2.6 (18.9 ммоль) ТЭА. Выдерживали 72 часа при 4oC. Упаривали, добавляли 300 мл этилацетата. Этилацетатный раствор промывали H2O, 5% NaHCO3, H2O, 0.5% NH4OH, H2O, насыщенным раствором NaCl. Органический слой высушивали над MgSO4, фильтровали и упаривали. Остаток растирали с гексаном.
Выход - 11.35 г (97%). Т.пл. 85-90oC; [α]
Rf - 0.356(1), 0.68(2), 0.245(3).
I4. Z-Glu-(OBut)-His-PheN2H3 получали из Z-Glu(OBut)-His-Phe-OMe аналогично синтезу соединения Z-Glu(OBut)-HisN2H3.
Выход - 86% Т.пл. выше 200oC; [α]
II. 1. BocProGlyOEt. BocPro 8.3 г (38.45 ммоль) растворяли в 50 мл CH2Cl2, охлаждали до -25oC, добавляли 38.45 ммоль (5.38 мл) ТЭА. Реакционную смесь охлаждали до (-25) - (-30)oC. При этой температуре из пипетки прибавляли 38.45 ммоль (4.84 мл) изобутилового эфира хлормуравьиной кислоты. Температуру реакционной смеси удерживали в интервале (-18) - (-20)oC 20 минут. Одновременно готовили раствор 5.9 г (42.3 ммоль) избыток 1.1 HClGlyOEt в 75 мл хлороформа, содержащего 5.92 мл ТЭА. Раствор охлаждали до -25oC и после образования смешанного ангидрида в первой колбе ее содержимое приливали сразу же к раствору эфира. Реакционную смесь выдерживали при температуре + 4oC 12 часов при перемешивании на магнитной мешалке. Реакционную смесь упаривали, добавляли 250 мл этилацетата, раствор этилацетата промывали 3 раза по 25 мл 0.1 н. HCl, 3 раза по 25 мл H2O, 1 раз насыщенным раствором NaCl. Органический слой высушивали над MgSO4, фильтровали и упаривали. Остаток высушивали в вакууме над P2O5/KOH и парафином.
Выход - 10.2 г (30.3 ммоль), 78.83%.
Rf - 0.5(7), 0.862(8), 0.719(10).
II.2. BocProGlyN2H3. BocProGlyOEt 10.2 г (30.3 ммоль) растворяли в 80 мл абсолютного метанола, добавляли 4-кратный избыток гидразин-гидрата 5.88 мл (121.2 ммоль). Перемешивали 12 часов на магнитной мешалке при комнатной температуре. Реакционную смесь упаривали, два раза упаривали с эфиром, остаток заливали эфиром (5 мл) и оставляли в холодильнике на ночь (для лучшей кристаллизации добавляли затравку). Выпавшие кристаллы отфильтровывали, промывали на фильтре эфиром, сушили в эксикаторе.
Выход - 6.9 г (20.79 ммоль), 68.62%.
Rf - 0.284 (7), 0.474(8), 0.189(9), 0.472(10). Т.пл.98-100oC.
II. 3. BocProGlyProOBzl. К охлажденному до -20oC раствору BocProGlyN2H3 4.7 г (14.6 ммоль) в 40 мл диметилформамида добавляли 58.4 ммоль (4-кратный избыток) раствора хлористого водорода в этилацетате и сразу же 1.73 мл (14.6 ммоль) трет-бутилнитрита, реакционную смесь перемешивали 30 минут при -5oC. Реакционную смесь охлаждали до -40oC и добавляли охлажденный до -10oC раствор 8.2 мл (58.4 ммоль) ТЭА в 4 мл ДМФА; когда температура реакционной смеси повышалась до -20oC добавляли 3.7 г (15.3 ммоль) избыток 1.05 HClProOBzl в 20 мл ДМФА и 2.14 мл ТЭА. Выдерживали при 4oC 24 часа, перемешивая на магнитной мешалке. Реакционную смесь упаривали, остаток растворяли в 200 мл этилацетата и промывали 2 раза по 20 мл H2O, 3 раза по 20 мл 10% KHSO4, 3 раза по 20 мл H2O, 3 раза по 20 мл 5% NaHCO3, 3 раза по 20 мл H2O. Этилацетатный слой высушивали над MgSO4. Упаривали, остаток заливали небольшим количеством эфира (10 мл). Оставляли в холодильнике. Для лучшей кристаллизации продукта добавляли затравку. Выпавшие кристаллы отфильтровывали, промывали на фильтре небольшим количеством эфира. Сушили в эксикаторе.
Выход - 5.358 г (11.65 ммоль), 79.92%.
Rf - 0.326(7), 0.390(9), 0.947(8), 0,716(10).
Т.пл. 125-126oC, [α]
II.4. ТФУProGlyProOBzl, 5.358 г (11.65 ммоль) BocProGlyProOBzl растворяли в 29.13 мл хлористого метилена, добавляли 29.13 мл ТФУ, выдерживали 45 минут при комнатной температуре, два раза упаривали с абс. этанолом, два раза с бензолом, два раза с эфиром, растворяли в бензоле и заливали гексаном. Гексан сливали, а полученное масло сушили в экстракторе над P2O5/KOH и парафином.
Выход - 4.63 г (9.7 ммоль), 98%.
Rf - 0.043(7), 0.247(8), 0.018(9).
III. 1. Z-Glu(OBut)-His-Phe-Pro-Gly-Pro-OBzl получали из соединений Z-Glu(OBut)-His-PheN2H3 и ТФУPro-Gly-Pro-OBzl аналогично синтезу Z-Glu(OBut)-His-Phe-OMe.
Выход - 88%. Т.пл. 40o(разл); [α]
Rf - 0.196(1), 0.605(3), 0.956(4).
III.2. H-Clu(OBut)-His-Phe-Pro-Gly-Pro-OH. 12.28 г (12.8 ммоль) соединения Z-Glu(ОBut)-His-Phe-Pro-Gly-Pro-OBzl растворяли в 20 мл смеси метанол-уксусная кислота-вода (6:1:1) и гидрировали над Pd-чернью 24 часа. Pd-чернь отфильтровывали, раствор упаривали два раза с бензолом, два раза с абс. метанолом. Высаждали из абс. метанола этилацетатом.
Выход - 9,8 г (90%). Т.пл. 95-98oC (разл.); [α]
Rf - 0.340(4), 0.252(5).
III. 3. HClGlu-His-Phe-Pro-Gly-Pro-OH. Растворяли 12.28 г (12.8 ммоль) H-Glu(OBut)-His-Phe-Pro-Gly-Pro-OH в 19.2 мл 1н. HCl/CH3COOH, выдерживали 45 минут при 20oC. Реакционную смесь высаждали из абс. эфиром, полученный осадок переосаждали из абс. метанола этилацетатом. Пептид отфильтровывали и сушили в вакууме над KOH, P2O5 и парафином.
Выход - 11.7 г (95%). Т.пл. 120oC (разл.).
Rf - 0.257(5).
Пример 2. Активность заявляемого гексапептида как стимулятора памяти оценивали по его влиянию на обучение животных. Сравнивали активность заявляемого гексапептида и известного гептапептида Семакса. Эксперименты выполнены на самцах белых нелинейных крыс массой 180-220 г. Исследуемые пептиды вводили внутрибрюшинно в водном растворе, в дозе 0.05 мг/кг за 15 минут до опыта. Животным контрольной группы вводили дистиллированную воду в соответствующем объеме (1 мл/кг). Исследование поведенческих эффектов пептидов проводили при помощи следующих тестов:
1) Выработка условного пищедобывательного рефлекса на место в T-образном лабиринте. Животных в течение 4-х дней после предварительной адаптации обучали находить пищу в одном из отсеков лабиринта. В ходе эксперимента регистрировали: количество выполненных реакций (число заходов в подкрепляемый отсек лабиринта и съедания приманки); величину латентного периода выхода из стартовой камеры лабиринта; время выполнения реакции; количество ошибок (число заходов в неподкрепляемый отсек лабиринта). Препараты вводили ежедневно за 15 минут до сеанса обучения.
2) Выработка условного рефлекса пассивного избегания болевого раздражителя. Обучение проводилось в экспериментальной камере, разделенной перегородкой с отверстием на два отсека: один - ярко освещенный, другой - затемненный. В первый день эксперимента животное помещали в освещенный отсек камеры и регистрировали время перехода в темный отсек, в котором крысу подвергали неизбегаемому удару электрическим током. Через 72 часа проводили проверку выработки навыка пассивного избегания болевого раздражителя. Животное на 2 минуты помещали в светлый отсек камеры и регистрировали латентный период перехода в темный отсек и суммарное время, проведенное в светлом отсеке. Препараты вводили в первый день опыта за 15 минут до помещения животного в экспериментальную камеру.
3) Выработка условной реакции активного избегания болевого раздражителя. Животных обучали совершать прыжок на полку в ответ на условный сигнал (звук электрического звонка), избегая таким образом болевого раздражения электрическим током (безусловный раздражитель). Каждому животному предъявляли ежедневно по 10 сочетаний условного и безусловного раздражителей в течение 4-х дней. В ходе эксперимента регистрировали количество реакций (число избеганий болевого раздражителя в ответ на условный сигнал). Препараты вводили ежедневно за 15 минут до сеанса обучения.
Достоверность отличий между группами оценивали при помощи параметрических и непараметрических критериев.
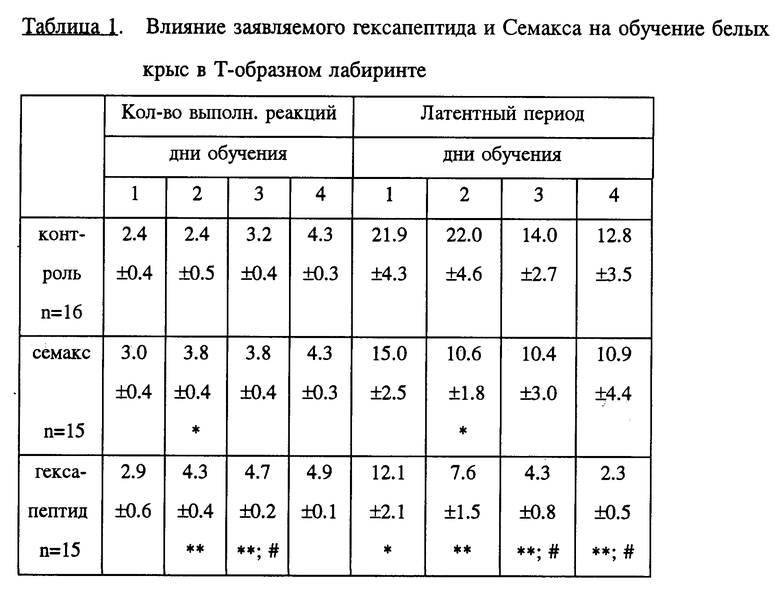
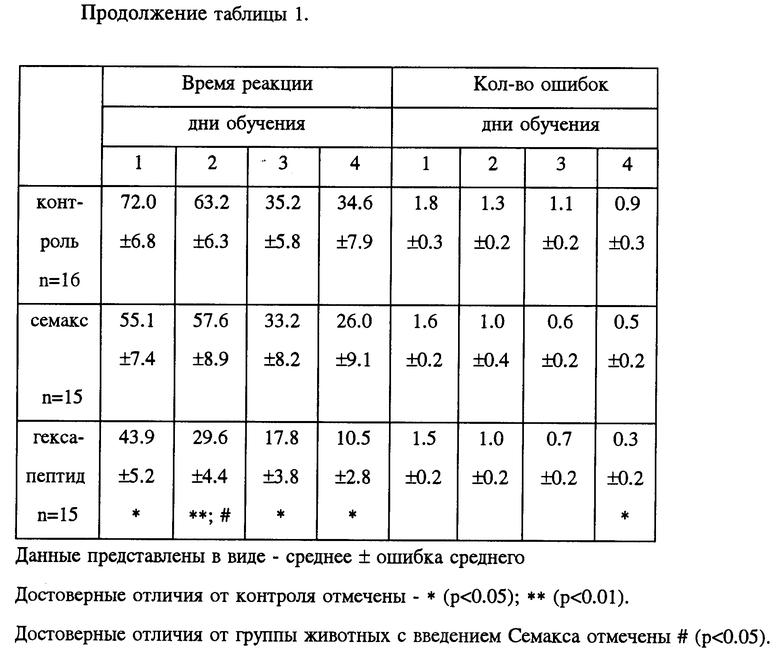
Исследовали влияние заявляемого гексапептида и известного гептапептида Семакса [3] на выработку условного пищедобывательного рефлекса на место в T-образном лабиринте. Результаты экспериментов представлены в табл. 1. Как видно из представленных данных, ежедневное введение гексапептида значительно ускоряет обучение животных в использованном тесте. В группе крыс, получивших инъекцию гексапептида, наблюдается достоверное увеличение количества выполненных реакций (на 80% и 46% во второй и третий дни обучения соответственно) по сравнению с контрольной группой. Кроме того, введение гексапептида вызывает значимое снижение величины латентного периода (на 45-82% в разные дни обучения), времени реакции (на 40-70%) и количества ошибочных реакций (на 60% в четвертый день обучения) по сравнению с контролем.
Сравнительный анализ активности заявляемого гексапептида и активности Семакса показал, что Семакс также ускоряет обучение животных в T-образном лабиринте (табл. 1.), однако его эффекты менее выражены, чем эффекты гексапептида. Количество выполненных реакций в группе животных, получавших гексапептид, достоверно выше, чем в группе крыс, которым вводили Семакс (на 24% в третий день обучения). Кроме того, введение гексапептида вызывает большее снижение латентного периода (на 60 и 79% в третий и четвертый дни обучения соответственно) и времени реакции (на 49% во второй день обучения), чем введение Семакса. На основании полученных результатов можно сделать вывод, что заявляемый гексапептид в дозе 0.05 мг/кг ускоряет выработку пищедобывательного рефлекса в T-образном лабиринте, причем его эффекты более выражены, чем эффекты Семакса.
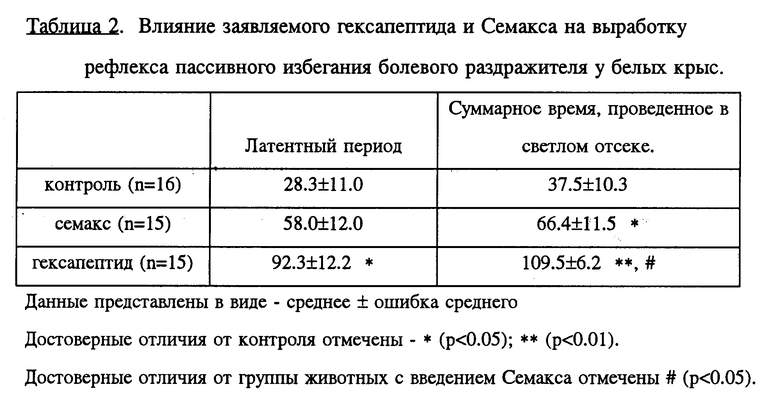
Изучали влияние заявляемого гексапептида и Семакса на выработку условного рефлекса пассивного избегания болевого раздражителя.
Результаты экспериментов представлены в таблице 2. Инъекция гексапептида значительно улучшает выработку навыка - величина латентного периода перехода из светлого отсека экспериментальной камеры в темный в 3.3 раза, а общее время, проведенное в светлом отсеке, в 2.9 раза больше в опытной группе, чем в контрольной. При этом величина показателей обучения в группе животных, получавших инъекцию гексапептида, в 1.6 раза больше, чем в группе крыс, которым вводили Семакс (p<0.05). Таким образом, можно заключить, что заявляемый гексапептид улучшает выработку условного рефлекса пассивного избегания эффективнее, чем Семакс.
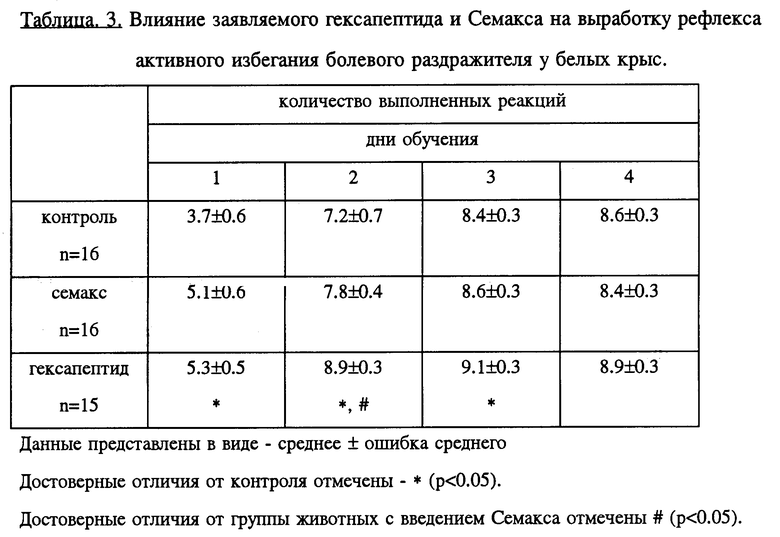
Исследовали влияние заявляемого гексапептида и Семакса на выработку условного рефлекса активного избегания болевого раздражителя.
Результаты экспериментов представлены в табл. 3. Как видно из представленных данных, ежедневное введение заявляемого гексапептида ускоряет выработку навыка избегания (количество выполненных реакций в опытной группе достоверно превышает величину этого показателя в контроле на 43, 23 и 8% в первый, второй и третий дни обучения соответственно). В группе животных, получавших инъекцию Семакса, также наблюдается увеличение количества выполненных реакций по сравнению с контролем (на 38 и 8% в первый и второй дни обучения соответственно), однако эти отличия не достигают уровня значимости (p=0.10). При этом количество выполненных реакций в группе животных с введением гексапептида достоверно (на 14%) превышает величину этого показателя в группе с введением Семакса.
Полученные результаты позволяют сделать вывод о том, что заявляемый гексапептид ускоряет выработку условного рефлекса активного избегания и его активность в этом тесте значительно превышает активность Семакса.
Таким образом, на основании полученных результатов можно заключить, что гексапептид формулы Glu-His-Phe-Pro-Gly-Pro ускоряет обучение животных в различных тестах, следовательно обладает активностью стимулятора памяти. При этом активность заявляемого гексапептида как стимулятора памяти значительно превышает активность гексапептида Семакс.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ АНТИКОАГУЛЯНТНО-ФИБРИНОЛИТИЧЕСКОЙ, АНТИТРОМБОЦИТАРНОЙ И АНТИТРОМБОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2286166C1 |
| ГЕПТАПЕПТИД, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ, СОЧЕТАЮЩЕЙСЯ С ТЕРМОРЕГУЛЯТОРНОЙ И/ИЛИ С СОСУДОДВИГАТЕЛЬНОЙ АКТИВНОСТЬЮ И/ИЛИ С ВЛИЯНИЕМ НА ПОВЕДЕНЧЕСКУЮ РЕАКЦИЮ ИСПЫТУЕМОГО, И СПОСОБ ИЗМЕНЕНИЯ ФИЗИОЛОГИЧЕСКОЙ АКТИВНОСТИ ДЕРМОРФИНА | 1997 |
|
RU2134121C1 |
| НООТРОПНОЕ СРЕДСТВО И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НООТРОПНОГО ДЕЙСТВИЯ | 1994 |
|
RU2045958C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИПСИХОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2411248C2 |
| РАВНОМЕРНОМЕЧЕННЫЙ ДЕЙТЕРИЕМ ИЛИ ТРИТИЕМ His-Phe-Arg-Trp-Pro-Gly-Pro | 2014 |
|
RU2544016C1 |
| Гептапептид в качестве стимулятора памяти пролонгированного действия | 1981 |
|
SU939440A1 |
| СЕМЕЙСТВО ПЕПТИДОВ, ОБЛАДАЮЩЕЕ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2286169C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНАЛОГОВ АДЕНОКОРТИКОТРОПНОГО ГОРМОНА (АКТГ), ПОСЛЕДОВАТЕЛЬНОСТИ (4-10), ОБЛАДАЮЩИХ НЕЙРОТРОПНОЙ АКТИВНОСТЬЮ, И ТЕТРАПЕПТИД ДЛЯ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2315057C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЧЕННЫХ ТРИТИЕМ ЛИНЕЙНЫХ ПЕПТИДОВ И ГЛИКОПЕПТИДОВ | 1983 |
|
SU1545503A3 |
| ГЕПТАПЕПТИД, ОБЛАДАЮЩИЙ СВОЙСТВАМИ ПСИХОСТИМУЛЯТОРА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ С ИММУНОТРОПНОЙ АКТИВНОСТЬ | 1983 |
|
RU1124544C |
Гексапептид может быть использован в медицине, а именно в области фармакологии. Получен новый физиологически активный гексапептид формулы Glu-His-Phe-Pro-Gly-Pro, обладающий активностью стимулятора памяти. Стимулирующая активность заявляемого препарата выявлена при обучении животных в различных тестах. Активность гексапептида значительно превышает активность известного стимулятора памяти препарата Семакс. Гексапептид ускоряет обучение животных в различных тестах. 3 табл.
Гексапептид формулы Glu-His-Phe-Pro-Gly-Pro, обладающий активностью стимулятора памяти.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Гептапептид в качестве стимулятора памяти пролонгированного действия | 1981 |
|
SU939440A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| НООТРОПНОЕ СРЕДСТВО И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НООТРОПНОГО ДЕЙСТВИЯ | 1994 |
|
RU2045958C1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Мышлякова Н.В., Клуша В.Е., Чипенс Г.И | |||
| Биологические свойства низкомолекулярных пептидов | |||
| Химико-фармацевтический журнал, 1981, т.15, N 1, c.10 - 20. | |||
Авторы
Даты
1999-06-20—Публикация
1998-04-27—Подача