Изобретение относится к области органической химии и может найти применение в аналитической химии и биологических исследованиях.
При изучении физиологически активных соединений необходимы их меченые аналоги.
Известно, что замена атомов соединений на их меченые аналоги не приводит к изменению каких-либо свойств исходного соединения (Evans E.A. - Tritium and its compounds London Butterworths, 1974, p. 48) [1].
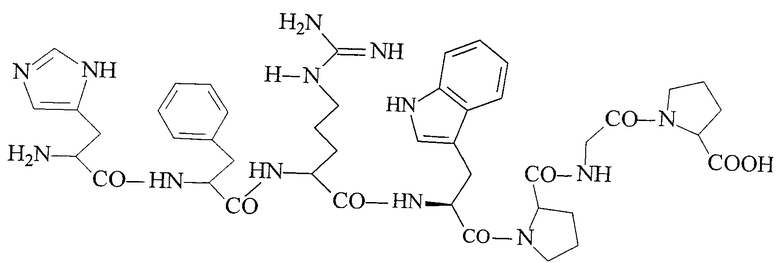
Известен His-Phe-Arg-Trp-Pro-Gly-Pro формулы I:
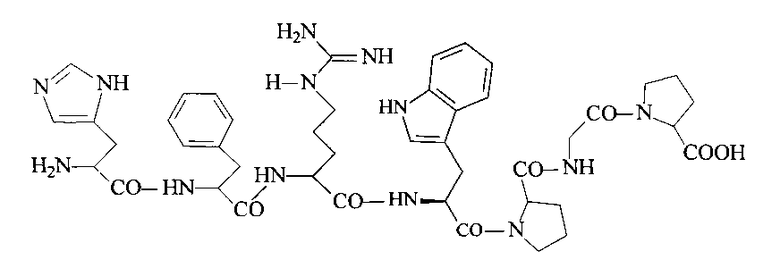
His-Phe-Arg-Trp-Pro-Gly-Pro - универсальный биорегулятор клеточных функций (регуляторный пептид) (Овчинников Ю.А. Биоорганическая химия. М. Просвещение. 1987. 815 с. [2]). Этот пептид кроме ноотропной и анксиолитической активности влияет на жизнеспособность клеток, вызывая статистически значимое увеличение. Показано его положительное биологическое воздействие на жизнеспособность in vitro глиальных клеток, полученных из коры больших полушарий мозга крыс, в условиях использования моделей ишемического инсульта. Сравнение активности пептида и семакса показало, что он при введении за 15 мин до сеанса обучения улучшает обучение животных эффективнее, чем семакс (Глазова Н.Ю., Левицкая Н.Г., Андреева Л.А., Каменский А.А., Мясоедов Н.Ф. // Докл. АН физиология. 1999. Т 367. №1, С. 137-140 [3]).
Однако его равномерномеченный дейтерием и тритием аналог не описан.
Техническим результатом, достигаемым настоящим изобретением, является расширение ассортимента меченых аналогов физиологически активных соединений.
Достигается указанный технический результат получением равномерномеченного дейтерием и тритием His-Phe-Arg-Trp-Pro-Gly-Pro формулы I:
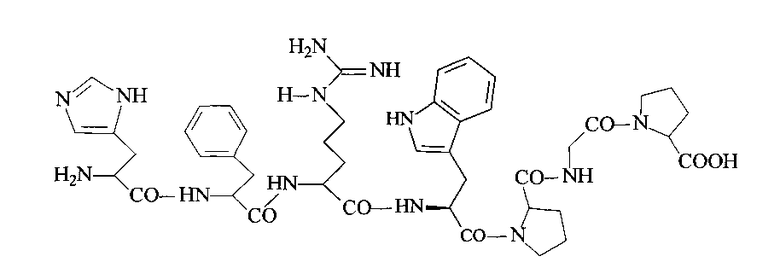
Ниже приведен пример реализации изобретения. Пример I.
Раствором 10 мг АКТГ(6-9)-PGP в 100 мкл метанола пропитывали 500 мг окиси алюминия и лиофилизировали. Высушенный остаток механически перемешивали с 20 мг 5% Pd/Al2O3.
В ампулу помещали 300 мг смеси, вакуумировали и заполняли газообразным дейтерием до давления 400 гПа. Реакцию вели при 200°C в течение 5 мин. Затем ампулу вакуумировали и вновь заполняли дейтерием и вели реакцию при 200°C в течение 7 мин. Ампулу снова вакуумировали, катализатор наносили на фильтр, вещество экстрагировали метанолом (5×2 мл). Экстракты упаривали, остаток растворяли в метаноле (3×1 мл) и вновь упаривали для удаления лабильного дейтерия.
По этой методике получен дейтерированный пептид, содержащий примерно 2.9 атома дейтерия. Распределение метки по данным масс-спектроскопии в аминокислотных фрагментах оказалось следующим (таблица 1).
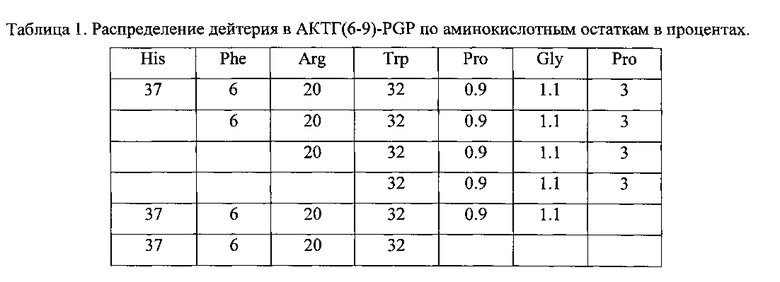
Пример II.
Раствором 10 мг АКТГ (6-9)-PGP в 100 мкл метанола пропитывали 500 мг окиси алюминия и лиофилизировали. Высушенный остаток механически перемешивали с 20 мг 5% Pd/Al2O3.
В ампулу помещали 130 мг смеси, вакуумировали и заполняли газообразным тритием до давления 400 гПа. Реакцию вели при 200°C в течение 15 мин. Ампулу снова вакуумировали, катализатор наносили на фильтр, вещество экстрагировали метанолом (5×0.5 мл). Экстракты упаривали, остаток растворяли в метаноле (3×1 мл) и вновь упаривали для удаления лабильного трития. Конечный метанольный раствор содержал 120 мКи пептида.
Равномерномеченные АКТГ(6-9)-PGP очищали препаративной высокоэффективной жидкостной хроматографией. После очистки радиохимическая чистота равномерномеченного АКТГ(6-9)-PGP - не менее 97-98%, выход - 30-40%, молярная радиоактивность - 26 Ки/ммоль (табл. 2).
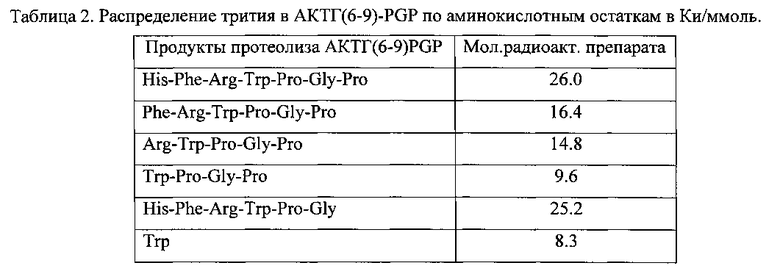
Анализ AKTT(6-9)-PGP проводили с использованием различных хроматографических систем.
Система 1: колонка ProntoSIL-120-5-C18 AQ DB-2003, 5.0 мкм, 2.0×75 мм; скорость элюции - 0.2 мл/мин, градиент 0-100, 12,5 мин; время удерживания АКТГ(6-9)-PGP - 7.55 мин.
Система 2: колонка Reprosil pur C18ag, 5 мкм, 4×150; система: А - вода-метанол-TFA (90:10:0.01), Б - метанол, градиент Б→0-100% за 15 мин, скорость элюции - 1 мл/мин; время удерживания АКТГ(6-9)-PGP - 9.29 мин.
Система 3: препаративную очистку АКТГ(6-9)-PGP проводили на колонке Kromasil 100C18, 8×150 мм, 7 мкм, система: А - вода-метанол-TFA (90:10:0.01), Б - метанол, градиент Б→0-100% за 30 мин, скорость потока - 2 мл/мин время удерживания - 17.45 мин.
Таким образом, получен равномерномеченный дейтерием и тритием His-Phe-Arg-Trp-Pro-Gly-Pro.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ ПИРО-Glu-His-Pro-NH | 2013 |
|
RU2513852C1 |
| МЕЧЕННЫЙ ТРИТИЕМ ПО ВСЕМ АМИНОКИСЛОТНЫМ ОСТАТКАМ 5-oxo-PRO-ARG-PRO | 2016 |
|
RU2624439C1 |
| МЕЧЕННЫЙ ДЕЙТЕРИЕМ Boc-Trp-Pro-Pro-Trp | 2024 |
|
RU2835090C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ДЕЙТЕРИЕМ ИЛИ ТРИТИЕМ 4-(2-АМИНОЭТИЛ)ПИРОКАТЕХОЛ С ИСПОЛЬЗОВАНИЕМ НАНОАЛМАЗНОГО ПОРОШКА | 2010 |
|
RU2422436C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЧЕННЫХ ТРИТИЕМ ЛИНЕЙНЫХ ПЕПТИДОВ И ГЛИКОПЕПТИДОВ | 1983 |
|
SU1545503A3 |
| ГЕКСАПЕПТИД, ОБЛАДАЮЩИЙ АКТИВНОСТЬЮ СТИМУЛЯТОРА ПАМЯТИ | 1998 |
|
RU2131743C1 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ 4-ИОДО-N-[4-МЕТОКСИ-3-(4-МЕТИЛ-1-ПИПЕРАЗИНИЛ)ФЕНИЛ]БЕНЗЕНСУЛЬФОНАМИД | 2012 |
|
RU2491281C1 |
| Равномерномеченный дейтерием и тритием 3-(1-метилпирролидин-2-ил)пиридин | 2014 |
|
RU2620190C2 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ [H]-14-ГИДРОКСИДАУНОМИЦИН АДРИАМИЦИНОНА | 2006 |
|
RU2305103C1 |
| Применение пептида His-Phe-Arg-Trp-Pro-Gly-Pro для профилактики дисбиоза при хроническом иммобилизационном стрессе | 2021 |
|
RU2770583C1 |
Изобретение относится к равномерномеченному дейтерием или тритием His-Phe-Arg-Trp-Pro-Gly-Pro, который может быть использован в аналитической химии и биологических исследованиях. 2 табл., 2 пр.
Равномерномеченный дейтерием или тритием His-Phe-Arg-Trp-Pro-Gly-Pro формулы I:
| СЕМЕЙСТВО ПЕПТИДОВ, ОБЛАДАЮЩИХ НЕЙРОТРОПНЫМИ СВОЙСТВАМИ | 2001 |
|
RU2206573C1 |
| Ю | |||
| А | |||
| Золотарев и др | |||
| Равномерно меченные тритием пептиды в исследованиях по их биодеградации in vivo и in vitro | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2015-03-10—Публикация
2014-03-13—Подача