Изобретение относится к органической химии, в частности к способу получения N,N-диметиламинометилированным ароматическим основаниям Шиффа формулы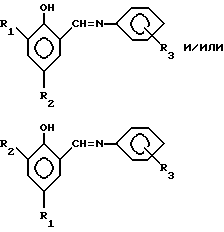
и/или
где R1 = H, R2 = -CHN(CH3)2);
R3 = H, o-CH3, n-CH3, n-OCH3, o-NO2, n-ON2, m-NO2,
которые могут быть использованы в качестве ускорителей отверждения эпоксидных смол.
Общеизвестно широкое применение в качестве ускорителей отверждения третичных аминов /Николаев А.Ф. "Химическая технология, свойства и применение пластических масс", Л., ЛГИ, 1977, с. 5./ Эффективными ускорителями процесса отверждения эпоксидных смол ангидридами карбоновых кислот являются 2,4,6-трис -/диметиламинометил/-фенол /Кошкин В.Р. и др. "Монолитные эпоксидные, полиуретановые и полиэфирные покрытия полов", М., Стройиздат, 1975, с. 10/ и 2,4,6-трис-/диметиламинометил/-резорцин /А.с. СССР N 407929/. Основания Шиффа как представители третичных аминов также используются для ускорения отверждения эпоксидных смол /А.с. СССР N 407929 и GB N 1377887./
Литературные источники утверждают, что все алифатические Шиффовы основания ускоряют реакцию сополимеризации эпоксидных смол. Причем, с увеличением количества азометиновых групп, ускоряющая способность этих соединений увеличивается /ЖПХ, 1990, В90, с.6084/. В литературе не описывается возможность использования ароматических оснований Шиффа в качестве ускорителей или самостоятельных отвердителей эпоксидных смол. Более того - утверждается, что азометиновые соединения, содержащие ароматическое ядро у третичного атома азота, лишены каталитической активности /ЖПХ, 1990, В90, с. 6084/, в отличие от алифатических оснований Шиффа.
На сегодняшний день известно большое количество изобретений по способу получения химических соединений по реакции Манниха в ряду ароматических соединений.
Описан способ получения продуктов реакции Манниха в ряду ароматических спиртов, например получение 2-N,N- /диметиламинометил/-фенола конденсацией фенола, формалина и амина в среде одноатомных спиртов С1-C5 /Chem. Ther., 1907, N2, s. 410/ или диоксана /J. Blass, Bull. Chem. France, 1966, 3120/. Выход целевого продукта составляет 85-90% от теории.
Известен способ получения выше упомянутых соединений конденсации фенола с N, N-тетраметилметиленбисамином /бисамином/ в среде органического растворителя /А. с. СССР N 1038339/, что является наиболее близким к заявляемому.
Несмотря на большое количество изобретений и разнообразие описанных способов получения продуктов реакции Манниха в ряду ароматических оснований, на сегодняшний день отсутствуют сведения о получении таковых для ароматических оснований Шиффа /АОШ/ формулы
и/или
и/или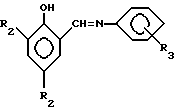
где R1 = H; R2 = -CH2N(CH3)2;
R3 = H, o-CH3, n-CH3, o-OCH3, n-OCH3, o-NO2, , n-NO2, m-NO2.
Целью изобретения является получение новых полифункциональных соединений - N,N-диметиламинометилированных АОШ, вышеуказанной формулы -, которые могут найти применение в качестве ускорителей отверждения эпоксидных смол или в качестве самостоятельных высокотемпературных отвердителей эпоксидных смол, т.е. появляется возможность использовать азометиновые соединения, содержащие ароматическое ядро у третичного атома азота.
Поставленная цель достигается тем, что исходные АОШ подвергают взаимодействию с N, N-тетраметилбисамином (бисамином) в среде C-C алифатических спиртов при мольном соотношении АОШ : бисамин : спирт, равном 1,0 : (2,1-2,5) : (2,5-10,0), при температуре 80-120oC и давлении 1-6 атм.
Процесс описывается следующими уравнениями:

и/или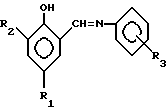
и/или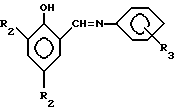
где R1 = H; R2 = -CH2N(CH3)2;
R3 = H, o-CH3, n-СН3, o-OCH3, n-ОСН3, o-NO2, n-NO2, m-NO2
Нами обнаружено, что использование доступного, дешевого бисамина, заявленные соотношения исходных реагентов и условия проведения синтезов позволяют получить аминометилированные ароматические основания Шиффа практически с количественными выходами и высокого качества. Данный способ получения безотходен, так как растворитель возможно вернуть в рецикл, а выделяющийся в ходе синтеза диметиламин можно использовать повторно, вернув его на стадию синтеза N,N'-тетраметилметиленбисамина. Каких-то других побочных продуктов в ходе синтеза не образуется.
Исходные реагенты должны соответствовать следующим требованиям:
1) салицилаланилин - (Бусев А.И. "Синтез новых органических реагентов для неорганического синтеза" МГУ, 1972, с. 82-94);
2) салицилиден-пара-толуидин - ТУ 6-09-06-699-75;
3) салицилиден-пара-анизидин - (Бусев А.И. "Синтез новых органических реагентов для неорганического синтеза" МГУ, 1972, с. 82-94
4) салицилиден-пара-нитроанилин - то же
5) салицилиден-мета-нитроанилин - то же;
6) салицилиден-орто-нитроанилин - то же;
7) салицилиден-орто-толуидин -
8) метанол - ГОСТ 6995-77;
9) этанол - ТУ 6-09-1710-77;
10) пропанол-1 - ТУ 6-09-4344-77;
11) изопропанол - ТУ 6-09-402-75;
12) бутанол-1 - ГОСТ 6006-78;
13) бутанол-2 - ТУ 6-09-08-1970-88;
14) изобутанол-1 - ГОСТ 6016-72;
15) пентанол-1 - ТУ 6-09-3467-78;
16) пентанол-2 - ТУ 6-09-3336-79.
17) Эпоксидная смола ЭД-20, УП606/2 - ГОСТ 10587-84;
18) Изометил-тетра-гидрофталевый ангидрид (ИМТГФА) - ТУ 38.103149-85.
Синтез аминометилированных АОШ осуществляют двумя способами.
Способ А осуществляли следующим образом.
В трехгорлую круглодонную колбу, снабженную механической мешалкой с гидрозатвором, газоотводящей трубкой с хлоркальциевым фильтром и обратным холодильником с охлаждающей ловушкой, термометром, загружают растворитель, АОШ, бисамин при их молярном соотношении АОШ : бисамин : спирт = 1,0 : (2,1-2,5) : (2,5-10,0). Выдерживают при температуре 80-120oC в течение 12-18 часов. Затем из реакционной смеси отгоняют растворитель и остатки бисамина. Получают прозрачную маслообразную жидкость от желтого до коричнево-вишневого цвета. Продукт переосаждают из соответствующего растворителя. После чего анализируют и определяют физико-химические константы.
Способ Б осуществляли следующим образом.
В автоклав загружают растворитель, АОШ, бисамин при их молярном соотношении АОШ : бисамин : спирт = 1,0 : (2,1-2,5) : (2,5-10,0). Выдерживают при температуре 110-130oC в течение 4-8 часов. Затем из реакционной смеси отгоняют растворитель и остатки бисамина. Получают прозрачную маслообразную жидкость от желтого до коричнево-вишневого цвета. Продукт переосаждают из соответствующего растворителя. После чего анализируют и определяют физико-химические константы.
Пример 1. Способ А.
В круглодонную колбу емкостью 100 мл, снабженную механической мешалкой, газоотводящей трубкой с хлоркальциевым фильтром и обратным холодильником с охлаждающей ловушкой, загружают 19,7 г (0,1 моль) салицилаланилина, 23 г (29,1 мл) этилового спирта (0,5 моль) и 25,5 г (34,5 мл) бисамина (0,25 моль). Реакционную смесь при перемешивании греют в течение 15 часов при температуре 80oC. Ход реакции контролируют с помощью индикаторной бумаги, следя за выделением диметиламина (ДМА), а также по анализу на пластинках с силуфолом (метод тонкослойной хроматографии). Затем отгоняют на роторной установке растворитель и остатки аминометилирующего агента. Выделяют прозрачную маслообразную жидкость желтого цвета. Переосаждают полученный продукт из соответствующего растворителя. Получают 29,85 г (96% от теоретического) продукта, характеризующегося следующими показателями.
Содержание титруемого азота, %: найдено - 8,68, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(арил)-бензальимин-2-ола, брутто формулы C19H25ON3 - 8,99%.
Элементный анализ:
вычислено, %: С-73,27; Н-8,09; N-13,49,
найдено, %: С-72,77; Н-8,11; N-12,99.
В ИК-спектре имеются: полоса поглощения 1622 см-1, характерная для C= N-группы; группа полос сильной интенсивности в области 2730-2980 см-1, характерная для -CH2-N(CH3)2 группы.
Пример 2. Способ Б.
В автоклав объемом 100 мл загружают 19,7 г (0,1 моль) салицилаланилина, 16 г (20,25 мл) метилового спирта (0,5 моль) и 21,4 г (28,9 мл) бисамина (0,21 моль). Автоклав герметизируют, нагревают реакционную массу при перемешивании до 110oC и выдерживают при этой температуре 4 часа. Затем автоклав захолаживают до 15-20oC и разгерметизировывают. Реакционную массу переливают в колбу и отгоняют растворитель и остатки бисамина. Выделяют прозрачную маслообразную жидкость желтого цвета. Переосаждают полученный продукт из соответствующего растворителя или смеси растворителей. Получают 30,25 (97,3% от теоретического) продукта, характеризующегося следующими показателями.
Содержание титруемого азота, %: найдено - 8,68, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(арил)-бензальимин-2-ола, брутто формулы C19H25ON3 - 8,99%.
Элементный анализ:
вычислено, %: С-73,27; Н-8,09; N-13,49.
найдено, %: С-72,87; Н-8,10; N-13,01.
В ИК-спектре имеются; полоса поглощения 1622 см-1, характерная для С= N-группы; группа полос сильной интенсивности в области 2730-2980 см-1, характерная для -CH2-N(CH3)2, группы.
Пример 3. Способ А.
21,1 г N-Салицилиден-п-толуидина (0,1 моль), 25,5 г (34,5 мл) бисамина (0,25 моль) и 60,1 г (77 мл) изопропанола (1,0 моль) греют при перемешивании при 83oC в течение 15 часов. Выделение продукта реакции осуществлялось аналогично примеру 1. Получают 30,2 г (92,8% с теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 8,38, вычислено для 3,5-ди-(N,N-диметиламинометил)-N-(пара-толуидин)- бензальимин-2-ола, брутто формулы С20H27ON3 - 8,60%.
Пример 4. Способ Б.
2-1,1 г N-Салицилиден-п-толуидина (0,1 моль), 21,4 г (28,9 мл) бисамина (0,21 моль) и 16 г (20,25 мл) метилового спирта (0,5 моль) нагревают в автоклаве при перемешивании до 110oC и выдерживают при этой температуре 4 часа. Выделение продукта реакции осуществлялось аналогично примеру 2. Получают 30,6 г (94,0% от теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 8,4, вычислено для 3,5-ди- (N,N-диметиламинометил)-N-(пара-толуидин)-бензальимин-2- ола, брутто - формулы С20H27ON3 - 8,6%.
Пример 5. Способ A.
22,7 г N-Салицилиден-п-анизидина (0,1 моль), 25,5 г (34,5 мл) бисамина (0,25 моль) и 37,1 г (46,1 мл) изобутанола греют при 100oC в течение 12 часов. Выделение продукта реакции осуществляли аналогично примеру 1. Получают 32,8 г (96,0% от теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 7,9, вычислено для 3,5-ди- (N,N-диметиламинометил)-N-(пара-анизидин)-бензальимин-2-ола, брутто формулы С20H27O2N3 - 8,2%.
Пример 6. Способ Б.
22,7 г N-салицилиден-п-анизидина (0,1 моль), 21,4 г (28,9 мл) бисамина и 16 г (20,25 мл) метилового спирта (0,5 моль) нагревают в автоклаве при перемешивании до 115oC и выдерживают при этой температуре 5 часов. Выделение продукта реакции осуществляли аналогично примеру 2. Получают 33,1 г (97,0% от теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 8,14, вычислено для 3,5-ди- (N,N-диметиламинометил)-N-(пара-анизидин)-бензальимин-2- ола, брутто формулы С20H27O2N3 - 8,20%.
Пример 7. Способ А.
19,7 г (0,1 моль) Салицилаланилина, 25,5 г (34,5 мл) бисамина (0,25 моль) и 16 г (0,5 моль) метилового спирта греют в течение 16 часов при температуре кипения метанола 64-65oC. После чего из реакционной смеси отгоняют растворитель и бисамин. Выделено 19,5 г (99,0% от теоретического) исходного салицилаланилина.
Пример 8. Способ А.
24,2 г (0,1 моль) N-Салицилиден-мета-нитроанилина, 25,5 г (34,5 мл) бисамина (0,25 моль) и 37 г (0,5 моль) бутанола-1 греют при температуре кипения реакционной смеси 117oC в течение 14 часов. Выделение продукта реакции осуществляли аналогично примеру 1. Получают 32,65 г (91,7% от теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 7,44, вычислено для 3,5-ди- (N,N-диметиламинометил)-N-(мета-нитроанилин)-бензальимин-2-ола, брутто формулы С19H24O3N4 - 7,89%.
Пример 9. Способ Б.
24,2 г (0,1 моль) N-Салицилиден-мета-нитроанилина, 21,4 г (28,9 мл) бисамина (0,21 моль) и 16 г (20,25 мл) метилового спирта (0,5 моль) нагревают в автоклаве при перемешивании до 120oC и выдерживают при этой температуре 7 часов. Выделение продукта реакции осуществляли аналогично примеру 2. Получают 33,5 г (94,0% от теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 7,54, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(мета-нитроанилин) -бензальимин-2-ола, брутто формулы С19H24О3N4 - 7,89%.
Пример 10. Способ A.
24,2 г (0,1 моль) N-Салицилиден-пара-нитроанилина, 25,5 г (34,5 мл) бисамина (0,25 моль) и 37 г бутанола-2 (0,5 моль) греют в течение 18 часов при температуре кипения реакционной смеси 117oC. Выделение продукта реакции осуществляли аналогично примеру 1. Получают 32,0 г (89,8% от теоретического) продукта, характеризующегося следующими показателями.
Содержание титруемого азота, %: найдено - 7,81, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(пара-нитроанилин)-бензальимин- 2-ола, брутто формулы С19H24O3N4 - 7,89%.
Пример 11. Способ Б.
24,2 г (0,1 моль) N-Салицилиден-пара-нитроанилина, 21,4 г (28,9 мл) бисамина (0,21 моль) и 16 г (20,25 мл) метилового спирта (0,5 моль) нагревают в автоклаве при перемешивании до 120oC и выдерживают при этой температуре 8 часов. Выделение продукта реакции осуществляли аналогично примеру 2. Получают 33,1 г (93,0% от теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 7,83, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(пара-нитроанилин)-бензальимин-2- ола, брутто формулы C19H24O3N4 - 7,89%.
Пример 12. Способ А.
22,7 г (0,1 моль) N-Салицилиден-пара-анизидина, 25,5 г (34,5 мл) бисамина (0,25 моль) и 44,0 г (54,0 мл) пентанола-1 (0,5 моль) греют при перемешивании при температуре 137,5oC в течение 15 часов. Выделение продукта реакции осуществляли аналогично примеру 1. Получают 31,75 (93,0% от теоретического) и 3,8 г пентанола-1, т.е. использование более высококипящего растворителя ведет к усложнению стадии выделения продукта.
Пример 13. Способ Б.
19,7 г (0,1 моль) N-Салицилиден-анилина, 21,4 г (28,9 мл) бисамина (0,21 моль) и 37,1 г (46,4 мл) изобутанола (0,5 моль) нагревают в автоклаве при перемешивании до 120oC и выдерживают при этой температуре 10 часов. Выделение продукта реакции осуществляли аналогично примеру 2. Получают 28,3 г (91,0% от теоретического) продукта, характеризующегося следующими показателями.
Содержание титруемого азота, %: найдено - 8,61, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(анилин)-бензальимин-2-ола, брутто формулы С19H25ON3 - 8,99%.
Пример 14. Способ A.
22,7 г (0,1 моль) N-Салицилиден-пара-толуидина, 61,26 г (82,8 мл) бисамина (0,6 моль) и 6,7 г (8,3 мл) бутанола-1 (0,09 моль) греют при перемешивании при температуре 110oC в течение 10 часов. Выделение продукта реакции осуществляли аналогично примеру 1. Получают 10,1 г 2-гидрокси-3- диметиламинометилбензальдегида и 20,5 г смолы не идентифицированного строения. Строение полученного продукта доказано методами ИК- и ПМР-спектроскопии. В ИК-спектре наблюдаются поглощения, характерные для валентных колебаний С=O (1663 см-1); OH (3051 см-1); N(CH3)2 (2854 и 2768 см-1) связей.
ПМР-спектр, м. д. : 2,23 с., 6Н(CH3); 6,81-7,47 м., 3H(ArCH); 9,75 с., 1H(CHO); 10,7 с., 1H(OH).
N (титр.) = 7,41%.
Пример 15. Способ А.
24,2 г (0,1 моль) N-Салицилиден-орто-нитроанилина, 25,5 г (34,5 мл) бисамина (0,25 моль) и 15 г (0,25 моль) пропанола-1 греют в течение 18 часов при температуре кипения реакционной смеси 97oC. Выделение продукта реакции осуществляли аналогично примеру 1. Получают 31,7 г (89,0% от теоретического) продукта, характеризующегося следующими показателями.
Содержание титруемого азота, %: найдено - 7,69, вычислено для 3,5-ди- (N, N-диметиламинометил)-N-(орто-нитроанилин)-бензальимин- 2-ола, брутто формулы C19H24O3N4 - 7,89%.
Пример 16. Способ Б.
24,2 г (0,1 моль) N-Салицилиден-орто-нитроанилина, 21,4 г (28,9 мл) бисамина (0,21 моль) и 16 г (20,25 мл) метилового спирта (0,5 моль) нагревают в автоклаве при перемешивании до 120oC и выдерживают при этой температуре 6 часов. Выделение продукта реакции осуществляли аналогично примеру 2. Получают 33,5 г (94,0% от теоретического) продукта, характеризующегося следующими показателями. Содержание титруемого азота, %: найдено - 7,78, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(орто-нитроанилин) -бензальимин-2-ола, брутто формулы С19H24O3N - 7,89%.
Пример 17. Способ Б.
21,1 г N-Салицилиден-о-толуидина (0,1 моль), 21,4 г (28,9 мл) бисамина (0,21 моль) и 16 г (20,25 мл) метилового спирта (0,5 моль) нагревают в автоклаве при перемешивании до 110oC и выдерживают при этой температуре 4 часа. Выделение продукта реакции осуществлялось аналогично примеру 2. Получают 31,25 г (96,0% от теоретического) продукта, характеризующегося следующими показателями.
Содержание титруемого азота, %: найдено - 8,4, вычислено для 3,5-ди- (N, N-диметиламинометил)-N-(орто-толуидин)-бензальимин-2-ола, брутто формулы С20H29ON3 - 8,6%.
Пример 18. Способ A.
21,1 г N-Салицилиден-о-толуидина (0,1 моль), 25,5 г (34,5 мл) бисамина (0,25 моль) и 88,15 г (108 мл) пентанола-2 (1,0 моль) греют при перемешивании при t = 118,5-119,5oC в течение 13 часов. Выделение продукта реакции осуществлялось аналогично примеру 1. Получают 30,85 г (94,8% от теоретического) продукта, характеризующегося следующими показателями.
Содержание титруемого азота, %: найдено - 8,38, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(орто-толуидин)- бензальимин-2-ола, брутто формулы C20H27ON3 - 8,60%.
Пример 19. Способ Б.
В автоклав объемом 100 мл загружают 19,7 г (0,1 моль) салицилаланилина, 16 г (20,25 мл) метилового спирта (0,5 моль) и 21,4 г (28,9 мл) бисамина (0,21 моль). Автоклав герметизируют, нагревают реакционную массу при перемешивании до 110oC и выдерживают при этой температуре 3 часа. Затем автоклав захолаживают до 15-20oC и разгерметизировывают. Реакционную массу переливают в колбу и отгоняют растворитель и остатки бисамина. Выделяют прозрачную маслообразную жидкость желтого цвета. Переосаждают полученный продукт из соответствующего растворителя или смеси растворителей. Получают 29,5 г (94,89% от теоретического) продукта, характеризующегося следующими показателями:
Содержание титруемого азота, %: найдено - 7,95, вычислено для 3,5-ди-(N, N-диметиламинометил)-N-(арил)-бензальимин-2-ола, брутто формулы C19H25ON3 - 8,99%.
В ИК-спектре имеются: полоса поглощения 1622 см-1, характерная для C=N группы; группа полос сильной интенсивности в области 2730-2980 см-1, характерная для -CH2-N(CH3)2 группы. Выделенный продукт анализировали методом высокоэффективной жидкостной хроматографии, расчет данных хроматографии по методу внутреннего стандарта позволяет сделать вывод о содержании состава смеси:
моно-маннихованного продукта - 30%,
ди-маннихованного продукта - 70%.
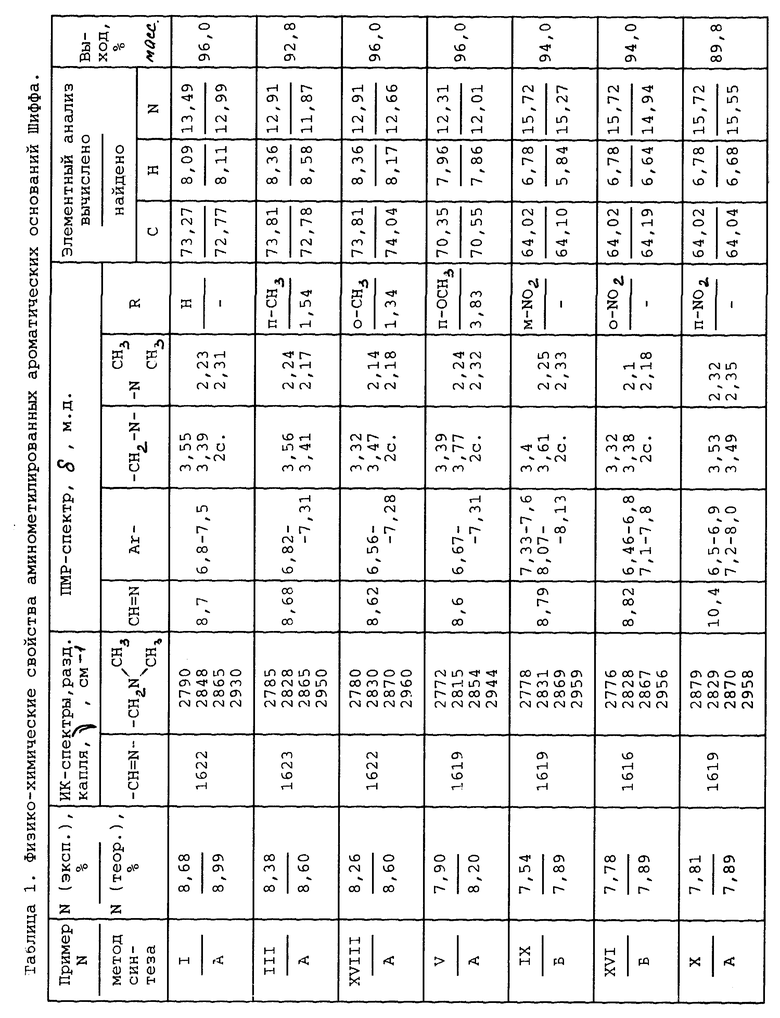
Строение полученных аминометилированных АОШ доказано методами ИК- и ПМР-спектроскопии, элементным анализом и данными потенциометрического титрования. Физико-химические константы ароматических азометинов заявленных в примерах 1-19 приведены в таблице 1.
Испытание синтезированных аминометилированных АОШ в качестве отвердителя провели по схеме /ЖПХ, 1990, В90, 6084/:
Отверждение композиций изучали с помощью дифференциального термического анализа (ДТА) в динамических условиях при скорости подъем температуры 5 град/мин. На термограммах фиксировали температуру экзотермического пика (Тмакс).
Термостойкость определяли с помощью термогравиметрического анализа (ДТГ) по температуре начала потери массы для композиций, отвержденных в динамических условиях при скорости нагрева 5 град/мин, и по температуре 5% потери массы для композиций, отвержденных в статических условиях.
Температуру стеклования (Тс) определяли дилатометрическим методом на приборе для ДТА и ДТГ - дериватографе, снабженном устройством для дилатометрических измерений.
Теплостойкость определяли на приборе Вика при нагрузке 49 Н.
Степень сшивки композиционных материалов находили экстрагированием кипящим ацетоном в аппарате Сокслета в течение 20 ч.
Пример 20 (прототип). Композиция, содержащая на 100 мас.ч. ЭД-20 70 мас. ч. ИМТГФА (изо-метил-тетрагидрофталевый ангидрид). Композицию отверждали в динамическом режиме при повышении температуры от 100oC до 350oC при скорости подъема температуры 5 град/мин.
Пример 21. Композиция, содержащая на 100 мас.ч. ЭД-20 70 мас.ч. ИМТГФА и 10 мас. ч. аминометилированных АОШ. Композицию отверждали в динамическом режиме при скорости нагрева 5 град/мин.
Данные дифференциального термического анализа (ДТА), результатов потенциометрического титрования представлены в таблице 2.
Пример 22 (прототип). Композиция, содержащая на 100 мас. ч. ЭД-20 70 мас. ч. ИМТГФА и 5 мас. ч. УП-606/2. Композицию отверждали в динамическом режиме при скорости нагрева 5 град/мин.
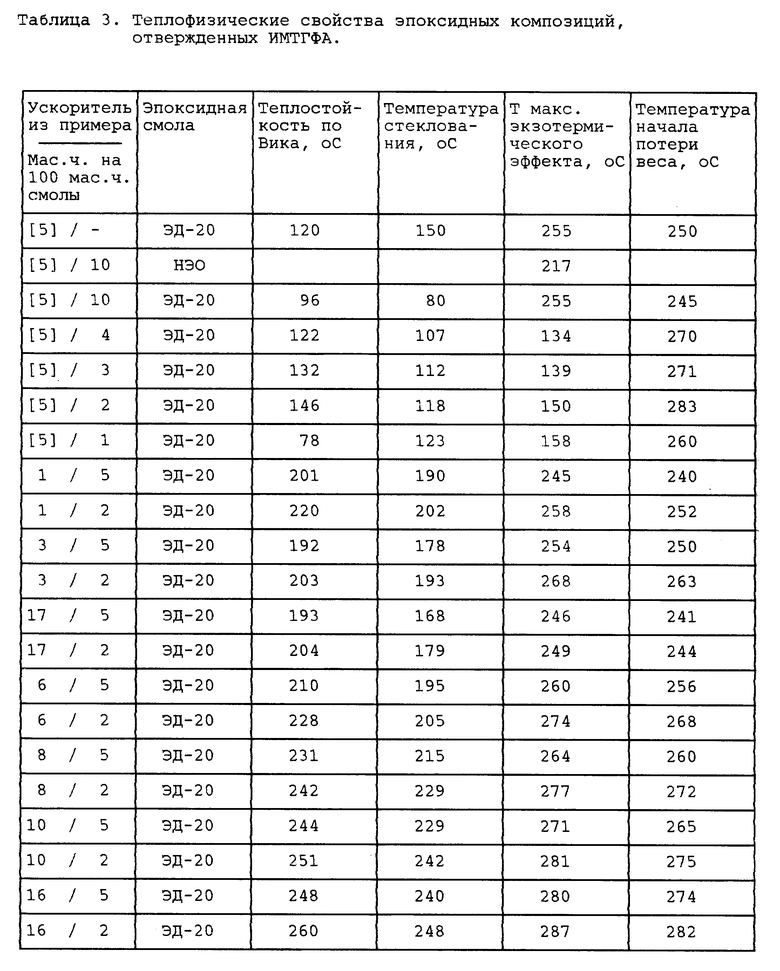
Данные теплофизических свойств эпоксидных композиций, полученных методом ДТА и методом термогравиметрического анализа, представлены таблице 3.
Композиции с аминометилированными АОШ в качестве ускорителя отверждения смолы ЭД-20 готовились аналогично примеру 22. Результаты представлены в таблице 2.
На основании представленных данных можно сделать вывод, что получены новые N, N-диметиламиномелированные основания Шиффа - 3,5-ди-(N,N-димeтилaминoмeтил-N-(apил)-бeнзaльимин-2-oлы, которые могут найти применение в качестве ускорителей отверждения эпоксидных смол.
Об их эффективности в качестве ускорителей реакции отверждения эпоксидных смол можно судить из данных, представленных в таблицах 2 и 3.

Предложены основания Шиффа формул I, II и III, где R1-H; R2-CH2N(CH3)2; R3-H, o-CH3, n-CH3, o-OCH3, n-OCH3, o-NO2, n-NO2, m-NO2, которые используются в качестве ускорителей отверждения эпоксидных смол. Соединения I,II,III получают взаимодействием ароматического основания Шиффа (АОШ) формулы (o-OH)C6H4-CH=N-C6H4-R3 с N,N-тетраметилметиленбисамином в среде С1-С5-алифатического спирта при молярном соотношении АОШ: бисамин: растворитель 1: (2,1-2,5): (2,5-10,0) в течение 4-18 ч при 18-120oC и давлении 1-6 атм. 2 с.п. ф-лы, 3 табл.
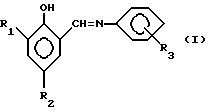
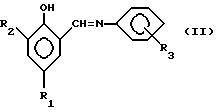

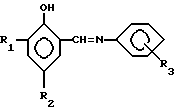
и/или
и/или
где R1 = H;
R2 = -CH2N(CH3)2;
R3 = H, o-CH3, n-CH3, o-OCH3, n-OCH3, o-NO2, n-NO2, m-NO2
в качестве ускорителей отверждения эпоксидных смол.
и/или
и/или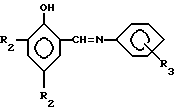
где R1 = H;
R2 = -CH2N(CH3)2;
R3 = H, o-CH3, n-CH3, o-OCH3, n-OCH3, o-NO2, n-NO2, m-NO2,
отличающийся тем, что ароматические основания Шиффа (АОШ) формулы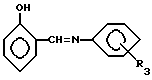
где R3 = H, o-CH3, n-CH3, o-OCH3, n-OCH3, o-NO2, n-NO2, m-NO2,
подвергают взаимодействию с N, N-тетраметилметиленбисамином в среде растворителя, выбранного из С1-С5-алифатических спиртов, при молярном соотношении АОШ : бисамин : растворитель 1,0 : (2,1 - 2,5) : (2,5 - 10,0), в течение 4 - 18 ч при 80 - 120oC и 1 - 6 атм.
| СПОСОБ ПОЛУЧЕНИЯ 5-ХЛОРСАЛИЦИЛИДЕН-4'-ДИМЕТИЛАМИНОАНИЛИНА И 5-ХЛОРСАЛИЦИЛИДЕН-4'-ДИЭТИЛАМИНОАНИЛИНА | 1966 |
|
SU214704A1 |
| 0 |
|
SU407929A1 | |
| 4-Окси-3-метоксибензилиденарилен(алкил)-имины как стабилизаторы смазочных масел | 1975 |
|
SU595299A1 |
| GB 1342214 A, 03.01.74 | |||
| US 4987255 A, 22.01.91 | |||
| Цифровой счетчик для счетных машин | 1934 |
|
SU43200A1 |
| Устройство для передачи и приема сигналов телеуправления | 1986 |
|
SU1377887A1 |
Авторы
Даты
1999-08-10—Публикация
1997-08-13—Подача