Изобретение относится к каталитической химии, в частности к получению ванадиевых катализаторов конверсии SO2 в SO3.
Известен способ приготовления катализатора для окисления диоксида серы, включающий смешение активных компонентов с синтетическим кремнеземом - силикагелем, полученным в два этапа: на первом - жидкое стекло и кислоту одновременно сливают при постоянных значениях pH 5.5 - 7.0, концентрации SiO2 80 - 100 г/л и скорости осаждения. На втором этапе - после длительного выдерживания (4 часа) в полученную суспензию вводят порошкообразный силикагель при определенном соотношении и с определенной величиной удельной поверхности. Пульпу высушивают, формуют, прокаливают. Способ позволяет получить высокоактивный катализатор, уменьшить количество сточных вод. Однако катализатор обладает достаточно высокой величиной кажущейся плотности и довольно низкой прочностью. (А.с. СССР N 1785733, 1993).
Известен также способ получения катализатора путем смешения раствора активных компонентов с гидрогелем, полученным осаждением из жидкого стекла в два этапа: на первом - из разбавленного раствора жидкого натриевого стекла (ρ ≈ 1.16 г/см3, т.е. 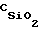 ≈ 130 г/л) гидрогель осаждают раствором сульфата алюминия до pH = 8.5. На втором - через 0.5 часа перемешивания добавляют серную кислоту
≈ 130 г/л) гидрогель осаждают раствором сульфата алюминия до pH = 8.5. На втором - через 0.5 часа перемешивания добавляют серную кислоту 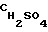 = 36%) до pH 1.5. Пульпу катализатора сушат, формуют и прокаливают. Способ позволяет получить высокоактивный катализатор, но насыпная плотность его весьма велика (см. табл.). Недостатком катализатора, полученного таким способом, является также довольно низкая механическая прочность. (А.С.СССР N 1616688, 1990).
= 36%) до pH 1.5. Пульпу катализатора сушат, формуют и прокаливают. Способ позволяет получить высокоактивный катализатор, но насыпная плотность его весьма велика (см. табл.). Недостатком катализатора, полученного таким способом, является также довольно низкая механическая прочность. (А.С.СССР N 1616688, 1990).
Цель изобретения - улучшение эксплуатационных характеристик катализатора - кажущейся плотности катализатора и механической прочности при сохранении высокой активности.
Цель достигается соблюдением ряда технологических приемов, обеспечивающих получение оптимальной структуры носителя, а именно: способ получения катализатора конверсии SO2 в SO3 включает смешение растворов активных компонентов, содержащих оксиды ванадия и щелочных металлов (К, Na, Cs, Rb) с синтетическим кремнеземом, полученным осаждением гидрокремнегеля из жидкого стекла раствором серной кислоты с последующей термообработкой и формовкой. Осаждение гидрокремнегеля проводят в два этапа: на первом этапе концентрацию диоксида кремния в пульпе поддерживают в пределах 50 - 160 г/л, при этом pH меняется от 12.5 - 10.5 до 4.0 - 8.5. На втором этапе концентрацию диоксида кремния скачкообразно повышают до 170 - 270 г/л путем добавления жидкого стекла, при этом значение pH возрастает до 12.0 - 9.0, после чего вновь приливают серную кислоту до pH 4.0 - 8.5.
Время приливания серной кислоты как на первом, так и на втором этапах составляет от 1 до 90 мин.
В контактном аппарате при заданной скорости газового потока реагентов для обеспечения заданной степени конверсии требуется определенное время контакта реагентов с катализатором, т.е. слой катализатора должен иметь определенную высоту, и значит не массу, а объем. Таким образом, расход загружаемого катализатора тем меньше, чем меньше его насыпная плотность, которая определяется порозностью слоя (долей пустого пространства между гранулами, т. е. их формой и размером) и кажущейся плотностью собственно массы катализатора.
Для гранул одинаковой формы и размера расход катализатора определяется только его кажущейся плотностью, которая зависит в значительной мере от его пористости.
Очевидно, что синтез катализатора с оптимальными эксплуатационными свойствами должен обеспечить наличие в нем оптимального по размерам и объему набора пор.
Эффективный катализатор должен содержать как тонкие поры, образующие развитую внутреннюю поверхность, так и средние и крупные. Объем двух последних должен быть достаточно большим, чтобы обеспечить низкую кажущуюся плотность, но и не чрезмерным, поскольку это может привести к снижению прочности катализатора.
При разработке способа получения носителя предпочтительнее пользоваться кажущейся плотностью, а не насыпной, т.к. кажущаяся плотность учитывает свойства только материала гранулы, а насыпная, кроме того, форму и крупность гранул.
Структура носителя в значительной мере задается условиями осаждения гидрогеля. Так, если оно проводится в условиях высоких концентраций SiO2 в пульпе, то образуется единовременно много первичных глобул (зародышей), которые, не успев вырасти, сразу слипаются между собой, образуя вторичные глобулы (агрегаты), обеспечивающие в дальнейшем наличие преимущественно крупных пор. Пульпа мгновенно "схватывается", т.е. превращается в нетекучую студнеобразную массу, которая после обезвоживания легко уплотняется. Формуется такой материал при малых усилиях, крупные поры легко "зажимаются", при этом общая пористость носителя недостаточна и мал объем тонких пор. Этим, по-видимому, объясняется пониженная активность и высокая величина кажущейся плотности. Пористость носителя можно было бы повысить за счет меньшего усилия при формовке, однако это приведет к резкому падению прочности.
В прототипе сделана попытка увеличить количество тонких и средних пор в катализаторе за счет получения более тонкопористого и менее "сминаемого" при формовке носителя. Это достигается использованием двух приемов:
1) осаждением геля из разбавленных растворов жидкого стекла, что позволяет иметь много индивидуальных зародышей, не агрегирующихся между собой;
2) выдерживанием раствора (0.5 часа) перед добавлением концентрированной кислоты, позволяющим даже в разбавленных растворах значительной доле глобул вырасти до разных размеров, что впоследствии обеспечит наличие не только мелких, но и средних пор.
Механизм формирования глобул поясняет сравнительный эксперимент, проведенный без указанного растягивания времени формирования глобул. Из разбавленного жидкого стекла образуется много мелких однородных по размеру неслипающихся зародышей, при этом пульпа сохраняет текучесть. После обезвоживания такого геля носитель имеет однородную тонкопористую структуру, в которой средние и крупные поры практически отсутствуют. Силикагель стекловиден, плохо сжимается, не формуется, имеет высокую кажущуюся плотность.
Таким образом, в прототипе созданы такие условия осаждения геля, которые закладывают образование мелких и средних пор, обеспечивающих активность при высокой механической прочности катализатора. Однако доля средних и крупных пор слишком мала, чтобы обеспечить низкую величину кажущейся плотности.
В предлагаемом решении осаждение гидрогеля на первом этапе идет из разбавленного жидкого стекла для обеспечения большого числа индивидуальных глобул и возможности их роста. На втором этапе к пульпе добавляют концентрированное жидкое стекло, т.е. скачкообразно повышают одновременно и концентрацию двуокиси кремния, и pH среды, после чего вновь добавляют серную кислоту. Образующийся в таком режиме носитель содержит поры и тонкие, и средние, и крупные. Он хорошо формуется, но не подвержен повышенной "сминаемости". Полученный на его основе катализатор обладает высокой активностью и пониженной кажущейся плотностью при высокой прочности. Возможно, высокое качество носителя связано со скачкообразным изменением концентрации SiO2 и соответственно pH.
Используемый в предлагаемом решении режим осаждения гидрокремнегеля в известной нам литературе не описан. Поскольку процесс гелеобразования сложен и многопараметричен, то механизм его формирования в данном случае может быть представлен лишь предположительно. Вероятно, на II этапе при повышении pH и, следовательно, повышении концентрации ионов OH- степень ионизации уже сформированных индивидуальных глобул возрастает. При последующем добавлении серной кислоты так же, как и у аналога, происходит агрегация глобул, поскольку концентрация SiO2 высока. Но в отличие от аналога эти агрегаты более "рыхлые" - ионизированные глобулы в них менее плотно упакованы, и поэтому у носителя кроме крупных пор, образованных агрегатами, появляются средние и тонкие, образованные зазорами между глобулами внутри агрегатов.
Предлагаемый способ регулирования структуры носителя более эффективен и надежен, чем у прототипа, поскольку обеспечивает больший объем крупных пор и не требует строгого соблюдения скорости слива кислоты (т.е. скорости изменения pH среды). Последнее затруднительно обеспечить во всем объеме промышленного реактора, учитывая особенности гелеобразующих структур. В предлагаемом способе структура носителя существенно не зависит от времени приливания серной кислоты в широком интервале как на I, так и на II этапе.
Пределы параметров обоснованы следующими закономерностями. На первом этапе при концентрации диоксида кремния менее 50 г/л образуется мало зародышей, снижается объем тонких пор, что приводит к уменьшению активности катализатора (см. таблицу). Повышение концентрации диоксида кремния выше 160 г/л приводит к снижению доли индивидуальных глобул, и уже на первом этапе начинается их агрегация. В результате из-за недостаточного количества тонких пор снижается активность катализатора при 420oC.
На втором этапе - при концентрации диоксида кремния менее 170 г/л образуются структуры с недостаточным количеством крупных пор и повышенной величиной кажущейся плотности. При концентрации выше 270 г/л ослабевает эффект "рыхлых" агрегатов, снижается объем тонких пор и активность при 420oC снижается.
Начальное значение pH на первом этапе задается свойствами раствора жидкого стекла, на втором этапе - определяется концентрациями растворов, используемых на первом этапе.
Величина конечного значения pH должна быть не менее 4.0 и не более 8.5, т.к. иначе снижается скорость фильтрации гидрокремнегеля.
Время приливания серной кислоты на первом и втором этапе должно быть не менее 1 мин, т.к. иначе возникает невоспроизводимость свойств катализатора, и не более 90 мин, т.к. в противном случае начинается процесс самопроизвольного уплотнения гелевой структуры, и кажущаяся плотность катализатора возрастает.
Сравнение предлагаемого решения с прототипом показывает, что оно обладает следующими отличиями:
- осаждение геля разбивается на два этапа, отличающихся концентрацией диоксида кремния, при этом второй этап осаждения ведут при повышенной концентрации диоксида кремния;
- в процессе осаждения наблюдается скачок pH, влияющий на характер роста полимеров, на степень их ионизации, а следовательно, на структуру носителя. Таким образом, заявляемый способ соответствует критерию "новизна".
Известны способы получения катализаторов данного класса, предполагающие ведение осаждения геля при высоких концентрациях диоксида кремния, однако из них не следует возможность получения при этом катализатора с низкой кажущейся плотностью, обладающих при этом высокой активностью и прочностью. Это позволяет сделать вывод о соответствии заявляемого способа критерию "существенные отличия".
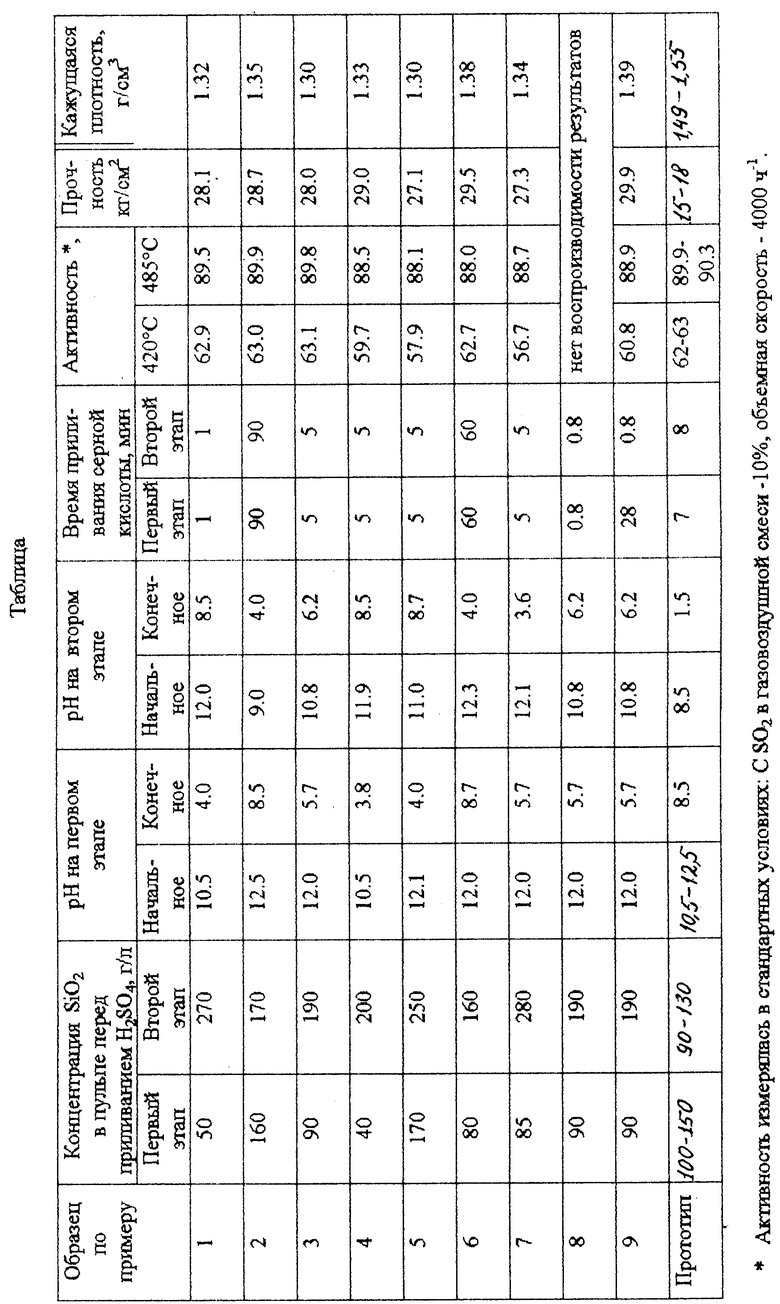
Порядок конкретной реализации способа описан в примерах, условия и свойства полученных катализаторов приведены в таблице.
Пример 1. Для приготовления носителя использовали стандартное жидкое натриевое стекло с плотностью 1.42 г/см3 и концентрацией SiO2 31.5%. К 201 мл жидкого стекла добавляли 1500 мл воды, раствор перемешивали в течение 5 мин. Концентрация SiO2 в растворе составила 50 г/л, pH среды - 10.5. Из разбавленного жидкого стекла на первом этапе осаждали гидрокремнегель, добавляя серную кислоту с концентрацией 92.5% в течение 1 мин до получения pH 4.0. К полученной пульпе на втором этапе доливали 799 мл стандартного жидкого стекла. Концентрация SiO2 в пульпе при этом составила 270 г/л, pH среды - 12.0. Далее вновь добавляли серную кислоту в течение 1 мин до получения pH 8.5. Пульпу гидрокремнегеля отфильтровывали, осадок промывали водой из расчета 15 л на 1 кг сухого SiO2.
Для приготовления 100 г катализатора к 50 г гидрокремнегеля (в расчете на сухой SiO2) добавляли 19.3 мл серной кислоты с содержанием H2SO4 92.5%, перемешивали в течение 1 ч, затем добавляли 82 мл раствора ванадата калия с концентрацией V2O5 92.5 г/л и K2O 171 г/л и перемешивали в течение 1 ч.
Пульпу упаривали досуха, полученный порошок увлажняли и экструдировали, гранулы сушили и прокаливали при 500oC в течение 2 ч.
Катализатор имел следующий состав, мас.%:
V2O5 - 7.5
K2O - 14.0
Na2О - 2.4
SiO2 - 50.0
Носитель - остальное
Пример 2. Катализатор готовили по примеру 1.
Концентрация SiO2 на первом этапе составляла 160 г/л, на втором -170 г/л; pH начальное соответственно - 12.5 и 9.0; pH конечное соответственно - 8.5 и 4.0; время приливания серной кислоты соответственно - 90 мин и 90 мин.
Пример 3. Катализатор готовили по примеру 1.
Концентрация SiO2 на первом этапе составляла 90 г/л, на втором - 190 г/л; pH начальное соответственно - 12.0 и 10.8; pH конечное соответственно - 5.7 и 6.2; время приливания серной кислоты соответственно - 5 мин и 5 мин.
Катализатор имел следующий состав, мас.%:
V2O5 - 9.5
K2O - 17.2
Na2O - 3.5
SO3 - 34.9
Носитель - остальное
Пример 4. Катализатор готовили по примеру 1.
Концентрация SiO2 на первом этапе составляла 40 г/л, на втором - 200 г/л; pH начальное соответственно - 10.5 и 11,9; pH конечное соответственно - 3.8 и 8.5; время приливания серной кислоты соответственно - 5 мин и 5 мин.
Пример 5. Катализатор готовили по примеру 1.
Концентрация SiO2 на первом этапе составляла 170 г/л, на втором - 250 г/л; pH начальное соответственно - 12.1 и 11.0; pH конечное соответственно - 4.0 и 8.7; время приливания серной кислоты соответственно - 5 мин и 5 мин.
Пример 6. Катализатор готовили по примеру 1.
Концентрация SiO2 на первом этапе составляла 80 г/л, на втором - 160 г/л; pH начальное соответственно - 12.0 и 12.3; pH конечное соответственно - 8.7 и 4.0; время приливания серной кислоты соответственно - 60 мин и 60 мин.
Пример 7. Катализатор готовили по примеру 1.
Концентрация SiO2 на первом этапе составляла 85 г/л, на втором - 280 г/л; pH начальное соответственно - 12.0 и 12.1; pH конечное соответственно - 5.7 и 3.6; время приливания серной кислоты соответственно - 5 мин и 5 мин.
Пример 8. Катализатор готовили по примеру 3.
Время приливания серной кислоты на первом этапе составляло 0.8 мин, на втором - 8 мин.
Пример 9. Катализатор готовили по примеру 3.
Время приливания серной кислоты на первом этапе составляло 28 мин, на втором - 8 мин.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА КОНВЕРСИИ SO В SO | 1998 |
|
RU2135282C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА КОНВЕРСИИ SO В SO | 2001 |
|
RU2186620C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА КОНВЕРСИИ SO В SO | 1998 |
|
RU2134158C1 |
| КАТАЛИЗАТОР КОНВЕРСИИ SO В SO | 1998 |
|
RU2134612C1 |
| КАТАЛИЗАТОР КОНВЕРСИИ SO В SO | 2000 |
|
RU2162367C1 |
| КАТАЛИЗАТОР КОНВЕРСИИ SO В SO | 2003 |
|
RU2242280C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА КОНВЕРСИИ SO В SO С ИСПОЛЬЗОВАНИЕМ ОТРАБОТАННОГО ВАНАДИЕВОГО КАТАЛИЗАТОРА | 1998 |
|
RU2129916C1 |
| КАТАЛИЗАТОР КОНВЕРСИИ SO2 В SO3 | 2003 |
|
RU2244590C1 |
| ШИХТА ДЛЯ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА КОНВЕРСИИ ДИОКСИДА СЕРЫ В ТРИОКСИД СЕРЫ | 2006 |
|
RU2314868C1 |
| Катализатор для конверсии So @ в So @ | 1987 |
|
SU1616688A1 |
Способ получения катализатора для конверсии SO2 в SO3 включает смешение растворов активных компонентов, содержащих оксиды ванадия и щелочных металлов (К, Na, Cs, Rb) с синтетическим кремнеземом с последующей термообработкой и формовкой. При этом кремнезем получают осаждением из жидкого стекла раствором серной кислоты в два этапа: на первом концентрацию диоксида кремнезема перед приливанием серной кислоты поддерживают 50-160 г/л, рН меняется от 12,5-10,5 до 4,0-8,5, на втором скачкообразно повышают концентрацию до 170-270 г/л и рН до 12,0-9,0 добавлением жидкого стекла, после чего вновь приливают серную кислоту до рН 4,0-8,5. Способ улучшает эксплуатационные характеристики катализатора - кажущуюся плотность катализатора и механическую прочность при сохранении высокой активности. 1 з. п. ф-лы, 1 табл.
| Катализатор для конверсии So @ в So @ | 1987 |
|
SU1616688A1 |
| SU 1785733 А1, 07.01.93 | |||
| DE 3322940 А1, 03.01.85 | |||
| DE 3033319 А1, 08.04.82. | |||
Авторы
Даты
1999-08-27—Публикация
1998-05-12—Подача