Изобретение относится к области исследования и анализа химических свойств вещества, а именно к исследованиям веществ в растворах с использованием фермента люциферазы, и может быть использовано в аналитической химии для экспрессного обнаружения люизита в водно-спиртовых экстрактах из различных сред при решении задач контроля загрязнений окружающей среды, а также экологического мониторинга в местах хранения и уничтожения запасов люизита.
Известен способ обнаружения люизита в водно-спиртовых экстрактах, в котором используют метод отгона образующегося в реакции со щелочью ацетилена с помощью водорода. Определение концентрации люизита или его оксида в исследуемом растворе производится колориметрическим методом по образованию розовой или вишневой окраски раствора. Предел обнаружения составляет 3-5 • 10-5 мг/мл (см. Руководство по работе в автомобильной радиометрической и химической лаборатории АЛ-4М. - М: Воениздат, 1988).
К причинам, препятствующим достижению указанного ниже технического результата при использовании известного способа, относится то, что в известном способе не достигается требуемая чувствительность обнаружения, возможность проведения количественных измерений концентраций люизита, необходимая производительность проведения анализа, а процесс выполнения измерения является трудоемким и требует высокой квалификации оператора.
Известен также способ определения люизита по выделяющемуся в процессе реакции с концентрированной серной кислотой в присутствии сернокислой меди и металлического цинка мышьяковистого водорода с последующим его взаимодействием с индикаторной бумагой и уксусно-свинцовой ватой (см. Руководство по работе в автомобильной радиометрической и химической лаборатории АЛ-4М. - М: Воениздат, 1988).
Наиболее близким способом того же назначения к заявленному изобретению по совокупности признаков является способ определения люизита в водно-спиртовых растворах, в котором путем взаимодействия анализируемого образца с реактивами судят о наличии люизита в данных растворах. Способ заключается в следующем: в пробирку к 4-6 мл исследуемого водно-спиртового раствора прибавляют 0.5 мл 30%-ного раствора едкого кали, раствор перемешивают и по истечении 4-5 мин подкисляют концентрированной уксусной кислотой до слабокислой реакции по лакмусу, приливают 0.5 мл реактива на ацетилен, состоящего из меди азотнокислой, аммиака, гидроксиламина солянокислого, желатина и спирта этилового. Окрашивание раствора в розовый или вишневый цвет и выпадение хлопьевидного осадка такого же цвета указывает на присутствие люизита или его оксида. Чувствительность определения 0.003-0.005 мг/мл (см. Руководство по работе в автомобильной радиометрической и химической лаборатории АЛ-4М. - М: Воениздат, 1988). Данный способ принят за прототип.
К причинам, препятствующим достижению указанного ниже технического результата при использовании известного способа, принятого за прототип, относится то, что в известном способе не достигается требуемая чувствительность обнаружения и производительность проведения анализов, возможность количественного измерения концентраций люизита в водно-спиртовых растворах, а процесс выполнения измерения является трудоемким и требует высокой квалификации оператора.
Задача изобретения - повышение чувствительности, производительности, возможность проведения измерения концентраций, а также снижение трудоемкости операций при обнаружении люизита в водно-спиртовых растворах вследствие применения биохимической реакции на основе взаимодействия фермента люциферазы с люизитом и последующим измерением интенсивности биолюминесценции.
Задача достигается тем, что в качестве реактива используется раствор, содержащий фермент люциферазу, миристиновый альдегид и флавинмононуклеотид, восстановленный в натрий-фосфатном буфере, а о наличии и величине концентрации люизита судят по отношению интенсивностей биолюминесценции в контрольной и опытной пробах.
При протекании биохимической реакции происходит генерация квантов света в видимой области спектра с длиной волны 490 нм, которые регистрируются ФЭУ. Квантовый выход реакции очень высок. В связи с этим возможна регистрация малейших изменений интенсивности биолюминесценции, вызванных изменением активности фермента под действием люизита. Кроме того, люцифераза является тиоловым ферментом, который резко снижает свою активность под действием тиоловых ядов, к которым относится люизит и который блокирует SH-группы активного центра фермента. Данное обстоятельство обеспечивает высокую чувствительность обнаружения люизита. Кроме того, биолюминесцентная реакция под действием фермента люциферазы протекает очень быстро. Время достижения максимальной интенсивности свечения составляет 2-3 с, что обеспечивает возможность получения информации о пробе при автоматизации процесса обработки информации в течение 10-20 с. Это позволяет достигать высокую производительность проведения анализа.
Пример проведения анализа.
Анализ проводят при температуре воздуха 20-22oC и влажности воздуха 65%.
Стандартные концентрации люизита создают методом последовательных разбавлений на 10%-ном этиловом спирте.
Получение субстрата люциферазной реакции (ФМН•H2) осуществляют искусственным путем с последующим введением в реакционную среду.
Биолюминесцентная реакция, запускаемая восстановленным флавинмононуклеотидом (ФМНH2), катализируется люциферазой. Чувствительность обнаружения люизита определяют по формуле: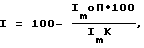
где Imоп, Imк - средние максимальные значения интенсивности свечения в опытной и контрольной пробах соответственно (определяют по результатам трех измерений).
При контрольных измерениях в биолюминесцентной системе, запускаемой ФМНH2, используют реакционную смесь следующего состава: 50 мкл 0.0005%-ной суспензии тетрадеканаля в воде, 20 мкл препарата люциферазы из Photobacterium leiognathi (активность 10 мВ/мкл, содержание белка - 0.18 мг/л), 50 мкл 0.1 М фосфатного буфера, pH 7.0; 200 мкл 10% C2H5OH и 500 мкл раствора ФМНH2 (5.4•10-4 М).
Для опытной пробы к реакционной смеси вместо 200 мкл 10%-ного этилового спирта добавляют раствор люизита заданной концентрации в 10% C2H5OH, остальные растворы те же.
Подготовка измерений.
Добавляют 10 мл 0.1 М натрий-фосфатного буфера (pH 7.0) к препарату люциферазы и тщательно перемешивают, не вспенивая. Добавляют к 50 мкл альдегида 5 мл H2O и тщательно перемешивают. Приготовляют растворы люизита. Заполняют резервуар для ФМНH2 раствором ФМН с ЭДТА, включают лампу, через 10 мин после восстановления ФМН (обесцвечивания раствора) приступают к анализу.
Процедура измерения.
Кювету, содержащую 50 мкл раствора миристинового альдегида, 20 мкл раствора препарата люциферазы и 50 мкл 0.1 M натрий-фосфатного буфера (pH 7.0), 200 мкл 10% C2H5OH помещают в биолюминометр и добавляют 500 мкл ФМНH2. Записывают динамику свечения в контроле или определяют максимальную интенсивность свечения. В кювету, содержащую 50 мкл раствора альдегида, 20 мкл раствора препарата люциферазы, добавляют 200 мкл раствора люизита и 50 мкл 0.1 М натрий-фосфатного буфера (pH 7.0), помещают в биолюминометр и добавляют 500 мкл ФМНH2. Записывают динамику свечения и определяют Im. Для уменьшения ошибки измерения проводят при постоянной температуре.
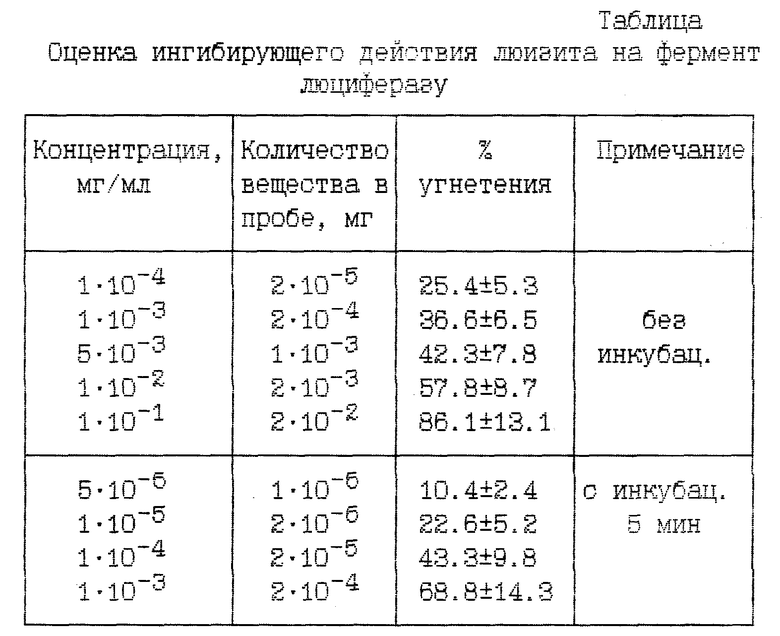
В таблице представлены результаты по проверке способа на чувствительность определения люизита.
Данные, представленные в таблице, свидетельствуют о том, что способ позволяет проводить определение люизита в водно-спиртовых экстрактах с чувствительностью 5•10-6 мг/мл или 1•10-6 мг в пробе.
Таким образом, предлагаемое изобретение предназначено для использования в промышленности, а именно в аналитической химии, для экспрессного обнаружения люизита в водно-спиртовых экстрактах из различных сред при решении задач контроля загрязнений окружающей среды, а также экологического мониторинга в местах хранения и уничтожения запасов люизита и подтверждена возможность его осуществления с помощью описанных в заявке известных средств и методов.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОЛЮМИНЕСЦЕНТНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ АКТИВНОСТИ ГУМИНОВЫХ ВЕЩЕСТВ | 2007 |
|
RU2376380C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО МНОГОКОМПОНЕНТНОГО РЕАГЕНТА ДЛЯ БИОЛЮМИНЕСЦЕНТНОГО АНАЛИЗА | 2003 |
|
RU2252963C1 |
| БИОЛЮМИНЕСЦЕНТНЫЙ БИОМОДУЛЬ ДЛЯ АНАЛИЗА ТОКСИЧНОСТИ РАЗЛИЧНЫХ СРЕД И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2009 |
|
RU2413772C2 |
| Способ определения активности протеаз | 1981 |
|
SU1027615A1 |
| ЭКСПРЕСС-СПОСОБ БИОТЕСТИРОВАНИЯ ПРИРОДНЫХ, СТОЧНЫХ ВОД И ВОДНЫХ РАСТВОРОВ | 2009 |
|
RU2413771C2 |
| СПОСОБ ДИАГНОСТИКИ АСПИРИНОРЕЗИСТЕНТНОСТИ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2007 |
|
RU2348041C1 |
| Способ определения количества высокомолекулярных спиртов в растворе | 1987 |
|
SU1495382A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВОВ У БОЛЬНЫХ ОСТРЫМ ЛЕЙКОЗОМ | 2012 |
|
RU2478206C1 |
| Способ определения уровня стрессоустойчивости человека | 2017 |
|
RU2665144C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОВТОРНЫХ ЦЕРЕБРОВАСКУЛЯРНЫХ ОСЛОЖНЕНИЙ У БОЛЬНЫХ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНЬЮ В СОЧЕТАНИИ С ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА В ОСТРОМ ПЕРИОДЕ ИШЕМИЧЕСКОГО ИНСУЛЬТА | 2010 |
|
RU2425640C1 |
Способ применяется для экспрессного обнаружения люизита в водно-спиртовых экстрактах из различных сред при решении задач контроля загрязнений окружающей среды, а также экологического мониторинга в местах хранения и уничтожения запасов люизита. При проведении анализа в качестве реактива используется раствор, содержащий фермент люциферазу, миристиновый альдегид и флавинмононуклеотид, восстановленный в натрий-фосфатном буфере, а о наличии и величине концентрации люизита судят по отношению интенсивностей биолюминесценции в контрольной и опытной пробах при длине волны 490 нм. Технический результат - повышение чувствительности, производительности, а также снижение трудоемкости процесса. 1 табл.
Способ определения люизита в водно-спиртовых экстрактах, основанный на взаимодействии анализируемого образца с реактивами, отличающийся тем, что в качестве реактива используется раствор, содержащий фермент люциферазу, миристиновый альдегид и флавинмононуклеотид, восстановленный в натрий-фосфатном буфере, а о наличии и величине концентрации люизита с чувствительностью 5•10-6 мг/мл или 1•10-6 мг в пробе судят по отношению интенсивностей биолюминесценции в контрольной и опытной пробах при длине волны 490 нм.
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| - М.: Воениздат, 1988 | |||
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ДИФЕНИЛАМИНОХЛОРАРСИНА | 1993 |
|
RU2084870C1 |
| Франке З | |||
| Химия отравляющих веществ | |||
| - М.: Химия, 1973, т.2, с.52-61, 100-101 | |||
| Егоров П.Т., Шляхов И.А., Алабин Н.И | |||
| Гражданская оборона | |||
| - М.: Высшая школа, 1977, с.123-127. | |||
Авторы
Даты
1999-11-10—Публикация
1998-02-03—Подача