Изобретение относится к амидам карбамоилкарбоновой кислоты общей формулы I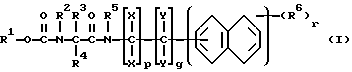
а также к их солям, где переменные имеют следующее значение:
R1 - C1-C8-алкил, R2 - водород, R3 - C1-C8-алкил, R4 и R5 - водород, X независимо друг от друга - водород, C1-C8-алкил, Y независимо друг от друга и независимо от указанных означает один из радикалов X; p, q независимо друг от друга означают 0, 1 при условии, что оба одновременно не могут иметь значение 0, r = 0, 1, 2, R6 - C1-C8-алкил, C1-C4-алкокси, галоген.
Соединения типа I, обладающие фунгицидным действием, уже известны из следующих публикаций: прежде всего из европейской заявки EP-A 554729 и заявки германии DE-A 4321897, а также из европейских заявок EP-A 398072, ЕР А 425925, EP-A 472996, EP-A 477639, EP-A 485794, EP-A 493683, EP-A 496239, EP-A 550788 и EP-A 587110. Однако по своей фунгицидной эффективности известные соединения пока еще не удовлетворяют соответствующим требованиям.
Исходя из этого, в основу изобретения была положена задача получить новые амиды карбамоилкарбоновой кислоты, которые обладали бы более эффективным действием против вредоносных грибов.
В соответствии с этой задачей были получены указанные выше соединения формулы I, их соли, а также содержащие их средства.
Далее, был создан способ получения соединений I и содержащих их средств, а также разработан способ борьбы с вредоносными грибами и предложено применение соединений I, их солей или содержащих их средств в этих целях.
Предмет патентной заявки Германии P 4431467.1, касающийся настоящего изобретения, включен в данную заявку в качестве ссылки.
Соединения формулы I могут быть получены по известной методике, исходя из соответствующих карбамоилкарбоновых кислот формулы II. Предпочтительно соединения I получают по описанному ниже способу А, соответственно способу Б (ссылки на публикации под названием "Houben-Weyl" относятся к "Houben-Weyl, Methoden der Organischen Chemie", 4е издание, издательство Thieme Verlag, Штутгарт).
Способ А
Амиды карбамоилкарбоновой кислоты формулы I получают благодаря тому, что карбамоилкарбоновые кислоты формулы II подвергают взаимодействию с аминами формулы III.
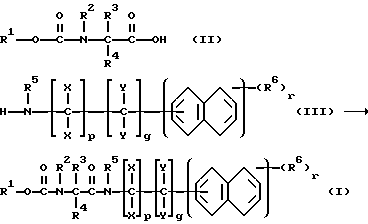
Карбамоилкарбоновые кислоты формулы II известны либо могут быть получены с помощью известных методов, прежде всего исходя из взятых за основу аминокислот (ср. "Hoeben-Weyl", том 15/1, стр. 46-305, прежде всего стр. 117-125).
Амины формулы III также известны либо их можно легко получить (ср. Organikum, издательство VEB Deutscher Verlag der Wissenschaften, 15е издание, Берлин, 1977, стр. 610 и далее; "Houben-Weyl", том 15/1, стр. 648-665; Indian J. Chem. 10, стр. 366 (1972)).
В этом способе А предпочтительно работают таким образом, что сначала карбамоилкарбоновые кислоты II переводят в карбоксиактивированные производные, прежде всего в ацилцианиды либо ангидриды (ср. Tetrahedron Letters, том 18, стр. 1595-1598 (1973), соответственно "Houben-Weyl", том 15/1, стр. 28-32). Затем эти производные вводят в реакцию с аминами III в присутствии оснований.
Для получения карбоксиактивированных ацилцианидов можно осуществлять, например, реакцию между карбамоилкарбоновыми кислотами II и диэтиловым эфиром цианфосфорной кислоты, прежде всего в инертном растворителе, таком как тетрагидрофуран или толуол.
Для получения карбоксиактивированных ангидридов предпочтительно осуществлять взаимодействие карбамоилкарбоновых кислот II с хлорангидридами угольной кислоты, такими как изобутиловый эфир хлормуравьиной кислоты, в присутствии оснований и при необходимости в инертном растворителе, таком как толуол или тетрагидрофуран.
Взаимодействие аминов III с карбоксиактивированными карбамоилкарбоновыми кислотами II проводят предпочтительно в растворителе, таком как дихлорметан, тетрагидрофуран или толуол.
В качестве оснований могут служить прежде всего сами амины III, причем обычно их возвращают в процесс из получаемого неочищенного продукта.
В одном из предпочтительных вариантов осуществления этой стадии способа карбамоилкарбоновую кислоту II, амин III, реагент, пригодный для получения карбкосиактивированного производного карбамоилкарбоновой кислоты II, и основание вводят в реакцию по так называемому способу получения в одном аппарате, при необходимости в инертном растворителе, после чего сырой продукт перерабатывают по известной методике с получением в результате амида карбамоилкарбоновой кислоты формулы I.
Способ Б
Амиды карбамоилкарбоновой кислоты формулы I получают благодаря тому, что амиды карбамоилкарбоновой кислоты I, в которых группа R1-O-(CO) представляет собой защитную группу, которую можно отщеплять по известной методике, переводят в амиды аминокислоты формулы IV и затем эти последние подвергают взаимодействию с эфирами хлормуравьиной кислоты формулы V в присутствии основания.
Стадия Ба: Получение амидов аминокислоты формулы IV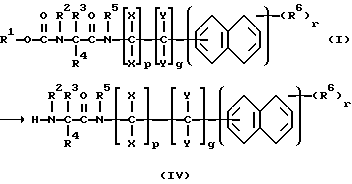
Отщепление группы R1-O-(CO) из амидов карбамоилкарбоновой кислоты I может осуществляться по известной методике (ср. "Houben-Weyl", том 15/1, стр. 46-305, прежде всего стр. 126-129).
Соответствующие отщепляемые группы содержат в качестве остатка R1 трет-бутиловую либо бензильную группу.
В случае R1 в значении трет-бутил, например отщепление, проводят обычно взаимодействием с кислотой, прежде всего с протонной кислотой, такой, в частности, как соляная кислота или трифторуксусная кислота (см. там же, стр. 126-129).
Пригодные для использования в качестве исходных веществ амиды карбамоилкарбоновой кислоты I могут быть получены по известным способам (ср. "Houben-Weyl", том 15/1, стр. 28-32) или же по способу А согласно изобретению.
Стадия Бб: Получение амидов карбамоилкарбоновой кислоты формулы I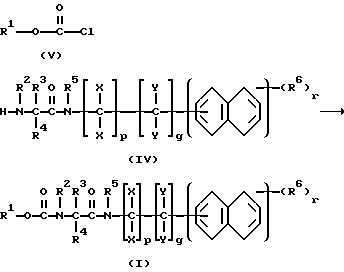
Получаемые в результаты синтеза на стадии Бб амиды аминокислоты формулы IV подвергают взаимодействию с эфирами хлормуравьиной кислоты формулы V в присутствии оснований.
Эфиры хлормуравьиной кислоты V общеизвестны либо могут быть получены с помощью известных способов. Такое взаимодействие осуществляют предпочтительно в органическом растворителе, прежде всего в толуоле, метиленхлориде или тетрагидрофуране, либо в смесях этих растворителей.
В качестве оснований могут рассматриваться в равной степени как неорганические, так и органические основания, причем предпочтительно органические основания, а среди них, в свою очередь, прежде всего третичные амины, такие, как триэтиламин, пиридин и N-метилпиперидиин. Реакцию проводят, как правило, в диапазоне температур от -40 до 50oC, предпочтительно от -10 до 20oC. В остальном проведение реакции для специалиста очевидно, что исключает необходимость дальнейших пояснений (ср. "Houben-Weyl", том 15/1, стр. 117-139).
Полученные по способам А, соответственно Б реакционные смеси подвергают переработке по обычной в этих случаях методике, например, смешением с водой, разделением фаз и при необходимости хроматографической очисткой сырых продуктов. Промежуточные и конечные продукты при этом получают частично в виде бесцветных либо слегка окрашенных в коричневатый цвет вязких масел, из которых при пониженном давлении и умеренно повышенной температуре удаляют летучие компоненты. Если промежуточные и конечные продукты образуются в виде твердых веществ, их очистку можно осуществлять также, например, путем перекристаллизации или дигерирования.
Соединения формулы I при определенных условиях в зависимости от типа заместителей могут быть получены в форме геометрических и/или оптических изомеров либо смесей изомеров. Как чистые изомеры, так и смеси изомеров обладают фунгицидным действием.
Составной частью изобретения являются также соли прежде всего кислотоустойчивых соединений формулы I, содержащие основные центры, прежде всего основные атомы азота, в частности соли минеральных кислот, таких, как серная кислота и фосфорная кислота, или кислот Льюиса, таких, как хлорид цинка. При этом тип соли обычно не играет роли. В контексте настоящего изобретения предпочтительны такие соли, которые не повреждают требующие защиты от вредоносных грибов растения, площади, материалы или помещения и которые не оказывают отрицательного воздействия на эффективность соединений I. Особенно важное значение среди таких солей имеют соли, пригодные для применения в сельском хозяйстве.
Соли соединений формулы I доступны для получения по известной методике, прежде всего их можно получить взаимодействием соответствующих амидов карбамоилкарбоновой кислоты I с вышеуказанными кислотами в воде или в инертном органическом растворителе при температурах в интервале от -80 до 120oC, прежде всего от 0 до 60oC. Получение солей, как правило, не зависит от давления, вследствие чего работают преимущественно при атмосферном давлении.
При указанной выше расшифровке соединений формулы I были использованы обобщающие понятия, общепринятые для обозначения следующих заместителей:
алкил: прямоцепочечные либо разветвленные алкильные группы с 1-8 атомами углерода, например, C1-C8алкил, как метил, этил, н-пропил, 1-метил-этил, н-бутил, 1-метилпропил, 2-метилпропил, 1,1-диметилэтил, н-пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 1,1-диметилпропил, 2,2-диметилпропил, 1,2-диметилпропил, 1-этилпропил, н-гексил, 2-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 2,2-диметилбутил, 3,3-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил и 1-этил-2-метилпропил.
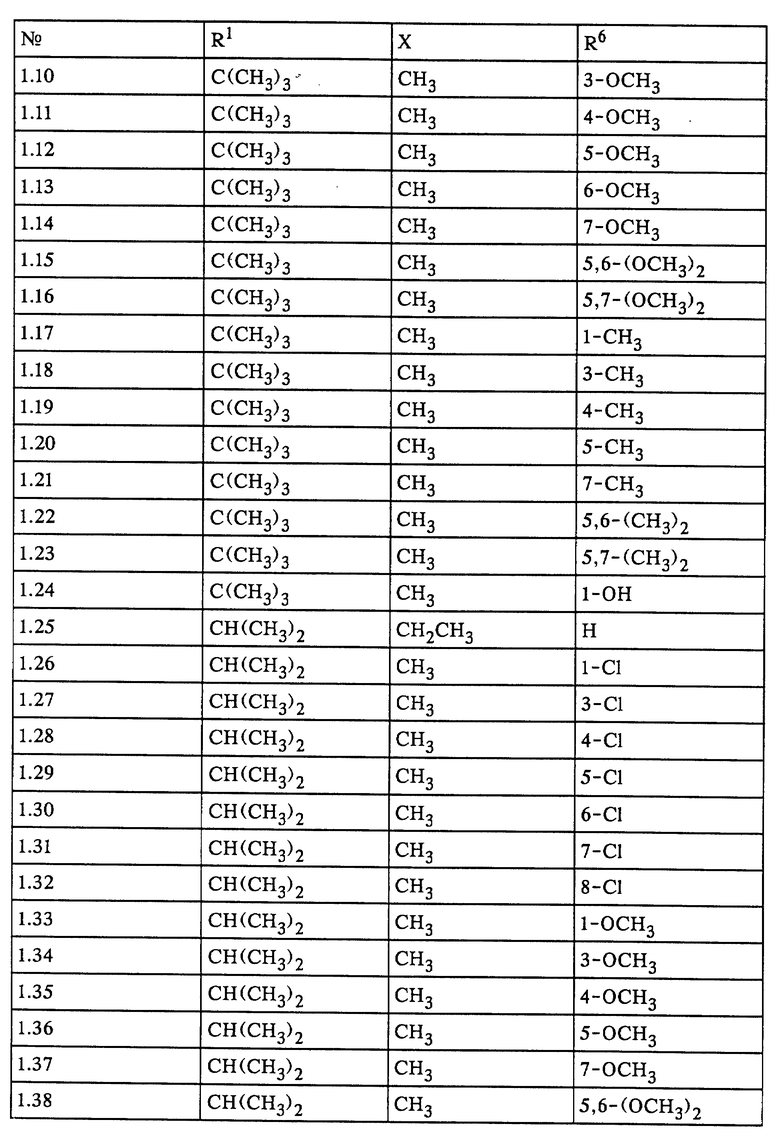
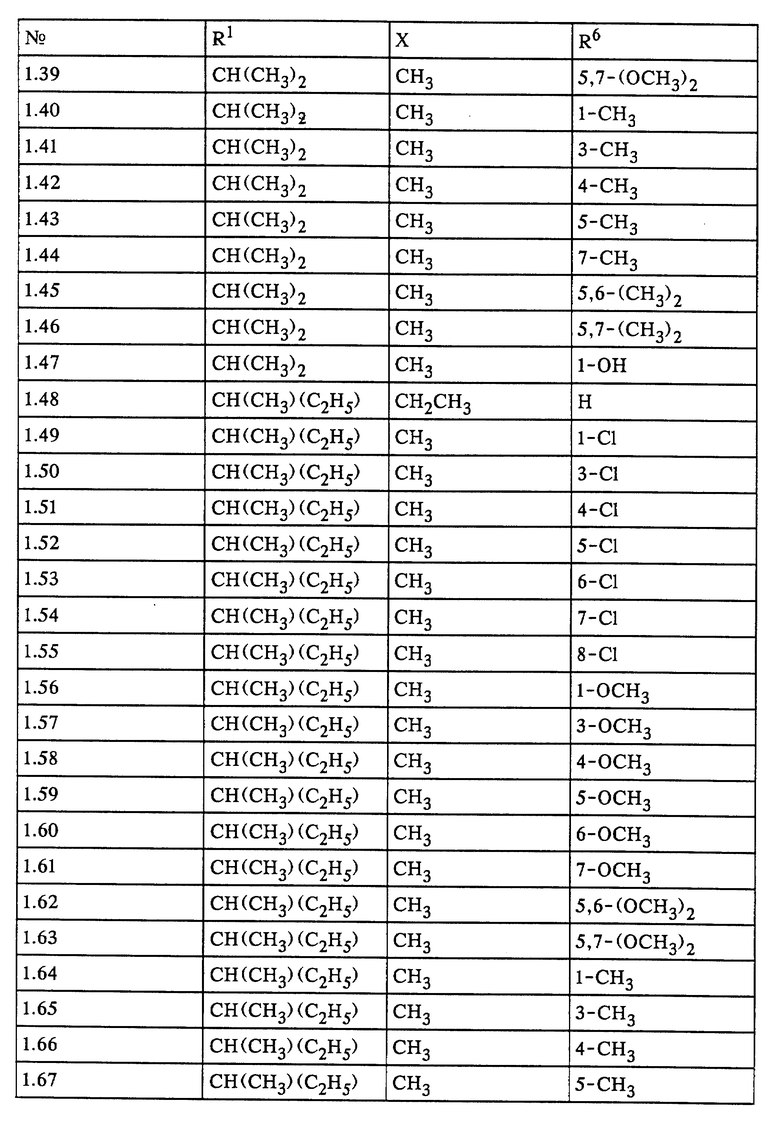
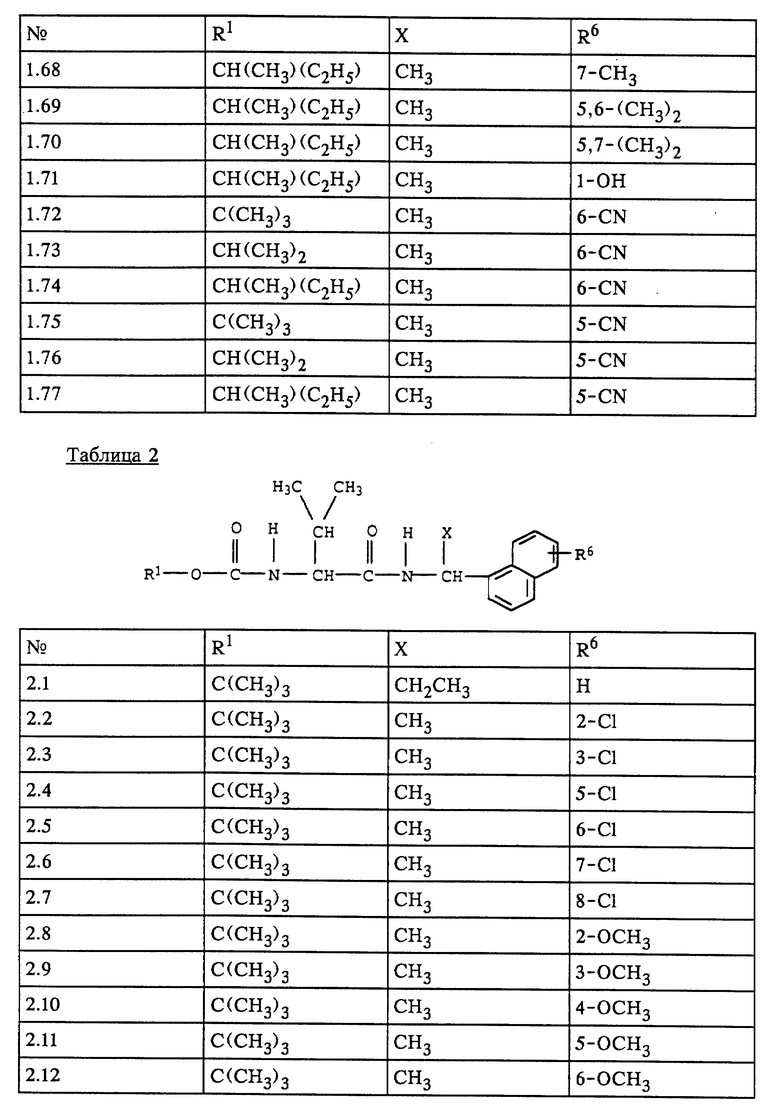
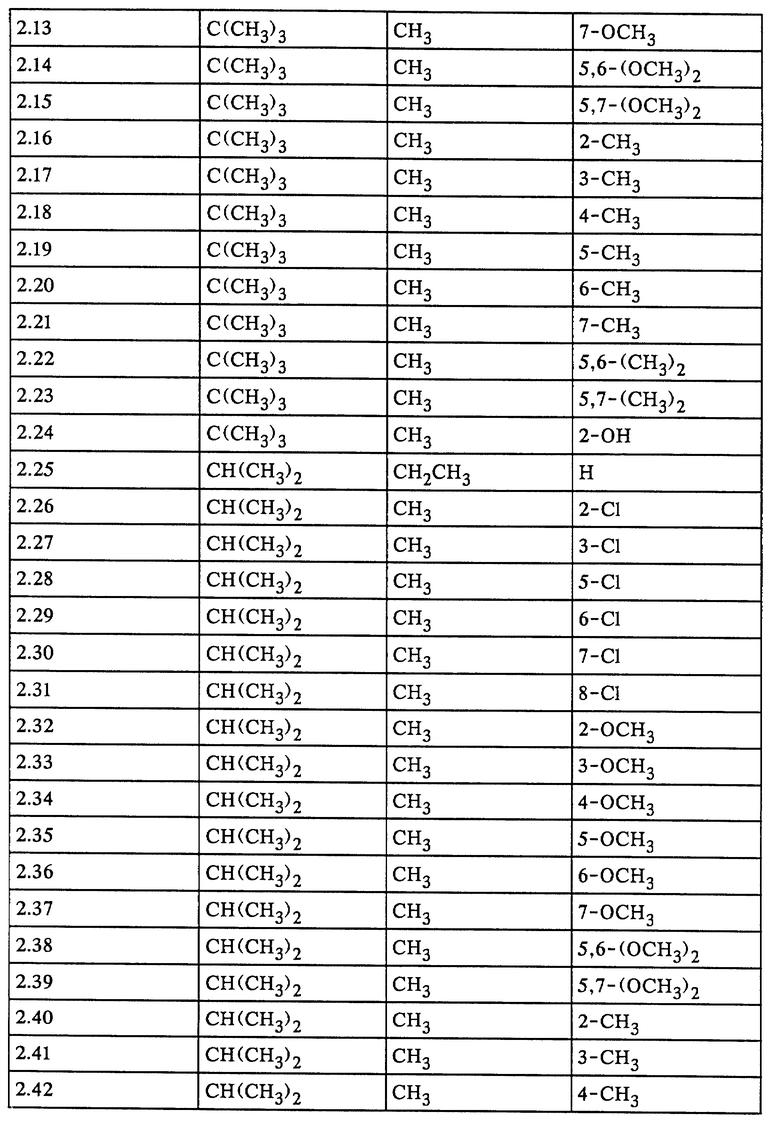
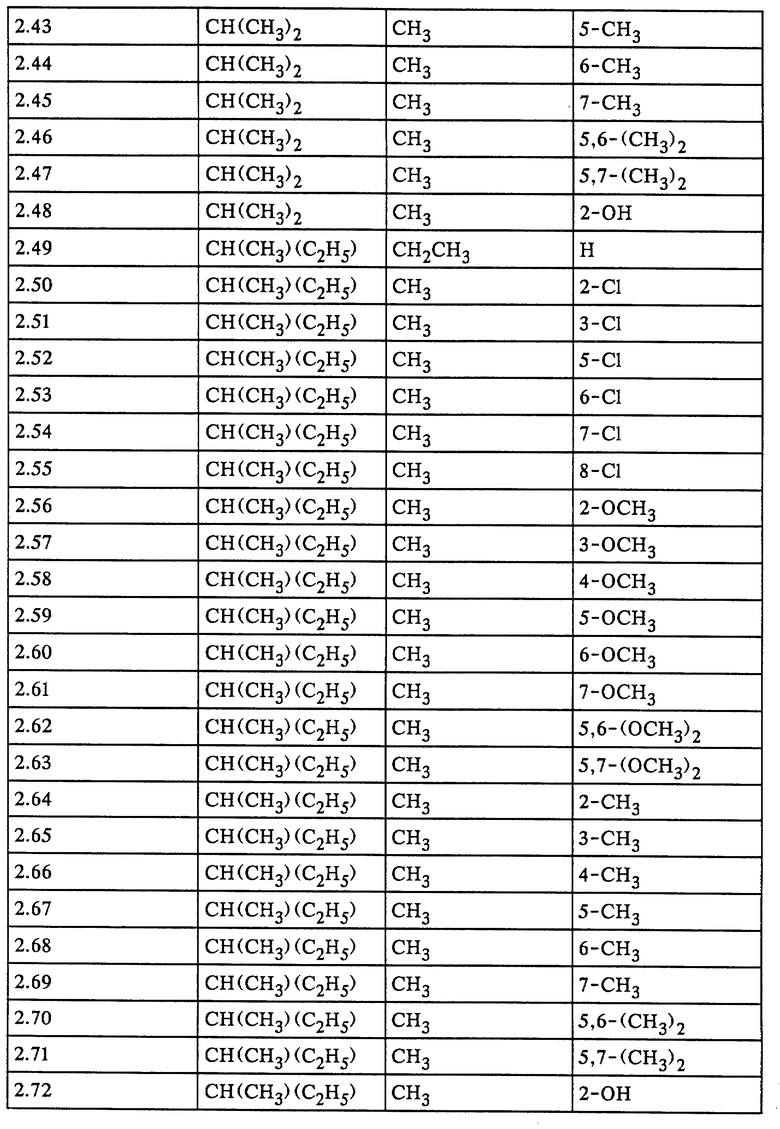
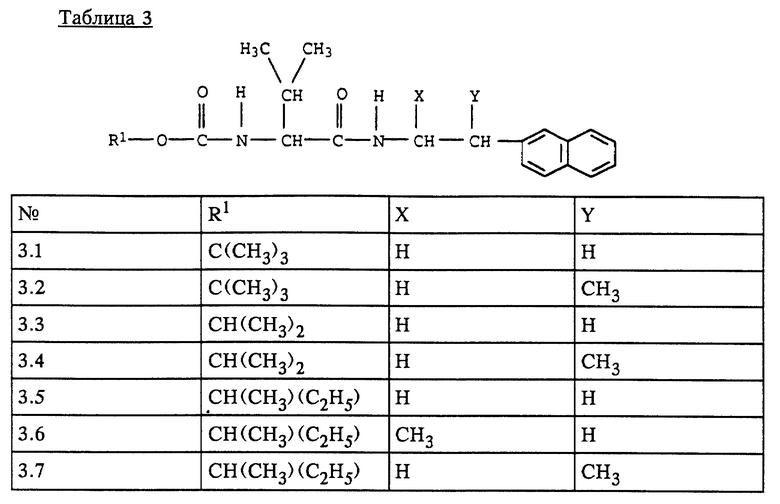
Наиболее предпочтительными с учетом их применения являются соединения формулы I, представленные в табл. 1-5.
Новые соединения формулы I и их соли пригодны для борьбы с вредоносными грибами.
Новые соединения формулы I и их соли могут применяться, например, в виде предназначенных для непосредственного опрыскивания растворов, порошков, суспензий, в том числе высококонцентрированных водных, масляных или каких-либо других суспензий или дисперсий, эмульсий, масляных дисперсий, паст, препаратов для опыливания, опудривания или гранулятов, причем обработку проводят различными методами, такими, как опрыскивание, обработка в виде туманов, опыливание, опудривание или полив. Методика и формы применения полностью зависят от целей применения, но во всех случаях должно быть обеспечено максимально тонкое и равномерное распределение действующих веществ по изобретению.
Обычно при обработке растений растения опрыскивают либо опыливают действующими веществами или же действующими веществами обрабатывают семена растений.
Композиции приготавливают по известной методике, например, разбавлением действующих веществ с помощью растворителей и/или введением наполнителей, при необходимости с использованием эмульгаторов и диспергаторов, причем в случае использования в качестве разбавителя воды могут применяться также другие органические растворители, служащие вспомогательными агентами растворимости.
В качестве таких вспомогательных агентов для указанных целей могут служить в основном следующие:
- растворители, такие, как ароматические углеводороды (например, ксилол), хлорированные ароматические углеводороды (например, хлорбензолы), парафины (например, нефтяные фракции), спирты (например, метанол, бутанол), кетоны (например, циклогексанон), амины (например, этаноламин, диметилформамид) и вода;
- наполнители, такие, как природная минеральная мука (например, каолины, гликоземы, тальк, мел) и синтетическая минеральная мука (например, тонкодисперсная кремниевая кислота, силикаты);
- эмульгаторы, такие, как неионогенные и анионные эмульгаторы (например, эфиры жирных спиртов и полиоксиэтилена, алкилсульфонаты и арилсульфонаты), и
- диспергаторы, такие, как отработанный лигнинсульфитный щелок и метилцеллюлоза.
В качестве поверхностно-активных веществ могут рассматриваться соли щелочных и щелочноземельных металлов и аммониевые соли ароматических сульфоновых кислот, например, лигнинсульфоновой кислоты, фенолсульфоновой кислоты, нафталинсульфоновой кислоты и дибутилнафталинсульфоновой кислоты, а также жирных кислот, алкил- и алкиларилсульфонаты, алкилсульфонаты, сульфаты лаурилового эфира и жирных спиртов, а также соли сульфированных гекса-, гепта- и октадеканолов, гликолевого эфира жирных спиртов, продукты реакции конденсации сульфированного нафталина и его производных с формальдегидом, продукты реакции конденсации нафталина, соответственно нафталинсульфоновых кислот с фенолом и формальдегидом, полиоксиэтиленоктилфеноловые эфиры, этоксилированный изооктил-, октил- или нонилфенол, полигликолевые эфиры алкилфенола и трибутилфенила, алкилариловые эфиры полиспиртов, изотридециловый спирт, конденсаты этиленоксида жирных спиртов, этоксилированное касторовое масло, простой полиоксиэтилен- или полиоксипропиленалкиловый эфир, ацетат эфира лаурилового спирта и полигликоля, сложные эфиры сорбита, отработанный лигнинсульфитный щелок или метилцеллюлоза.
Порошковые препараты, препараты для опыливания и опурдивания могут изготавливаться смешением или совместным измельчением действующих веществ с каким-либо твердым наполнителем.
Грануляты, например, грануляты в оболочке, импрегнированные грануляты и гомогенные грануляты могут быть получены за счет связывания действующих веществ с твердыми наполнителями. Такими твердыми наполнителями могут служить минеральные земли, в частности силикагель, кремниевые кислоты, силикаты, тальк, каолин, известняк, известь, мел, болюс, лесс, глина, доломит, диатомовая земля, сульфат кальция и сульфат магния, оксид магния, измельченные синтетические вещества, удобрения, такие, как сульфат аммония, фосфат аммония, нитрат аммония, мочевины и продукты растительного происхождения, такие, как мука зерновых, мука из коры деревьев, древесная мука и мука из ореховой скорлупы, целлюлозные порошки или какие-либо другие твердые наполнители.
Примерами описанных выше композиций являются следующие:
I. Раствор из 90 мас.ч. соединения формулы I согласно изобретению и 10 мас.ч. N-метил α пирролидона, предназначенный для применения в виде мельчайших капель.
II. Смесь из 10 мас.ч. соединения формулы I согласно изобретению, 70 мас. ч. ксилола, 10 мас.ч. продукта присоединения 8-10 моль этиленоксида к 1 моль N-моноэтаноламида олеиновой кислоты, 5 мас.ч. кальциевой соли додецилбензолсульфоновой кислоты, 5 мас.ч. продукта присоединения 40 моль этиленоксида к 1 моль касторового масла; после тонкого и равномерного распределения этой композиции в воде получают соответствующую дисперсию.
III. Водная дисперсия из 10 мас.ч. соединения формулы I согласно изобретению из 40 мас. ч. циклогексанона, 30 мас.ч. изобутанола и 20 мас.ч. продукта присоединения 40 моль этиленоксида к 1 моль касторового масла.
IV. Водная дисперсия из 10 мас.ч. соединения формулы I согласно изобретению, 25 мас.ч. циклогексанола, 55 мас.ч. фракции нефтяного топлива с температурой кипения 210-280oC, получаемой при перегонке нефти, и 10 мас.ч. продукта присоединения 40 моль этиленоксида к 1 моль касторового масла.
V. Измельченная в молотковой мельнице смесь из 80 мас.ч. предпочтительно твердого соединения формулы I согласно изобретению, 3 мас.ч. натриевой соли диизобутилнафталин-2-сульфоновой кислоты, 10 мас.ч. натриевой соли лигнинсульфоновой кислоты из отработанного сульфитного щелока и 7 мас.ч. порошкообразного силикагеля; после тонкого и равномерного распределения этой смеси в воде получают соответствующий раствор для опрыскивания.
VI. Гомогенная смесь из 3 мас.ч. соединения формулы I согласно изобретению и 97 мас.ч. тонкодисперсного каолина; этот препарат для опыливания содержат 3 мас.% действующего вещества.
VII. Гомогенная смесь из 30 мас.ч. соединения формулы I согласно изобретению, 62 мас.ч. порошкообразного силикагеля и 8 мас.ч. парафинового масла, которое напыляют на поверхность этого силикагеля; благодаря такой методике приготовления действующее вещество приобретает хорошую адгезионную способность.
VIII. Устойчивая водная дисперсия из 40 мас.ч. соединения формулы I согласно изобретению, 10 мас. ч. натриевой соли конденсата фенол-сульфоновой кислоты-мочевины-формальдегида, 2 мас. ч. силикагеля и 48 мас.ч. воды, которую можно дополнительно разбавлять.
IX. Устойчивая масляная дисперсия из 20 мас.ч. соединения формулы I согласно изобретению, 2 мас.ч. кальциевой соли додецилбензолсульфоновой кислоты, 8 мас. ч. полигликолевого эфира жирного спирта, 20 мас.ч. натриевой соли конденсата фенолсульфоновой кислоты-мочевины-формальдегида и 50 мас.ч. парафинового минерального масла.
Новые соединения отличаются исключительно высокой эффективностью против широкого спектра фитопатогенных грибов, прежде всего относящихся к классу дейтеромицетов, аскомицетов, фикомицетов и базидиомицетов. Они обладают частично системным действием и могут применяться в качестве фунгицидов для обработки листвы и в качестве почвенных фунгицидов.
Особое значение они имеют для борьбы с многочисленными грибами, поражающими различные культурные растения, такие, как пшеница, рожь, ячмень, овес, рис, кукуруза, газонные травы, хлопчатник, соя, кофе, сахарный тростник, виноград, плодовые и декоративные растения, овощные культуры, такие, как огурцы, бобовые и тыквенные, а также поражающими семена этих растений.
Принцип применения соединений формулы I состоит в том, что грибы либо семена, растения, материалы или почву, требующие защиты от поражения грибами, обрабатывают фунгицидно эффективным количеством действующих веществ. Такую обработку проводят до либо после заражения материалов, растений или семян грибами.
Соединения формулы I особенно пригодны для борьбы со следующими болезнями растений: Erysiphe graminis (настоящая мучнистая роса) на зерновых, Erysiphe cichoracearum и Sphaerotheca fuliginea на тыквенных, Podosphaera leucotricha на яблоневых, Uncinula necator на виноградной лозе, виды Puccinia на зерновых, виды Rhizoctonia на хлопчатнике и дернине, виды Ustilago на зерновых и сахарном тростнике, Venturia inaequalis (парша) на яблоневых, виды Helminthosporium на зерновых, Septoria nodorum на пшенице, Botrytis cinerea (серая гниль) на землянике, виноградной лозе, декоративных растениях и овощных культурах, Cercospora arachidicola на земляном орехе, Pseudocercosporella herpotrichoides на пшенице, ячмене, Pyricularia oryzae на рисе, Phytophthora infestans на картофеле и томатах, виды Fusarium и Verticillium на различных культурах, Plasmopara viticola на виноградной лозе, виды Alternaria на овощных и плодовых культурах.
Новые соединения могут применяться также для защиты материалов, в частности древесины, например, от такого возбудителя, как Paecilomyces variotii.
Фунгицидные препараты содержат действующие вещества, как правило, в количестве от 0,1 до 95, предпочтительно от 0,5 до 90 мас.%. Нормы расхода в зависимости от того, какой эффект хотят получить, составляют от 0,025 до 2, предпочтительно от 0,1 до 1 кг действующего вещества на гектар. При обработке семенного материала действующие вещества применяют, как правило, в количестве от 0,001 до 50, предпочтительно от 0,01 до 10 г на кг семян.
Предлагаемые согласно изобретению средства при их использовании в качестве фунгицидов могут применяться также с другими действующими веществами, например, с гербицидами, инсектицидами, регуляторами роста, фунгицидами или же с удобрениями. При смешении с фунгицидами при этом во многих случаях достигают расширения спектра фунгицидного действия.
Ниже представлен перечень фунгицидов, в сочетании с которыми могут применяться соединения по изобретению, причем этот перечень служит для пояснения таких комбинационных возможностей, не ограничивая объем изобретения.
К указанным фунгицидам относятся сера, дитиокарбаматы и их производные, такие, как ферридиметилдитиокарбамат, диметилдитиокарбамат цинка, этиленбисдитиокарбамат цинка, этиленбисдитиокарбамат марганца, марганец-цинк-этилендиаминбисдитиокарбамат, тетраметилтиурамдисульфид, аммиачный комплекс цинк-(N, N-этиленбис- дитиокарбамат), аммиачный комплекс цинк-(N,N'-пропиленбисдитиокарбамат), цинк-(N, N'пропиленбисдитиокарбамат), N,N'-полипропиленбис(тио-карбамоил)дисульфид; нитропроизводные, такие, как динитро(1-метилгептил)фенилкротонат, 2-втор-бутид-4,6-динитрофенил-3,3-диметилакрилат, 2-втор-бутил-4,6-динитрофенилизопропилкарбонат, диизопропиловый эфир 5-нитроизофталевой кислоты; гетероциклические субстанции, такие, как 2-гептадецил-2-имидазолинацетат, 2,4-дихлор-6-(о-хлоранилино)-s-триазин, O,O-диэтилфталимидфосфонтиоат, 5-амино-1-[бис(диметиламино)фосфинил] -3-фенил-1,2,4-триазол, 2,3-дициан-1,4-дитиоантрахинон, 2-тио-1,3-дитиоло-[4,5-b]хиноксалин, метиловый эфир 1-(бутилкарбамоил)-2-бензимидазолкарбаминовой кислоты, 2-метоксикарбониламинобензимидазол, 2-(фурил-(2))-бензимидазол, 2-(тиазолил-(4))бензимидазол, N-(1,1,2,2-тетрахлорэтилтио)тетрагидрофталимид, N-трихлорметилтиотетрагидрофталимид, N-трихлорметилтиофталимид, диамид N-дихлорфторметилтио-N'N'-диметил-N-фенилсерной кислоты, 5-этокси-3-трихлорметил-1,2,3-тиадиазол, 2-роданметилтиобензтиазол, 1,4-дихлор-2,5-диметоксибензол, 4-(2-хлорфенилгидразоно)-3-метил-5-изоксазолон, пиридин-2-тио-1-оксид, 8-гидроксихинолин, соответственно его медная соль, 2,3-дигидро-5-карбоксанилидо-6-метил-1,4-оксатиин, 2,3-дигидро-5-карбоксанилидо-6-метил-1,4-оксатиин-4,4-диоксид, анилид 2-метил-5,6-дигидро-4H-пиран-3-карбоновой кислоты, анилид 2-метилфуран-3-карбоновой кислоты, анилид 2,5-диметилфуран-3-карбоновой кислоты, анилид 2,4,5-триметилфуран-3-карбоновой кислоты, циклогексиламид 2,5-диметилфуран-3-карбоновой кислоты, амид N-циклогексил-N-метокси-2,5-диметилфуран-3-карбоновой кислоты, анилид 2-метилбензойной кислоты, анилид 2-иодбензойной кислоты, N-формил-N-морфолин-2,2,2-трихлорэтилацеталь, пиперазин-1,4-диилбис-1-(2,2,2-трихлорэтил)формамид, 1-(3,4-дихлоранилино)-1-формиламино-2,2,2-трихлорэтан, 2,6-диметил-N-тридецилморфолин, соответственно его соли, 2,6-диметил-N-циклододецилморфолин, соответственно его соли, N-[3-(п-трет-бутилфенил)-2-метилпропил]-цис-2,6-диметилморфолин, N-[3-(п-трет-бутилфенил)-2-метилпропил]пиперидин, 1-[2-(2,4-дихлорфенил)-4-этил-1,3-диоксолан-2-илэтил]-1H-1,2,4-триазол, 1-[2-(2,4-дихлорфенил)-4-н-пропил-1,3-диоксолан-2-илэтил] -1H-1,2,4-триазол, N-(н-пропил)-N-(2,4,6-трихлорфеноксиэтил)-N'-имидазолилмочевина, 1-(4-хлорфенокси)-3,3-диметил-1-(1H-1,2,4-триазол-1-ил)-2-бутанон, 1-(4-хлорфенокси)-3,3-диметил-1-(1H-1,2,4-триазол-1-ил)-2-бутанол, (2-хлорфенил)-(4-хлорфенил)-5-пиримидинметанол, 5-бутил-2-диметиламино-4-гидрокси-6-метилпиримидин, бис(п-хлорфенил)-3-пиридинметанол, 1,2-бис(3-этоксикарбонил-2-тиоуреидо)бензол, 1,2-бис(3-метоксикарбонил-2-тиоуреидо)бензол, [2-(4-хлорфенил)этил] -(1,1-диметилэтил)-1H-1,2,4- триазол-1-этанол, 1-[3-(2-хлорфенил)-1-(4-фторфенил)-оксиран-2-илметил]-1H-1,2,4-триазол; а также ряд других фунгицидов, таких, как додецилгуанидинацетат, 3-[3-(3,5-диметил-2-оксициклогексил)-2-гидроксиэтил] глутаримид, гексахлорбензол, DL-метил-N-(2,6-диметилфенил)-N-фуроил(2)аланинат, метиловый эфир DL-N-2,6-диметилфенил)-N-(2'-метоксиацетил)аланина, N-(2,6-диметилфенил)-N-хлорацетил-DL-2-аминобутиролактон, метиловый эфир DL-N-(2,6-диметилфенил)-N-(фенилацетат)аланина, 5-метил-5-винил-3-(3,5-дихлорфенил)-2,4-диоксо-1,3-оксазолидин, 3-[3,5-дихлорфенил(5-метил-5-метоксиметил)]-1,3-оксазолидин-2,4-дион, 3-(3,5-дихлорфенил)-1-изопропилкарбамоилгидрантоин, имид N-(3,5-дихлорфенил)-1,2-диметилциклопропан-1,2-дикарбоновой кислоты, 2-циано-[N-(этиламинокарбонил)-2-метоксимино] ацетамид, 1-[2-(2,4-дихлорфенил)пентил]-1H-1,2,4-триазол, 2,4-дифтор--α--1H-1,2,4-триазолил-1-метил)бензгидриловый спирт, N-(3-хлор-2,6-динитро-4-трифторметилфенил)-5-трифторметил-3-хлор-2- аминопиридин, 1-((бис(4-фторфенил)метилсилил)метил)-1H-1,2,4-триазол, стробилурины, такие, как метил-E-метоксимино-[α-(о-толилокси)-о-толил] ацетат, метил-E-2-{2-[6-(2-цианофенокси)пиридимин-4-ил-окси] фенил} -3- метоксиакрилат, метил-E-метоксимино-[α- (2,5-диметилокси)-о-толил]ацетамид, анилинопиримидины, такие, как N-(4,6-диметилпиримидин-2-ил)анилин, N-[4-метил-6-(1-пропинил)пиримидин-2-ил] анилин, N-[4-метил-6-циклопропил-пиримидин-2-ил]анилин, фенилпирролы, такие, как 4-(2,2-дифтор-1,3-бензодиоксол-4-ил)-пиррол-3-карбонитрил, амиды коричной кислоты, такие, как морфолид 3-(4-хлорфенил)-3-(3,4-диметоксифенил)акриловой кислоты,
Пример синтеза
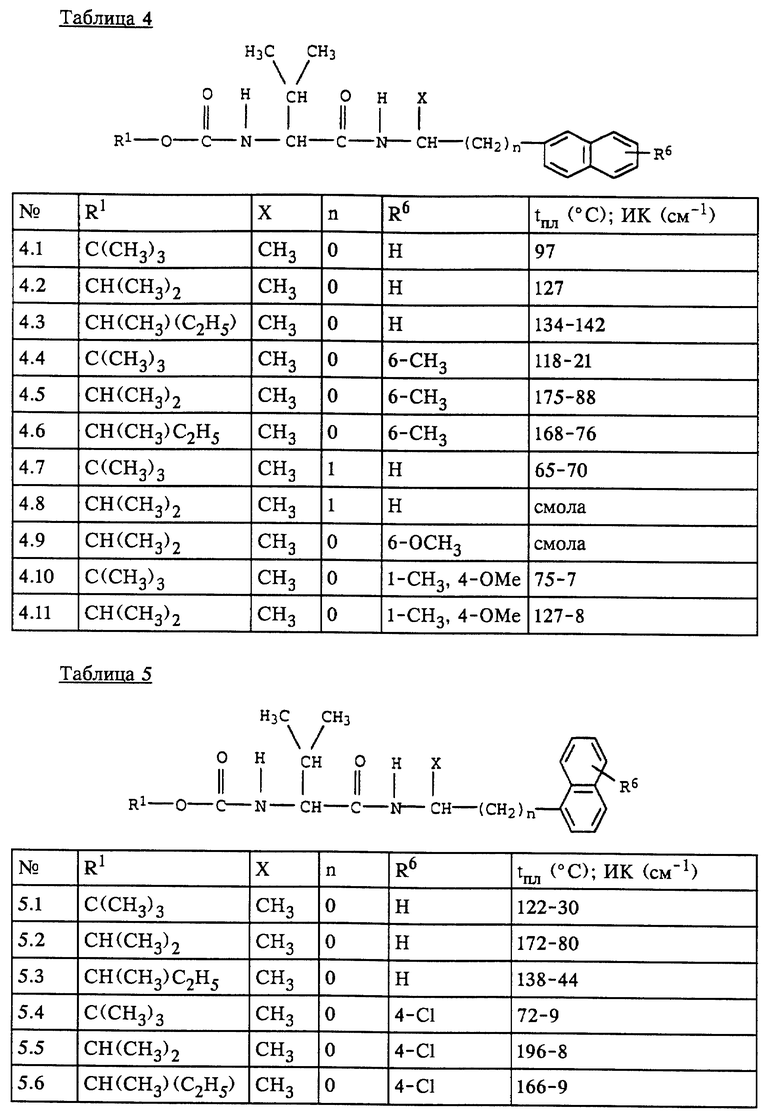
Приведенные в нижеследующем примере синтеза рекомендации могут использоваться при соответствующей модификации исходного соединения для получения других представителей соединений формулы I. Физические характеристики полученных таким путем продуктов представлены в таблицах 4 и 5.
N-(изопропилоксикарбонил)-L-валин-(1-( β- нафтил)этил)амид (соединение N 4.2 в таблице 4)
К раствору из 14,2 г (65 ммоль) трет-бутоксикарбонил-L-валина и 13,6 г (65 ммоль) 1-амино-1-( β- нафтил)этана в 300 мл тетрагидрофурана добавляли 13,3 г (65 ммоль) диэтилового эфира цианфосфорной кислоты. В течение 1 ч при 0oC и в течение 15 ч при 20oC перемешивали. Затем растворитель удаляли и остаток растворяли 300 мл этилового эфира уксусной кислоты. Органическую фазу промывали соответственно 200 мл 5%-ного едкого натра, 10%-ной соляной кислоты, 10%-ного по массе раствора гидрокарбоната натрия и воды, сушили и концентрировали. В результате получили 18,0 г (49 ммоль) N-(трет-бутилоксикарбонил)-L-валин-(1-( β- нафтил)этил)амида (tпл 97oC).
К 17,0 г (46 ммоль) этого соединения добавляли при охлаждении 50 мл трифторуксусной кислоты и смесь перемешивали 1 ч при 0oC. Затем нагревали до 20oC, трифторкусусную кислоту практически полностью отгоняли, остаток растворяли в 300 мл дихлорметана и промывали его соответственно 200 мл 2 н. едкого натра, 5%-ного по массе раствора гидрокарбоната натрия и воды. После сушки и концентрирования органической фазы получили 10,7 г (40 ммоль) L-валин-(1-( β- -нафтил)этил)амида в виде желтого вязкотекучего масла.
0,54 г (2,0 ммоль) Этого соединения и 0,22 г (2,2 ммоль) триэтиламина в 40 мл толуола смешивали при 0oC с 0,24 г (2,1 ммоль) изопропилового эфира хлормуравьиной кислоты и перемешивали в течение 15 ч при 20oC. После удаления растворителя остаток растворяли в 50 мл этилового эфира уксусной кислоты и промывали соответственно 40 мл 10%-ной по массе соляной кислоты, 10%-ного по массе раствора гидрокарбоната натрия и воды. После сушки органической фазы растворитель удаляли. В результате получили 0,58 г (1,6 ммоль) указанного в заголовке соединения в виде бесцветного кристаллического остатка (tпл 127oC).
Примеры по применению
В следующих опытах, проводившихся для исследования и подтверждения фунгицидной эффективности соединений формулы I, использовали эмульсию, содержащую 10 мас.% действующего вещества и 80 мас.% смеси, включающей 70 мас.% циклогексанола, 20 мас. % Nekanil®LN (Lutensol®AP6, смачиватель с эмульгирующим и диспергирующим действием на основе этоксилированных алкилфенолов) и 10 мас. % Emulphor®EL (Emulan®EL, эмульгатор на основе этоксилированных жирных спиртов). Требуемую концентрацию действующего вещества получали за счет разбавления этой эмульсии водой.
Действие против Plasmopara viticola
Листья горшечных растений виноградной лозы сорта "Muller-Thurgau" опрыскивали водным раствором, содержавшим 80 мас.% действующего вещества и 20 мас. % эмульгатора из расчета по сухой субстанции. Для определения продолжительности действия активных веществ растения после того, как покрывавший листья раствор высох, помещали на 8 дней в теплицу. Лишь затем листья инфицировали взвесью зооспор Plasmopara viticola (ложная мучнистая роса винограда). Растения выдерживали сначала в течение 48 ч в камере в насыщенной водными парами атмосфере при 24oC, а затем в течение 5 дней в теплице при 20-30oC. По истечении этого времени с целью ускорить вскрытие носителя спорангия растения повторно помещали на 16 ч во влажную камеру. После этого проводили визуальную оценку степени поражения грибами нижней поверхности листьев.
В этом тесте степень поражения листьев растений, обработанных водной композицией, содержавшей 250 част./млн или 63 част./млн соответственно одного из соединений NN 4.1, 4.2, 4.3, 4.4, 4.5, 4.6, 4.7, 4.8, 4.9, 4.10, 5.2, 5.3, 5.4, 5.5 и 5.6, составляла: в случае обработки 250 част./млн действующего вещества 0-5% поверхности листьев, а в случае обработки 63 част./млн 0-25% поверхности листьев. В отличие от этого степень поражения листьев необработанных растений составляла 80%.
Действие против Phytophthora infestans
Листья горшечных растений томатов сорта "Grobe Fleischtomate" опрыскивали водным раствором, содержавшим 80 мас.% действующего вещества и 20 мас.% эмульгатора из расчета по сухой субстанции. Через 24 ч листья инфицировали взвесью зооспор гриба Phytophthora infestans. Затем растения помещали в насыщенную водными парами камеру при 16-18oC. По истечении 6 дней степень поражения необработанных, но инфицированных контрольных растений достигла такого уровня, который позволил проводить визуальную оценку фунгицидной эффективности испытуемых субстанций.
В этом тесте степень поражения листьев растений, обработанных водной композицией, содержавшей 250 част./млн или 63 част./млн соответственно одного из соединений NN 4.1, 4.2, 4.3, 4.4, 4.5, 4.6, 4.8, 4.9, 5.2, 5.4, 5.5 и 5.6, составляла от 0 до 15% поверхности листьев. В отличие от этого листья необработанных растений были поражены на 90%.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИМИНООКСИМЕТИЛЕНАНИЛИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), СРЕДСТВА ДЛЯ БОРЬБЫ С ВРЕДИТЕЛЯМИ, СПОСОБ БОРЬБЫ С ВРЕДИТЕЛЯМИ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1995 |
|
RU2143423C1 |
| СРЕДСТВО БОРЬБЫ С ВРЕДОНОСНЫМИ ГРИБАМИ И СПОСОБ БОРЬБЫ С ВРЕДОНОСНЫМИ ГРИБАМИ | 1996 |
|
RU2158083C1 |
| ПРОИЗВОДНЫЕ 2-[(2-АЛКОКСИ-6-ТРИФТОРМЕТИЛПИРИМИДИН-4-ИЛ)ОКСИМЕТИЛЕН]ФЕНИЛУКСУСНОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СРЕДСТВО ДЛЯ БОРЬБЫ С ВРЕДИТЕЛЯМИ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ | 1995 |
|
RU2166500C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛУКСУСНОЙ КИСЛОТЫ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ СРЕДСТВА | 1995 |
|
RU2165411C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛУКСУСНОЙ КИСЛОТЫ И СРЕДСТВО БОРЬБЫ ПРОТИВ НАСЕКОМЫХ И ПАУКООБРАЗНЫХ И ПРОТИВ ВРЕДОНОСНЫХ ГРИБОВ | 1995 |
|
RU2162075C2 |
| ФУНГИЦИДНАЯ СМЕСЬ И СПОСОБ БОРЬБЫ С ВРЕДОНОСНЫМИ ГРИБАМИ | 1995 |
|
RU2176138C2 |
| ФУНГИЦИДНАЯ СМЕСЬ, СПОСОБ БОРЬБЫ С ВРЕДОНОСНЫМИ ГРИБАМИ | 1995 |
|
RU2152154C2 |
| ПРОИЗВОДНЫЕ БЕНЗАМИДОКСИМОВ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ, ФУНГИЦИДНЫЕ СРЕДСТВА, СПОСОБ БОРЬБЫ С ФИТОПАТОГЕННЫМИ ГРИБАМИ | 1998 |
|
RU2192412C2 |
| 2-[1', 2', 4'-ТРИАЗОЛ-3'-ИЛОКСИМЕТИЛЕН]АНИЛИДЫ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ И СРЕДСТВО БОРЬБЫ С ВРЕДОНОСНЫМИ ГРИБАМИ | 1995 |
|
RU2165927C2 |
| 2-[(ДИГИДРО)ПИРАЗОЛИЛ-3'-ОКСИМЕТИЛЕН]АНИЛИДЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, СРЕДСТВО БОРЬБЫ С СЕЛЬСКОХОЗЯЙСТВЕННЫМИ ВРЕДИТЕЛЯМИ И ВРЕДОНОСНЫМИ ГРИБАМИ И СПОСОБЫ БОРЬБЫ | 1995 |
|
RU2151142C1 |
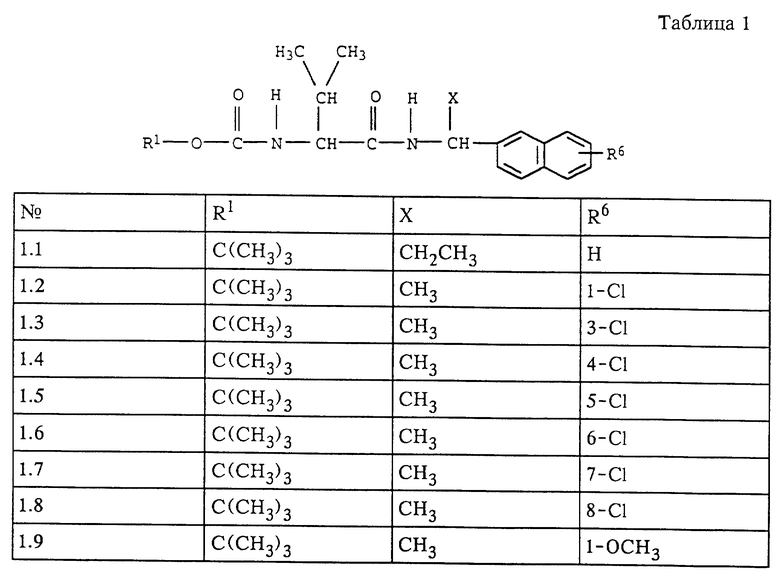
Описываются новые амиды карбамоилкарбоновой кислоты общей формулы (I), где R1 - С1 - С8-алкил; R2 - водород; R3 - С1 - С8-алкил; R4 и R5 - водород, Х независимо друг от друга - водород, С1 - С8-алкил, Y независимо друг от друга - один из радикалов Х; q и p независимо друг от друга обозначают 0, 1 при условии, что оба одновременно не могут иметь значение 0; r = 0, 1, 2, и их соли, которые обладают фунгицидной активностью. Описываются способ их получения, средство и способы для борьбы с вредоносными грибами. 7 с.п. ф-лы, 5 табл.
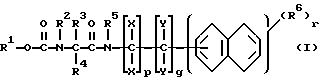
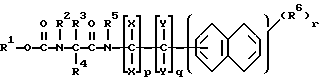
и их соли,
где R1 - C1 - C8-алкил;
R2 - водород;
R3 - C1 - C8-алкил;
R4 и R5 - водород;
X независимо друг от друга - водород, C1 - C8-алкил; Y независимо друг от друга - один из радикалов X;
q и p независимо друг от друга обозначают 0, 1 при условии, что оба одновременно не могут иметь значение 0;
r = 0, 1, 2;
R6 - C1 - C8-алкил, C1 - C4-алкокси, галоген.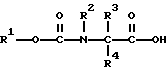
подвергают взаимодействию с амином общей формулы III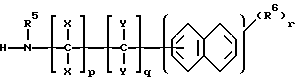
3. Способ получения амидов карбамоилкарбоновой кислоты общей формулы I по п. 1, отличающийся тем, что а) амид карбамоилкарбоновой кислоты общей формулы I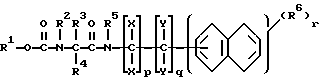
где группа R1-O-(CO) представляет собой защитную группу, которую можно отщеплять по известной методике,
переводят в амид аминокислоты формулы IV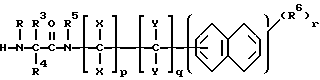
и б) полученный таким путем амид аминокислоты формулы IV подвергают взаимодействию с эфиром хлормуравьиной кислоты общей формулы V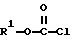
в присутствии основания.
| Концентрационный стол | 1970 |
|
SU398072A1 |
| Машина для производства растительного пергамента | 1973 |
|
SU472996A1 |
| Рабочая клеть | 1974 |
|
SU485794A1 |
| Магниторазрядный манометр | 1974 |
|
SU493683A1 |
| Способ извлечения платины из отработанного алюмоплатинового катализатора | 1974 |
|
SU496239A1 |
| EP 0550788 A1, 1993 | |||
| Способ получения производных карбаминовой кислоты | 1974 |
|
SU520912A3 |
| Способ получения смеси для пропитки полиамидных волокон, содержащей перфторалкильные группы, эпихлоргидриновые группы и остатки двухатомного спирта уретанов | 1986 |
|
SU1445555A3 |
| Карбаматы хлоральамидов двухосновных карбоновых кислот, обладающие фунгицидной активностью | 1975 |
|
SU545103A1 |
| EP 554729 A1, 1993. | |||
Авторы
Даты
2000-02-27—Публикация
1995-08-19—Подача