Изобретение относится к конструкции, разработке, композиции и применению новых кальцимиметических молекул, способных воздействовать аналогичным образом на внеклеточные ионы кальция на клетках, к кальцилитическим молекулам, которые блокируют активность внеклеточных ионов кальция на клетки, и к способам их применения и идентификации.
Оно также относится к новому суперсемейству рецепторов неорганических ионов, которое включает среди других рецепторы кальция, нуклеиновым кислотам, кодирующим такие рецепторы, к клеткам, тканям и животным, содержащим такие нуклеиновые кислоты, к антителам к рецепторам, к анализу с использованием рецепторов и к способам, относящимся ко всему вышесказанному.
Последующее описание предоставляет краткую информацию, относящуюся к настоящему изобретению. Это не означает, что любая приведенная здесь информация представляет собой уровень техники для заявляемого изобретения, ни то, что любая из публикаций специально или безоговорочно относятся к уровню техники этого изобретения.
Некоторые клетки в организме отвечают не только на химические сигналы, но также на ионы, такие как внеклеточные ионы кальция /Ca2+/. Изменения концентрации внеклеточного Ca2+ (упоминаемой здесь как "/Ca2+/") изменяют функциональные ответы этих клеток. Одной такой специализированной клеткой является паратироидная клетка, которая секретирует паратироидный гормон /ПТГ/. ПТГ является принципиальным эндокринным фактором, регулирующим Ca2+ гомеостаз в крови и внеклеточных жидкостях.
ПТГ при действии на клетки кости и почек увеличивает уровень Ca2+ в крови. Такое увеличение /Ca2+/ затем действует как сигнал отрицательной обратной связи, подавляя секрецию ПТГ. Обратное соотношение между /Ca2+/ и секрецией ПТГ образует основной механизм поддержания гомеостаза Ca2+ в целом.
Внеклеточный Ca2+ действует непосредственно на паратироидную клетку, регулируя секрецию ПТГ. Было предположено существование белка поверхности паратироидной клетки, который определяет изменение /Ca2+/. Этот белок действует как рецептор внеклеточного Ca2+ /"рецептор Ca2+"/ и предполагают, что он определяет изменения /Ca2+/ и инициирует функциональный клеточный ответ, секрецию ПТГ. Например, роль рецепторов Ca2+ и внеклеточного Ca2+ при регулировании внеклеточного Ca2+ и функции клетки рассмотрена Неметом с сотр., 11 Cell Calcium 319, 1990, роль Ca2+-рецепторов в парафолликулярных и паратироидных клетках рассмотрена Неметом с сотр., 11 Cell Calcium 323, 1990, и роль Ca2+-рецепторов на костные остеокласты рассмотрены Зайди, 10 Biosceince Reports 493, 1990.
Другие клетки организма, особенно остеокласт в кости, окологломерулярные, проксимальные канальцевые клетки в почках, кератиноцит в эпидермисе, парафолликулярная клетка в щитовидной железе, интестинальные клетки, трофобласт в плаценте, обладают способностью чувствовать изменения /Ca2+/. Было предположено, что рецепторы Ca2+ поверхности клеток также могут присутствовать на этих клетках, придавая им способность определять и инициировать или быть способными давать ответ на изменения /Ca2+/.
В паратироидных клетках, остеокластах, парафолликулярных клетках (C-клетках), кератиноцитах, окологломерулярных клетках в трофобластах увеличение /Ca2+/ вызывает увеличение концентрации внутриклеточного свободного Ca2+ ("/Ca2+/в"). Такое увеличение может быть вызвано притоком внеклеточного Ca2+ или мобилизацией Ca2+ из внутриклеточных органелл. Изменения /Ca2+/в легко контролируются и количественно определяются при использовании флуориметрических индикаторов, таких как fura-2 или indo-1 (Molecular Probes, Eugene, OR). Измерение /Ca2+/в обеспечивает анализ для оценки способности молекул действовать как агонисты или антагонисты на рецептор Ca2+.
В паратироидных клетках увеличение концентрации внеклеточного Ca2+ вызывает быстрое и временное увеличение /Ca2+/в, за которым следует более низкое, но еще продолжительное повышение /Ca2+/в. Кратковременное повышение /Ca2+/в возникает из-за мобилизации внутриклеточного Ca2+, тогда как более низкое продолжительное повышение является результатом притока внеклеточного Ca2+. Мобилизация внутриклеточного Ca2+ осуществляется за счет повышенного образования инозитол-1,4,5-трифосфата /ИФ3/ и диацилглицерина, двух биохимических индикаторов, которые ассоциированы с рецепторзависимой мобилизацией внутриклеточного Ca2+ в других различных клетках.
В дополнение к Ca2+ другие двух- и трехвалентные катионы, такие как Mg2+, Sr2+, Ba2+, La3+ и Gd3+, также вызывают мобилизацию внутриклеточного Ca2+ в паратироидных клетках. Mg2+ и La3+ также повышают образование ИФ3, все эти неорганические катионы подавляют секрецию ПТГ. Постулированный Ca2+-рецептор на паратироидной клетке, следовательно, является смешанным, поскольку он определяет различные внеклеточные двух- и трехвалентные катионы.
Способность различных соединений подражать внеклеточному Ca2+ in vitro обсуждалась Неметом с сотр. /спермин и спермидин/ в Calcium-Binding Proteins in Health and Disease 1987, Academic Press, Inc. p.p. 33-35, Брауном с сотр. /например, неомицин/ 128, Endocrinology 3047, 1991, Ченом с сотр. /дильтиазем и его аналог, TA-3090/ 5, J. Bone and Mineral Res. 581, 1990, и Зайди с сотр. /верапамил/ 167, Biochem. Biophys Res. Comm. 807, 1990.
Браун с сотр., 6, J. Bone and Mineral Res. 11, 1991, обсуждает существующие теории, относящиеся к воздействиям ионов Ca2+ на паратироидные клетки, и предлагает, что результаты могут быть объяснены как рецепторподобным механизмом, так и рецепторнезависимым механизмом следующим образом.
Поливалентные катионы /например, двухвалентные и трехвалентные катионы/ оказывают различные воздействия на паратироидную функцию, такие как ингибирование секреции паратироиодного гормона (ПТГ) и аккумуляция цАМФ, стимуляция аккумуляции инозитолфосфатов и повышение концентрации цитозолического кальция. Полагают, что эти воздействия должны быть опосредованы через "рецепторподобный" механизм. Ингибирование агонистстимулированной аккумуляции цАМФ двухвалентными и трехвалентными катионами, например, блокируется последующей предварительной инкубацией с коклюшным токсином. Итак, putative рецептор поливалентного катиона может быть соединен для ингибирования аденилатциклазы с регуляторным белком /G/ ингибирования гуанинового нуклеотида, Gв.
Недавно мы показали, что поликатионный антибиотик, неомицин, подобен по воздействиям двух- и трехвалентным катионам в некоторых аспектах паратироидной функции. Для определения, являются ли эти воздействия специфическими для этого агента или представляют собой более общее воздействие поликатионов, мы испытали воздействия сильноосновных пептидов, полиаргинина и полилизина, а также протамина на одинаковые параметры в диспергированных бычьих паратироидных клетках. Результаты показывают, что паратироидная клетка отвечает на различные поликатионы, а также на поливалентные катионы возможно по подобным биохимическим путям. Эти результаты были обсуждены в терминах недавно постулированной, "рецепторнезависимой" модуляции белков поликатионами в других системах.
Предполагалось, что Ca2+-рецептор должен быть аналогичным другим G-белоксвязанным рецепторам /например, гликопротеин/, но недавние исследования с другими типами клеток выдвинули возможность, что поликатионы могут модулировать клеточную функцию по альтернативным или дополнительным механизмам. Например, в маст (mast) клетках различные амфипатические катионы, включая мастопаран, пептид из яда осы, 48/80, синтетический поликатион и полилизин, повышают секрецию по чувствительному к коклюшному токсину механизму, предполагая включение G-белка. Не было идентифицировано классического рецептора поверхности клетки, который мог бы медиировать воздействия этих различных агентов. Кроме того, было показано, что эти же соединения активируют непосредственно очищенные G-белки в растворе или в искусственных фосфолипидных везикулах. На основании этих наблюдений было предложено, что амфипатические катионы активируют G-белки и, в свою очередь, секрецию маст-клеток по "рецепторнезависимому" механизму.
Было также показано, что поликатионы интенсивно взаимодействуют с кислыми фосфолипидами. Полилизины с различной длиной цепи /20-1000 аминокислот/ связываются с искусственными фосфолипидными везикулами с константами диссоциации в интервале от 0,5 нМ до 1,5 μМ. Способность к связыванию непосредственно зависит от длины полилизиновой цепи, у полимеров из 1000 аминокислот Kd 0,5 нМ, более короткие полимеры имеют более высокие величины Kd, а лизин не вступает в реакцию в заметной степени. Такое соотношение между активностью и длиной цепи подобно наблюдаемому для эффектов полилизина10200, полилизина3800 и лизина на паратироидную функцию.
Возможно, что связыванием поликатионов с биомембранами продуцирует некоторые из их биологических действий. Было постулировано, что проницаемость плазматических мембран, индуцированная у некоторых типов клеток различными порообразующими агентами, включая поликатионы, будет способствовать их взаимодействию с фосфатидилсеринподобной структурой. Кроме того, "рецепторнезависимая" активация очищенных G-белков амфипатическими катионами будет возможной, когда эти белки включены в фосфолипидные везикулы.
Ионы кальция в миллимолярном интервале концентраций также вызывают заметные изменения структуры мембраны. В некоторых случаях кальций может или антагонизировать или усиливать взаимодействие поликатионов с мембранными липидами. Эти выводы приводят к возможности, что воздействия как поливалентных катионов, так и поликатионов на паратироидные клетки могут включать рецепторнезависимый механизм, не требующий наличия классического G-белоксвязанного рецептора на поверхности клетки. Однако требуются дополнительные исследования, чтобы объяснить молекулярную основу Ca2+ чувствительности этих и других типов клеток. /Цитирования опущены/.
Шобэк и Чен /6/ Supplement 1/, J. Bone and Mineral Res. 1991, 5135 и Pakke с сотр. /6/ Supplement 1/ J. Bone and Mineral Res. 1991, 5118/ описали эксперименты, в которых было указано, что Ca2+-рецептор или Ca2+-сенсор присутствует в паратироидных клетках. Матричная РНК, изолированная из таких клеток, может быть экспрессирована в ооцитах, и требуется получить такие ооциты с фенотипом, который может быть объяснен наличием Ca2+-рецепторного белка.
Краткое изложение изобретения
Заявитель показал, что Ca2+-рецепторные белки у определенных специализированных клеток включены целиком в Ca2+-метаболизм, чтобы определять и отвечать на изменения концентрации внеклеточного Ca2+. Хотя эти рецепторы принимают участие в некоторых общих характеристиках, они могут подвергаться селективному воздействию различных фармакологических агентов. Как будет детально описано ниже, некоторые молекулы идентифицируются по селективной активности на Ca2+-рецепторы паратироидных клеток, остеокластов и C-клеток.
Ca2+-рецепторы представляют собой дискретные молекулярные мишени для нового класса молекул, которые имитируют /"кальцимиметики"/ или антагонизируют /кальцилитики"/ воздействия внеклеточного Ca2+. Такие рецепторы находятся на поверхности клетки и имеют низкое сродство к внеклеточному Ca2+ (кажущаяся Kd обычно больше, чем примерно 0,5 мМ). Такие рецепторы могут включать механизм свободного или связанного эффектора, как определено Купером, Блумом и Ротом "The Biochemical Basis of Neuropharmacology", Ch. 4. Итак, такие рецепторы отличаются от рецепторов внутриклеточного Ca2+, например кальцимодулина и трипонинов. Кальциметики, например, действуют на Ca2+-рецепторы селективно, чтобы непосредственно или не непосредственно снизить фунцию паратироидных клеток или остеоскластов или стимулировать функцию C-клеток. Кальцимиметики и кальцилитики настоящего изобретения позволяют создать новую терапию для гиперпаратироидизма, остеопороза и других Ca2+-зависимых заболеваний. Настоящая заявка в одном аспекте относится к конъюгированию лекарственного препарата с антителом, обеспечивая ему направленную доставку препарата к Ca2+-рецепторам у каждого из этих трех типов клеток и других типов клеток, которые определяют и отвечают на изменения /Ca2+/.
Заявитель сначала продемонстрировал белок Ca2+-рецептора в паратироидных клетках и фармакологически дифференциировал такие Ca2+-рецепторы в других клетках, таких как C-клетки и остеокласты. Заявитель также в первую очередь описал способы, по которым могут быть идентифицированы молекулы, активные у этих Ca2+-рецепторов, и использованы в качестве ведущих молекул при обнаружении, разработке, конструировании, модификации и/или конструкции полезных кальцимиметиков или кальцилитиков, которые являются активными у Ca2+-рецепторов. Такие кальцимиметики или кальцилитики являются полезными при лечении различных болезненных состояний, характеризующихся аномальными уровнями одного или более компонентов, например полипептидов, таких как гормоны, ферменты или факторы роста, экспрессия и/или секреция которых регулируется или находится под воздействием одного или нескольких Ca2+-рецепторов. Далее, идентификация различных Ca2+-рецепторов в различных типах клеток и специфический ответ таких рецепторов на различные ведущие молекулы позволяет дать замысел и конструкцию специфических молекул, активных при лечении специфических заболеваний, которые могут находиться под влиянием таких специфических Ca2+-рецепторов. Например, аномальные уровни секреции паратироидного гормона могут быть подвергнуты действию таких специфических молекул без воздействия на уровни секреции других регулируемых Ca2+ гормонов и т.п.
Идентификации таких ведущих молекул препятствовало отсутствие до настоящего времени системы скрининга с большим количеством исходного материала для обнаружения активных молекул и отсутствие основных структурных данных, на базе которых конструируют эффективные кандидаты в лекарства. Теперь эти преграды сняты с помощью клонирования Ca2+-рецептора паратироидных клеток и функционально родственных рецепторов и систематического исследования структурных признаков некоторых ведущих молекул, которые активируют такие клонированные Ca2+-рецепторы и функционально родственные рецепторы. Клонирование Ca2+-рецептора также дает возможность разработать трансфекционные клеточные линии, пригодные для скрининга с большим количеством исходного материала природного продукта или молекулярных библиотек и синтетических молекул. Это вместе с исследованиями структура - активность, обсужденными выше, обеспечивает технологию, необходимую для разработки новых кальцимиметиков и кальцилитиков.
Заявитель приспособил такие процедуры в этой заявке. кДНК кальциевого рецептора бычьей паратироидной клетки была клонирована и депонирована в АТСС под номером хранения АТСС 75416. При использовании этого клона легко могут быть получены рецепторы неорганических ионов в других тканях и видовых гомологах. Например, Ca2+-рецептор человеческой паратироидной клетки может быть клонирован при скрининге библиотек нуклеиновых кислот или при скрининге функциональной экспрессии в Xenopus ооцитах и могут быть определены структурные признаки органических молекул, необходимые для активности на Ca2+-рецепторе, с помощью испытаний выбранных природных продуктов или библиотек других молекул и последующих исследований структура - активность.
Итак, в первом аспекте, изобретение относится к фармацевтической композиции, включающей молекулу, которая или обладает активностью, подобной внеклеточному Ca2+, вызывая увеличение /Ca2+/в в клетке, или блокируют увеличение /Ca2+/в, вызванное внеклеточным Ca2+. Молекула имеет ЭК50 менее или равную 5 μМ и не является протамином.
Термин "миметический" означает, что молекула обладает одним или несколькими специфическими воздействиями внеклеточного Ca2+ на отвечающую на внеклеточный Ca2+ клетку. Термин не требует, чтобы имитировались все биологические функции внеклеточного Ca2+, но по крайней мере одну такую функцию имитируют. Кроме того, не требуется, чтобы молекула связывалась с тем же самым центром на Ca2+-рецепторе, как это делает внеклеточный Ca2+ (смотри, например, новое соединение NPS 467 и его действие в примере 20 ниже). Термин "блокировать" означает, что одно такое воздействие Ca2+ снижается или предотвращается молекулой. ЭК50 может быть определена с помощью анализа, как описано ниже, где измеряется подобная активность и концентрация молекулы, которая имитирует половину максимального мимикрирующего эффекта, является ЭК50. Наоборот, ЭК50 кальцилитика является тем количеством, которое блокирует половину максимальной активности. Предпочтительно такие анализы измеряют возрастание /Ca2+/в и подтверждают специфичность к Ca2+-рецепторам с помощью описанных ниже способов или их эквивалента.
В предпочтительных вариантах биоанализ, описанный здесь, показывает, что повышение /Ca2+/в в клетке является кратковременным, имеющим длительность менее одной минуты, и повышение /Ca2+/в является быстрым, происходящим за 30 секунд; и молекула также /а/ вызывает продолжительное (более 30 секунд) повышение /Ca2+/в, /б/ вызывает увеличение уровней инозитол-1,4,5-трифосфата и/или диацилглицерина, например, за менее чем 60 секунд, и /в/ ингибирует образование допамин- или изопротеренолстимулизованного АМФ. В дополнение к этому кратковременное увеличение /Ca2+/в устраняет предварительную обработку клетки в течение 10 минут 10 мМ фторида натрия или кратковременное повышение уменьшается при короткой предварительной обработке (не более 10 минут) клетки активатором протеинкиназы C, например форболмиристатацетатом (ФМА), мезерейном или /-/индолактамом V.
В паратироидной клетке эти молекулы, которые являются активными во всех анализах, описанных выше, являются особенно полезными в настоящем изобретении, поскольку они являются специфическими по своим воздействиям на Ca2+-рецептор такой клетки. Это особенно справедливо для описанного выше эффекта предварительной обработки ФМА.
В более предпочтительном варианте клетка является паратироидной клеткой и молекула ингибирует секрецию паратироидного гормона из клетки. Другие предпочтительные варианты включают молекулы, которые вызывают увеличение /Ca2+/в, что определяется, например, как увеличение Cl- потока, имеющегося обычно в Xenopus ооците, инъецированном мРНК из паратироидной клетки, костного остеокласта, окологломерулярной почечной клетки, проксимальной почечной канальцевой клетки, периферической канальцевой почечной клетки, клетки толстой восходящей ветви петли Хенля и/или собирающей протоки, кератиноцита в эпидермисе, парафолликулярной клетки в тироидных /C-клетках/, интестинальной клетки, трофобласта в плаценте, тромбоцита, васкулярной клетки гладкой мышцы, клетки сердечного предсердия, клетки, секретирующей гастрин и глюкагон, почечной мезангиальной клетки и клетки грудной железы.
В других предпочтительных вариантах молекула вызывает мобилизацию внутриклеточного Ca2+, вызывая увеличение /Ca2+/в, клетка является остеобластом или C-клеткой и молекула ингибирует резорбцию кости in vivo, клетка является остеокластом и молекула ингибирует костную резорбцию in vitro или клетка является C-клеткой и молекула стимулирует секрецию кальцитонина in vitro или in vivo, и наиболее предпочтительно молекула является кальцимиметической или кальцилитической, имеющей ЭК50 или ИК50 при Ca2+-рецепторе меньше или равную 5 μМ и даже более предпочтительно меньшую или равную 1 μМ, 100 нмолярную, 10 нмолярную или 1 нмолярную. Такие низкие ЭК50 или ИК50 являются выгодными, потому что они позволяют использовать более низкую концентрацию молекулы in vitro или in vivo для лечения или диагностики. Открытие молекул с такими низкими ЭК50 или ИК50 дает возможность конструировать и синтезировать подобным образом мощные и эффективные молекулы.
Под "кальцимиметической" молекулой понимают любую молекулу, которая обладает одной или более активностями внеклеточного Ca2+ и предпочтительно имитирует активность Ca2+ у рецептора Ca2+. Например, при использовании в отношении паратироидной клетки она является молекулой, которая при испытании на паратироидных клетках in vitro обладает одной или более, а предпочтительно всеми из последующих характеристик, как измерено с помощью методик, хорошо известных на данном уровне техники:
1. Молекула вызывает быстрое (время до пика < 5 с) и кратковременное увеличение /Ca2+/в, которое является невосприимчивым к ингибированию 1 μМ La3+ или Gd3+. Увеличение /Ca2+/в продолжает существовать в отсутствие внеклеточного Ca2+, но исчезает при предварительной обработке иономицином (в отсутствие внеклеточного Ca2+).
2. Молекула делает возможным увеличение /Ca2+/в, вызванное субмаксимальными концентрациями внеклеточного Ca2+.
3. Увеличение /Ca2+/в, вызванное внеклеточным Ca2+, не ингибируется дигидропиридинами.
4. Кратковременное увеличение /Ca2+/в, вызванное молекулой, снимается предварительной обработкой в течение 10 минут 10 мМ фторида натрия.
5. Кратковременное увеличение /Ca2+/в, вызванное молекулой, снижается предварительной обработкой активатором протеинкиназы C /ПКС/, таким как форболмиристатацетат /ФМА/, мезерейн или /-/-индолактам V. Суммарное действие активатора протеинкиназы C является сдвигом вправо кривой концентрация - ответ на молекулу без воздействия на максимальный ответ.
6. Молекула вызывает быстрое (< 30 с) увеличение образования инозитол-1,4,5-трифосфата или диацетилглицерина.
7. Молекула ингибирует образование допамин- или изопротеренолстимулированного циклического АМФ.
8. Молекула ингибирует секрецию ПТГ.
9. Предварительная обработка коклюшным токсином (100 нг/мл в течение > 4 часов) блокирует ингибирующее действие молекулы на образование циклического АМФ, но не оказывает влияния на увеличение /Ca2+/в, инозитол-1,4,5-трифосфата или диацетилглицерина, ни на снижение секреции ПТГ.
10. Молекула вызывает увеличение /Ca2+/в, как определяется, например, как увеличение потока Cl- в Xenopus ооцитах, инъецированных мРНК, обогащенной поли/A/+, из бычьих или человеческих паратироидных клеток, но не оказывает воздействия на Xenopus ооциты, инъецированные водой или мРНК мозга крысы или печени.
11. Подобным образом, используя клонированный рецептор из паратироидных клеток, молекула будет вызывать ответ в Xenopus ооцитах, инъецированных специфической кДНК, мРНК или синтетической смысловой РНК /кРНК/, кодирующей рецептор.
Под "кальцилитической" молекулой понимают любую молекулу, которая блокирует одну или более активностей внеклеточного Ca2+ на чувствительную к внеклеточному Ca2+ клетку, предпочтительно при действии в качестве антагониста на Ca2+-рецептор. Например, при использовании в отношении паратироидной клетки она является молекулой, которая при испытании на паратироидных клетках in vitro обладает одной или более, а предпочтительно всеми из следующих характеристик, как измерено с помощью методик, хорошо известных на данном уровне техники:
1. Молекула блокирует, частично или полностью, способность к увеличению концентраций внеклеточного Ca2+, чтобы:
а) увеличить /Ca2+/в,
б) мобилизовать внутриклеточный Ca2+,
в) увеличить образование инозитол-1,4,5-трифосфата,
г) снизить образование допамин- или изопротеренолстимулированного циклического АМФ, и
д) ингибировать секрецию ПТГ.
2. При низкой /Ca2+/, т.е. 0,5 мМ, молекула сама не изменяет /Ca2+/в.
3. Молекула блокирует увеличение потока Cl- в Xenopus ооцитах, инъецированных поли/A/+-мРНК из бычьих или человеческих паратироидных клеток, вызванного внеклеточным Ca2+ или кальцимиметическими соединениями, но не в Xenopus ооцитах, инъецированных водой или мРНК мозга крысы или печени/
4. Подобным образом при использовании клонированного рецептора из паратироидных клеток молекула будет блокировать ответ в Xenopus ооцитах, инъецированных специфической кДНК, мРНК или кДНК, кодирующей Ca2+-рецептор, вызванный внеклеточным Ca2+ или кальцимиметическим соединением.
Параллельные определения полезных кальцимиметиков и кальцилитиков на Ca2+-рецепторы на других типах клеток являются очевидными из приведенных ниже примеров.
Рецептор Ca2+ способен определить и ответить на некоторые неорганические поликатионы и поликатионные органические молекулы. Например, паратироидная клетка не способна различить увеличение концентрации внеклеточного Ca2+ из-за добавления этих органических поликатионов возможно потому, что эти органические молекулы действуют точно подобно внеклеточному Ca2+ у Ca2+-рецепторов. Кальцимиметические молекулы настоящего изобретения являются особенно хорошими агонистами Ca2+-рецептора и могут быть использованы в качестве лекарств, которые изменяют выбранные клеточные функции, например секрецию ПТГ из паратироидных клеток. В противоположность Ca2+ большинство этих молекул действует только на один или более, но не на все Ca2+-рецепторы и, следовательно, обеспечивают способность специфически воздействовать на один Ca2+-рецептор.
Эти молекулы также обеспечивают ведущие структуры для разработки дополнительных новых лекарств, эффективных для лечения различных заболеваний, где имеют значения /Ca2+/в и /Ca2+/, таких как гиперпаратироидизм, остеопороз, болезнь Пагета, гипертония, почечная болезнь, заболевание кожи, сердечно-сосудистое заболевание, расстройства свертывания крови, желудочно-кишечные заболевания, эндокринные заболевания, аномальности метаболизма воды и рак.
Кальцимиметики и кальцилитики могут быть сформулированы в виде фармацевтических композиций, которые являются полезными для регулирования уровня внеклеточного свободного Ca2+ у пациента и для мимикрирующего действия внеклеточного Ca2+ на клетку, выбранную в описанной выше группе, при введении пациенту такой фармацевтической композиции. До настоящего изобретения заявитель не знал о каких-либо таких молекулах, действующих на Ca2+-рецептор, полезных для лечения заболеваний, вызванных нерегулярностью в работе или регуляцией Ca2+-рецептора, или заболеваний у животных, имеющих нормальные Ca2+-рецепторы, но которые могут быть вылечены при активации или дезактивации таких Ca2+-рецепторов.
В еще одном предпочтительном варианте молекула имеет ЭК50, меньшую или равную 5 μМ для одной или более, но не для всех клеток, выбранных в группе, состоящей из паратироидных клеток, костных остеокластов, окологломерулярных почечных клеток, проксимальных почечных канальцевых клеток, периферических канальцевых почечных клеток, клеток толстой восходящей ветви петли Хенля и/или собирающей протоки, кератиноцита в эпидермисе, парафолликулярной клетки в щитовидной железе (C-клетки), интестинальной клетки, трофобласта в плаценте, тромбоцита, васкулярной клетки гладкой мышцы, клетки сердечного предсердия, клеток, секретирующих гастрин и глюкагон, почечной мезангиальной клетки и клетки грудной железы.
Специфичность действия таких молекул является тем, что особенно выгодно в настоящем изобретении, поскольку она обеспечивает специфическое лечение и диагностику in vivo и in vitro и открытие дополнительных кальцимиметических или кальцилитических молекул.
В специальных предпочтительных вариантах молекула является положительно заряженной при физиологическом pH и выбрана в группе, состоящей из разветвленных или циклических полиаминов, положительно заряженных полиаминокислот и аралкиламинов, например разветвленный полиамин имеет формулу H2N-/CH2/j -/NRi -/CH2/j /k-NH2, где k является целым числом от 1 до 10, каждый j является одинаковым или различным и представляет собой целое число от 2 до 20, а каждый Ri является одинаковым или различным и выбран в группе, состоящей из водорода и -/CH2/j -NH2, где j имеет указанные ранее значения, и по крайней мере один Ri не является водородом.
В альтернативном варианте молекула имеет формулу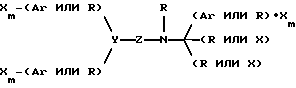
где каждый X независимо выбран в группе, состоящей из H, CH3, CH3O, CH3CH2O, Br, Cl, F, CF3, CHF2, CH2F, CF3O, CH3S, OH, CH2OH, CONH2, CN, NO2 и CH3CH2, Ar является гидрофобным фрагментом, каждый R независимо выбран в группе, состоящей из водорода, метила, этила, пропила, изопропила, бутила, изобутила, циклопентила, циклогексила, циклогептила, циклооктила, инденила, инданила, дигидроиндолила, тиодигидроиндолила, 2-, 3- или 4-пиперид/ин/ила, Y выбран в группе, состоящей из CH, азота и ненасыщенного углерода, Z выбран в группе, состоящей из кислорода, азота, серы,
где каждый n независимо равен 1-4 включительно, а каждый m независимо равен 0-5 включительно. Наиболее предпочтительно молекула является кальцимиметической или кальцилитической.
В предпочтительных вариантах гидрофобный фрагмент выбран в группе, состоящей из фенила, 2-, 3- или 4-пиридила, 1- или 2-нафтила, 1- или 2-хинолила, 2- или 3-индолила, бензила и фенокси; молекула является производным R-фенилпропил-α-фенетиламина и молекула имеет формулу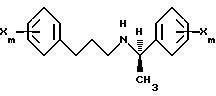
где каждый X предпочтительно независимо выбран в группе, состоящей из Cl, F, CF3, CH3 и CH3O.
В соответствии с предпочтительным аспектом настоящего изобретения новые аналоги и производные фенилпропил-α-фенетиламина имеют формулу
где alk является алкиленом с прямой или разветвленной цепью, содержащей 1-6 атомов углерода, R1 является низшим алкилом с 1-3 атомами углерода или низшим галоидалкилом с 1-3 атомами углерода, замещенным 1-7 атомами галоида, R2 и R3 являются независимо выбранными карбоциклическими арильными или циклоалкильными группами, или моноциклическими или бициклическими, имеющими 5- или 6-членные циклы, необязательно замещенные 1-5 заместителями, независимо выбранными среди низшего алкила с 1-3 атомами углерода, низшего галоидалкила с 1-3 атомами углерода, замещенного 1-7 атомами галоида, низшего алкокси с 1-3 атомами углерода, галоида, нитро, амино, алкиламино, амидо, низшего алкиламидо с 1-3 атомами углерода, циано, гидроксила, ацила с 2-4 атомами углерода, низшего оксиалкила с 1-3 атомами углерода или низшего тиоалкила с 1-3 атомами углерода. Подходящие карбоциклические арильные группы являются группами, имеющими одно или два кольца, по крайней мере одно из которых имеет ароматический характер, и включают карбоциклические арильные группы, такие как фенил, и бициклические арильные группы, такие как нафтил. Как видно из приведенной выше формулы, соединения, охватываемые ею, могут существовать в виде рацемических смесей и в виде индивидуальных изомеров. Особенно предпочтительными являются производные R-фенилпропил-α-фенетиламина, которые проявляют повышенную активность при понижении сывороточного ионизированного кальция.
Предпочтительные соединения включают те, у которых alk является н-пропиленом. Также предпочтительными являются соединения, у которых R1 является метилом. Также предпочтительными являются те соединения, у которых R2 и R3 являются необязательно замещенными фенилами.
Особенно предпочтительные соединения включают те, у которых R2 является монозамещенным фенилом, более предпочтительно метазамещенным. Особенно предпочтительные R3 группы включают незамещенный или монозамещенный фенил, особенно ортозамещенный. Предпочтительные заместители для R2 включают галогид, галоидалкил, предпочтительно тригалоидметил, и алкокси, предпочтительно метокси. Предпочтительные заместители для R3 включают галоид, предпочтительно хлор.
Во втором родственном аспекте изобретение относится к способу лечения пациента, имеющего заболевание или состояние, характеризующееся аномальной /Ca2+/ или /Ca2+/в в одной или более клетках или в крови, или в плазме, или во внеклеточных жидкостях. Способ включает стадию введения пациенту терапевтически эффективного количества молекулы, которая или имитирует активность внеклеточного Ca2+, вызывая повышение /Ca2+/в в клетке, или блокирует повышение /Ca2+/в, вызванное внеклеточным Ca2+.
Под "аномальным" понимают, что пациент по сравнению с общей популяцией имеет другой метаболизм Ca2+, который находится под воздействием одного или более белков /например, гормонов/ в крови или внеклеточных жидкостей организма, или других молекул, которые влияют на уровень внеклеточного и/или внутриклеточного Ca2+. Итак, заболевания включают гиперпаратироидизм, остеопороз и другие костные и минерально-зависимые болезни и т.п. (как описано, например, в стандартных медицинских справочниках, таких как "Harrison's Principles of Internal Medicine"). Такие заболевания лечат в настоящем изобретении молекулами, которые имитируют или блокируют один или несколько эффектов Ca2+ и в результате непосредственно или косвенно влияют на уровни белков или других молекул в организме пациента.
Под "терапевтически эффективным количеством" понимают количество, которое устраняет до некоторой степени один или более симптомов заболевания или состояния пациента. Дополнительно, под "терапевтически эффективным количеством" понимают количество, которое возвращает к нормальным, частично или полностью, физиологические или биохимические параметры, ассоциированные с или вызванные заболеванием или состоянием. Обычно это количество находится между примерно 1 нмолем и 1 μмолем молекулы, в зависимости от ее ЭК50 и возраста пациента, его размеров и заболевания.
В предпочтительных вариантах молекула имеет ЭК50 меньше или равную 5 μМ и она не является протамином; и наиболее предпочтительно взаимодействует с Ca2+-рецептором кальцимиметически или кальцилитически. Наиболее предпочтительно молекула выбрана среди одной из описанных выше.
В других предпочтительных вариантах пациент имеет заболевание, характеризующееся аномальным уровнем одного или более компонентов, уровень которых регулируется или находится под воздействием активности одного или более рецепторов Ca2+, и молекула является активной на Ca2+-рецепторе клетки, выбранной в группе, состоящей из паратироидных клеток, костных остеокластов, окологломерулярных почечных клеток, проксимальных почечных канальцевых клеток, периферических канальцевых почечных клеток, клеток толстой восходящей ветви петли Хенля и/или собирающей протоки, кератиноцита в эпидермисе, парафолликулярной клетки в тироиде (C-клетки), интестинальной клетки, трофобласта в плаценте, тромбоцита, васкулярной клетки гладкой мышцы, клетки сердечного предсердия, клеток секретирующих гастрин и глюкагон, почечной мезангиальной клетки и клетки грудной железы.
В других еще предпочтительных вариантах молекула снижает уровень паратироидного гормона в сыворотке пациента, например, до такого уровня, который имеется у нормального индивидуума, или до степени, достаточной, чтобы вызывать снижение Ca2+ в плазме, и молекула обеспечивается в количестве, достаточном для того, чтобы вызвать терапевтически нужный эффект у пациента.
В третьем аспекте изобретение относится к способу диагностики заболевания или состояния у пациента путем идентификации количества и/или места нахождения (и/или функциональной целостности) одного или более рецепторов Ca2+ в организме пациента и сравнения с тем количеством и/или местом нахождения (и/или функциональной целостностью), которые наблюдаются у нормальных пациентов как указания на наличие заболевания или состояния.
В предпочтительных вариантах способ является иммуноаналитическим, в котором используют антитело к рецептору Ca2+ для идентификации количества и/или места расположения и/или функциональной целостности Ca2+-рецепторов, или анализ включает обеспечение меченой кальцимиметической или кальцилитической молекулы, которая связывается с Ca2+-рецептором, и диагностируемым заболеванием является рак, например эктопическая опухоль паращитовидной железы, или состояние, характеризующееся уровнем выше нормального числа остеокластов в кости или повышенным уровнем активности остеокластов в кости.
В четвертом аспекте изобретение относится к способу идентификации молекулы, полезной в качестве терапевтической молекулы. Способ включает скрининг потенциально полезной молекулы или по ее способности имитировать активность внеклеточного Ca2+ в клетке, или блокировать повышение /Ca2+/в, вызванное внеклеточным Ca2+, и определение того, имеет ли молекула ЭК50 или ИК50 меньше или равную 5 μМ.
В других аспектах изобретение относится к рекомбинантному Ca2+-рецептору, к клетке, включающей рекомбинантный Ca2+-рецептор, очищенной нуклеиновой кислоте, кодирующей Ca2+-рецептор, биологической активности и применению молекулы NPS 019, новым соединениям или композициям с NPS 459, NPS 467 и NPS 568 (см. фиг. 36) и к способу идентификации молекулы, которая имитирует или блокирует одну или более активностей Ca2+ на первом Ca2+-рецепторе, но не на втором Ca2+-рецепторе, например, при использовании рекомбинантного Ca2+-рецептора.
В другом аспекте применяют клетку, включающую рекомбинантный Ca2+-рецептор/ы/ из почки, в качестве тест-системы для скрининга антибиотиков (например, аминогликозидных антибиотиков) на активность к кальциевым рецепторам, которые вызывают почечную токсичность у людей.
Термин "рекомбинантный" означает включение любого Ca2+-рецептора, полученного методиками рекомбинантной ДНК, так что он отличается от Ca2+-рецептора природного происхождения или местом его расположения, чистотой, или структурой. Обычно такой рецептор будет находиться в клетке в количестве, отличающемся от того, которое обычно наблюдается в природе.
Под "очищенным" понимают, что антитело или нуклеиновая кислота отличается от антитела или нуклеиновой кислоты природного происхождения, являясь отделенными от антитела или нуклеионовой кислоты, с которыми они встречаются в природе, например в векторной системе, так что они могут быть использованы для экспрессии рекомбинантного Ca2+-рецептора. Предпочтительно антитело или нуклеиновая кислота поставляются в виде однородного препарата по стандартным методикам.
Такие клонированные рецепторы могут быть экспрессированы в желаемой клетке и выделены и кристаллизованы, чтобы можно было провести определение структуры. Такая структура даст возможность сконструировать полезные молекулы настоящего изобретения, которые могут связываться с Ca2+-рецептором. Кроме того, эквивалент таких рецепторов может быть клонирован с использованием первого клона в качестве зонда для клонов в другой клетке, кДНК или геномных библиотек.
Антитела к клонированному рецептору могут быть изолированы и использованы в качестве лекарственных средств в настоящем изобретении, или в качестве диагностических инструментов для определения количества Ca2+-рецепторов, и/или мест расположения, и/или функциональной целостности для диагностики Ca2+-вызванных заболеваний или состояний. Такие антитела также могут быть использованы in vivo путем внутреннего введения в качестве кальцимиметиков или кальцилитиков.
Итак, в общем, изобретение относится к кальцимиметическим или кальцилитическим молекулам, способным действовать или как селективные агонисты, или антагонисты по отношению к Ca2+-рецептору одной или более, но не всех клеток, выбранных в группе, состоящей из паратироидных клеток, костных остеокластов, окологломерулярных почечных клеток, проксимальных почечных канальцевых клеток, периферических канальцевых почечных клеток, клеток толстой восходящей ветви петли Хенля и/или собирающей протоки, кератиноцита в эпидермисе, парафолликулярной клетки в тироиде (C-клеток), интестинальной клетки, трофобласта в плаценте, тромбоцита, васкулярной клетки гладкой мышцы, клетки сердечного предсердия, клеток, секретирущих гастрин и глюкагон, почечной мезангиальной клетки и клетки грудной железы. Такая композиция может включать любой фармацевтически приемлемый носитель, известный на данном уровне техники, для обеспечения фармацевтической композиции.
Изобретение также относится к модуляции ряда Ca2+-рецепторов у пациента по стандартным методикам, например антисмысловой, и родственным технологиям (например, рибозимы), в качестве терапевтического средства для состояния болезни.
Настоящее изобретение обеспечивает способы идентификации молекул, которые влияют на активность Ca2+-рецептора, используя анализ, как определено ниже, для определения кальцимиметиков и/или кальцилитиков. Кроме того, молекулы, найденные эффективными для снижения или повышения экспрессии Ca2+-рецептора на транскрипционном или трансляционном уровне при использовании анализа, или антител, или других методик, описанных выше, могут быть определены для терапевтических применений.
Приведенное выше краткое изложение было сделано в значительной степени в связи с предпочтительным вариантом, который относится в общем к кальциевым рецепторам. В другом аспекте изобретение относится к новому суперсемейству полипептидных рецептор/сенсорных молекул. Клон кДНК, BoPCaR I, описанный здесь и должным образом депонированный, представляет собой первый такой клон, описанный для кодирования рецептора/сенсора, который является членом этого суперсемейства. Для целей настоящего изобретения рецепторы/сенсоры, принадлежащие к этому суперсемейству, называют рецепторами неорганических ионов.
Новое суперсемейство рецепторов неорганических ионов включает множество таких молекул, которые связаны друг с другом подобием аминокислотной последовательности, структурой и/или функцией. В общем эти признаки также отличают членов этого суперсемейства рецепторов от всех рецепторов/сенсоров, известных в настоящее время на данном уровне техники. Члены этого суперсемейства рецепторов в первую очередь отличаются функционально по их неожиданной способности определять и отвечать на изменения уровней неорганических катионов, таких как кальций, магний, калий, натрий или ионы водорода и т.п., и при ощущении таких ионов вызывать изменения в клеточных функциях. Такие изменения могут включать изменения на уровнях вторичного мессенджера, как это происходит с известным G-белком, связанным с рецепторами, или изменения ионного потока через мембрану, или т.п. Также существуют другие члены этого суперсемейства, которые ощущают неорганические анионы, такие как ионы фосфата или хлорида. Все такие рецепторы входят в область настоящего изобретения, как оно здесь описано. Дополнительно все выделенные лиганды природного происхождения или синтетические для рецепторов/сенсоров, принадлежащих к суперсемейству рецепторов неорганических ионов, входят в область настоящего изобретения. В дополнительном аспекте изобретение относится к терапевтическому применению любых таких природных или синтетических лигандов для рецепторов неорганических ионов.
Дополнительным аспектом настоящего изобретения является то, что рецепторы, принадлежащие к суперсемейству рецепторов
неорганических ионов, могут быть активированы возбудителем, другим, чем связывание лиганда. Например, некоторые члены этого суперсемейства рецепторов активируются физическими силами, такими как силы растяжения, действующие на мембраны клеток, экспрессирующих такие рецепторы. Все такие рецепторы входят в область настоящего изобретения.
Рецепторы неорганических ионов могут быть использованы таким образом, как описано выше в связи с предпочтительным рецептором. Рекомбинантные рецепторы, экспрессированные в разнообразных типах тканей, включая человеческие типы тканей, могут быть использованы для скрининга (включая скрининг с большим количеством материала, израсходованного за определенный срок) для открытия лекарств способами, известными специалистам в данной области. Ионмиметики и ионлитики могут быть легко идентифицированы. Процедуры могут быть приспособлены для индивидуальной функции рецептора. Например, может быть применен активированный кальцием поток хлорида с рецептором неорганического иона, который образует кальциевый канал или который питается (nutrilises) внутриклеточным кальцием. Лигандпропускающие ионные каналы известны на данном уровне техники. Рецепторы неорганических ионов, которые соединены с вторичными мессенджерными системами, позволяют проводить анализ, как описано выше, включая измерение циклического АМФ и инозитолфосфатов. Клетки, которые имеют рекомбинантные рецепторы, связанные с легко детектируемыми агентами, также могут быть использованы, такие как G-белковые сочетания рецепторов с дисперсией пигмента в меланофорах, как описано в литературе. Следовательно, изобретение полностью дает способы обнаружения агентов, которые являются миметиками или литиками рецепторов неорганических ионов, а также самих таких миметиков и литиков, включая те, что предпочтительно выбраны из миметиков и литиков, детально описанных выше. Подобным образом изобретение охватывает диагностику и лечение болезней и состояний, относящихся к рецепторам неорганических ионов, как описано выше в связи с предпочтительным вариантом. Например, заболевания, ассоциированные с повышенными уровнями рецептора неорганических ионов, могут быть диагностированы на основании анализа таких повышенных уровней. Терапевтические молекулы могут быть идентифицированы путем скрининга агентов, которые имитируют активность относящегося к проблеме нативного иона или которые модифицируют действие или мощность имеющего отношение к делу нативного иона. Экспрессия специфической ткани, а также уровни экспрессии могут быть оценены и т.п.
Итак, в настоящем аспекте изобретения обеспечивается новое суперсемейство изолированных рецепторов неорганических ионов и также обеспечиваются их единичные фрагменты. Предпочтительно изолированные рецепторы являются человеческими рецепторами, а наиболее предпочтительно изолированный рецептор является кальциевым рецептором, экспрессированным в тканях или клетках, выбранных в группе, состоящей из паращитовидной железы, сосудистой, почечной ткани, эпидермиса, щитовидной железы, остеокласта, кишечника, грудной железы, трофобласта, тромбоцита, секретирующей гастрин, секретирующей глюкагон, сердечной и мозговой, и их единичных фрагментов. Изобретение, кроме того, относится к полипептидным фрагментам вышеупомянутых рецепторов неорганических ионов, которые обладают желаемой активностью. Например, фрагмент может включать точное место связывания или центр, которые связываются с миметиками, агонистами или антагонистами. Другие полезные фрагменты включают те, которые имеют только наружную часть, охватывающие мембрану участки или внутриклеточную часть рецептора. Кроме того, фрагменты являются полезными для образования химерных рецепторов с фрагментами других рецепторов, как более детально описано ниже. Изобретение также относится к мутантам или аналогам и другим производным изолированных рецепторов. Так, изобретение охватывает не только белки природного происхождения, но и их производные.
Изобретение также относится к нуклеотидным последовательностям, кодирующим вышеупомянутые рецепторы неорганических ионов и их фрагменты и производные. Такие нуклеотидные последовательности могут быть получены с помощью разнообразных процедур и описание настоящего изобретения позволяет специалисту в данной области получить кДНК или геномные клоны, кодирующие такие рецепторы. Например, могут быть приготовлены зонды гибридизации на основе нуклеотидной последовательности BoPCaR I. Когда геномные библиотеки для кДНК библиотек из любой ткани скринируют при низкой убедительности таких зондов, получают гибридизирующие клоны, которые кодируют другие члены суперсемейства. Дополнительно, могут быть легко получены антитела, которые связываются с клонированными или изолированными рецепторами неорганических ионов. Такие антитела также могут быть использованы для выделения других рецепторов изобретения по методикам экспрессия-клонирование, известным специалистам в данной области. Также может быть применена "прогулка" гена-мишени для идентификации и клонирования членов суперсемейства рецепторов неорганических ионов. Дополнительно клоны могут быть получены с помощью процедур экспрессии-клонирования, как описано выше. Эти процедуры могут быть адаптированы для индивидуальной функции интересующего рецептора неорганического иона. Например, также могут быть применены потоки хлорида, активированные кальцием, для клонирования рецептора неорганического иона, который образует кальциевый канал или который мобилизует внутриклеточный кальций. Лигандоткрытые ионные каналы, как описано выше, известны на данном уровне техники. Например, серотониноткрытый ионный канал был клонирован таким образом. Однако рецепторы настоящего изобретения отличаются от других известных лигандоткрытых ионных каналов по своим аминокислотным последовательностям и тем, что они чувствуют такие неорганические ионы, как кальций, магний, ионы водорода, ионы фосфата и т.п.
Также специалисту в данной области следует учитывать, что каждый клонированный рецептор, полученный таким образом, обеспечивает такие новые зонды ДНК или антител, которые сами используются для идентификации еще дополнительных клонов, кодирующих рецепторы неорганических ионов. Кроме того, следует учитывать, что получив последовательность более чем одного такого рецептора, как подчеркнуто выше, становится доступной информация, имеющая отношение к сохранению локализованной последовательности, которая является полезной для получения еще дополнительных клонов, кодирующих другие члены этого суперсемейства. Такие сохраненные последовательности также могут происходить из анализа общей структуры BoPCaR I, так как она обычно включает внеклеточную область, трансмембранную область и внутриклеточную область.
Итак, обеспечиваются изолированные нуклеиновые кислоты, кодирующие рецепторы неорганических ионов и их единичные фрагменты. Предпочтительным рецептором является кальциевый рецептор, который экспрессируется в тканях или клетках, выбранных в группе, описанной выше. Наиболее предпочтительно нуклеиновая кислота кодирует человеческий рецептор неорганического иона или его единичный фрагмент. Изобретение, кроме того, обеспечивает выделение эндогенных регуляторных элементов, контролирующих экспрессию вышеупомянутых рецепторов неорганических ионов, и агенты, которые способны агонизировать или антагонизировать активность этих регуляторных элементов, также могут быть идентифицированы.
Изобретение, кроме того, обеспечивает рекомбинантные клетки, экспрессирующие нуклеиновые кислоты изобретения. В таких клетках нуклеиновая кислота может быть под контролем ее геномных регуляторных элементов или может быть под контролем экзогенных регуляторных элементов, включающих экзогенный промотор. Под термином "экзогенный" понимают промотор, который обычно не связан in vivo транскрипционно с кодирующей последовательностью для рецептора неорганических ионов.
Обеспечиваются антитела к вышеуказанным рецепторам неорганических ионов, а также антитела к аллостерическим участкам таких рецепторов и идиотипы таких рецепторов.
Также обеспечиваются агенты, связывающие рецептор неорганических ионов, соединенные с токсином. Такие агенты могут быть антителами и как таковые являются иммунотоксинами. Такие иммунотоксины могут быть полезными, например, для уничтожения клетки, экспрессирующей рецептор неорганического иона, in vitro или in vivo.
В дополнение к этому изобретение обеспечивает трансгенных нечеловеческих млекопитающих, содержащих трансген, кодирующий рецептор неорганического иона или его единичный фрагмент. Такие трансгены могут быть полезными для воздействия или изменения экспрессии рецептора неорганического иона или инактивации экспрессии рецептора неорганического иона, например, через гомологическую рекомбинацию. Другие трансгены могут быть обеспечены в таких млекопитающих, включая трансгены, кодирующих антисмысл или белок, который способен изменить экспрессию нативного гена рецептора неорганических ионов. Такое изменение может быть сверхрегуляцией, понижающей регуляцией или полной инактивацией.
Так, обеспечиваются способы, включающие контактирование клетки с агентом, который связывается с клеточным компонентом с целью воздействия на экспрессию рецептора неорганического иона. Такие агенты могут связываться с промоторами, другими регуляторными агентами, действующими на промоторы, агенты, способные к связыванию с рецептором, и нуклеиновыми кислотами, кодирующими рецептор или его единичный фрагмент. Контактирование может быть путем внеклеточного введения, путем обеспечения трансгена, кодирующего агент, или любым другим подходящим методом в зависимости от применения, для которого предназначен конкретный способ.
Другие признаки и преимущества изобретения будут видны из последующего описания его предпочтительных вариантов и из формулы изобретения.
Описание предпочтительных вариантов
На фиг. 1 представлены типичные молекулы, полезные в изобретении.
На фиг. 2 приведен график, показывающий увеличение /Ca2+/в, вызванное внеклеточным Ca2+ в quin-2- или fura-2-нагруженных бычьих паратироидных клетках. Исходная /Ca2+/ составляла 0,5 мМ (с использованием CaCl2) и на каждой стрелке увеличивалась с инкрементами 0,5 мМ.
На фиг. 3 приведен график, показывающий мобилизацию /Ca2+/в в бычьих паратироидных клетках. Исходная /Ca2+/ составляет 0,5 мМ и понижается до < 1 μМ при добавлении EGTA, как указано. /а/ Внеклеточный Mg2+ (8 мМ, конечная) вызывает увеличение /Ca2+/в в отсутствие внеклеточного Ca2+. /б/ Предварительная обработка иономицином /1 μМ/ блокирует ответ на Mg2+. /в/ Предварительная обработка 5 μМ молекулы 1799 (митохондриальный разобщитель) не оказывает действия на ответ на Mg2+.
На фиг. 4 представлен график, показывающий предпочтительные ингибирующие воздействия низкой концентрации Gd3+ на стационарное увеличение /Ca2+/в и что высокая концентрация Gd3+ вызывает кратковременное повышение /Ca2+/в в бычьих паратироидных клетках. Верхняя картинка: контроль; исходная концентрация внеклеточного Ca2+ составляет 0,5 мМ и увеличивается на 0,5 мМ на каждом острие стрелки. Средняя картинка: Gd3+ (5 мМ) блокирует стационарное состояние, но не кратковременное повышение /Ca2+/в, вызванное внеклеточным Ca2+. Нижняя картинка: Gd3+ /50 мМ/ вызывает кратковременное повышение /Ca2+/в и снимает как кратковременный, так и продолжительный ответы на внеклеточный Ca2+. На средней и нижней картинках было добавлено точно достаточное количество EGTA, чтобы хелатировать предпочтительно Gd3+: удаляется блок притока Ca2+ и резко возрастает /Ca2+/в.
На фиг. 5 представлен график, показывающий, что воздействия ФМА на /Ca2+/в, образование ИФ3 и секреция ПТГ устраняются при увеличении концентраций внеклеточного Ca2+ в бычьих паратироидных клетках. Для каждого варианта имеется сдвиг на кривой концентрация - ответ для внеклеточного Ca2+. Также отмечается, что кривые концентрация - ответ варьируют сигмоидально при линейном увеличении /Ca2+/.
На фиг. 6 приведен график, показывающий, что увеличение /Ca2+/в, вызванное спермином, прогрессивно снижается при увеличении /Ca2+/ в бычьих паратироидных клетках. Спермин /200 μМ/ прибавляют во время, указанное острием стрелки. На этом и на всех последующих чертежах числа, приведенные на чертеже, представляют собой /Ca2+/в в нМ.
На фиг. 7 представлен график, показывающий, что спермин мобилизует внутриклеточный Ca2+ в бычьих паратироидных клетках. EGTA прибавляют для снижения /Ca2+/ до < 1 àM перед добавлением спермина /200 μМ/, как указано (слева на чертеже). Предварительная обработка иономицином /1 μМ/ блокирует ответ на спермин (справа на чертеже).
На фиг. 8а и 8б приведены графики, показывающие, что спермин повышает /Ca2+/в и ингибирует секрецию ПТГ в бычьих паратироидных клетках подобно внеклеточному Ca2+. Данные для дозы спермина на кривых концентрация - ответ являются средними из двух экспериментов.
На фиг. 9 представлен график, показывающий контрастирующие эффекты ФМА на ответы на внеклеточный Ca2+ и на ответы на АТФγs в бычьих паратироидных клетках. Левая картинка: кривая концентрация - ответ для ингибирования, вызванного внеклеточным Ca2+, образования циклического АМФ сдвинута вправо с помощью ФМА /100 нМ/. Средняя картинка: ФМА не влияет на способность АТФγs увеличивать /Ca2+/в. Отметим также, что кривая концентрация - ответ для АТФγs показывает классический сигмоидальный характер как функция Log концентрации в противоположность внеклеточным двухвалентным катионам.
На фиг. 10 приведен график, показывающий мобилизацию внутриклеточного Ca2+ в человеческих паратироидных клетках, вызванную внеклеточным Mg2+. Клетки были получены из аденомы и выдержаны в ванне из буфера, содержащего 0,5 мМ внеклеточного Ca2+. /а/ Кратковременное и продолжительное повышения /Ca2+/в, вызванные внеклеточным Mg2+ /10 мМ, конечная/, показывают, что на продолжительное увеличение не влияет нимодипин /1 μМ/, но понижается La3+ /1 μМ/ и быстро возвращается, когда La3+ селективно хелатируют низкими концентрациями EGTA. /б/ La3+ /1 μМ/ блокирует продолжительное, но не кратковременное повышение /Ca2+/в, вызванное внеклеточным Mg2+. /в/ Цитозольный Ca2+, кратковременно вызванный внеклеточным Mg2+, существует в отсутствие внеклеточного Ca2+.
На фиг. 11 представлен график, показывающий мобилизацию внутриклеточного Ca2+, вызванную неомицином или протамином, в бычьих паратироидных клетках. На всех чертежах исходная /Ca2+/ и /Mg2+/ составляет 0,5 и 1 мМ соответственно. На фиг. 11 /а/ и /б/ концентрации Ca2+ и Mg2+ увеличены до 2 и 8 мМ от 0,5 и 1 мМ соответственно. На фиг. 11 /в/ - /и/ прибавляли неомицин B /30 μ\М/ или протамин /1 μг/мл/, как указано. Прибавляют La3+ /1 μМ/, EGTA /1 мМ/ или иономицин /100 нМ/, как указано. Каждый чертеж является отражением опыта из 5 или более испытаний с использованием по крайней мере 3 различных клеточных препаратов. Bar = 1 мин.
На фиг. 12 представлен график, показывающий, что неомицин B блокирует кратковременное, но не блокирует стационарное увеличение /Ca2+/в, вызванное внеклеточным Ca2+ в бычьих паратироидных клетках. Слева контроль: /Ca2+/ сначала равна 0,5 мМ и увеличивается с инкрементами 0,5 мМ у каждой открытой стрелки перед добавлением неомицина B /30 μМ/. Справа: прибавляют неомицин B /30 μМ/ перед /Ca2+/. Bar = 1 мин.
На фиг. 13 представлен график, показывающий, что неомицин B или протамин ингибируют секрецию ПТГ при концентрациях, которые вызывают увеличение /Ca2+/в в бычьих паратироидных клетках. Клетки инкубировали при указанных концентрациях органического поликатиона в течение 30 минут в присутствии 0,5 мМ внеклеточного Ca2+. Открытые символы: контрольные ответы по секреции ПТГ в присутствии 0,5 (кружочки) или 2 мМ (ромбики) внеклеточного Ca2+. Величины для /Ca2+/в являются ромбовидными символами. В экспериментах с протамином использовали бычьи клетки, а в экспериментах с неомицином B использовали человеческие (аденома) паратироидные клетки. Каждая точка является средним ± SEM из 3 экспериментов.
На фиг. 14 представлены графические данные, показывающие предпочтительные ингибирующие эффекты ФМА кратковременные изменения цитозольного Ca2+, вызванные спермином в бычьих паратироидных клетках. Исходная /Ca2+/ равна 0,5 мМ, прибавляли спермин /200 μМ/ или АТФ /50 μМ/, как указано. Bar = 1 мин.
На фиг. 15 представлены графически результаты, показывающие, что ФМА сдвигает вправо кривые концентрация - ответ для индуцированного внеклеточным Ca2+ и неомицином B увеличения /Ca2+/в в бычьих паратироидных клетках. Клетки предварительно обрабатывали ФМА в течение 1 мин перед повышением /Ca2+/ или перед добавлением неомицина B, как указано. Каждая точка является средним ± SEM из 3-5 экспериментов.
На фиг. 16 представлены графически результаты, показывающие, что ФМА сдвигает вправо кривые концентрация - ответ для индуцированного внеклеточным Ca2+ и спермином ингибирования секреции ПТГ в бычьих паратироидных клетках. Клетки инкубировали с указанной /Ca2+/ и спермином в течение 30 минут в присутствии (зачерненные кружочки) и в отсутствие (открытые кружочки) 100 нМ ФМА. Каждая точка является средним ± SEM из 3 экспериментов.
На фиг. 17 представлены графически результаты, показывающие, что протамин повышает образование инозитолфосфатов в бычьих паратироидных клетках. Паратироидные клетки инкубировали всю ночь в культуральной среде, содержащей 4 μКю/мл 3H-мио-инозитола, промыли и инкубировали при указанной концентрации протамина при 37oC. После 30 с реакцию прекращали добавлением CHCl3:MeOH:HCl и ИФ1 (кружочки) и ИФ3 (треугольники) разделяли анионообменной хроматографией. Каждая точка является средним из 2 экспериментов, каждый выполнен в трех повторностях.
На фиг. 18 представлены графически результаты, показывающие, что ФМА снижает образование ИФ1, вызванное внеклеточным Ca2+ или спермином в бычьих паратироидных клетках. Меченые 3H-мио-инозитолом клетки экспонировали при указанной /Ca2+/ или спермина в течение 30 секунд перед прекращением реакции и определением ИФ1 анионообменной хроматографией. Hatched колонки: клетки предварительно обрабатывали ФМА /100 нМ/ в течение 5 минут перед повышением /Ca2+/ или добавлением спермина. Каждая величина является средней из 2 экспериментов, каждый осуществлен троекратно.
На фиг. 19 представлены графически результаты, показывающие кратковременное и продолжительное повышения /Ca2+/в, вызванные неомицином B в человеческих (аденома) паратироидных клетках. /Ca2+/ равна 0,5 мМ. /а/ Продолжительное повышение /Ca2+/в, вызванное неомицином B /10 μМ/, понижается La3+. /б/ Кратковременное повышение /Ca2+/, вызванное неомицином B, не подвергается влиянию La3+. /в/ Кратковременное повышение /Ca2+/в существует в отсутствие внеклеточного Ca2+.
На фиг. 20 представлены графически результаты, показывающие, что неомицин B вызывает колеблющееся повышение потока Cl- в Xenopus ооцитах, экспрессирующих Ca2+-рецептор. Верхний чертеж для ооцита три дня спустя после инъекции поли/A/+-мРНК человеческой (гиперпластичной) паратироидной клетки. Нижний чертеж для ооцита, инъецированного водой. Неомицину B не удалось вызвать ответ в пяти инъецированных водой ооцитах, а карбахол вызвал ответ в одной, что показано. На обоих чертежах удерживающий потенциал составляет -76 мВ.
На фиг. 21 представлены графически результаты, показывающие, что неомицину B не удалось оказать основное воздействие или вызвать увеличение в C-клетках. Контроль, левый чертеж: fura-2-нагруженные гМТС 6-23 клетки сначала промывали в буфере, содержащем 1 мМ Ca2+ перед повышением /Ca2+/ до 3 мМ. Правый чертеж: предварительная обработка 5 мМ неомицина B.
На фиг. 22 представлены графически результаты, показывающие, что внеклеточный Ca2+ вызывает увеличение /Ca2+/в в остеокластах крыс. Микрофлуориметрическая регистрация в единственном остеокласте крысы, нагруженном indo-1 и суперслитом в течение указанного времени с буфером, содержащим указанную /Ca2+/. Нормальный буфер, суперслитый между полосами, содержал 1 мМ Ca2+.
На фиг. 23 представлены графически результаты, показывающие, что спермин или неомицин B не смогли вызвать увеличение /Ca2+/в в остеокластах крыс. indo-1-нагруженный остеокласт был суперслит с указанной концентрацией спермина или неомицина B (пустые полоски) один или вместе с 20 мМ Ca2+ (темные полоски).
На фиг. 24 представлены графически результаты, показывающие различное действие аргиотоксина (показанного как аргиопин на чертеже, структуры также показаны на фиг. 1) 659 и аргиотоксина 636 на /Ca2+/в в бычих паратироидных клетках. Исходная /Ca2+/ равна 0,5 мМ и была повышена до 1,5 мМ, где указано (правый чертеж) N. Где указано, прибавляли аргиотоксин 659 /300 μМ/ или аргиотоксин 636 /400 μМ/.
На фиг. 25 представлены графически результаты, показывающие, что внеклеточный Mg2+ или Gd3+ вызывают колеблющееся увеличение потока Cl- в Xenopus ооцитах, инъецированных поли/A/+-мРНК бычьей паратироидной клетки. На чертеже /а/ концентрация внеклеточного Ca2+ составила < 1 μМ, а на чертеже /б/ 0,7 мМ. Чертеж /в/ показывает, что внеклеточный Mg2+ не смог вызвать ответ в ооцитах, инъецированных только мРНК для рецептора вещества K, хотя суперслияние с веществом K вызывает ответ. Удерживающий потенциал составил от -70 до -80 мВ.
На фиг. 26 представлены графически результаты, показывающие, что внеклеточный Ca2+ вызывает колеблющееся повышение потока Cl- в Xenopus ооцитах, инъецированных поли/A/+-мРНК человеческой (гиперпластичной) паратироидной ткани. Ооцит был испытан на отвечаемость на внеклеточный Ca2+ через три дня после инъекции 50 нг поли/A/+-мРНК. Удерживающий потенциал составил -80 мВ.
На фиг. 27 представлены графически результаты, показывающие мобилизацию внутриклеточного Ca2+ в бычьих паратироидных клетках, вызванную будмунхиамином. Будмунхиамин /300 μМ, структура показана выше/ был добавлен, где указано.
На фиг. 28 представлены графически результаты, показывающие, что способность к мобилизации внутриклеточного Ca2+ в паратироидных клетках является стреоспецифической. Бычьи паратиродиные клетки, нагруженные fura-2, сначала были суспендированы в буфере, содержащем 0,5 мМ внеклеточного Ca2+, перед добавлением указанной концентрации каждой молекулы.
На фиг. 29 представлены графически результаты, показывающие влияние La3+ на /Ca2+/в в остеокластах. Показан типичный график для единственного остеокласта крысы, нагруженного indo-1. При низких концентрациях La3+ частично блокирует повышение /Ca2+/в, вызванное внеклеточным Ca2+.
На фиг. 30а и 30б представлены графически результаты, показывающие мобилизацию внутриклеточного Ca2+, вызванную внеклеточным Mn2+, в остеокласте крысы. Внеклеточный Mn2+ вызывает зависящее от концентрации повышение /Ca2+/в (фиг. 30а), которое существует в отсутствие внеклеточного Ca2+ (фиг. 30б).
На фиг. 31а и 31б графически представлены результаты, показывающие мобилизацию /Ca2+/в в остеокласте крысы, вызванную молекулой NPS 449 (см. фиг. 38). Изолированные остеокласты крысы, нагруженные indo-1, подвергают суперслиянию с указанными концентрациями MPS 449 в присутствии (фиг. 31а) или в отсутствие /фиг. 31б/ 1 мМ внеклеточного CaCl2.
На фиг. 32 графически представлены результаты, показывающие мобилизацию внутриклеточного Ca2+ в C-клетках, вызванную NPS 019 (см. фиг. 1). гМТС 6-23 клетки были нагружены fura-2 и промыты в буфере, содержащем 0,5 мМ /Ca2+/. Где указано, прибавляют NPS 019 до конечной концентрации 10 μМ. Типичные чертежи показывают, что кратковременное повышение /Ca2+/в, вызванное NPS 019, является неподдающимся ингибированию La3+ (средний чертеж) и существует в отсутствие внеклеточного Ca2+ (правый чертеж).
На фиг. 33 графически представлены результаты, показывающие, что NPS 456 (фиг. 36) вызывает колеблющееся повышение потока Cl- в Xenopus ооцитах, которые были инъецированы поли/A/+-мРНК бычьей паратироидной клетки.
На фиг. 34 графически представлены результаты, показывающие, что внеклеточный Ca2+ вызывает колеблющееся повышение потока Cl- в Xenopus ооцитах, которые были инъецированы мРНК человеческого отсетокласта. Ооцит был испытан на отвечаемость на внеклеточный Ca2+ через три дня после инъекции 50 нг суммарной поли/A/+-мРНК.
На фиг. 35 графически представлены результаты, показывающие, что Ca2+-рецептор паратироидной клетки кодируется мРНК в интервале 2,5-3,5 kb поли/A/+-мРНК бычьей паратироидной клетки фракционировали по размеру в градиентах глицерина и собрали десять фракций. Каждую фракцию инъецировали /50 нг/ фракцию// отдельно в Xenopus ооциты. Через три дня исследовали ооциты на их способность отвечать на неомицин B /10 μМ/ с колеблющимся повышением потока Cl-.
На фиг. 36 показана химическая структура молекул, происходящих из дифенилпропил-α-фенетиламина, иллюстрирующая семейство молекул, которые были получены и скринированы для нахождения полезных молекул изобретения.
На фиг. 37 приведены графически результаты, показывающие что NPS 021 является кальцилитическим соединением, которое блокирует влияние внеклеточного Ca2+ на /Ca2+/в в бычьих паратироидных клетках. Клетки сначала промывают буфером, содержащим 0,5 мМ CaCl2, и, где указано, повышают /Ca2+/ до конечной концентрации 2 мМ (левый чертеж). Добавление NPS 021 /200 μМ/ не вызывает изменения /Ca2+/в, но ингибирует увеличение /Ca2+/в, вызванное внеклеточным Ca2+ (правый чертеж).
На фиг. 38 приведен график, показывающий ответ Ca2+ in vivo на NPS R, S-467.
На фиг. 39 приведен график, показывающий ответ ПТГ in vivo на NPS R, S-467.
На фиг. 40 приведен график, показывающий ответ сывороточного Ca2+ in vivo на 25 мг/кг NPS R, S-467.
На фиг. 41 приведен график, показывающий ответ /Ca2+/в in vivo в бычьих паратироидных клетках на различные энантиомеры NPS 467.
На фиг. 42 приведен график, показывающий ответ сывороточного Ca2+ in vivo у крыс на различные энантиомеры NPS 467.
На фиг. 43а приведена реакционная схема получения фендилина или аналогов фендилина или производных, приведенных на фиг. 36. На фиг. 43б приведена реакционная схема синтеза NPS 467.
На фиг. 44 приведена кривая доза - ответ, показывающая, что NPS 467 снижает сывороточный ионизированный кальций у крыс при оральном введении.
На фиг. 45 приведена рестрикционная карта плазмиды, содержащей BoPCaR I, депонированной в АТСС под номером хранения АТСС 75416.
На фиг. 46 приведена рестрикционная карта BoPCaR I.
На фиг. 47 приведена нуклеотидная последовательность (примерно 90% точности) фрагмента 2,2 Ко секвенированной BoPCaR I.
Кальцимиметические и кальцилитические молекулы
Кальцимиметические и кальцилитические молекулы, полезные в изобретении, в общем описаны ниже. Эти молекулы могут быть легко идентифицированы с использованием скрининговых процедур для определения молекул, которые имитируют или антагонизируют активность Ca2+ у Ca2+-рецепторов. Примеры таких процедур приведены ниже. Эти примеры не являются ограничивающими изобретение, но только иллюстрируют способы, которые легко использовать или модифицировать специалисту в данной области.
Обычно кальцимиметические и кальцилитические молекулы идентифицируют путем скрининга молекул, которые созданы по образцу описанных ниже (называемых ведущими молекулами). Как можно видеть из приведенного ниже, имеется несколько специфических кальцимиметиков и кальцилитиков, полезных у различных Ca2+-рецепторов. Производные молекулы легко конструируются по стандартным процедурам и испытываются по одному из многих протоков, известных специалистам в данной области. Может быть легко отобрано много молекул, чтобы идентифицировать наиболее полезную в настоящем изобретении.
Органические катионные молекулы, которые имитируют или антагонизируют действия Ca2+ в других системах, имеют структуру, требующуюся для активности на Ca2+-рецепторе. Рациональная схема для других полезных молекул включает изучение молекулы, про которую известно, что она является кальцимиметиком или кальцилитиком, а затем модификацию структуры известной молекулы. Например, полиамины являются потенциальными кальцимиметиками, поскольку спермин имитирует действие Ca2+ в нескольких системах in vitro. Результаты показывают, что спермин на самом деле вызывает изменения /Ca2+/в, а секреция ПТГ напоминает секрецию, вызванную внеклеточными двух- и трехвалентными катионами (см. ниже). Наоборот, Ga3+ противодействует влиянию Gd3+ на рецептор/ы/ кальция бычьего паратироида. Следовательно, приведенные ниже эксперименты позволяют показать, что такая феноменология, полученная со спермином, включает одинаковые механизмы, используемые внеклеточным Ca2+. При этом оцениваются воздействия спермина на различные физиологические и биохимические параметры, которые характеризуют активацию Ca2+-рецептора. Молекулы, обладающие подобными воздействия, являются полезными в настоящем изобретении и могут быть обнаружены путем отбора или получения молекул, имеющих структуру, подобную спермину. Как только обнаружена другая полезная молекула, этот процесс отбора может быть легко повторен.
Для ясности ниже приводится определенная серия протоколов скрининга для идентификации таких полезных молекул, которые являются активными у Ca2+-рецептора паратироидной клетки, или которые действуют как агонисты или антагонисты клеточного ответа на изменения /Ca2+/. Эквивалентный анализ может быть использован для молекул, активных у других Ca2+-рецепторов или других рецепторов неорганических ионов, или которые, иначе, имитируют или антагонизируют клеточные функции, регулируемые /Ca2+/ или другими ионами. Эти анализы являются примерами процедур, которые полезны для обнаружения молекул, включая кальцимиметические молекулы, настоящего изобретения. Эквивалентные процедуры могут быть использованы для обнаружения литических молекул, включая кальцилитические молекулы, путем скрининга таких молекул по наибольшему антагонизму действия на ион, включая внеклеточный Ca2+. Анализ in vitro может быть использован для характеристики селективности, насыщенности и обратимости этих миметиков и литиков по стандартным методикам.
Процедура скрининга
Обычно бычьи паратироидные клетки, нагруженные fura-2, сначала суспендируют в буфере, содержащем 0,5 мМ CaCl2. Испытуемое вещество прибавляют в кювету в малом объеме (5-15 мкл) и отмечают любые изменения сигнала флуоресценции. Проводят кумулятивное увеличение концентрации испытуемого вещества в кювете до тех пор, пока не достигнут какой-либо заранее определенной концентрации или не будут отмечены изменения сигнала флуоресценции. Если не отмечаются изменения сигнала флуоресценции, молекула считается неактивной и дальнейшие испытания не проводят. При начальных исследованиях, например с молекулами типа полиамина, молекулы испытывают при таких высоких концентрациях как 5-10 мМ. Поскольку теперь известны более мощные молекулы (см. ниже), максимальную концентрацию снижают. Например, более новые молекулы испытывали при концентрациях до 500 мМ или менее. Если не отмечается изменений при флуоресценции при этой концентрации, молекула может считаться неактивной.
Молекулы, вызывающие увеличение /Ca2+/в, подвергают дополнительным исследованиям. Двумя основными характеристиками молекулы, существенными для признания ее кальцимиметической молекулой, являются мобилизация внутриклеточного Ca2+ и чувствительность к РКС активаторам. Было найдено, что молекулы, вызывающие мобилизацию внутриклеточного Ca2+ ФМА-чувствительным образом, однозначно являются кальцимиметическими молекулами и ингибируют секрецию ПТГ. При необходимости могут быть проведены дополнительные испытания для подтверждения этого мнения. Далее, если молекула вызывает мобилизацию внутриклеточного Ca2+ ФМА-чувствительным образом, ее направляют на скрининг на человеческих паратироидных клетках. Например, проводят измерения /Ca2+/в для определения ЭК50 и измеряют способность молекулы ингибировать секрецию ПТГ в человеческих паратироидных клетках, которые были получены от пациентов, подвергшихся операции по первичному или вторичному гиперпаратироидизму. Более низкие ЭК50 или ИК50 соответствуют более мощным как кальцимиметики или кальцилитики молекулам.
Измерение /Ca2+/в с fura-2 обеспечивает очень быстрое средство скрининга новых органических молекул по активности. За день может быть исследовано 10-15 молекул и оценена их способность мобилизовать внутриклеточный Ca2+ (или нет). Также может быть оценена чувствительность любого наблюдаемого увеличения /Ca2+/в к понижению ФМА. Кроме того, один клеточный препарат может обеспечить данные по /Ca2+/в, уровню циклического АМФ, ИФ3 и секреции ПТГ. Типичная процедура заключается в нагрузке клеток fura-2 и последующем разделении клеточной суспензии на две, большую часть клеток используют для измерения /Ca2+/в, а оставшиеся инкубируют с молекулами для оценки их действия на циклический АМФ и секрецию ПТГ. Благодаря чувствительности радиоиммуноанализа к циклическому АМФ ПТГ, обе переменные могут быть определены в одной инкубационной пробирке, содержащей 0,3 мл клеточной суспензии (около 500000 клеток). Измерения инозитолфосфатов требуют затрат времени при скрининге. Однако ионообменные колонки, элюируемые хлоридом (а не форматом), обеспечивают быстрое средство для скрининга образования ИФ3, поскольку не требуется применения роторного испарения (на которое затрачивается около 30 часов). Этот способ позволяет обработать около 100 образцов за один день. Те молекулы, которые вызывают интерес при оценке по измерению /Ca2+/в, циклического АМФ, ИФ3 и ПТГ, затем подвергают более строгому анализу путем исследования образования различных инозитолфосфатов и оценки их изомерных форм ВЭЖХ.
Интересные молекулы, определенные в этих протоколах, затем оценивают на специфичность, например, исследуя их влияние на /Ca2+/в в кальцитонинсекретирующих C-клетках, используя, например, клеточную линию МТС 6-23 крыс.
Ниже приводятся иллюстрации методик, полезных для этих скрининговых процедур. Примеры типичных результатов для различных испытаний кальцимиметических или кальцилитических молекул приведены на фиг. 2-34.
Получение паратироидной клетки
Паратироидные железы получают от свежезабитых детенышей (в возрасте 12-15 недель) на местной скотобойне и транспортируют в лабораторию в охлажденном на льду буфере для паратироидных клеток (ПКБ), который содержит (мМ): NaCl 126, KCl 4, MgCl2 1, Na-HEPES 20, pH 7,4, глюкоза 5,6 и различные количества CaCl2, например 1,25 мМ. Человеческие паратиродиные железы, полученные от пациентов, подвергнувшихся хирургическому удалению паратироидной ткани при первичном или уремическом гиперпаратироидизме (ГПТ), обрабатывали так же, как и бычьи ткани. Железы обрезают от избытка жира и соединительной ткани, а затем режут тонкими ножницами на кубики приблизительно 2-3 мм. Готовят диссоциированные клетки при переваривании коллагеназой. Диссоциированные клетки затем очищают центрифугированием в буфере Перколля. Полученный в результате препарат паратироидных клеток по существу не содержит красных кровяных клеток, адипоцитов и капиллярной ткани, как проверено фазовой контрастной микроскопией и окрашиванием Суданом черным B. Диссоциированные и очищенные паратироидные клетки находятся в виде маленьких кластеров, содержащих 5-20 клеток. Клеточная вариабельность, как показано исключением трипаном синим или этидиний бромидом, обычно составляет 95%.
Хотя для экспериментальных целей клетки могут быть использованы в этой точке, физиологические ответы (суперподавляемость секреции ПТГ и остаточные уровни /Ca2+/в) будут лучше после культивирования клеток в течение ночи. Первичная культура также имеет то преимущество, что клетки могут быть помечены изотопами вблизи изотопного равновесия, как необходимо для исследований, включающих измерения метаболизма инозитолфосфата (см. ниже). После очистки на градиентах Перколля клетки несколько раз промывают смесью 1:1 Хэм F12 - Дульбекко модифицированной средой Игла (GIBCO), дополненной 50 μг/мл стрептомицина, 100 E/мл пенициллина, 5 μг/мл гентамицина и ИТС+. ИТС+ представляет собой предварительно смешанный раствор, содержащий инсулин, трансферрин, селен и бычий сывороточный альбумин/БСА/ - линоленовую кислоту (Collaborative Research, Bedford, MA). Затем клетки переносят в пластиковые колбы (75 или 150 см2, Фалькон) и инкубируют при 37oC во влажной атмосфере 5% CO2. Не добавляют сыворотку к этим ночным культурам, поскольку ее наличие позволяет клеткам присоединяться к пластику, вызывает пролиферацию и дедифференцирование. Клетки, культивированные в указанных выше условиях, легко удаляются из колбы декантацией и показывают такую же вариабельность, как и свежеприготовленные клетки.
Измерение цитозольного Ca2+
Очищенные паратироидные клетки снова суспендируют в 1,25 мМ CaCl2 - 2% БСА - ФСБ, содержащем 1 μМ fura-2-ацетоксиметилового эфира, и инкубируют при 37oC в течение 20 минут. Затем клетки осаждают центрифугированием, повторно суспендируют в том же буфере, удаляя эфир, и инкубируют еще 15 минут при 37oC. Клетки последовательно промывают дважды ФСБ, содержащим 0,5 мМ CaCl2 и 0,5% БСА, и выдерживают при комнатной температуре (около 20oC). Непосредственно перед использованием клетки разбавляют в пять раз предварительно подогретым 0,5 мМ CaCl2 - ФСБ, чтобы получить конечную концентрацию БСА 0,1%. Концентрация клеток в кювете, использованной для измерения флуоресценции, составляет 1-2•106 /мл.
Флуоресценцию нагруженных индикатором клеток измеряют при 37oC на спектрофлуориметре (Biomedical Instrumentation Group, Universtity of Pennsylvania, Phyladelphia, PA), оборудованном держателем термостатированной кюветы и магнитной мешалкой, используя длины волн возбуждения и эмиссии 340 и 510 нм соответственно. Эта флуоресценция показывает уровень цитозольного Ca2+. Сигналы флуоресценции калибруют, используя дигитонин (50 μг/мл, конечная), чтобы получить максимум флуоресценции (Fmax), и EGTA (10 мМ, pH 8,3, конечная), чтобы получить минимальную флуоресценцию (Fmin), и константу диссоциации 224 нм. Утечка красителя зависит от температуры и чаще всего происходит в первые 2 минуты после нагревания клеток в кювете, утечка красителя увеличивается только очень медленно после этого. Чтобы точно откалибровать утечку красителя, клетки помещают в кювету и перемешивают при 37oC в течение 2-3 минут. Затем удаляют клеточную суспензию, клетки осаждают центрифугированием и надосадочную жидкость возвращают в чистую кювету. Надосадочную жидкость затем обрабатывают дигитонином и EGTA, как выше, чтобы получить оценку утечки красителя, которая составляет обычно 10-15% от суммарного Ca2+-зависимого флуоресцентного сигнала. Эту оценку вычитают из кажущейся Fmin.
Измерение секреции ПТГ
В большинстве экспериментов используют клетки, нагруженные fura-2, при исследовании секреции ПТГ. Нагруженные fura-2 паратироидные клетки не изменяют своего секреторного ответа на внеклеточный Ca2+. Клетки суспендируют в ПСБ, содержащем 0,5 мМ CaCl2 и 0,1% БСА. Инкубацию проводят в пластиковых пробирках (Фалькон 2058), содержащих 0,3 мл клеточной суспензии с или без малых объемов CaCl2 и/или органических поликатионов. После инкубации при 37oC в течение различного времени (обычно 30 мин) пробирки помещают на лед и клетки осаждают центрифугированием при 2oC. Образцы надосадочной жидкости доводят до pH 4,5 уксусной кислотой и хранят при -70oC. Этот протокол используют как для бычьих, так и человеческих паратироидных клеток.
Для бычьих клеток количество ПТГ в образцах надосадочной жидкости определяют путем гомологического радиоиммуноанализа с использованием GW-1 антитела или его эквивалента при конечном разбавлении 1/45000. 125I-ПТГ (65-84, ИНКСТАР, Стиллвотер, МН) используют в качестве метки и разделяют фракции с помощью активированного декстраном угля. Счет образцов и данные восстановления осуществлены на гамма-счетчике Паккард Кобра 5005.
Для человеческих клеток используют коммерчески доступный радиоиммунологический аналитический набор (INS-PTH; Nichols Institute, Los Angeles, CA - Николс Инститьют, Лос Анжелес, КА), который распознает интактный и N-концевой человеческий ПТГ, потому что GW-1 антитело плохо распознает человеческий ПТГ.
Измерение циклического АМФ
Клетки инкубировали, как описано выше, для изучения секреции ПТГ и в конце инкубации отбирают образец 0,15 мл и переносят в 0,85 мл горячей (70oC) воды и нагревают при этой температуре в течение 5-10 минут. Пробирки затем несколько раз замораживают и оттаивают и клеточный дебрис осаждают центрифугированием. Порции надосадочной жидкости ацетилируют и определяют концентрации циклического АМФ радиоиммуноанализом.
Измерение образования инозитолфосфата
Метят фосфолипидные мембраны путем инкубирования паратироидных клеток с 4 мКю/мл 3H-инозитола в течение 20-24 часов. Затем клетки промывают и снова суспендируют в ФСБ, содержащем 0,5 мМ CaCl2 и 0,1% БСА. Инкубации проводят в микроцентрифужных пробирках в отсутствие и в присутствии различных концентраций органического поликатиона в течение различного времени. Реакции заканчивали добавлением 1 мл хлороформа/метанола/ 12 N HCl (200:100:1, объем/объем/объем). Затем прибавляют водный гидролизат фитиновой кислоты (200 мкл), 25 мг фосфата /пробирку/. Пробирки центрифугируют и 600 мкл водной фазы разбавляют в 10 мл воды.
Инозитолфосфаты разделяют ионообменной хроматографией, используя AGI-X8 в хлорид- или форматной форме. Когда должны быть определены только уровни ИФ3, используют хлоридную форму, тогда как используют форматную форму для разрешения основных инозитолфосфатов /ИФ3, ИФ2 и ИФ1/. Для определения только ИФ3 разбавленный образец наносят на колонку в хлоридной форме и промывают колонку 10 мл 30 мМ HCl, затем 6 мл 90 мМ HCl и элюируют ИФ3 3 мл 500 мМ HCl. Последний элюат разбавляют и подсчитывают. Для определения всех основных инозитолфосфатов разбавленный образец наносят на колонку в форматной форме и элюируют последовательно ИФ1, ИФ2 и ИФ3 путем увеличения концентраций форматного буфера. Образцы, элюированные из форматных колонок, подвергают роторному испарению, остатки переводят в коктейль и подсчитывают.
Изомерные формы ИФ3 оценивают ВЭЖХ. Реакции прекращают добавлением 1 мл 0,45 М перхлорной кислоты и хранят на льду в течение 10 мин. После центрифугирования устанавливают pH надосадочной жидкости равным 7-8 с помощью NaHCO3. Экстракт затем наносят на Партисил SAX анионообменную колонку и элюируют при линейном градиенте формата аммония. Различные фракции затем обессоливают Дауэксом с последующим роторным испарением перед жидкостным сцинцилляционным счетом на Паккард Трикарб 1500 LSC.
Для всех методов разделения инозитолфоcфатов были использованы соответствующие контроли с применением аутеничных стандартов для определения, не препятствуют ли органические поликатионы разделению. Если это так, образцы обрабатывают катионообменной смолой для удаления мешающей молекулы перед разделением инозитолфосфатов.
Измерение цитозольного Ca2+ в C-клетках
Неопластичные С-клетки, происходящие из мозговой тироидной карциномы крысы (r MTC 6-23), полученные из Американской коллекции типовых культур (АТСС N 1607), культивировали в виде монослоев на Дальбеко модифицированной среде игла (ДМЕМ) плюс 15% лошадиной сыворотки в отсутствие антибиотиков. Для измерений /Ca2+/в клетки с 0,02% ЕДТА /0,05% трипсина промывают дважды ФСБ, содержащим 1,25 мМ CaCl2 и 0,5% ВСА, и нагружают fura-2, как описано выше для паратироидных клеток. Измерения /Ca2+/в проводят, как описано выше, с соответствующими коррективами для утечки красителя.
Измерение /Ca2+/в в остеокластах крысы
Остеокласты были получены из 1-2-дневных крыс Спраг-Дейли с использованием асептических условий. Крысят умерщвляли обезглавливанием, удаляли задние лапы, быстро освобождали бедра от мягкой ткани и помещали в предварительно подогретую F-12/ДМЕМ среду, ДМЕМ содержит 10% фетальной телячьей сыворотки и антибиотики (пенциллин - стрептомицин - гентамицин, 100 E/мл - 100 μнг/м - 100 μг/мл). Кости двух крысят разрезали вдоль длины и помещали в 1 мл культуральной среды. Костные клетки получают при осторожном растирании в порошок костных фрагментов пластиковой пипеткой и разбавлении культуральной средой. Костным фрагментом дают отстояться и равные порции (около 1 мл) среды переносят на культуральный планшет с 6-ю ячейками, имеющими 25-миллиметровые стеклянные покровные стекла. Клеткам дают осесть в течение 1 часа при 37oC во влажной атмосфере 5% CO2 - воздух. Покровные стекла затем промывают 3 раза свежей средой для удаления неприкрепившихся клеток. Измерения /Ca2+/в в остеокластах осуществляют в течение 6-8 часов после удаления неприкрепившихся клеток.
Клетки, прикрепившиеся к покровным стеклам, нагружают indo-1 путем инкубации с 5 μМ indo-1 ацетоксиметиловым эфиром /0,01% Плюроник F28 в течение 30 минут при 37oC в F-12/ДМЕМ без сыворотки, содержащей вместо этого 0,5% БСА. Покровные стекла затем промывают и инкубируют дополнительно 15 минут при 37oC в F-12/ДМЕМ без эфира перед переносом в камеру суперслияния, смонтированную на предметном столике Никон Диафот инвертного микроскопа, оборудованного для микрофлуориметрии. Остеокласты легко идентифицируются по их большому размеру и наличию множества ядер. Клетки подвергают суперслиянию с буфером (обычно ФСБ, содержащий 0,1% БСА и 1 мМ Ca2+) со скоростью 1 мл/мин с или без испытуемого вещества. Флуоресценция, испускаемая при возбуждении 340 нм, была направлена через световой путь микроскопа на дихроичное зеркало 440 нм, и собирают с помощью фотоумножительных трубок интенсивность флуоресценции при 495 и 405 нм. Пропускные способности фотоумножительных трубок амплифицировали, digitised и хранили в 80386 PC. Соотношения интенсивности флуоресценции использовали для оценки /Ca2+/в.
Экспрессия ооцита
В дополнительных исследованиях в скрининговых протоколах использовали Xenopus ооциты, инъецированные мРНК из бычьих или человеческих паратироидных клеток, и измеряли поток Cl- как косвенный метод контроля повышения /Ca2+/в. Ниже приводится пример испытания влияния неомицина.
Ооциты инъецировали обогащенной поли/A/+-мРНК из человеческой паратироидной ткани (гиперпластичные железы из случая вторичного ГПТ). Через 3 дня ооциты испытывали на их ответ на неомицин. Неомицин B вызывает колеблющееся повышение потока Cl-, которое прекращается при суперслиянии с несодержащим лекарства солевым раствором (см. фиг. 20). Ответы на неомицин B наблюдали при концентрациях между 100 μМ и 10 мМ. Для обеспечения того, чтобы ответ, вызываемый неомицином B, был зависящим от инъекции паратироидной мРНК, определили влияние неомицина B на потоки в инъецированных водой ооцитах.
В каждом из пяти исследованных ооцитов неомицин B (10 мМ) не вызывал какого-либо изменения в потоке. Известно, что около 40% ооцитов отвечает на карбахол, эффект, медиированный эндогенным мускариновым рецептором. В пяти исследованных ооцитах один показал направленные внутрь потоки в ответ на карбахол, и это показано на фиг. 20б. Следовательно, в клетках, экспрессирующих мускариновый рецептор в сочетании с повышением /Ca2+/в и потоком Cl-, неомицин B не вызывает ответа. Это указывает, что ответ на неомицин B зависит от экспрессии специфического белка, кодируемого мРНК паратироидной клетки. Совершенно серьезно предполагается, что в интактных клетках неомицин B действует непосредственно на Ca2+-рецептор, изменяя функцию паратироидной клетки.
Конструирование лекарства из ведущих молекул
Некоторые органические молекулы имитируют или антагонизируют действие внеклеточного Ca2+ при воздействии на Ca2+-рецептор, как показано здесь. Однако испытанные молекулы необязательно пригодны в качестве кандидатов в лекарства, но они служат для демонстрации того, что гипотеза о терапии, основанной на Ca2+-рецепторе, является правильной. Эти молекулы могут быть использованы для определения структурных признаков, которые могут вызвать их воздействие на Ca2+-рецептор и, следовательно, выбрать молекулы, полезные в настоящем изобретении.
Пример такой аналитической процедуры приводится ниже. Этот пример детализирован в приводимых ниже примерах, но является полезным здесь, чтобы показать основную причину, которая может быть использована для конструирования полезных молекул настоящего изобретения из ведущих молекул, обсуждаемых здесь. Специалистам в данной области известны аналитические стадии, определенные в примере, и что аналогичный анализ может быть проведен на других ведущих молекулах до тех пор, пока не будет определено наиболее желаемое кальцимиметическое или кальцилитическое соединение.
Другие примеры также приведены ниже. Вместе представленные данные показывают, что полезные ведущие молекулы будут иметь ароматические группы, которые предпочтительно замещены в одном или более положениях, и могут иметь разветвленные или линейные, замещенные или незамещенные алкильные группы, как желательно. В дополнение к этому, важно, чтобы выбирались молекулы правильной стереоспецифичности, чтобы обеспечить более высокое сродство к желаемому Ca2+-рецептору. Следовательно, эти данные отмечают в известном уровне техники то, что соответствует ведущим молекулам, которые могут быть дериватизированы для нахождения оптимальных желаемых молекул настоящего изобретения, почти как описано ниже.
Хотя они и различаются по структуре, испытанные молекулы могут иметь общие признаки, которые могут быть исследованы. В этом примере была исследована корреляция между чистым положительным зарядом и мощностью при мобилизации внутриклеточного Ca2+. Протамин /+21; ЭК50 = 40 нМ/ является более эффективным, чем неомицин B (+6; ЭК50 = 20 μМ в человеческих паратироидных клетках и 40 μМ в бычьих паратироидных клетках), который является более эффективным, чем спермин (+4; ЭК50 = 150 μМ) для вызова мобилизации /Ca2+/в в паратироидных клетках. Эти результаты вызывают вопрос, только ли один положительный заряд определяет мощность, или же имеются другие структурные признаки, которые вносят свой вклад в активность на Ca2+-рецепторе. Это важно определить вначале, потому что это в значительной мере согласуется с мнением, что Ca2+-рецептор может быть мишенью для эффективных и специфических терапевтических молекул. Итак, могут быть изучены различные другие органические поликатионы, родственные неомицину B и спермину, для определения соотношения между чистым положительным зарядом молекулы и ее мощностью для мобилизации внутриклеточного Ca2+.
Первую серию исследованных молекул составляют аминогликозиды. Молекулы исследовали на бычьих паратироидных клетках и определяли их ЭК50 для мобилизации внутриклеточного Ca2+. Для аминогликозидов порядок мощности вызывания кратковременного цитозольного Ca2+ располагается следующим образом: неомицин B (ЭК50 = 20 или 40 μМ), гентамицин (150 μМ), беканамицин (200 μМ), стрептомицин (600 μМ). Канамицин и линкомицин не оказывали воздействия при испытаниях при концентрациях 500 μМ. Чистый положительный заряд у этих аминогликозидов при pH 7,3 составляет неомицин B /+6/ > гентамицин /+5/ = беканамицин /+5/ > канамицин /средний +4,5/ > стрептомицин /+3/ > линкомицин /+1/. Затем внутри аминогликозидной серии имеется некоторая корреляция между чистым положительным зарядом, но она не является абсолютной и канамицин, про который можно предположить, что он будет более мощным, чем стрептомицин, не проявляет активности.
Испытания различных полиаминов выявили дополнительные и более заметные несоответствия между чистым положительным зарядом и мощностью. Исследовали три структурных класса полиаминов: /1/ с прямой цепью, /2/ с разветвленной цепью и /3/ циклические. Структуры исследованных полиаминов приведены на фиг. 1. Среди полиаминов с прямой цепью спермин /+4; ЭК50 = 150 μМ/ является более мощным, чем пентаэтиленгексамин /+6; ЭК50 = 500 μМ/ и тетраэтиленпентамин /+5; ЭК50 = 2,5 μМ/, хотя последние молекулы имеют больший чистый положительный заряд.
Мы синтезировали некоторые полиамины с разветвленной цепью, которые имели различное количество вторичных и первичных аминогрупп и, следовательно, различались по чистому положительному заряду. Две таких молекулы, NPS 381 и NPS 382, были исследованы на воздействие на /Ca2+/в в бычьих паратироидных клетках. NPS 382 /+8; ЭК50 = 50 μМ/ является примерно вдвое более мощным, чем NPS 381 /+10; ЭК50 = 100 μМ/, хотя он имеет вдвое меньший положительный заряд.
Подобное несоответствие между положительным зарядом и мощностью было отмечено в экспериментах с циклическими полиаминами. Например, гексациклен /+6; ЭК50 = 20 μМ/ является более мощным, чем NPS 383 /+8; ЭК50 = 150 μМ/. Результаты, полученные с этими полиаминами, показывают, что положительный заряд не является единственным фактором, вносящим свой вклад в мощность.
Дополнительные исследования обеспечили понимание структурных признаков молекул, которые придают активность по отношению к Ca2+-рецептору паратироидной клетки. Одним из структурно важных признаков является внутримолекулярное расстояние между азотами (которые несут положительный заряд). Так, спермин является в 50 раз более мощным, чем триэтилентатрамин (ЭК50 = 8 мМ) при вызывании увеличения /Ca2+/в в бычьих паратироидных клетках, ходя обе молекулы несут чистый положительный заряд +4. Единственным различием в структуре между этими двумя полиаминами является количество метиленовых групп, разделяющих азоты: у спермина оно равно 3-4-3, тогда как у триэтилентатрамина оно равно 2-2-2. Это кажущееся незначительным изменение в расстояниях между азотами обеспечивает существенные различия мощности, и полагают, что конформационные соотношения между азотами внутри молекулы являются критическими. Это поддерживается результатами, полученными с гексацикленом и пентаэтиленгексамином. Первая молекула является просто циклическим аналогом последней и содержит такое же количество метиленовых групп между всеми азотами, хотя наличие циклической структуры увеличивает мощность в 25 раз. Эти результаты указывают, что сам по себе положительный заряд не является критическим фактором, определяющим активность органической молекулы по отношению к Ca2+-рецептору.
Другие серии экспериментов выявили важность ароматических групп при определении активности по отношению к Ca2+-рецептору. Результаты были получены с двумя арилалкиламинами, выделенными из яда паука Argiope lobata. Эти молекулы, аргиотоксин 636 и аргиотоксин 659, имеют идентичные поликатионные участки, соединенные с различными ароматическими группами (фиг. 24). Аргиотоксин 659 вызывает колеблющееся увеличение /Ca2+/в в бычьих паратироидных клетках при испытаниях при концентрации от 100 до 300 μМ. Напротив, аргиотоксин 636 не оказывает такого действия при испытаниях при подобных концентрациях (фиг. 24). Единственное различие в структуре между этими двумя арилалкиламинами находится в ароматической части молекулы: аргиотоксин 659 содержит 4-оксииндольный фрагмент, тогда как аргиотоксин 636 содержит 2,4-диоксифенильную группу. Чистый положительный заряд на этих двух арилалкиламинах является одинаковым /+4/, так что их различные мощности должны быть результатом различия в ароматических группах. Это показывает, что чистый положительный заряд один не определяет мощность. Однако реальной значимостью этих данных является открытие того, что ароматические группы вносят значительный вклад в способность молекул активировать Ca2+-рецептор.
Агатоксин 489 /NPS 017/ и Агатоксин 505 /NPS 015/ оба вызывают мобилизацию внутриклеточного Ca2+ в паратироидных клетках с ЭК50 6 и 22 μМ соответственно. Единственным различием в структуре этих молекул является гидроксильная группа в индольном фрагменте (фиг. 1). Это показывает, что замещения в ароматической части молекулы могут оказывать влияние на мощность. Это указывает, что должны быть изучены другие ведущие молекулы, включая молекулы, имеющие замещенные ароматические фрагменты.
Структурные признаки, систематически варьируемые в ведущих молекулах, описанных здесь, включают (1) чистый положительный заряд, (2) количество метиленовых групп, разделяющих азоты, и (3) циклические варианты, например, полиаминов с и без изменений расстояний за счет метиленовых групп и чистого положительного заряда. В дополнение к систематическим вариациям структуры может быть исследовано место расположения ароматических групп, например, в различных арилалкиламинах, выделенных из ядов ос и пауков, и могут быть получены синтетические молекулы путем сочетания коммерчески доступных ароматических фрагментов с аргиотоксинным полиаминым фрагментом. Аргиотоксинный полиаминный фрагмент можно легко просочетать с любым ароматическим фрагментом, содержащим карбоновую кислоту. Следовательно, просто подвергнуть скринингу гидроксильные и метоксипроизводные фенилуксусной кислоты и бензойной кислоты, а также серий оксииндолуксусной кислоты. Также могут быть получены аналоги, содержащие гетероароматические функциональности и оценена их активность.
Сравнение мощности и эффективности среди таких молекул выявит оптимальную структуру и место расположения ароматической группы при постоянном положительном заряде.
Одна из структурных вариаций полиаминового фрагмента, который возможно повышает мощность, представляет собой циклическую версию родственной молекулы с прямой цепью. Будмунхиамин A, выделенный из растения Albizia amara, представляет собой циклическое производное спермина (фиг. 1). Добавление будмунхиамина A к бычьим паратироидным клеткам вызывает быстрое и кратковременное увеличение /Ca2+/в, которое существует в отсутствие внеклеточного Ca2+ и притупляется предварительной обработкой ФМА. Следовательно, он вызывает мобилизацию внутриклеточного Ca2+ в паратироидных клетках, возможно воздействуя на Ca2+-рецептор. Он является равномощным со спермином /ЭК50 около 200 μМ/, хотя несет на один положительный заряд меньше /+3/, чем спермин.
Результаты, полученные с будмунхиамином A, показывают предсказуемую важность исследований структура - активность, и нужно получить новую структурную информацию при испытаниях природных продуктов. Так, легко осуществляется скрининг природных продуктов, рационально отобранных на основании структурной информации, например молекулы могут быть отобраны на основании хорошо установленных хемотаксономических принципов с использованием оснований с соответствующими данными, таких как Напралерт (Napralert). Например, макроциклические полиаминные алкалоиды, происходящие из мотыльковых бобовых культур, относящихся к Albizia, таких как Pithocolobium, и другие происходящие из растений молекулы могут быть подвергнуты скринингу.
На фиг. 36 представлен второй пример из серии молекул, которые были подвергнуты скринингу для определения полезных молекул настоящего изобретения. Эти молекулы обычно происходят из фендилина и испытаны для определения их соответствующих ЭК50. Кроме того, испытания родственных молекул, таких как NPS 447 и NPS 448, показали стереоспецифические эффекты молекулярной структуры. Наиболее активные соединения, испытанные до настоящего времени, являются новыми соединениями, обозначенными NPS 467 и NPS 568, которые имеют величины ЭК50 менее 5 μМ. На данном уровне техники при рассмотрении этих серий молекул могут быть определены другие подходящие производные, которые могут быть испытаны в изобретении.
Эти примеры показывают общую схему и процесс скрининга, полезные в настоящем изобретении, и указывают, что банки дополнительных соединений и природных продуктов могут быть скринированы, как желательно для специалистов в данной области, чтобы определить другие полезные ведущие молекулы или новые молекулы настоящего изобретения.
Как обсуждалось выше, примеры молекул, полезных в качестве кальцимиметиков, включают разветвленные или циклические полиамины, положительно заряженные полиаминокислоты и арилалкиламины. Кроме того, другие положительно заряженные органические молекулы, включая молекулы природного происхождения и их аналоги, являются полезными кальциметиками. Эти молекулы природного происхождения и их аналоги предпочтительно имеют такое соотношение заряда к массе, которое коррелирует с этими соотношениями для приведенных здесь в качестве примеров молекул. (Примеры включают материалы, выделенные из морских видов, ядов членистоногих, наземных растений и ферментационных бульонов, происходящих из бактерий и грибов). Предполагается, что одна группа предпочтительных молекул природного происхождения и полезных аналогов в качестве кальцимиметиков будет иметь отношение положительный заряд : молекулярная масса (в дальтонах) от примерно 1:40 до 1:200, предпочтительно от примерно 1: 40 до 1:100. Более определенные примеры таких молекул приведены ниже.
Полиамины
Полиамины, полезные как кальцимиметики в настоящем изобретении, могут быть разветвленными или циклическими. Разветвленные или циклические полиамины потенциально обладают более высокой кальцимиметической активностью, чем их аналоги с прямой цепью. То есть разветвленные или циклические полиамины обычно обладают более низкой ЭК50, чем соответствующие линейные полиамины с таким же эффективным зарядом при физиологическом pH (см. табл. 1).
"Разветвленные полиамины", как использовано здесь, означают цепную молекулу, состоящую из коротких алкильных мостиков или алкильных групп, соединенных вместе аминными связями, и также содержащую точки, в которых цепь разветвляется. Эти "точки разветвления" могут быть локализованы или у атома углерода, или у атома азота. Точка разветвления у атома азота представляет собой обычно третичный амин, но он также может быть четвертичным. Разветвленный полиамин может иметь 1-20 точек разветвления, предпочтительно 1-10 точек разветвления.
Обычно алкильные мостики и алкильные разветвления в разветвленных полиаминах содержат 1-50 атомов углерода в длину, предпочтительно 2-6 атомов углерода. Алкильные разветвления также могут быть прерваны одним или более гетероатомами (азотом, кислородом или серой) или замещены функциональными группами, такими как галоид, включая фтор, хлор, бром или йод, гидроксилонитро, ацилокси (R'COO-), ациламидо (R'CONH-), или алкокси (-OR'), где R' может содержать 1-4 атома углерода. Алкильные разветвления также могут быть замещены группами, которые положительно заряжены при физиологическом pH, такими как амино или гуанидо. Эти функциональные заместители могут добавлять или изменять физические свойства, такие как растворимость для повышения активности, выделение или биодоступность молекулы.
Разветвленные полиамины могут иметь три или более цепей и точек концевых разветвлений. Эти концевые точки могут быть метильными группами или аминогруппами, предпочтительно аминогруппами.
Одна предпочтительная группа молекул представляет собой группу разветвленных полиаминов, имеющих формулу
H2N -/CH2/j -/NRi -/CH2/j /k - NH2
где k является целым числом от 1 до 10, каждый j является одинаковым или различным и является целым числом от 2 до 20, и каждый Ri является одинаковым или различным и выбран в группе, состоящей из водорода и /CH2/j - NH2, где j имеет указанные ранее значения, и по крайней мере один Ri не является водородом.
Особенно предпочтительными разветвленными полиаминами настоящего изобретения являются молекулы N1, N1, N5, N10, N14, N14-гексакис-/3-аминопропил/спермина и N1, N1, N5, N14, N14-тетракис-/3-аминопропил/спермина, упоминаемые как NPS 381 и NPS 382 соответственно на фиг. 1.
"Циклические полиамины", как использовано здесь, относятся к гетероциклам, содержащим два или более гетероатома (азота, кислорода или серы), по крайней мере два из которых являются атомами азота. Гетероциклы обычно имеют от примерно 6 до примерно 20 атомов в цикле, предпочтительно от примерно 10 до примерно 18 атомов в цикле. Гетероатомы азота разделены 2-10 атомами углерода. Гетероциклы также могут быть замещены у азотных центров аминоалкильными или аминоарильными группами /NH2-R-/, где R является аминоарилом или низшим алкилом с 2-6 атомами углерода.
Особенно предпочтительные циклические полиамины настоящего изобретения показаны на фиг. 1 в виде гексациклена /1,4,7,10,13,16-гексаазациклооктадекана/ и NPS 383.
Полиаминокислоты
Полиаминокислоты, полезные в настоящем изобретении, могут содержать два или более положительно заряженных аминокислотных остатка при физиологическом pH. Эти положительно заряженные аминокислоты включают гистидин, лизин и аргинин. Эти полипептиды будут варьировать по длине от 2 до 800 аминокислот в длину, предпочтительно от 20 до 300 аминокислот в длину. Эти полипептиды могут состоять из единственного повторяющегося аминокислотного остатка или могут иметь различные белки природного происхождения или ферменты.
Аминокислотные остатки, составляющие полиаминокислоты, могут быть любыми из двадцати встречающихся в природе аминокислот, или другими альтернативными остатками. Альтернативные остатки включают, например, позиции настоящего изобретения и также могут содержать компоненты, происходящие из молекулы или иона, которые действуют как метка. Может быть использовано большое разнообразие метящих фрагментов, включая радиоизотопы, хромофоры и флуоресцентные метки. Радиоизотопная метка особенно легко детектируется in vivo. Радиоизотопы могут быть введены координацией в виде катионов в порфириновую систему. Полезные катионы включают технеций и индий. В композициях положительно заряженная молекула может быть связана или ассоциирована с меткой.
Способы синтеза
Стратегии синтеза и модификация полиаминов включают использование различных групп, защищающих аминогруппу (фталимидо, BOC, CBZ, бензил и нитрил), которые могут быть селективно удалены для конструирования функционализированной молекулы. Включенные способы синтеза являются модельными, после того как их использовали для конструирования аргиопинов 636 и 659 и других арилалкиламино, происходящих из ядов пауков.
Протяженность цепи из 2-4 метиленовых групп обычно создается путем алкилирования соответствующим N-/бромалкил/фталимидом. Смесь 1:1,2 амина и бромалкилфталимида кипятят с обратным холодильником в ацетонитриле в присутствии 50% KF на Целите. Удлинение цепи также осуществляют путем алкилирования заданного амина акрилонитрилом или этилакрилатом. За ходом реакции следят с помощью ТСХ и очищают промежуточные продукты на силикагеле, используя сочетания дихлорметана, метанола и изопропиламина. Конечные продукты очищают катионным обменом /HEMA-SB// и ВЭЖХ-ОФ /Видак C-18/. Чистоту и структуру подтверждают с помощью 1H- и 13C-ЯМР и масс-спектрометрией высокого разрешения /EI, CI и/или FAB/.
BOC-защищающие группы вводят при обработке амина /1oC или 2o/ дитрет-бутилдикарбонатом в дихлорметане в присутствии каталитического количества диметиламинопиридина. Бензильные защищающие группы вводят одним из двух путей: /1/ конденсацией 1o амина с бензальдегидом с последующим восстановлением боргидридом натрия или /2/ алкилированием 2o амина бензилбромидом в присутствии KF. Амидные связки и циклизации обычно осуществляют при реакции амина (1o или 2o) со сложным эфиром N-оксисукцинимида данной кислоты. Это осуществляется непосредственно (в случае циклизаций) при обработке "аминокислоты" дициклогексилкарбодиимидом в разбавленных условиях.
Снятие защиты фталимидной функциональностью осуществляют восстановлением гидразином при кипячении с обратным холодильником в метаноле. Снятие защиты BOC-функциональностью осуществляют в безводной ТФУК. Снятие защиты бензильной, нитрильной и CBZ-функциональностями осуществляют путем восстановления в ледяной уксусной кислоте под давлением водорода 55 фунт/дюйм2 (= 3,867 кг/см2) в присутствии каталитического количества гидроксида палладия на угле. Нитрильные функциональности (в присутствии бензильных и CBZ групп) селективно восстанавливаются водородом в присутствии губчатого никеля Ренея.
Специально разветвленные полиамины обычно получают из простых диаминоалканов формулы NH2-/CH2/n - NH2, или простых полиаминов, таких как спермидин или спермин. Один из двух первичных (концевых) аминов защищают или "маскируют" защищающей группой, такой как BOC /трет-бутилоксикарбонил/, фталимидо, бензил, 2-этилнитрил /продукт реакции конденсации Михаэля амина и акрилонитрила/, или амид. Типичная реакция заключается в присоединении BOC-защищающей группы при обработке ди-трет-бутилдикарбонатом (BOC-ангидридом)
Монозащищенный продукт отделяют от незащищенного и дизащищенного продуктов с помощью простой хроматографической методики или дистилляцией.
Оставшийся свободный амин в монозащищенном продукте затем селективно алкилируют (или ацилируют) алкилирующим (или ацилирующим) агентом. Для обеспечения моноалкилирования свободный амин частично защищают конденсацией с бензальдегидом с последующим восстановлением боргидридом натрия с образованием N-бензильного производного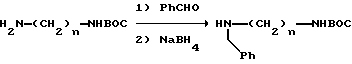
N-Бензильное производное затем вводят в реакцию с алкилирующим агентом. Типичным алкилирующим агентом является N-/бромалкил/фталимид, который реагирует следующим образом:
Например, используют N-/бромбутил/фталимид для удлинения или разветвления цепи на четыре метиленовые группы. Альтернативно, реакция с акрилонитрилом с последующим восстановлением цианогруппы будет удлинять цепь на три метиленовые группы и аминогруппу.
Защищающие группы на полученной в результате молекуле с удлиненной цепью затем могут быть селективно отщеплены с получением нового свободного амина. Например, используют трифторуксусную кислоту для удаления BOC-группы, каталитическое гидрирование используют для восстановления нитрильной функциональности и удаления бензильной группы, а гидразин используют для удаления фталимидных групп следующим образом: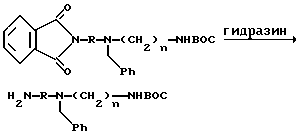
Новый свободный амин может быть алкилирован (или ацилирован) затем, как указано выше, для увеличения длины полиамина. Этот процесс повторяют до тех пор, пока не получат желаемую длину цепи и количество разветвлений. На конечной стадии снятие защиты с продукта приводит в результате к желаемому полиамину. Однако могут быть проведены дополнительные модификации на защищенном конце перед снятием защиты следующим образом.
Например, перед BOC-защиты полиамин ацилируют сложным эфиром П-оксисукцинимида и 3,4-диметоксифенилуксусной кислоты с получением дизащищенного полиамина
Это приводит в результате к получению арилалкилполиамина. Затем селективно удаляют BOC-группы с помощью трифторуксусной кислоты, чтобы открыть другой аминоконец, который может быть удлинен, как описано выше.
Некоторые разветвленные полиамины могут быть получены путем одновременного алкилирования или ацилирования свободных первичных и вторичных аминов в полиамине, полученном, как выше. Например, обработка спермина избытком акрилонитрила с последующим каталитическим восстановлением приводит к следующему: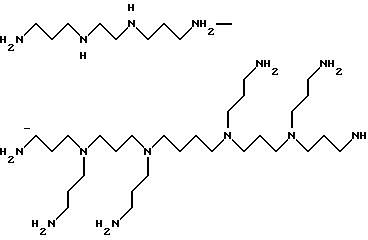
Циклические амины могут быть получены, как выше, начиная с таких исходных материалов, как гексацилен (Aldrich Chem.).
Полиаминокислоты, входящие в область настоящего изобретения, могут быть получены рекомбинантными методиками, известными на данном уровне техники, или могут быть синтезированы с использованием стандартных твердофазных методик, известных на данном уровне техники. Твердофазный синтез начинают с карбоксильного конца пептида, используя μ-аминозащищенную аминокислоту. Могут быть использованы BOC-защищающие группы для всех аминогрупп, даже если пригодны другие защищающие группы. Например, BOC-lys-OH может быть этерифицирован на подложке из хлорметилированной полистирольной смолы. Подложка из полистирольной смолы предпочтительно представляет собой сополимер стирола с примерно 0,5-2% дивинилбензола в качестве сшивающего агента, который делает полистирольный полимер полностью нерастворимым в некоторых органических растворителях. Смотри Stewart et al., Solid-Phase Peptide Synthesis /1969/, W. H. Freeman Co., San Francisco; и Merrifield J. Am. Chem. Soc. /1963/ 85: 2419-2154. Эти и другие методы пептидного синтеза также подтверждаются примерами в патентах США NN 3862925, 3842067, 3972859 и 4105602.
Пептидный синтез может использовать ручные методики или быть осуществлен автоматически с использованием, например, Applied Biosystems 403A Peptide Synthesizer /Foster City, California/ или Biosearch SAM II автоматический пептидный синтезатор /Biosearch, Inc., San Rafael, California/, следуя инструкциям, приведенным в инструктивном руководстве, прилагаемом производителем.
Арилалкиламины являются природными продуктами, выделенными по известным методикам, или синтезированы, как описано Jasys et al., Tetrahedrom Lett. /1988/, 29: 6223-6226, и Nason et al., Tetrahedron Lett. /1989/ 30: 2337-2340.
Один общий протокол получения фендилина /или аналогов фендилина, показанных на фиг. 36/ является следующим. В круглодонной колбе емкостью 10 мл, снабженной стержневой магнитной мешалкой и каучуковой перегородкой, обрабатывают 1,0 ммоль 3,3'-бисфенилпропиламина (или первичного алкиламина) в 2 мл этанола 1,1 ммоль фенола и 1,0 ммоль ацетофенола /или замещенного ацетофенона/. Туда прибавляют 2,0 ммоль MgSO4 и 1,0 ммоль NaCHBH3. Смесь перемешивают в атмосфере азота при комнатной температуре /около 20oC/ в течение 24 часов. Реакционную смесь выливают в 50 мл эфира и 3 раза промывают 1 N NaOH и один раз рассолом. Эфирный слой сушат над безводным K2CO3 и разгоняют в вакууме. Затем продукт очищают хроматографией на колонке или ВЭЖХ, содержащей стационарную фазу из оксида кремния с сочетаниями CH2Cl2-метанол-изопропиламин /обычно 3% метанола и 0,1% изопропиламина в метиленхлориде/.
В предпочтительной процедуре получения фендилина или аналогов фендилина (таких как представлены на фиг. 36) используют изопропоксид титана /IV/ и она была модифицирована исходя из методов, описанных в J. Org. Chem. 55: 2552 /1990/. Для синтеза NPS 544 был использован тетрахлорид титана /способ описан в Tetrahedron Letters 31: 5547 /1990// вместе изопропоксида титана /IV/. Реакционная схема представлена на фиг. 43а. На фиг. 43а R, R' и R'' означают углеводородные группы. В соответствии с одним вариантом в колбе емкостью 4 мл смешивают 1 ммоль амина /1// обычно первичного амина/ и 1 ммоль кетона или альдегида /2/ /обычно ацетофенона/, затем обрабатывают 1,25 ммоль изопропоксида титана /IV/ /3/ и оставляют при перемешивании при комнатной температуре на 30 минут. Альтернативно может быть использован вторичный амин вместо /1/. Некоторые реакции будут давать тяжелые осадки или твердые продукты, которые подогревают/нагревают (до их точки плавления), чтобы обеспечить перемешивание/смешивание в течение некоторого времени во время реакции. Реакционную смесь обрабатывают 1 мл этанола, содержащего 1 ммоль цианборгидрида натрия /4/ и полученную смесь затем оставляют при комнатной температуре при перемешивании время от времени на 16 часов. После этого времени реакцию закаливают, добавляя примерно 500 мкл воды. Потом реакционную смесь разбавляют примерно 4 мл в сумме этилового эфира и затем центрифугируют. Удаляют верхнюю органическую фазу и выпаривают на роторном испарителе. Полученный продукт /6/ частично очищают хроматографией на короткой колонке с силикагелем /или альтернативно, используя препаративную ТСХ на оксиде кремния/, используя сочетание дихлорметан:метанол:изопропиламин /обычно 95: 5: 0,1/, перед очисткой с помощью ВЭЖХ /нормальная фаза с использованием оксида кремния с дихлорметаном:метанолом:изопропиламином или обращенная фаза, C-18 с 0,1% ТФУК с ацетонитрилом или метанолом/.
Если подходит или желательно, может быть проведено хиральное разделение с использованием таких методов, как описано в примере 21.
Рецептура и введение
Как показано здесь, молекулы изобретения могут быть использованы для:
а) имитации или антагонизма одного или более эффектов внеклеточного иона, включая внеклеточный Ca2+;
б) влияния на уровень свободного внеклеточного Ca2+ у индивидуума; и
в) лечения таких заболеваний, как гиперпаратироидизм, остеопороз и гипертония.
Обычно заболевания или состояния, включающие рецептор неорганического иона, теперь могут быть изучены, диагностированы и/или благоприятно пролечены. Хотя в общем было показано, что молекулы оказывают действие на паратироидные клетки, они также могут модулировать Ca2+-рецепторы на других клетках, включая костные остеокласты, окологломерулярные почечные клетки, проксимальные почечные канальцевые клетки, периферические канальцевые почечные клетки, клетки толстой восходящей ветви петли Хенля и/или собирающей протоки, кератиноцит в эпидермисе, парафолликулярные клетки в тироиде /C-клетки/, интестинальные клетки, трофобласт в плаценте, тромбоцит, васкулярную клетку гладкой мышцы, клетки сердечного предсердия, клетки, секретирующие гастрин и глюкагон, почечную мезангиальную клетку и клетку грудной железы.
Хотя эти молекулы обычно используют при лечении людей, они могут быть использованы для лечения подобных и идентичных заболеваний у других теплокровных животных, таких как другие приматы, сельскохозяйственные животные, такие как свиньи, коровы и птица; и спортивных животных и домашних животных, таких как лошади, собаки и кошки.
При терапевтических и/или диагностических применениях молекулы изобретения могут быть сформулированы для различных способов введения, включая системное и местное или локализованное введение. Методики и рецептуры в общем могут быть найдены в Remington's Pharmaceutical Science, Mack Publishing Co. Истон, ПА.
Для системного введения предпочтительным является оральное введение. Альтернативно может быть использована инъекция, например внутримышечная, внутривенная, интраперитонеальная и подкожная. Для инъекции молекулы изобретения формулируют в жидкие растворы, предпочтительно в физиологически совместимые буферы, такие как раствор Хенка или раствор Рингера. Кроме того, молекулы могут быть сформулированы в твердой форме и повторно растворены или суспендированы непосредственно перед использованием. Также включены лиофилизированные формы.
Системное введение также может быть через слизистую или через кожу, или молекулы могут быть введены орально. Для введения через слизистую или через кожу в рецептуре используют подходящие пенетранты, позволяющие перейти барьер. Такие пенетранты в общем известны на данном уровне техники и включают, например, для введения через слизистую желчные соли и производные фусидовой кислоты. Кроме того, могут быть использованы детергенты для облегчения проникновения. Введение через слизистую может быть осуществлено через аэрозоли для носа, например, или с использованием суппозиториев. Для орального введения молекулу формулируют в традиционные для орального введения формы, такие как капсулы, таблетки и тоники.
Для местного введения молекулы изобретения формулируют в виде мазей, бальзамов, гелей или кремов, как это является обычным на данном уровне техники.
Как показано в примерах ниже, количества различных соединений настоящего изобретения, которые должны быть введены, могут быть определены по стандартным методикам. Обычно это количество находится между 1 и 50 мг/кг животного, подлежащего лечению.
Рекомбинантные рецепторы
Скринирование природных продуктов традиционно обеспечивает ведущие структуры для разработки различных терапевтических молекул. Однако скринирование большого количества исходного материала из банков природных молекул или банков других молекул на активность по отношению к Ca2+-рецептору ранее было невозможно. Для достижения этой способности лучше всего клонировать кДНК Ca2+-рецептора, а затем создать трансфецированные клеточные линии, пригодные для скрининга с большим количеством исходного материала. Структура рецептора может быть дополнительно использована, чтобы понять молекулярную геометрию центров связывания лигандов, и такую информацию используют для улучшения рациональной программы конструирования лекарства, как обсуждалось выше. Ограниченные исследования структура - активность и испытания выбранных молекул природных продуктов обеспечит основные исходные структурные данные, необходимые для направления рациального скрининга природных продуктов и конструкции лекарства.
Открытие суперсемейства генов дает такие же преимущества в отношении всех рецепторов неорганических ионов. Хотя последующее описание часто будет относиться к методологии клонирования кальциевого рецептора, специалисту в данной области должно быть понятно, что методология в общем применима к клонированию всех рецепторов неорганических ионов.
Эти рекомбинантные рецепторы позволяют сначала скринировать миметики и литики, включая кальцимиметики и кальцилитики. Например, путем анализа связывания с рецепторами. Это является особенно полезным при скрининге человеческих рецепторов для идентификации терапевтически полезных соединений.
кДНК Ca2+-рецептора бычьей и человеческой паратироидной клетки может быть клонирована путем функциональной экспрессии в Xenopus ооциты. Это дает возможность контролировать увеличение внутриклеточного Ca2+ в Xenopus ооцитах косвенно путем измерения потока через эндогенны Ca2+-активированный Cl--канал. Амплификация ответа, вызванного этим сигнальным трансдукционным путем, дает возможность детекции рецепторных белков, кодируемых мРНК при очень низких уровнях. Это позволяет детектировать рецептор-специфические клоны кДНК без необходимости высокого сродства лигандов, специфической антисыворотки или информации с последовательности белка или нуклеиновой кислоты. Пример такой процедуры приводится ниже.
Получают взрослых самок Xenopus laevis из Xenopus I /Ann Arbor, MI/ и выдерживают в соответствии со стандартными процедурами. Вырезают доли яичника у гипертермически анестезированных лягушек. Кластеры ооцитов переносят в модифицированный солевой раствор Барта (МБС). Индивидуальные ооциты получают при инкубации в МБС, содержащем 2 мг/мл коллагеназы /Сигма, тип 1A/, в течение 2 часов при 21oC и отбирают для инъекции ооциты V-VI стадии.
Стеклянные капиллярные трубки /диаметр 1 мм/ вытягивают до тонкого конца и вручную обламывают, чтобы получить диаметр кончика около 15 μм. Каплю мРНК /1 нг/нл/ в воде, обработанной диэтилпирокарбонатом /ДЭПК/ помещают в парафилм и всасывают в капиллярную трубку. Затем капиллярную трубку соединяют с пикоспиртцером /WPI, Instruments/ и устанавливают объем воздушно-пульсируемых капелек, чтобы выводить 50 нг мРНК /обычно 50 нл/. Используют 35-миллиметровые культуральные чашки с нейлоновой прокладкой, закрепленной на дне, чтобы закрепить ооциты во время инъекции мРНК в вегетативный полюс. Инъецированные ооциты помещают в 35-миллиметровую культуральную чашку, содержащую МБС, 100 μг/мл пенициллина и 100 μг/мл стрептомицина и инкубируют при 18oC в течение 3 дней.
После инкубации ооцит помещают в пластиковую камеру емкостью 100 мкл и подвергают суперслиянию с МБС при скорости потока 0,5 мл/мин, используя перистальтический насос. Добавляют испытуемые молекулы или неорганические поликатионы быстрым движением пробирки в различных буферах. Регистрирующие и пропускающие ток электроды были сконструированы из тонкой стенки капиллярной трубки, оттянутой до сопротивления 1-3 МОм и заполненной 3 М KCl. Ооциты были проколоты /с анимального полюса/ двумя электродами при наблюдении под микроскопом и присоединены к Axon Istruments Axoclamp 2A вольт-кламп усилителю, который используют для установления холдинг-потенциала /-70 до -80 мВ/ и для измерения токов, которые пропускают для поддержания холдинг-потенциала. Токи регистрируют непосредственно на ленточном самописце.
Для приготовления мРНК получают ткань от детенышей или пациентов со вторичным ГПТ, подвергнувшихся хирургическому удалению паратироидных желез. Нет необходимости готовить очищенные клетки; используют целые кусочки железы, чтобы приготовить мРНК, которая направляет экспрессию Ca2+-рецептора в Xenopus ооцитах. Суммарную клеточную РНК готовят путем экстракции кислым гуанидинийтиоцианатом/фенолом гомогенизированных желез. Используют олиго-dT целлюлозную хроматографию для отбора поли/A/+ мРНК по стандартным процедурам. Для фракционирования по размерам используют центрифугирование с градиентами глицерина. Денатурируют мРНК 20 мМ метилгидроксида ртути и нагружают /50-100 μг при концентрации 1 мг/мл/ в линейном 15-30% градиенте глицерина, приготовленном в пробирках Бекман TLS55. После центрифугирования при 34000 об/мин в течение 16 часов собирают градиентные фракции 0,3 мл и разбавляют равным объемом воды, содержащей 5 мМ бета-меркаптоэтанола. Затем извлекают мРНК двумя циклами осаждения этанолом. При желании мРНК /50-100 μг поли/A/+/ может быть отделена на препаративном геле 1,2% агарозы/6,0 М мочевины вместе с интервалом маркеров РНК по размерам. После визуализации мРНК окрашиванием этидиний бромидом вырезают пластинки геля, содержащие РНК со ступенями по размеру 1-2 kb. мРНК извлекают из пластин агарозного геля, используя матрицу связывания РНК /согласно стандартному протоколу поставщика, Strategene, Inc./, и фракции извлеченной мРНК элюируют обработанной ДЭПК водой.
Количества извлеченной мРНК оценивают измерением поглощения УФ. Интервал размеров мРНК, содержащейся в каждой фракции глицеринового градиента, определяют электрофорезом на формальдегид/агарозном геле, используя малое количество /0,5 μг/ каждого образца. Целостность мРНК оценивали in vitro трансляцией каждого образца. Используют лизаты ретикулоцита /коммерчески доступные наборы, БРЛ/ для трансляции 0,05-0,5 μг каждой фракции мРНК. Полученные в результате 35S-меченые белки анализируют SDS-ПАГЭ. Интактная мРНК способна направить синтез белков полного интервала размеров, грубо соответствующих размерам индивидуальных фракций мРНК.
Конструируют библиотеку кДНК в векторе λZAPII, следуя модификациям техники Гублера и Хоффмана. В качестве исходного материала используют РНК из фракции/й/, дающих наилучший ответ при анализе ооцита. Синтезы однониточной кДНК примировали олиго-dT/NotI праймер-линкером. Синтез второй нити был осуществлен методом аутопримирования RNase H/ДНК полимеразой 1. Двуниточная кДНК была дефосфолирована T4 ДНК полимеразой и EcoRI адапторы лигируют тупым концом к кДНК T4 лигазой. После NotI переваривание для отщепления линкера отбирают по размерам кДНК полной длины путем эксклюзивной хроматографии на Сефакрил 500 НА. Первая нить кДНК была радиомеченой α-32P-dАТФ и весь синтез и стадии извлечения контролируют по последующему включению радиоактивности, кДНК полной длины, извлеченную из колонки, разделяющей по размерам, лигируют к переваренным EcoRI/NotI λZAPPI дугам. Лигированную смесь подвергают тест-заполнению с коммерчески доступным высокоэффективным заполняющим экстрактом /Strategene, Inc. / и высевают на соответствующий штамм-хозяин /XLI-голубой/. Определяют процент рекомбинантного фага по соотношению белого к голубому бляшек при высеве библиотеки на IPTG и X-gal.
Определяют средний размер вставки из десяти произвольно выбранных клонов. Фаговую ДНК "мини-препс" переваривали EcoRI и NotI для выделения вставки, и определяют размер электрофорезом на агарозном геле. Библиотека состоит из > 90% рекомбинантного фага и размер вставки колеблется от 1,5 до 4,2 kb. Лигированный рекомбинант упаковывали в большом масштабе, чтобы генерировать 800000 праймерных клонов. Оттитровывают упакованную смесь и высевают по 50000 бляшек на пластину 15 см. Элюируют каждый пул из 50000 клонов СМ буфером и хранят индивидуально.
Используют исходный лизат с пластины каждого из пулов клона для маломасштабного приготовления фага ДНК. Частицы фага концентрируют осаждением полиэтиленгликолем и очищают фаг ДНК перевариванием протеиназой K с последующей экстракцией фенолом:хлороформом. Переваривают 20 мкг ДНК NotI и используют в качестве матрицы для in vitro транскриции смысловой нити РНК. In vitro транскрипцию осуществляют по стандартным протоколам, используя T7 РНК полимеразу и 5'-кэп аналог m7GpppG в 50 μл общего реакционного объема. После ДНКаза 1/протеиназа K переваривания и экстракции фенолом/хлороформом концентрируют РНК осаждением этанолом и используют для инъекции ооцитов.
Инъецируют ооциты синтетической мРНК /кРНК/ из каждого из 16 субпулов библиотеки, содержащего 50000 независимых клонов каждый. После инкубации в течение 3-4 дней анализируют ооциты по способности 10 μМ неомицина вызывать Ca2+-зависимый Cl--поток. Пул, обозначенный "пул 6", дал положительный сигнал и, следовательно, содержит клон кДНК, кодирующий функциональный кальциевый рецептор. Для того чтобы уменьшить вариабельность пула 6 и, следовательно, продолжить очистку клона кальциевого рецептора, содержащегося в этом пуле, фаг пула 6 пересевают при μ 20000 бляшек на пластину и собирают урожай с 12 пластин. Готовят ДНК из каждого из этих субпулов и синтезируют кРНК. Снова инъецируют ооциты кРНК и анализируют через 3-4 дня по способности 10 μМ неомицина вызывать Ca2+-зависимый Cl--поток. Субпул пула 6-3 является положительным и этот пул подвергают дополнительному циклу посева, снижая вариабельности пула до примерно 5000 клонов на пул. Снова анализируют пулы путем приготовления кРНК и инъекции в ооциты. Субпул пулы 6-3.4 является положительным. Для ускорения дальнейшей очистки положительного клона в пуле 6-3.4 фаг ДНК из этого пула высвобождают в виде плазмиды ДНК путем суперинфекции хелперным фагом, ExAssist (Strategene). Трансфекция высвобожденных плазмид в бактериальный штамм DH5alphaF' приводит в результате к трансформированным бактериальным колониям на ампициллиновых пластинах. Они были собраны в пул из 900 клонов каждый. Затем получают плазмиду ДНК из каждого субпула и синтезируют кРНК и анализируют ее обычным образом. Субпул 6-3.4.4 является положительным. Бактерии, содержащие плазмиду субпула 6-3.4.4, последовательно высевают в субпулы по μ 50 клонов в каждом. Продолжение этого процесса, как ожидается, приведет в результате к единственному клону, кодирующему функциональный кальциевый рецептор.
Имеется альтернативный анализ для определения экспрессии кальциевого рецептора в ооцитах. Например, ооциты могут быть нагружены 45Ca++ и затем обработаны кальцимиметиком. Мобилизация 45Ca++ из внутриклеточных пулов приводит в результате к четкому увеличению оттока 45Ca++, который легко определить. Флуоресцентные Ca++-индикаторы также могут быть инъецированы в ооциты. В
этом случае ооциты, экспрессирующие кальциевый рецептор, будут показывать повышенную флуоресценцию при активации кальцимиметиком. Эти анализы могут быть применены для клонирования кальциевых рецепторов вместо электрофизиологического анализа индуцированного кальцием Cl--потока, описанного в примере выше. В дополнение к этому, кальцимиметический лиганд, использованный в процедуре клонирования, не требует неомицина, как указывалось выше, но вместо этого могут быть, например, Gd+++, Ca++, Mg++ или другое кальцимиметическое соединение.
В начальных экспериментах использовали Xenopus ооциты, инъецированные водой или поли/A/+-обогащенной мРНК /50 нг/ из бычьих паратироидных клеток. Через 3 дня исследовали ооциты на их способность повышать внутриклеточный Ca++ в ответ на увеличение концентрации внеклеточных двух- и трехвалентных катионов. Ооциты прокалывали регистрирующими и пропускающими ток электродами и оценивали /Ca2+/в косвенно путем измерения токов через эндогенный Ca2+-активированный Cl--канал. В ооцитах, инъецированных поли/A/+-обогащенной мРНК из бычьих (или человеческих, фиг. 26) паратироидных клеток, повышение концентрации внеклеточного Ca2+ от 0,7 до 3, 5 или 10 мМ вызывает быстрое и кратковременное увеличение Cl--потока, которое затем колеблется около более высокого основного потока. Увеличение концентрации внеклеточного Mg2+ от 1 до 10 мМ подобным образом вызывает колеблющееся повышение Cl--потока. Ответ Cl--потока на внеклеточный Mg2+ существует при снижении концентрации внеклеточного Ca2+ до < 1 μМ (фиг. 25).
Непроникающий трехвалентный катион Gd /600 μМ/ также вызывает колеблющееся повышение Cl--потока (фиг. 25). Такое повышение Cl--потока, которое колеблется и существует при номинальном отсутствии внеклеточного Ca2+, отмечается, когда ооциты имели возможность экспрессировать другие Ca2+-мобилизирующие рецепторы и были стимулированы соответствующими лигандами (например, веществом K, фиг. 25). В этих случаях увеличение Cl--потока отражает мобилизацию внутриклеточного Ca2+. Эти начальные исследования подобным образом показали, что внеклеточные катионы мобилизуют внутриклеточный Ca2+ в ооцитах, инъецированных мРНК паратироидных клеток.
Ооциты, инъецированные водой, не показывают какого-либо изменения Cl--потока при экспозиции внеклеточным Ca2+ /10 мМ/ или Mg2+ /20 или 30 мМ/. В одной серии экспериментов ооциты были инъецированы мРНК, кодирующей рецептор вещества K. В этих ооцитах внеклеточный Mg2+ /20 мМ/ не вызывает какого-либо потока, но клетки энергично отвечали на добавление вещества K (фиг. 25). Эти эксперименты показывают, что не имеется эндогенной чувствительности ооцита на внеклеточный Ca2+ или Mg2+.
Подобные эксперименты были проведены с использованием ооцитов, инъецированных поли/A/+-обогащенной мРНК, полученной из человеческих паратироидных желез (гиперпластичная ткань из случая вторичного ГПТ). В этих ооцитах увеличение концентрации внеклеточного Ca2+ вызывает обратимое повышение Cl--потока, которое колеблется (фиг. 26). Подобным образом добавление 300 μМ La3+ вызывает колеблющееся повышение Cl--потока. Повышение концентрации внеклеточного Mg2+ от 1 до 10 мМ вызывает увеличение Cl--потока, которое существует в отсутствие внеклеточного Ca2+. Дополнительные эксперименты подтверждают, что ответ на внеклеточный Ca2+ является зависящим от концентрации. Так, в трех инъецированных мРНК ооцитах Cl--поток увеличивался до максимального 111±22 нА при 3 мМ и 233±101 нА при 10 мМ внеклеточного Ca2+.
Результаты, полученные с Xenopus ооцитами, показывают наличие мРНК в паратироидных клетках, кодирующей/их/ белок/и/, которые могут придавать обычно нечувствительным клеткам чувствительность к внеклеточному Ca2+. Кроме того, способность внеклеточного Mg2+ вызывать колеблющиеся повышения Cl--потока в отсутствие внеклеточного Ca2+ показывает, что Cl--поток зависит от мобилизации внутриклеточного Ca2+, а не от притока внеклеточного Ca2+. Результаты, полученные с La3+, подобным образом показывают, что экспрессированный белок/и/ связан с мобилизацией внутриклеточного Ca2+. Вместе эти данные показывают, что экспрессированный белок/и/ действует как рецептор поверхности клетки, а не канал. Эти исследования дают неоспоримое доказательство существования Ca2+-рецепторного белка на поверхности паратироидных клеток и показывают возможность использования системы Xenopus ооцитов для осуществления молекулярного клонирования Ca2+-рецепторной кДНК.
В других сериях экспериментов мРНК паратироидной клетки была фракционирована по размерам центрифугированием в градиенте глицерина. Собирали 10 фракций. Каждую группу инъецировали в Xenopus ооциты и после 3 дней инкубационного периода ооциты анализировали на экспрессию Ca2+-рецептора. Эти ооциты, инъецированные фракциями 4-6, показали самое большое и наиболее стойкое увеличение Cl--потока в ответ на внеклеточный Ca2+ (фиг. 35). Эти результаты указывают, что Ca2+-рецептор кодируется мРНК с размером в интервале 2,5-3,5 кв. Это указывает, что стратегия использования прямой экспрессии РНК, синтезированной из библиотеки транскрипционных векторов кДНК, является осуществимой. Эксперименты фракционирования по размерам этого вида были проведены и в каждом из трех различных экспериментов по фракционированию были получены подобные результаты.
Фракции мРНК, полученные и охарактеризованные в предшествующих экспериментах, могут быть проанализированы инъекцией в ооциты. Для каждой мРНК фракции 10-20 ооцитов инъецируют 50 нг РНК при концентрации 1 нг/л в воде. Инъецированные ооциты выдерживают при 18oC в течение 48-72 часов, после чего их оценивают по экспрессии Ca2+-рецептора, используя измерение Cl--потока. Для каждой группы инъецированных ооцитов определяли количество положительных на экспрессию рецептора, а также величину измеренного Ca2+-зависимого Cl--потока. В качестве отрицательных контролей ооциты инъецировали поли/A/+-обогащенной мРНК печени крысы, дрожжевой РНК или водой.
Ожидалось, что мРНК в интервале 2,5-3,5 кв. будет кодировать рецептор. мРНК большого размера может сделать необходимой попытку клонирования, основанную на гибридном истощении паратироидной мРНК перед инъекцией ооцита. Эта стратегия не зависит от генерации клонов кДНК полной длины для успеха. Если не получена экспрессия рецептора с фракцией мРНК одного размера, ооциты инъецируют фракциями смешанного размера для определения сочетания, которое даст появиться функциональному рецептору. Если окажется, что необходимо множество субъединиц для образования функционального рецептора, используют стратегию клонирования гибридного истощения экспрессии. В этой попытке отбирают клоны на основании их способности истощать определенные типы мРНК из суммарной популяции мРНК. Идентифицируют клон, кодирующий единственную субъединицу, по его способности предотвращать образование активного мультисубъединичного комплекса. При истощающем скринировании можно идентифицировать клоны, кодирующие все необходимые субъединицы.
Такой подход позволяет выделить клоны, кодирующие индивидуальные субъединицы, требующиеся для образования комплексного функционального рецептора. Анализируют синтетическую мРНК из пулов клонов на их способности индуцировать экспрессию Ca2+-рецептора в Xenopus ооцитах по тем же самым методикам, что использовались для анализа исходных фракций мРНК. Первоначально исследуют 10 пулов, представляющих 100000 первичных клонов каждый. Пулы клонов, показывающих положительный ответ, скринировали при более низкой /обычно 4-10-кратной/ вариабельности, и снова дополнительно разделяют положительные пулы и скринируют. Этот процесс субфракционирования библиотеки продолжают до тех пор, пока не будут идентифицированы индивидуальные положительные клоны. В качестве отрицательного контроля для анализа экспрессии ооцита генерируют антисмысловые транскрипты из тех матриц ДНК, которые индуцируют положительный ответ. Антисмысловые транскрипты не способны дать аутентичный рецептор и это будет контролем любого неспецифического положительного сигнала, возникающего при инъекции синтетической РНК. Другой проблемой является тот факт, что синтетическая РНК может случайно "отравить" трансляцию в инъекцированных ооцитах по неопределенному механизму. Для контроля этой возможности синтетические РНК, дающие отрицательный ответ, соинъецируют при различных разбавлениях с мРНК паратироидной клетки, чтобы определить, дают ли они неспецифическое наложение на экспрессию Ca2+-рецептора.
При идентификации индивидуального клона, кодирующего Ca2+-рецептор, вставка кДНК будет вырезана из вектора и использована для широкомасштабной синтетической РНК. Инъекция ооцита этим единственным видом РНК позволит грубо оценить характеристики экспрессированного рецептора.
Если размер мРНК, кодирующий Ca2+-рецептор, является слишком большим для клонирования прямой транскрипцией и экспрессией, или если включено множество субъединиц, используется техника гибридного истощения скринирования пулов клонов. Готовят кДНК вставку ДНК из пулов клонов из отобранной по размерам библиотеки кДНК паратироидных клеток. Эту ДНК гибридизуют с мРНК паратироидной клетки в условиях, которые допускают образование дуплексов ДНК/РНК. Извлекают неотожженную гибрид-истощенную РНК и используют для инъекций ооцита. Могут быть использованы другие методы гибридного истощения или гибрид-блокировки, альтернативные и хорошо известные специалистам в этой области. ДНК из пулов клонов, содержащих последовательности, представляющие собой мРНК Ca2+-рецептора, истощают от этой мРНК из суммарной популяции мРНК паратироидной клетки, и экспрессия рецептора снижается или отсутствует при инъекции ооцита. Способ субфракционирования продолжается на пулах клонов с пониженной вариабельностью, на каждой стадии анализируют клонированную ДНК, что истощает мРНК, кодирующую Ca2+-рецептор из общей популяции мРНК паратироидной клетки. Применение внутреннего контроля во время анализа гибридного истощения обеспечивает, чтобы гибрид-истощенная РНК являлась интактной и способной быть транслированной в ооците.
Человеческие паратироидные клетки экспрессируют бета-адренергетический рецептор, связанный с аденилат циклазой. Этот рецептор может быть экспрессирован в ооцитах, где он способен к агонист-индуцированной активации эндогенной аденилатциклазы. Во время скрининга гибрид-истощение клонов Ca2+-рецептора ооциты, инъецированные гибрид-истощенной мРНК, анализируют на активацию изопротеренол-индуцированной аденилатциклазы. Положительный ответ в этом анализе служит указанием, что любое наблюдаемое ингибирование ответа Ca2+-рецептора является специфическим, а не благодаря общему ингибированию суммарной популяции мРНК.
Стратегия скрининга гибрид-истощение может привести в результате к изоляции клонов, которые не содержат полной области кодирования белка. Положительные клоны, выделенные по этой стратегии скрининга, секвенируют для определения их способности кодировать белок. Northern-блот-анализ РНК человеческой паратироидной железы позволяет определить размер полной мРНК, соответствующей специфическим клонам. Если положительные клоны оказываются неполной длины, клонированную кДНК можно будет использовать в качестве зонда гибридизации для скрининга библиотеки кДНК паратироидной железы для полных кДНК.
Различные клеточные линии способны к связыванию экзогенно экспрессированных рецепторов с эндогенно функциональными ответами. Ряд таких клеточных линий /например, NIH-3T3, Hela, NG115, CHO, HEK 293 и COS7/ может быть испытан для подтверждения, что они лишены эндогенного Ca2+-рецептора. Такие линии, лишенные ответа на внешний Ca2+, могут быть использованы для установления стабильных трансфецированных клеточных линий, экспрессирующих клонированный Ca2+-рецептор.
Получение этих стабильных трансфектантов осуществляется трансфекцией соответствующей клеточной линии с эукариотическим вектором экспрессии, таким как pMSG, в которой была клонирована кодирующая последовательность кДНК Ca2+-рецептора в множественный сайт клонирования. Такие векторы экспрессии содержат область промотора, такую как промотор вируса опухоли грудной железы мыши /MMTV/, который управляет транскрипцией высокого уровня кДНК в различных клетках млекопитающих. Кроме того, эти векторы содержат гены для селекции клеток, которые стабильно экспрессируют интересующую кДНК. Отбираемый маркер в pMSG векторе кодирует фермент, ксантин-гуанинфосфорибозилтрансферазу /XGPRT/, которая придает устойчивость к метаболическому ингибитору, который добавляют к культуре, чтобы убить нетрансфецированные клетки. Различные векторы экспрессии и схемы селекции обычно оценивают, чтобы определить оптимальные условия для получения клеточных линий, экспрессирующих Ca2+-рецептор, для использования в скрининговом анализе с высоким расходом исходного вещества.
Наиболее эффективный способ трансфекции эукариотических клеточных линий плазмидой ДНК меняется с заданным типом клеток. Конструкция для экспрессии Ca2+-рецептора вводится в культивируемые клетки с помощью подходящей техники, или Ca2+ фосфатным осаждением, DEAE-декстран трансфекцией, липофекцией или электропорацией.
Клетки, которые имели стабильно введенную трансфекционную ДНК, были идентифицированы по их устойчивости к селекционной среде, как описано выше, и клональные клеточные линии будут продуцироваться размножением устойчивых колоний. Экспрессия кДНК Ca2+-рецептора этими клеточными линиями будет оцениваться гибридизацией в растворе и Northern-блот-анализом. Функциональная экспрессия рецепторного белка будет определяться измерением мобилизации внутриклеточного Ca2+ в ответ на внесенные извне агонисты Ca2+-рецептора.
Клонирование Ca2+-рецептора обеспечивает возможность проведения как структурных, так и функциональных исследований этого нового рецептора. Рекомбинантно полученный рецептор может быть кристаллизован для структурных исследований. Стабильно трансфецированные клеточные линии, экспрессирующие рецептор, могут быть использованы для скрининга с высоким расходом исходного вещества природного продукта или других банков соединений. Молекулы требуемой мощности и специфичности могут быть помечены /радиоактивно или флуоресцентно/. Возможность испытания молекул/экстрактов для замещения таких меченых молекул образует основу анализа с высоким расходом исходного вещества для скрининга.
Другая стратегия клонирования рецептора неорганического иона в ооциты является следующей.
Общие процедуры выделения, дефолликуляции и инъекции ооцитов лягушки описаны ниже. Вкратце, шпорцевых лягушек Xenopus laevis анестезируют погружением в 0,17% трикаин, удаляют долю яичника и разрезают на маленькие кусочки. Изолируют индивидуальные ооциты V-VI стадии, используя L-образные капиллярные трубки, после инкубации ткани яичника в не содержащем кальция буфере при комнатной температуре в течение 90 минут. Отделенные ооциты /обычно 200-300 на эксперимент/ затем инкубируют в растворе коллагеназы /Сигма, тип II; 2 мг/мл/ еще 90 минут, после чего фолликулярный слой может быть удален тонким пинцетом. Дифолликулированные ооциты инкубируют в течение ночи в лягушачьем рингере /ND96/ при 17oC и удаляют дегенерированные ооциты /обычно < 2-3% от всех/. Выжившие ооциты затем инъецируют 50 нл воды /контроль/ или поли/A/+РНК /15-50 нг/ооцит; в 50 нл воды/ и затем инкубируют 2-4 дня при 17oC. /Лягушачий рингер, ND96, содержит /мМ/: NaCl /96/, KCl /2/, CaCl2 /0,5/, MgCl2 /0,5/, HEPES /5/, пируват /2,5//.
Экстрагируют суммарную РНК из ткани /почки, остеокласты и т.д./ гуанидинийтиоцианатом и отделяют на подушке CsCl. Затем выделяют поли/A/+РНК хроматографией на олиго/dT/целлюлозе /два прохода через колонку/. Целостность поли/A/+РНК оценивают электрофорезом на агарозном геле. Способность 25-50 нг поли/A/+РНК дать повышение Ca2+-зависимой активности Cl--канала при экспозиции с внеклеточным Gd3+ оценивают /например как доказательство активности Ca2+-рецептора/. Следующей стадией является локализация активности мРНК, экспрессирующей Ca2+-рецептор, в маленьком интервале размеров /≈ 1 кв./. Для этой цели выделяют ≈ 100 мг поли/A/+РНК на градиенте сахарозы и собирают с градиента 40 фракций по размерам. Альтернативно ≈ 200-300 мг поли/A/+РНК могут быть фракционированы препаративным электрофорезом с непрерывным потоком в агарозном геле /Hediger M.A., Anal. Biochem. 159: 280-86 /1986/ и собирают 70-90 фракций. Инъецируют X. laevis ооциты пулами фракций [3-5 фракций/пул] поли/A/+РНК [0,2-0,5 нг/ооцит] фракций из пула/ов/ и оценивают способность этих пулов давать повышение активности Ca2+-рецепторов. Индивидуальные фракции из пула/ов/, дающие самую высокую активность Ca2+-рецептора, инъецируют в ооциты, чтобы определить фракцию /фракции/ внутри пула поли/A/+РНК, которая дает самую высокую экспрессию Ca2+-рецептора в ооцитах.
Конструируют направленную библиотеку кДНК из этого пула поли/A/+РНК, используют Суперскрипт плазмидную систему /pSPORTI; BRL/. кДНК генерируют используя Суперскрипт, MuMLV-RT, обратные транскрипты /многие из которых имели полную длину кодирующей области/. кДНК разделяют по размерам гель-электрофорезом и экстрагируют область кДНК соответствующего размера /на основании интервала размеров поли/A/+РНК, используя GENECLEAN II-BioI0I/. Эту кДНК выбранного размера затем направленно лигируют в pSPORTI плазмидный вектор, используя NotI праймер у 3'-конца и адаптер для SalI с 5'-конца. Полученные в результате плазмиды вводят в ELECTROMAX DHIOB клетки /BRL/ электропорацией. Трансформированные бактерии выращивают на нитроцеллюлозных фильтрах /500-800 колоний на фильтр/ и основные фильтры хранят при 4oC /короткий срок/ или -70oC /длинный срок/. Репликатные фильтры выращивают и выделяют плазмиду ДНК из фильтров, линеаризуют рестрикционным разрезанием, а затем используют в качестве матрицы для синтеза смысловой кДНК путем транскрипции in vitro /T7 промотор в присутствии Cap-аналога/. Пулы кРНК индивидуально инъецируют в ооциты, которые оценивают по экспрессии Gd3+-индуцированной /1-100 μМ/ активности Cl--потоков. Используют стандартную процедуру sib селекции для идентификации клона, который экспрессирует активность Ca2+-рецептора в ооцитах.
Рестрикционную карту кДНК Ca2+-рецептора создают и походящие рестрикционные фрагменты субклонируют в pSPORTI. Субклонированные кДНК двунаправленно секвенируют, используя стандартные методики /Секвеназа Полимераза 2® 2, USB/.
Используют секвенирующие праймеры /18-mer/, где необходимо секвенировать области внутри или между субклонами или разрешить сжатые или неясные области последовательности. Определяют кодирующую область для белка Ca2+-рецептора от наиболее длинной открытой рамки считывания, которая имеет начальный участок, предпочтительно гомологичный консенсусной последовательности Козака. Используют гидропатию и другие белковые алгоритмы, чтобы генерировать топологию белка Ca2+-рецептора. Сравнивают нуклеотидную последовательность кДНК, аминокислотную последовательность белка Ca2+-рецептора и топологию белка с такими же данными для других Ca2+-рецепторов и другими известными кДНК и белками, имеющимися в базе данных. Гомологичные области могут представлять домены, включающие связывание катиона или регуляцию.
Предпочтительный в настоящее время способ выделения нуклеиновой кислоты рецептора неорганических ионов основан на скрининге гибридизацией.
Можно использовать область специфических праймеров или зондов, происходящую из BoPCaR I, для примирования синтеза ДНК и амплификации PCR, а также для идентификации колоний, содержащих клонированную ДНК, кодирующую член семейства рецепторов неорганических ионов, используя известные методы /Innis et al., PCR Protocol, Acedemic Press, San Diego, CA (1990)/.
При использовании праймеров, которые происходят из нуклеиновой кислоты, кодирующей рецептор неорганического иона, специалист в данной области должен понимать, что при использовании очень жестких условий, отжиге при 50-60oC, последовательности, которые более чем на 76% гомологичны праймеру, будут амплифицироваться. При использовании менее жестких условий, отжиге при 35-37oC последовательности, которые более чем на 40-50% гомологичны праймеру, будут амплифицироваться.
При использовании зондов ДНК, происходящих из рецепторов неорганических ионов для гибридизации колония/бляшка, специалист в данной области должен понимать, что при использовании очень жестких условий, гибридизация при 50-65oC, SX SSPC, 50% формамида, промывка при 50-60oC, 0,5X SSPC, последовательности, имеющие области, которые более чем на 90% гомологичны зонду, могут быть получены, а при применении менее жестких условий, гибридизация при 35-37oC, SX SSPC, 40-45% формамида, промывка при 42oC, SSPC, будут получены последовательности, имеющие области, которые более чем на 35-45% гомологичны зонду.
Любые ткани могут быть использованы в качестве источника геномной ДНК, кодирующей члены семейства рецепторов неорганических ионов. Однако в отношении РНК наиболее предпочтительным источником являются ткани, которые экспрессируют повышенные уровни желаемого члена семейства рецепторов неорганических ионов. В настоящем изобретении используют инъекцию ооцитов и двухэлектродный вольт-кламп целевого ооцита для идентификации экспрессии из такого тканевого источника. Однако, используя описанные здесь последовательности, теперь можно идентифицировать такие клетки, используя последовательность рецептора неорганического иона в качестве зонда в процедурах Northern-блот или in situ гибридизации, устраняя таким образом необходимость в процедурах, применяемых для клонирования первого члена семейства, и устраняя необходимость получения РНК из ткани, которая экспрессирует повышенные уровни рецептора неорганического иона.
Кроме того, настоящее изобретение обеспечивает способы идентификации клеток и тканей, которые экспрессируют член семейства рецепторов неорганических ионов. Например, могут быть использованы зонд, состоящий из последовательности ДНК, например BoPCaR I, ее фрагмента, или последовательности ДНК, кодирующей другой член семейства белковых рецепторов неорганических ионов, в качестве зонда или праймера амплификации для детектирования клеток, которые экспрессируют матричный гомолог для зонда или праймера. Специалист в данной области может легко адаптировать обычные доступные методики амплификации и детектирования нуклеиновых кислот таким образом, что он применяет зонды или праймеры, основанные на последовательностях, кодирующих член семейства рецепторов неорганических ионов.
Взяв соответствующие клетки или ткани, экспрессирующие другие рецепторы, эти рецепторы могут быть клонированы аналогичным образом тому, что описано выше для кальциевого рецептора паратироидной клетки. Например, мРНК из человеческой остеокластомной ткани кодирует остеокластный кальциевый рецептор (фиг. 34). Следовательно, для выделения клона для человеческого остеокластного рецептора необходимо только выделить мРНК из остеокластомной ткани, получить библиотеку кДНК и проанализировать/фракционировать субпулы, как описано выше. Кроме того, предпочтительные рецепторы для скрининга лекарств имеют человеческое происхождение. Клон, кодирующий рецептор из одного вида, может быть использован для получения соответствующего клона человеческой кДНК путем кроссгибридизации, как это хорошо известно специалистам в данной области. В дополнение к этому, клон из паратироидной клетки или рецептор другой клетки позволяет выделить гены, кодирующие подобные белки, чувствительные к неорганическим ионам, в других клетках, и экспрессировать такие белки. Это достигается различными путями. Саузерн-блот-анализ человеческой геномной ДНК, использующий кДНК Ca2+-рецептора в качестве зонда гибридизации, даст указание на ряд родственных последовательностей, кодирующих внутри генома; гибридизация в условиях различной жесткости даст указание на степень расхождения среди родственных последовательностей. Это обеспечит информацию о потенциальном числе генов, кодирующих белки родственных рецепторов. Northern-блот-анализ кДНК Ca2+-рецептора в качестве зонда определит, одинаковые или родственные транскрипты находятся в различных тканях. Если детектируются родственные транскрипты, гомологичные Ca2+-рецептору паратироидной клетки, относительно просто получить клоны этих мРНК, или скринированием соответствующей библиотеки кДНК или методиками полимеразной цепной реакции /PCR/.
"Прогулка" по целевым генам /TGW/ является модификацией стандартной полимеразной цепной реакции /PCR/, которая позволяет амплифицировать неизвестные последовательности ДНК, соседние с короткими сегментами известной последовательности. Parker et al. , Nucl. Acids Res., 19: 3055 /1991/. В отличие от обычных PCR методик, которые амплифицируют последовательности ДНК между двумя известными праймерными участками, TGW может амплифицировать последовательности ДНК, соседнюю с одним таким участком. Итак, TGW может служить заменой традиционного клонирования и методов скринирования библиотеки для выделения последовательностей вверх или вниз от известных последовательностей. Процедура может быть использована для выделения генов из любой исходной матрицы ДНК, для которой известно ограниченное количество информации с последовательности.
Во-первых, проводят параллельно несколько стандартных PCR реакций, используя один "целевой праймер-мишень" и различные "прогулочные праймеры". Целевой праймер-мишень является последовательностью - специфическим праймером, точно комплементарным известной последовательности интересующей молекулы ДНК и направленным к неизвестным соседним последовательностям. "Прогулочные праймеры" являются неспецифическими последовательностями, некомплементарными к ДНК вбилизи целевого праймера-мишени. "Прогулочные праймеры" могут быть любыми олигонуклеотидами, неродственными последовательности праймера-мишени. В первой серии PCR продукты получают только, когда прогулочный праймер отжигает нить ДНК, соседнюю с и комплементарную нити, с которой гибридизуется праймер-мишень. Интересующие продукты PCR предпочтительно находятся внутри интервала размеров 5 килооснований. Продукты амплификации получают как примерно на 60% ошибочно спаренных нуклеотидов внутри прогулочного праймера по отношению к матрице ДНК. Требуется отличное спаривание оснований только для первых 3' нуклеотидов прогулочного праймера, но частичная гомология допускается иначе. Температура отжига является ключевой переменной при определении числа PCR продуктов, как определено электрофорезом на агарозном геле.
Во-вторых, анализ олигомерного удлинения осуществляется с использованием "праймера внутренней детекции". Этот праймер представляет собой известные последовательности между двумя предыдущими праймерами, соседними с праймером-мишенью. Праймер внутренней детекции подвергают действию киназы с 32P-гамма-АТФ, затем используют в единственном PCR цикле с ДНК от первой PCR в качестве матрицы. Такое удлинение идентифицирует продукты в первой PCR, соседней с праймером-мишенью. Эти новые продукты идентифицируют электрофорезом на агарозном геле и ауторадиографически. Любые продукты, которые не гибридизуются с праймером внутренней детекции, представляют собой несоприкасающиеся продукты амплификации, полученные любой подгруппой праймеров.
Последнее, полосы, идентифицированные при анализе олигомерного удлинения, вырезают из геля, реамплифицируют по стандартной PCR, используя праймер-мишень и прогулочный праймер, с которыми первоначально получена полоса. Эту новую PCR полосу затем секвенируют непосредственно, получая ранее неизвестную информацию о последовательности.
Для расширения информации в противоположном направлении готовят комплементы праймера-мишени и праймера внутренней детекции и их порядок является обратным в протоколе.
При осуществлении скрининга гибридизацией и клонирования следует учитывать следующее. Поскольку имеется вырожденность генетического кода, существует более одного кодона для почти всех аминокислот /за исключением триптофана и метионина/. Кроме того, частота использования любого конкретного кодона отличается от нечеловеческих по сравнению с человеческими. Олигонуклеотиды синтезируют с учетом вырожденности кодонов и человечески-предпочтительными кодонами. Кроме того, олигонуклеотиды с различными перестановками возможных кодонов также синтезируют. Чтобы избежать избыточного количества, нужно синтезировать не все возможные последовательности, получаемые в результате вырожденности кода. Далее, выбирают подгруппы кодонов, которые встречаются наиболее часто.
Полученные таким образом новые клоны рецепторов могут быть оценены функционально экспрессией или в ооцитах или трансфекцией клеточных линий. Трансфецированные клеточные линии, экспрессирующие клетка-специфический рецептор неорганического иона, затем могут обеспечить средство скрининга с большим расходом исходного материала для молекул, которые действуют специфически на ион-чувствительный механизм, например, остеокластов или окологломерулярных клеток.
В альтернативном способе кальциевый рецептор может быть клонирован экспрессией в эукариотические клетки. Например, может быть получена библиотека кДНК из паратироидной мРНК и клонирована в эукариотический вектор экспрессии, такой как pCDNAI. Субпулы из этой библиотеки могут быть трансфецированы в эукариотические клетки, такие как COS7 или HEK293 клетки, давая в результате кратковременную экспресию относительно высокого уровня последовательностей кодируемых кДНК. Клетки, трансфецированные клоном с функцией кальциевого рецептора, будут экспрессировать кальциевый рецептор, который затем может быть активирован кальцием, неомицином или другими кальцимиметическими соединениями. Если клетки сначала нагружают флуорометрическим индикатором для /Ca2+/в активация кальциевого рецептора приводит в результате к увеличению флуоресценции. Идентифицируют библиотеку субпулов, содержащих кальциевый рецептор, по их способности при трансфекции в эукариотические клетки вызывать кальциевое или кальцимиметически-специфическое повышение флуоресценции. Такая флуоресценция может быть детектирована при использовании или флуориметра или сортировщика флуоресцентно-активированных клеток /FACS/.
Мы также разработали "анализ улавливания кальция" для детекции COS 7 клеток, экспрессирующих G-белок, соединенный с рецепторами. В этом анализе трансфецируют монослой COS 7 клеток клонами кДНК из библиотеки бычьей паратироидной кДНК /например, субфракциями или пулами из библиотеки, приготовленной в pCDNAI / и анализируют их по их способности улавливать радиоактивный 45Ca++ в ответ на обработку агонистом рецептора Ca2+. Монослои переносят в эмульсию для ауторадиографии и идентифицируют клетки, которые улавливают 45Ca++, по наличию кластеров фотографических зерен в затемненном поле микроскопа. Библиотеку пулов, которые дают положительный сигнал, затем последовательно подразделяют до тех пор, пока не будет идентифицирована единственная кДНК, которая продуцирует сигнал.
Кальциевые рецепторы очевидно являются функционально родственными классу рецепторов, которые используют так называемые "G"-белки для связывания лиганда, связанного с внутриклеточными сигналами. Такие "G-связанные" рецепторы могут вызывать повышение внутриклеточного циклического АМФ за счет стимуляции аденилилциклазы с помощью рецептора, активированного "G"-белком, или сам может вызывать снижение циклического АМФ за счет ингибирования аденилилциклазы рецептором, активированным "G"-белком. Другой рецептор, активированный G-белками, вызывает изменения уровней инозитолтрифосфата, приводя в результате к выделению Ca++ из внутриклеточных пулов. Этот последний механизм является особенно уместным для кальциевых рецепторов. Все известные G-связанные рецепторы являются структурно родственными, имеющими семь сохраненных трансмембранных областей. Ряд таких рецепторов был клонирован, основываясь на гомологии последовательности в ранее клонированные рецепторы. Одна особенно полезная попытка заключается в применении дегенерации гомологичных праймеров до кодирущих областей сохраненных трансмембранных доменов и амплификации областей ДНК, кодирующих эти последовательности, используя реакцию полимеразной цепи /PCR/. Так, такие олигонуклеотидные праймеры смешивают с геномной ДНК или кДНК до РНК, выделенной из выбранной ткани, и проводят PCR. Могут потребоваться некоторые эксперименты, чтобы специально амплифицировать новые последовательности G-связанных рецепторов из выбранной ткани, поскольку нет необходимости идентифицировать уже известные G-связанные рецепторы, но это хорошо понятно специалисту в данной области /смотри, например, Buck L. and Axel R. /1991/, Cell, 65: 175-187/.
Кальциевые рецепторы также могут быть клонированы с помощью такой попытки PCR. Два примера дегенеративных пар олигонуклеотидных праймеров, которые могут быть использованы для PCR амплификации последовательностей, кодирующих кальциевые рецепторы, приведены в конце описания. Первая пара основана на кроссгомологии, показанной большинством G-связанных рецепторов в последовательностях, кодирующих трансмембранные домены II и VII соответственно. Вторая праймерная пара основана на кроссгомологии, показываемой более разделенными субгруппами G-связанных рецепторов, которые включают кальцитонин, секретин, ПТГ и GLP рецепторы. Эта пара соответствует сохраненным последовательностям, кодирующим трансмембранные домены III и VII. Когда одну или обе эти две пары праймеров смешивают с кДНК из паратироидной или остеокластной ткани, например, амплификация PCR приводит в результате к генерации амплифицированных ДНК примерно 500-800 пар оснований. Эти ДНК могут быть выделены и проанализированы на наличие последовательностей кальциевых рецепторов. Например, каждая амплифицированная последовательность может быть использована в качестве зонда, чтобы выделить клон кДНК полной длины, который затем может быть оценен в одном или более анализов, приведенных ниже, чтобы определить, кодируется ли рецептор неорганического иона.
В альтернативном способе рецептор неорганического иона может быть клонирован при использовании моноклональных антител, генерированных против рецептора. Моноклональные антитела дают мощный инструмент для иммуноаффинной очистки определенных белков. Так, могут быть получены данные для очищенной ограниченной аминокислотной последовательности из интересующего белка и использованы для конструирования зондов олигонуклеотидных последовательностей, чтобы скринировать клоны полной последовательности кДНК.
Будет описан пример, включающий кальциевый рецептор. Для получения гибридом используют целые клетки бычьей паратироидной железы в качестве иммуногена. Получают очищенные диспергированные клетки и препараты живых или фиксированных клеток инъецируют интраперитонеально подходящему штамму мышей в соответствии с установленными процедурами. Приводятся стандартные протоколы схемы иммунизации и получения гибридом. Используют двустадийную процедуру скриннинга для идентификации гибридом, секретирующих моноклональные антитела, которые распознают Ca2+-рецептор. Начальный скрининг будет идентифицировать эти моноклональные антитела, которые распознают поверхностные антигены паратироидных клеток. Затем используют иммуногистохимические методики для скрининга гибридомных супернатантов на наличие мышиных антител, которые связаны с поверхностью паратироидных клеток. Этот скрининг может быть осуществлен на фиксированных сечениях ткани паратироидной железы или на диспергированных клетках в первичной культуре. Методики этого анализа хорошо разработаны в литературе.
Этот скрининг позволит идентифицировать гибридому, продуцирующие антитела к различным детерминантам на поверхности клетки, и ожидается, что моноклональные антитела, специфические для Ca2+-рецептора составят только их маленькую подгруппу. Для идентификации моноклональных антител, которые связываются с Ca2+-рецептором, оценивают гибридомные супернатанты, которые являются тест-положительными при начальном скрининге, на их способность блокировать ответ культивируемых паратироидных клеток на агонисты Ca2+-рецептора. Ожидается, что некоторые антитела, которые связаны с внеклеточной областью рецептора, будут ингибировать или активировать связывание лиганда или, иначе, воздействовать на или оказывать свое действие на активацию рецептора.
Моноклональные антитела, положительные в обоих скринингах, охарактеризованы вестерн-блоттингом, иммуноосаждением и иммуногистохимически. Это позволяет определить размер антигена, который распознается, и его распределение в ткани. Затем используют соответствующее моноклональное антитело для очистки белка Ca2+-рецептора иммуноаффинной хроматографией по стандартным методикам. Получают достаточное количество белка, чтобы осуществить определение ограниченной аминокислотной последовательности. Затем конструируют дегенеративные олигонуклеотидные зонды на основании информации о пептидной последовательности. Потом эти зонды используют для скрининга библиотек кДНК паратироидной железы на пулы полной длины Ca2+-рецептора. Полученные клоны охарактеризованы секвенированием ДНК и функциональной экспрессией в системе ооцита и при культивировании клеточной линии млекопитающего.
Альтернативно антитела могут быть использованы для скрининга библиотек экспрессии, например библиотек кДНК в λgIII или его эквиваленте, чтобы определить те клоны, которые экспрессируют антигенно реактивный белок. Затем такие клоны могут быть секвенированы для определения, кодируют ли они белок, который может быть Ca2+-рецептором.
Специалистам в данной области также следует учитывать, что могут быть использованы библиотеки фагового распределения для клонирования и анализа кальциевых рецепторов вместо моноклональных антител. В этих библиотеках антитело-вариабельные области или произвольные пептиды встроены в фаговые векторы экспрессии таким образом, что области антител или пептидов обнаруживаются на поверхности фаговой частицы. Фаги, которые несут области антител или пептидов, способных к высокоспецифичному связыванию с кальциевыми рецепторами, будут связываться с клетками, которые несут эти рецепторы /например, паратироидными клетками, C-клетками, остеокластами и т.д./. Сотни миллионов таких фагов могут быть приготовлены против этих типов клеток, предпочтительно выбирают те фаги, которые могут связываться с этими клетками /которые включают связывание фагов с кальциевыми рецепторами/. Таким образом, сложность библиотеки может быть резко уменьшена. Несколько повторов этого процесса приведут в результате к пулу фагов, которые связывают использованный тип клеток. Впоследствии скрининг, описанный выше для моноклональных антител, может быть использован для выделения фага, который несет связывающее кальциевый рецептор антитело или пептидные области, а эти фаги могут быть использованы для выделения кальциевых рецепторов для их структурной идентификации и клонирования. Наборы для получения таких несущих фаги библиотек являются коммерчески доступными /например, Stratacyte, or Cambridge Antibody Tecnology L. /. Рекомбинантный фаг, наделенный такими свойствами связывания кальциевого рецептора, также может быть использован вместо моноклональных антител в различных анализах кальциевых рецепторов. Такой фаг также может быть использован в скринингах с большим количеством исходного материала связывания-конкуренции для идентификации органических соединений, способных к функциональному связыванию с кальциевыми рецепторами, которые могут служить как ведущие структуры для разработки лекарств для людей, действующих на кальциевые рецепторы.
По другой альтернативе может быть использовано сродство поперечно-сшитых радиолигандов к таким рецепторам для выделения рецепторного белка, как описано Pilch and Czech, I Receptor Biochem. Methodol. 161, 1984. Ковалентное присоединение радиолиганда допускает интенсивную промывку для удаления неспецифического связывания. Например, молекулу с высоким сродством, например произвольный сополимер аргинина и тирозина /MM = 22 K, соотношение arg: tyr = 4:1/, который мобилизует внутриклеточный Ca2+ с ЭК50 около 100 мМ или менее, йодируют 125I и сшивают. Протамины, благодаря их намного меньшему размеру, могут быть предпочтительными в исследовании сшивки и могут быть подвергнуты восстановительному алкилированию, как описано в Dottavio-Martin and Ravel, 87, Analyt. Biochem. 562, 1978.
Неспецифическая метка минимально сохраняется при сшивке в присутствии немеченных поликатионов и двух- и трехвалентных катионов. При высоких концентрациях этих молекул неспецифические взаимодействия метки с поверхностью клетки могут быть снижены.
Изобретение обеспечивает выделенные последовательности нуклеиновых кислот, кодирующие рецепторы неорганических ионов, и сами выделенные рецепторы. Оно также обеспечивает единичные фрагменты вышеупомянутых последовательностей. Термин "выделенный" означает последовательность нуклеиновой кислоты: /i/ амплифицированную in vitro, например, полимеразной цепной реакцией полимеразной цепи /PCR/; /ii/ синтезированные, например, химическим синтезом; /iii/ рекомбинантно полученные при клонировании; или /iv/ очищенные, например, расщеплением или разделением в геле. Термин "изолированный" при использовании в описаниях полипептида или аминокислотной последовательности относится к полипептидам, полученным в результате экспрессии системы с использованием выделенных последовательностей нуклеиновых кислот изобретения, а также полипептидов, синтезированных, например, методами химического синтеза, и полипептидов, выделенных из нативных биологических материалов, а затем последовательно очищенных с использованием традиционных белковых аналитических процедур.
В область настоящего изобретения также включены единичные фрагменты рецепторов неорганических ионов. Термин "единичные фрагменты" относится к частям рецептора, которым не найдены дубликаты в известных последовательностях по данным настоящего изобретения. Эти полипептидные фрагменты могут быть легко идентифицированы как единичные при просмотре базы данных для белков, известных на время изобретения для идентичных пептидов. В дополнение к генерации фрагментов рецепторов при экспрессии клонированных частичных последовательностей рецептора ДНК фрагменты могут быть генерированы непосредственно из интактного белка. Белки специфически расщепляют протеолитическими ферментами, включая, но не ограничиваясь ими, трипсин, химотрипсин или пепсин. Каждый из этих ферментов является специфическим для типа белковой связи, которую он расщепляет. Трипсин катализирует гидролиз пептидных связей, у которых карбонильная группа идет из основной аминокислоты, обычно аргинина или лизина. Пепсин и химотрипсин катализируют гидролиз пептидных связей от ароматических аминокислот, в частности триптофана, тирозина и фенилаланина. Дополнительные группы расщепленных полипептидных фрагментов генерируются путем превентивного расщепления на участке, который является восприимчивым к протеолитическому ферменту. Например, реакция ε-аминогруппы лизина с этилтрифтортиоацетатом в мягких щелочных условиях в растворе приводит к блокированию аминокислотных остатков, которые соседствуют с пептидной связью, не являющейся более восприимчивой к гидролизу трипсином. Goldberger et al., Biochem. 1:401 /1962/. Следовательно, обработка такого полипептида трипсином расщепляет только аргининовые остатки. Полипептиды также могут быть модифицированы для создания пептидных связей, которые являются восприимчивыми к протеолитическому гидролизу, катализируемому ферментом. Например, алкилирование цистеиновых остатков β-галоэтиламинами дает пептидные связи, которые гидролизуются трипсином, Lindley, Nature, 178:647 /1956/. В дополнение к этому могут быть использованы химические реагенты, которые расщепляют полипептидные цепи у специфических остатков Witcop., Adv. Protein Chem. 16: 221 /1961/. Например, цианогенбромид расщепляет полипептиды по метиониновым остаткам. Gross and Witkip, J. Am. Chem. Soc., 83: 1510 /1961/. Следовательно, при обработке рецептора неорганического иона, такого как, например, человеческий кальциевый рецептор или его фрагмент, различными сочетаниями модификаторов, протеолитическими ферментами и/или химическими реагентами генерируют многочисленные дискретные перекрывающиеся пептиды различного размера. Эти пептидные фрагменты могут быть выделены и очищены из таких переваров хроматографическими методами.
Альтернативно фрагменты могут быть синтезированы с использованием соответствующих твердофазных синтетических процедур. Steward and Young Solid Phase Peptide Synthesis, Freemantle, San Fransisco, CA /1968/.
Фрагменты могут быть использованы в анализах, как связывающие ион-агенты, при получении антител и т.п. Фрагменты также могут быть отобраны по наличию желаемых биологических активностей. Например, фрагмент может включать только участок связывания или участок, который связывается с агонистами или антагонистами /например, кальцием/, как описано здесь. Такие фрагменты легко идентифицировать специалистам в данной области, используя рутинные методы определения специфического связывания фрагмента. Например, в случае кальциевого рецептора испытуемый фрагмент может быть экспрессирован с использованием технологии рекомбинантной ДНК фрагментом гена, кодирующего рекомбинантный рецептор. Это фрагмент затем контактируют с кальцием или другим химикатом в подходящих условиях ассоциации, чтобы определить, связывается ли кальций с фрагментом. Эти фрагменты являются полезными при скрининговом анализе агонистов и антагонистов кальция и терапевтического эффекта, где он является полезным для удаления кальция из сыворотки или других тканей организма.
Другие полезные фрагменты включают те, которые имеют только внешний участок, охватывающий мембрану участок или внутриклеточный участок рецептора. Эти участки легко идентифицируются при сравнении аминокислотной последовательности рецептора с последовательностями известных рецепторов или другими стандартными методиками. Эти фрагменты являются полезными для формирования химерных рецепторов с фрагментами других рецепторов, так что клетка, лишенная рецептора, может быть сформирована с внутриклеточной частью, которая осуществляет желаемую функцию внутри этой клетки, и внеклеточной частью, которая вызывает ответ клетки на наличие ионов или тех агонистов или антагонистов, которые описаны здесь. Такие химерные рецепторные гены, когда соответственно сформулированы, являются полезными при генетической терапии при различных заболеваниях, включая дисфункцию рецепторов, или когда модуляция рецепторной функции обеспечивает желаемый эффект у пациента. Кроме того, химерные рецепторы могут быть сконструированы таким образом, что внутриклеточная область сочетается с желаемым ферментным процессом, который может быть детектирован колориметрически, радиометрически, люминометрически, спектрофотометрически или флуорометрическим анализом, и активируется при взаимодействии внеклеточного участка с его нативным лигандом /например, кальцием/ или агонистами или антагонистами изобретения. Клетки, экспрессирующие такие химерные рецепторы, являются основой для облегчения скрининга для обнаружения новых агонистов и/или антагонистов изобретения.
Изобретение также относится к мутантам или аналогам и другим производным изолированных рецепторов, как описано здесь. Так, изобретение охватывает не только встречающиеся в природе белки, но и их производные. Такие производные обладают желаемой рецепторной активностью, описанной здесь, и обычно идентифицируются описанными здесь методами. Хотя приводятся примеры таких белков и генов, кодирующих их, эти примеры не ограничивают изобретение, но только демонстрируют вариацию, которая может быть ассоциирована с такими генами и белками. Обычно ген будет иметь аминокислотную последовательность нативного рецептора, но могут быть изменены одно или более аминокислотных положений, которые не оказывают существенного влияния на рецепторную активность полученного рецепторного белка. Так, например, в неконсервативных областях белка кальциевого рецептора /т.е. тех областях, которые не являются необходимыми для рецепторной активности/ аминокислоты могут быть делетированы, добавлены или заменены. В более консервативных областях, которые требуются для рецепторной активности, аминокислоты могут быть более консервативно замещены. Например, один или более аминокислотных остатков внутри последовательности могут быть замещены другой аминокислотой подобной полярности, которая действует как функциональный эквивалент. Замещение аминокислоты внутри последовательности может быть выбрано среди других членов класса, к которому принадлежит аминокислота. Неполярные /гидрофобные/ аминокислоты включают аланин, лейцин, изолейцин, валин, пролин, фенилаланин, триптофан и метионин. Полярные нейтральные аминокислоты включают глицерин, серин, треонин, цистеин, тирозин, аспарагин и глютамин. Положительно заряженные (основные) аминокислоты включают аргинин, лизин и гистидин. Отрицательно заряженные /кислотные/ аминокислоты включают аспарагиновую кислоту и глютаминовую кислоту.
Специалистам в данной области должно быть понятно, что могут быть использованы стандартные процедуры для определения консервативных и неконсервативных областей белка, применяя технику мутагенеза in vitro или делеционный анализ, и что все такие производные являются эквивалентами описанным здесь ниже.
Также в область изобретения включены рецепторные белки или их единичные фрагменты или их производные, которые дифференциально модифицированы во время или после трансляции, например, фосфорилированием, гликозилированием, сшивкой, ацилированием, протеолитическим расщеплением, связыванием с молекулой антитела, молекулой мембраны или другим лигандом /Ferguson et al., 1988, Ann. Res. Biochem., 57: 285-320/.
Кроме того, последовательности рекомбинантных нуклеиновых кислот изобретения могут быть сконструированы таким образом, чтобы модифицировать процессинг или экспрессию рецепторных последовательностей. Например, и это не является ограничением, кодирующая последовательность может быть объединена с промоторной последовательностью и/или участком связывания рибосомы, используя хорошо охарактеризованные методы, а в результате облегчается улучшенная экспрессия и биодоступность.
Дополнительно, данная рекомбинантная кодирующая последовательность может быть мутирована in vitro или in vivo, чтобы создать вариации кодирующих областей и/или образовать новые участки рестрикции эндонуклеазами, или разрушить ранее существовавшие, чтобы облегчить дополнительно модификацию in vitro. Может быть использована любая техника мутагенеза, известная на данном уровне техники, включая, но не ограничиваясь, in vitro сайтнаправленный мутагенез /Hutchinson et al. , 1978, J. Biol. Chem. 253:6551/, используя TABR-линкеры /Фармациа/, PCR-направленный мутагенез и т.п.
В дополнение к этому кодоны могут быть модифицированы таким образом, что, хотя они кодируют идентичную аминокислоту, такой кодон может быть предпочтительным кодоном при выборе системы экспрессии.
Изобретение также обеспечивает единичные фрагменты нуклеиновой кислоты, кодирующей рецептор неорганического иона. Термин "единичные фрагменты" относится к частям нуклеиновой кислоты, для которых не найдены идентичные дубликаты в известных последовательностях на дату изобретения. Эти фрагменты могут быть легко идентифицированы
при анализе базы данных нуклеиновых кислот, существующих на дату изобретения, чтобы детектировать дубликаты. Единичные фрагменты являются полезными, между прочим, в процедурах клонирования и анализа.
Кроме того, изобретение обеспечивает агенты, связывающие рецептор, включая антитела и/или их фрагменты, которые могут быть конъюгированы с фрагментом токсина, или экспрессированы вместе с фрагментом токсина как рекомбинантный слитый белок. Фрагмент токсина будет связан с и входить в клетку-мишень при использовании взаимодействия связывающего агента и соответствующего поверхностного рецептора клетки-мишени. Фрагмент токсина, с которым агент, антитело и/или фрагмент конъюгированы, может быть белком, таким как, например, pokeweed противовирусный белок, рицин, гелонин, абрин, дифтерийный экзотоксин, или Pseudomonas эндотоксин. Фрагментом токсина также может быть испускающий большую энергию радионуклид, такой как кобальт-60. Химическая структура токсинного фрагмента не предназначена для ограничения изобретения каким-либо путем. Специалистам в данной области следует учитывать, что большее разнообразие возможных фрагментов может быть соединено со связующими агентами. Смотри, например, "Conjugate Vaccines", Contributions to Microbiology and Immunology, J.M. Cruse and R.E. Lewis, Jr. (eds). Carger Press, New York, 1989. Следует также учитывать, что многие токсинные фрагменты, включая специально перечисленные выше, считаются фармацевтически приемлемыми.
Конъюгирование связующего агента с другим фрагментом /например, бактериальным токсином/ может быть осуществлено с помощью любой химической реакции, которая будет связывать две молекулы настолько, чтобы обе молекулы сохранили свою соответствующую активность. Такое связывание может включать многие химические механизмы, например ковалентное связывание, аффинное связывание, интеркаляцию, координационное связывание и комплексообразование. Предпочтительным связыванием, однако, является ковалентное связывание. Ковалентное связывание может быть достигнуто или путем прямой конденсации существующих боковых цепей, или путем введения внешней мостиковой молекулы. Многие двухвалентные и поливалентные связующие агенты являются полезными при связывании молекул белков, таких как антитела, с другими молекулами. Например, типичные сочетающие агенты могут включать органические соединения, такие как тиоэфиры, карбодиимиды, сукцинимидные эфиры, диизоцианаты, глутаральдегиды, диазобензолы и гексаметилендиамины. Этот перечень не предназначен исчерпать различные классы связывающих агентов, известных на данном уровне техники, в нем просто приведены примеры наиболее обычных связывающих агентов. /Смотри, Killen and Lindstrom, 1984, "Specific killing of lymphocytes that cause experimental Autoimmune Myasthenia Gravis by toxin-acetylcholine receptor conjugates". Jour. Immun. 133:1335-2549; Jansen, F.K., H. E. Blythman, D. Carriere, P. Casella, O. Gros, P. Gros, J.C. Laurent. F. Paclucci, B. Pau, P. Pncelet, G. Richer, H.Vidal, and G.A. Voisin, 1982, "Immunotoxins: Hybrid molecules combining high specificity and potent cytotoxicity". Immunological Reviews 62:185-216; and Vitetta et al., и выше/.
Используя методики рекомбинантной ДНК, настоящее изобретение обеспечивает клетки-мишени, включая клетки-мишени млекопитающих, которые сконструированы для экспрессии рецепторов неорганических ионов. Например, гены для таких рецепторов, клонированные в соответствии с приведенными выше методиками, могут быть вставлены в клетки, которые от природы экспрессируют рецепторы, таким образом, что рекомбинантный ген экспрессирует при намного более высоких уровнях.
Настоящее изобретение также обеспечивает системы экспериментальных моделей для изучения физиологической роли рецепторов. В этих модельных системах рецепторы неорганических ионов, фрагменты или их производные могут быть или введены в систему или получены внутри системы. Такие модельные системы могут быть использованы для изучения эффектов или функции клетки при избытке или недостатке рецептора. Экспериментальные модельные системы могут быть использованы для изучения эффектов в клетках или культивируемых тканях, в целом животном, или в конкретных клетках или тканях внутри целого животного, или в системах культивируемых тканей, или сверх определенных интервалов времени /включая длительность эмбриогенеза/. Предпочтительным вариантом является анализ, включающий клонированные рецепторы или их части, в частности включая те, что являются полезными в анализе скрининга лекарств с большим расходом исходных материалов.
В дополнительных вариантах изобретения может быть использован рекомбинантный ген для инактивации эндогенного гена путем гомологичной рекомбинации и в результате создания дефицитной по рецептору неорганического иона клетки, ткани или животного. Например, и это не является ограничением, может быть сконструирован рекомбинантный ген, содержащий вставленную мутацию /например, neo ген/, который при вставке его в геном реципиентной клетки, ткани или животного инактивирует транскрипцию рецептора. Такая конструкция может быть введена в клетку, такую как эмбриональную стволовую клетку, с помощью такой методики, как трансфекция, трансдукция, инъекция, и т.п. Стволовые клетки, лишенные интактной рецепторной последовательности, могут генерировать трансгенные животные, дефицитные по этому рецептору.
"Трансгенным животным" является животное, имеющее клетки, которые содержат ДНК, которая искусственно вставлена в клетку, эта ДНК становится частью генома животного, которое развивается с такой клеткой. Предпочтительными трансгенными животными являются приматы, мыши, крысы, коровы, свиньи, лошади, козы, овцы, собаки и кошки. Трансгенная ДНК может кодировать человеческие рецепторы неорганических ионов.
В дополнительном варианте изобретения нативная экспрессия у животного может быть снижена при введении определенного количества антисмысловой РНК или ДНК, эффективного для снижения экспрессии рецептора.
Различные способы доступны для получения трансгенных животных, ассоциированные с настоящим изобретением. ДНК может быть инъецирована в пронуклеус оплодотворенного яйца перед слиянием мужского и женского пронуклеусов, или инъецирована в ядро зародышевой клетки /например, ядро двуклеточного эмбриона/ с последующей инициацией деления клетки /Brinster et al., Proc. Nat. Acad. Sci. USA, 82: 4438-4442 /1985/. Эмбрионы могут быть инфицированы вирусами, особенно ретровирусами, модифицированными несущей рецептур неорганического иона последовательностью изобретения.
Плюрипотентные стволовые клетки, происходящие из внутренней клеточной массы эмбриона и стабилизированные в культуре, могут быть подвергнуты манипуляциям в культуре для введения нуклеотидных последовательностей изобретения. Трансгенное животное может быть получено из таких клеток путем имплантации в бластоцит, который имплантируют приемной матери и позволяют дойти до срока.
Животные, подходящие для трансгенных экспериментов, могут быть получены из стандартных коммерческих источников, таких как Чарльз Ривер /Вилмингтон, МА/, Теконик /Джермантаун, НЙ/, Харлан Спраг Доули /Индианаполис, ИН/ и т.д.
Процедуры манипуляций с эмбрионом грызунов и микроинъекции ДНК в пронуклеусы зиготы хорошо известны специалистам в данной области /Hogan et al., выше/. Процедуры микроинъекций в яйца рыб, амфибий и птиц детализированы у Houdebine and Chourrout, Experientia, 47: 897-905 /1991/. Другие процедуры для введения ДНК в ткани животных описаны в патенте США N 4945050 /Sandford et al., 30 июля 1990/.
Только в качестве примера для получения трансгенной мыши вызывают суперовуляцию у самки мыши. Самок помещают с самцами и спарившихся самок умерщвляют асфиксией CO2 или цервикальной дислокацией и извлекают эмбрион из вырезанных яйцеводов. Удаляют окружающие скопления клеток. Пронуклеарные эмбрионы затем промывают и хранят до времени инъекции. Взрослых самок мышей на произвольной стадии цикла спаривания с вазектомизированными самцами. Реципиентных самок покрывают одновременно с донорными самками. Эмбрионы затем переносят хирургически.
Процедура генерации трансгенных крыс подобна таковой для мышей. Смотри, Hammer et al., Cell, 63: 1099-1112 /1990/.
Методы культивирования эмбриональных стволовых /ЭС/ клеток и последующее получение трансгенных животных путем введения ДНК в ЭС клетки с использованием таких методов, как электропорация, осаждение фосфата кальция/ДНК и прямая инъекция, также хорошо известны специалистам в данной области. Смотри, например, Teratocarcinomas and Embryonic Stem Cell, A Practical Approach, E.J. Robertson, IRL Press /1987/.
В случаях, включающих произвольную интеграцию гена, клон, содержащий последовательность/и/ изобретения, сотрансфецируют с геном, кодирующим устойчивость. Альтернативно, ген, кодирующий устойчивость к неомицину, физически связывают с последовательностью/ми/ изобретения. Трансфекцию и выделение желаемых клонов осуществляют любым из нескольких методов, хорошо известных специалистам в данной области /E.J. Robertson, выше/.
Молекулы ДНК, введенные в ЭС клетки, также могут быть интегрированы в хромосому по способу гомологичной рекомбинации, Capecci, Science, 244: 1288-1292 /1989/. Способ положительной селекции рекомбинационного события /например, neo-устойчивость/ и двойной положительной-отрицательной селекции /например, neo-устойчивость и устойчивость к ганцикловиру/ и последующая идентификация целевых клонов PCR были описаны Capecci, выше, и Joyner et al. , Hature, 338: 153-156 /1989/, содержание которых приведено здесь в качестве уровня техники. Конечной фазой процедуры является инъекция ЭС клеток-мишеней в бластоциты и перенос бластоцитов псевдобеременным самкам. Полученных в результате химерных животных размножают и потомство анализируют саузерн-блоттингом для идентификации индивидуумов, которые несут трансген.
Процедуры получения млекопитающих - не грызунов и других животных обсуждались другими авторами. Смотри, Houdebine and Chourrout, выше; Fursel et al. , Science, 244: 1281-1288 /1989/; и Simms et al., Bio/Technology, 6: 179-183 /1988/.
Применения
Первичный гиперпаратироидизм /ГПТ/ характеризуется гиперкальциемией и повышенными уровнями циркулирующего ПТГ. Один из основных дефектов при ГПТ проявляется в пониженной чувствительности паратироидных клеток к отрицательной обратной связи регулирования внеклеточного Ca2+. Следовательно, в ткани пациента с первичным ГПТ "график" для внеклеточного Ca2+ сдвигается вправо, так что требуются более высокие, чем нормальная, концентрации внеклеточного Ca2+ для снижения секреции ПТГ. Кроме того, при первичном ГПТ даже высокие концентрации Ca2+ часто снижают секрецию ПТГ лишь частично. При вторичном /уремическом/ ГПТ подобное повышение графика для внеклеточного Ca2+ наблюдается даже при такой степени, при которой подавление Ca2+ секреции ПТГ является нормальным. Изменения в секреции ПТГ параллельны изменениям /Ca2+/в: график для вызванного внеклеточным Ca2+ повышения /Ca2+/в сдвинут вправо, а величина такого повышения уменьшена. Кроме того, окрашивание ткани с моноклональным антителом, которое появляется для распознавания Ca2+-рецептора, уменьшается в аденомах и гиперпластичных паратироидных клетках.
Ca2+-рецептор представляет собой дискретное молекулярное целое для фармакологической интервенции. Молекулы, которые имитируют или антагонизируют действие внеклеточного Ca2+, являются благоприятными при длительном уходе как при первичном, так и при вторичном ГПТ. Такие молекулы обеспечивают дополнительный импульс, требующийся для подавления секреции ПТГ, без которого гиперкальциемическое состояние само не может быть достигнуто. Такие молекулы с большей эффективностью, чем внеклеточный Ca2+, могут устранить возможный неподавляемый компонент секреции РТГ, который особенно причиняет беспокойство в аденомных тканях. Альтернативно или дополнительно, такие молекулы могут подавлять синтез ПТГ, поскольку была показана продолжительная гиперкальциемия, чтобы снизить уровни препроПТГ мРНК в бычьих и человеческих аденомных паратироидных тканях. Продолжительная гиперкальциемия также подавляет пролиферацию паратироидных клеток in vitro, так что кальцимиметики также могут быть эффективными при ограничении гиперплазии паратироидных клеток, характерной для вторичного ГПТ.
Другие клетки в организме могут отвечать непосредственно на физиологические изменения концентрации внеклеточного Ca2+. Секреция кальцитонина из паратироидных клеток в тироиде /C-клетках/ регулируется изменениями концентрации внеклеточного Ca2+. Секреция ренина из окологломерулярных клеток в почках, подобно секреции ПТГ, снижается при увеличении концентраций внеклеточного Ca2+. Внеклеточный Ca2+ вызывает мобилизацию внутриклеточного Ca2+ в этих клетках. Другие почечные клетки отвечают на кальций следующим образом: повышенный Ca2+ ингибирует образование 1,25 /OH/2 витамина D периферическими канальцевыми клетками, стимулирует продукцию кальций-связывающего белка в периферических канальцевых клетках и ингибирует канальцевую реабсорбцию Ca2+ и Mg2+ и действие вазопрессина на модулярную толстую восходящую ветвь петли Хенля /MTAL/, снижает действие вазопрессина на корковые клетки собирающей протоки и воздействует на васкулярные клетки гладкой мышцы в кровеносных сосудах почечной гломерулы. Кальций промотирует дифференциацию интестинальных кубковых клеток, клеток грудной железы и клеток кожи. Он также ингибирует секрецию предсердного натриуретического пептида из сердечного предсердия, снижает цАМФ аккумуляцию в тромбоцитах, изменяет секрецию гастрина и глюкагона, и действует на васкулярные клетки гладкой мышцы, модифицируя секрецию клетки вазоактивными факторами. Выделенные остеокласты отвечают на повышение концентрации внеклеточного Ca2+ соответствующим повышением /Ca2+/в, что частично создается мобилизацией внутриклеточного Ca2+. Повышение /Ca2+/в в остеокластах ассоциировано с ингибированием функциональных ответов /костной резорбции/ аналогов на секрецию ПТГ в паратироидных клетках. Выделение щелочной фосфатазы из формирующих кость остеокластов непосредственно стимулируется кальцием. Итак, имеется достаточно указаний, чтобы предположить, что Ca2+ в дополнение к его повсеместной роли как внутриклеточного сигнала также функционирует как внеклеточный сигнал для регулирования ответов некоторых специализированных клеток. Молекулы настоящего изобретения могут быть использованы для лечения заболеваний, ассоциированных с разрушающими Ca2+ ответами в этих клетках.
Клонирование Ca2+-рецептора в паратироидные клетки и другие клетки позволит непосредственно оценить наличие гомологичных белков в других клетках. Таким образом может быть получено семейство структурно гомологичных Ca2+-рецепторных белков. Такие рецепторы позволят понять, как эти клетки детектируют внеклеточный Ca2+ и дадут возможность оценить механизм/ы/ как место действия лекарств, описанных здесь, эффективных при лечении ГПТ, остеопороза и гипертонии, и новые способы лечения других костных и минерал-родственных заболеваний.
Другие применения обсуждены выше. Например, рекомбинантные Ca2+-рецепторные белки могут быть использованы при лечении и введены по стандартным методикам, например, трансфекцией нуклеиновой кислоты, кодирующей такой белок. В дополнение к этому такой белок является полезным при анализе кальцимиметических молекул настоящего изобретения.
Следующие примеры иллюстрируют изобретение, но не ограничивают его область.
Примеры
В приведенных здесь исследованиях было найдено, что различные органические молекулы мобилизуют внутриклеточный Ca2+ и снижают секрецию ПТГ в паратироидных клетках. Эти молекулы структурно различны, но большинство имеет чистый положительный заряд при физиологическом pH. Катионная природа органических молекул играет важную роль, но не является единственным фактором, определяющим активность.
Пример 1: Скрининг кальцимиметических молекул на бычьих паратироидных клетках.
Диссоциированные бычьи паратироидные клетки очищают на градиентах Перколля и культивируют всю ночь на не содержащей сыворотки среде. Затем клетки нагружают fura-2 и флуорометрически измеряют концентрацию свободного внутриклеточного Ca2+. Изменения /Ca2+/в используют для скрининга молекул, активных на Ca2+-рецепторе. Для того чтобы считать молекулу кальцимиметической, требуется, чтобы она показывала нормальные эффекты, вызываемые повышением внеклеточного Ca2+, и приводила к быстрой активации Ca2+-рецептора. То есть:
1) Молекула должна вызывать повышение /Ca2+/в; повышение /Ca2+/в может существовать в отсутствие внеклеточного Ca2+ и/или молекула может потенциально повышать /Ca2+/в, вызванную внеклеточным Ca2+.
2) Молекула должна вызывать снижение изопротеренолстимулированное образование циклического АМФ, которое блокируется коклюшным токсином.
3) Молекула должна ингибировать секрецию ПТГ в том же самом интервале концентраций, который вызывает повышение /Ca2+/в.
4) Кривые концентрация - ответ для повышения /Ca2+/в и секреции ПТГ молекулой должны быть сдвинуты вправо активатором ПКС, таким как форболмиристатацетат /ФМА/.
Испытано несколько структурно различных классов молекул: полиамины, аминогликозиды, антибиотики, протамин и полимеры лизина или аргинина. Структура этих молекул представлена на фиг. 1. На фиг. 1 приведены чистый положительный заряд у молекул и их ЭК50, вызывающие мобилизацию внутриклеточного Ca2+ в бычьих паратироидных клетках.
В общем более высокий положительный заряд на молекуле соответствует ее более высокой мощности в вызывании мобилизации внутриклеточного Ca2+. Однако были найдены некоторые поразительные исключения для этой кажущейся роли, как обсуждено ниже.
Как можно видеть из чертежей, спермин, неомицин B и протамин вызывают быстрое и кратковременное повышение /Ca2+/в в fura-2-нагруженных бычьих паратироидных клетках (фиг. 6, 7, 11). Однако они не вызывают продолжительного, стационарного повышения /Ca2+/в в бычьих паратироидных клетках (фиг. 6, 11), хотя они делают это в человеческих паратироидных клетках (фиг. 19). В этом отношении они подобны цитозольному Ca2+ ответу, вызванному внеклеточным Mg2+, который вызывает мобилизацию внутриклеточного Ca2+, не сопровождающуюся притоком внеклеточного Ca2+ в бычьих клетках (фиг. 11б). Кратковременное повышение /Ca2+/в, вызванное спермином, неомицином B или протамином, не блокируются низкими концентрациями /1 μМ/ La3+ или Gd3+ /фиг. 11г, ж/. Кратковременное повышение цитозольного Ca2+, вызванное молекулами поликатионов, существует в отсутствие внеклеточного Ca2+, но блокируется, когда клеточные запасы Ca2+ истощены предварительной обработкой иономицином (фиг. 7; 11 з, и). Следовательно, все эти молекулы вызывают мобилизацию внутриклеточного Ca2+ в паратироидных клетках.
Было дополнительно показано, что молекулярные поликатионы мобилизуют такой же пул внутриклеточного Ca2+, как пул, использованный внеклеточным Ca2+. Итак, повышение концентрации внеклеточного Ca2+ прогрессивно ингибирует кратковременное повышение /Ca2+/в, вызванное спермином (фиг. 6). Наоборот, максимально эффективные концентрации спермина или неомицина B (фиг. 12) блокируют кратковременное, но не стационарное повышение /Ca2+/в, вызванное внеклеточным Ca2+.
Значит спермин, неомицин B и протамин ингибируют секрецию ПТГ в такой же степени, что и внеклеточный Ca2+. Такие ингибирующие эффекты на секрецию были получены при концентрациях, которые вызывают мобилизацию внутриклеточного Ca2+ (фиг. 8, 13). Эти находки имеют отношение к пониманию механизмов, вносящих свой вклад в регулирование секреции ПТГ внеклеточным Ca2+. Поскольку различные неорганические поликатионы все ингибируют секрецию, еще только внеклеточный Ca2+ вызывает продолжительное стационарное повышение /Ca2+/в, такое повышение /Ca2+/в не может быть в значительной мере включено в регуляцию секреции. Мобилизация внутриклеточного Ca2+, а не приток внеклеточного Ca2+, является по существу механизмом, ассоциированным с ингибированием секреции. Это является важным, потому что это определяет достаточный механизм воздействия, если молекула воздействует на секрецию ПТГ; молекулы, селективно стимулирующие приток внеклеточного Ca2+, будут относительно неэффективными при подавлении секреции ПТГ.
Подобно мобилизации внутриклеточного Ca2+, вызванной внеклеточным Ca2+, мобилизация, вызванная молекулярными поликатионами, снижается ФМА. Типичный эксперимент, показывающий предпочтительные ингибирующие эффекты ФМА на кратковременное появление цитозольного Ca2+, вызванное спермином, показан на фиг. 14. Кратковременное появление цитозольного Ca2+, вызванное АТФ, является неэффективным, даже когда используют субмаксимальные концентрации АТФ. Эффект ФМА на кратковременное появление цитозольного Ca2+, вызванное молекулярными поликатионами, параллелен его действию на ответы на внеклеточный Ca2+; в обоих случаях имеется сдвиг вправо на кривой концентрация - ответ (фиг. 15). Подавляющее действие ФМА на /Ca2+/в сопровождается потенцирующим действием на секрецию, которое снимается при более высоких концентрациях органических поликатионов (фиг. 16).
Мобилизация внутриклеточного Ca2+, вызванная молекулярными поликатионами, ассоциируется с увеличением образования инозитолфосфатов. Например, протамин вызывает быстрое (в течение 30 с) повышение образования ИФ3, которое сопровождается ростом уровня ИФ1. Оба эти эффекта зависят от концентрации внеклеточного протамина (фиг. 17). Кроме того, предварительная обработка ФМА "затупляет" образование инозитолфосфатов, вызванное молекулярными поликатионами. Типичные результаты, полученные со спермином, приведены на фиг. 18.
Спермин, неомицин B и протамин уменьшают индуцированное изопротеренолом повышение циклического АМФ. Подобно ингибирующему действию внеклеточного Ca2+ на образование циклического АМФ, ингибирующее действие, вызванное молекулярными поликатионами, блокируется предварительной обработкой токсином коклюша (табл. 2).
Коклюшный токсин /PTx/ блокирует ингибирующее действие внеклеточного Ca2+ и молекулярных поликатионов на образование циклического АМФ. Культивируют бычьи паратироидные клетки в течение 16 часов с или без 100 нг/мл коклюшного токсина. Клетки последовательно промывают и инкубируют в течение 15 минут с 10 μМ изопротеренола с или без указанных концентраций внеклеточного Ca2+ или молекулярных поликатионов. Определяют суммарный циклический АМФ /клетки + супернатант/ с помощью РИА и выражают результаты как процент от уровня, полученного при 0,5 мМ Ca2+ /112±17 пмоль/106 клеток/. Каждая величина является средней ± SEM из трех экспериментов.
В человеческих паратироидных клетках внеклеточный Mg2+ вызывает продолжительное стационарное повышение /Ca2+/в в дополнение к быстрому кратковременному повышению (фиг. 10). Как и в бычьих паратироидных клетках, отвечающих на внеклеточный Ca2+, стационарное повышение /Ca2+/в, вызываемое Mg2+ в человеческих паратироидных клетках, приводит в результате к притоку Ca2+ через нечувствительные к напряжению каналы (фиг. 10а). Это влияние Mg2+ на стационарную /Ca2+/в в человеческих паратироидных клетках наблюдается как в аденомной, так и в гиперпластичной тканях.
Испытывали неомицин B и спермин на влияние на /Ca2+/в в человеческих паратироидных клетках, полученных из аденомной ткани. Типичные результаты с неомицином B показаны на фиг. 19. Неомицин B вызывает не только кратковременное, но дополнительное и стационарное повышение /Ca2+/в в человеческих паратироидных клетках (фиг. 19а). Так, в человеческих клетках схема изменения /Ca2+/в, вызванного внеклеточным Ca2+, Mg2+ или неомицином B, являются очень похожей.
Кратковременное возникновение цитозольного Ca2+, вызванное неомицином B, существует в присутствии La3+ /1 μМ/ и в отсутствие внеклеточного Ca2+. Следовательно, неомицин B вызывает мобилизацию внутриклеточного Ca2+ в человеческих паратироидных клетках. Неомицин B ингибирует секрецию ПТГ из человеческих паратироидных клеток при концентрациях, которые вызывают мобилизацию внутриклеточного Ca2+ (фиг. 13). Однако имеется некоторое различие в ответах человеческих и бычьих паратироидных клеток на неомицин B. ЭК50 неомицина B для мобилизации внутриклеточного Ca2+ составляет 40 μМ в бычьих и 20 μМ в человеческих паратироидных клетках (см. фиг. 13 и 15), тогда как мощность спермина является подобной в бычьих и человеческих паратироидных клетках /ЭК50 = 150 μМ/. Итак, хотя бычьи клетки могут быть использованы для начального исследования для скрининга тест-молекул на активность, важно провести последующие исследования с использованием человеческих паратироидных клеток.
Для оценки влияния молекулярных поликатионов на C-клетки используют неопластические клеточные линии, происходящие из медуллярной тироидной карциномы крысы /гМТС 6-23 клетки/. Как спермин /10 μМ/, так и неомицин B /5 μМ/ не оказывают влияния на фоновую /Ca2+/в в этих клетках. Ни одна из этих молекул не дает ответа на последующее добавление внеклеточного Ca2+. Типичные результаты, документирующие отсутствие влияния неомицина B, показаны на фиг. 21. Неомицин B /1 μМ/ или спермин /1 или 5 μМ/ не вызывают какого-либо повышения /Ca2+/в в остеокластах /фиг. 23/. На чертеже показано, что возникает некоторая возможность ответа на последующее повышение концентрации внеклеточного Ca2+, хотя это не является согласующимся с полученными данными. В двух других клетках спермин /5 μМ/ снова не оказывает влияния на фоновую /Ca2+/в и вызывает незначительное ингибирование /около 15%/ индуцированного внеклеточным Ca2+ повышения /Ca2+/в. В третьей клетке неомицин B /5 μМ/ не оказывает влияния на фоновую /Ca2+/в и не воздействует на повышение /Ca2+/в, вызванное внеклеточным Ca2+. Суммарная картина, которая получается из этих исследований, заключается в том, что спермин и неомицин B не оказывают влияния на фоновые или стимулированные уровни цитозольного Ca2+ в остеокластах.
Неудача молекулярных поликатионов повлиять на Ca2+-чувствительные механизмы C-клеток или остеокластов показывает возможность открыть или сконструировать новые ведущие молекулы, которые специфически действуют на Ca2+-рецептор паратироидной клетки или, иначе, модулируют одну или более функций нормального ответа паратироидных клеток на /Ca2+/в.
Скрининг различных других молекул более детально описан ниже и результаты суммированы в табл. 1.
Пример 2: Скрининг полиаминов.
Полиамин с прямой цепью /спермин, спермидин, ТЕТА, ТЕРА, и РЕНА/ и два их производных /NPS 381 и NPS 382/ были скринированы, как в примере 1. Было найдено, что все молекулы мобилизуют внутриклеточный Ca2+ в бычьих паратироидных клетках. Порядок их мощности приведен в табл. 3, при этом чистый положительный заряд указан в скобках.
Путресцин /+2/ и кадаверин /+2/ являются неактивными при концентрации 2 мМ.
Другой полиамин с прямой цепью, ДАДД, ведет себя несколько отлично от других полиаминов и описан в примере 7.
Пример 4: Скрининг аминогликозидных антибиотиков.
Шесть антибиотиков подвергли скринингу, как в примере 1. Полученные в результате ЭК50 для мобилизации внутриклеточного Ca2+ в порядке возрастания мощности представлены в табл. 4.
Канамицин /+4,5/ и линкомицин /+1/ не вызывали эффекта при концентрации 500 μМ. Внутри аминогликозидной серии имеется корреляция между чистым положительным зарядом и мощностью. Однако неомицин является значительно более мощным, чем различные полиамины /NPS 381, NPS 382, NPS 383, РЕНА/, которые имеют равный или больший положительный заряд. Поскольку аминогликозидные антибиотики этого типа обладают почечной токсичностью, которая может быть родственной взаимодействию с кальциевым рецептором в почках, такой скрининг может быть полезным для отбора по токсичности при разработке новых аминогликозидных антибиотиков.
Пример 5: Скрининг пептидов и полиаминокислот.
Протамин и полимеры лизина или аргинина с различной длиной пептидной цепи подвергают скринингу на их способность мобилизовать внутриклеточный Ca2+, как в примере 1. Полученные в результате ЭК50 для мобилизации внутриклеточного Ca2+, в порядке их мощности, представлены в табл. 5.
Чистый положительный заряд этих полимеров увеличивается с увеличением ММ. Итак, что касается аминогликозидов, имеется прямая корреляция между чистым зарядом и мощностью среди этой серии полиаминокислот. Протамин по существу является полиArg с чистым положительным зарядом +21.
Пример 6: Скрининг арилалкиламинов.
Молекулы, выбранные в классе арилалкиламиновых токсинов, происходят из ядов ос и пауков, они были скринированы, как в примере 1.
Филантотоксин-433 /+3/ не оказывает влияния при концентрации 500 μМ. Он подобен по структуре аргиотоксинам, описанным ниже.
Аргиотоксин-636 /400 μМ/ не вызывает увеличения /Ca2+/в, но дает возможные цитозольные Ca2+-ответы при последующем добавлении внеклеточного Ca2+. Имеется общий признак для всех молекул, что они активируют Ca2+-рецептор, и это также видно для различных внеклеточных двухвалентных ионов. Более детально это рассматривается в примере 7.
В противоположность аргиотоксину-636 аргиотоксин-659 вызывает повышение /Ca2+/в с ЭК50 300 μМ. Аргиотоксин-659 отличается от аргиотоксина-636 наличием оксииндольного фрагмента, а не диоксифенильной группы. Это является единственным различием структуры этих двух молекул. Итак, различие в мощности связано с природой ароматической группы, а не в полиаминной цепи, которая несет положительный заряд.
Пример 7: Скрининг блокаторов Ca2+-каналов.
Блокаторы Ca2+-каналов, то есть тех молекул, которые блокируют приток внеклеточного Ca2+ через чувствительные к напряжению Ca2+-каналы, были скринированы, как в примере 1. Имеется три структурных класса блокаторов Ca2+-каналов: /1/ дигидропиридины, /2/ фенилалкиламины, и /3/ бензотиазепины.
Ни один из испытанных дигидропиридинов [нифедипин, нитрендипин, ВАУ К 8644, и /-/ 203-791 и /+/ 202-791] не оказывает какого-либо действия на фоновую /Ca2+/в или повышение /Ca2+/в, вызванное внеклеточным Ca2+ при испытаниях при концентрации 1 μМ. Предыдущие исследования показали, что паратироидные клетки, лишены чувствительных к напряжению Ca2+-каналов, но имеют нечувствительные к напряжению Ca2+-каналы, которые регулируются Ca2+-рецептором.
Исследованными фенилалкиламинами являются верапамил, Д-600 /метоксипроизводное верапамила/, ТМВ-8, и аналог ТМВ-8, NPS 384. Первые три молекулы были испытаны при концентрации 100 μМ. Фенилалкиламины ведут себя отлично от других исследованных молекул. Они не вызывают изменения /Ca2+/в при добавлении к клеткам, промытым в буфере, содержащим низкую концентрацию внеклеточного Ca2+ /0,5 мМ/. Однако верапамил, Д-600, и ТМВ-8 дают возможность мобилизации внутриклеточного Ca2+, вызванной внеклеточными двухвалентными катионами, и они дополнительно блокируют приток внеклеточного Ca2+. При промежуточных уровнях внеклеточного Ca2+ /1-1,5 мМ/ эти молекулы были способны вызвать маленькое, но сильное повышение /Ca2+/в, которое возникает при мобилизации внутриклеточного Ca2+.
Фенилалкиламины действуют по-другому, чем органические поликатионы, подобные неомицину. Данные подтверждают, что верапамил, Д-600 и ТМВ-8 являются частичными агонистами или аллостерическими активаторами Ca2+-рецептора, в противоположность другим исследованным молекулам, которые являются полными агонистами.
Молекула NPS 384 при концентрации 300 μМ не вызывает повышения /Ca2+/в, но блокирует приток внеклеточного Ca2+. Испытания при более высоких концентрациях может выявить способность этой молекулы вызывать мобилизацию внутриклеточного Ca2+.
Хотя способность этих молекул блокировать приток является интригующей, но не полностью неожиданной, это представляет собой способность этих молекул вызывать кратковременное повышение /Ca2+/в /возникающее благодаря мобилизации внутриклеточного Ca2+/, что является важным. Рассматриваемый эксперимент с измерениями /Ca2+/в в паратироидных клетках показывает, что кратковременное повышение /Ca2+/в почти неизменно является результатом мобилизации внутриклеточного Ca2+ и, следовательно, отражает активацию Ca2+-рецептора.
Исследованный бензотиазепин, дильтиазем, во всех отношениях подобен верапамилу и Д-600 и также является эффективным при 100 μМ.
Следует упомянуть, что за исключением фенилалкиламинов все испытанные выше активные молекулы вызывают повышение /Ca2+/в, которая имеет величину, подобную вызываемой максимальной эффективной концентрацией внеклеточного Ca2+. Это показывает, что эти молекулы являются такими же эффективными, как и внеклеточные двухвалентные катионы. Это сопоставимо с активностью фенилалкиламинов, которые возможно действуют только как частичные агонисты.
Среди фенилалкиламинов выяснились некоторые интересные соотношения структура - активность. Значительным является различие мощностей молекул, подобных ТМВ-8 и NPS 384. ТМВ-8 делает возможным кратковременное повышение /Ca2+/в при 100 μМ, тогда как NPS 384 не может сделать это даже при 300 μМ, хотя эти молекулы несут одинаковый чистый положительный заряд. Из этого следует, что некоторые другие структурные различия, не имеющие отношения к чистоту заряду, придают большую мощность ТМВ-8.
Пример 8: Скрининг молекул на человеческих паратироидных клетках.
Спермин и неомицин испытывали на воздействие на /Ca2+/в на человеческих паратироидных клетках, полученных из желез, удаленных хирургическим путем, и приготовленных, как в примере 1.
Было найдено, что в человеческих паратироидных клетках спермин вызывает только маленькое повышение /Ca2+/в при испытаниях при концентрации 300 μМ.
С другой стороны, неомицин вызывает сильное повышение /Ca2+/в в человеческих паратироидных клетках при испытании в концентрации 20 μМ. Величина ответа, вызванного неомицином, равна величине, вызванной максимально эффективной концентрацией внеклеточного Ca2+.
Пример 9: Скрининг молекул на Xenopus ооцитах.
Ооциты, инъецированные мРНК из человеческих паратироидных клеток, экспрессируют Ca2+-рецептор и мобилизуют внутриклеточный Ca2+ в ответ на различные двух- и трехвалентные катионы. Использование этого скрининга позволяет испытать действие непосредственно на Ca2+-рецепторе. Ооциты, экспрессирующие Ca2+-рецептор, также ответили нескольким молекулам, активным к интактным паратироидным клеткам, при скрининге, как описано ниже. Гексациклен вызвал мобилизацию внутриклеточного Ca2+ при концентрации 135 μМ. Неомицин /100 μМ/ и NPS 382 /5 μМ/ также являются эффективными. Это предлагает несомненное доказательство, показывающее, что эти молекулы действуют на Ca2+-рецептор или на некоторые другие белки, тесно связанные с их функцией.
Например, мы можем детектировать экспрессию Ca2+-рецептора в ооцитах, измеряя мобилизацию 45Ca2+. В этих экспериментах ооциты инъецируют бычьей паратироидной мРНК или водой и потом 72 часа экспонируют в сыворотке или 10 μМ неомицина. Перед стимулированием ооциты нагружают 45Ca2+. Стимуляция сывороткой в течение 20 минут приводит в результате к выделению внеклеточного 45Ca2+, представляющего собой 45% повышения по сравнению с мнимым контролем в буфере. Контроль с 10 μМ неомицина в течение 20 мин. приводит в результате к 76% повышения выделения 45Ca2+. Анализ является достаточно чувствительным для использования при клонировании Ca2+-рецептора, и имеет преимущество большего расхода исходного вещества, чем электрофизиологическое измерение Ca2+-активированного Cl--потока.
В другом примере получают человеческую остеокластомную ткань из биопсии костной ткани. Ооциты, инъецированные мРНК, выделенной из этой ткани, контролируются 30 мМ Ca2+. Контроль не дает ответа, тогда как 8 из 12 опытов, инъецированных остеокластомной мРНК, ответили соответственно /фиг. 34/. Эти эксперименты обеспечили первое доказательство, что Ca2+-ответ остеокластов на внеклеточный Ca2+ в действительности закодирован генетически. Результаты также указывают, что остеокластный Ca2+-рецептор может быть клонирован экспрессией в Xenopus ооциты.
Пример 10: Молекулярный скрининг на остеокластах крыс.
Различные чувствительности паратироидных клеток и остеокластов крыс к внеклеточному Ca2+ предполагают, что их Ca2+-рецепторы являются различными. Хотя паратироидные клетки отвечают на внеклеточный Ca2+ при концентрациях между 0,5 и 3 мМ, остеокласты отвечают, только когда уровень внеклеточного Ca2+ повышается выше 5 мМ. Такая более высокая концентрация Ca2+ является физиологически не присущей остеокластам; поскольку они резорбируют кость, локальная концентрация внеклеточного Ca2+ может достигать таких высоких уровней, как 30 мМ.
Скринирование молекул с крысиными остеокластами осуществляется следующим образом. Получают остеокласты из длинных костей новорожденных крысят. Измеряют /Ca2+/в в единичных клетках, используя флурометрический индикатор indo -1. Испытывали спермин, спермидин, неомицин и верапамил и ни один из них не вызвал какого-нибудь значительного повышения /Ca2+/в в остеокластах /хотя незначительные ответы детектируются/.
При концентрации 1 мМ спермидин вызывает незначительное повышение /Ca2+/в /около 10% от вызванного максимальной концентрацией внеклеточного Ca2+/. Ни неомицин /10 мМ/, ни спермин /10 или 20 мМ/ не вызывают повышения /Ca2+/в в остеокластах крыс. Неомицин /10 мМ/ не блокирует повышения /Ca2+/в, вызванного последующим добавлением 25 мМ внеклеточного Ca2+. Предварительная обработка спермином /20 мМ/, однако, снижает ответ на внеклеточный Ca2+. Верапамил /100 μМ/ не вызывает детектируемого повышения /Ca2+/в, но блокирует ответ на внеклеточный Ca2+.
Сравнение остеокластов и паратироидных клеток показывает, что молекулы, активные на последних, являются относительно неэффективными в остеокластах. Это показывает, что лекарства, мишенью которых является специфический Ca2+-рецептор, без воздействия на другие типы этих рецепторов, присутствующих на других Ca2+-чувствительных клетках, уже разработаны. Подобным образом, также могут быть разработаны лекарства, активные к двум или более таким Ca2+-рецепторам.
Скрининг на кальцимиметическую и кальцилитическую активность на кальциевом рецепторе остеокласта
Соединения, обладающие активностью на кальциевом рецепторе остеокласта, могут быть обнаружены при измерении /Ca2+/в в единичных остеокластах крысы, как описано выше. Усовершенствованный анализ дает возможность использовать умеренные до высокого количества исходного соединения. Этот новый способ основан на использовании остеокластов кролика, которые могут быть получены с высоким выходом /105 на животное/ и чистотой /95% клеток являются остеокластами/. Чистота препарата остеокласта кролика позволяет измерить /Ca2+/в, осуществляя его на популяциях клеток. Поскольку регистрируемый сигнал флуоресценции является усредненным ответом популяции, внутриклеточная вариабельность сведена к минимуму и точность опыта резко повышена. Это, в свою очередь, дало возможность скринировать больше соединений на активность.
Остеокласты кролика получают из 6-дневных крольчат. Животных умерщвляют обезглавливанием, удаляют длинные кости и помещают в остеокластную среду /ОС-среда: альфа-минимальная существенная среда содержит 5% фетальной бычьей сыворотки и пенициллин - стрептомицин/. Кости разрезают на секции скальпелем и помещают в 2 мл ОС-среды в коническую центрифужную пробирку емкостью 50 мл. Костные секции измельчают дроблением до тех пор, пока не получат довольно гомогенную суспензию костных частиц. Затем суспензию разбавляют 25 мл ОС-среды и препарат осторожно встряхивают /"в вихре"/ в течение 30 секунд. Костным частицам дают отстояться в течение 2 минут, после чего удаляют супернатант и прибавляют в центрифужную пробирку емкостью 50 мл. Костные частицы ресуспендируют в ОС-среде, взвихривают, седиментируют и собирают, как описано. Объединяют супернатанты от двух сборов и центрифугируют, полученный после центрифугирования осадок ресуспендируют в Перколле. Затем суспензию центрифугируют и удаляют белую вязкую полосу чуть ниже мениска и промывают ОС-средой. Стадия центрифугирования Перколля дает в результате значительное улучшение по чистоте и позволяет рассеять остеокласты с высокой плотностью, пригодной для измерения /Ca2+/в в популяции клеток. Клетки рассевают в соответствующие покровные стекла для измерения /Ca2+/в в соответствии с одним из описанных ниже методов. При необходимости чистота препарата может быть улучшена. В этом случае клетки культивируют всю ночь и затем промывают содержащим Ca2+ и Mg2+ буфером. Затем погружают монослой клеток в не содержащий Ca2+ и Mg2+ буфер, содержащий 0,02% ЕДТА и 0,001% проназы, на 5 минут. Затем удаляют этот буфер и заменяют ОС-средой и оставляют клетки покрытыми на 1-2 часа перед нагрузкой клеток флуорометрическим индикатором и измеряют /Ca2+/в, как описано выше.
В одном варианте эта методика позволяет измерение /Ca2+/в в популяциях остеокластов с использованием флуоресцентной микроскопии. Очищенным остеокластам дают возможность прикрепиться к покровным стеклам диаметром 25 мм и затем нагружают indo-1. Покровные стекла хранили в камере для суперслияния и помещают на предметный столик флуоресцентного микроскопа. Применение объектива с низкой мощностью /4х/ дает поле, содержащее 10-15 остеокластов, которые могут быть визуализированы. В одной вариации флуоресценция каждой клетки в поле зрения может быть зарегистрирована одновременно и сохранена отдельно для последующего анализа. Изменения /Ca2+/в каждой клетки могут быть оценены и рассчитывают средний ответ всех клеток в поле зрения. В другом варианте можно зарегистрировать флуоресценцию от всего поля зрения клеток и сразу обработать. В еще одном варианте окончательные данные представлены в виде среднего ответа от клеток, имеющихся в поле микроскопа. Исходя из этого внутриклеточная вариабельность сводится к минимуму и точность анализа значительно повышается. Этот способ дает возможность скринировать 10-20 соединений в неделю на активность на кальцевом рецепторе.
В более предпочтительном варианте эта методика позволяет измерять /Ca2+/в в популяциях остеокластов, используя традиционный флуорометр. Очищенным остеокластам дают возможность прикрепиться к прямоугольным покровным стеклам. В одном варианте используют стандартную кварцевую кювету /1 см2/ и покровные стекла 2х1,35 см. В другом варианте используют микрокювету /0,5 см2/ и стеклянные покровные стекла 1 х 0,75 см. В любом случае клетки нагружают fura-2 или любым другим подходящим флуорометрическим индикатором для измерения /Ca2+/в. Регистрируют флуоресценцию нагруженных индикатором клеток, как описано выше для бычьих паратироидных клеток. Этот метод позволяет использовать большее количество исходного вещества, чем флуоресцентная микроскопия, и дает возможность оценивать 20-50 соединений в неделю на активность к остеокластному кальциевому рецептору.
В наиболее предпочтительном варианте может быть использована методика измерения /Ca2+/в в остеокластах в планшете с 96 лунками. Очищенные остеокласты высевают при высокой плотности в каждую ячейку планшета с 96 лунками, а затем нагружают подходящим флуорометрическим индикатором. Регистрируют флуоресценции каждой ячейки, используя флуорометр для прочтения планшетов. Этот способ может быть полностью автоматизирован с использованием роботов, и можно скринировать с высоким расходом исходного вещества 50-100 соединений в неделю.
Примеры других Ca2+-рецепторов
Следующие примеры показывают, что поскольку имеются подтипы рецепторов для молекулярных лигандов, также должны иметься подтипы Ca2+-рецепторов, которые могут быть дифференциально подвергнуты действию лекарств. Ca2+-рецепторы паратироидных клеток восприимчивы к уровням внеклеточного Ca2+ около 1,5 мМ, тогда как Ca2+-рецептор на остеокласте отвечает на уровни около 10 мМ /фиг. 22/. Неомицин или спермин, которые активируют Ca2+-рецептор паратироидной клетки, не действуют на Ca2+-рецепторы на C-клетках или остеокластах /фиг. 21 и 23/. Эти данные представляют собой первое доказательство для фармакологически различных подтипов Ca2+-рецепторов и эти данные используют для конструирования и разработки лекарств, которые действуют селективно на конкретный тип Ca2+-рецептора. В действительности, испытания ведущих молекул демонстрируют такие специфические для клеток эффекты. Например, NPS 449, который вызывает повышение /Ca2+/в в остеокластах, не оказывает влияния на /Ca2+/в в паратироидных клетках. Наоборот, NPS 447, который активирует Ca2+-рецептор паратироидной клетки, является эффективным при активации Ca2+-рецептора остеокласта только при концентрациях в 10 раз больших. Наконец, агатоксин 489, хотя не является очень мощным при активации Ca2+-рецептора C-клетки /ЭК50 = 150 μМ/, является достаточно мощным активатором Ca2+-рецептора паратироидной клетки /ЭК50 = 3 μМ/. Ведущие молекулы, разработанные в настоящее время, будут селективно воздействовать на активность Ca2+-чувствительных клеток определенного типа in vivo.
Лекарства с меньшей специфичностью необязательно будут терапевтически нежелательными. Так, снижение остеокластной активности и стимулирование секреции кальцитонина представляет собой две различные попытки ингибирования костной резорбции. Лекарства, мишенью которых являются Ca2+-рецепторы обеих этих клеток, могут быть очень эффективными при лечении остеопороза. Поскольку ПТГ также включен в регулирование костного метаболизма, лекарства, действующие на Ca2+-рецептор паратироидной клетки, также могут быть полезными при лечении и/или профилактике остеопороза.
Результаты некоторых тест-молекул показаны ниже. В табл. 6 приведена сравнительная активность кальцимиметических молекул. Бычьи паратироидные клетки и C-клетки /гМТС 6-23 клетки/ нагружают fura-2, и остеокласты крыс indo-1 и определяют мощность указанных молекул по мобилизации внутриклеточного Ca2+ путем конструирования кумулятивных кривых концентрация - ответ. Молекулы, указанные как "неактивные", не изменяют /Ca2+/в при испытаниях при концентрации 1 μМ.
Пример 11: Ведущие молекулы для паратироидного Ca2+-рецептора.
Исследования структуры-активности с использованием полиаминов и арилалкиламинов привело к испытанию молекул, структурно близких к NPS 456. NPS 456 является мощным активатором Ca2+-рецептора паратироидных клеток. Эта молекула является достопримечательной, потому что она обладает только одним положительным зарядом и при этом является намного более мощной, чем многие многоосновные молекулы. Короткая /2 минуты/ предварительная обработка ФМА сдвигает кривую концентрация - ответ вправо для NPS 456. Это указывает, что NPS 456 работает по такому же механизму, использованному внеклеточным Ca2+. NPS 456 вызывает мобилизацию внутриклеточного Ca2+ в Xenopus ооцитах, экспрессирующих Ca2+-рецептор паратироидной клетки, что показывает прямое действие на Ca2+-рецептор /фиг. 33/. Кроме того, NPS 456 содержит хиральный углерод и, следовательно, существует в двух изомерных формах. Были синтезированы оба изомера и исследованы на активность R-изомер, NPS 447, является в 12 раз более мощным, чем S-изомер, NPS 448 /фиг. 28/. Это является первой демонстрацией того, что Ca2+-рецептор может распознать органическую молекулу стереоспецифическим образом.
Поскольку NPS 447 является структурно простой молекулой с селективным и мощным действием на Ca2+-рецептор паратироидной клетки, исследование структуры-активности для этой молекулы является простым. Целью этого исследования является генерация множества родственных молекул с различными характеристиками, из которых может быть выбран окончательный кандидат. Эти усилия уже выявили некоторые структурные области NPS 447, которые вносят вклад в активность и мощность. Например, новое соединение NPS 459 является аналогом NPS 447, которое является меньшим /MM < 240/ и близким по мощности
к родственному соединению /молекуле/, тогда как несколько других аналогов являются относительно неактивными. Наиболее интересные молекулы из этого проекта аналогов могут быть взяты в испытания in vivo на воздействие на секрецию ПТГ и уровней Ca2+ в сыворотке /см. примеры 15, 16, 17, 18 и 23/.
Новое соединение NPS 467 является даже меньшей молекулой, чем NPS 447, а первая является примерно в 3 раза более мощной, чем последняя при вызове повышения /Ca2+/в в паратироидных клетках. Подобно NPS 456 NPS 467 является рацемической смесью. Разделение NPS 467 на его энантиомеры обеспечивает изомер даже более высокой мощности, чем рацемическая смесь /см. пример 16/. Далее, исследования структуры-активности молекул, родственных NPS 447, NPS 467 и NPS 568 ожидаемо дали чистые изомеры с большей мощностью, чем эти молекулы в их рацемической форме.
Результаты, полученные с NPS 456 /фиг. 33/ показывают, что он вызывает колеблющееся повышение Cl--потока при концентрации 100 μМ. NPS 456 является наиболее мощной молекулой, активирующей Xenopus ооциты, экспрессирующие Ca2+-рецептор паратироидных клеток. Результаты, полученные в этой системе экспрессии с неомицином и NPS 456, показывают, что эти молекулы действуют непосредственно на Ca2+-рецептор.
Пример 12: Ведущие молекулы для Ca2+-рецептора остеокласта.
Стратегия, использованная для запуска механизма действия внеклеточного Ca2+ на остеокласт, была подобной стратегии, доказавшей эффективность в паратироидных клетках. Первые эксперименты исследовали влияние La3+ на /Ca2+/в в единичных остеокластах крыс, нагруженных флуорометрическим индикатором indo-1. Как описано выше, трехвалентные катионы, подобные La3+, являются непроникающими и блокируют приток Ca2+. Низкие микромолекулярные концентрации La3+ частично снижают вызванное внеклеточным Ca2+ повышение /Ca2+/в /фиг. 29/. Демонстрация La3+-устойчивого повышения /Ca2+/в обеспечивает доказательство мобилизации внутриклеточного Ca2+. Результаты этих экспериментов параллельны полученным в паратироидных клетках и предполагают, что подобные механизмы используются внеклеточным Ca2+ для регулирования /Ca2+/в в обоих типах клеток.
Другая серия экспериментов показывает, что внеклеточный Mn2+ вызывает кратковременное повышение /Ca2+/в /фиг. 30а/, которое существует в отсутствие внеклеточного Ca2+ /фиг. 30б/. Эти результаты также указывают на мобилизацию внутриклеточного Ca2+. Хотя Mn2+ может входить в некоторые клетки, маловероятно, что он сделает это в остеокласте, потому что Mn2+ подавляет флуоресценцию indo-1. Так, если Mn2+ проникает внутриклеточно, должно наблюдаться снижение, а не повышение флуоресцентного сигнала.
Результаты, полученные с различными двух- и трехвалентными катионами, все говорят о наличии Ca2+-рецептора на поверхности остеокласта, что сочетается с мобилизацией внутриклеточного Ca2+ и притоком внеклеточного Ca2+ через нечувствительные к напряжению каналы. Результаты показывают наличие генетического материала в человеческих остеокластах, который кодирует белок Ca2+-рецептора (см. ниже). Кратковременное повышение /Ca2+/в, полученное в результате мобилизации внутриклеточного Ca2+, является достаточным для ингибирования остеокластной костной резорбции in vitro. Итак, как и с паратироидными клетками, активация Ca2+-рецептора возможно является жизнеспособным средством ингибирования активности остеокластов.
NPS 449 в настоящее время является ведущей молекулой для кальцимиметических лекарств на этот рецептор. Он является маленькой молекулой /MM < 425/ и мобилизует внутриклеточный Ca2+ в остеокластах крыс с ЭК50 около 150 μМ /фиг. 31а и 31б/. Хотя мощность NPS 449 является относительно низкой, он имеет простую структуру с единственным положительным зарядом, и ожидается, что он обладает желаемыми фармакодинамическими и фармакокинетическими свойствами.
NPS 449 был исследован на его способность ингибировать костную резорбцию in vitro. Это было сделано с помощью морфометрического анализа образования ямок на тонких слоях бычьей кортикальной кости с использованием сканирующей электронной микроскопии. Остеокласты крыс инкубировали в течение 24 часов на костных пластинах в присутствии и в отсутствие различных концентраций NPS 449. NPS 449 вызывает зависящее от концентрации ингибирование костной резорбции с ИК50 10 μМ. Ожидаемые результаты обеспечиваются первой демонстрацией того, что молекулы, действующие на этот новый участок, могут ингибировать остеокластную костную резорбцию. Более мощные аналоги NPS 449 будут генерированы с использованием синтетической химии и будут испытаны и проанализированы с использованием описанных здесь способов.
Пример 13: Ведущие молекулы для Ca2+-рецептора C-клетки.
Активация Ca2+-рецептора C-клетки стимулирует секрецию кальцитонина, который затем действует на остеокласты, ингибируя костную резорбцию. Кальцимиметические лекарства, селективно действующие на C-клетки, являются полезными для лечения остеопороза.
Мобилизацию внутриклеточного Ca2+ используют в качестве функционального показателя активности Ca2+-рецептора. Усилия по скринингу в C-клетках облегчаются доступностью культивируемых клеточных линий, экспрессирующих C-клеточный фенотип /например, клетки медуллярной тироидной карциномы крыс; гМТС 6-23 клетки/. На начальной стадии отобрали три арилалкиламиновые молекулы. Две имеют природное происхождение /агатоксин 489 и агатоксин 505/, а другая /NPS 019/ является синтетическим аналогом агатоксина. Агатоксин 505, как было найдено, блокирует вызванное внеклеточным Ca2+ повышение /Ca2+/в с ИК50 3 μМ. Ингибирующее действие является результатом блокирования чувствительного к напряжению Ca2+ канала L-типа, имеющегося в этих клетках. Напротив, агатоксин 489, как было найдено, мобилизует внутриклеточный Ca2+ в гМТС клетках с ЭК50 150 μМ. Он является первой обнаруженной органической молекулой, которая, как было найдено, активирует Ca2+-рецептор C-клетки. Синтетический аналог, NPS 019, является даже более мощным и мобилизует внутриклеточный Ca2+ с ЭК50 5 μМ (фиг. 32). Существенным является то, что единственным структурным различием между NPS 019 и агатоксином 489 является наличие или отсутствие гидроксильной группы. Тот факт, что такие слабые различия в структуре сильно влияют на мощность молекул, указывает на структурно специфический участок связывания на Ca2+-рецепторе. Это, в свою очередь, предлагает путь, по которому могут быть разработаны очень мощные и селективные активаторы Ca2+-рецепторов.
NPS 019, который является маленькой молекулой /MM < 500/, является ведущей молекулой для разработки кальцимиметиков Ca2+-рецептора C-клетки и может быть испытан на его способность стимулировать секрецию кальцитонина in vitro. Последующее испытание in vivo затем определит способность этой молекулы стимулировать секрецию кальцитонина и ингибировать костную резорбцию. Эти исследования in vivo осуществляются на крысах. Результаты, полученные в этих исследованиях, которые, как ожидается, будут положительными, обеспечат первое доказательство, что маленькая органическая молекула, действующая на новый рецептор, может стимулировать секрецию кальцитонина и подавлять костную резорбцию.
Пример 14: Кальцилитическая активность NPS 021 на паратироидные клетки.
Соединение, которое считается кальцилитическим, должно блокировать действие внеклеточного Ca2+ или кальцимиметического соединения на чувствительную к Ca2+ клетку. Примером кальцилитического соединения является NPS 021, структура которого приведена на фиг. 1. В бычьих паратироидных клетках, нагруженных fura-2, NPS 021 блокирует повышение /Ca2+/в, вызванное внеклеточным Ca2+. ИК50 NPS 021 для блокирования этого ответа составляет около 200 àM и при концентрации около 500 àM повышение /Ca2+/в, вызванное внеклеточным Ca2+, отсутствует. Существенно, что сам NPS 021 не вызывает какого-либо изменения /Ca2+/в при испытаниях при низких /Ca2+/ /0,5 мМ; фиг. 37/. Ga3+ также является кальцилитиком к Xenopus ооцитам, экспрессирующим клонированный Ca2+-рецептор: сам Ga3+ не оказывает воздействия на Cl--потоки, активированные Gd3+, кальцимиметиком, но предварительная обработка Ga3+ блокирует действие Gd3+.
Пример 15: NPS 467 снижает сывороточный ионизированный кальций.
Соединения, показавшие активацию Ca2+-рецептора бычьей паратироидной клетки in vitro, были испытаны на гипокальцимиметическую активность in vivo. Самцов крыс Спраг-Доули /200 г/ выдерживали на низкокальциевой диете в течение недели перед получением испытуемого вещества или носителя в качестве контроля. Собирают кровь из хвостовой вены через 3 часа после интраперитонеального введения NPS 467. Измеряют ионизированный Ca2+ в цельной крови или в сыворотке на Циба-Корнинг 634 анализаторе в соответствии с инструкциями, приложенными к прибору. Измеряют суммарный сывороточный кальций, альбумин и фосфат по хорошо известным на данном уровне техники методикам.
NPS 467 вызывает зависящее от дозы снижение сывороточного Ca2+ или содержания Ca2+ в цельной крови /фиг. 38/. Падение Ca2+ в крови в это время было параллельным пропорциональному падению уровней суммарного кальция крови. Не имеется изменений уровней сывороточного альбумина или фосфата при любой исследованной дозе. При предварительных исследованиях NPS 467 в дозах, эффективных для понижения Ca2+ крови, вызывает зависящее от дозы снижение уровней ПТГ в кровотоке /фиг. 39/. Гипокальциемическое действие NPS 467 является максимальным в течение трех часов и возвращается к контрольному уровню через 24 часа /фиг. 40/.
NPS 467 (см. пример 16) также является эффективным при понижении сывороточного ионизированного Ca2+ у крыс, выдерживаемых на нормальной, насыщенной кальцием диете. Единственная доза NPS R-467 /10 мг/кг и.п./ вызывает быстрое падение уровней сывороточного ионизированного Ca2+, который является максимальным в течение 1 часа /22% снижения от контрольного уровня/ и остается пониженным до или вблизи этого уровня в течение времени до 6 часов.
Пример 16: NPS 467 снижает сывороточный ионизированный кальций стереоспецифическим образом.
NPS 467 является рацемической смесью. Разрешение NPS 467 на его энантиомеры достигается разделением на хиральной колонке. R-изомер является примерно в 100 раз более мощным, чем S-изомер при активации Ca2+-рецептора бычьих паратироидных клеток in vitro, как оценено по способности энантиомеров вызывать повышение /Ca2+/в в паратироидных клетках /фиг. 41/. Подобным образом, такое же разрешение новых соединений NPS 568 на его энантиомеры показывает, что R-изомер является в 40 раз более мощным, чем S-изомер при вызывании мобилизации внутриклеточного Ca2+ в бычьих паратироидных клетках /см. табл. 6/.
Исследовали изомеры NPS 467 на их действие на сывороточный Ca2+, как в примере 15. В соответствии с результатами in vitro R-изомер NPS 467 является более мощным, чем S-изомер при понижении сывороточного Ca2+ in vivo /фиг. 42; каждое соединение было испытано при концентрации 5 мг/кг массы тела/.
Пример 17: NPS 467 снижает сывороточный ионизированный кальций у in vivo модели вторичного гиперпаратироидизма.
Приемлемой и широко используемой моделью на животном вторичного гиперпаратироидизма, возникающего при хронической почечной недостаточности, являются 5/6 нефрэктомизированные крысы. Животные, перенесшие такую хирургическую операцию, становятся сначала гипокальциемическими и для поддержания уровней сывороточного Ca2+ делается компенсирующая гиперплазия паратироидных желез и повышение уровней циркулирующего ПТГ. Самцы крыс Спраг-Доули /250 г/, перенесшие 5/6 нефрэктомию, оставлены для выздоровления на 2 недели. За это время они становятся нормокальцимиками /благодаря повышенным уровням сывороточного ПТГ/. Введение NPS R-467 /10 мг/кг и.п./ вызывает быстрое /в течение 2 часов/ падение уровней сывороточного ионизированного Ca2+ до 83% от контроля на модели животного с вторичным гиперпаратироидизмом. Это предполагает, что соединения этого сорта будут эффективно снижать секрецию ПТГ у пациентов с вторичным гиперпаратироидизмом и гиперпластичными паратироидными железами.
Пример 18: NPS 467 не может снизить уровни сывороточного ионизированного кальция у паратироидэктомизированных животных.
Для определения первичной ткани-мишени, на которую действует NPS 467, вызывая гипокальциемический ответ, паратироидные железы у крыс хирургически удалены. Животные, перенесшие тотальную паратироидэктомию, становятся гипокальцимиками и сильно зависят от диетического кальция для поддержания гомеостаза сывороточного Ca2+. Паратироидэктомизированные животные имеют уровни сывороточного ионизированного Ca2+ 0,92 мМ, которые постепенно падают до 0,76 мМ через 6 часов после еды. Введение единичной дозы NPS R-467 /10 мг/кг и. п. / не вызывает какого-либо изменения в уровнях сывороточного ионизированного Ca2+ в течение 6 часов. Эти результаты показывают, что интактные паратироидные железы требуются для гипокальциемического действия NPS R-467. Данные дополнительно показывают, что NPS R-467 может иметь мишенью паратироидные железы in vivo. Результаты прелагают путь, по которому NPS R-467 действует на Ca2+-рецептор паратироидной клетки in vivo, чтобы подавить секрецию ПТГ и в результате вызвать падение уровней сывороточного ионизированного Ca2+.
Пример 19: NPS 467 повышает внутриклеточный кальций в паратироидных железах человека.
Готовят диссоциированные паратироидные клетки из паратироидной аденомы, полученной хирургически путем от пациента с первичным гиперпаратироидизмом. Клетки нагружают fura-2 и измеряют /Ca2+/в, как описано выше. Как NPS R-467, так и NPS R-568 вызывают повышение, зависящее от концентрации, /Ca2+/в. ЭК50 для NPS R-467 b NPS R-568 составляют 20 и 3 μМ соответственно. Следовательно, оба эти соединения могут повышать /Ca2+/в в паратироидной человеческой ткани и, следовательно, можно ожидать снижения уровней сывороточного ПТГ и Ca2+ у пациентов с первичным гиперпаратироидизмом.
Пример 20: Механизм действия NPS 467 на кальциевый рецептор паратироидной клетки.
Используют дисссоциированные бычьи паратироидные клетки для дальнейшего изучения механизма действия NPS 467 на уровень рецептора. В присутствии 0,5 мМ внеклеточного Ca2+ NPS R-467 вызывает быстрое и кратковременное повышение /Ca2+/в, которое существует в присутствии 1 μМ La3+ и частично снижается при предварительной обработке ФМА /100 нМ за 2 минуты/. Все эти результаты согласуются с действием NPS R-467 на Ca2+-рецептор. Однако ответ цитозольного Ca2+ на NPS R-467 исчезает, когда паратироидные клетки суспендируют в не содержащем Ca2+ буфере. Это предполагает, что NPS R-467 сам не может вызывать мобилизации внутриклеточного Ca2+. Однако он вызывает ответы в паратироидных клетках и ооцитах, когда присутствует незначительное количество внеклеточного Ca2+. Это предполагает, что частичное занятие Ca2+-связывающих участков требуется от NPS R-467, чтобы вызывать ответ. Для проверки этой гипотезы паратироидные клетки суспендируют в не содержащем Ca2+ буфере и экспонируют при субмаксимальной концентрации неомицина. Неомицин используют потому, что он имитирует почти во всех отношениях эффекты внеклеточного Ca2+ на паратироидные клетки и на Xenopus ооциты, экспрессирующие Ca2+-рецептор паратироидной клетки. Добавление 10 àM неомицина само не вызывает повышения /Ca2+/в в этих условиях. Однако последующее добавление NPS R-467 /30 μМ/ теперь вызывает кратковременное повышение /Ca2+/в, которое из-за отсутствия внеклеточного Ca2+ должно вызываться мобилизацией внутриклеточного Ca2+. Когда клетки, промытые не содержащим Ca2+ буфером, экспонируют с 30 àM NPS R-467, не имеется повышения /Ca2+/в. Эта концентрация NPS R-467 является максимально эффективной для повышения /Ca2+/в при наличии внеклеточного Ca2+ /0,5 мМ/. Однако последующее добавление неомицина /10 μМ/ теперь вызывает кратковременное повышение /Ca2+/в . Возможно неомицин связывает тот же самый участок, что и внеклеточный Ca2+, и может функционально заменить его. Используя субмаксимальную концентрацию, которая сама не вызывает ответа, достигают частичного занятия Ca2+-связывающего участка и обеспечивают активацию Ca2+-рецептора NPS R-467.
Дополнительные исследования, кроме того, определяющие механизм действия NPS R-467, были проведены. Клетки снова суспендируют в не содержащем Ca2+ буфере, чтобы обеспечить, чтобы любое наблюдаемое повышение /Ca2+/в было результатом мобилизации внутриклеточного Ca2+. Однако в этих экспериментах используют максимально эффективную концентрацию /100 μМ/ неомицина. В отсутствие внеклеточного Ca2+ 100 μМ неомицина вызывает быстрое и кратковременное повышение /Ca2+/в. Последующее добавление 30 μМ NPS R-467 не вызывает повышения /Ca2+/в. В сходном эксперименте прибавляют 30 μМ NPS R-467 перед 100 μМ неомицина. Как ожидалось, NPS R-467 не вызывает какого-либо повышения /Ca2+/в. Однако он не влияет на повышение /Ca2+/, вызванное последующим добавлением 100 μМ неомицина. Эти результаты, полученные с максимально эффективными концентрациями NPS R-467 и неомицина, подтверждают, что эти два соединения действуют не на один и тот же участок. Далее, результаты могут быть в достаточной мере объяснены постулированием двух различных центров на Ca2+-рецепторе, один из которых связывает внеклеточный Ca2+ и неомицин, а другой связывает NPS R-467 и структурно родственные соединения /такие как NPS R-568/. Лиганд, связывающий с первым центром, может привести в результате к полной активации Ca2+-рецептора, тогда как лиганд, связывающий последний, может только встретиться и/или быть функционально релевантным, когда центр связывания внеклеточного Ca2+ занят до некоторой до сих пор еще не определенной степени. Возможно, что лиганд, связывающий с центром связывания внеклеточного Ca2+, подвергается действию ранее закрытым центром связывания NPS R-467. Возможно, что центр связывания NPS R-467 является аллостерическим участком, который повышает активацию рецептора в ответ на связывание лиганда у центра связывания внеклеточного Ca2+.
Данные показывают, что Ca2+-рецептор паратироидной клетки обладает по крайней мере двумя отдельными центрами для органических лигандов. Один центр связывает физиологический лиганд, внеклеточный Ca2+, и некоторые органические поликатионы, подобные неомицину. Связывание с таким центром приводит в результате к полной активации Ca2+-рецептора, повышению /Ca2+/в и ингибированию секреции ПТГ. NPS R-467 и NPS R-568 определяют ранее нераспознаваемый центр связывания на Ca2+-рецепторе. Связывание с этим центром может происходить только и/или являться результатом полной активации Ca2+-рецептора, когда центр связывания внеклеточного Ca2+ частично занят. Лиганды, действующие на любой центр, являются эффективными для снижения уровней сывороточного Ca2+ in vivo.
Аллостерический центр на кальциевом рецепторе паратироидной клетки
Кальцимиметические соединения, которые активируют кальциевый рецептор бычьей паратироидной клетки, такие как NPS R-467 и NPS R-568, не вызывают мобилизации внутриклеточного Ca2+ в отсутствие внеклеточного Ca2+. далее, они повышают чувствительность Ca2+-рецептора к активации внеклеточным Ca2+, вызывая, следовательно, сдвиг влево кривой концентрация - ответ для внеклеточного Ca2+. Благодаря этому маловероятно, чтобы они действовали на тот же центр рецептора, что и внеклеточный Ca2+. Напротив, органические и неорганические поликатионы вызывают мобилизацию внутриклеточного Ca2+ в отсутствие внеклеточного Ca2+ и, следовательно, возможно действуют на тот же самый центр, что и внеклеточный Ca2+. Соединения, подобные NPS R-568, по-видимому, действуют аллостерическим образом и их активность зависит от некоторого минимального уровня внеклеточного Ca2+. Это допускает, что требуется частичное занятие центра связывания внеклеточного Ca2+ на рецепторе для соединений, подобных NPS R-568, чтобы быть эффективными. Эта модель соответствует наблюдениям, описанным в примере 20.
Другие детали механизма действия NPS R-568 на Ca2+-рецептор паратироидной клетки, однако, более точно исследуются при изучении связывания, при котором оценивается специфическое связывание радиомеченого /используя 3H, например/ NPS R-568. Имеется несколько молекулярных механизмов, которые могут объяснить активность NPS R-568 на Ca2+-рецепторе паратироидной клетки. В одном механизме /модель 1/ NPS R-568 может связываться с Ca2+-рецептором в центре, который, когда занят, является недостаточным, чтобы функционально активировать рецептор. Активация встречается только, когда достигается некоторый уровень занятости центра/ов/ связывания внеклеточного Ca2+. В альтернативном механизме /модель 2/ занятость центра связывания внеклеточного Ca2+ может обнаружить скрытые центры связывания для таких соединений, как NPS R-568. Занятие этого скрытого центра NPS R-568 затем повышает сродство и/или эффективность связывания у центра внеклеточного Ca2+. Любой механизм включает формирование аллостерической активации Ca2+-рецептора таким соединением, как NPS R-568. Это не является единственными возможными механизмами, которые могут объяснить действие соединений, подобных NPS R-568, на Ca2+-рецептор паратироидной клетки. Другие механизмы действия могут быть предложены по результатам изучения связывания, описанным ниже.
Для дальнейшего исследования механизма действия соединений, подобных NPS R-568, на Ca2+-рецептор паратироидной клетки может быть осуществлено изучение связывания с использованием 3H-NPS R-568. Специфическое связывание 3H-NPS R-568 с интактными паратироидными клетками или мембранами, приготовленными из паратироидных клеток, сначала исследовали хорошо известными на данном уровне техники методиками. Затем были измерены кинетические параметры связывания как функция концентрации внеклеточного Ca2+. Scatchard анализ данных даст количество центров связывания и кажущееся сродство рецепторного центра с 3H-NPS R-568. Эти параметры затем исследовали как функцию изменений в уровне внеклеточного Ca2+ в буфере, использованном для анализа. Если модель 1 является правильной, тогда значительный уровень специфического связывания будет встречаться в отсутствие внеклеточного Ca2+. Большие изменения кинетических параметров связывания как функции уровня внеклеточного Ca2+ будут благоприятствовать модели 2. Ожидается, что различные другие неорганические и органические поликатионы, описанные выше в других примерах, будут вызывать подобные изменения параметров связывания 3H-NPS R-568, как это делает внеклеточный Ca2+. Это будет поддерживаться путем, которым поликатионы действуют на центр связывания внеклеточного Ca2+, который отличается от того, по которому связывается соединение, подобное NPS R-568.
Пример 21: Получение NPS 467.
В круглодонной колбе емкостью 250 мл смешивают 10,0 г /100 ммоль/ 3'-метоксиацетофенона и 13,5 г /100 ммоль/ 3-фенилпропиламина и обрабатывают 125 ммоль /35,5 г/ изопропоксида титана /IV/. Реакционную смесь перемешивают 30 минут при комнатной температуре в атмосфере азота. После этого времени прибавляют по каплям 6,3 /100 ммоль/ цианборгидрида натрия в 100 мл этанола в течение 2 минут. Реакционную смесь перемешивают при комнатной температуре в азоте в течение 16 часов. После этого времени реакционную смесь переносят в 2-литровую делительную воронку с 1,5 л этилового эфира и 0,5 л воды. Фазы уравновешивают и отделяют эфирный слой. Оставшуюся водную фазу тщательно экстрагируют четыре раза порциями по 1 л эфира. Объединяют промывки, сушат над безводным карбонатом калия и разгоняют, получая прозрачное светло-желтое масло.
ТСХ анализ этого материала на оксиде кремния с использованием хлороформа:метанола:изопропиламина /100:5:1/ показывает продукт с Rf 0,65 со следами двух исходных материалов с Rf 0,99 /3'-метоксиацетофенон/ и Rf 0,0 /3-фенилпропиламин/.
Реакционную смесь хроматографируют через оксид кремния /48 х 4,6 см/, используя градиент хлороформ-метанол-изопропиламин от /99:1:0,1/ до /90:10: 0,1/, получают 13,66 г очищенного NPS 467. Этот материал растворяют в гексане-изопропаноле /99: 1/, содержащем 0,1% диэтиламина, получают раствор с концентрацией 50 мг/мл. Хиральное разрешение осуществляют хроматографией 4 мл этого раствора /200 мг, максимум до достижения разделения/ через Хирацел /25 х 2 см/, используя 0,7% изопропиламина, 0,7% диэтиламина в гексане при 100 мл/мин, контролируя оптическую плотность при 260 нм. В этих условиях /с инъекциями 100 мг материал/ легко элюируемый изомер /NPS 467R/ начинает выходить из колонки через à26 мин, последний элюирующийся изомер /NPS 457S/ начинает выходить через 34 минуты. Разрешение при нулевой линии осуществляют в этих условиях. Каждый оптический изомер /свободное основание/ превращают в соответствующую солянокислую соль при растворении 3 г свободного основания в 100 мл этанола и обработке его 100 мл воды, содержащей 10 молярных эквивалентов HCl. Лиофилизация этого раствора дает белый твердый продукт.
NPS 568.
NPS 568 является структурным аналогом NPS 467, который является более мощным при вызывании повышения /Ca2+/в в бычьих и человеческих паратироидных клетках. Подобно NPS 467 действие NPS 568 является стереоспецифическим и R-изомер является более мощным энантиомером /см. табл. 6/, NPS R-568 в настоящее время является ведущим кальцимиметическим соединением с селективной активностью у Ca2+-рецептора паратироидной клетки. Он ведет себя, хотя и с большей мощностью, подобно NPS R-467, как описано в примерах выше. Так, NPS R-568 вызывает повышение /Ca2+/в в бычьих паратироидных клетках стереоспецифическим образом /см. табл. 6/. NPS R-568 не вызывает повышения /Ca2+/в в отсутствие внеклеточного Ca2+, но он усиливает ответы на внеклеточный Ca2+. NPS R-568 сдвигает кривую концентрация - ответ для внеклеточного Ca2+ влево.
Оральное введение NPS R-568 крысам вызывает зависящее от дозы снижение уровней сывороточного Ca2+ /ЭД50 = 7 мг/кг/. Гипокальциемический ответ, вызванный оральным введением NPS R-568, является быстрым вначале и параллельным снижению уровней сывороточного ПТГ. Гипокальциемический ответ, вызванный введением NPS R-568, только маргинально действует перед полной нефрэктомией. Однако NPS R-568 не вызывает гипокальциемического ответа у паратироидэктомизированных крыс. NPS R-568, следовательно, может быть селективно нацелен на Ca2+-рецептор паратироидной клетки in vivo и вызвать ингибирование секреции ПТГ. Снижение уровней сывороточного ПТГ вместе с результирующей гипокальциемией являются желательными терапевтическими эффектами в случаях гиперпаратироидизма. Синтез NPS R-568 приведен ниже.
Пример 22: Получение NPS 568.
NPS 568 получают с использованием методик, описанных в примере 21, заменив на эквивалентное количество 3-/2-хлорфенил/пропиламина 3-фенилпропиламин. Было найдено, что при перемешивании смеси 3'-метоксиацетофенона, 3-/2-хлорфенил/пропиламина и изопропоксида титана /IV/ в течение 5 часов перед обработкой Na CNBH3/ETOH приводит в результате к значительно более высокому выходу /98%/.
Пример 23: NPS 467 снижает сывороточный ионизированный кальций при оральном введении.
Крыс /самцов, Спраг-Доули, 250-300 г/ кормили стандартным крысиным кормом и выдерживали без еды в течение ночи перед экспериментом. Суспендировали NPS R-467 в кукурузном масле и вводили в виде единичной оральной дозы через gavage иглу. Три часа спустя отбирают образец крови из хвостовой вены и определяют уровень ионизированного Ca2+. На фиг. 44 показано, что NPS R-467 вызывает зависящее от дозы снижение уровней ионизированного Ca2+ в сыворотке при оральном введении.
Пример 24: Способ клонирования BoPCaRI.
Стратегию клонирования-экспрессии с использованием ооцитов Xenopus laevis используют для индентификации кДНК, кодирующей бычий тироидный кальциевый рецептор. Эти методики описаны здесь только вкратце, а более полное описание предшествует этому в разделах описания методик, которые могут быть использованы для клонирования дополнительных форм Ca2+-рецептора из других типов клеток. Обогащенную поли/A/+ РНК сначала готовят из бычьих паратироидных желез, используя экстракцию гуанидинийтиоцианатом, центрифугирование через CSCl и хроматографию на олиго/dT/целлюлозе. Инъекция полученной в результате поли/A/+-обогащенной РНК в ооциты /25-50 нг/ооцит/ придает чувствительность к повышенным внеклеточным концентрациям Ca2+ и трехвалентного катиона /1-100 μМ/ Gd3+, как описано здесь, так что два катиона вызывают активированный кальцием поток хлорида. Такие потоки не вызываются в контрольных яйцеклетках, инъецированных водой. Шпорцевые лягушки X. laevis были выбраны за счет количества даваемых ими ооцитов, показывающих: /i/ высокий уровень зрелости /а именно, стадия V, VI/; /ii/ высокую активность Cl--потоков, активированных Ca2+ ионофорами, подобными A23187; /iii/ высоким уровнем функциональной экспрессии Gd3+-индуцированных Cl--потоков при инъекции 25 нг/ооцит суммарной поли/A/+РНК, выделенной из бычьего паратироида. Затем мРНК подвергают фракционированию по размерам, используя препаративный электрофорез в агарозном геле в непрерывном потоке (Hediger M.A., Anal. Biochem. 159: 280-286 /1986/), чтобы получить фракции поли/A/+-мРНК, дополнительно обогащенные транскриптами, кодирующими Ca2+-рецептор. Пик активности (например, ооциты, инъецированные мРНК из этих фракций, показывают повышенную экспрессию Gd3+-активированных Cl--потоков) получают с интервалом размеров 4-5,5 kb. Используют мРНК для получения отобранной по размерам, направленной кДНК библиотеки в плазмиде pSPORTI, которая обогащена транскриптами полной длины. Затем синтезируют смысловые комплементарные РНК (кДНК) из вставок ДНК, собранных из 350-500 независимых клонов из этой библиотеки, и инъецируют в ооциты, наблюдают Gd3+-активированный Cl--потоки после инъекции РНК с одного фильтра, содержащего 350 колоний. Получение и инъекция кРНК из последовательно уменьшающихся пулов клонов приводит к выделению единственного клона (BoPCaR I) со вставкой кДНК 5,3 kb, которая экспрессирует сильно повышенную Ca2+-рецепторную активность после инъекции кРНК в ооциты. Плазмиду, содержащую BoPCaRI кДНК (см. плазмиду, фиг. 45; рестрикционную карту, фиг. 46; и частичную нуклеотидную последовательность, фиг. 47) была депонирована в ATCC под номером хранения ATCC 75416.
BoPCaRI кДНК находится вне интервала размеров отобранной по размерам РНК, которая, как обнаружено, экспрессирует вызванную неомицином активность Cl--каналов в Xenopus ооцитах. Это согласуется с возможностью, что различные изоформы или множественные гены могут маскировать другие члены семейства генов Ca2+-рецепторов.
Некоторые фармакологические и биохимические критерии были использованы для идентификации этого клона как кодирующего bona fide бычий паратироидный Ca2+-рецептор. Ооциты, экспрессирующие клонированный рецептор, но не ооциты, инъецированные водой, отвечают на повышение концентраций внеклеточного Ca2+ /1,5-5 мМ/ или Gd3+ /20-600 μМ/ сильным увеличением Cl--потоков /до по крайней мере 1,8 микроампер/, что в несколько раз больше, чем наблюдаемое для поли/A+/-инъецированных ооцитов. Эти ответы заметно возрастают в течение периода времени от одного /1/ до четырех /4/ дней после инъекции яйцеклетки кРНК, приготовленной из BoPCaRI кДНК. Кроме того, интервалы концентраций двух катионов, вызывающих этот ответ, очень похожи на интервалы, приведенные ранее для действия на бычьи паратироидные клетки in vitro неомицина /20-100 μМ/, который является известным для близкой имитации эффектов Ca2+ на паратироидные клетки, полученные изменения в Cl--потоке в ооцитах по существу идентичны изменениям, полученным с Ca2+ или Gd3+, и они происходят в том же интервале концентраций, выше которых антибиотик moculates паратироидную функцию in vitro. Наконец, in vitro трансляция РНК, полученной из клона, приводит в результате к единственному главному белку на полиакриламидных гелях с молекулярной массой около 100 кДа, этот синтез был усилен включением dog панкреатических микросом, сопутствующих увеличению кажущейся молекулярной массы на 10-15%. Последнее предполагает, что клонированный рецептор взаимодействует интенсивно с мембранами, как можно было ожидать от целостного мембранного белкового рецептора, и гликозилирует в его нативной форме. Исследования с лектин конканавалином A указывают, что Ca2+-рецептор подобен гликопротеину. Так, фармакологические свойства клонированного рецептора, который экспрессирует с высокими уровнями в ооцитах, а также биохимические исследования, проведенные до настоящего времени, полностью соответствуют по идентичности бычьим паратироидным Ca2+ динамикам /как приведено в примерах по изменениям в Ca2+-активированных Cl--потоках с ооцитах/.
Диагностическое применение
NPS R-568 или другие соединения, активные на кальциевом рецепторе, могут быть использованы в качестве диагностического инструмента. Особенно полезным в качестве диагностического инструмента является фармацевтический препарат такого соединения. В одном примере фармацевтический препарат, содержащий кальцимиметическое соединение для паратироидных клеток, такое как NPS R-568, может быть введен орально или другим путем введения гиперкальциемическим пациентам с симптомами ментальной депрессии. Если эти симптомы возникают из основного гиперпаратироидного состояния, такого как первичный гиперпаратироидизм, тогда введение NPS R-568 или соединения, которое действует подобным образом, будет смягчать симптомы. Если симптомы не смягчаются, тогда ментальная депрессия является результатом какого-то другого патологического состояния, которое не является гиперпаратироидизмом. Итак, кальцимиметические соединения для паратироидных клеток могут быть использованы при дифференциации диагноза ментальной депрессии.
Симптомы и признаки, общие для гиперпаратироидизма и других заболеваний, также могут быть дифференциально диагностированы, описанным выше образом. Такие разделенные сигналы и симптомы включают, но не ограничиваются, гипертонию, мышечную слабость и общее ощущение болезни. Облегчение этих симптомов с последующим лечением кальцимиметическим соединением Ca2+-рецептора паратироидной клетки будет указывать, что проблема возникает в результате их гиперпаратироидизма.
В другом примере соединение, действующее как антагонист /кальцилитик/ у Ca2+-рецептора C-клетки, может быть введено, как описано выше, для диагностирования медуллярной тироидной карциномы. В этом случае введение кальцилитического соединения Ca2+-рецептора C-клетки будет снижать уровень сывороточного кальцитонина, который может быть легко измерен радиоиммуноанализом. Определенные симптомы, ассоциированные с медуллярной тироидной карциномой, такие как диаррея, также могут быть проконтролированы для определения, исчезают ли они или уменьшаются после введения кальцилитического соединения.
В третьем примере соединение, действующее как кальцимиметик на Ca2+-рецептор окологломерулярной клетки, может быть использовано при дифференциальном диагнозе гипертонии. В этом случае введение кальцимиметического соединения к Ca2+-рецептору окологломерулярных клеток может быть осуществлено, как описано выше. Снижение кровяного давления до нормального уровня будет происходить, если гипертония является результатом главным образом или исключительно повышенных уровней ренина, а не другого альтернативного патологического состояния.
В другом примере соединение, действующее как специфический кальцимиметик на Ca2+-рецептор остеокласта, может быть использовано в дифференциальной диагностике высоко- или низкоопрокидывающих форм остеопороза. В этом случае такое соединение может быть введено в подходящем фармацевтическом препарате и измерены уровни сывороточной щелочной фосфатазы, остеокальцина, пиридинолиновые и/или деоксипиридинолиновые сшивки, и/или некоторые другие предикативные маркеры костной резорбции и/или формирования, известными на данном уровне техники способами. Большое снижение одного или более из этих параметров будет указывать на высокоповорачивающий остеопороз, тогда как незначительное снижение или его отсутствие для этих параметров будет указывать на низкоповорачивающий остеопороз. Такая информация будет диктовать соответствующее лечение. Антирезорбтивные лекарства не должны быть единственной терапией для низкоповорачивающего остеопороза.
Эти примеры не являются исчерпывающими, но служат для иллюстрации, что специфические Ca2+-рецепторы могут быть мишенями для фармацевтических препаратов и что наблюдаемые эффекты от таких препаратов на функции организма и/или химических составляющих могут быть использованы диагностически. В общем кальцимиметические и кальцилитические соединения, которые действуют на Ca2+-рецепторы различных клеток, описанные выше, могут быть использованы для диагностики различных заболеваний, ассоциированных с клетками конкретного типа. Эти заболевания включают, но не ограничиваются ими, костные и минерально-связанные заболевания /как описано у Coe et al., Disorders of Bone and Mineral Metabolism, Raven Press, 1990/, почечные заболевания, эндокринные заболевания, рак, сердечно-сосудистые заболевания, неврологические заболевания, желудочно-кишечные заболевания и заболевания, ассоциированные с беременностью. Примеры заболеваний людей или заболеваний, в которых такие молекулы могут быть терапевтически эффективными, являются следующими: /1/ Ожидается, что кальцимиметики облегчают псориаз за счет снижения пролиферации анормальных клеток кожи. /2/ Поскольку Ca2+ блокирует действие вазопрессина на MTAL и кортикальные собирающие клетки, ожидается, что кальцимиметики снизят удерживание воды в состояниях избытка вазопрессина, таких как синдром несоответствующей секреции вазопрессина /АДН/. Наоборот, антагонисты рецепторов кальция, используемые в состояниях АДН дефицита, как ожидается, усиливают действие любого имеющегося АДН, такого как при частичном несахарном диабете. /3/ Кальцимиметики могут быть использованы для лечения гипертонии /а/ путем снижения секреции ренина, /б/ путем стимуляции продукции сосудорасширителей, таких как ПТГрП /ПТГ-родственный пептид/, сосудами гладких мышц. /4/ Кальцимиметики, как ожидается, увеличивают слипаемость тромбоцитов, это может быть полезным, когда счет тромбоцитов является низким. Наоборот, ожидается, что кальцилитики ингибируют функцию тромбоцитов в состояниях, когда имеется гиперкоагулируемость. /5/ Кальций промотирует дифференциацию клеток ободочной кишки и грудной железы. Как ожидается, кальцимиметики снижают опасность рака ободочной кишки или молочной железы. /6/ Кальций промотирует выделение мочевого кальция в MTAL. Ожидается, что кальцимиметики обладают полезным гипокальциемическим действием при лечении гиперкальциемических заболеваний. Ингибирующее действие кальцимиметиков на остеокласты и стимуляция ими секреции гипокальциемического пептида кальцитонина делает их возможно полезными при лечении гиперкальциемии и ее симптомов. Кальцимиметики также могут улучшать гипокальциемические симптомы путем активации кальциевых рецепторов. Наоборот, ожидается, что кальцилитики снижают выделение мочевого кальция и могут быть полезными при лечении почечных камней. В дополнение к этому кальций подавляет образование 1,25-диоксивитамина D в проксимальных почечных канальцах, и этот метаболит витамина D часто сверхпродуцирует почечные камни у пациентов и вносит вклад в их гиперкальциурию. Подавление образования 1,25-диоксивитамина D кальцимиметиком, как ожидается, будет полезным для лечения почечной кальциевой каменной болезни. /7/ Эндогенные амины могут воспроизвести симптомы у уремических пациентов кальцимиметического или литического действия. Ожидается, что кальцимиметики и/или кальцилитики улучшат эти симптомы. /8/ Некоторая часть почечной токсичности аминогликозидных антибиотиков может быть медиирована взаимодействием этих лекарств с почечными кальциевыми рецепторами. Ожидается, что наличие кальциевого рецептора сделает возможным легкое проведение скрининга лекарства при разработке новых лекарств этих классов для сведения к минимуму почечной токсичности. Кроме того, антагонист почечного кальциевого рецептора будет предотвращать или лечить эту почечную токсичность, если он имеет отношение к этому механизму. /9/ Некоторые из генетических компонентов кальций-зависимых расстройств, таких как остеопороз, почечные камни и гипертония, как ожидается, имеют отношение к наследственным проблемам с определенными формами рецептора. Теперь они могут быть изучены и проведен генетический скрининг/тестирование с использованием реагентов на основе рецептора. Человеческое заболевание, семейная кальциурическая гиперкальциемия, может быть благодаря дефекту рецептора кальция. Может быть проведено определяющее диагностическое разделение случаев promary наследственного (?) гиперпаратироидизма с помощью технологии на основе рецепторов. /10/ Кальциевые рецепторы имеются в плаценте и ожидается, что они влияют на расстройства плацентарной функции и перенос питательных веществ к растущему плоду.
Другие варианты находятся внутри формулы изобретения, приведенной в конце описания.
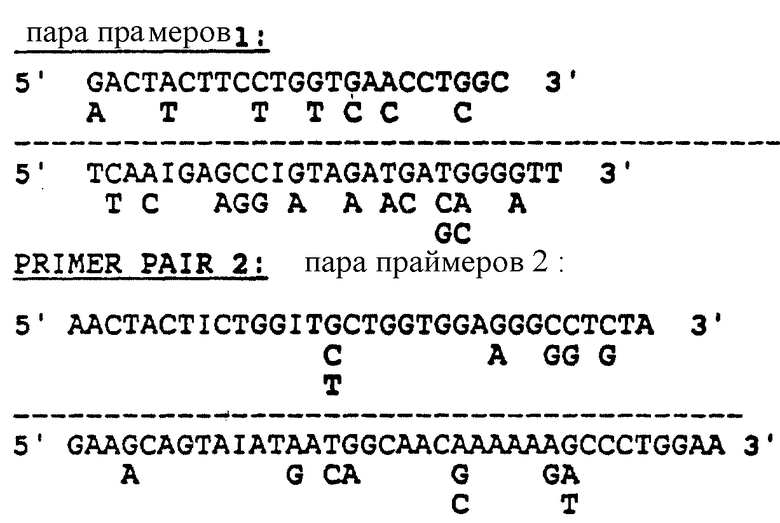



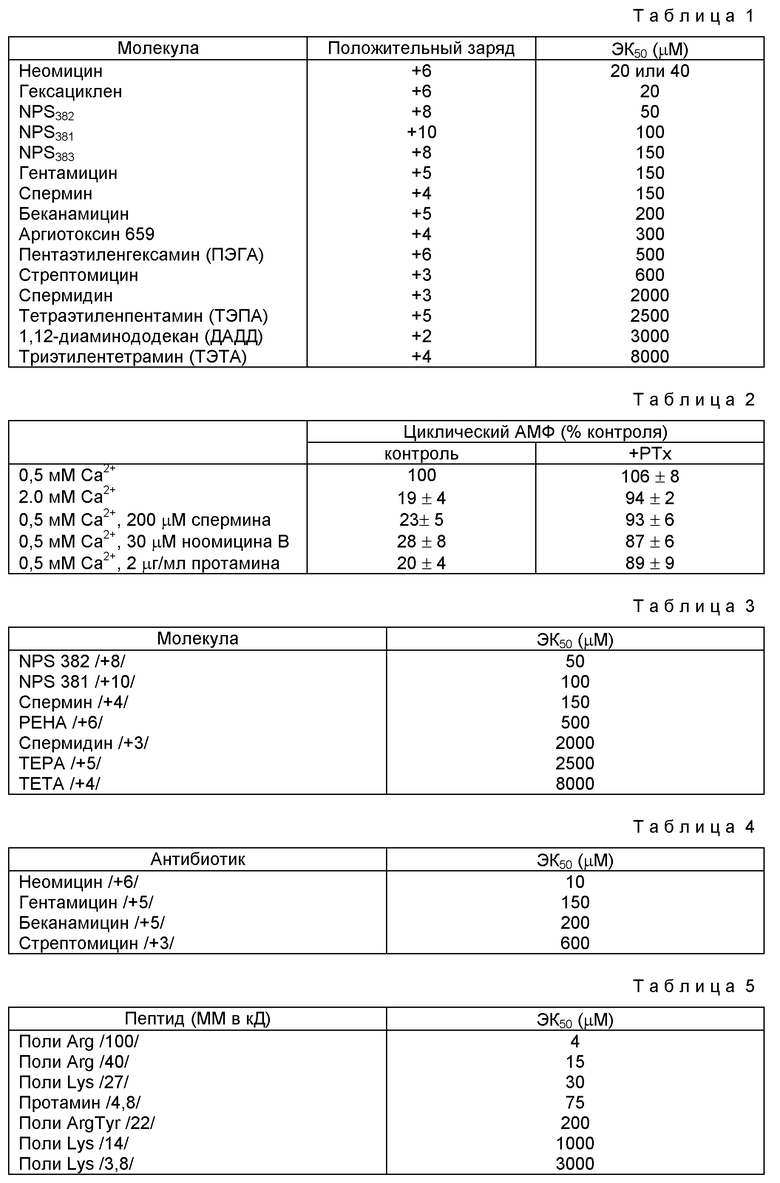
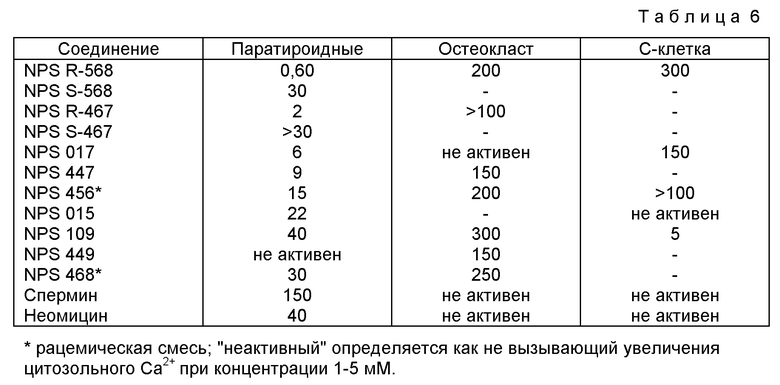
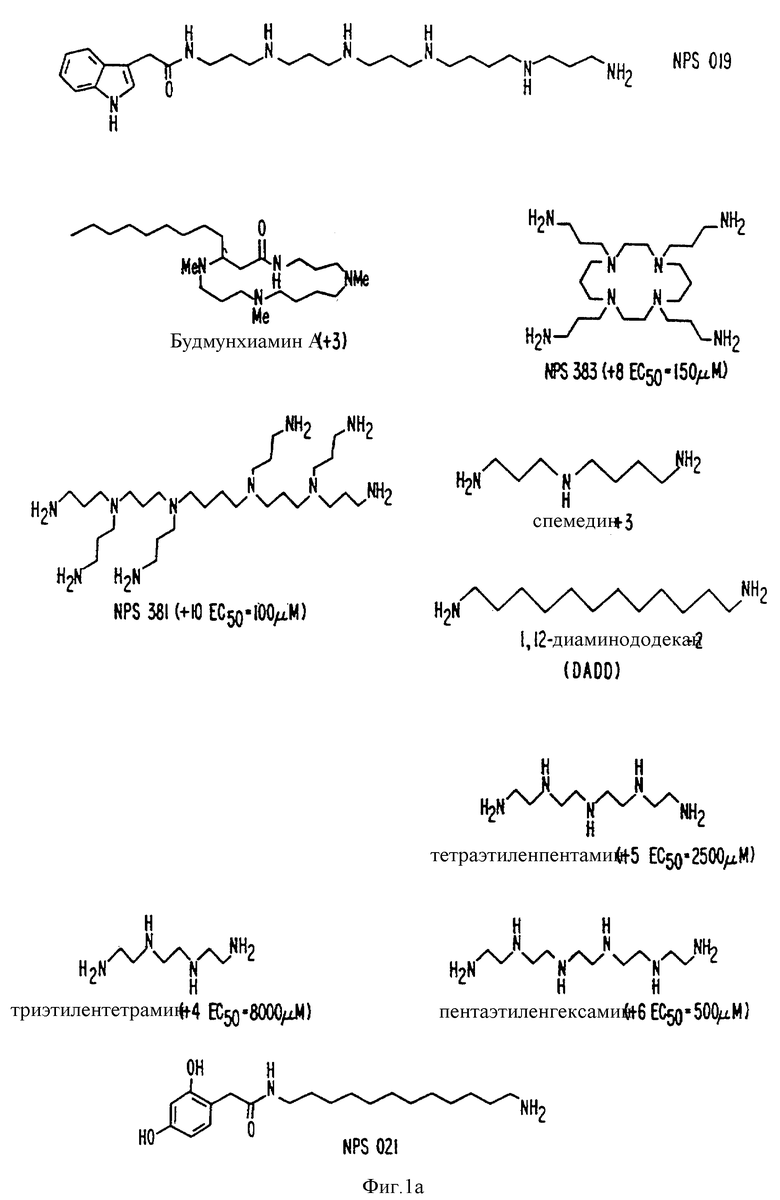

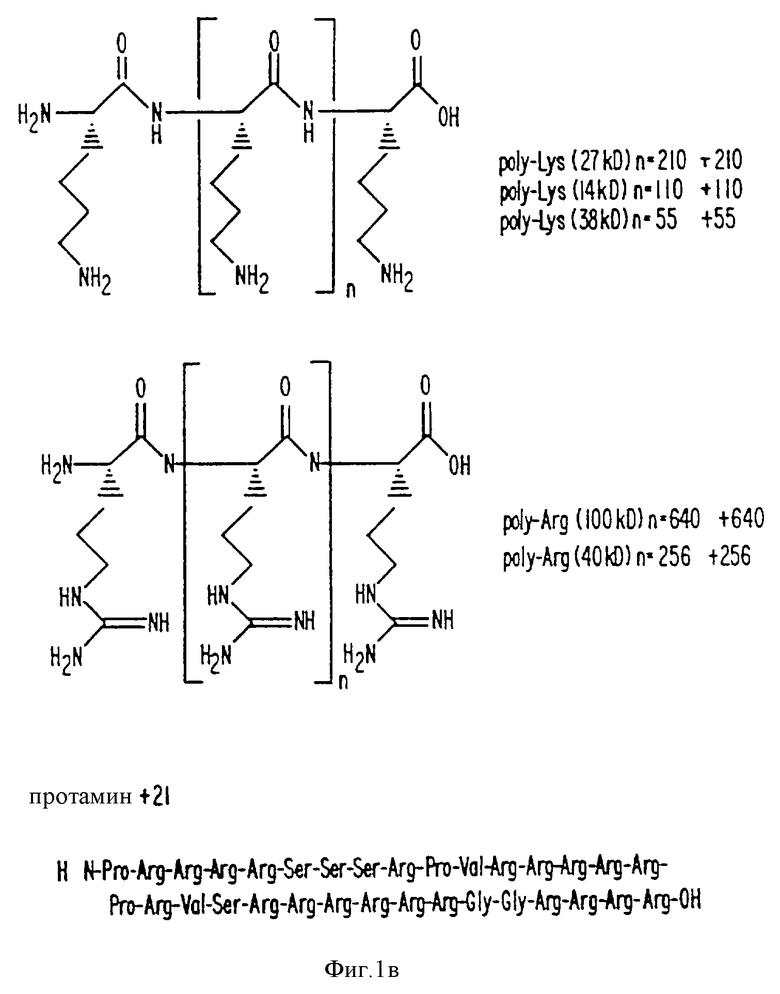

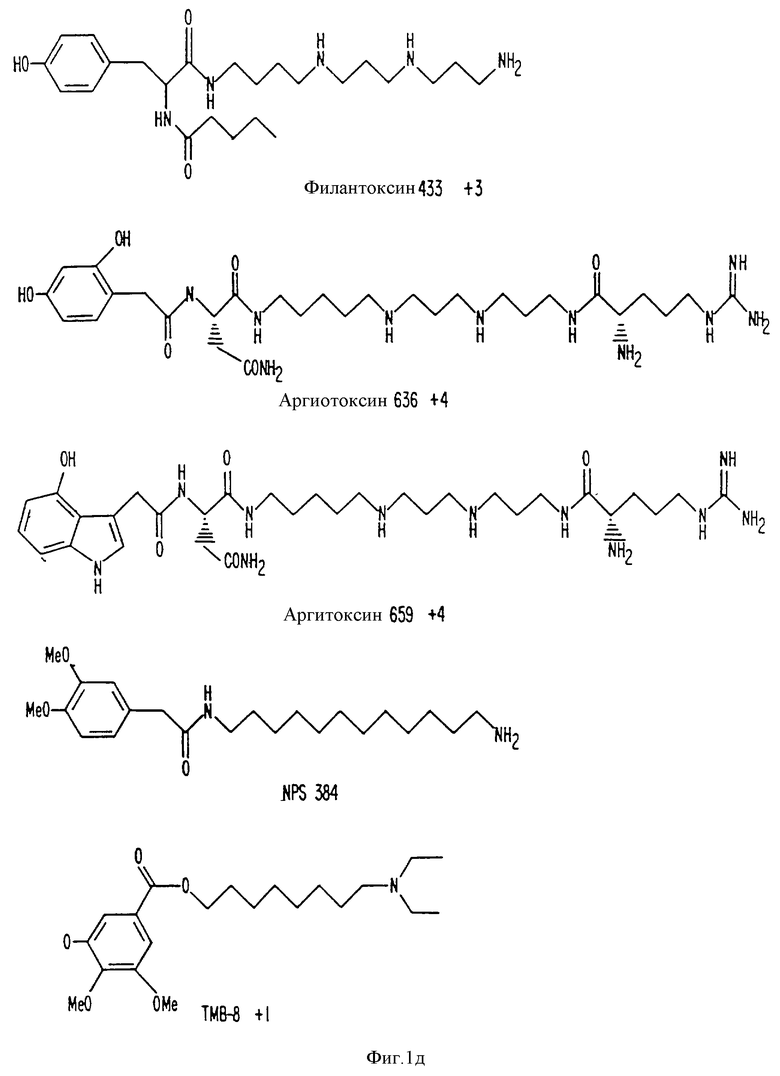

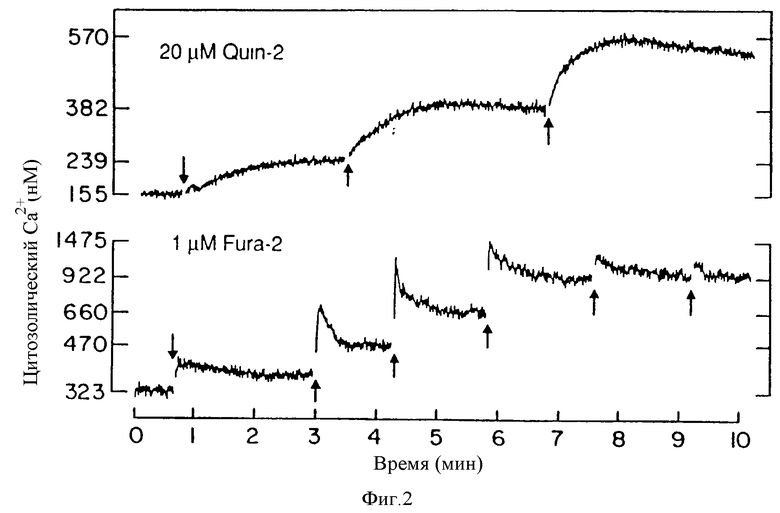

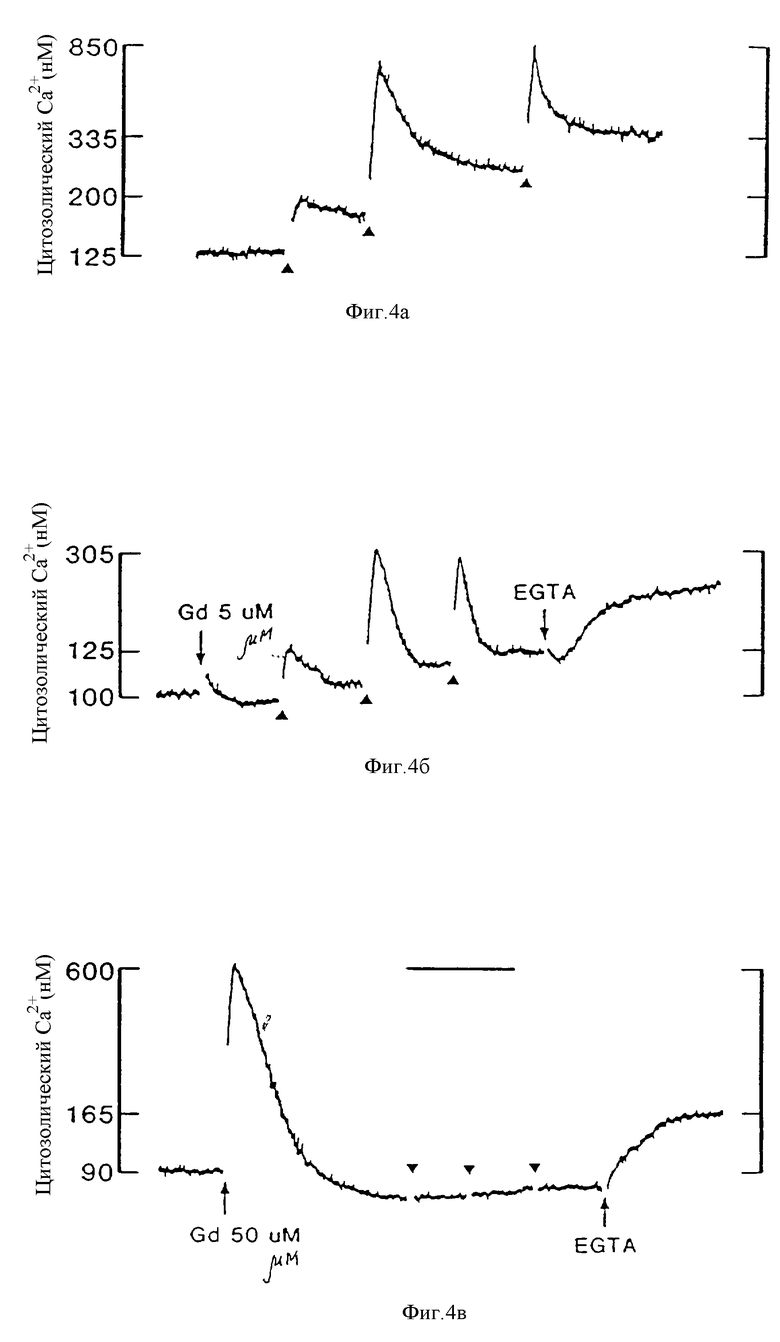


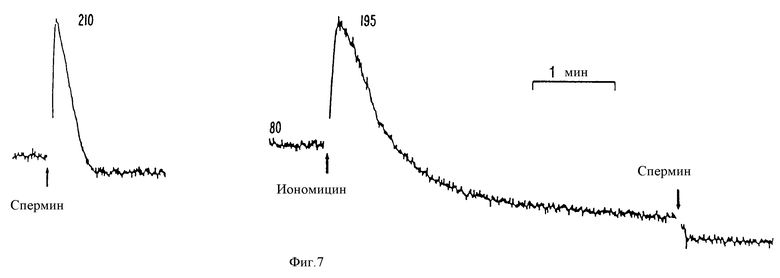

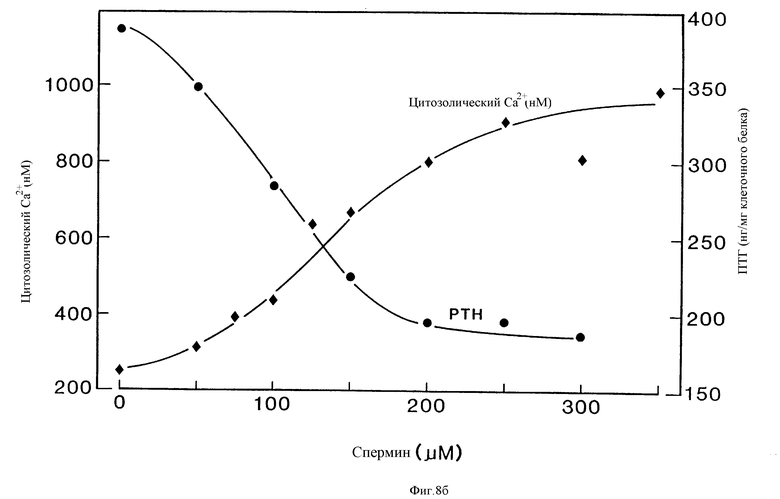

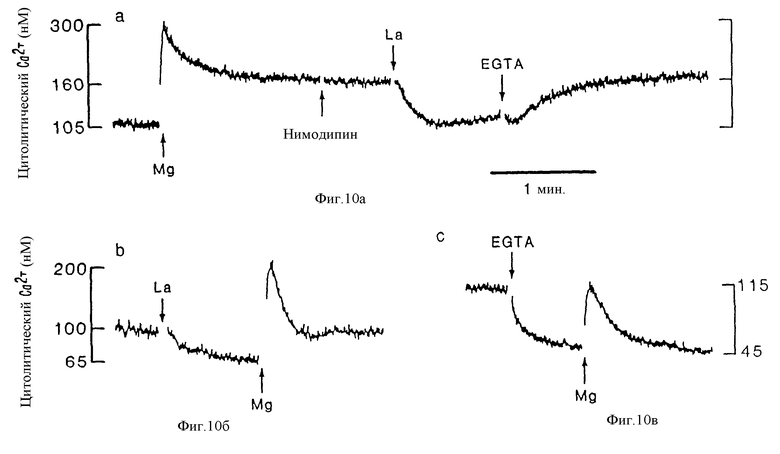


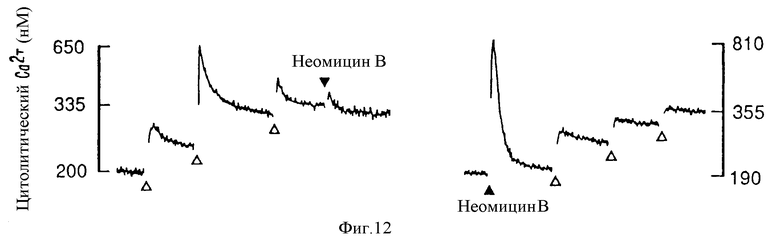
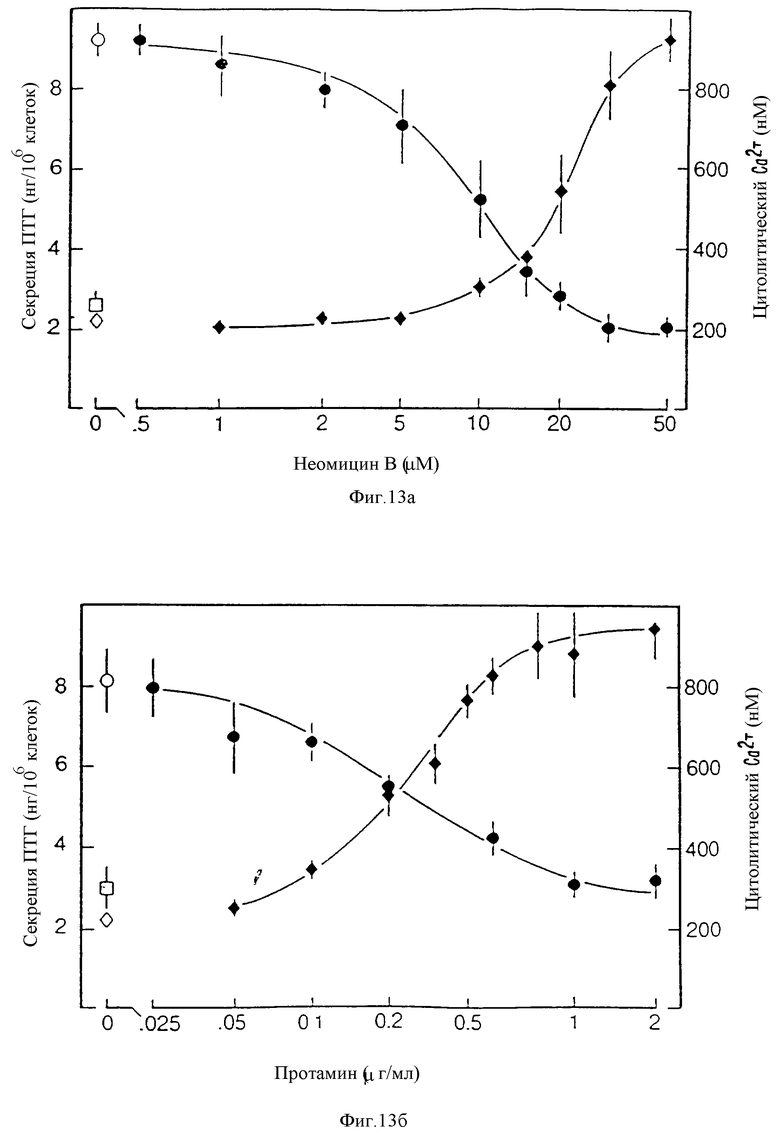
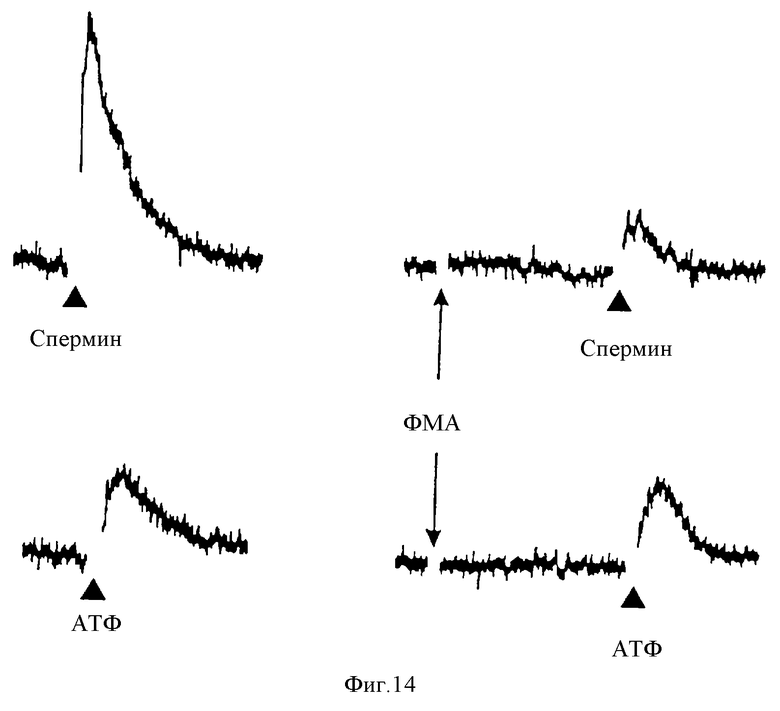


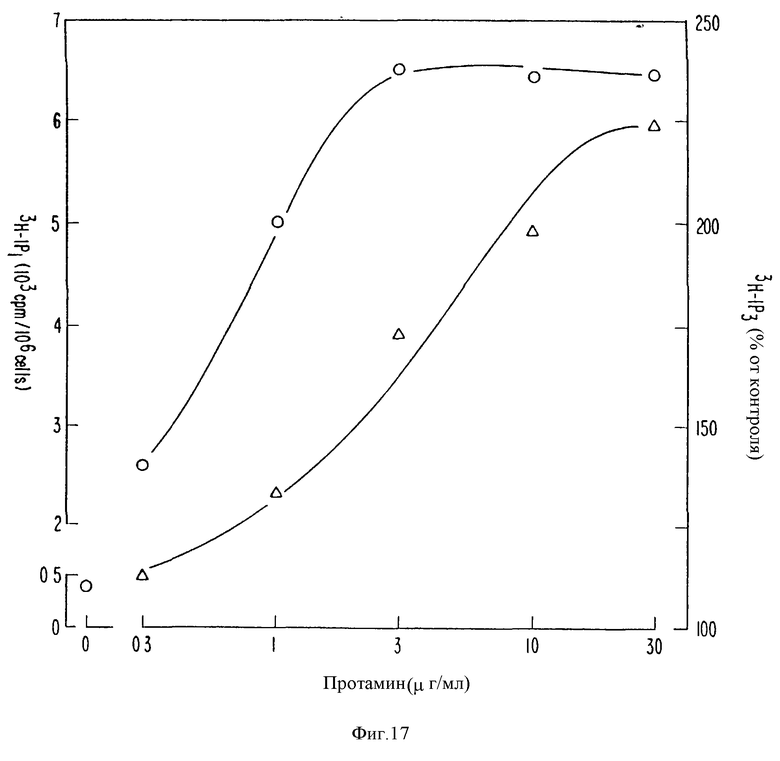
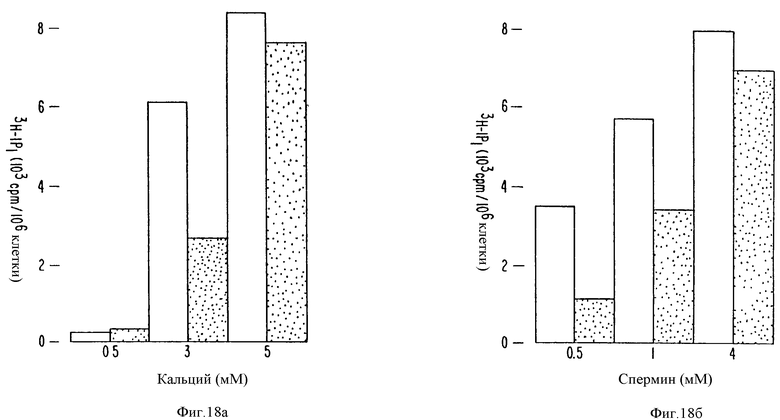
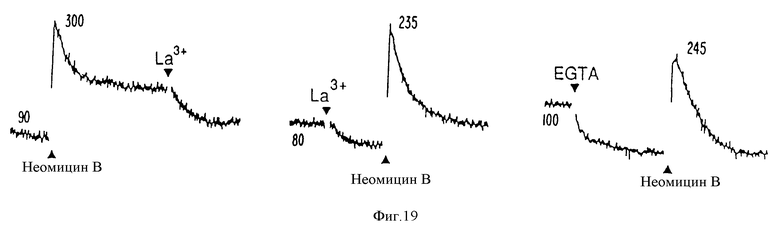
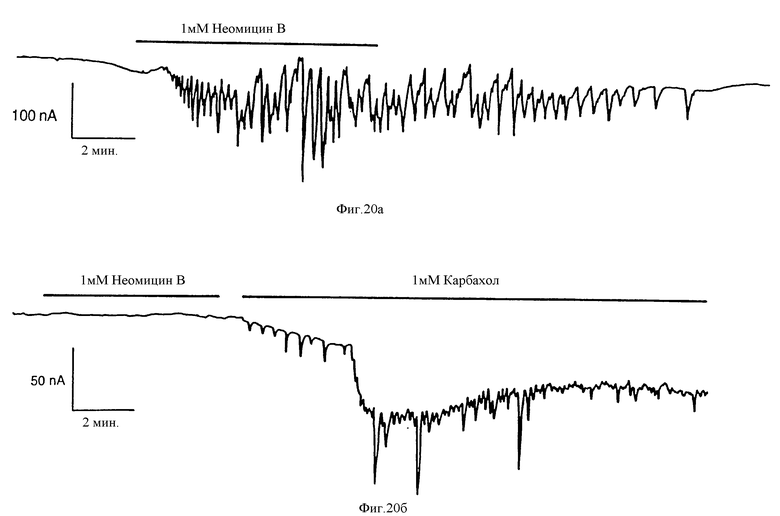
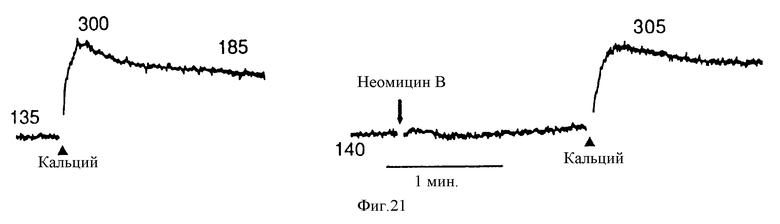

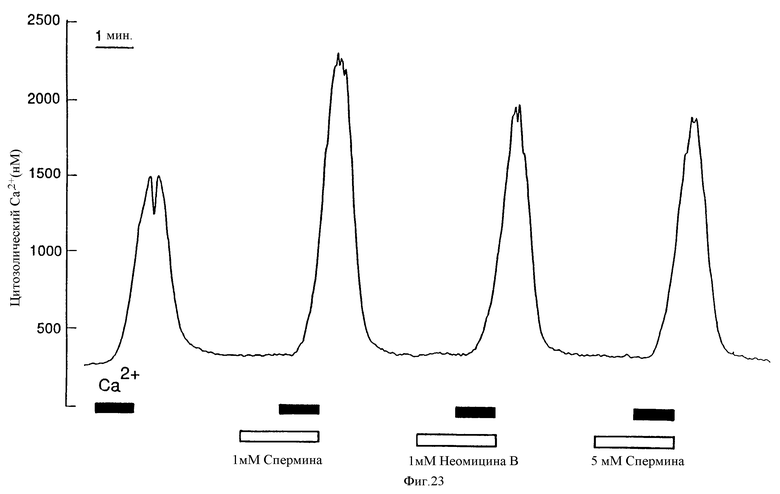
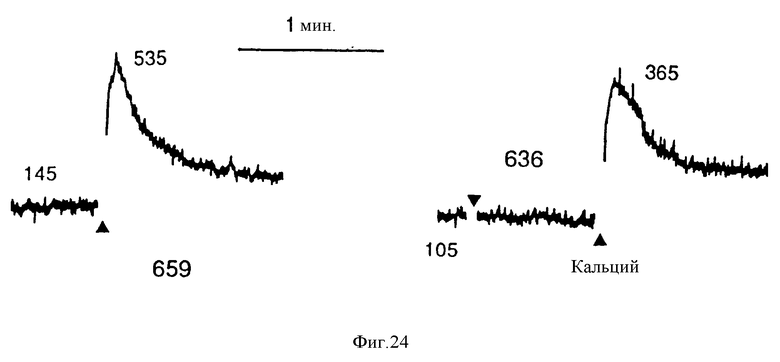
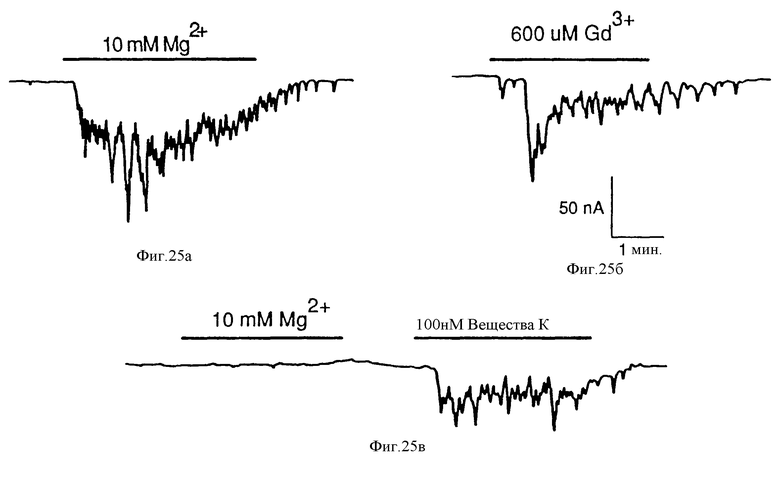
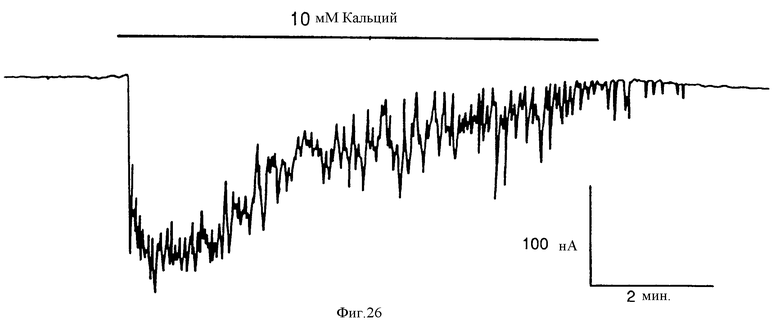

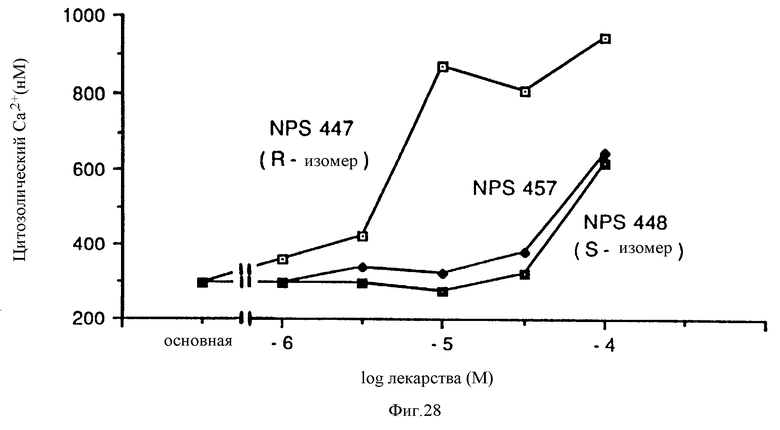

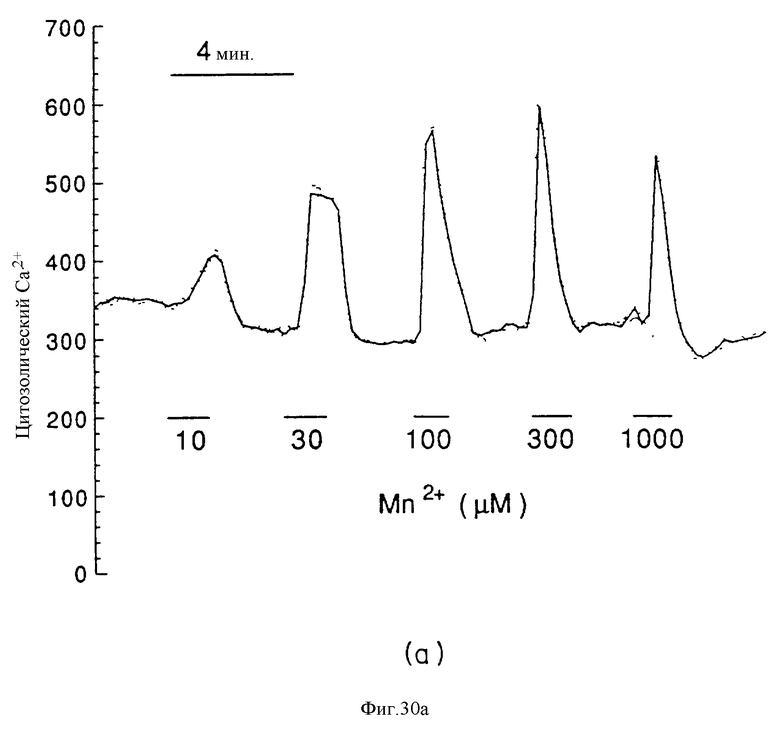
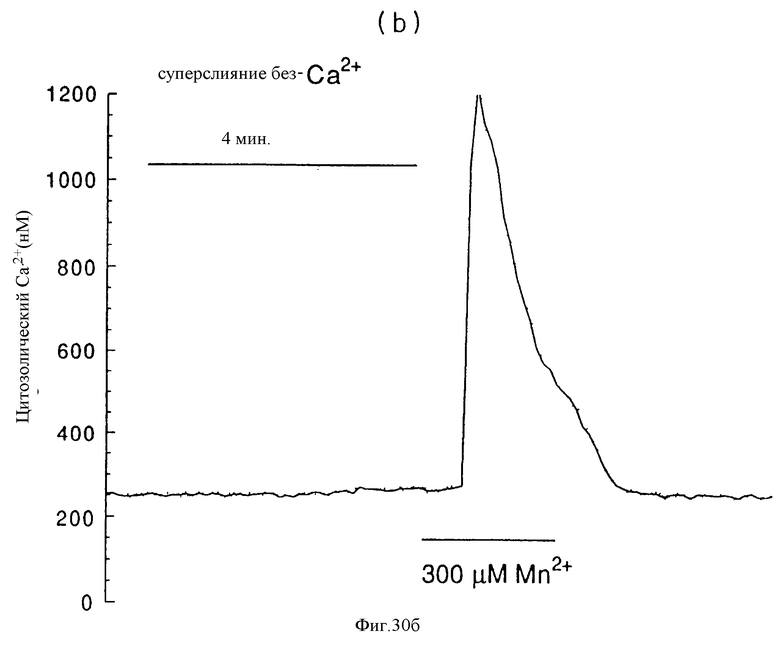
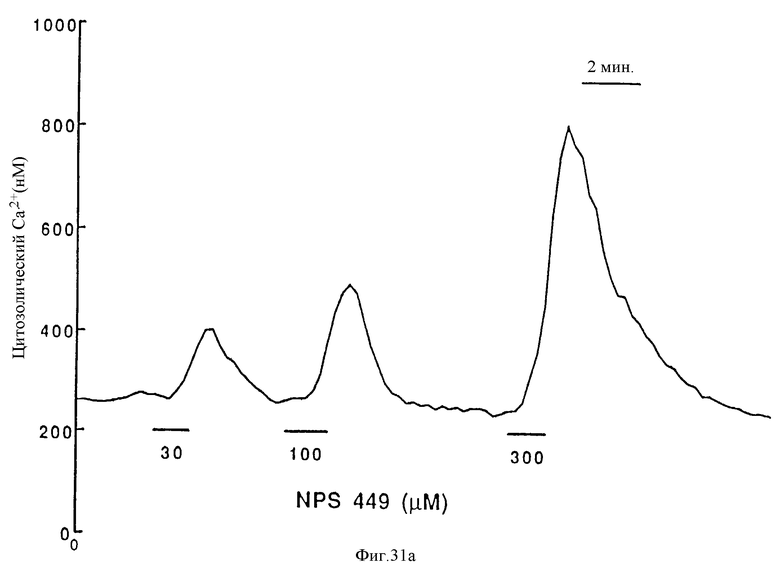
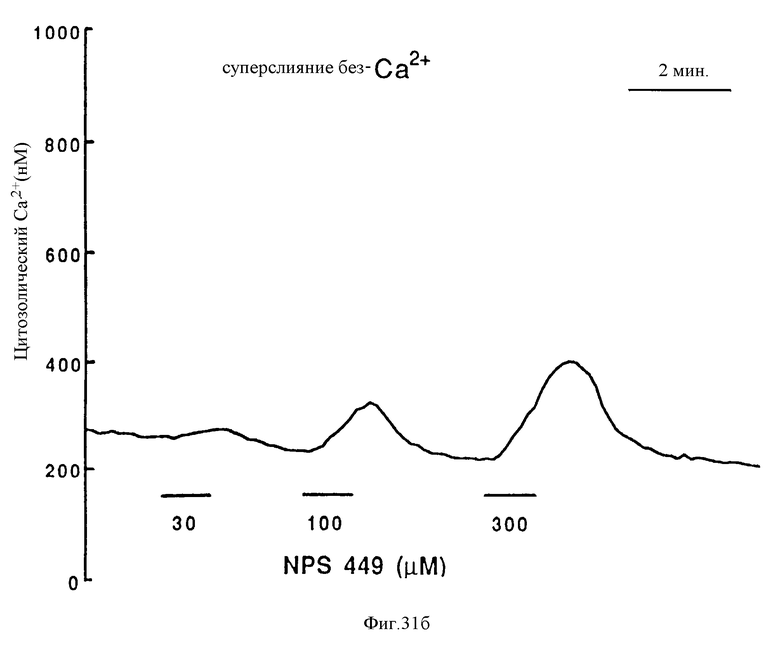
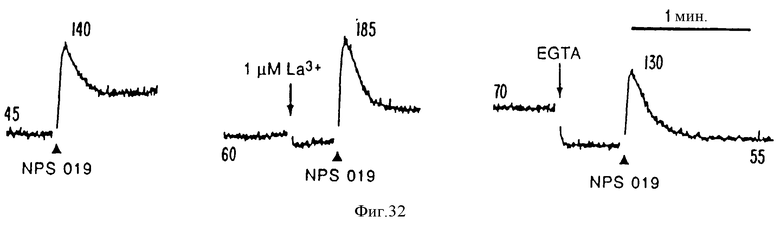

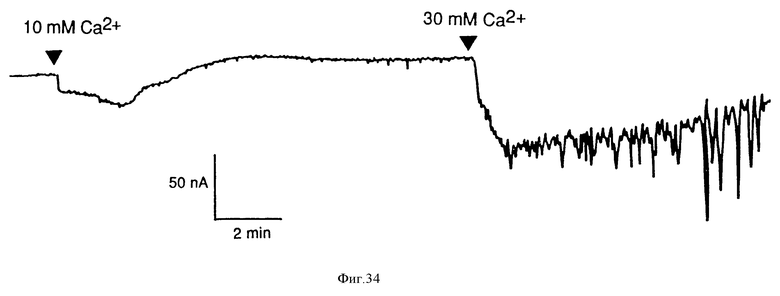

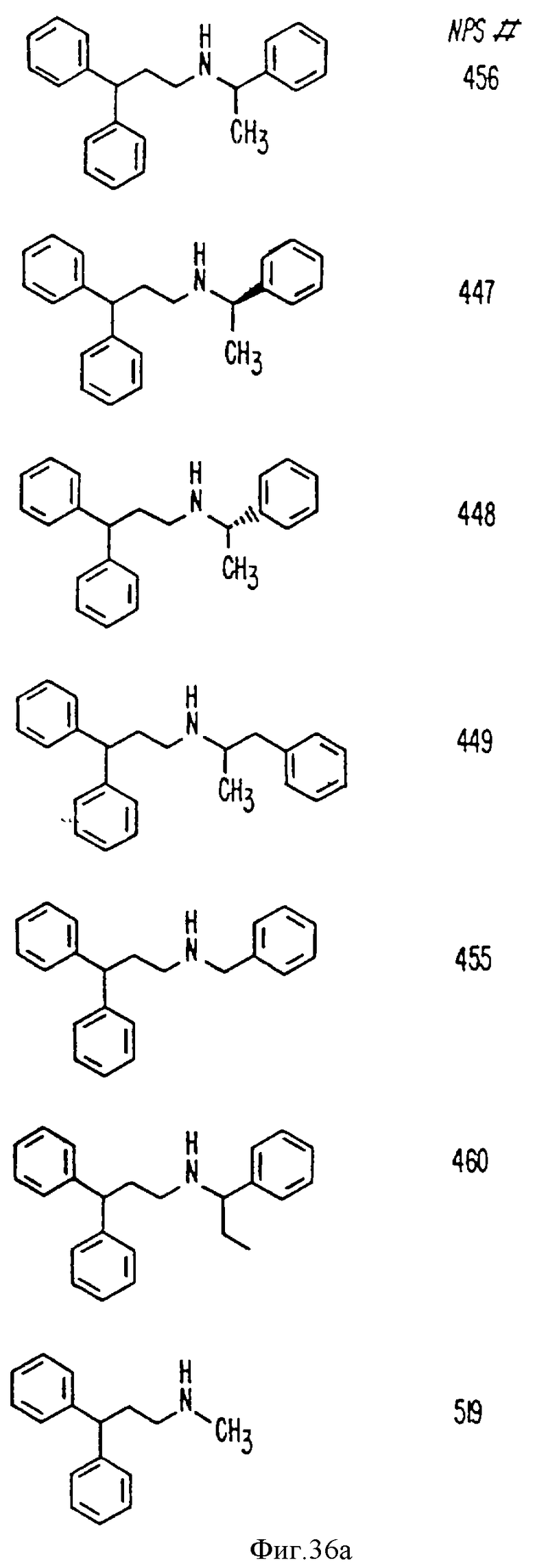
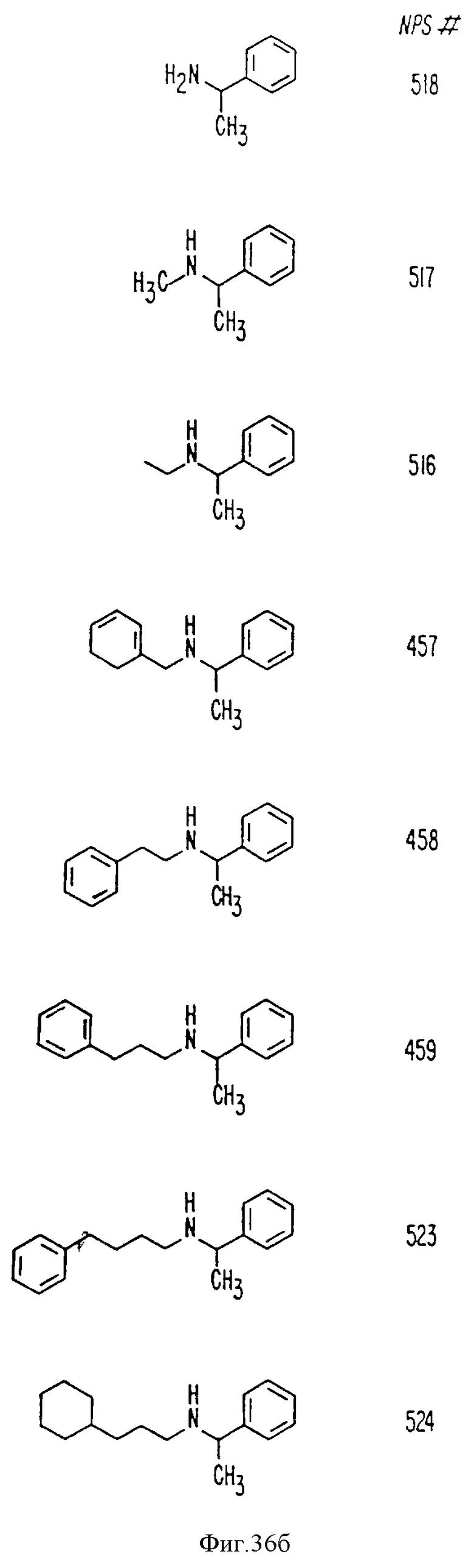

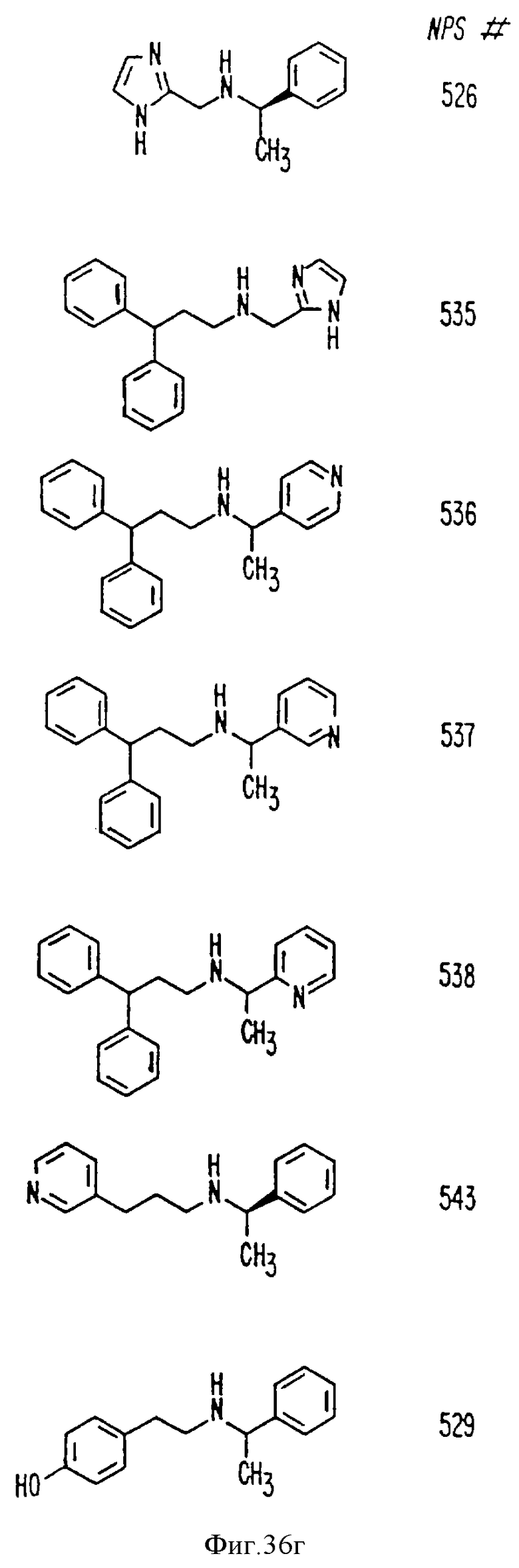
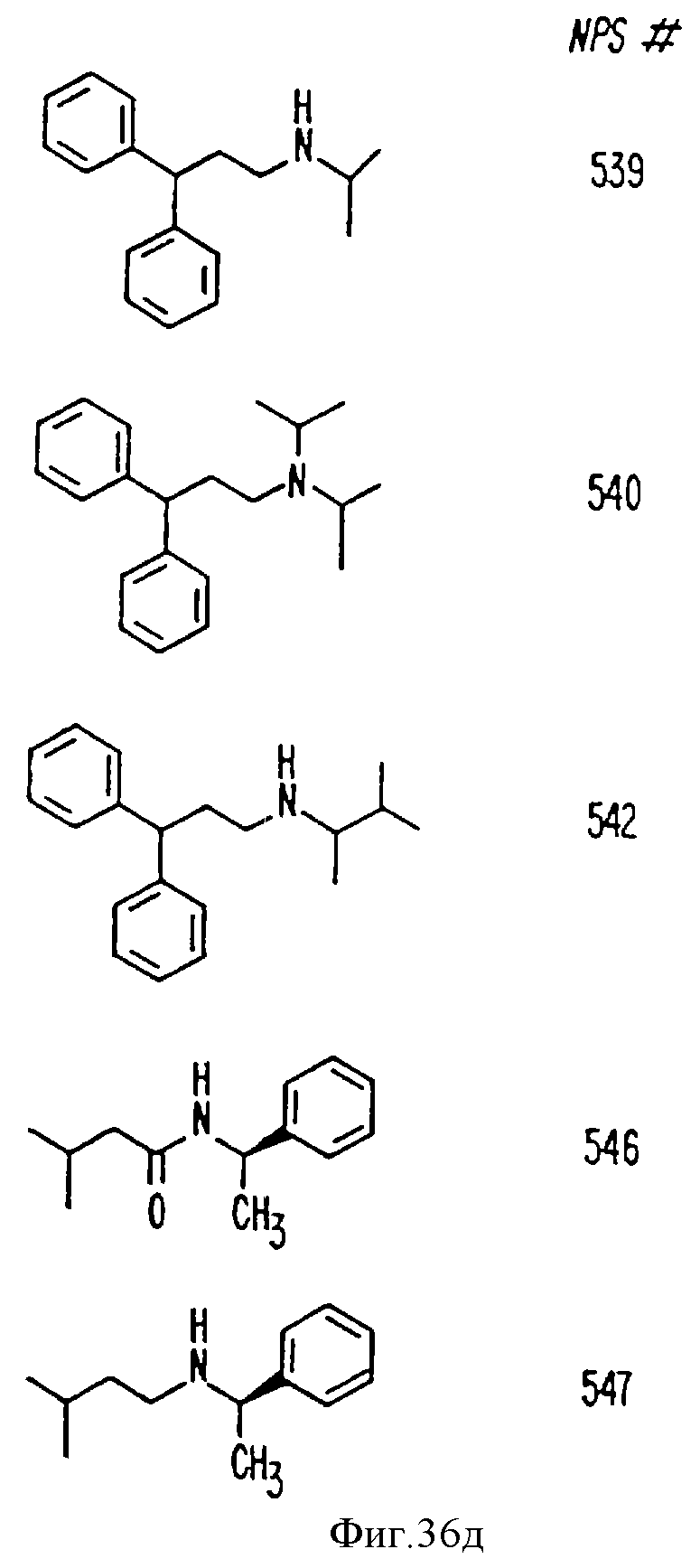
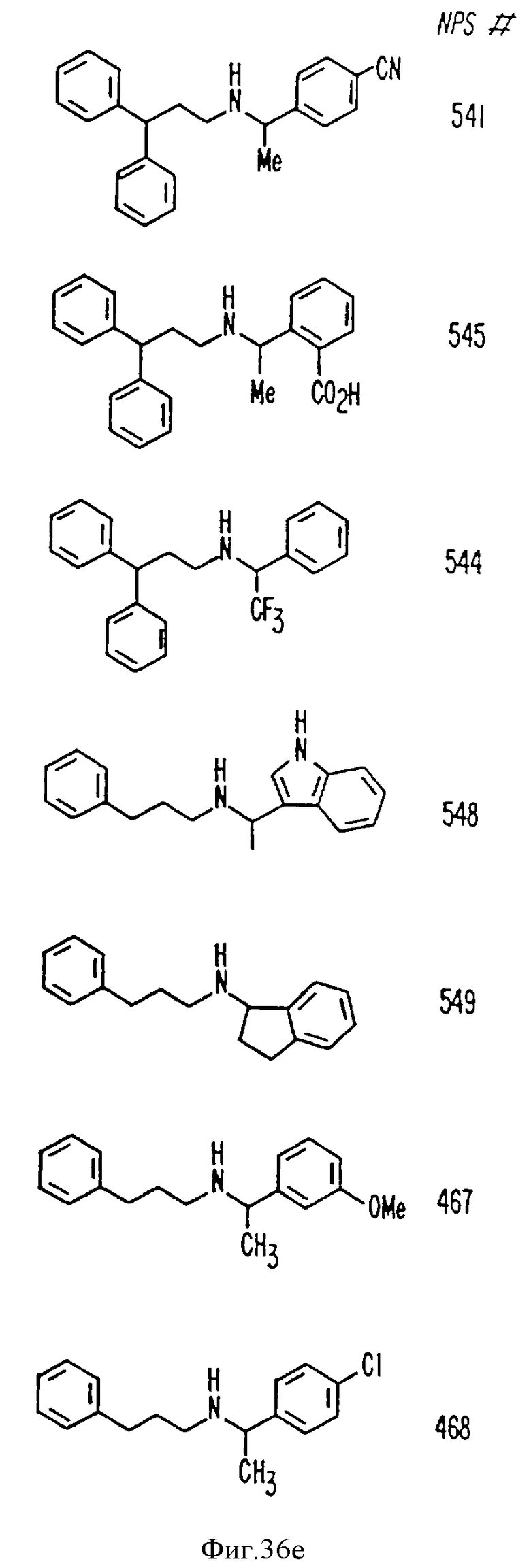
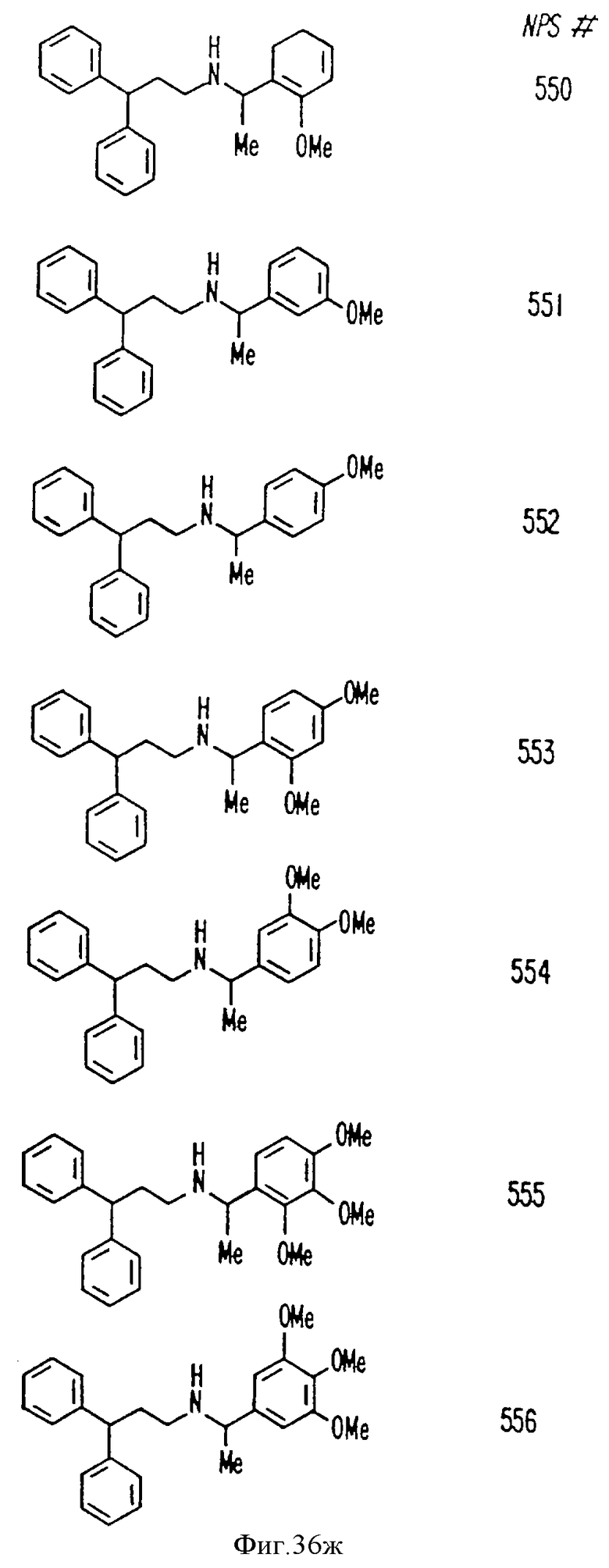
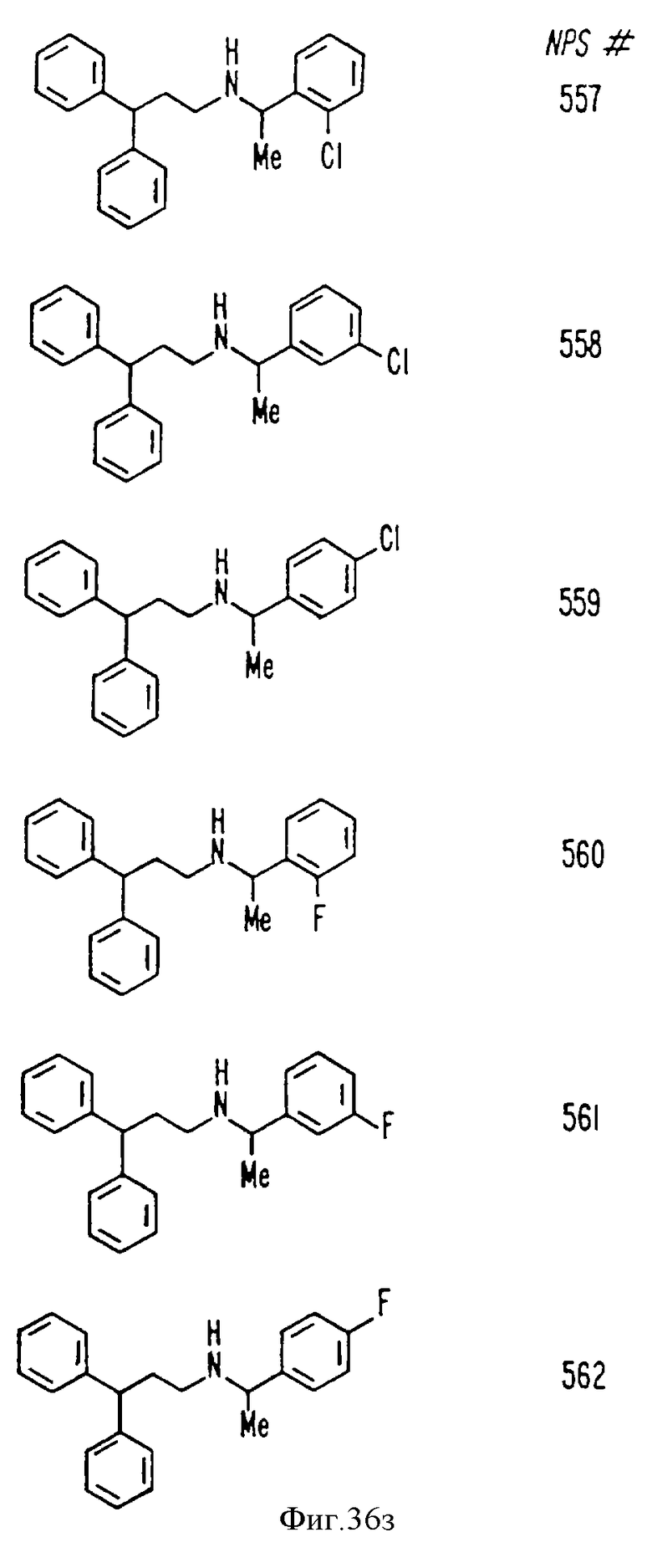
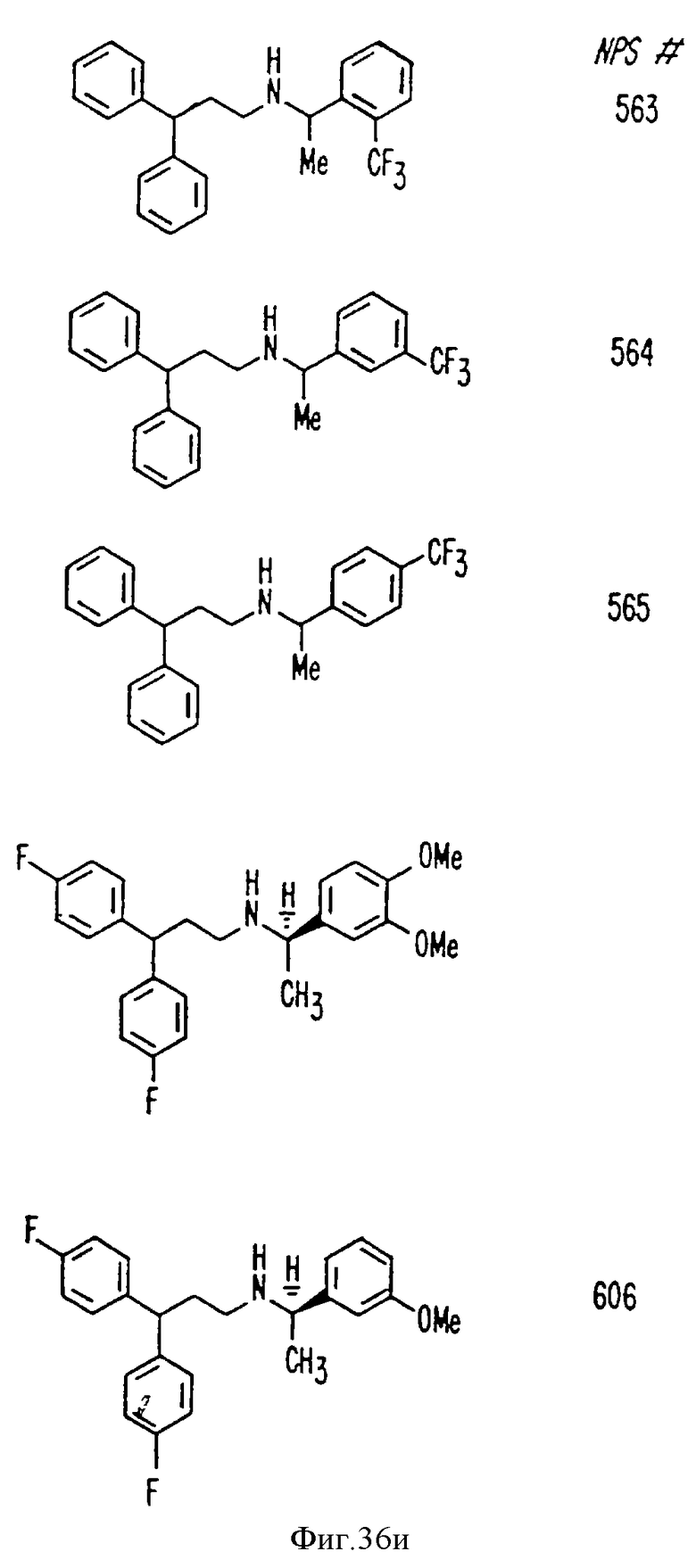
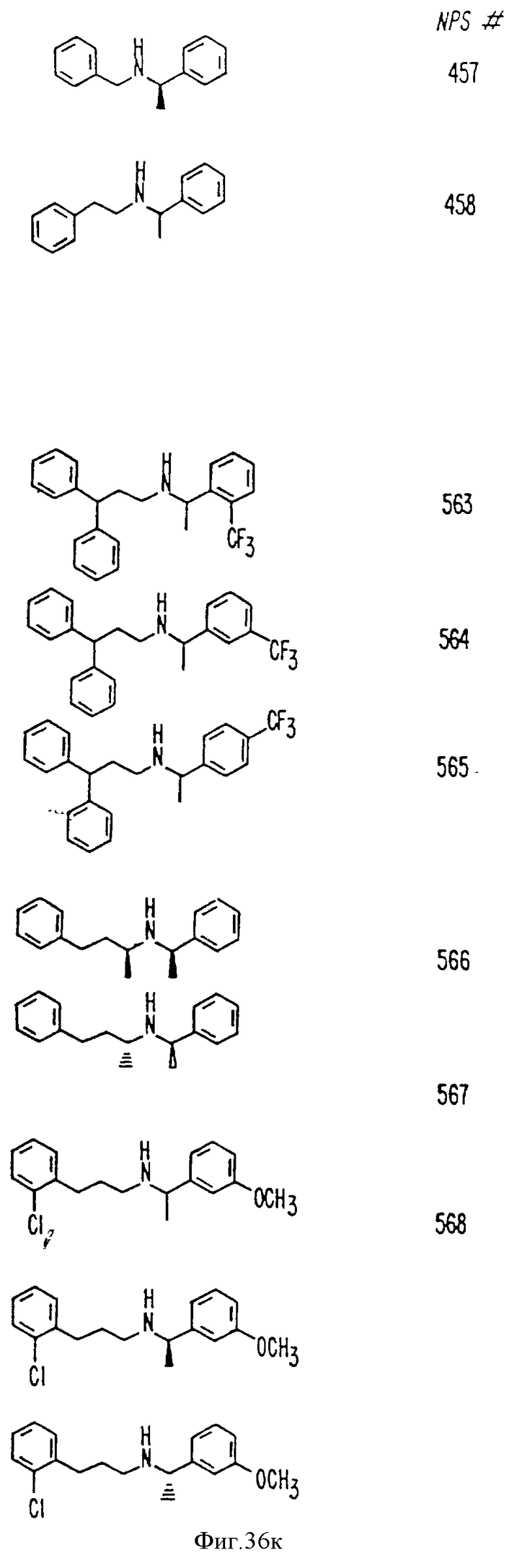

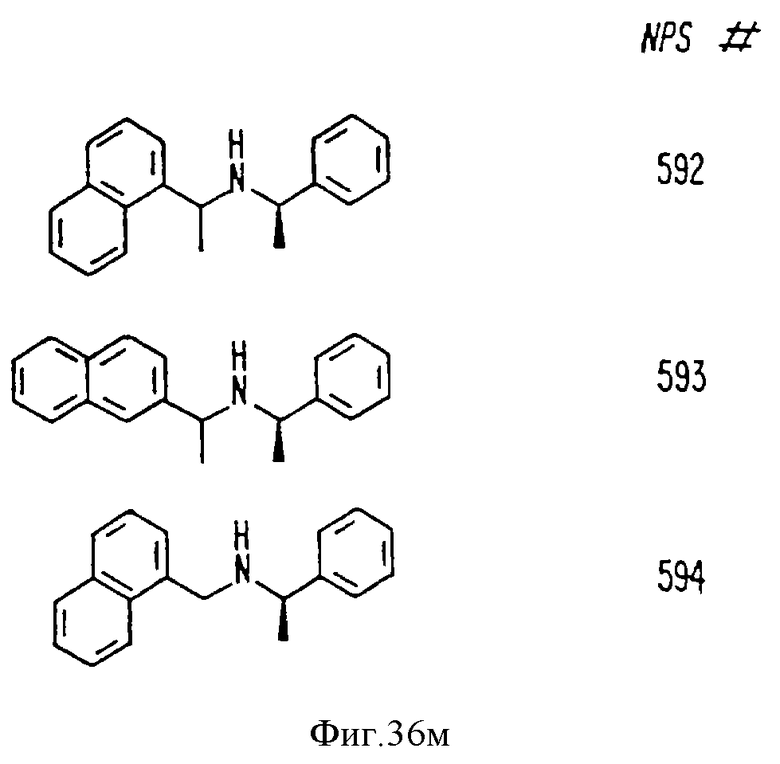




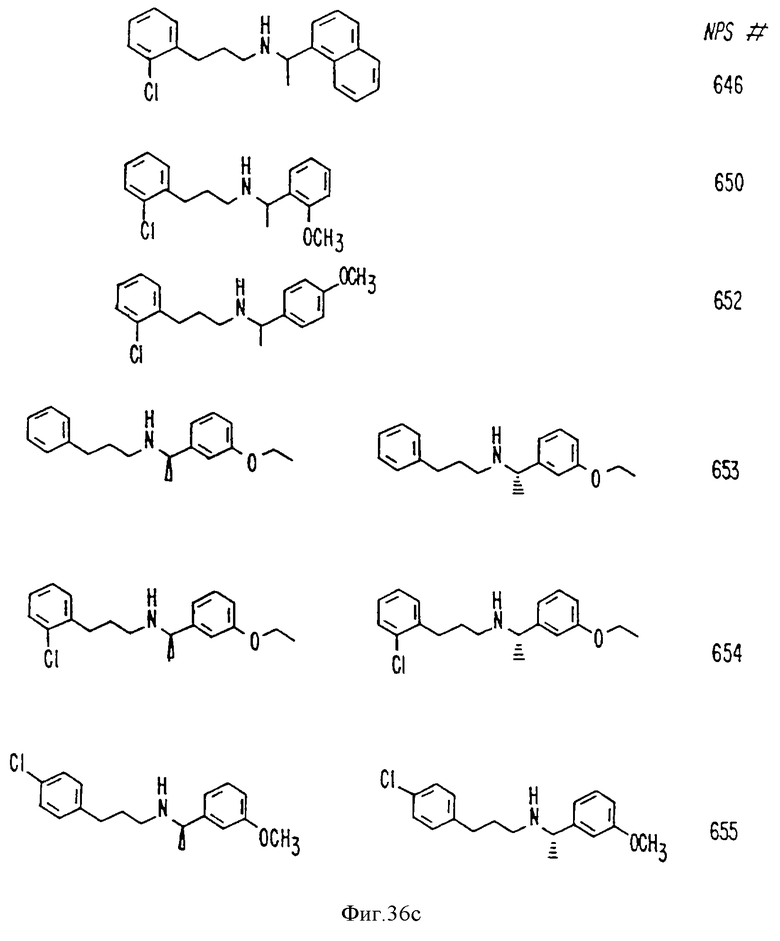

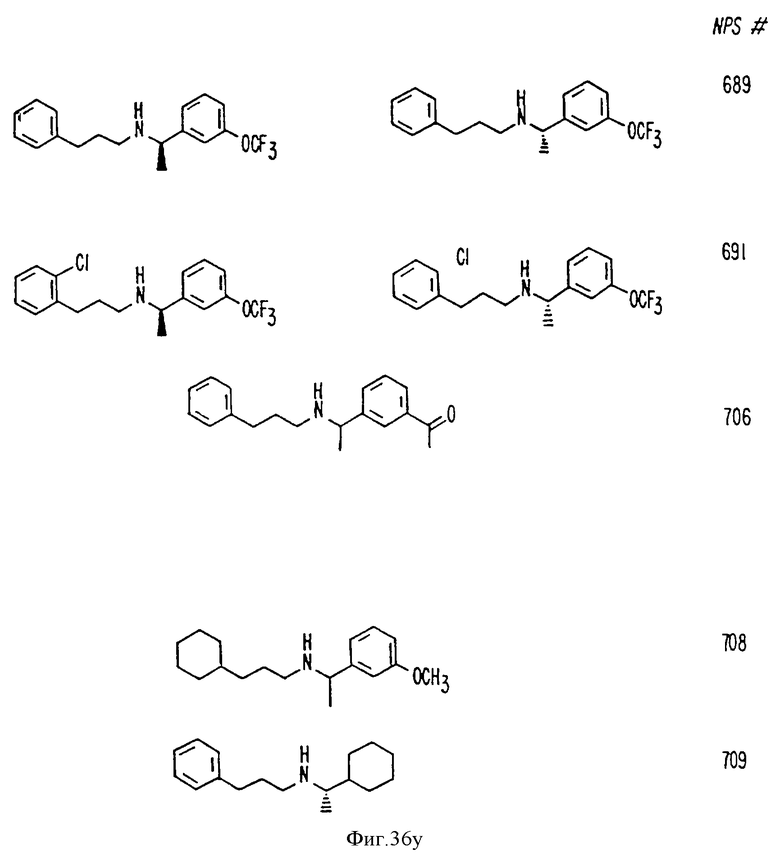
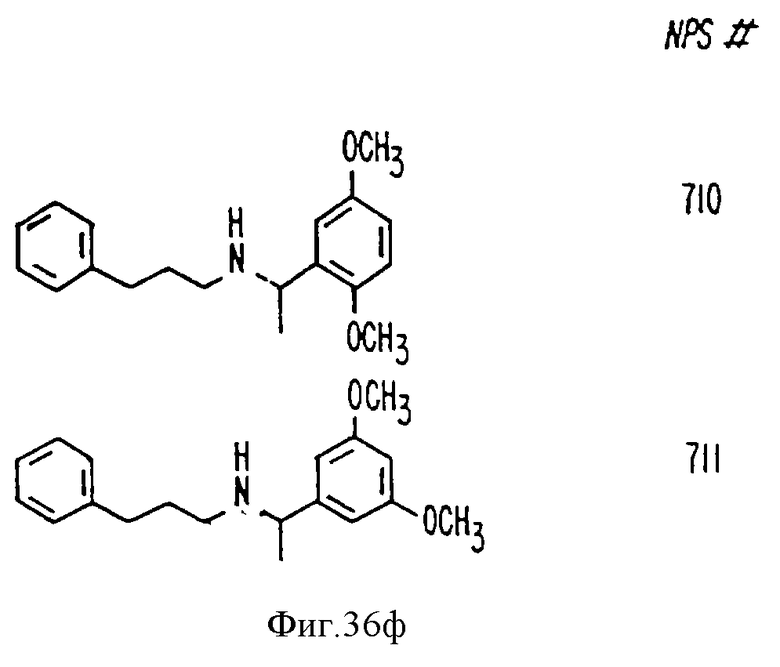
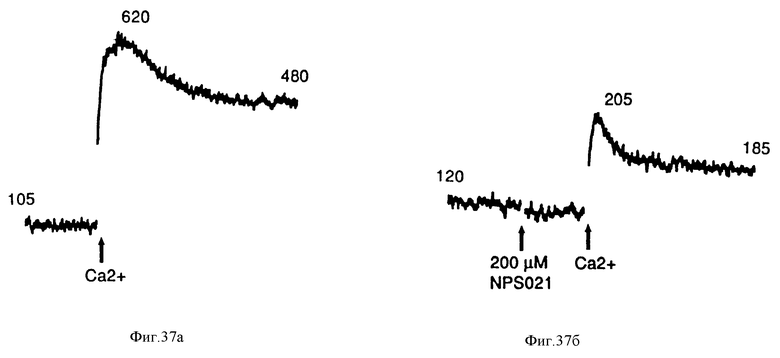
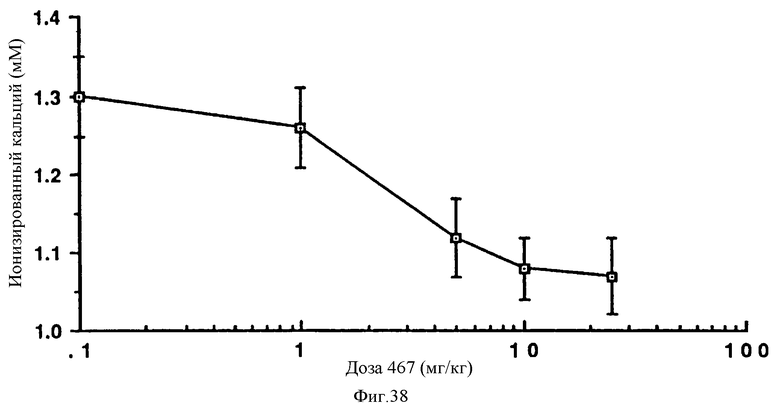
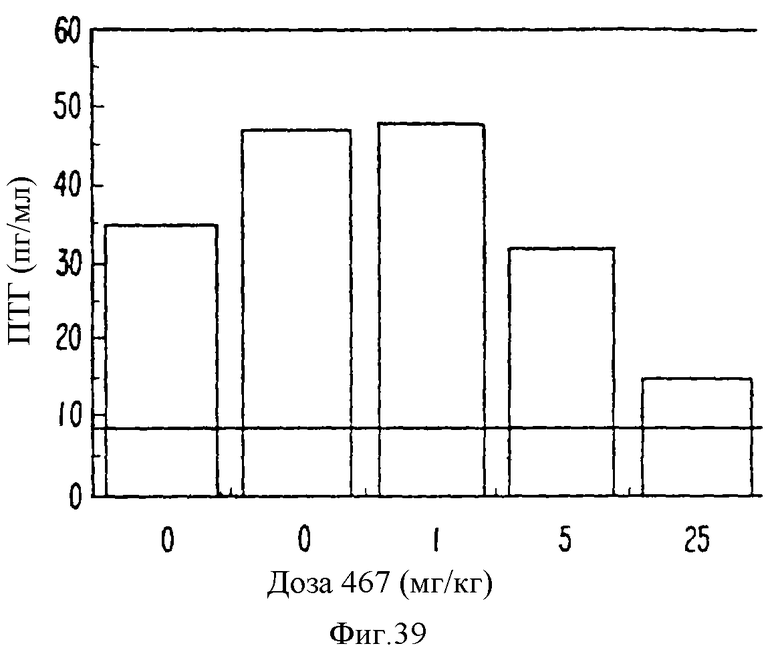

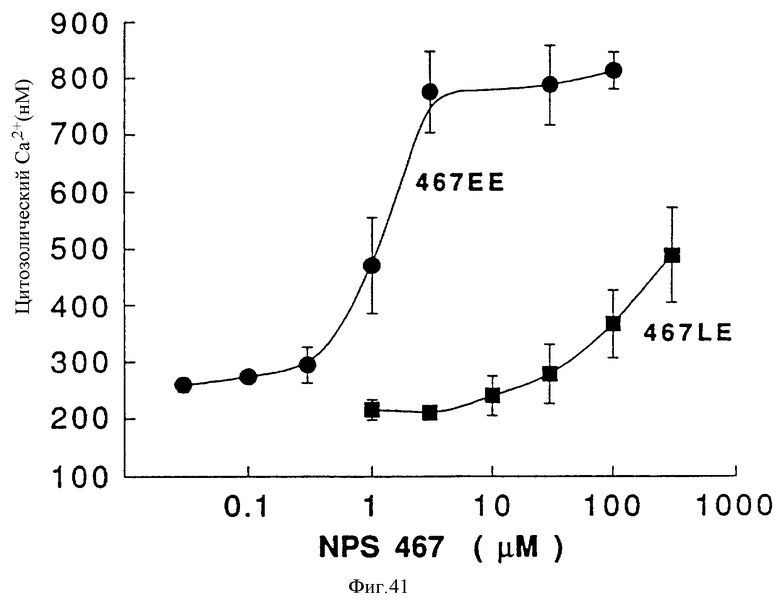
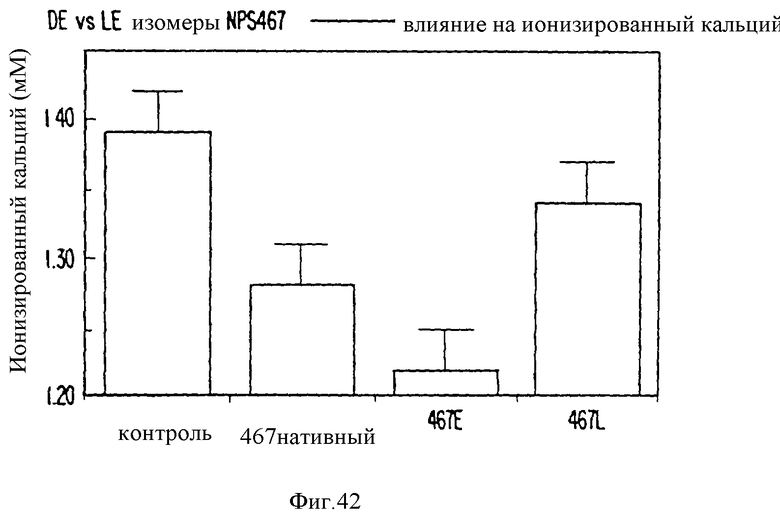


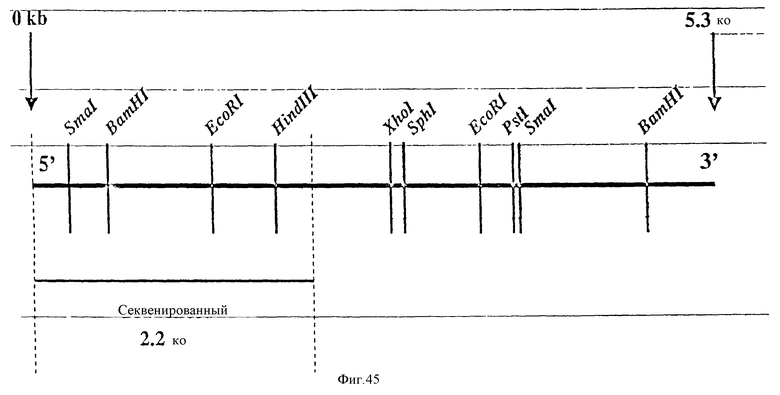
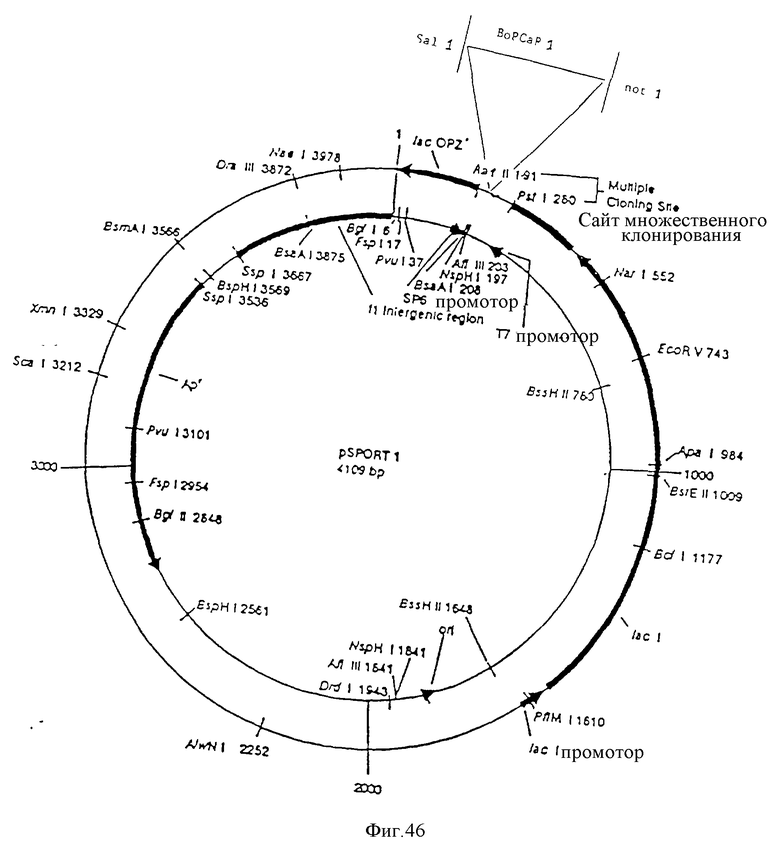

Изобретение относится к медицине, точнее препаратам и способам лечения и исследования, связанным с рецепторами кальция и др. неорганических ионов. Предпочтительно молекула способна воздействовать как селективный агонист или антагонист на Са+2-рецептор одной или более, но не всех клеток, выбранных из группы, состоящей из паратироидных клеток, костных остеокластов, окологломерулярных почечных клеток, проксимальных канальцевых почечных клеток, периферических канальцевых почечных клеток, клеток толстой восходящей ветви петли Хенля и/или собирающей протоки, кератиноцита в эпидермисе, парафолликулярной клетки в тироиде (С-клеток), интестинальных клеток, трофобласта в плаценте, тромбоцита, клетки сосудов гладкой мышцы, клетки сердечного предсердия, клеток, секретирующих гастрин и глюкагон, почечной, мезангиальной клетки и клетки грудной железы. Изобретение расширяет арсенал средств, способных блокировать активность внеклеточных ионов кальция, при различных патологиях. 6 с. и. 50 з.п. ф-лы, 47 ил., 6 табл.
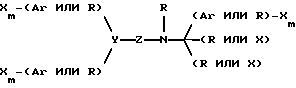
где X каждый независимо друг от друга выбирается из группы, состоящей из H, CH3, CH3O, CH3CH2O, Br, Cl, F, CF3, CHF2, CH2F, CF3O, CH3S, OH, CH2OH, CONH2, CN, NO2 и CH3CH2,
Ar выбирается из группы, состоящей из фенильной, 2- , 3- или 4-пиридильной, 1- или 2-нафтильной, 1- или 2-хинолинильной, 2- или 3-индолильной, бензильной и феноксильной групп;
R каждый независимо друг от друга выбирается из группы, состоящей из атома водорода, метильной, этильной, пропильной, изопропильной, бутильной, изобутильной, циклопентильной, циклогексильной, циклогептильной, циклооктильной, инденильной, инданильной, дигидроиндолильной, тиодигидроиндолильной и 2-, 3- или 4-пиперид(ин)ильной групп;
Y выбирается из группы, состоящей из группы CH, атома азота и ненасыщенного атома углерода;
Z выбирается из группы, состоящей из атомов кислорода, азота, серы,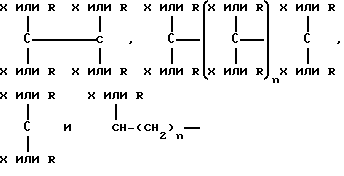
где каждый n независимо друг от друга больше или равен 1, но меньше или равен 4;
m каждый независимо друг от друга больше или равен 0, но меньше или равен 5,
и его фармацевтически приемлемые соли и комплексы,
где названное соединение не является верапамилом или D-600, и фармацевтически приемлемый носитель.
5. Композиция по п.4, отличающаяся тем, что каждый X независимо выбран из группы, состоящей из Cl, F, CF3, CH3 и CH3O.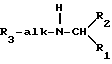
где alk является разветвленной или неразветвленной алкиленовой цепочкой с количеством атомов углерода от 1 до 6;
R1 представляет собой низшую алкильную группу с количеством атомов углерода от 1 до 3 или низшую галогеналкильную группу с количеством атомов углерода от 1 до 3, которые имеют в качестве заместителей от 1 до 7 атомов галогена;
R2 и R3 представляют собой независимо друг от друга выбираемые моноциклические или бициклические карбоциклические арильные или циклоалкильные группы, имеющие 5- или 6-членные циклы, возможно содержащие заместители в количестве от 1 до 5, которые независимо друг от друга выбираются из группы, состоящей из OCF3, низшей алкильной группы с количеством атомов углерода от 1 до 3, низшей галогеналкильной группы с количеством атомов углерода от 1 до 3, которые имеют в качестве заместителей от 1 до 7 атомов галогена, низшей алкоксильной группы с количеством атомов углерода от 1 до 3, атома водорода, нитро-, амино-, алкиламино-, амидогрупп, низшей алкиламидогруппы с количеством атомов углерода от 1 до 3, циангруппы, гидроксильной группы, ацильной группы с количеством атомов углерода от 2 до 4, низшей гидроксиалкильной группы с количеством атомов углерода от 1 до 3 и низшей тиоалкильной группы с количеством атомов углерода от 1 до 3,
при условии, что, если R3 является циклоалкильной группой, alk соответствует - CH2-, а R1 представляет собой CH3, то тогда R2 не является 4-аминофенильной группой, кроме этого, при условии, что названное соединение не является N-(3, 4, 5-триметоксибензил)-1-фенэтиламином, N-бензил-1-фенилбутиламином, N-фенилпропил-1-фенилбутиламином, N-циклогексилметил-1-фенилпропиламином или α-метил-бензил-м-нитробензиламином,
или его фармацевтически приемлемая соль.
| Огнетушитель | 0 |
|
SU91A1 |
| US 5021551, 05.06.91 | |||
| "Calcium binding Proteins in Heflth and Disease", Acad | |||
| Press | |||
| Jnc., N.-J | |||
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
Авторы
Даты
2000-03-10—Публикация
1993-02-23—Подача