Изобретение относится к технологии получения полимера олефинов, в частности, к металлоценовому катализатору и способу получения полимера олефинов.
Известен металлоценовый катализатор для получения полимера олефинов, включающий по меньшей мере одно металлоценовое соединение с (замещенными) индениловыми остатками в качестве лигандов, в особенности изопропилен (циклопентадиенил) (1-инденил)дихлорцирконий (см. заявку EP N 0407870, МКИ: C 08 F 32/08, 1991).
Недостаток получаемых при помощи известного металлоценового катализатора полимеров олефинов, которые могут применяться для получения полимерных сплавов и формованных изделий, состоит в том, что их физико-механические свойства являются не совсем удовлетворительными.
Задачей настоящего изобретения является предоставление катализатора, с помощью которого возможно получение полимера олефинов с улучшенными физико-механическими свойствами, в особенности полиолефинов с уменьшенной кристалличностью, повышенной ударной вязкостью, повышенной прозрачностью, высокой текучестью при температурах переработки, низким молекулярным весом и пониженной точкой плавления.
Поставленная задача решается предлагаемым металлоценовым катализатором для получения полимера олефинов, представляющим собой стерически жесткое металлоценовое соединение, содержащее в качестве лигандов по меньшей мере две замещенные или незамещенные циклопентадиенильные группы, связанные между собой через моноциклическую кольцевую систему, причем одна циклопентадиенильная группа анеллирована к моноциклической системе, и эта система лигандов отлична от 4 η5 -3-алкил-циклопентадиенил)- 4,6,6-триметил-( η5 -2-алкил-4,5-тетрагидропенталена) и представляет собой соединение формулы (I)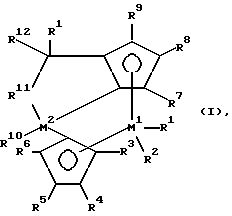
где М - металл группы IVб Периодической системы,
R1 и R2 одинаковы или различны и означают атом галогена, алкил с 1-10 атомами углерода, или группу NR13 2, где R13 означает алкил с 1 - 10 атомами углерода,
R3, R4, R5, R6, R7, R8 и R9 одинаковы или различны и означают атом водорода, алкил с 1 - 10 атомами углерода, или остаток -R13-SiR
R10 - алкил с 1-20 атомами углерода,
R11 и R12 одинаковы или различны и означают алкил с 1 - 20 атомами углерода, арил с 6 - 20 атомами углерода, алкенил с 2 - 12 атомами углерода,
n - целое число от 1 до 10.
Моноциклическая система предпочтительно имеет 6 кольцевых атомов.
В вышеприведенной общей формуле (I) радикалы имеют следующие предпочтительные значения:
М означает цирконий,
R1 и R2 одинаковый означают атом галогена,
R3, R4, R5, R6, R7, R8 и R9 одинаковы или различны и представляют собой водород, алкил с 1-4 атомами углерода,
R10 - алкил с 1-6 атомами углерода,
R11 и R12 одинаковы или различны и означают метил или фенил,
n - 2.
Предлагаемый катализатор может быть нанесен на носитель и/или форполимеризован.
Получение предлагаемого металлоценового катализатора вышеприведенной формулы (I) поясняется следующей реакционной схемой. При этом М1 означает металл основной группы Ia, IIa или IIIa.
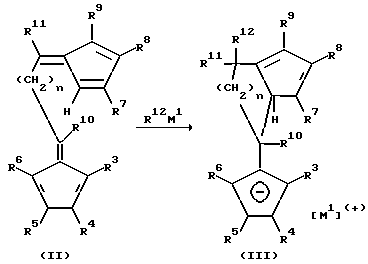
Дифульвены формулы (II) получаются из дикетонов (см. Chem. Ber. 114, 1226 (1981); там же 109, 3426 (1976); там же 107, 2453 (1974) или кетоальдегидов по известным из литературы способам (см. J. Org. Chem. 57 (1992) 2504; там же, 49 (1984) 1849; журнал Химия, 46 (1992) 377).
Превращение дифульвена (II) до лигандной системы формулы (III) осуществляют путем взаимодействия с металлоорганическим соединением (таким, как, например, метиллитий, бутиллитий, фениллитий) или реагентом Гриньяра.
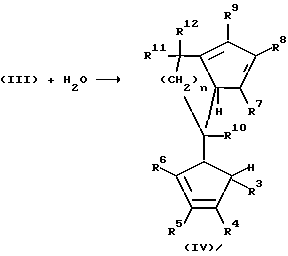
Соли формулы (III) могут подвергаться непосредственному превращению до соответствующих дианионных соединений формулы (V) путем депротонирования, например, бутиллитием. Гидролиз соединения (III) приводит к образованию бисциклопентадиенового соединения (IV), которое получается как смесь структурных изомеров и может очищаться хроматографией. Путем двукратного депротонирования соединения (IV), например бутиллитием, образуется дианионное соединение формулы (V).
Превращение до имеющих мостик металлоценов формулы (I), а также выделение желаемых комплексов в принципе известны. Для этого дианион формулы (V) подвергается взаимодействию с соответствующим галогенидом металла, таким как, например, тетрахлорид циркония, в инертном растворителе. Металлоцены формулы (I) можно также синтезировать непосредственно из дифульвенов структуры (II) без выделения промежуточных продуктов.
Пригодными растворителями являются алифатические или ароматические растворители, такие как, например, гексан или толуол, эфирные растворители, такие как, например, тетрагидрофуран или диэтиловый эфир или галогенированные углеводороды, такие как, например, хлористый метилен или галогенированные ароматические углеводороды, такие как, например, о-дихлорбензол.
Бис-циклопентадиенильные соединения формулы (IV), при которых по меньшей мере один из остатков R3 до R6, а также по меньшей мере один из остатков R7 до R9 является водородом, и по меньшей мере один из остатков R3 до R9 отличен от водорода, могут превращаться по известным из литературы способам до фульвенов формулы (IVa) или (IVb). Это поясняется следующей реакционной схемой, где R13, R14, R16 и R17 одинаковы или различны и имеют значение радикала R10: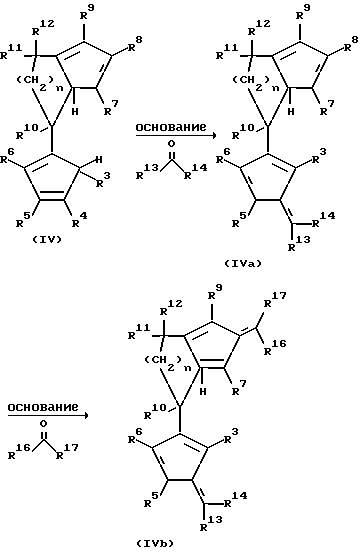
Взаимодействие фульвена (IVa) с металлоорганическими соединениями формулы R15M1 (причем R13, R14, R15, R16 и R17 одинаковы или различны и имеют значение радикала R10; М1 имеет вышеуказанное значение) приводит к образованию моноанионного соединения (IlIa).
Применение двух эквивалентов соединения формулы R15М1 приводит непосредственно к образованию дианионного соединения (Va):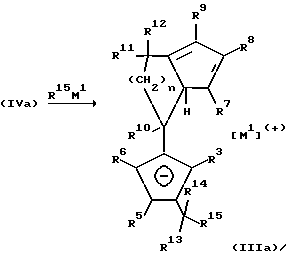
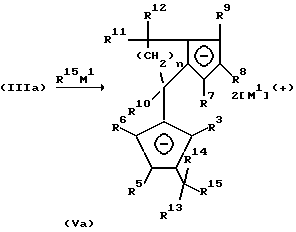
Превращение фульвена (Vlb) приводит, соответственно превращению (IVa), к образованию дианионного соединения (Vb).
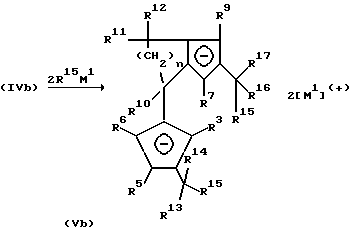
Бис-циклопентадиенильные анионы формулы (Vb) могут подвергаться взаимодействию с соединениями Rp 18MX,
где
М - имеет вышеуказанное значение,
X - удаляемая группа, такая как галоген, тозилат, трифторметансульфонат,
R18 имеет значение радикала R10, и
p - целое число от 1 до 5.
Это поясняется следующей реакционной схемой: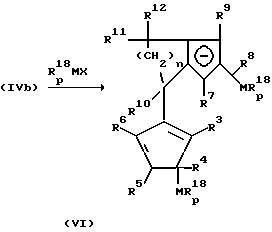
Соединения формулы (VI), при которых по меньшей мере один из остатков R3 до R6, а также по меньшей мере один из остатков R7 до R9 является водородом, могут превращаться до металлоценов согласно изобретению.
Соли соединений формулы (IlIa) могут непосредственно превращаться до соответствующих дианионовых соединений формулы (Va) путем депротонирования, например бутиллитием. Превращение до имеющих мостик металлоценов формулы (I) осуществляется соответственно превращению соединения формулы (V) до целевого соединения формулы (I).
Дальнейшая возможность получения металлоценовых соединений согласно изобретению состоит в том, что моноциклические системы, к которым анеллирована циклопентадиениловая группа, причем эти моноциклические системы имеют функциональные группы, которые могут служить уделяемыми группами в реакциях замещения (такими как, например, бромид или тозилат), подвергают взаимодействию, например с циклопентадиенильными или инденил-литиевыми соединениями.
Металлоцены согласно изобретению представляют собой высокоактивные катализаторы для полимеризации олефинов. В зависимости от структуры замещения лигандов металлоцены могут получаться как смесь изомеров. Металлоцены преимущественно применяются в виде чистых изомеров. Но применение рацемата является, в большинстве случаев, достаточным.
Можно, однако, применять и чистый энантиомер в (+)- или (-)- форме. С помощью чистых энантиомеров возможно получение оптически активного полимера. Рекомендуется, однако, разделение конфигурационных изомерных форм металлоценов, так как ответственный за полимеризацию центр (атом металла) в этих соединениях создает полимер, имеющий другие свойства. Для определенных областей применения, например мягких формованных изделий, это может быть вполне желательным.
Металлоценовый катализатор согласно изобретению может включать также еще сокатализатор.
В принципе, в качестве сокатализатора пригодно любое соединение, которое благодаря своей кислотности по Льюсу может переводить нейтральный металлоцен в катион и стабилизировать последний ("лабильная координация"). Сверх этого, сокатализатор или образовавшийся из него анион не должен вступать в дальнейшую реакцию с образовавшимся металлоценовым катионом. Как сокатализатор предпочтительно применяется алюминиевое соединение и/или соединение бора, в частности применяют алюмоксан. При этом предпочитают линейный алюмоксан формулы (VII) и/или циклический алюмоксан формулы (VIII),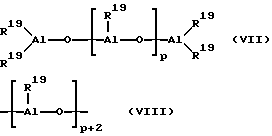
где остатки R19 одинаковы или различны и означают водород или углеводородную группу с 1 - 20 атомами углерода, такую как алкил с 1 - 18 атомами углерода, арил с 6 - 18 атомами углерода или бензил, а p - целое число от 2 до 50, предпочтительно 10 до 35.
Предпочтительно остатки R19 одинаковы и означают водород, метил, изобутил, фенил или бензил, особенно предпочтительно метил.
В случае, если остатки R19 различны, то они предпочтительно означают метил и водород или альтернативно метил и изобутил, причем содержание водорода или изобутила в остатках R19 предпочтительно составляет от 0,01 до 40%.
Способы получения алюмоксанов известны. Точная пространственная структура алюмоксанов неизвестна (см. J. Am. Chim. Soc. (1993) 115, 4971). Является, например, мыслимым, что цепи и кольца объединяются с образованием двухмерных или трехмерных структур.
Независимо от способа получения, всем алюмоксановым растворам свойственно меняющееся содержание непрореагировавшегося исходного алюминиевого соединения, имеющегося в свободном виде или в качестве аддукта.
Перед применением для осуществления реакции полимеризации металлоценовое соединение можно предварительно активировать сокатализатором, в особенности алюмоксаном, что позволяет заметно повысить его активность. Предварительная активация металлоценового соединения осуществляется предпочтительно в растворе. При этом металлоценовое соединение предпочтительно растворяется в растворе алюмоксана в инертном углеводороде. Как инертный углеводород годится алифатический или ароматический углеводород. Предпочтительно используется толуол.
Концентрация алюмоксана в растворе составляет примерно от 1 вес.% до предела насыщения, предпочтительно от 5 до 30 вес.%, в пересчете на общее количество раствора. Металлоцен может применяться в такой же концентрации, предпочтительно, однако, он применяется в количестве от 10-4 до 1 моль на моль алюмоксана. Продолжительность предварительной активации составляет 5 минут до 60 часов, предпочтительно 5 до 60 минут. Рабочая температура составляет от -78 до +100oC, предпочтительно 0 до 70oC.
Металлоценовое соединение применяется предпочтительно в концентрации, в пересчете на переходный металл, 10-3 до 10-8, предпочтительно 10-4 до 10-7 моль переходного металла на дм3 растворителя или на дм3 объема реактора. Алюминоксан используется предпочтительно в концентрации от 10-6 до 10-1 моль, предпочтительно 10-5 до 10-2 моль на дм3 растворителя или на дм3 объема реактора. Другие указанные сокатализаторы применяются, приблизительно, в эквимолярных количествах по отношению к металлоценовому соединению. В принципе, однако, возможны также более высокие концентрации.
Алюмоксан можно получить различным образом по известным способам. Один из способов состоит, например, в том, что алюминий-углеводородное соединение и/или гидридоалюминий-углеводородное соединение подвергают взаимодействию с водой (в газообразном, твердом, жидком или связанном виде, например в виде кристаллизационной воды) в инертном растворителе (таком как, например, толуол). Для получения алюминоксана с различными остатками R19 с водой подвергают взаимодействию два соответствующих триалкила алюминия.
Дальнейшим объектом изобретения является способ получения полимера олефинов путем полимеризации по меньшей мере одного олефина на металлоценовом катализаторе и выделения получаемого полимера, состоящий в том, что в качестве металлоценового катализатора используют стерически жесткое металлоценовое соединение вышеприведенной общей формулы (I).
В предлагаемом способе гомо- или сополимеризации предпочтительно подвергают по меньшей мере один олефин формулы Ra-CH=CH-Rb, где Ra и Rb одинаковы или различны и означают атом водорода или углеводородный остаток с 1 - 20 атомами углерода, в особенности, 1 - 10 атомами углерода, или Ra и Rb вместе со связывающими их атомами образуют одно или несколько колец. Примерами таких олефинов являются 1-олефины, такие как этилен, пропилен, 1-бутен, 1-пентен, 1-гексен, 4-метил-1-пентен или 1-октен, стирол, циклические и ациклические диены, такие как 1,3-бутадиен, изопрен, 1,4-гексадиен, норборнадиен, винилнорборнен или 5-этилиденнорборнен. Предпочтительно осуществляют гомополимеризацию этилена или сополимеризацию этилена и одного или нескольких 1-олефинов с 3-20 атомами углерода, таких как пропилен, и/или одного или нескольких диенов с 4-20 атомами углерода, таких как 1,3-бутадиен.
Полимеризация производится предпочтительно при температуре от -60 до +250oC, особенно предпочтительно, 50 до 200oC. Давление составляет предпочтительно 0,5 до 2000 бар, особенно предпочтительно 5 до 64 бар.
Полимеризация может проводиться непрерывно или периодически одно- или многостадийно в растворе, массе, суспензии или в газовой фазе. Преимущественно полимеризацию осуществляют в газовой фазе.
Предлагаемый способ может проводиться в присутствии одного из вышеуказанных сокатализаторов.
Для удаления имеющихся в олефине катализаторных ядов является выгодной очистка алюминиевым соединением, предпочтительно алкилалюминием, таким как триметилалюминий или триэтилалюминий. Эта очистка может осуществляться, с одной стороны, в самой полимеризационной среде, или, с другой стороны, олефин предварительно приводится в контакт с алюминиевым соединением с последующим выделением из реакционной смеси и подачей на полимеризацю.
Предлагаемый способ можно осуществлять в присутствии водорода, служащего в качестве регулятора молекулярного веса и/или для повышения активности катализатора. При этом возможно получение низкомолекулярных полиолефинов.
Металлоценовое соединение предпочтительно подвергается взаимодействию с сокатализатором вне реактора полимеризации при применении пригодного растворителя. При этом может также проводиться нанесение на носитель.
В предлагаемом способе может также осуществляться форполимеризация в присутствии металлоценового соединения. Для форполимеризации предпочтительно используется подаваемый на полимеризацию олефин (или один из подаваемых на полимеризацию олефинов).
Применяемый в способе согласно изобретению катализатор может иметь носитель. Путем нанесения на носитель можно, например, регулировать морфологию зерен получаемого полиолефина. При этом металлоценовое соединение может подвергаться взаимодействию сперва с носителем, а затем с сокатализатором. Можно также сначала наносить сокатализатор на носитель, а затем сокатализатор подвергать взаимодействию с металлоценовым соединением. Другим вариантом является нанесение на носитель продукта реакции металлоценового соединения и сокатализатора. Пригодными носителями являются, например, силикагели, окиси алюминия, твердый алюминоксан или другие неорганические носители, такие как, например, хлористый магний. Пригодным носителем является также полиолефин в виде мелкодисперсного порошка.
Сокатализатор, например алюмоксан, предпочтительно наносят на носитель, такой как, например, силикагели, окиси алюминия, твердый алюминоксан, другие неорганические носители или также полиолефин в виде мелкодисперсного порошка, а затем подвергают взаимодействию с металлоценом.
В качестве неорганических носителей могут использоваться окиси, образовавшиеся пиролитическим способом путем сгорания элементарных галогенидов в кислородно-водородном пламени, или получаемые как силикагели с определенным гранулометрическим составом, имеющие определенные формы зерен.
Получение сокатализатора на носителе может осуществляться, например, следующим образом в взрывобезопасном реакторе из нержавеющей стали, оснащенном системой перекачивания со ступенью давления 60 бар, системой снабжения инертным газом, охлаждающей рубашкой для регулирования температуры и второй системой циркуляции охлаждающей жидкости через находящийся на системе перекачивания теплообменник. Система перекачивания засасывает при помощи насоса содержимое реактора через расположенный в днище реактора патрубок и подает его в смеситель и оттуда по нагнетательному трубопроводу через теплообменник обратно в реактор. Подводящий трубопровод смесителя выполнен с сужающимся по поперечному сечению участком, вызывающим повышенную скорость потока, при этом в зоне турбулентности указанного участка в осевом направлении и против направления течения потока размещена линия узкого поперечного сечения, через которую может подаваться тактами определенное количество воды в атмосфере находящегося под давлением 40 бар аргона. Контроль за реакцией осуществляется пробоотборником, расположенным на циркуляционной системе перекачивания.
В принципе, однако, пригодны также другие реакторы.
В вышеописанный реактор объемом 16 дм3 подают 5 дм3 декана в инертной атмосфере. Прибавляют 0,5 дм3 (= 5,2 моль) триметилалюминия при 25oC. После этого 250 г силикагеля марки SD 3216-30 (торговый продукт фирмы Грейс АГ, DE), который предварительно сушат при 120oC в продуваемом аргоном псевдоожиженном слое, подают через воронку для твердых веществ в реактор и гомогенно распределяют при помощи мешалки и системы перекачивания. Воду в общем количестве 76,5 г подают по порциям объемом 0,1 см3 в течение 3,25 ч каждые 15 с в реактор. Давление, вызываемое аргоном и образовавшимися газами, постоянно держится регулировочным клапаном при 10 бар. После подачи всего количества воды система перекачивания отключается, а перемешивание продолжается еще 5 ч при 25oC.
Полученный таким образом сокатализатор на носителе используется как 10%-ная суспензия в н-декане. Содержание алюминия составляет 1,06 ммоль Al на см3 суспензии. Выделившееся твердое вещество содержит 31 вес.% алюминия, а суспендирующий агент содержит 0,1 вес.% алюминия.
После этого металлоцен согласно изобретению наносят на сокатализатор на носителе тем, что растворенный металлоцен перемешивают с сокатализатором. Растворитель удаляют и заменяют углеводородом, в котором как сокатализатор, так и металлоцен являются нерастворимыми.
Реакцию для получения имеющей носитель катализаторной системы осуществляют при температуре от -20 до +120oC, предпочтительно 0 до 100oC, особенно предпочтительно при 15 до 40oC. Металлоцен подвергается взаимодействию с имеющим носитель сокатализатором тем, что сокатализатор в виде 1 до 40%-ной по весу, предпочтительно 5 до 20 %-ной по весу суспензии в алифатическим инертном суспендирующем агенте, таком как н-декан, гексан, гептан, дизельное топливо, приводят в контакт с раствором металлоцена в инертном растворителе, таком как толуол, гексан, гептан, дихлорметан, или с тонкоизмельченным твердым металлоценом. Но возможно и взаимодействие раствора металлоцена со сокатализатором в качестве твердого вещества.
Реакция осуществляется путем интенсивного смешения, например, перемешивания при молярном соотношении Al/M от 100:1 до 10000:1, предпочтительно от 100: 1 до 3000:1, в течение 5-120 минут, предпочтительно 10 - 60 минут, особенно предпочтительно 10 - 30 минут, в инертной атмосфере. Во время реакции для получения имеющей носитель катализаторной системы, в частности при применении металлоценов согласно изобретению, имеющих максимум абсорбции в видимой области, встречаются изменения цвета реакционной смеси, с помощью которых можно следить за протеканием реакции.
После завершения реакции надосадочный раствор отделяется, например, фильтрацией или декантированием. Оставшееся твердое вещество 1 - 5 раз промывают инертным суспендирующим агентом, таким как толуол, н-декан, гексан, дизельное топливо, дихлорметан, для удаления растворимых веществ в образовавшемся катализаторе, в особенности для удаления непрореагировавшегося и, следовательно, растворимого металлоцена.
Полученная таким образом катализаторная система на носителе может, после вакуумной сушки, в виде порошка, или еще имея растворитель, снова суспендироваться и в виде суспензии в одном из вышеназванных инертных суспендирующих агентах подаваться на полимеризацию.
В случае, если полимеризация проводится в суспензии или в растворе, то применяется общепринятый для способа низкого давления по Циглеру инертный растворитель. Работают, например, в алифатическом или циклоалифатическом углеводороде, таком как, например, пропан, бутан, гексан, гептан, изооктан, циклогексан, метилциклогексан. Кроме того, можно использовать бензиновую фракцию или гидрированную фракцию дизельного топлива. Возможно также применение толуола. Предпочтительно полимеризация проводится в жидком мономере.
До подачи катализатора, в особенности имеющей носитель катализаторной системы (из металлоцена согласно изобретению и имеющего носитель сокатализатора, например, из металлоцена согласно изобретению и алюминийорганического соединения на полиолефиновом порошке в мелкодиспергированном виде), можно дополнительно вводить в реактор другое алкилалюминиевое соединение, такое как, например, триметилалюминий, триэтилалюминий, триизобутилалюминий, триоктилалюминий или изопренилалюминий, служащее для инертизации полимеризационной системы (например, для отделения имеющихся в олефине катализаторных ядов). Это соединение добавляется в концентрации от 100 до 0,01 ммоль Al на кг содержимого реактора. Предпочитаются триизобутилалюминий и триэтилалюминий в концентрации от 10 до 0,1 ммоль Al на кг содержимого реактора. Таким образом, при синтезе имеющей носитель катализаторной системы молярное соотношение Al/M можно выбрать небольшим.
При применении инертных растворителей мономеры подаются в газообразном или жидком виде.
Полимеризация может быть любой продолжительности, так как применяемая в способе согласно изобретению катализаторная система отличается только незначительным зависящим от времени уменьшением активности.
Применяемые в способе согласно изобретению металлоцены годятся, в особенности, для получения полиолефинов, имеющих уменьшенную кристалличность, повышенную ударную вязкость, повышенную прозрачность, высокую текучесть при температуре переработки, а также уменьшенную температуру плавления.
Основными областями применения таких полиолефинов являются рецептуры пластификаторов и смазок клеев-расплавов, масс для покрытий, уплотнений, изоляций, или звукоизоляционных материалов.
Путем применения водорода или повышения температуры полимеризации доступны также полиолефины с низкой молярной массой, такие как воски, твердость или точку плавления которых можно варьировать через содержание сомономеров.
Наоборот, путем выбора условий полимеризации также возможно получение высокомолекулярных полиолефинов, которые годятся как термопластичные материалы. Последние являются пригодными, в особенности, для получения формованных изделий, таких как пленки, плиты или крупногабаритные пустотелые изделия, например трубы.
Путем выбора метода полимеризации и вида сомономеров, а также количеств сомономеров можно получать сополимеры олефинов с эластомерными свойствами, такие как, например, тройные полимеры этилена, пропилена и 1,4-гексадиена.
Нижеследующие примеры служат для более подробного пояснения изобретения.
Получение металло-органических соединений и обращение с ними проводят с исключением воздуха и влаги в атмосфере аргона (техника Шленка). Все требуемые растворители до использования абсолютируют путем многочасового кипячения над пригодным осушителем и последующей дистилляции в атмосфере аргона.
Получение исходных дикетонов и кетоальдегидов осуществляют по известным в литературе методам. Циклопентадиен и метилциклопентадиен получают путем крекинга димеров и хранят при -35oC.
Определение соотношения Al/CH3 в алюмоксане осуществляют путем разложения пробы серной кислотой и определения объема образующихся газов в нормальных условиях, а также путем комплексометрического титрования алюминия в растворенной пробе по Шварценбаху.
Целевые соединения идентифицируют путем 1Н-ЯМР, 13C-ЯМР и ИК-спектроскопии.
Указанные точки плавления полимера и теплоты плавления являются результатами осуществления дифференциально-сканирующей калометрии при расплавлении со скоростью нагрева 10oC/мин.
Используемый в сравнительных примерах растворимый в толуоле метилалюмоксан поставляется фирмой ВИТКО в качестве 10%-ного толуольного раствора. Он содержит 36 мг Al/мл.
Определение содержания сомономеров осуществляется путем 13C-ЯМР по методу Рандалла (см. Macromolecules 1994, 27, 2120).
Нижеследующие примеры поясняют получение целевых продуктов формулы (I) и их исходных и промежуточных продуктов. Для названий промежуточных и целевых продуктов употреблена номенклатура МСТПХ (Междунар. союз по теоретической и прикладной химии). Данная номенклатура поясняется на примере соединения [4- (η5 -4'-метил-циклопентадиенил)-4,7,7-триметил- 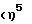 -4,5,6,7-тетрагидроинденил] -дихлорциркония. Циклическая система, которая является мостиком обоих циклопентадиениловых лигандов этого соединения, имеет шесть кольцевых атомов углерода (C4, C5, C6, C7, C8, C9) и три метиловых заместителя. Одна циклопентадиениловая группа однократно анеллирована к циклической системе, вторая находится как заместитель на циклической системе.
-4,5,6,7-тетрагидроинденил] -дихлорциркония. Циклическая система, которая является мостиком обоих циклопентадиениловых лигандов этого соединения, имеет шесть кольцевых атомов углерода (C4, C5, C6, C7, C8, C9) и три метиловых заместителя. Одна циклопентадиениловая группа однократно анеллирована к циклической системе, вторая находится как заместитель на циклической системе.
А. Получение бисфульвенов формулы (II)
Пример 1a
Синтез 2,5-бис(2,4-циклопентадиен-1-илиден)гексана
11,0 г (96,3 ммоль) 2,5-гександиона и 12,7 г (193 ммоль) свежеполученного путем крекинга циклопентадиена растворяют в 60 мл метанола, охлаждают до 0oC и смешивают с 8,60 г (121 ммоль) пирролидина. После 90-минутного перемешивания при 0oC реакционный раствор гидролизуют 5 мл ледяной уксусной кислоты и 50 мл воды, подвергают двукратному экстрагированию, каждый раз 70 мл диэтилового эфира, а объединенные органические фазы промывают насыщенным раствором хлористого натрия, сушат над сульфатом магния и растворитель удаляют в вакууме. Получают 18,0 г (89%) дифульвена в качестве маслянистого остатка оранжево-красного цвета.
Пример 1б
Синтез 2,5-бис(циклопента-2,4-диен-1-илиден)ундекана
Раствор 3,50 г (19,9 ммоль) 2,5-ундекандиона в 100 мл метанола и 10 мл тетрагидрофурана охлаждают до 0oC и смешивают с 3,92 мл (3,14 г, 47,5 ммоль) свежеполученного путем крекинга циклопентадиена. К оранжево-красному прозрачному реакционному раствору в течение 10 мин добавляют каплями 6,28 мл (5,40 г, 76,0 ммоль) свежедистиллированного пирролидина. При этом реакционный раствор в течение 10 мин окрашивается в темно-красный цвет. После этого реакционному раствору дают нагреваться до комнатной температуры и для завершения реакции перемешивают в течение дальнейших 3 дней. В целях переработки пирролидин нейтрализуют 4 мл ледяной уксусной кислоты и гидролизуют 100 мл воды. Экстрагируют два раза, каждый раз 100 мл пентана, промывают объединенные органические фазы несколько раз насыщенным водным раствором хлористого натрия и сушат над сульфатом магния. После удаления растворителя в вакууме получают 4,16 г (78%) сырого циклопентадиенилидена в качестве темно-красного масла.
В результате хроматографии на колонке, содержащей силикагель, дезактивированной триэтиламином, с применением в качестве элюента смеси пентана и диэтилового эфира в соотношении 100:1, получают дифульвен в качестве оранжево-красного масла.
Б. Синтез имеющих мостик бисциклопентадиенильных анионов формулы (V)
Пример 2
Синтез 4- (η5- циклопентадиенил)-4,7,7-триметил- (η5- 4,5,6,7-тетрагидроилиденил)-дилития
К раствору 10,0 г (47,5 ммоль) 2,5-бис-(2,4-циклопентадиен-1- илиден)гексана в 150 мл диэтилового эфира при интенсивном перемешивании медленно добавляют каплями 62,4 мл (99,8 ммоль) 1,60 м. эфирного раствора метиллития при 0oC. Реакционному раствору дают нагреваться до комнатной температуры. После 24-часового перемешиваня получают осадок бежевого цвета. После фильтрации и многократной промывки пентаном получают 13,2 г (89%) дилитиевой соли в качестве порошка бежевого цвета, которая координирована с молярным эквивалентом диэтилового эфира.
Пример 3
Синтез 4-( η5-циклопентадиенил)-4,7-диметил-7-фенил- (η5-4,5,6,7-тетрагидроилиденил)-дилития
83,4 мл (74,3 моль) 0,89 м. раствора фениллития в диэтиловом эфире добавляют каплями при 0oC к раствору 7,10 г (33,7 ммоль) дифульвена по примеру 1 в 100 мл диэтилового эфира. При этом приблизительно через 5 минут начинается выпадение осадка бежевого цвета. Реакционному раствору дают нагреваться до комнатной температуры и перемешивают в течение дальнейших 12 часов при 25oC. После фильтрации, многократной промывки пентаном и сушки в вакууме, создаваемом при помощи масляного насоса, получают 10,3 г (82%) дилитиевой соли в качестве порошка бежевого цвета, имеющей высокую чувствительность к гидролизу.
Пример 4
Синтез 4- (η5- циклопентадиенил)-4,7-диметил-7-6утил- (η5 -4,5,6,7-тетрагидроилиденил)-дилития
Раствор 15,0 г (71,3 ммоль) дифульвена по примеру 1, растворенного в 100 мл диэтилового эфира, охлаждают до -30oC и, при интенсивном перемешивании, медленно смешивают с 94 мл (150 ммоль) 1,60 м. раствора н-бутиллития в гексане. При этом образуется осадок лимонно-желтого цвета. Реакционному раствору дают нагреваться до комнатной температуры и перемешивают для завершения реакции еще в течение дальнейших 24 часов. После этого выпавший осадок отфильтровывают, многократно промывают пентаном и сушат в вакууме, создаваемом при помощи масляного насоса. Получают 29,0 г (91%) дилитиевой соли в качестве имеющего высокую чувствительность к гидролизу порошка бежевого цвета, с которым еще координирован молярный эквивалент диэтилового эфира.
В. Синтез имеющих мостик циклопентадиенов формулы (IV)
Пример 5
Синтез 4-циклопентадиенил-4,7,7-триметил-4,5,6,7-тетрагидро-1H-индена
К суспензии 7,35 г (23,5 ммоль) дилитиевой соли по примеру 2 в 50 мл диэтилового эфира добавляют каплями при 0oC 50 мл дегазированной воды. При этом суспензия бежевого цвета сразу исчезает и получают прозрачную оранжевого цвета фазу диэтилового эфира. Затем фазы разделяют в делительной воронке, водную фазу экстрагируют еще два раза, каждый раз 25 мл диэтилового эфира и объединенные органические фазы промывают 20 мл насыщенного раствора хлористого натрия. После сушки над сульфатом магния и удаления растворителя в вакууме получают 5,1 г (96%) гидролизованного продукта в качестве масла оранжево-красного цвета.
Пример 6
Получение 4-циклопентадиенил-4,7-диметил-4-фенил- 4,5,6,7-тетрагидро-1H-индена
Охлажденную до 0oC желтую суспензию 3,64 г (9,72 ммоль) дилитиевой соли по примеру 3 в 50 мл диэтилового эфира гидролизуют путем медленного добавления 20 мл дегазированной воды. При этом суспензия исчезает, и получают прозрачный раствор оранжевого цвета. После двукратной экстракции, каждый раз 20 мл диэтилового эфира, объединенные органические фазы многократно промывают насыщенным водным раствором хлористого натрия и сушат над сульфатом магния. Путем последующего удаления растворителя в вакууме получают 2,62 г (94%) гидролизованного продукта в качестве оранжевого масла.
Пример 7
Получение 4-циклопентадиенил-4,7-диметил-4-бутил- 4,5,6,7-тетрагидро-1H-индена
Охлажденную до 0oC желтую суспензию 5,00 г (17,33 ммоль) дилитиевой соли по примеру 4 в 50 мл диэтилового эфира гидролизуют путем медленного добавления 20 мл дегазированной воды. При этом суспензия исчезает, и получают прозрачный раствор оранжевого цвета. После двукратной экстракции, каждый раз 20 мл диэтилового эфира, объединенные органические фазы многократно промывают насыщенным водным раствором хлористого натрия и сушат над сульфатом магния. Путем последующего удаления растворителя в вакууме получают 4,59 г (96%) гидролизованного продукта в качестве оранжевого масла.
Г. Синтез имеющих мостик циклопентадиеново-фульвеновых лигандов формулы (IVa) путем дополнительного введения заместителей (введение различных остатков R12, R13, R14, R16, R17)
Пример 8a
Синтез 4-(3'-изопропилиден-циклопента-1,4-диенил)-4,7,7-триметил-4,5,6,7-тетрагидро-1H-индена
7,70 г (34,0 ммоль) циклопентадиенилтетрагидроинденила по примеру 5 растворяют в 70 мл метанола и охлаждают до 0oC. Затем к оранжево-красному реакционному раствору добавляют последовательно 2,96 г (51,0 ммоль) ацетона и 4,83 г (68,0 ммоль) пирролидина. После 5-часового перемешивания при 0oC для завершения реакции продолжают перемешивать в течение 2 часов при комнатной температуре, после чего реакцию прекращают путем добавления 4 мл ледяной уксусной кислоты. Красный прозрачный реакционный раствор гидролизуют 200 мл воды и получаемую при этом желтую суспензию подвергают трехкратной экстракции диэтиловым эфиром, взятым в количестве по 50 мл. После многократной промывки объединенных органических фаз насыщенным водным раствором хлористого натрия и сушки над сульфатом магния получают 8,00 г (88 %) целевого фульвена в качестве воскообразного осадка оранжево-красного цвета.
Пример 8б
Получение 4-циклопентадиенил-4,7-диметил-7-аллил- 4,5,6,7-тетрагидро-1H-индена
К раствору 16,8 г (79,8 ммоль) 2,5-бис(2,4-циклопентадиен-1-илиден)гексана по примеру 1, растворенного в 100 мл диэтилового эфира, и 50 мл тетрагидрофурана добавляют каплями, интенсивно перемешивая, при 0oC в течение часа 0,60 м. раствора аллилового реагента Гриньяра (175 ммоль) в диэтиловом эфире. После окончания добавления перемешивают при комнатной температуре в течение ночи, получаемую суспензию желто-оранжевого цвета охлаждают до 0oC и осторожно гидролизуют водным насыщенным раствором хлористого аммония. Органическую фазу отделяют, три раза промывают, каждый раз 50 мл насыщенного водного раствора хлористого натрия и сушат над сульфатом магния. После удаления растворителя в вакууме масляного насоса получают 17,5 г (87%) продукта в качестве масла оранжевого цвета.
Д. Синтез дианионных комплексов формулы (Va)
Пример 9а
Синтез 4-[3'-трет. бутил-( -η5-циклопентадиенил)]-4,7,7- триметил- (η5 -4,5,6,7-тетрагидро-инденил)дилития
При взаимодействии тетрагидроинденилфульвена по примеру 8 с 2 эквивалентами эфирного раствора метиллития при 0oC получают уже через несколько секунд осадок интенсивного желтого цвета. Перемешивают еще в течение 12
часов при комнатной температуре. После фильтрации, промывки пентаном и сушки в вакууме, создаваемом при помощи масляного насоса, получают дилитиевую соль, которая без предварительной идентификации далее превращается.
Пример 9б
Синтез [4-(-η5-циклопентадиенил)] -4,7-диметил-7-аллил-(-η5-4,5,6,7-тетрагидроинденил)дилития
10,5 г продукта по примеру 8б растворяют в 100 мл диэтилового эфира, охлаждают до 0oC, затем добавляют каплями 57,6 мл раствора н-бутиллития (1,60-молярного в гексане, 92,0 ммоль) После перемешивания в течение 18 часов при комнатной температуре получают осадок желто-бежевого цвета, который отфильтровывают, многократно промывают пентаном и сушат в вакууме, создаваемом при помощи масляного насоса. Дилитиевую соль получают в качестве твердого вещества бежевого цвета, с которым координирован еще один молярный эквивалент диэтилового эфира. Выход: количественный.
Е. Синтез металлоценов формулы (I)
Пример 10
Синтез 4 -(-η5 -циклопентадиенил)-4,7,7-триметил- (η5-4,5,6,7- тетрагидроинденил)-дихлорциркония
К охлажденной до -78oC суспензии 9,58 г (30,7 ммоль) дилитиевого соединения по примеру 2 в 200 мл толуола прибавляют порциями в течение 10 мин 7,50 г (32,2 ммоль) тетрахлорида циркония. После 50-часового перемешивания при комнатной температуре осадок отфильтровывают и фильтрат оранжевого цвета сгущают досуха в вакууме. После многократной промывки пентаном получают 4,38 г (37 %) дихлорида цирконоцена в качестве порошка оранжево-желтого цвета.
Для очистки порошок оранжево-желтого цвета в течение нескольких дней экстрагируют пентаном в циркуляционной фритте, причем после удаления растворителя в вакууме, создаваемом при помощи масляного насоса, получают 1,70 г (14%) дихлорида цирконоцена в качестве желтого порошка с точкой плавления 223oC (разл., определенной путем дифференциально-сканирующей калометрии).
Пример 11
Синтез 4-(η5циклопентадиенил)-4,7,7-триметил-(- η5-4,5,6,7- тетрагидро-инденил)дихлортитана
Суспензию 5,46 г (17,5 ммоль) дилитиевого эфирата по примеру 2 в 200 мл толуола охлаждают до -78oC и смешивают с 3,3 г (17,5 ммоль) тетрахлорида титана. При этом реакционный раствор сразу же окрашивается в темно-красный цвет. Перемешивают в течение 30 часов при комнатной температуре, отфильтровывают от нерастворимого вещества и темно-красную толуольную фазу сгущают досуха в вакууме, создаваемом при помощи масляного насоса. После многократной промывки пентаном получают 1,85 г дихлорида титаноцена в качестве коричнево-бежевого порошка. Сырой продукт экстрагируют пентаном в течение нескольких дней в циркуляционной фритте, причем после удаления растворителя получают 780 мг (13%) дихлорида титаноцена в качестве коричневого твердого вещества с точкой плавления 259oC (разл., определенной путем дифференциально-сканирующей калометрии).
1H-ЯМР (200.1 МГц, CDCl3); δ = 7.06-7.03, 6.94-6.91, 6.82-6.76, 5.87-5.84, 5.82-5.78, 5.62-5.59 (6 x m, 7H, 1-H до 3-H и 2'-H до 5'H); 2.45 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq) = 14.2 Гц, 3J(H6ax/H5eq) = 6.3 Гц, 3J(H6eq/H5eq) = 2.7 Гц); 2.31 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax) = 14.0 Гц, 3J(H6ax/H5ax) = 14.0 Гц, 3J(H6eq/H5ax) = 6.2 Гц); 1.91 (ddd, 1H, 6ax-H, 2J(H6eq/H6ax) = 14.0 Гц, 3J(H5ax/H6ax) = 14.0 Гц, 3J(H5eq/H6ax) = 6.3 Гц; 1,69 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq) = 14.0 Гц, 3J(H5ax/H6eq) = 6.2 Гц, 3J(H5eq/H6eq)=2.7 Гц); 1,86 (s, 3H, 10-H); 1.25 и 1.11 млн.д. (2 x s, 6H, 11-H и 12-H).
Пример 12
Синтез [4-( -η5-циклопентадиенил)-4,7,7-триметил (η5-4,5,6,7-тетрагидроинденил)]-дихлорциркония из 2,5-бис(2,4-циклопентадиен-1-илиден)гексана
К раствору 10,0 г (47,5 ммоль) 2,5-бис(2,4-циклопентадиен-1- илиден)гексана по примеру 1 в 150 мл толуола прибавляют медленно при интенсивном перемешивании 62,4 мл (99,8 ммоль) 1,60 м. эфирного раствора метиллития при 0oC. После окончания добавления перемешивают в течение 24 часов при комнатной температуре, затем охлаждают до -30oC и добавляют 9,32 г (40 ммоль) тетрахлорида циркония. После 30-часового перемешивания при комнатной температуре отфильтровывают от хлористого лития и фильтрат сгущают досуха в вакууме. После многократной промывки пентаном получают 4,02 г (26%) дихлорида циркония.
1H-ЯМР (200.1 МГц, CDCl3) δ =6.73-6.70, 6.44-6.41, 5.73-5.70 (3 x m, 3H, 1-H до 3-H), 6.70-6.67, 6.53-6.48, 6.08-6.03, 5.88-5.82 (4 x m, 4H, 2'-H до 5'-H); 2.42 (ddd, 1H, 5eq-H, 2J(H5axH5eq)=14.8 Гц, 3J(H6ax/H5eq)=6.0 Гц; 3J(H6eq/H5eq)= 2.2 Гц); 2.30 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)= 14.8 Гц, 3J(H6ax/H5ax)=14.3 Гц, 3J(H6eq/H5ax)=5.3 Гц; 2.00 (ddd, 1H, 6ax-H, 2J(H6eq/H6ax)= 14.8 Гц, 3J(H5ax/H6ax)= 14.3 Гц, 3J(H5eq/H6ax)=6.0 Гц); 1.72 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)=14,8 Гц, 3J(H5ax/H6eq)=5.3 Гц, 3J(H5eqH6eq)= 2.2 Гц; 1,83 (s, 3H, 10-H); 1.33 и 1.10 млн. д. (2 x s, 6H, 11-H и 12-H).
Пример 13
Синтез обоих диастереомеров 4-(η5-циклопентадиенил)- 4,7-диметил-7-фенил- (η5- 4,5,6,7-тетрагидроинденил)-дихлорциркония
К охлажденной до -78oC суспензии 4,37 г (11,7 ммоль) дилитиевой соли по примеру 3 в 200 мл толуола добавляют порциями 2,72 г (11,7 ммоль) тетрахлорида циркония. Реакционной смеси дают нагреваться до комнатной температуры и суспензию оранжевого цвета перемешивают еще в течение 20 часов при 20oC. После фильтрации из фильтрата удаляют растворитель в вакууме, создаваемом при помощи масляного насоса, и получаемый при этом маслянистый остаток оранжево-красного цвета переводят в порошок путем интенсивного перемешивания в 20 мл пентана. После удаления пентана в вакууме получают 2,64 г (50%) дихлорида цирконоцена в качестве порошка желто-оранжевого цвета. На основе данных спектра 1Н-ЯМР сырого продукта соотношение диастереомеров составляет примерно 8:1.
1H-ЯМР (200.1 МГц, CDCl3): δ = 7.24-6.89 (т, 5H, Ph-H); 6.78-6.73, 6.54-6.50, 6.22-6.20, 5.97-5.94 (4 x м, 7H, 1-H до 3-H и 2'-H до 5'-H); 2.30-2.22, 1,92-1.84 (2 x m, 4H, 5-H, 6-H); 1.76, 1.71 млн.д. (2 x s, 6H, 10-H и 11-H).
Пример 14
Синтез обоих диастереомеров 4-(- η5- циклопентадиенил)-4,7-диметил-7-бутил-(η5-4,5,6,7-тетрагидроинденил)-дихлорциркония
Суспензию 7,80 г (22,0 ммоль) дилитиевой соли по примеру 4 в 200 мл толуола охлаждают до -78oC, а затем порциями добавляют 5,10 г (22,0 ммоль) тетрахлорида циркония. Реакционной смеси дают нагреваться до комнатной температуры и суспензию желто-оранжевого цвета перемешивают еще в течение 48 часов, после чего отфильтровывают от нерастворимого вещества и удаляют растворитель в вакууме, создаваемом при помощи масляного насоса. Получаемое масло красно-оранжевого цвета переводят в порошок путем интенсивного перемешивания с пентаном. Получают 2,72 г (30 %) дихлорида цирконоцена, который очищают путем экстракции пентаном в течение нескольких дней в циркуляционной фритте. Спектр 1H-ЯМР тонкого желтого осадка показывает два набора сигналов в соотношении 15: 1. Из получаемого желтого фильтрата можно после хранения при -30oC получать небольшое количество кристаллов. Эти кристаллы чистых диастереомеров дихлорида цирконоцена позволяют идентификацию отдельных сигналов спектра 1H-ЯМР. При этом выкристаллизовавшиеся из пентанового раствора кристаллы соответствуют тому диастереомеру, которого образуется меньше всего. Кристаллы можно получать также из 1,35 г (14 %) желтого тонкого порошка тем, что приблизительно 100 мг порошка растворяют в небольшом количестве хлористого метилена и путем диффузии пентана в этот раствор осуществляют очень медленную кристаллизацию. Главным продуктом является другой диастереомер.
1H-ЯМР (200.1 мГц, CDCl3): δ =6.73-6.67, 6.52-6.47, 6,41-6.38, 6.08-6.04, 5.87-5.83, 5.76-5.73 (6 x m, 7H, 2'-H до 5'-H и 1-H до 3-H); 2.48-2.16 (м, 3H, 5eq-H, 5ax-H, 6ax-H): 1.91-1.84 (m, 1H, 6eq-H); 1.83 (s, 3H, 10-H); 1.35-0.85 (3 x m, 6H, nBu-CH2), 1.25 (s, 3H, 11-H); 0.82-0.77 млн.д. (pt, 3H, nBu-CH3).
Пример 15
Синтез 4-(η5-циклопентадиенил)-4,7-диметил-7-бутил- (η5-4,5,6,7-тетрагидроинденил)-дихлоргафния
К охлажденной до -78oC суспензии 2,00 г (5,64 ммоль) дилитиевой соли по примеру 4 в 150 мл толуола прибавляют 1,81 r (5,65 ммоль) тетрахлорида гафния. Оранжевой суспензии дают нагреваться до комнатной температуры и для завершения реакции перемешивают еще в течение двух дней. Затем отфильтровывают от нерастворимого вещества и оранжево-красный фильтрат сгущают досуха в вакууме масляного насоса. К оранжево-красному остатку добавляют 30 мл пентана и интенсивно перемешивают в течение ночи. После удаления растворителя в вакууме получают 700 мг (24 %) дихлорида гафноцена в качестве порошка бежевого цвета. В спектре 1H-ЯМР неочищенного продукта можно найти лишь один диастереомер.
1H-ЯМР (200.1 МГц, CDCl3): δ =6.63-6.58, 6.42-6.39, 6.33-6.30, 5.99-5.96, 5.81-5.78, 5.66-5.63 (6 x m, 7H, 2'-H до 5'-H и 1-H до 3-H): 2.38 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq)=14.0 Гц, 3J(H6ax/H5eq)=5.7 Гц, 3J(H6eq/H5eq)= 3.2 Гц); 2.23 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)=14.0 Гц, 3J(H6ax/H5ax)=14.4 Гц, 3J(H6eq/H5ax)= 6.8 Гц); 1.98 (ddd, 1H, 6ax-H, 2J(H6eq/H6ax)= 14,4 Гц, 3J(H5ax/H6ax)=14,4 Гц, 3J(H5eq/H6ax)=5.7 Гц, 1,85 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)= 14.4 Гц, 3J(H5ax/H6eg)=6.8 Гц, (H5eq/H6eq)=3.2 Гц), 1.90 (s, 3H, 10-H); 1.27 (s. 3H, 11-H); 1.35-1.07 (3 x m, 6H, nBu-CH3); 0.84-0.76 млн.д. (pt, 3H, nBu-CH3).
Точка плавления: 151oC (определенная путем дифференциально-сканирующей калометрии).
Пример 16
Синтез обоих диастереомеров 4-(η5-циклопентадиенил)-4,7-диметил-7-бутил-(η5-4,5,6,7-тетрагидроинденил)-дихлортитана
Если 5,95 г (16,8 ммоль) дилитиевой соли по примеру 4 суспендируют в 120 мл толуола, то при добавлении 3,18 г (16,8 ммоль) тетрахлорида титана при -78oC суспензия бежевого цвета сразу же окрашивается в темно-красный цвет. Суспензию перемешивают еще 36 часов при комнатной температуре, после чего отделяют от осадка и темно-красный фильтрат сгущают досуха в вакууме, создаваемом при помощи масляного насоса. При этом получают 1,54 г (24%) обоих диастереомеров дихлорида титаноцена в качестве коричнево-красного порошка. Согласно спектру 1H-ЯМР неочищенного продукта соотношение обоих диастереомеров составляет 8:1. Если коричнево-красный порошок экстрагируют пентаном в течение нескольких дней в циркуляцонной фритте, то из фильтрата выпадает коричневый осадок. При этом в спектре 1H-ЯМР можно установить, что пентановый раствор включает оба изомера в соотношении 1:1 (150 мг, 2,3%), в то время, как коричневый порошок (720 мг, 11%) представляет собой почти чистый диастереомер.
1H-ЯМР (200.1 МГц, CDCl3): δ =7.06-6.96, 6.95-6.92, 6.82-6.74, 5,89-5.85, 5.83-5.79, 5.64-5.61 (6 x m, 7H, 2'-H до 5'-H и 1-H до 3-H); 2.40-2.27, 1.89-1.75 (2 x m, 4H, 5eq-H 5ax-H, 6ax-H, 6eq-H); 1.86 (s, 3H, 10-H); 1.35-0.89 (m, 6H, nBu-CH2); 1.21 (s, 3H, 11-H); 0.84-0.77 млн.д. (pt, 3H, nBu-СH3).
Точка плавления: 134oC (определенная путем дифференциально-сканирующей калометрии).
Пример 17
Синтез { 4-(3'-[трет. -бутил-(η5-циклопентадиенил)] -4,7,7- триметил-(η5-4,5,6,7-тетрагидроинденил)}дихлорциркония
Суспензию 2,84 г (7,71 ммоль) дилитиевой соли по примеру 9a в 150 мл толуола охлаждают до -78oC. После добавления порциями 1,79 г (7,71 ммоль) тетрахлорида циркония реакционной смеси дают нагреваться до комнатной температуры и перемешивают еще 48 часов. Затем отделяют от нерастворимого вещества, оранжевую толуольную фазу сгущают в вакууме, создаваемом при помощи масляного насоса, и получаемое оранжево-красное масло переводят в порошок путем интенсивного перемешивания в пентане. При этом получают 787 мг (23%) региоизомерных дихлоридов цирконоцена в качестве оранжево-желтого порошка. Согласно спектру 1H-ЯМР неочищенный продукт включает оба диастереомера в соотношении 1:1. Путем экстракции оранжево-желтого порошка пентаном в циркуляционной фритте получают 370 мг (11%) дихлоридов цирконоцена в соотношении 1:1.
1H-ЯМР (200.1 МГц, CDCl3): δ =6.76-6.72, 6.69-6.65, 6.53-6.50, 6.43-6.32, 5.99-5.97, 5.88-5.82, 5.72-5.61 (7 x m, 12H, 1-H, 2-H, 3-H, 2'-H, 4'-H, 5'-H): 2.37-2.33, 2.10-1.85, 1.75-1.62 (3 x m, 8H, 5-H и 6-H); 1.82, 1.81 (2 x s, 6H, 10-H); 1,33 (bs, 6H, 11-H или 12-H); 1.31, 1.25 (2 x s, 18H, nBu-CH3); 1,12, 1,09 млн.д. (2 x s, 6H, 11-H или 12-H).
Ж. Синтез металлоценово-диалкильных комплексов
Пример 18
Синтез 4-(η5-циклопентадиенил)-4,7,7-триметил-(η5-4,5,6,7-тетрагидроинденил)-цирконийдиметила
К суспензии 1,03 г (2,66 ммоль) дихлорида цирконоцена по примеру 10 в 50 мл диэтилового эфира медленно добавляют каплями 3,30 мл (5,33 ммоль) 1,60 м. эфирного раствора метиллития при -78 oC. Реакционной смеси дают медленно нагреваться до комнатной температуры в ванне охлаждающей смеси и дополнительно перемешивают еще 5 часов при комнатной температуре. Растворитель удаляют в вакууме и бесцветный остаток экстрагируют три раза пентаном, взятым в количестве по 50 мл. Объединенные пентановые растворы сгущают и для кристаллизации хранят при -25oC. После отделения растворителя и сушки в вакууме, создаваемом при помощи масляного насоса, получают 700 мг (76 %) цирконоцендиметила в качестве бесцветного кристаллического порошка.
1H-ЯМР (200.1 МГц, CDCl3): δ =6.58-6.50, 6.38-6.34, 5.91-5.87, 5.47-5.53, 5.34-5.31 (5 x m, 7H, 1-H до 3-H и 2'-H до 5'-H); 2.18 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq)= 14.0 Гц, 3J(H6ax/H5eq)=5.9 Гц, 3J(H6eqH5eq)=3.1 Гц; 2,09 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)= 14,0 Гц, 3J(H6eq/H5ax)=14.0 Гц, 3J(H6eq/H5ax)= 5.31 Гц; 1.80 (ddd, 1H, 6ax-H, 2J(H6eq/H6ax)= 14.0 Гц, 3J(H5ax/H6ax)=14.0 Гц, 3J(H5eq/H6ax)=5.9 Гц; 1.57 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)= 14.0 Гц, 3J(H5ax/H6eq)=5.3 Гц, 3J(H5eq/H6eq)=3.1 Гц; 1,53 (s, 3H, 10-H); 1,19, 1.12 (2 x s, 6H, 11-H и 12-H), 0.26 и 0.34 млн.д. (2 x s, 6H, 13-CH3 и 14-CH3).
Точка плавления: 114oC (определенная путем дифференциально-сканирующей калометрии).
Пример 19
Синтез обоих диастереомеров 4-(η5-циклопентадиенил)-4,7-диметил-7-(2-пропен-1-ил)-(η5-4,5,6,7-тетрагидроинденил)-дихлортитана
2,45 г (7,24 ммоль) дилитиевого соединения по примеру 9б растворяют в 80 мл тетрагидрофурана, получаемый прозрачный раствор оранжевого цвета охлаждают до -78oC и смешивают с 2,42 r (7,24 ммоль) аддукта тетрахлорида титана и бис-тетрагидрофурана. При этом реакционная смесь сразу же окрашивается в темно-красный цвет. Реакционной смеси дают нагреваться до комнатной температуры и перемешивают еще 2 дня. После удаления растворителя в вакууме получают порошок коричневого цвета. Путем экстракции неочищенного продукта пентаном в циркуляционной фритте получают 0,22 г (9%) обоих аллилтитаноценов в качестве коричневого порошка. Согласно данным спектра 1H-ЯМР продукт содержит оба диастереомера в соотношении 2:1.
1H-ЯМР (200.1 МГц, CDCl3): δ =7.05-7.01, 6.94-6.91, 6.85-6.80, 6.75-6.73, 5.87-5.79, 5.63-5.61 (6 x m, 2'-H до 5'-H и 1-H до 3-H); 5.63-5.40, 5.15-4.80 (2 x m, винил-CH и винил-CH2); 2.38-2.17, 2.10-2.06, 1.86-1.77 (3 x m, 5-H, 6-H, аллил-CH2): 1,85 (s, 10-H); 1.24, 1.10 млн.д. (2 x s, 11-H).
Пример 20
Синтез обоих диастереомеров [4-(η5-циклопентадиенил)-4,7-диметил-7-(2-пропен-1-ил)- (η5 -4,5,6,7-тетрагидроинденил)]-дихлорциркония
7,56 г (22,3 ммоль) дилитиевого соединения по примеру 9б суспендируют в 200 мл толуола и охлаждают до -78oC. Добавляют порциями 5,21 г (22,3 ммоль) тетрахлорида циркония. Реакционную смесь оставляют стоять в течение 30 минут при -78oC, после чего ей дают нагреваться в течение 4 часов до комнатной температуры и перемешивают еще в течение дальнейших 12 часов. Получаемую суспензию оранжевого цвета фильтруют на фритте типа Г4, остаток два раза промывают толуолом, взятым в количестве по 30 мл, и фильтрат сгущают досуха в вакууме, создаваемом при помощи масляного насоса. При этом получают масло оранжево-красного цвета, которое путем добавления 50 мл пентана и последующего интенсивного перемешивания переводят в порошок. После удаления растворителя в вакууме получают 5,04 г (55%) порошковых аллилцирконоценов желто-оранжевого цвета. Путем многократной экстракции сырого продукта 100 мл пентана в циркуляционной фритте получают 2,34 г (26%) аллилцирконоценов в качестве желтого порошка. Точка плавления: 99oC (определенная путем дифференциально-сканирующей калометрии). Согласно данным спектра 1H-ЯМР продукт содержит оба диастереомера в соотношении 1,5:1.
1H-ЯМР (200.1 МГц, CDCl3): δ =6.73-6.67, 6.55-6.47, 6.41-6.38, 6.08-6.04, 5.94-5.80, 5.76-5.72 (6 x m, 2'-H до 5'-H и 1-H до 3-H); 5.62-5.41, 5.20-4.83 (2 x m, винил-CH и винил-CH2); 2.55-2.17, 2.09-2.05, 1.97-1.69 (3 x m, 5-H, 6-H, аллил-CH2); 1.83 (s, 3H, 10-H); 1.27, 1.09 млн.д. (2 x s, 11-H (цис-изомер) и 11-H (транс-изомер)).
Пример 21
Синтез обоих диастереомеров [4-(η5-циклопентадиенил)-4,7-диметил-7-(3-(9-борабицикло)нонил-В)пропил-(η5-4,5,6,7-тетрагидроинденил)]-дихлорциркония
210 г (0,51 ммоль) дихлоридов аллилцирконоцена по примеру 20 растворяют в 50 мл толуола и смешивают при комнатной температуре с 62 мг (0,51 ммоль) 9-борабициклононила. Перемешивают в течение 36 часов при комнатной температуре, удаляют растворитель в вакууме и получаемое масло оранжево-желтого цвета смешивают с 30 мл диэтилового эфира. Прозрачный раствор сгущают до 10 мл и охлаждают в течение нескольких часов до -30oC, в результате чего получают 208 мг (78%) диастереомеров в качестве оранжево-желтого порошка с точкой плавления 74oC (определенной путем дифференциально-сканирующей калометрии).
Пример 22
Синтез { 4-[3'-изопропил-(η5-циклопентадиенил)] 1-4,7,7-триметил-(η5-4,5,6,7-тетрагидроинденил)}дихлорциркония
а) Синтез 4-(3'-изопропил-циклопентадиенил)-4,7,7-триметил-4,5,6,7-тетрагидро-1H-индена
К суспензии 2,17г (57,3 ммоль) гидрида литийалюминия в 100 мл диэтилового эфира добавляют каплями при комнатной температуре раствор 6,11 г (22,9 ммоль) тетрагидроинденилфульвена по примеру 8а в 20 мл диэтилового эфира. После сильной, но не очень экзотермической реакции суспензию оранжевого цвета нагревают с обратным холодильником еще в течение трех часов. Затем охлаждают в ледяной ванне до 0oC и гидролизуют осторожно ледяной водой. Получаемый при этом белый объемистый осадок два раза экстрагируют диэтиловым эфиром, взятым в количестве по 50 мл, и объединенные органические фазы промывают водным раствором хлористого натрия. После сушки над сульфатом магния и после удаления растворителя в вакууме получают 5,63 г (92 %) замещенного изопропилом анса-лиганда в качестве масла оранжевого цвета. Также в этом случае продукт состоит из большого количества обусловленных двойной связью изомеров, так что возможна лишь грубая классификация сигнальных групп в спектре 1H-ЯМР.
б) Синтез {4-[3'-изопропил- (η5 -циклопентадиенил)]- 4,7,7-триметил- 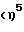 -4,5,6,7-тетрагидроинденил)}дилития
-4,5,6,7-тетрагидроинденил)}дилития
4,21 г (15,7 ммоль) замещенного изопропилом лиганда растворяют в 70 мл диэтилового эфира и добавляют каплями при 0oC 21,6 мл (34,5 ммоль) 1,60 м. раствора метиллития. Раствор быстро обесцвечивается с образованием белого осадка. После окончания прикапывания перемешивают еще в течение дальнейших 15 часов при комнатной температуре. Затем осадок отфильтровывают и два раза промывают диэтиловым эфиром, взятым в количестве по 15 мл. Получают 5,20г (93%) крайне чувствительной к воздействию воздуха дилитиевой соли в качестве порошка бежевого цвета, включающей один молярный эквивалент диэтилового эфира.
в) Синтез {4-[3'-изопропил- (η5 -циклопентадиенил)]-4,7,7-триметил- (η5 -4,5,6,7- тетрагидроинденил)}дихлорциркония
К охлажденной до -78oC суспензии 5,20 г (14,7 ммоль) дилитиевой соли в 200 мл толуола медленно добавляют 3,40 г (14,6 ммоль) тетрахлорида циркония. Образовавшуюся суспензию бежевого цвета перемешивают в течение 24 часов при комнатной температуре, нерастворимое вещество отделяют и прозрачный остаток оранжевого цвета сгущают приблизительно до 50 мл в вакууме, создаваемом при помощи масляного насоса. Спектроскопическое исследование 1H-ЯМР толуольной фазы показывает, что в этой фазе находятся оба диастереомера в соотношении 1: 1. Путем добавления 2 мл пентана и хранения в холодильнике при -20oC осаждается твердое вещество желтого цвета (1,42 г), в котором обогащен один из диастереомеров (соотношение 8:1). В толуольной фазе в обратном соотношении обогащен другой диастереомер (1,62 г): общий выход составляет 49 %.
Если растворять приблизительно 100 мг выпавшего желтого порошка в хлористом метилене, то после последующей медленной диффузии пентана в этот раствор получают кристаллы, которые представляют собой диастереомер 4R*-{4-[3'-изопропил-(η5-циклопентадиенил)]-4,7,7-триметил (η5-4,5,6,7-pR*-тетрагидроинденил)}дихлорцирконий.
1H-ЯМР (200.1 МГц, CDCl3): δ =6.79-6.75, 6.48-6.38, 6.24- 6.21, 5.99-5.95, 5.56-5.54, 5.44-5.41 (6 x m, 6H, 1-H, 2-H, 3-H, 2'-H, 4'-H, 5'-H): 2,91 (s, 1H, iPr-CH, 3J(iPr-CH3/iPr/CH)= 6.9 Гц); 2.41 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq)= 14.5 Гц, 3J(H6ax/H5eq)=6.2 Гц, 3J(H6eq/H5eq)=2.8 Гц); 2.28 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)=14.5 Гц, 3J(H6ax/H5ax)=14.5 Гц, 3J(H6eq/H5ax)= 5.6 Гц); 2.01 (ddd, 1H, 6ax-H, 2J(H6eqH6ax)= 14.5 Гц, 3J(H5ax/H6ax)=14.5 Гц, 3J(H5eq/H6ax)=6.2 Гц; 1.72 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)= 14.5 Гц, 3J(H5axH6eq)=5.6 Гц, 3J(H5eq/H6eq)=2.8 Гц; 1.78 (s, 3H, 10-H); 1.32, 1.11 (2 x s, 6H, 11-H и 12-H); 1.24, 1.09 млн.д. (2 x d, 6H, iPr-CH3, 3J(iPr- CH/iPr-CH3)=6.9 Гц.
Точка плавления: 193oC (определенная путем дифференциально-сканирующей калометрии).
Пример 23
Синтез { 4[3'-изопропил-(η5-циклопентадиенил)1-4,7,7- триметил-(2-изопропил-(η5-4,5,6,7-тетрагидроинденил)]}дихлорциркония
а) Синтез 4-(3'-изопропил-циклопентадиенил)-4,7,7-триметил- (2-изопропил-4,5,6,7-тетрагидро-1H-индена)
Вариант 1
Стадия А
2-изопропилиден-4-(3'-изопропилиден- циклопента-1', 4'-диенил)-4,7,7-триметил-(4,5,6,7-тетрагидро-2H- инден)
8,32 г (34,2 ммоль) монофульвена по примеру 8а растворяют в смеси 50 мл метанола и 20 мл пентана и получаемый прозрачный раствор оранжево-красного цвета охлаждают до 0oC. Путем последовательного добавления 2,61 г (3,31 мл, 45,0 ммоль) ацетона и 6,08 г (7,10 мл, 85,5 ммоль) пирролидина реакционный раствор становится темно-красным через 36 минут. После перемешивания в течение 7 дней при комнатной температуре к реакционной смеси добавляют последовательно 5 мл ледяной уксусной кислоты, 150 мл воды и 50 мл пентана.
После двукратной экстракции водной фазы пентаном объединенные органические фазы несколько раз промывают насыщенным водным раствором хлористого натрия и сушат над сульфатом магния. После удаления растворителя в вакууме, создаваемом при помощи масляного насоса, получают 9,04 г (86%) указанного дифульвена в качестве красного масла. Часть красного масла смешивают с пентаном и подвергают хроматографии на содержащей силикагель (величиной зерен 60 меш; продукт фирмы Мерк, DE) колонке, предварительно дезактивированной триэтиламином. В качестве растворителя применяют смесь пентана и триэтилового эфира в соотношении 100:5 (общий выход < 10%).
Стадия Б
4-(3'-изопропил-циклопентадиенил)-4,7,7-триметил- (2-изопропил-4,5,6,7-тетрагидро-1H-инден)
В трехгорлую колбу с холодильником интенсивного охлаждения и капельной воронкой подают 3,03 г (80,0 ммоль) гидрида литийалюминия в 100 мл диэтилового эфира, и при интенсивном перемешивании при комнатной температуре добавляют 6,47 г (21,1 ммоль) полученного на стадии А дифульвена, растворенного в 50 мл диэтилового эфира. По окончании добавления реакционную смесь нагревают с обратным холодильником в течение 5 часов и затем осторожно гидролизуют 100 мл воды. При этом получают серый осадок окиси алюминия и желтую фазу диэтилового эфира. Последнюю декантируют, серый осадок экстрагируют несколько раз диэтиловым эфиром и объединенные фазы диэтилового эфира промывают насыщенным водным раствором хлористого натрия. После сушки над сульфатом магния и удаления растворителя в вакууме получают 6,25 г (96%) восстановленного дифульвена в качестве масла оранжево-красного цвета, которое можно перерабатывать без дальнейшей очистки.
Вариант II
Стадия А
2,5-бис[(изопропил)циклопента-2,4-диен-1-илиден]-гексан
К раствору 2,78 мл (2,71 г, 23,8 ммоль) 2,5-гександиона и 4,00 г (47,6 ммоль) изопропилциклопентадиена в 50 мл метанола добавляют каплями при 0oC 5,90 мл (5,07 г, 71,3 ммоль) свежедистиллированного пирролидина. При этом реакционный раствор сразу же становится темно-красным. После перемешивния в течение дальнейших 15 часов при 0oC избыточный пирролидин нейтрализуют путем добавления раствора 2 мл ледяной уксусной кислоты в 100 мл воды. Экстрагируют два раза диэтиловым эфиром, взятым в количестве по 100 мл, объединенные органические фазы промывают несколько раз насыщенным водным раствором хлористого натрия и сушат над сульфатом магния. После удаления растворителя в вакууме получают 5,20 г (75%) дифульвена в качестве темно-красного масла.
Очистка дифульвена осуществляется путем хроматографии на колонке, содержащей силикагель, дезактивированный триэтиламином, используемым в качестве смеси с пентаном в соотношении 1: 100. В качестве элюента применяют смесь пентана и диэтилового эфира в соотношении 1:1. Получают 1,72 г (25 %) дифульвена в качестве красного масла.
Стадия Б
а) 4-(3'-изопропил-циклопентадиенил)-4,7,7- триметил-(2-изопропил-4,5,6,7-тетрагидро-1H-инден
600 мг (2,04 ммоль) замещенного бис-изопропилом дифульвена со стадии А растворяют в 10 мл диэтилового эфира и медленно смешивают при 0oC с 2,55 мл 1,60 м. эфирного раствора метиллития. Реакционной смеси дают нагреваться до комнатной температуры. Через 24 часов получают суспензию оранжевого цвета, которую охлаждают до 0oC и затем гидролизуют 10 мл воды. После экстракции диэтиловым эфиром в количестве 20 мл и сушки над сульфатом магния получают 520 мл (82%) целевого продукта в качестве оранжевого масла.
б) { 4-[3'-изопропил- (η5 -циклопентадиенил)]-4,7,7-триметил-[2- изопропил (η5 -4,5,6,7-тетрагидроинденил)}дихлорцирконий
К раствору 500 г (1,61 ммоль) замещенного бисизопропилом соединения со стадии Б варианта I или II в 20 мл пентана добавляют каплями 2,00 мл (3,22 ммоль) 1,60 м. эфирного раствора метиллития при 0oC. Реакционной смеси дают нагреваться до комнатной температуры, и через 12 часов получают мутную суспензию оранжевого цвета, которую охлаждают до -78oC и смешивают с 373 мг (1,61 ммоль) тетрахлорида циркония. После 24-часового перемешивания при комнатной температуре отфильтровывают от нерастворимого вещества и удаляют растворитель в вакууме. Получают 300 мг (40 %) обоих диастереомеров
анса-цирконоцена в качестве порошка оранжевого цвета. В спектре 1H-ЯМР обнаруживают резонансные сигналы обоих диастереомеров в соотношении 1:1 (определены при помощи изопропиловых групп).
1H-ЯМР (200.1 МГц, CDCl3): δ =6.44-6.41, 6.24-6.15, 5.95-5.91, 5.68-5.60, 5.33-5.29, 5.18-5.17 (6 x m, 10H, 2'-H, 4'-H, 5'-H, 1-H и 3-H); 3.13-2.83, 2.46-2.16, 2.08-1.93, 1.78-1.72 (4 x m, 12H, 2 x iPr-CH и 5-H и 6-H); 1.76, 1.72 (2 x s, 6H, 10-H): 1.28-1.07 мнл.д. (m, 36H, 11-H, 12-H, 4 x iPr-CH3).
Пример 24
Синтез { 4-[3'-триметилсилил-(η5-циклопентадиенил)1-4,7,7-триметил-[2-триметил-силил-(η5-4,5,6,7-тетрагидроинденил)1}дихлорциркония
а) Синтез 4-(3'-триметилсилил-циклопентадиенил)-4,7,7- триметил-(2-триметил-силил-4,5,6,7-тетрагидро-1H-индена)
Раствор 6,81 г (21,8 ммоль) дилитиевого эфирата по примеру 9 в 50 мл тетрагидрофурана охлаждают до 0oC и при перемешивании прикапывают 5,50 мл (4,74 г, 43,6 ммоль) триметилсилилхлорида. Реакционной смеси дают нагреваться в течение ночи до комнатной температуры, получаемую мутную суспензию оранжевого цвета гидролизуют путем добавления 50 мл дегазированной воды, и затем экстрагируют петролейным эфиром. После сушки над сульфатом магния и удаления растворителя в вакууме получают 6,54 г (81%) масла красно-оранжевого цвета.
б) Синтез {4-[3'-триметилсилил- (η5 -циклопентадиенил)]-4,7,7- триметил-[2-триметил-силил (η5 -4,5,6,7-тетрагидроинденил)]}дилития
К охлажденному до 0oC раствору 3,30 г (8,90 ммоль) замещенного бистриметил-силилом соединения со стадии а) в 40 мл пентана прикапывают при перемешивании 11,1 мл (17,8 ммоль) 1,60 м. эфирного раствора метиллития. При этом получают, при выделении газа, осадок белого цвета. Для завершения реакции продолжают перемешивать еще в течение 24 часов при комнатной температуре, после чего белый осадок отфильтровывают и промывают пентаном. После сушки в вакууме, создаваемом при помощи масляного насоса, получают 2,60 г (76%) дилитиевой соли в качестве белого пирофорного остатка.
в) Синтез {4-[3'-триметилсилил-(η5-циклопентадиенил)]-4,7,7-триметил-[2-триметил-силил (η5-4,5,6,7-тетрагидроинденил)]}дихлорциркония
К охлажденной до -78oC суспензии 2,60 г (6,79 ммоль) замещенной бистриметил-силилом дилитиевой соли со стадии б) в 100 мл толуола добавляют порциями 1,58 г (6,79 ммоль) тетрахлорида циркония. Реакционной смеси дают нагреваться до комнатной температуры, и после 24-часового перемешивания получают суспензию оранжевого цвета. После отделения нерастворимого вещества и сгущения досуха получают красное масло. Путем добавления 20 мл пентана и последующей переработки получают 1,54г (43%) обоих диастереомеров анса-цирконоцена в качестве порошка оранжевого цвета. Точка плавления: 151oC (разл., определенная путем дифферециально-сканирующей калометрии).
Нижеследующие примеры более подробно поясняют способ согласно изобретению.
Пример 25
В полимеризационный реактор емкостью 500 мл подают в качестве сокатализатора метилалюмоксан, растворяют в 250 мл толуола и охлаждают до -50oC. При помощи газоподводящей трубы пропускают пропен, причем избыточный пропен может улетучиваться через счетчик пузырьков. Как только имеется желаемое количество жидкого пропена (приблизительно, 39 до 35 мл), подачу мономера прекращают. Затем устанавливают желаемую температуру полимеризации. После чего добавляют раствор указанного в таблице 1 катализатора а)-в) в небольшом количестве толуола. По истечении необходимого времени полимеризации реакцию прекращают путем добавления 500 мл солянокислого метанола, причем избыточный пропен улетучивается при интенсивном кипении раствора. Выделение полимера осуществляется путем отделения толуольной фазы и экстракции водно-метанольной фазы диэтиловым эфиром. Соединенные толуольные и этиловые фазы сгущают досуха в вакууме.
Данные по параметрам опыта и достигнутым при этом результатам приведены в таблице 1.
Пример 26
В стальном автоклаве объемом 2 дм3 с отшлифованными поверхностями стенок проводят газофазную полимеризацию этилена. Кипящий слой создается механическим путем при помощи способной к перемещению по стенкам двухвинтовой мешалки с применением 10 г полиэтиленового порошка. Через бюретку последовательно добавляют сокатализатор (2 ммоль триизобутилалюминия в 2 см3 изопентана), и 1 г 4-(η5-циклопентадиенил)-4,7,7-триметил-(η5-4,5,6,7- тетрагидроинденил)дихлорциркония (25,8 ммоль Zr) на SiO2-носителе. Затем проводят полимеризацию в течение 1 часа при 8 бар парциального давления этилена при температуре 80oC. Реакцию прекращают путем сброса давления в автоклаве. Получают 36 г полиэтилена соответственно активности 3,6 кг полиэтилена/г металлоцена. Коэффициент вязкости полимера составляет 70 мл/г.
Пример 27
Сухой реактор объемом 1,5 дм3 промывают азотом и наполняют при 20oC 0,75 дм3 деароматизированной бензиновой фракции с пределами кипения от 100 до 120oC. Затем газовое пространство реактора промывают до свободного от азота состояния путем 5-кратного напрессовывания 2 бар пропилена и понижения давления. Затем добавляют 3,75 дм3 толуольного раствора метилалюмоксана (5 ммоль Al, n = 18). При перемешивании реактор нагревают до 30oC, а при скорости вращения мешалки 500 об/мин добавляют мономеры (парциальное давление этилена и пропилена, а также количество 5-этилиден-2-норборнена в см3, см. таблицу 2).
0,125 мг металлоцена 4-(η5-3'-метилциклопентадиенил)-4,7,7-три-метил-(η5-2- метил-4,5,6,7-тетрагидроинденил)]дихлорциркония растворяют в 1,25 см3 толуольного раствора метилалюмоксана (1,67 ммоль Al, n = 18) и в течение 15 минут получаемый раствор оставляют стоять для завершения реакции, после чего раствор подают в реактор, подлежащую полимеризации среду доводят до 50oC и соответствующим охлаждением держат при этой температуре в течение часа. Затем путем добавления 2 мл изопропанола полимеризацию прекращают, полимер осаждают путем спуска содержимого реактора в ацетон и сушат в вакууме при 80oC (полимер стабилизуют ирганоксом 1010, 0,1 вес.%). Параметры опыта и достигнутые при этом результаты приведены в таблице 2.
Пример 28
В автоклав емкостью 1,5 дм3, который подвергают предварительной тщательной промывке аргоном, подают 600 см3 раствора 180 см3 стирола (дистиллированного при пониженном давлении) в толуоле. Путем многократного напрессовывания аргона (1 бар) раствор насыщают аргоном. В подготовленный таким образом реактор подают противотоком 10 см3 толуольного раствора метилалюмоксана (10,1 вес. %-ный раствор метил-алюмоксана молекулярного веса 1300 г/моль по криоскопическому определению). Раствор 10 мг 4- (η5 -3'-изопропил-циклопентадиенил)-4,7,7-триметил-(η5-4,5,6,7-тетрагидроинденил), дихлорциркония в 10 см3 толуольного раствора метилалюмоксана добавляют после предварительной 15-минутной активации. (В случае регулирования молекулярного веса с помощью водорода можно здесь напрессовать водород.) При перемешивании (750 об/мин) полимеризацию проводят в течение двух часов, при температуре 70 oC. Затем полимеризационную смесь выпускают в сборник и сразу добавляют 5 дм3 этанола, перемешивают в течение 10 минут, и выпавший продукт фильтруют. Фильтровальный осадок три раза промывают, попеременно 10%-ной соляной кислотой и этанолом. Затем промывают водой до нейтральной реакции, остаток суспендируют в этаноле и снова фильтруют. Очищенный таким образом полимер сушат в течение 15 часов при 80oC в вакууме (0,2 бар).
После сушки получают 5,2 г полимера, имевшего температуру стеклования 102oC.
Пример 29
В автоклав емкостью 1,5 дм3 который подвергают предварительной тщательной промывке этеном, подают 600 см3 раствора 180 см3 стирола (дистиллированного при пониженном давлении) в толуоле. Путем многократного напрессовывания этена (1 бар) раствор насыщают этеном. В подготовленный таким образом реактор подают противотоком 10 см3 толуольного раствора метилалюмоксана (10,1 вес. %-ный раствор метилалюмоксана молекулярного веса 1300 г/моль по криоскопическому определению). Раствор 10 мг 4- (η5-3'-изопропил-циклопентадиенил)-4,7,7-триметил-(η5-4,5,6,7-тетрагидроинденил) дихлорциркония в 10 см3 толуольного раствора метилалюмоксана добавляют после предварительной 15-минутной активации. (В случае регулирования молекулярного веса с помощью водорода можно здесь напрессовать водород). При перемешивании (750 об/мин) полимеризацию проводят при температуре 70oC в течении часа, причем путем дополнительной подачи давления этена держат при 1 бар. Затем полимеризационную смесь выпускают в сборник, добавляют 5 дм3 этанола, перемешивают в течение 10 минут, а затем выпавший продукт фильтруют. Фильтровальный осадок три раза промывают, попеременно 10 %-ной соляной кислотой и этанолом. Затем промывают водой до нейтральной реакции, остаток суспендируют в этаноле и снова отфильтруют. Очищенный таким образом полимер сушат в течение 15 часов при 80oC в вакууме (0,2 бар). После сушки получают 21 г бесцветного полимера, имеющего температуру стеклования -24oC и коэффициент вязкости 30 см3/г.
Пример 30
Для получения раствора катализатора растворяют 10 мл металлоцена а) (см. пример 25) в 10 мл толуольного раствора метилалюмоксана и перемешивают в течение 15 минут. В подвергнутый инертизации реактор с мешалкой емкостью 1,5 дм3 подают 900 мл дизельного топлива (диапазон кипения 100-120oC) и нагревают до 70 oC. Раствор катализатора добавляют и при 750 об/мин проводят одночасовую полимеризацию этилена (7 бар), после чего давление в реакторе сбрасывают, полимер фильтруют из суспензии, промывают ацетоном и сушат в течение 12 часов в вакуумном сушильном шкафу. Получают 39,2 г полиэтилена с коэффициентом вязкости 72 см3/г.
Пример 31
Пример 25 повторяют в применении следующих металлоценов 1 до 5.
1: [4-(η5-циклопентадиенил)-4,7,7-триметил-(η5-4,5,6,7- тетрагидроинденил)]-дихлорцирконий
2:[4-(η5-циклопентадиенил)-4,7-диметил-7-бутил-(η5-4,5,6,7-тетрагидроинденил)]-дихлорцирконий
3:[4-(η5-циклопентадиенил)-4,7-диметил-7-фенил-(η5-4,5,6,7-тетрагидроинденил)]-дихлорцирконий
4:[4-(η5-3-метил-циклопентадиенил)-4,7,7-диметил-(η5-4,5,6,7-тетрагидро-инденил)]дихлорцирконий
5: [4-(η5-трет. -бутил-циклопентадиенил)-4,7,7-диметил-(η5-4,5,6,7-тетрагидро-инденил)]дихлорцирконий
Данные по параметрам опыта и достигнутым при этом результатам приведены в таблице 3.
Пример 32
В лабораторный автоклав в атмосфере азота подают 500 мл дизельного топлива (диапазон кипения 100 - 120oC), 20 мл гексена и 10 мл 10 вес. %-ного раствора метилалюмоксана в толуоле были поданы под азотом и нагревают до 70oC при перемешивании со скоростью 700 об/мин. 10 мг металлоцена N 5 растворяют в 1 мл 10 вес.%-ного толуольного раствора метилалюмоксана. Полимеризацию начинают путем добавления раствора металлоцена и металлалюмоксана и напресовывания 4 бар этилена. По истечении 15 минут полимеризацию прекращают подачей CO2 и содержимое реактора добавляют к 200 мл метанольной соляной кислоты. Смесь перемешивают в течение 5 часов для удаления алюминия, затем полимер отфильтровывают, промывают водой и ацетоном и для определения выхода сушат в течение 12 часов в вакууме при 80oC.
Получают 4,8 г сополимера этилена и 1-гексена с коэффициентом вязкости 70 см3/г. Для удаления остаточного сомономера пробу в количестве 1 г при нагревании растворяют в дизельном топливе (диапазон кипения 100-120oC), затем осаждают, фильтруют, промывают ацетоном и еще раз сушат в вакууме при 80oC. Согласно данным дифференциально-сканирующей калометрии точка плавления составляет 110,5oC, а согласно 13 C-ЯМР содержание гексена равно 4,6 мол.%.
Пример 33
Опыт Й примера 25 повторяют с применением 10 мг металлоцена [4-(η5-3-изопропил-циклопентадиенил)-4,7,7-диметил-(η5-4,5,6,7-тетрагидроинденил)] -дихлорциркония. Получают 4 г сополимера с коэффициентом вязкости 22 см3/г, который после чистки имеет определенную путем дифференциально-сканирующей калометрии точку плавления 102oC. Согласно данным 13 C-ЯМР содержание гексена составляет 7,1 мол.%.
Физико-химические характеристики соединений примеров 11 - 20, 22, 23
Соединение примера 11
1H-ЯМР (200.1 МГц, CDCl3); δ = 7.06-7.03, 6.94-6.91, 6.82-6.76, 5.87-5.84, 5.82-5.78, 5.62-5.59 (6 x m, 7H, 1-H до 3-H и 2'-H до 5'H); 2.45 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq) = 14.2 Гц, 3J(H6ax/H5eq) = 6.3 Гц, 3J(H6eq/H5eq) = 2.7 Гц); 2.31 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)=14.0 Гц, 3J(H6ax/H5ax)=14.0 Гц, 3J(H6eq/H5ax)= 6.2 Гц); 1.91 (ddd, 1H, 6ax-H, 2J(H6eq/H6ax)= 14.0 Гц, 3J(H5ax/H6ax)= 14.0 Гц, 3J(H5eq/H6ax)= 6.3 Гц); 1,69 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)=14.0 Гц, 3J(H5ax/H6eq)=6.2 Гц, 3J(H5eq/H6eq)=2.7 Гц); 1.86 (s, 3H, 10-H); 1.25 и 1.11 млн.д. (2 x s, 6H, 11-H и 12-H).
Соединение примера 12
1H-ЯМР (200.1 МГц, CDCl3); δ =6.73-6.70, 6.44-6.41,5.73-5.70 (3 x m, 3H, 1-H до 3-H), 6.70-6.67, 6.53-6.48, 6.08-6.03, 5.88-5.82 (4 x m, 4H, 2'-H до 5'-H); 2.42 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq)=14.8 Гц, 3J(H6ax/H5eq)=6.0 Гц; 3J(H6eq/H5eq)=2.2 Гц); 2.30 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)=14.8 Гц 3J(H6ax/H5ax)=14.3 Гц, 3J(H6eq/H5ax)=5.3 Гц; 2.00 (ddd, 1H, 6ax-H, 2J(6eqH6ax)= 14.8 Гц, 3J(H5ax/H6ax)= 14.3 Гц, 3J(H5eq/H6ax)=6.0 Гц); 1.72 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)=14,8 Гц, 3J(H5ax/H6eq)=5.3 Гц, 3J(H5eq/H6eq)= 2.2 Гц); 1,83 (s, 3H, 10-H); 1.33 и 1.10 млн.д. (2 x s, 6H, 11-H и 12-H).
Соединение примера 13
1H-ЯМР (200.1 МГц, CDCl3): δ = 7.24-6.89 (т, 5H, Ph-H); 6.78-6.73, 6.54-6.50, 6.22-6.20, 5.97-5.94 (4 x m, 7H, 1-H до 3-H и 2'-H до 5'-H); 2.30-2.22, 1,92-1.84 (2 x m, 4H, 5-H, 6-H); 1.76, 1.71 млн.д. (2 x s, 6H, 10-H и 11-H).
Соединение примера 14
1H-ЯМР (200.1 МГц, CDCl3): δ =6.73-6.67, 6.52-6.47, 6,41-6.38, 6.08-6.04, 5.87-5.83, 5.76-5.73 (6 x m, 7H, 2'-H до 5'-H и 1-H до 3-H); 2.48-2.16 (м, 3H, 5eq-H, 5ax-H, 6ax-H); 1.91-1.84 (m, 1H, 6eq-H); 1.83 (s, 3H, 10-H); 1.35-0.85 (3 x m, 6H, nBu-CH2); 1.25 (s, 3H, 11-H); 0.82-0.77 млн.д. (pt, 3H, nBu-CH3).
Соединение примера 15 (транс-изомер)
1H-ЯМР (200.1 МГц, CDCl3): δ =6.63-6.58, 6.42-6.39, 6.33-6.30, 5.99-5.96, 5.81-5.78, 5.66-5.63 (6 x m, 7H, 2'-H до 5'-H и 1-H до 3-H); 2.38 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq)=14.0 Гц, 3J(H6ax/H5eq)=5.7 Гц, 3J(H6eq/H5eq)= 3.2 Гц); 2.23 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)=14.0 Гц, 3J(H6axH5ax)=14.4 Гц, 3J(H6eq/H5ax)=6.8 Гц); 1.98 (ddd, 1H, 6ax-H, 2J(H6eqH6ax)=14,4 Гц, 3J(H5axH6ax)=14,4 Гц, 3J(H5eq/H6ax)=5.7 Гц; 1,85 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)= 14.4 Гц, 3J(H5axH6eq)=6.8 Гц, 3J(H5eqH6eq)=3.2 Гц); 1.90 (s, 3H, 10-H); 1.27 (s, 3H, 11-H); 1.35-1.07 (3 х m, 6H, nBu-CH2); 0.84-0.76 млн.д. (pt, 3H, nBu-CH3).
Точка плавления: 151oC (определенная путем дифференциально-сканирующей калометрии).
Соединение примера 16
1H-ЯМР (200.1 МГц, CDCl3): δ =7.06-6.96, 6.95-6.92, 6.82-6.74, 5,89-5.85, 5.83-5.79, 5.64-5.61 (6 x m, 7H, 2'-H до 5'-H и 1-H до 3-H); 2.40-2.27, 1.89-1.75 (2 x m, 4H, 5eq-H, 5ax-H, 6ax-H, 6eq-H); 1.86 (s, 3H, 10-H); 1.35-0.89 (m, 6H, nBu-CH2); 1.21 (s, 3H, 11-H); 0.84-0.77 млн.д. (pt, 3H, nBu-CH3).
Точка плавления: 134oC (определенная путем дифференциально-сканирующей калометрии).
Соединение примера 17
1H-ЯМР (200.1 МГц, CDCl3): δ =6.76-6.72, 6.69-6.65, 6.53-6.50, 6.43-6.32, 5.99-5.97, 5.88-5.82, 5.72-5.61 (7 x m, 12H, 1-H, 2-H, 3-H, 2'-H, 4'-H, 5'-H); 2.37-2.33, 2.10-1.85, 1.75-1.62 (3 x m, 8H, 5-H и 6-H); 1.82, 1.81 (2 x s, 6H, 10-H); 1,33 (bs, 6H, 11-H или 12-H); 1.31, 1.25 (2 x s, 18H, tBu-CH3); 1,12, 1,09 млн.д. (2 x s, 6H, 11-H или 12-H).
Соединение примера 18
1H-ЯМР (200.1 МГц, CDCl3): δ =6.58-6.50, 6.38-6.34, 5.91-5.87, 5.47-5.53, 5.34-5.31 (5 x m, 7H, 1-H до 3-H и 2'-H до 5'-H); 2.18 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq)= 14.0 Гц, 3J(H6ax/H5eq)=5.9 Гц, 3J(H6eq/H5eq)=3.1 Гц; 2,09 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)= 14,0 Гц, 3J(H6eq/H5ax)=14.0 Гц, 3J(H6eq/H5ax)= 5.3 Гц); 1.80 (ddd, 1H, 6ax-H, 2J(H6eq/H6ax)= 14.0 Гц, 3J(H5ax/H6ax)=14.0 Гц, 3J(H5eqH6ax)=5.9 Гц; 1.57 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)= 14.0 Гц, 3J(H5ax/H6eq)=5.3 Гц, 3J(H5eq/H6eq)=3.1 Гц; 1,53 (s, 3H, 10-H); 1,19, 1.12 (2 x s, 6H, 11-H и 12-H), 0.26 и 0.34 млн.д. (2 x s, 6H, 13-CH3 и 14-CH3).
Т. пл. : 114oC. (определенная путем дифференциально-сканирующей калометрии).
Соединение примера 19
1H-ЯМР (200.1 МГц, CDCl3): δ =7.05-7.01, 6.94-6.91, 6.85-6.80, 6.75-6.73, 5.87-5.79, 5.63-5.61 (6 x m, 2'-H до 5'-H и 1-H до 3-H); 5.63-5.40, 5.15-4.80 (2 x m, винил-CH и винил-CH3); 2.38-2.17, 2.10-2.06, 1.86-1.77 (3 x m, 5-H, 6-H, аллил-CH2); 1,85 (s, 10-H); 1.24, 1.10 млн.д. (2 x s, 11-H).
Соединение примера 20
1H-ЯМР (200.1 МГц, CDCl3): δ =6.73-6.67, 6.55-6.47, 6.41-6.38, 6.08-6.04, 5.94-5.80, 5.76-5.72 (6 x m, 2'-H до 5'-H и 1-H до 3-H); 5.62-5.41, 5.20-4.83 (2 x m, винил-CH и винил-CH2); 2,55-2.17, 2.09-2.05, 1.97-1.69 (3 x m, 5-H, 6-H, аллил-CH2); 1.83 (s, 3H, 10-H); 1.27, 1.09 млн.д. (2 x s, 11-H (цис-изомер) и 11-H (транс-изомер)).
Соединение примера 22
1H-ЯМР (200.1 МГц, CDCl3): δ =6.79-6.75, 6.48-6.38, 6.24-6.21, 5.99-5.95, 5.56-5.54, 5.44-5.41 (6 x m, 6H, 1-H, 2-H, 3-H, 2'-H, 4'-H, 5'-H); 2,91 (s, 1H, iPr-CH, 3J(iPr-CH3/iPr/CH)= 6.9 Гц); 2.41 (ddd, 1H, 5eq-H, 2J(H5ax/H5eq)= 14.5 Гц, 3J(H6ax/H5eq)=6.2 Гц, 3J(H6eq/H5eq)=2.8 Гц); 2.28 (ddd, 1H, 5ax-H, 2J(H5eq/H5ax)=14.5 Гц, 3J(H6ax/H5ax)=14.5 Гц, 3J(H6eq/H5ax)= 5.6 Гц); 2.01 (ddd, 1H, 6ax-H, 2J(H6eq/H6ax)= 14.5 Гц, 3J(H5ax/H6ax)=14.5 Гц, 3J(H5eq/H6ax)=6.2 Гц; 1.72 (ddd, 1H, 6eq-H, 2J(H6ax/H6eq)= 14.5 Гц, 3J(H5axH6eq)=5.6 Гц, 3J(H5eq/H6eq)=2.8 Гц; 1.78(s, 3H, 10-H); 1.32, 1.11 (2 x s, 6H, 11-H и 12-H); 1.24, 1.09 млд.д.(2 x d, 6H, iPr-CH3, 3J(iPr-CH/iPr-CH3)=6.9 Гц.
Точка плавления: 193oC (определенная путем дифференциально-сканирующей калометрии).
Соединение примера 23
1H-ЯМР (200.1 МГц, CDCl3): δ =6.44-6.41, 6.24-6.15, 5.95-5.91, 5.68-5.60, 5.33-5.29, 5.18-5.17 (6 x m, 10H, 2'-H, 4'-H, 5'-H, 1-H и 3-H); 3.13-2.83, 2.46-2.16, 2.08-1.93, 1.78-1.72 (4 x m, 12H, 2 x iPr-CH и 5-H и 6-H); 1.76, 1.72 (2 x s, 6H, 10-H); 1.28-1.07 мнл.д. (m, 36H, 11-H, 12-H, 4 x iPr-CH3).
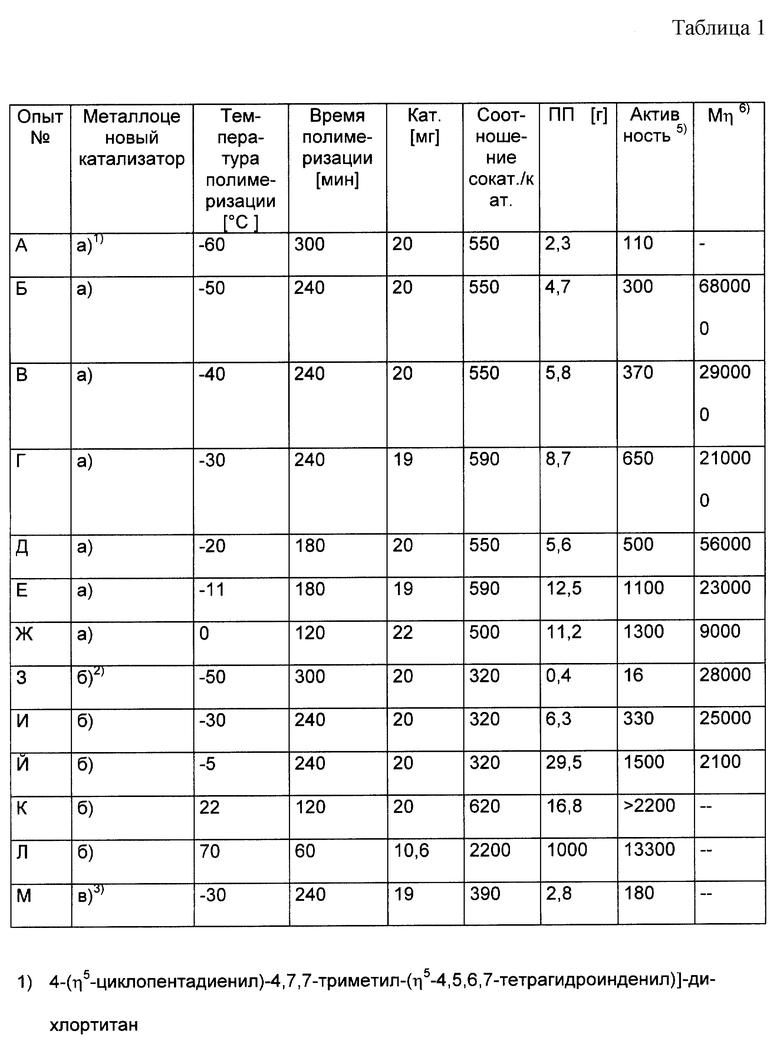

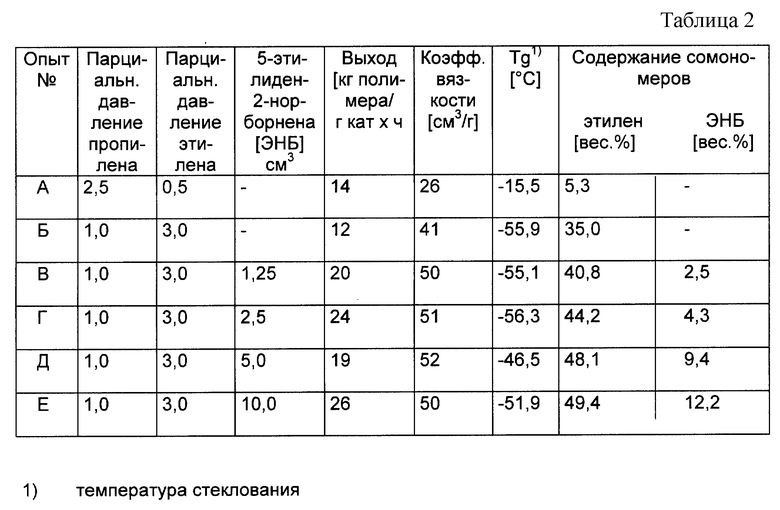
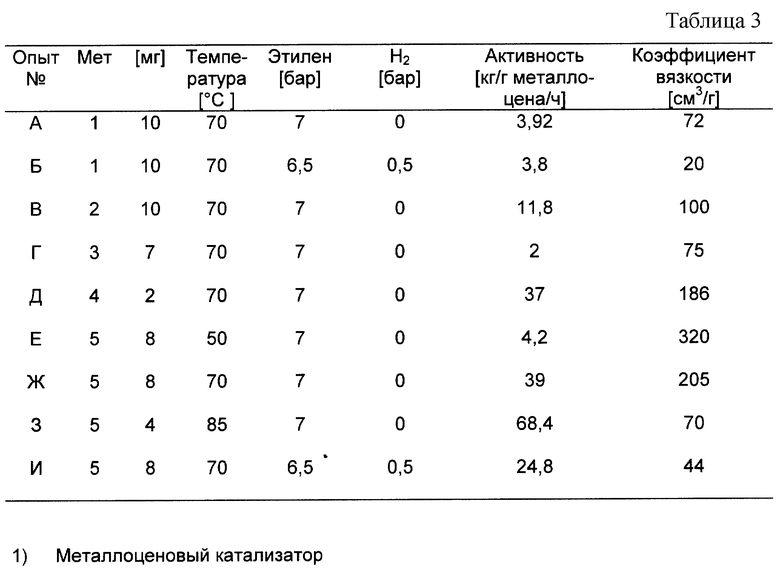
Описывается металлоценовый катализатор для получения полимера олефинов, представляющий собой стерически жесткое металлоценовое соединение, содержащее в качестве лигандов по меньшей мере две замещенные или незамещенные циклопентадиенильные группы, связанные между собой через моноциклическую кольцевую систему, причем одна циклопентадиенильная группа анеллирована к моноциклической системе, и эта система лигандов отлична от 4-η5-3-алкил-циклопентадиенил)-4,6,6-триметил-η5-2-алкил-4,5-тетрагидропенталена) и представляет собой соединение формулы I, где М - металл группы IVб Периодической системы, R1 и R2 одинаковы или различны и означают атом галогена, алкил с 1-10 атомами углерод, или группу NR2 13, где R13 означает алкил с 1-10 атомами углерода, R3, R4, R5, R6, R7, R8 и R9 одинаковы или различны и означают атом водорода, алкил с 1-10 атомами углерода, или остаток -R13-SiR
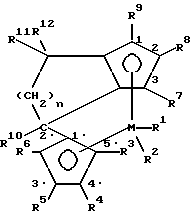
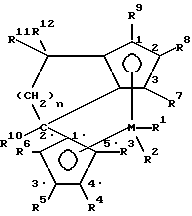
где M - металл группы IVб Периодической системы;
R1 и R2 одинаковы или различны и означают атом галогена, алкил с 1 - 10 атомами углерода или группу NR2 13, где R13 означает алкил с 1 - 10 атомами углерода;
R3, R4, R5, R6, R7, R8 и R9 одинаковы или различны и означают атом водорода, алкил с 1 - 10 атомами углерода, или остаток -R13 -SiR3 13-, где R13 имеет вышеуказанное значение;
R10 - алкил с 1 - 20 атомами углерода;
R11 и R12 одинаковы или различны и означают алкил с 1 - 20 атомами углерода, арил с 6 - 20 атомами углерода, алкенил с 2 - 12 атомами углерода;
n - целое число от 1 до 10.
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОКИПЯЩИХ ФТОРПАРАФИНОВ | 0 |
|
SU407870A1 |
| Катализатор высокотемпературной полимеризации этилена и сополимеризации этилена с @ -олефинами | 1987 |
|
SU1641193A3 |
| Способ получения титаноценов | 1988 |
|
SU1713438A3 |
| Задающий генератор | 1973 |
|
SU490256A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| УСТРОЙСТВО ДЛЯ ОТМЫВАНИЯ КЛЕЙКОВИНЫ | 1970 |
|
SU421209A3 |
| Задающий генератор | 1973 |
|
SU490256A1 |
Авторы
Даты
2000-07-27—Публикация
1994-12-21—Подача