Изобретение относится к синтезу органических соединений, в частности получению одорантов для природного газа, используемого как топливо в теплоэнергетике, автотранспорте и других отраслях промышленности.
Способы получения меркаптанов или тиолов достаточно широко известны в органической химии (см. Химическая энциклопедия.- М.: Большая Российская Энциклопедия, 1995, т. 4, c. 573). В частности, используются методы, основанные на использовании реакций, приводящих к замещению гидроксильных групп в спиртах на тиогруппы. Так, метилмеркаптан синтезируют путем взаимодействия раствора гидросульфида калия (получается путем насыщения раствора гидроксида калия сероводородом) с нейтрализованной гидроксидом натрия, упаренной и отфильтрованной от кристаллов сульфата смесью дымящей серной кислоты и абсолютного метилового спирта. Реакция идет при 30oC. Выделившийся в ходе реакции продукт конденсируют в приемнике, охлаждаемом смесью соли и снега до -15oC (см. Рапопорт Ф.М., Ильинская А.А. Лабораторные методы получения чистых газов. - М.: Госхимиздат, 1963, c. 414-419). В качестве примесей присутствует некоторое количество сероводорода и метилсульфида. Однако выход продукта в данной реакции по метанолу невысокий и составляет 10-15%. Недостатком метода является также наличие побочных продуктов в виде сульфатных солей. Помимо этого недостаточно полной может быть конденсация метилмеркаптана, т.к. при указанной температуре он обладает относительно высоким давлением насыщенных паров.
Способ получения чистого метилмеркаптана с высокими выходами (порядка 90%) заключается в следующем. Метилизотиомочевину и диметилсульфат растворяют в воде, после упаривания и добавления спирта кристаллизуется сернокислая соль, разложением которой путем нагревания с раствором щелочи получают собственно метилмеркаптан (см. Губен И. Методы органической химии.- М.: ОНТИ, 1935, т. 3, вып. 3, c. 494). В качестве побочных продуктов выделяется, как и в предыдущем случае, сульфат натрия, а также твердый дициандиамид. Диметилсульфат для данной реакции может быть получен при реакции между хлорсульфоновой кислотой и метиловым спиртом, проводимой при охлаждении реакционной смеси. В данном случае недостатками способа является как наличие побочных продуктов, так и более высокая стоимость реагентов, препятствующая использованию метода в широком масштабе. Кроме того, используемые вещества обладают повышенной токсичностью.
Известен также способ получения метилмеркаптана, включающий прямой синтез метилмеркаптана из газовой смеси, содержащей пары метилового спирта и сероводород, при давлении от 5 до 15 бар и температуре в пределах 300-500oC в присутствии катализатора на основе оксида алюминия. Из продукционной смеси метилмеркаптан выделяют абсорбционными и дистилляционными методами. Исходная газовая смесь содержит избыток сероводорода при мольном соотношении сероводорода к метанолу 1,1: 3. Не вступившие в реакцию реагенты находятся в обороте при добавлении необходимого количества сероводорода и метилового спирта для образования смеси в потребном количестве с исходным составом (см. EP 0850922 A1, C 07 C 319/08, 01.07.1998). По одному из примеров проведения вышеуказанного процесса при мольном соотношении сероводорода к метанолу на уровне 1,8 условный выход по спирту составляет около 75% (соответственно по сероводороду - около 40%). Основной недостаток способа состоит в применении высокого давления при обязательном требовании к производству, состоящему в предотвращении малейшего попадания метилмеркаптана и сероводорода в окружающую среду.
Наиболее близким к предлагаемому способу является прямой синтез метилмеркаптана из бинарной смеси эквивалентных количеств паров метилового спирта и сероводорода, осуществляемый при атмосферном давлении пропусканием смеси над катализатором (пемза, покрытая на 1/3 азотнокислым торием и нагреваемая сначала до 270oC, а затем до 400oC) при 380oC (см. Губен И. Методы органической химии. - М. : ОНТИ, 1935, т. 3, вып. 3, с. 494). При более высоких температурах продукт, согласно данным автора монографии, разлагается на сероводород и соответствующий алкен (непредельный углеводород). После осуществления каталитической реакции остаются неизрасходованные реагенты: сероводород и метиловый спирт, которые загрязняют окружающую среду. Для предотвращения этого их необходимо улавливать, что снижает экономическую эффективность метода. Еще одним недостатком, присущим большинству известных способов синтеза метилмеркаптана, когда в качестве одного из реагентов выступает сероводород, является получение различных отходов, например в виде растворов солей органических соединений. Выход продукта при указанных условиях проведения процесса составляет не более 41%.
Известен способ получения катализатора для производства метилмеркаптана из паров метилового спирта и сероводорода, включающий пропитку пористого носителя, например пемзы, раствором нитрата тория и термическое разложение этой соли путем ступенчатого нагревания сначала до 270oC, а затем до 400oC (см. Губен И. Методы органической химии.- М.: ОНТИ, 1935, т. 3, вып. 3, c. 494). Собственно каталитическим действием обладает образующийся при этом оксид тория (ThO2), являющийся согласно имеющимся сведениям наиболее эффективным для проведения процесса. При этом, однако, используемые соединения тория обладают естественной радиоактивностью, что является недостатком способа.
Наиболее близким к предлагаемому изобретению является способ получения катализатора для прямого синтеза метилмеркаптана из смеси паров метилового спирта и сероводорода, включающий пропитку пористого носителя, например оксида алюминия с удельной поверхностью 350 м2/г водными растворами соединений вольфрама и калия с последующей термообработкой (см. а.с. RU 2120822 C1, 6 B 01 J 23/30, 27.10.98. Бюл. N 30). Основным недостатком способа является получение катализатора, в котором собственно каталитическим действием обладают получаемые оксиды вольфрама (VI) в аморфном виде, с недостаточной для масштабного производства активностью, которой не обеспечивается высокая степень взаимодействия метилового спирта и сероводорода.
Известен способ получения сероводорода, основанный на взаимодействии водорода и серы при определенной температуре (Некрасов Б.В. Основы общей химии, т. 1. - M. : Химия, 1965, с. 310). Процесс взаимодействия может быть описан следующей реакцией:
H2 + S = H2S + 5 ккал.
Сложность проведения подобного процесса не привела к его техническому использованию.
Наиболее близким к предлагаемому изобретению является способ получения сероводорода, основанный на действии разбавленных кислот на сульфиды металлов, например на сернистое железо (Некрасов Б.В. Основы общей химии, т.1.- M.: Xимия, 1965, с. 310)
FeS+2HCl=FeCl2+H2S.
Недостатки данного способа - невозможность организации циклического процесса и высокая стоимость соляной кислоты.
Общей технической задачей настоящего изобретения является создание автономного (главным образом не привязанного к производству сероводорода) простого безотходного способа получения метилмеркаптана, обеспечивающего достаточно полное использование реагентов и выделение продукта из реакционной смеси. При этом одновременно решаются задачи получения катализатора, обеспечивающего более высокую степень взаимодействия метилового спирта и сероводорода без применения радиоактивных реагентов, и реализации такого способа получения сероводорода, который обеспечивает безотходность производства в целом.
По сути создаваемое изобретением автономное производство метилмеркаптана требует лишь поставок недифицитных серной кислоты и метилового спирта.
Основные технические результаты при реализации изобретения состоят в увеличении выхода основного продукта и степени превращения исходных реагентов, в безопасном проведении процесса катализа, в защите окружающей среды из-за практически полного предотвращения выбросов газов, содержащих вредные вещества, твердых и жидких отходов.
Указанные технические результаты достигаются за счет того, что в способе производства метилмеркаптана, включающем пропускание бинарной смеси паров метилового спирта и сероводорода при атмосферном давлении через последовательно установленные по ходу смеси трубчатые реакторы с катализатором, возврат непрореагировавших компонентов смеси в голову процесса при добавлении необходимого количества метилового спирта и сероводорода и выделение компонентов из продукционной газовой смеси путем конденсации, в качестве катализатора используют оксиды молибдена или вольфрама, процесс проводят при температуре 390-430oC и объемной скорости смеси в реакторах на уровне 100-1000 ч-1 с использованием сероводорода, полученного при взаимодействии разбавленной кислоты и сульфида металла, а конденсацию проводят ступенчато с выделением образовавшейся при реакции воды охлаждением газовой смеси до 70-90oC, непрореагировавшего метилового спирта - охлаждением до 8-30oC и образовавшегося метилмеркаптана путем пропускания оставшейся смеси при температуре 0- (-5)oC через раствор, нейтральный по отношению к сероводороду соли, например хлорида кальция с концентрацией 0,5-6 мас.%. Число последовательно установленных реакторов составляет не менее двух, преимущественно 2-6. Исходную бинарную смесь приготавливают путем пропускания сероводорода через метиловый спирт, а содержание метилового спирта в смеси регулируют изменением его температуры. По одному из вариантов выделение воды, метилового спирта и метилмеркаптана проводят после каждого реактора, оставшийся сероводород пропускают через метиловый спирт, а полученную смесь направляют на следующий реактор, причем в смеси, поступающей на каждый реактор, поддерживают эквимолярный состав реагентов. По другому варианту исходная смесь содержит двух-пятикратный избыток метилового спирта против эквимолярного количества, выделение воды проводят после каждого реактора, а выделение метилового спирта и метилмеркаптана - на выходе из последнего реактора.
В способе получения катализатора для производства метилмеркаптана из бинарной смеси паров метилового спирта и сероводорода, включающем приготовление раствора, содержащего соединения вольфрама или молибдена, пропитку полученным раствором пористого носителя и его последующую сушку и обжиг, для приготовления раствора с концентрацией от 0,1 мас.% до насыщенного используют вольфрамат или молибдат аммония, в раствор вводят водорастворимый полимер в количестве 0,1-30 мас.% от массы взятой воды, пористый носитель до пропитки подвергают формовке и спеканию, после пропитки осуществляют сушку при температуре 50-120oC и обжиг на воздухе при температуре 400-450oC в течение 1-4 ч и далее в токе инертного газа, например азота, при температуре 300-450oC в течение 1-4 ч. В качестве пористого носителя используют шамот - ультралегковес или диатомит. В качестве водорастворимого полимера используют метилцеллюлозу, поливинилпирролидон или поливиниловый спирт.
В способе получения сероводорода для производства метилмеркаптана путем разложения сульфида металла кислотой в качестве кислоты используют серную кислоту, а в качестве сульфида металла - сульфид бария в кускообразном виде с крупностью фракции 5-20 мм, образовавшийся при взаимодействии сульфат бария восстанавливают природным газом в противоточном пересыпном термохимическом реакторе при температуре 950-1050oC в течение 50-60 мин, а полученный при этом сульфид бария вновь направляют на взаимодействие.
Заявляемый способ получения метилмеркаптана включает, как и известный, пропускание смеси заданных количеств сероводорода и паров метилового спирта через катализатор, полученный путем пропитки пористого носителя водным раствором соединений вольфрама или молибдена с последующей сушкой и обжигом, а также конденсацию полученного продукта при охлаждении. Помимо этого он имеет следующие отличия. В качестве носителя катализаторов используют материал, которому предварительно задают необходимую конфигурацию и размер путем формовки и спекания, например шамот - ультралегковес, аэросил и пр. Для получения катализаторов в качестве растворов солей используют растворы с концентрацией от 0,1 мас.% до насыщенных, а соли берут не дающие после термообработки посторонних примесей в катализаторе, например молибдат или вольфрамат аммония. Растворы для пропитки носителей включают, кроме того, водорастворимый полимер в количестве 0,1-30 мас.% от массы взятой воды, после пропитки носители подвергают сушке при 50-120oC до удаления влаги. Обжиг проводят на воздухе при 400-450oC в течение 1-4 ч и далее с продувкой инертным газом, например азотом, при 300-450oC до восстановления оксида переходного металла с получением не менее 3% низших оксидов вольфрама или молибдена и приобретения катализатором интенсивной синей или фиолетовой окраски в течение 1-4 ч.
Сероводород для синтеза метилмеркаптана получают следующим образом. Исходный сульфат щелочноземельного металла, например бария, с крупностью фракции 5-20 мм восстанавливают до сульфида природным газом в противоточном пересыпном термохимическом реакторе при температуре 950-1050oC и общем времени пребывания в указанном реакторе 50-60 мин. Далее полученный сульфид обрабатывают серной кислотой с выделением сероводорода, а получающийся сульфат вновь направляют на восстановление. Необходимо, с нашей точки зрения, сделать следующее замечание. Известен способ восстановления сульфата бария природным газом в печах с кипящим слоем (см., например, Позин M.E. Технология минеральных солей, часть 1, издательство "Химия", Ленинградское отделение, 1970, с. 434). Высокотемпературный процесс в кипящем слое чрезвычайно сложен и имеет весьма малую степень (32-36%) использования восстановителя (природного газа). В случае предлагаемого изобретения значительно упрощается аппаратурное оформление при повышении степени использования природного газа до 50-60%.
Реакционную стехиометрическую смесь, используемую при каталитическом синтезе, готовят, пропуская газообразный сероводород через метиловый спирт или смешивая с его парами, регулируя содержание последнего в смеси путем изменения температуры метилового спирта. Далее реакционную смесь пропускают последовательно через реакторы, например трубчатого типа, с катализатором при температуре реакторов 350-430oC с объемной скоростью 100-1000 ч-1. Количество последовательно соединенных реакторов от 2 до 6, после каждого из них проводят конденсацию выделившейся в реакции воды охлаждением до 70-90oC, а затем метилового спирта охлаждением до 8-30oC и конденсацию метилмеркаптана - путем пропускания оставшейся части смеси при температуре 0-(-5)oC через раствор соли, не взаимодействующей с метилмеркаптаном и сероводородом, например хлорида кальция, в концентрации 0,5-6 мас.%. Оставшийся сероводород после пропускания через метиловый спирт направляют на следующий реактор. По другому варианту в реакционной смеси используют избыток метилового спирта по отношению к стехиометрическому от 2 до 5 раз. При этом конденсацию метилового спирта осуществляют после прохождения последнего реактора и операции конденсации воды. Сконденсированный метиловый спирт направляют на повторное использование в реакции путем подачи в емкости, через которые пропускают сероводород. Оставшийся после прохождения всех реакторов сероводород также направляют в начало цикла синтеза, смешивая его со свежим сероводородом, поступающим от обработки сульфида щелочноземельного металла серной кислотой.
Выбор в качестве носителей катализаторов материалов, которым путем формовки и спекания предварительно задают необходимую конфигурацию, обеспечивает при осуществлении реакции синтеза целевого продукта оптимальные условия контактирования газов с поверхностью катализаторов.
Использование насыщенных растворов солей, не дающих в ходе термообработки посторонних примесей, дает возможность получения катализаторов с максимальным насыщением поверхности носителя оксидами переходных металлов с одновременным уменьшением размера частиц кристаллизующихся при сушке солей, что приводит к увеличению удельной поверхности катализаторов. Концентрации солей, меньшие чем 0,1 мас.%, не обеспечивают достаточного количества катализатора при пропитке носителей.
Дополнительное введение в растворы для пропитки носителей водорастворимых полимеров, например поливинилового спирта, обеспечивает при сушке и обжиге пропитанных носителей еще более значительное увеличение удельной поверхности, связанное с тем, что полимер, связывая ионы, содержащие переходные металлы, препятствует кристаллизации солевых форм, приводя к их аморфизации. Помимо этого полимерсодержащие растворы обладают более высокой покрывающей и пленкообразующей способностью, лучше смачивают поверхность носителей, повышая равномерность каталитических покрытий. Выбор концентрации полимеров обусловлен тем, что при их содержании менее 0,1% от массы, взятой для приготовления раствора воды, не обеспечивается положительный эффект увеличения удельной поверхности и улучшения пленкообразования. С другой стороны, большие, чем 30% их концентрации, приводят к чрезмерному увеличению количества выделяющихся при обжиге газов, не давая дополнительно ощутимого положительного эффекта.
Интервал температур сушки заготовок выбран исходя из того, что при более низких температурах процесс удаления растворителя становится слишком длительным, а при более высоких происходит закипание не удалившегося еще растворителя, что приводит к нарушению сплошности каталитического покрытия и частичному разрушению носителя.
Нижний предел температуры обжига катализаторов выбран с тем расчетом, чтобы было обеспечено полное разложение солей, синтез оксида переходного металла, выгорание остатков полимерной части композиции. Верхний предел ограничен тем, что при более высоких температурах оксидный катализатор претерпевает рекристаллизацию, сопряженную с уменьшением его удельной поверхности, а также происходят нежелательные взаимодействия между покрытием и носителем, изменяющие химическую природу катализатора, снижающие активность последнего. Время обжига выбрано исходя из того, что за более короткий его промежуток не успевают достаточно полно осуществиться вышеназванные процессы, а более длительное время экономически нецелесообразно, приводя к дополнительному расходу энергии на обжиг, т.к. эти процессы практически реализованы в достаточной для обеспечения положительного эффекта мере. Дополнительный обжиг катализатора в среде инертного газа позволяет получить частично восстановленную форму оксида переходного металла (т.е. низшие оксиды вольфрама или молибдена, соответствующие химической формуле WO3-x, MoO3-x, где x = 0,05-0,5), которая обладает необходимой для осуществления синтеза метилмеркаптана каталитической активностью. Интервал температур обжига в данном случае выбран исходя из того, что более низкие температуры не приводят к восстановлению в достаточной мере оксида, а при более высокой температуре происходит его перекристаллизация с уменьшением удельной поверхности. Признаком, характеризующим осуществление частичного восстановления, является приобретение катализатором интенсивной синей или фиолетовой окраски, поэтому процесс термообработки проводят до приобретения указанного цвета в течение 1-4 ч.
Температура 350-430oC, при которой находился в реакторах катализатор, была выбрана с учетом того, что при более низкой температуре реакционная смесь не успевала нагреться до той степени, когда кинетические особенности прохождения реакции позволяли получать достаточно высокий выход метилмеркаптана. Более высокие температуры приводили к снижению выхода продукта за счет его термического разложения.
Объемная скорость пропускания реакционной смеси через катализатор 100-1000 ч-1 была взята потому, что при скоростях больше 1000 ч-1 реакция не успевала пройти достаточно полно и снижался выход продукта. Меньшие, чем 100 ч-1, скорости замедляли ход синтеза и были нецелесообразны из-за повышенного расхода катализаторов.
Крупность фракции 5-20 мм исходных сульфатов щелочноземельных металлов использована по той причине, что более крупные фракции не успевают прореагировать в термохимическом реакторе, а более мелкие требуют специального измельчения с дополнительными затратами времени и энергии, кроме того, выделяют значительное количество пыли. К преимуществам метода относится то, что используемые для получения сероводорода сульфаты низкой стоимости являются отходами других производств, что позволяет решить проблему утилизации и улучшения экологической обстановки. Температура термохимической обработки и ее время выбраны в пределах 950-1050oC и 50-60 мин соответственно, т.к. при более низких значениях указанных параметров не достигается достаточно высокая степень превращения в реакции восстановления до сульфидов. С другой стороны, верхние пределы выбраны так, чтобы не было дополнительного расхода энергии и времени сверх необходимого для получения положительного эффекта.
Выбор соотношения компонентов в реакционной смеси был основан на том, что в случае их стехиометрических количеств 1:1 наблюдается максимальный выход продукта на каждой из стадий синтеза. Преимуществами использования избыточных количеств метилового спирта является возможность реализации технологической схемы, где отсутствуют операции конденсации метанола и метилмеркаптана после каждого из реакторов. Избыток метанола задается в пределах 2-5 раз, т.к. при более высоких его количествах снижается относительный выход в реакции и тратится дополнительная энергия на его испарение и конденсацию. Меньшие избытки приводят к тому, что уже после первого реактора состав смеси приближается к стехиометрическому, и реакция замедляется.
Температурные интервалы конденсации воды выбраны исходя из того, что при более высокой температуре конденсация не является достаточно полной из-за высокого давления насыщенных паров. Нижний предел ограничен необходимостью не допустить на этой операции конденсации значительных количеств метилового спирта. Аналогичным образом выбраны температуры конденсации метанола, при которой не должен выделяться метилмеркаптан.
Конденсацию целевого продукта необходимо проводить в интервале температур 0-(-5)oC, т.к. при более высоких температурах конденсация проходит недостаточно полно, при более низких - возникает потребность в дополнительных затратах на охлаждение приемников. Использование солевых растворов для поглощения метилмеркаптана обосновано тем, что при конденсации в обычном приемнике он находится в смеси с неизрасходованным сероводородом, что повышает летучесть получаемого продукта и уменьшает его извлечение из реакционной смеси. Введение солевого раствора как еще одной фазы имеющейся в наличии смеси снижает летучесть продукта, увеличивая его выход на стадии разделения компонентов и не требует охлаждения до более низких температур. Концентрация солевых растворов выбрана так, чтобы поглощение было, с одной стороны, эффективно (при концентрациях выше 6 мас.% количество конденсируемого метилмеркаптана на единицу объема раствора падает), с другой стороны - растворы с меньшей 0,5 мас.% концентрацией нельзя охладить до требуемых температур без его замерзания.
На чертеже приведена принципиальная схема получения метилмеркаптана по одному из вариантов. Восстановление сульфата бария на стадии 1 проходит при подаче в аппарат собственно сульфата бария и природного газа. На стадии 2 проходит образование сероводорода при взаимодействии сульфида бария и серной кислоты. Сероводород испаряет метиловый спирт на стадии 3. Реакционная смесь поступает в реактор на стадию получения метилмеркаптана 4. После стадии получения метилмеркаптана 4 смесь газов последовательно проходит стадии конденсации воды 5, конденсации метилового спирта 6 и конденсации метилмеркаптана 7. После первой ступени в смесь газов подают свежий сероводород, и на второй ступени вновь повторяются стадии 3, 4, 5, 6 и 7. Дожиг природного газа проводят на стадии 8, используя горячий газ после сжигания для нагрева природного газа перед восстановлением сульфата бария, нагрева сероводорода и аппаратуры. Сконденсировавшийся метилмеркаптан является конечным продуктом, конденсат метилового спирта вновь используют в процессе, водяной конденсат используют для разбавления серной кислоты.
Пример 1.
Были взяты носители катализаторов из шамота - ультралегковеса, сформованного и спеченного таким образом, что были получены цилиндрические заготовки диаметром 20 мм и толщиной 10 мм. Носители были пропитаны путем погружения их в насыщенный раствор молибдата аммония, содержащий 0,1 мас.% метилцеллюлозы, затем подвергнуты сушке до удаления влаги при температуре 50oC, после этого обжигу при температуре 400oC в течение 4 ч на воздухе и в течение 1 ч до приобретения катализатором синей окраски при 450oC в потоке азота. Полученные таким образом катализаторы, содержащие 3,2% низших оксидов молибдена, помещали в два последовательно установленных трубчатых реактора и подавали в них после их нагревания до 350oC реакционную смесь, полученную пропусканием сероводорода через метиловый спирт, содержащую эквимолярные количества сероводорода и метилового спирта. При этом сероводород получали следующим образом. Исходный сульфат бария с крупностью 5 мм восстанавливали в противоточном пересыпном термохимическом реакторе природным газом при 950oC и общем времени пребывания в нем 60 мин. Затем полученный сульфид бария обрабатывали для выделения сероводорода серной кислотой, а возникающий сульфат бария направляли вновь на восстановление. После прохождения реакционной смесью первого реактора ее охлаждали до 90oC, что сопровождалось конденсацией выделившейся в ходе реакции воды, затем проводили дальнейшее охлаждение до 30oC с выделением непрореагировавшего метилового спирта. Конденсацию метилмеркаптана осуществляли пропусканием оставшейся части реакционной смеси через водный раствор хлорида кальция, содержащий 6 мас.% этой соли, при температуре -5oC. Оставшийся сероводород вновь барботировали через метиловый спирт и направляли во второй реактор, после которого повторяли операции, аналогичные проведенным для разделения реакционной смеси после первого реактора. Объемная скорость прохождения смеси через реакторы составляла 100 ч-1. Оставшийся после второго реактора непрореагировавший сероводород направляли в начало цикла синтеза, смешивая со свежими порциями этого газа. Сконденсированный метиловый спирт использовали в реакции путем подачи его в емкости, через которые продували сероводород. Таким образом, было получено 12,2 г метилмеркаптана при расходе 8,6 г метилового спирта. Использование реагентов при работе установки синтеза в циклическом режиме составило 98%.
Пример 2.
Были взяты носители катализаторов из диатомита, сформованного и спеченного таким образом, что были получены сферические заготовки диаметром 2 мм. Носители были пропитаны путем погружения их в 0,1%-ный раствор вольфрамата аммония, содержащий 30 мас.% поливинилпирролидона, затем подвергнуты сушке до удаления влаги при температуре 120oC, после этого обжигу при температуре 450oC в течение 1 ч на воздухе и в течение 4 ч до приобретения катализатором фиолетовой окраски при 300oC в потоке азота. Полученные таким образом катализаторы, содержащие 4,1% низших оксидов вольфрама, помещали в трубчатые реакторы и подавали в них после их нагревания до 430oC реакционную смесь, полученную смешиванием сероводорода с парами метилового спирта, содержащую в 4 раза больше метилового спирта, чем стехиометрическое количество. Сероводород получали следующим образом. Исходный сульфат бария с крупностью 20 мм восстанавливали в противоточном пересыпном термохимическом реакторе природным газом при 1050oC и общем времени пребывания в нем 50 мин. Затем полученный сульфид бария обрабатывали для выделения сероводорода серной кислотой, а возникающий сульфат бария направляли вновь на восстановление. После прохождения реакционной смесью первого реактора ее охлаждали до 70oC, что сопровождается конденсацией выделившейся в ходе реакции воды. После этого реакционную смесь направляли на следующую ступень синтеза, общее число которых составляло 6. После прохождения реакционной смесью последнего реактора и конденсации воды проводили дальнейшее охлаждение до 8oC с выделением непрореагировавшего метилового спирта. Конденсацию метилмеркаптана осуществляли пропусканием оставшейся части реакционной смеси через водный раствор хлорида кальция, содержащий 0,5 мас.% этой соли, при температуре 0oC. Объемная скорость прохождения смеси через реакторы составляла 1000 ч-1. Оставшийся после прохождения всех реакторов непрореагировавший сероводород направляли в начало цикла синтеза, смешивая со свежими порциями этого газа. Сконденсированный метиловый спирт использовали в реакции путем подачи его в емкости, через которые продували сероводород. Таким образом, было получено 16,7 г метилмеркаптана при расходе 11,2 г метилового спирта.
Использование заявляемого технического решения, представляющего собой группу связанных единым замыслом изобретений, обеспечивает следующие технико-экономические преимущества:
- автономность производства метилмеркаптана из сероводорода и метилового спирта, связанную в основном с получением сероводорода непосредственно в условиях производства основного продукта,
- безотходность процесса получения сероводорода и метилмеркаптана,
- исключение выбросов газообразных, жидких и твердых веществ, загрязняющих окружающую среду,
- высокая степень взаимодействия паров метилового спирта и сероводорода, обеспечиваемая предлагаемым катализатором и технологией,
- исключение при получении катализатора дорогостоящих компонентов,
- простота предлагаемых способов,
- цикличность процесса, обеспечивающая полное использование исходных веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛМЕРКАПТАНА | 2004 |
|
RU2394023C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛМЕРКАПТАНА ИЗ ДИАЛКИЛСУЛЬФИДОВ И ДИАЛКИЛПОЛИСУЛЬФИДОВ | 2008 |
|
RU2490255C2 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ МЕТИЛМЕРКАПТАНА ИЗ МЕТАНОЛА И СЕРОВОДОРОДА | 2004 |
|
RU2358803C2 |
| КАТАЛИЗАТОР ДЛЯ СИНТЕЗА МЕТИЛМЕРКАПТАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2190467C2 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ МЕТИЛМЕРКАПТАНА | 2008 |
|
RU2497588C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛМЕРКАПТАНА | 2006 |
|
RU2408577C2 |
| КАТАЛИЗАТОР СИНТЕЗА МЕТИЛМЕРКАПТАНА | 1997 |
|
RU2120822C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА | 1999 |
|
RU2147927C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛМЕРКАПТАНОВ В МНОГОЗОННОМ РЕАКТОРЕ С НЕПОДВИЖНЫМ СЛОЕМ | 2007 |
|
RU2443686C2 |
| КАТАЛИЗАТОР ДЛЯ СИНТЕЗА МЕТИЛМЕРКАПТАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2191069C2 |
Изобретение относится к получению одорантов для природного газа, в частности к безотходному способу получения метилмеркаптана, а также к способу получения катализатора, обеспечивающего более высокую степень взаимодействия метилового спирта и сероводорода и использованию такого способа получения сероводорода, который обеспечивает безотходность производства в целом. Метилмеркаптан получают пропусканием бинарной смеси паров метилового спирта и сероводорода при атмосферном давлении через последовательно установленные по ходу смеси трубчатые реакторы с катализатором, возврат непрореагировавших компонентов смеси в голову процесса при добавлении необходимого количества метилового спирта и сероводорода и выделение компонентов из продукционной газовой смеси путем конденсации. В качестве катализатора используют оксиды молибдена или вольфрама, процесс проводят при температуре 390 - 430oC и объемной скорости смеси в реакторах на уровне 100 - 1000 ч-1 с использованием сероводорода, полученного при взаимодействии разбавленной кислоты и сульфида металла, а конденсацию проводят ступенчато с выделением образовавшейся при реакции воды охлаждением газовой смеси до 70 - 90oC, непрореагировавшего метилового спирта - охлаждением до 8 - 30oC и образовавшегося метилмеркаптана путем пропускания оставшейся смеси при температуре 0 - (-5)oC через раствор, нейтральный по отношению к сероводороду соли, например хлорида кальция с концентрацией 0,5 - 6 мас.%. Число последовательно установленных реакторов составляет не менее двух. Способ получения катализатора заключается в приготовлении раствора, содержащего соединения вольфрама или молибдена, пропитку полученным раствором пористого носителя и его последующие сушку и обжиг. Для приготовления раствора с концентрацией от 0,1 мас. % до насыщенного используют вольфрамат или молибдат аммония, в раствор вводят водорастворимый полимер в количестве 0,1 - 30 мас.% от массы взятой воды, пористый носитель до пропитки подвергают формовке и спеканию, после пропитки осуществляют сушку при 400 - 450oC в течение 1 - 4 ч и далее в токе инертного газа, например азота, при 300 - 450oC в течение 1 - 4 ч. В качестве пористого носителя используют шамот - ультралегковес или диатомит. В качестве водорастворимого полимера используют метилцеллюлозу, поливинилпирролидон или поливиниловый спирт. Способ получения сероводорода для производства метилмеркаптана включает разложение сульфида бария в кускообразном виде с крупностью фракции 5 - 20 мм серной кислотой. Образовавшийся при взаимодействии сульфат бария восстанавливают природным газом в противоточном пересыпном термохимическом реакторе при 950 - 1050oC в течение 50 - 60 мин, а полученный при этом сульфид бария вновь направляют на взаимодействие. Технический результат состоит в увеличении степени превращения исходных реагентов, в безопасном проведении процесса, в защите окружающей среды из-за практически полного предотвращения выбросов газов, содержащих вредные вещества, твердых и жидких отходов. 3 с. и 6 з.п. ф-лы, 1 ил.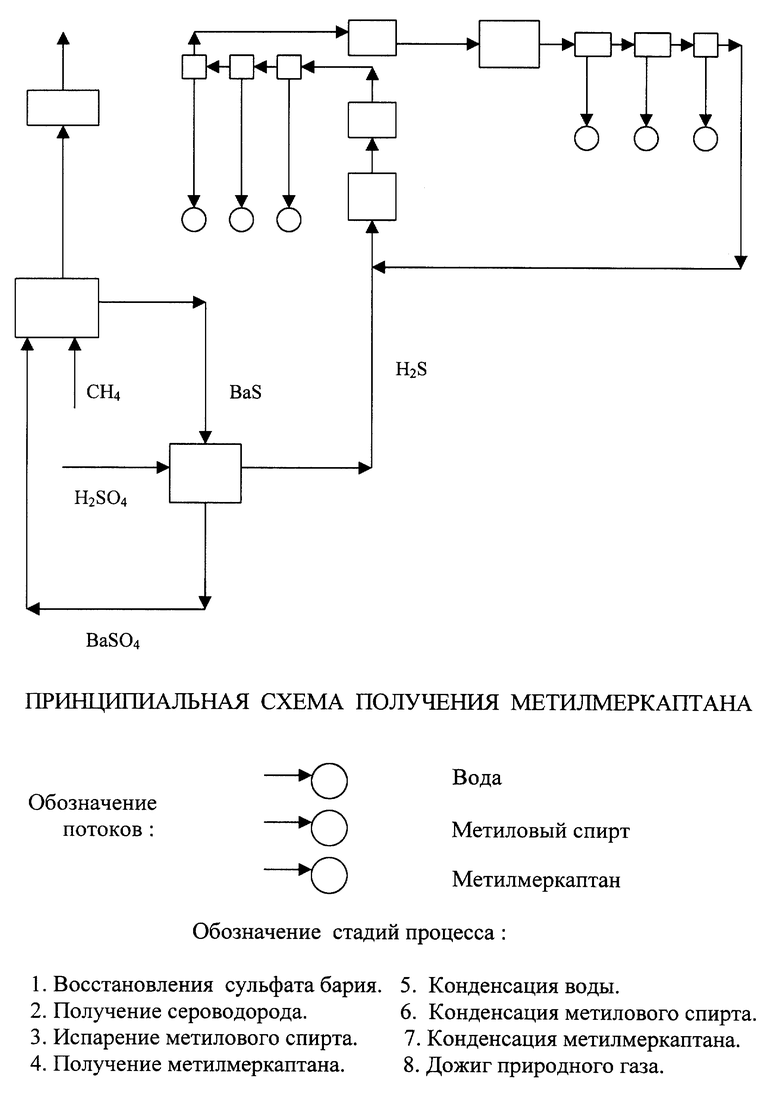
| ГУБЕН И | |||
| Методы органической химии | |||
| - М.: ОНТИ, 1935, т.3, вып.3, с.494 | |||
| КАТАЛИЗАТОР СИНТЕЗА МЕТИЛМЕРКАПТАНА | 1997 |
|
RU2120822C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ СИНТЕЗА МЕТИЛМЕРКАПТАНА | 1988 |
|
SU1608923A1 |
| SU 1316127 А1, 20.10.1996 | |||
| ХИМИЧЕСКАЯ ЭНЦИКЛОПЕДИЯ | |||
| - М., 1995, с.651 | |||
| Способ получения метилмеркаптана | 1974 |
|
SU545255A3 |
| Винтовой компрессор | 1979 |
|
SU850922A1 |
Авторы
Даты
2000-10-10—Публикация
1999-03-10—Подача