Изобретение относится к медицине, а именно к фармакологии, и касается выделения из органов животных комплекса биологически активных веществ, который может использоваться в клинической геронтологии (гериатрии) как фармакологическое средство, обладающее антиоксидантной и геропротекторной активностью.
Известно, что одними из ведущих механизмов старения организма являются нарастание молекулярных повреждений, вызываемых свободными радикалами, и нарушение функции системы антиоксидантной защиты организма, а также нарушение физиологических функций эпифиза [1, 2, 3].
Известны препараты, проявляющие геропротекторную и антиоксидантную активность. Добавление в пищу известного ингибитора радикальных процессов ионола (2,6-ди-трет.бутил-4-метилфенола) способствовало увеличению времени жизни мышей с ускоренным старением линии LAF1 [4]. Однако лекарственный препарат на основе 2,6-ди-трет.бутил-4-метилфенола (дибунол) выпускается в виде линимента и применяется у людей, в основном, при онкологических заболеваниях в урологической практике [5] . Введение в пищу антиоксиданта этоксихина (сантохин) увеличивало продолжительность жизни мышей линии C3H [6]. Увеличение продолжительности жизни лабораторных животных вызывает также малотоксичный водорастворимый антиоксидант - хлоргидрат 2-этил-6-метил-3-оксипиридина, структурного аналога витамина B6 [7, 8]. Незначительное увеличение продолжительности жизни в эксперименте давали 2-меркаптоэтаноламин, бутилгидрокситолуол, цистеин, 3-гидроксипиридин, центрофеноксин, молочная и глюконовая кислоты, глутатион [9, 10]. Однако эти химические соединения не являются лекарственными препаратами и не нашли применения в медицине в качестве геропротекторных средств. Увеличивали продолжительность жизни в эксперименте витамины A, C, E [11, 12, 13]. Однако перенасыщение организма этими витаминами может неблагоприятно влиять на функциональное состояние органов и систем, обуславливает быстрое развитие гипервитаминоза. Известен препарат β-катехин, в состав которого входят витамины и растительные вещества, обладающиe антиоксидантным действием [14]. Применение этого препарата мышам с ускоренным старением линии SAM-P8 увеличивало выживаемость животных. При этом механизмы геропротекторной активности этого комбинированного препарата недостаточно изучены, что ограничивает его внедрение в клиническую практику. После 7-месячного содержания мышей линии SAM, склонных к ускоренному старению, на диете с увеличенным содержанием карнозина (β-Ala-His) уменьшалась смертность животных [15]. Следует отметить, что карнозин не является лекарственным препаратом, его геропротекторные свойства изучены недостаточно. Незначительное увеличение средней продолжительности жизни мышей вызывало применение гормона эпифиза - мелатонина [16]. Эффекты мелатонина связывают с его антиоксидантными свойствами [17]. Однако применение мелатонина у Drosophila melanogaster линии ВЭС, селектированнoй на высокий уровень эмбриональной смертности, не оказывало геропротекторного эффекта, хотя и сопровождалось антиоксидантным эффектом. Мелатонин не является лекарственным препаратом, а выпускается в качестве биологически активной добавки к пище.
В качестве геропротекторного средства используется лекарственный препарат, содержащий новокаин, - геровитал [18] - прототип фармакологического средства и способа профилактики и лечения возрастной патологии. Недостатком этого препарата являются возможное отрицательное действие на функции сердечно-сосудистой системы, аллергизирующее действие, иногда - ухудшение сна, появление чувства беспокойства, боли в мышцах и суставах.
Наиболее близким аналогом в отношении способа получения комплекса биологически активных полипептидов из эпифиза мозга животных и заявленного фармакологического средства является способ получения вещества, обладающего геропротекторным и антиаксидантным действием [19], однако при использовании указанного способа при экстракции из ткани эпифиза извлекается большое количество веществ неполипептидной природы, которые и определяют основное действие (противоопухолевое) известного препарата.
Задача, на решение которой направлено заявляемое изобретение, состоит в расширении видов биологической активности целевого продукта, полученного путем выделения из эпифиза животных комплекса полипептидных фракций, а также в создании фармакологического средства, содержащего целевой продукт, полученный заявляемым способом в качестве активного начала, обладающего антиоксидантным и геропротекторным действием.
Согласно заявляемому изобретению комплекс биологически активных полипептидов из эпифиза мозга животных получают путем измельчения эпифиза, экстракции 3%-ным раствором уксусной кислоты в присутствии хлористого цинка, обработки надосадочной жидкости ацетоном, промывания органическим растворителем, причем экстракцию проводят при температуре 7-15oC в течение 48 ч, pH 3,0-4,0, экстракт отделяют от балластных веществ сепарированием, обработку надосадочной жидкости ацетоном проводят в соотношении 1:5 при t = 5oC, отстаивают до образования сформировавшегося осадка, надосадочную жидкость сифонируют, полученный осадок промывают ацетоном в соотношении 1:(15-20), отстаивают до осветления надосадочной жидкости и сифонируют ее, осадок фильтруют и промывают ацетоном при комнатной температуре, высушивают и готовят водный раствор с содержанием пептидов 15-35 мг/мл, полученный раствор перемешивают, центрифугируют, затем высокомолекулярные водорастворимые фракции отделяют ультрафильтрацией через материалы с задерживающей способностью до 15000 Да, полученный целевой продукт лиофилизируют.
Согласно заявляемому изобретению целевой продукт, полученный заявляемым способом, содержит комплекс полипептидов с молекулярной массой от 1000 до 12000 Да.
Согласно заявляемому изобретению целевой продукт, полученный заявляемым способом, в ультрафиолетовом спектре имеет полосы с максимумом поглощения при 274 ± 3 нм, что характерно для веществ полипептидной природы.
Согласно заявляемому изобретению фармакологическое средство содержит фармацевтически приемлемый компонент и активное начало, причем в качестве активного начала содержит эффективное количество целевого продукта, полученного заявляемым способом и представляющего собой комплекс выделенных из эпифиза животных биологически активных полипептидов с молекулярной массой от 1000 до 12000 Да.
Согласно заявляемому изобретению фармакологическое средство обладает антиоксидантной и геропротекторной активностью.
Различные лекарственные формы фармакологического средства могут содержать в качестве фармацевтически приемлемых компонентов - вещества, указанные в Государственной Фармакопее.
Согласно заявляемому изобретению способ профилактики и лечения возрастной патологии заключается во введении субъекту, нуждающемуся в этом, терапевтически эффективного количества фармакологического средства, включающего в себя в качестве активного начала целевой продукт, полученный заявляемым способом и представляющий собой комплекс выделенных из эпифиза животных биологически активных полипептидов с молекулярной массой от 1000 до 12000 Да, в дозах от 0,1 до 1,0 мг на 1 кг веса тела в течение 10-40 дней в зависимости от характера течения и тяжести заболевания.
Во время проведения сравнительных исследований in vivo на экспериментальных моделях были обнаружены новые терапевтические эффекты препарата, полученного заявляемым способом, такие как антиоксидантное и геропротекторное действие.
Изобретение иллюстрируется примером конкретного выполнения способа (пример 1); примерами испытания биологической активности продукта, полученного заявляемым способом (примеры 2, 3, 4); примерами результатов клинического изучения препарата, демонстрирующего его фармакологические свойства и подтверждающего возможность достижения лечебного эффекта (примеры 5, 6).
Пример 1.
Эпифиз крупного рогатого скота измельчают и загружают в реактор, в котором предварительно приготовлен 3%-ный раствор уксусной кислоты (из расчета на 1 кг сырья - 10 л 3%-ного раствора уксусной кислоты) и охлажден до температуры 7-15oC. По окончании загрузки содержимое реактора тщательно перемешивают, затем добавляют 1%-ный раствор хлористого цинка в 3%-ном растворе уксусной кислоты (из расчета на 1 кг сырья - 10 г хлористого цинка), перемешивают до 45 мин. Экстракцию проводят при температуре 7-15oC в течение 48 ч, pH 3,0-4,0 при периодическом перемешивании.
Отделение экстракта от балластных веществ проводят на сепараторе. В экстракт добавляют ацетон из расчета 1:5, смесь охлаждают до 5oC и выдерживают до образования сформировавшегося осадка. Осуществляют сифонирование надосадочной жидкости. Затем доливают ацетон из расчета 15-20 л на 1 кг сырья. Отстаивают до осветления надосадочной жидкости. Осуществляют сифонирование надосадочной жидкости.
Проводят фильтрацию. Осадок порционно промывают ацетоном с температурой не более 25oC и высушивают.
Готовят раствор с содержанием пептидов 15-35 мг/мл. Высушенный осадок растворяют в воде. Воду для растворения охлаждают до 15oC и фильтруют через фильтр с диаметром пор 0,2 мкм. Перемешивают в течение 30 мин, отделяют нерастворимую часть центрифугированием.
Для отделения высокомолекулярной водорастворимой фракции проводят ультрафильтрацию через материалы с задерживающей способностью 15000 Да. После окончания ультрафильтрации целевой продукт лиофилизируют.
Для получения фармакологического средства целевой продукт растворяют, добавляют фармацевтически приемлемый компонент, например, изотонический 0,9%-ный раствор натрия хлорида, стерилизуют и лиофилизируют.
Препарат представляет собой лиофилизированный порошок белого или белого с желтоватым оттенком цвета и содержит комплекс биологически активных полипептидов от 1000 до 12000 Да. Препарат умеренно растворим в растворе натрия хлорида изотоническом 0,9%-ном и воде.
Отсутствие в препарате высокомолекулярных белковых компонентов подтверждает то, что при добавлении к 1%-ному раствору препарата 10%-ного раствора трихлоруксусной кислоты раствор препарата остается прозрачным.
Для определения в препарате пептидных связей к его раствору добавляют биуретовый реактив. Окрашивание раствора в фиолетовый цвет свидетельствует об имеющихся в препарате пептидных связях.
С целью определения в препарате полипептидов и их фракций использовали методы ультрафиолетовой спектрофотометрии, гель-хроматографии, высокоэффективную жидкостную хроматографию и электрофорез в полиакриламидном геле.
Ультрафиолетовый спектр раствора препарата в вводе снимали в области длин волн от 250 до 350 нм с максимумом поглощения при 274±3 нм.
Методом гель-хроматографии на сефадексе G-25 (колонка диаметром 12 мм, объемом 70 мм, уравновешенная 5%-ной уксусной кислотой), установлено, что в состав препарата входят вещества с молекулярной массой не более 12000 Да.
С помощью обращенно-фазовой высокоэффективной жидкостной хроматографии в градиенте ацетонитрила (сорбент "Lichrosorb C 18", колонка 2х62 см) было установлено, что в состав препарата входят преимущественные полипептидные фракции (от 70 до 90%), а высокомолекулярные компоненты в препарате отсутствуют.
По данным электрофореза в 15%-ном полиакриламидном геле молекулярная масса полипептидов составляет от 1000 до 12000 Да. Аминокислотный состав препарата определяли на анализаторе "LKB-3201" (Швеция). В табл. 1 приведен аминокислотный состав целевого продукта.
Фармакологическое средство (далее препарат) содержит в качестве активного начала эффективное количество целевого продукта, полученного указанным способом и представляющего собой комплекс биологически активных полипептидов с молекулярной массой от 1000 до 12000 Да и фармацевтически приемлемый компонент.
При этом в качестве фармацевтически приемлемого компонента можно использовать, например, 0,9%-ный раствор NaCl или гликокол.
Во время проведения сравнительных исследований in vivo на экспериментальных моделях были обнаружены новые терапевтические эффекты препарата, полученного заявляемым способом, такие как антиоксидантная и геропротекторная активность.
Изучение возможного токсического влияния на организм препарата, полученного заявляемым способом, проводилось в соответствии с "Требованиями к доклиническому изучению общетоксического действия новых фармакологических веществ", 1984 г. (изданы Управлением по внедрению новых лекарственных препаратов и медицинской техники МЗ СССР).
Цель изучения состояла в определении переносимых токсических доз препарата, оценке степени и характера патологических изменений в различных органах и системах организма и выявлении зависимости токсических эффектов от дозы и длительности применения препарата.
Изучение "острой" токсичности препарата, полученного заявляемым способом, было проведено при однократном введении его животным по методу Кербера. Исследование выполнено на 96 мышах - самцах массой 20-22 г. Животные были разделены на 8 групп по 12 мышей в каждой. Препарат растворяли в стерильном 0,9%-ном растворе NaCl и вводили внутримышечно в дозах от 700 до 1500 мг/кг. Наблюдение за животными вели в течение 14 суток. ЛД50 рассчитывали с помощью графика зависимости гибели животных от вводимой дозы препарата.
В результате проведенного исследования установлено, что ЛД50 для белых беспородных мышей при однократном введении препарата составляет 992±27.2 мг/кг. Необходимо отметить, что ЛД50 препарата для мышей превышает предполагаемую однократную терапевтическую дозу (0.01-0.1 мг/кг) в среднем в 10000 раз.
"Хроническую" токсичность препарата, полученного заявляемым способом, изучали при повторном и длительном введении его крысам и кроликам. Животным ежедневно вводили внутримышечно препарат в дозе 1,0 мг/кг в течение 6 месяцев. Оценивали общее состояние животного, состав и свойства периферической крови, функции сердечно-сосудистой системы, печени, поджелудочной железы, почек и надпочечников. Часть животных подвергали патоморфологическому исследованию с целью оценки состояния различных отделов головного и спинного мозга, сердца, аорты, легких, печени, почек, органов эндокринной и иммунной систем.
При изучении "хронической" токсичности препарата, полученного заявляемым способом, в дозе, которая в 10-100 раз превышала предполагаемую терапевтическую дозу, было установлено, что общее состояние животных, двигательная активность, а также основные функции изученных органов и систем находились в пределах физиологической нормы. При патоморфологическом исследовании различных органов животных также не было обнаружено патологических изменений. Следовательно, препарат, полученный заявляемым способом, при длительном введении животным не обладает токсическими свойствами, препятствующими дальнейшему его применению в качестве лекарственного средства.
Пример 2.
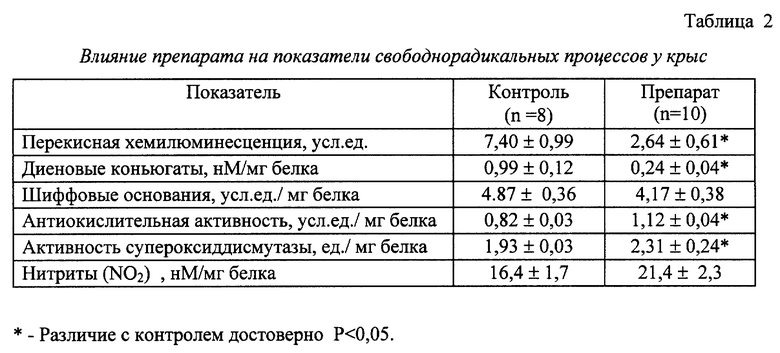
Для изучения антиоксидантной активности использовали экспериментальные модели, позволяющие оценить способность биологически активных веществ эпифиза проявлять указанную активность. Препарат вводили крысам весом 180-200 г в течение 5 суток подкожно в дозе 0,5 мг. После этого в сыворотке крови животных определяли показатели свободнорадикальных процессов (интенсивность перекисной хемилюминесценции, перекисного окисления липидов, содержание диеновых конъюгатов, шиффовых оснований и др.). Полученные результаты представлены в табл. 2.
Показано, что препарат существенно (в 3-4 раза) подавляет интенсивность перекисной хемилюминесценции в сыворотке крови и перекисного окисления липидов, что выражалось, в частности, в значительном снижении (в 4,1 раза) содержания диеновых конъюгатов, тогда как содержание шиффовых оснований имело тенденцию к снижению. Эти результаты свидетельствуют об избирательном ингибирующем влиянии препарата на начальные этапы перекисного окисления липидов. Кроме того, после введения препарата наблюдали достоверное увеличение общей антиокислительной активности сыворотки крови. При этом активность супероксиддисмутазы в сыворотке крови увеличивалась на 19,7% (P < 0,05). В механизме антиоксидантного действия препарата основную роль играет его влияние на ферментативные системы антиоксидантной защиты.
Пример 3.
Для изучения антиоксидантной активности использовали экспериментальные модели, позволяющие оценить способность биологически активных веществ эпифиза проявлять указанную активность.
Изучено влияние препарата на интенсивность процессов перекисного окисления липидов в тканах мух (D. Melanogaster).
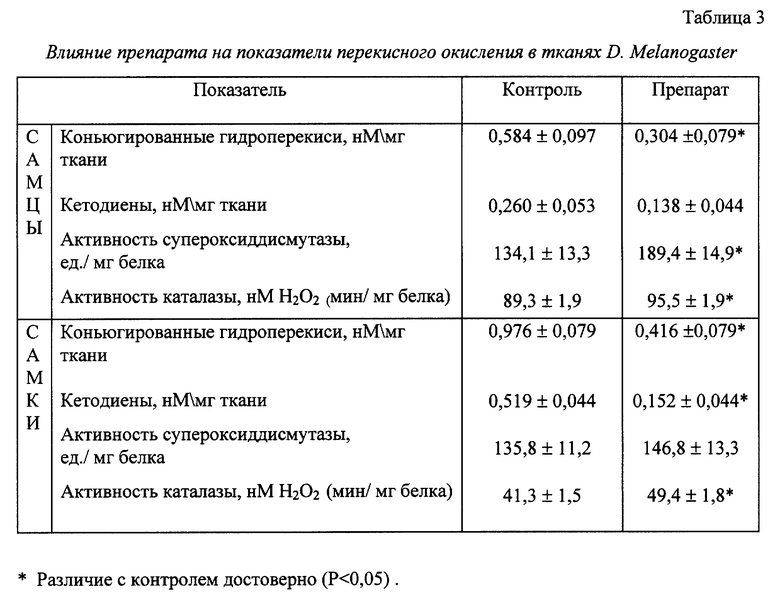
Препарат добавляли в среду питания личинок мух в концентрации 100 мкг/мл. Продукты перекисного окисления липидов у мух определяли в возрасте 11 суток. Результаты исследования приведены в табл. 3.
Применение препарата привело к достоверному уменьшению содержания конъюгированных гидроперекисей и кетодиенов в тканях D. Melanogaster.
Под влиянием препарата достоверно увеличивалась активность каталазы у самцов и самок мух и увеличивалась активность супероксиддисмутазы у самцов дрозофил. Полученные результаты свидетельствуют об отчетливом антиоксидантном действии препарата.
Пример 4.
Для изучения геропротекторной активности использовали экспериментальные модели, позволяющие оценить способность биологически активных веществ эпифиза проявлять указанную активность.
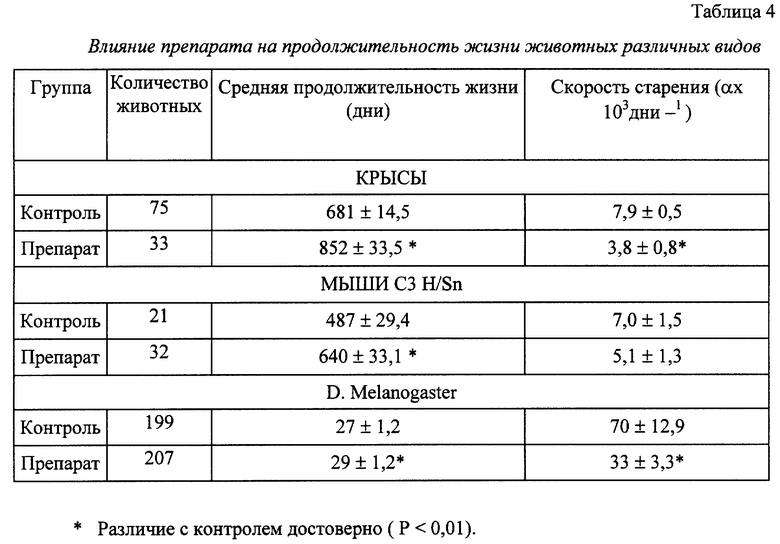
Известно, что антиоксиданты обладают широким спектром действия на различные физиологические системы организма, в частности, при введении в организм они влияют на процессы обмена веществ, энергетический обмен, иммунитет и обладают геропротекторными свойствами. В эксперименте на различных видах животных была изучена эффективность применения заявляемого препарата как геропротектора. Полученные результаты приведены в табл. 4.
Введение препарата крысам и мышам способствовало увеличению средней продолжительности жизни и замедляло скорость старения животных. Сходные результаты были получены при использовании препарата у D. Melanogaster. Следует отметить, что при изучении на крысах и дрозофилах было выявлено, что геропротекторный эффект препарата коррелировал с его высоким антиоксидантным потенциалом.
Выявленные в результате экспериментального доклинического исследования новые свойства препарата позволяют считать показанным его применение при ряде заболеваний, развивающихся с возрастом, таких как сердечно-сосудистые заболевания, гормональные и метаболические нарушения, диабет у пожилых, дистрофические заболевания костей и т.д.
Приведенные ниже примеры клинического применения препарата подтверждают возможность его применения в клинической практике с достижением указанного терапевтического эффекта.
Пример 5.
Изучена эффективность препарата у 57 женщин в возрасте от 40 до 55 лет, страдающих климактерической миокардиопатией и ишемической болезнью сердца.
Препарат вводили пациентам внутримышечно ежедневно в дозе 10 мг (курсовая доза составила 100 мг). Эффективность препарата оценивали через 10-14 дней после окончания лечения. Применение препарата снижало проявление вегетососудистых нарушений у женщин. Гормональные исследования показали снижение уровня эстрадиола и повышение уровня гонадотропных гормонов в крови, что сопровождалось улучшением клинических данных. После лечения препаратом уровень эстрадиола у больных составил 64,75 ± 12,62 нм/мл, что было достоверно ниже, чем у больных, не получавших препарат. После введения препарата у больных улучшалась функция миокарда. До лечения наиболее характерными были нарушения в виде отрицательных, изоэлектрических или двухфазных зубцов "T" в грудных отведениях V1 - V3 электрокардиограммы. Нарушение автоматизма у больных в основном проявлялось в виде синусовой тахикардии. Кроме того, у ряда больных наблюдали нарушения возбудимости миокарда по типу суправентрикулярной экстрасистолии и пароксизмальной тахикардии. Кроме того, характерным признаком нарушений на электрокардиограмме при ишемической болезни сердца были горизонтальная депрессия сегмента ST в отведениях V3 - V6, инверсия зубца "T", блокада правой и левой ножек пучка Гиса, снижение вольтажа зубцов и удлинение систолического показателя.
Применение препарата у больных способствовало нормализации показателей электрокардиограммы как в покое, так и при физических нагрузках. На фоне обратного развития клинических проявлений заболевания наблюдали положительную динамику кардиограммы - улучшение функции автоматизма, исчезновение синусовой тахикардии, улучшение периода реполяции в виде положительной динамики конечной части желудочкового комплекса, исчезновение суправентрикулярной и желудочковой экстрасистолии и пароксизмов желудочковой тахикардии. По данным велоэргометрии толерантность к физической нагрузке у больных после применения препарата повысилась как по мощности пороговой нагрузки и времени нагрузки, так и по объему выполняемой работы. Улучшение показателей гемодинамики у больных после лечения свидетельствовало об оптимизации сократительной функции миокарда и повышении экономичности работы сердца.
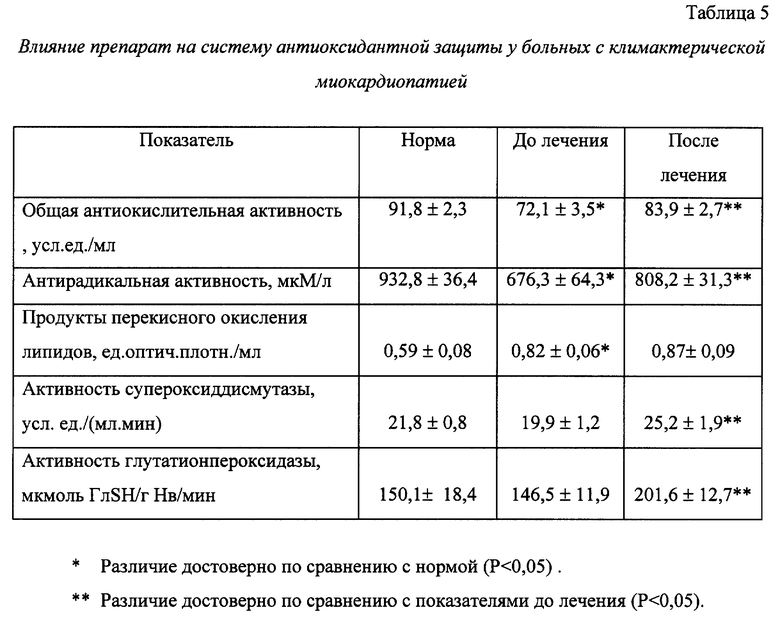
При изучении антиокислительной и антирадикальной активности сыворотки больных до лечения было установлено, что с возрастом происходит снижение общей антиокислительной и антирадикальной активности крови. После лечения наблюдалось достоверное повышение показателей общей антиокислительной и антирадикальной активности сыворотки крови, уменьшение содержания продуктов перекисного окисления липидов, а также повышение активности супероксиддисмутазы и глутатионпероксидазы. Полученные результаты приведены в табл. 5.
Полученные результаты клинического изучения свидетельствуют об эффективности использования препарата для коррекции системы антиоксидантной защиты при преждевременном старении и возрастной патологии.
Пример 6.
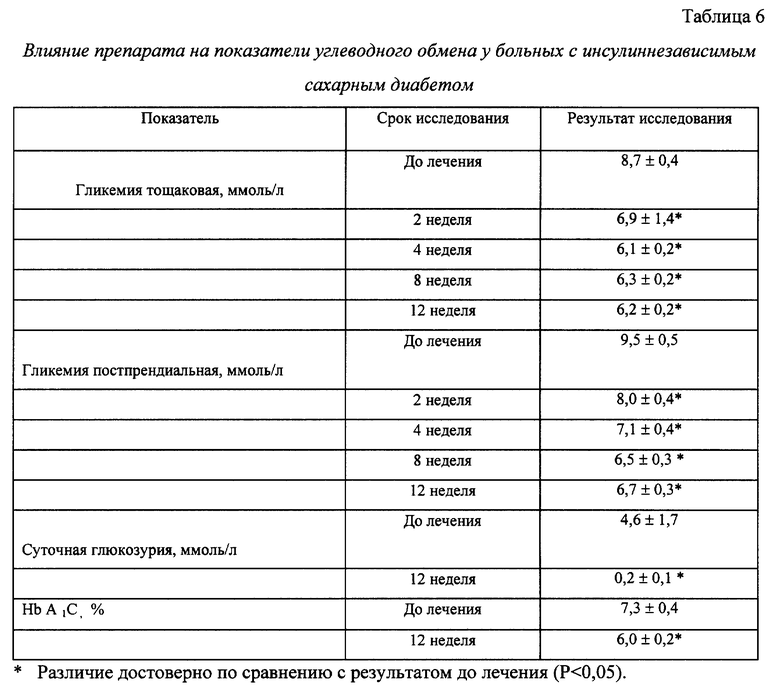
Изучено влияние препарата на состояние сердечно-сосудистой системы и процессы обмена у 33 больных (17 мужчин и 16 женщин) с инсулиннезависимым сахарным диабетом и длительностью заболевания 6,0 ± 1,5 года. Средний возраст пациентов составил 52,8 ± 1,8 года. По результатам обследование в соответствии с критериями ВОЗ у всех больных была установлена гипертоническая болезнь I - II стадии. С целью лечения препарат вводили пациентам внутримышечно, ежедневно по 10 мг в течение 10 дней. Результаты, полученные при изучении показателей углеводного обмена, приведены в табл. 6.
После введения препарата было отмечено снижение тощаковой гликемии на 15% (на 2-й неделе), на 22% (на 4-й неделе) и на 29,4% к 12-й неделе наблюдения.
Постпрендиальная гликемия снижалась на 18,2% через 2 недели, на 28% через 4 недели и на 41% к 12-й неделе наблюдения за пациентами.
Кроме того, у пациентов после лечения препаратом наблюдалось достоверное снижение уровня гликозилированного гемоглобина к 12-й неделе наблюдения. В то же время показатели гликемии, гликозурии и гликозилированного гемоглобина у пациентов контрольной группы (24 человека) достоверно не изменялись на протяжении всего периода наблюдения.
Таким образом, у больных с инсулиннезависимым сахарным диабетом применение препарата оказывало положительное влияние на углеводный обмен, нарушение которого происходит при старении организма. В этих условиях препарат проявлял выраженное геропротекторное действие.
Источники информации
1. Harman D. Aging and disease: extending functional life span // Ann. N.Y. Acad. Sci. - 1996. - Vol. 786. - P. 321-336.
2. Pierpaoli W. Neuroimmunomodulation of aging: a program in the pineal gland // Ann. N.Y. Acad. Sci. - 1998. - Vol. 840. - P. 491-497.
3. Yu B. P., Yang R. Critical evaluation of the free radical theory of aging: a proposal for the oxidative stress hypothesis // Ann. N.Y. Acad. Sci. - 1996. - Vol. 786. - P. 1-11.
4. Harman D. Free radical theory of aging: effect of free radical reaction inhibitors on the mortality rate of male LAF1 mice // J. Gerontol. - 1968. - Vol. 23. - P. 476.
5. Машковский М. Д. Лекарственные средства (Пособие для врачей). - М.: Медицина, 1993. - Ч. II, гл. 10. - с. 213-215.
6. Comfort A., Youhotsky-Gore J., Pathmanathan K. Effect of ethoxyquin on the longevity of C3H mice // Nature. - 1971. - Vol. 229. - P. 254-255.
7. Обухова Л.К. Химические геропротекторы, увеличение продолжительности жизни // Усп. химии. - 1975. - Т. 44. - с. 1914-1925.
8. Эмануэль Н. М. , Обухова Л.К., Смирнов Л.Д., Бунто Т.В. Замедление процесса старения у лабораторных мышей при воздействии хлоргидрата 2-этил-6-метил-3-оксипиридина // Изв. АН СССР. Сер. биол. - 1977. - N 1. - С. 32-37.
9. Обухова Л. К., Эмануэль Н.М. Молекулярные механизмы замедления старения антиоксидантами // Общие проблемы биологии / ВИНИТИ. - 1984. - Т.4. - С.44-80.
10. Фролькис В.В., Мурадян Х.К. Экспериментальные пути продления жизни. - Л.: Наука, 1988.
11. Baker G.T. Effect of various antioxidants on aging in Drosophila // Toxicol. Ind. Health. - 1993. - Vol. 9. - P. 163-186.
12. Epstein J., Himmelhoch S., Gershon D. Studies on ageing in nematodes. III. Electron-microscopical studies on age-associated cellular damage // Mech. Age. Dev. - 1972. - P. 245-255.
13. Massie H.R., Aiello V.R., Williams T.R. et al. Effect of vitamin A on longevity // Exp. Gerontol. - 1993. - Vol. 28. - P. 601-610.
14. Kumari M. V., Yoneda Т., Hiramatsu M. Effect of "beta CATECHIN" on the life span of senescence accelerated mice (SAM-P8 strain) // Biochem. Mol. Biol. Int. - 1997. - Vol. 41, N 5. - P. 1005-1011.
15. Болдырев A.A. Карнозин. Биологическое значение и возможности применения в медицине. - M.: Изд-во МГУ, 1998. - 320 с.
16. Pierpaoli W., Regelson W. Pineal control of aging: effect of melatonin and pineal grafting in aging mice // Proc. Nat. Acad. Sci. USA - 1986. - Vol. 91.- P. 787-791.
17. Reiter R., Tang L., Garcia J.J., Mucoz H.A. Pharmacological actions of melatonin in oxygen radical pathophysiology // Life Sci. - 1997. - Vol. 60, N 25. - P. 2255-2271.
18. Машковский М.Д. Лекарственные средства. - M.: Медицина, 1993. - Ч. I, гл. 3. - С. 375.
19. Анисимов В.Н., Арутюнян А.В, Хавинсон В.Х. / / Докл. АН - 1997. - Т. 352. - N 6. - С. 831-833.2

Изобретение относится к медицине, а именно к фармакологии, и касается выделенных из эпифиза животных комплекса биологически активных полипептидов. Последний получают путем измельчения эпифиза, экстракции уксусной кислотой при температуре 7-15oС в присутствии хлористого цинка, обработки надосадочной жидкости ацетоном, органическим растворителем, осадок фильтруют, промывают ацетоном, высушивают, готовят раствор с содержанием пептидов 15-35 мг/мл, водорастворимые фракции отделяют ультрафильтрацией и получают целевой продукт, содержащий комплекс полипептидов с молекулярной массой от 1000 до 12000 Да. Предложено фармакологическое средство, содержащее в качестве активного начала указанный выше комплекс и способ профилактики и лечения возрастной патологии путем введения эффективного количества фармакологического средства. Технический результат - расширение арсенала эпифизарных биологически активных средств. 3 с. и 3 з.п. ф-лы, 6 табл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| АНИСИМОВ В.Н | |||
| и др | |||
| Роль пептидов эпифиза в регуляции гомеостаза | |||
| - Успехи современной биологии, 1993, т.113, вып.6, с.752-762 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч.1, гл.3, с.375 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО ПРЕПАРАТА ИЗ ТКАНЕЙ МОЗГА | 1994 |
|
RU2071335C1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| МЕМБРАНОСТАБИЛИЗИРУЮЩЕЕ И АНТИОКСИДАНТНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО "РИКАВИТ" | 1985 |
|
RU2006224C1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| US 4067963 A, 10.01.1978 | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Способ прогнозирования гемодинамических нарушений при спинномозговой анестезии во время операции кесарево сечение у первородящих юного возраста | 2017 |
|
RU2657784C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| СОПОЛИМЕРИЗУЕМЫЕ СЕРОСОДЕРЖАЩИЕ УСИЛИТЕЛИ АДГЕЗИИ И КОМПОЗИЦИИ, ИХ СОДЕРЖАЩИЕ | 2013 |
|
RU2624019C2 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| ЖАРОВАЯ ТРУБА КАМЕРЫ СГОРАНИЯ | 1971 |
|
SU464206A1 |
Авторы
Даты
2001-02-20—Публикация
2000-06-29—Подача