Изобретение относится к области химии, а именно к способам получения калийсберегающего диуретика, а именно спиронолактона (верошпирона, альдактона) из доступного сырья - стеринов растительного и животного происхождения.
Спиронолактон [ 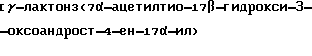 пропионовая кислота] формулы (I).
пропионовая кислота] формулы (I).
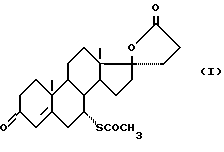
является высокоэффективным диуретиком, имеющим целый ряд преимуществ по сравнению с другими диуретиками: не изменяет структуры почечного эпителия, не характеризуется диабетогенным действием, может применяться при гипокалиемии, вызванной другими диуретиками.
Способы получения спиронолактона (I) предусматривают разновидности ацетиленового синтеза и далее металлирование этинильной группы и ее карбоксилирование с предварительной защитой  гидрирование тройной связи, лактонизацию и построение
гидрирование тройной связи, лактонизацию и построение  структуры. Выходы на отдельных стадиях высоки и составляют 88-95% [1-11].
структуры. Выходы на отдельных стадиях высоки и составляют 88-95% [1-11].
В известных способах необходимо использовать на различных ступенях синтеза две защитные группы: этиленкетальную (на стадии карбоксилирования) и енолэфирную (на стадии введения 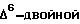 связи).
связи).
Кроме того, существенным недостатком этих способов является крупномасштабное использование ацетилена, применение в качестве металлирующего агента гидрида натрия, бутиллития, реактива Гриньяра, а также использование на стадии гидрирования палладиевого катализатора или применение давления в случае никель-боридного катализатора, что усложняет процесс.
Другой путь построения молекулы спиронолактона основан на использовании 17-спирооксиранов.
Наиболее близким к предложенному является способ получения спиронолактона общей формулы (I), заключающийся в том, что андростендион (АД) формулы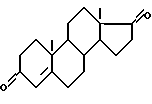
подвергают защите  метиленируют по 17-кетогруппе диалкилсульфонийметилидом, генирируемым in situ из триметилсульфонийбромида с последующим построением
метиленируют по 17-кетогруппе диалкилсульфонийметилидом, генирируемым in situ из триметилсульфонийбромида с последующим построением  структуры, превращением полученного оксиранового цикла в лактоновый, присоединением тиоуксусной кислоты и выделением целевого продукта [12].
структуры, превращением полученного оксиранового цикла в лактоновый, присоединением тиоуксусной кислоты и выделением целевого продукта [12].
В известном способе декарбоалкоксилирование осуществляется на последней стадии, и сложноэфирная группировка в лактонном кольце, проходя несколько стадий, может гидролизоваться и образовывать побочный продукт, снижающий выход основного продукта. Кроме того, реакция декарбоалкоксилирования проводится в жестких условиях: при высокой температуре и давлении в присутствии сильной кислоты.
Техническим результатом предложенного способа является повышение выхода основного продукта путем исключения образования побочных продуктов и осмоления реакционной массы, проведение реакций в более мягких условиях.
Технический результат достигается тем, что в способе получения 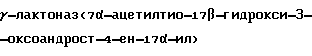 пропионовой кислоты формулы (I)
пропионовой кислоты формулы (I)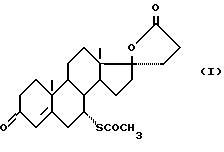
заключающемся в том, что андростендион или его производное формулы (II)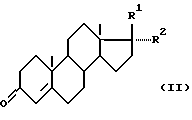
где R1 - карбонитрил, R2 - гидроксил, подвергают защите 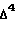 4-3-кетосистемы, метиленированию по 17- кетогруппе диалкилсульфонийметилидом, генирируемым in situ из триалкилсульфонийгалогенида с последующим превращением полученного оксиранового цикла в лактонный, построением
4-3-кетосистемы, метиленированию по 17- кетогруппе диалкилсульфонийметилидом, генирируемым in situ из триалкилсульфонийгалогенида с последующим превращением полученного оксиранового цикла в лактонный, построением  системы, присоединением тиоуксусной кислоты и выделением целевого продукта, построение
системы, присоединением тиоуксусной кислоты и выделением целевого продукта, построение  системы осуществляют после построения лактонного кольца и одновременного декарбоалкоксилирования путем нагревания в апротонном растворителе в присутствии каталитических количеств насыщенных водных растворов солей сильных оснований и сильных кислот, и последующей селективной функционализацией 6-го положения стероидной молекулы с помощью реакций галоидирования - дегидрогалоидирования.
системы осуществляют после построения лактонного кольца и одновременного декарбоалкоксилирования путем нагревания в апротонном растворителе в присутствии каталитических количеств насыщенных водных растворов солей сильных оснований и сильных кислот, и последующей селективной функционализацией 6-го положения стероидной молекулы с помощью реакций галоидирования - дегидрогалоидирования.
Причем андростендион (АД) получают путем микробиологического окисления стеринов растительного или животного происхождения общей формулы (III)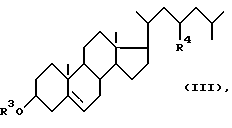
где R3 - ацил, или алкил, или карбокси-ацил, или атом H, R4 - H или C2H5, а производное андростендиона формулы (II) с R1 - карбонитрил, a R2 - гидроксил получают путем взаимодействия АД с ацетонциангидрином.
Кроме того, защиту  производного андростендиона формулы (II) можно осуществлять путем образования спирокеталей на основе этиленгликоля, или 2 - моно - или 2,2 - дизамещенных или незамещенных производных 1,3 - пропандиола, или пирролидиновых или морфолиновых енаминов или енолэфиров.
производного андростендиона формулы (II) можно осуществлять путем образования спирокеталей на основе этиленгликоля, или 2 - моно - или 2,2 - дизамещенных или незамещенных производных 1,3 - пропандиола, или пирролидиновых или морфолиновых енаминов или енолэфиров.
Кроме того, генерирование диалкилсульфонийметилида in situ из триалкилсульфонийгалогенида осуществляют в присутствии сильного основания.
Причем в качестве сильного основания используют трет-бутилаты или гидриды, или гидратированные гидроокиси щелочных металлов.
Кроме того, указанное генерирование можно осуществлять также в присутствии катализатора межфазового переноса.
Кроме того, в качестве катализатора межфазового перехода использовать четвертичные аммонийные соли в эффективном количестве.
В качестве четвертичной аммонийной соли можно использовать триалкилариламмонийгалогениды.
Кроме того, в реакции галоидирования в качестве агента можно использовать дибромантин или N- или N-бромсукцинимид, а дегидрогалоидирование проводят в среде апротонного растворителя с помощью солей щелочных и щелочноземельных металлов.
Способ получения 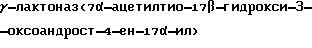 пропионовой кислоты (спиронолактона) формулы (I) осуществляется по следующей схеме:
пропионовой кислоты (спиронолактона) формулы (I) осуществляется по следующей схеме: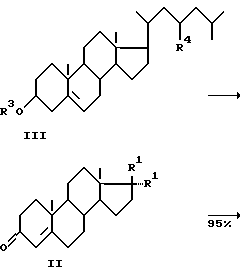
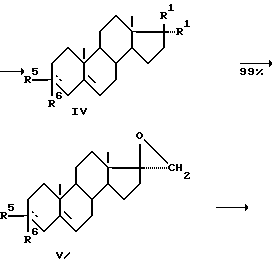
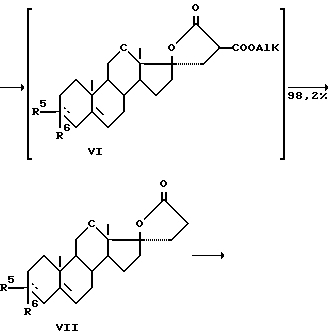
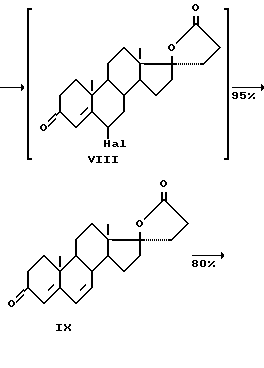
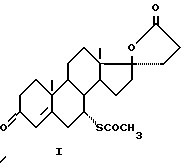
где R5 и R6 - енолэфир или циклический кеталь, или енамин.
Андростендион (АД), полученный путем микробиологического окисления стеринов растительного или животного происхождения общей формулы (III), или его производное (II), полученное путем взаимодействия АД с ацетонциангидрином, первоначально подвергают защите по 3- кетогруппе с образованием енолэфиров, или циклических кеталей, или енаминов (соединение общей формулы (IV). Затем это соединение метиленируют по 17-кетогруппе действием диалкилсульфонийметилида, генерируемого in situ из триалкил-сульфонийгалогенида в присутствии сильного основания и катализатора межфазового переноса (или без него) в апротонном растворителе.
Полученный с выходом 99% оксиран (V) превращают в спиролактон (VII) конденсацией его с диалкилмалонатом в присутствии алкоголята натрия с последующим декарбоалкоксилированием путем нагревания реакционного продукта в апротонном растворителе при температуре кипения в присутствии каталитических количеств насыщенных водных растворов солей сильных кислот и сильных оснований. Селективную функционализацию 6-го положения осуществляют с помощью последовательных реакций бромирования - дегидробромирования, причем для направленного введения брома при C6 используют реагенты аллильного бромирования, такие как N-бромсукцинимид или N- бромацетамид, или дибромантин в апротонном растворителе. Реакцию дегидробромирования проводят без выделения промежуточного продукта (VIII) в присутствии солей щелочных или щелочно-земельных металлов при температуре 60-80oC. Образующийся с выходом 95% спиродиен (IX) подвергают взаимодействию с тиоуксусной кислотой. Общий выход спиронолактона (I), соответствующего требованию фармакопеи, составляет 45 - 50%, считая на стерины (III), или 70,2%, считая на производные АД (II).
Изобретение иллюстрируется следующими примерами
Пример 1. Энолэфир АД (3 - метоксиандрост -3,5- диен -17-он).
К раствору 19 г триметилортоформиата в 146 мл метанола добавляют 62,5 г АД. Суспензию перемешивают в течение 15 мин и добавляют медленно 142 мл раствора 0,125 г сульфосалициловой кислоты в 26,74% растворе триметилортоформиата в метаноле. Реакционную массу выдерживают при температуре 20...25oC в течение 1 ч 15 мин. По окончании выдержки реакционную массу охлаждают до 10. . . 15oC, добавляют медленно 46,9 мл ацетона и выдерживают в течение 1 ч при этой же температуре. Затем добавляют 0,5 мл триэтиламина до pH 7-8, охлаждают реакционную массу до 0...+2oC и прибавляют раствор 1,52 г едкого натра в 260 мл воды. По окончании выдержки осадок отфильтровывают, промывают на фильтре раствором 0,38 г едкого натра в 65 мл воды и 0,25% раствором триэтиламина в метаноле.
Получают 62,3 г енолэфира АД (95%) с т.пл.171...173oC.
Пример 2.
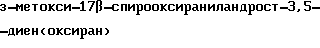
Растворяют при перемешивании 74 г гранулированного едкого натра в 34 мл воды и 1,3 л диметилсульфоксида при температуре 90-95oC. После охлаждения до 60-65oC к полученной суспензии прибавляют 100 г триметилсульфонийбромида, 6 г триэтилбензиламмонийхлорида (ТЭБАХ) и 130 г 3-метоксиандроста - 3,5 - диен - 17-она (енолэфира АД) и перемешивают в токе азота 4 ч при этой температуре. Реакционную смесь охлаждают до температуры 22 ± 4oC, выливают в 2 л охлажденной до температуры +10oC воды. Реакционную смесь охлаждают до (3 ± 2)oC и дают выдержку при этой температуре в течение 1 ч. Осадок отфильтровывают, промывают 105 мл охлажденного до (3 ± 2)oC метанола, сушат до постоянной массы. Получают 134,7 г (99% от теоретического) оксирана в виде кремового кристаллического порошка, т. пл. 128...131oC, содержание исходного енолэфира АД не выше 2% (ТСХ-анализ).
Пример 3.
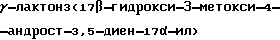 пропионовой кислоты (лактон).
пропионовой кислоты (лактон).
36 г металлического натрия растворяют при перемешивании в 1,8 л абсолютного этилового спирта и прибавляют 238 мл (251 г) малонового эфира и 315 г оксирана. Реакционную смесь кипятят в течение 4,5...6 ч. Затем отгоняют при атмосферном давлении этанол в количестве 1,5 л, а к остатку прибавляют 1,5 л диметилсульфоксида и 350 мл 14,3% водного раствора хлорида натрия. Реакционную массу нагревают до 100oC и перемешивают 3,5...5 ч. Охлажденную до 35oC реакционную массу выливают в 5,25 л воды и перемешивают 20 мин при этой температуре. Затем охлаждают до 5oC и выдерживают 2 ч. Осадок: отфильтровывают, промывают водой до pH 7, сушат. Получают 351,3 г (98,2%) лактона с т.пл. 219oC.
Пример 4.
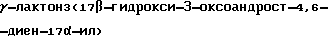 пропионовой кислоты спиродиен).
пропионовой кислоты спиродиен).
К суспензии 62,5 г лактона в 93,8 мл ацетона и 12,5 мл воды порциями при перемешивании прибавляют 25 г дибромантина или 28 г N- бромсукцинимида. В процессе прибавления температура поднимается до (28 ± 2)oC. Суспензия сначала растворяется, а потом из раствора выпадает осадок. Дают выдержку при этой температуре 20 мин. Затем к реакционной массе прибавляют 187,6 мл диметилформамида и 7,5 г (5,3 г 100%) бромистого лития и 6,8 г углекислого лития и перемешивают при (79 ± 1)oC 3,5...4 ч. После охлаждения до (20 ± 1)oC реакционную смесь отфильтровывают от неорганических солей, промывают 73 мл диметилформамида. Объединенный диметилформамидный раствор полученного спиродиена прикапывают за 25. . .30 мин в 1100 мл воды, охлажденной до 3 ± 2oC, и выдерживают 30 мин при этой температуре. Осадок отфильтровывают, промывают 160 мл воды до нейтральной р-ции. Сушат при 40...50oC до постоянной массы. Получают 54,5 г (60%-ного, 43,6 г 100%-ного, 95% от теоретического) спиродиена в виде кремового кристаллического порошка, т.пл. 140oC, [α]
Пример 5.
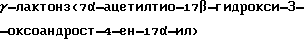 пропионовой кислоты (спиронолактон).
пропионовой кислоты (спиронолактон).
20 г технического спиродиена растворяют в 70 мл метанола при нагревании, прибавляют 2 г активированного угля и кипятят 30 мин. Полученный раствор фильтруют от угля, промывают 40 мл горячего метанола. К отфильтрованному реакционному раствору прибавляют 8 мл тиоуксусной кислоты, кипятят 3 ч при перемешивании в токе азота. Реакционную массу охлаждают и выдерживают 3 ч при -5. . .-10oC. Осадок отфильтровывают и промывают 40 мл охлажденного метанола.
Получают 16,64 г (85% от теоретического) технического спиронолактона в виде желтоватого кристаллического порошка с т.пл. 185-192oC. После очистки из смеси ацетон-ментанол выход спиронолактона фармакопейного качества 80% от теоретического, считая на спиродиен.
Пример 6. Андрост-4-ен-3,17-дион(II, АД, R1 и R2 вместе кетогруппа)
Культуру Mycobacterium smegmatis ВКПМ Ac-1552 в 6-дневном возрасте, выросшую на агаровой среде следующего состава (в г/л): глюкоза - 10, соевая мука - 3, лимонная кислота - 2,2, мочевина - 0,5, дигидрофосфат калия - 0,5, хлорид аммония -1, сульфат магния - 0,5, сульфат железа - 0,05, агар-агар ~ 25, вода дистиллированная, pH до стерилизации - 6,8-7,0, переносят в 30 мл жидкой посевной среды в конические плоскодонные колбы вместимостью 250 мл. Состав посевной среды (г/л): глюкоза - 10, соевая мука - 3, мочевина - 0,5, лимонная кислота - 2,2, хлорид аммония -1, дигидрофосфат калия - 0,5, сульфат железа - 0,05, сульфат магния - 0,5, карбонат кальция - 1,5, вода дистиллированная, pH до стерилизации - 7,0. Инкубируют 48 ч на качалке при интенсивном перемешивании 220 об/мин (эксцентриситет 5 см) и температуре 30oC.
Выращенную культуру вносят в количестве 10 об.% в среду следующего состава (г/л): глюкоза - 10, соевая мука - 10, мочевина - 0,5, гидрофосфат аммония - 1,5, лимонная кислота - 2,2, сульфат магния - 0,2, сульфат железа - 0,05, карбонат кальция - 1,5, вода дистиллированная, pH до стерилизации - 7,0. Среду разливают в аналогичные колбы по 30 мл. До стерилизации в среду добавляют хорошо гомогенизированный холестерин в количестве 1% (концентрация 10 г/л). Ферментацию проводят на качалке в условиях, описанных для получения вегетативного посевного материала, в течение 96±4 ч. По окончании ферментации (концентрация АД - 7,0 г/л по данным ВЭЖХ анализа) культуральную жидкость отделяют от биомассы на центрифуге. Биомассу экстрагируют водным ацетоном (60-65% содержания).
Растворитель упаривают в вакууме до прекращения погона. Из образовавшейся водной суспензии отфильтровывают технический целевой продукт. После перекристаллизации из хлористого метилена и гексана получают АД с выходом 70% и температурой плавления 172-174oC.
Пример 7.
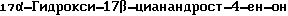 (II, циангидрин АД, R1=CN, R2=OH)
(II, циангидрин АД, R1=CN, R2=OH)
К раствору 1,63 г NaOH в 280 мл метанола добавляют 100 г АД (II). Суспензию нагревают до 40oC и добавляют последовательно 13,8 мл воды и 47,8 мл ацетонциангидрина. Реакционную массу выдерживают при температуре 35-36oC в течение ч и добавляют медленно по каплям 59 мл воды, затем выдерживают при комнатной температуре. По окончании реакции добавляют медленно 217 мл воды и выдерживают 2 ч при комнатной температуре. Осадок отфильтровывают, промывают на фильтре смесью воды и метанола (2:1 соответственно) и водой до pH 7.
Получают 104,45 г циангидрина АД с выходом 95,5%, с температурой плавления 174-176oC.
Пример 8.
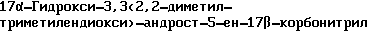 (IV, 3-пропиленкеталь циангидрина АД, R1= CN, R2= OH и R5 и R6 вместе 2,2-диметил-1,3-диоксановый цикл)
(IV, 3-пропиленкеталь циангидрина АД, R1= CN, R2= OH и R5 и R6 вместе 2,2-диметил-1,3-диоксановый цикл)
Суспензию 104,45 г циангидрина АД (II) в 522 мл хлористого метилена охлаждают до температуры 0...-5oC и в токе азота добавляют последовательно 105 мл триэтилового эфира oрто-муравьиной кислоты, 156,7 г неопентилгликоля и 15,67 г n- толуолсульфокислоты. Реакционную массу перемешивают в течение 8 ч. По окончании реакции медленно добавляют раствор 68,3 г гидрокарбоната натрия в 1,3 л воды. Суспензию охлаждают до температуры 0...+5oC и выдерживают в течение ч. Остаток отфильтровывают, промывают водой до pH 7.
Получают 130,52 г хроматографически чистого 3-пропиленкеталя циангидрина АД с выходом 98%, с температурой плавления 252oC (с разложением).
[α]
Масс-спектр, m/z: 372 [M-HCN]+; 286 [M-HCN-C5H10O]+.
ИК-спектр, ν, см-1: 3396 (ОН), 2252 (C≡N), 1672 (C=C), 1102, 1020 (-O-C-O-).
ПМР-спектр, δ, м.д.: 0,92 с и 0,96 с (3H 18-СН3 и 3H 19-СН3); 1,05 с (6H 2CH3 диоксанового цикла); 3,55 м (4H 2CH2-O диоксанового цикла); 5,42 уш.с. (1H 6-Н).
Пример 9.
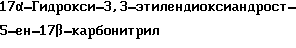 (IV, 3-этиленкеталь циангидрина АД, R1=CN, R2=OH и R5 и R6 вместе 1,2- диоксолановый цикл)
(IV, 3-этиленкеталь циангидрина АД, R1=CN, R2=OH и R5 и R6 вместе 1,2- диоксолановый цикл)
К суспензии 20 г циангидрина АД (II) в 20 мл этиленгликоля добавляют 40 мл 30% раствора метилортоформиата в метаноле и 0,4 г n-толуолсульфокислоты.
Реакционную массу нагревают до 60oC и перемешивают 2 ч. По окончании реакции реакционную массу охлаждают до 25oC и добавляют 0,6 мл триэтиламина (pH 8-9).
Реакционную массу охлаждают до температуры 0...-5oC и перемешивают 2-3 ч. Осадок отфильтровывают, промывают на фильтре метанолом, сушат.
Получают 19 г 3-этиленкеталя циангидрина АД с выходом 83,6% и температурой плавления 218-220oC.
Пример 10.
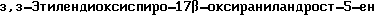 (V, 3-этиленкеталь оксирана, R5 и R6 вместе 1,2- диоксолановый цикл)
(V, 3-этиленкеталь оксирана, R5 и R6 вместе 1,2- диоксолановый цикл)
К смеси 7,2 г 3-этиленкеталя циангидрина АД и 6,8 г триметилсульфонийбромида в 145 мл диметилсульфоксида добавляют 7,2 г порошкообразного едкого натра. Суспензию перемешивают в течение 10 ч при температуре 60oC. Затем к реакционной массе медленно добавляют 200 мл воды, массу охлаждают до комнатной температуры. Осадок отфильтровывают, промывают водой.
Получают 6,52 г 3-этиленкеталя оксирана с выходом 94% и температурой плавления 186-189oC.
[α]
ПМР-спектр, δ, м. д. CDCl3: 0,94 с (3H, 18-СН3); 1,09 с (3H, 19-СН3); 2,78 с (2H, оксиранил, CH2); 3,97 с (4H 2CH2-O диоксоланового цикла); 5,4 м (1H винилон, Н).
Далее процесс ведется аналогично примерам 3-5.
Примеры с енаминной защитой
Пример 11. 3-(1-Пирролидинил)-андроста-3,5-диен-17-он (II, R5 и R6 вместе пирролидиновый заместитель)
К суспензии 10 г АД в 40 мл метанола, нагретой до температуры кипения, добавляют медленно 5 мл пирролидина. По окончании реакции реакционную массу охлаждают до температуры 0-5oC. Осадок отфильтровывают, промывают на фильтре охлажденным метанолом. Получают 10,7 г (90%) пирролидинового енамина АД с температурой плавления 217-220oC.
Пример 12. 3-(4-Морфолинил)-андроста-3,5-диен-17-он (II, R5 и R6 вместе морфолиновый заместитель)
К суспензии 20 г АД в 120 мл бензола добавляют 50 мл морфолина и 0,03 г n-толуолсульфокислоты. Смесь кипятят, периодически удаляя отделяющуюся воду. По окончании реакции реакционную массу охлаждают до комнатной температуры. Растворитель упаривают в вакууме до прекращения погона. К остатку добавляют 10 мл петролейного эфира (фракция с температурой кипения 70-90oC). Осадок отфильтровывают, промывают петролейным эфиром.
Получают 23,8 г (95,9%) морфолинового енамина АД с температурой плавления 205-207oC.
Источники информации
1. Enlinger E., Magnus P. J.Am.Chem.Soc., 1980, v.102, 15, p.5004-5011.
2. Sturtz G., Yanakej J., Synthesis, 1980, 4, p.289-291.
3. Pat. US 3738983, 1974 г.
4. Pat. US 3682894, 1973 г.
5. Pat. US 4057542, 1977 г.
6. Заявка Японии 57-85400, 1978 г.
7. Заявка Японии 57-197300, 1978 г.
8. Pat. US 4265816, 1980 г.
9. Заявка Японии 61-359, 1981 г.
10. Pat. US 4211701, 1980 г.
11. Заявка Японии 53-124252, 1974 г.
12. Pat. FR 2216273, 2281357, 1974 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРЕГНАНОВ | 1999 |
|
RU2156255C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОРТИКОСТЕРОИДОВ | 1999 |
|
RU2156256C1 |
| СПОСОБ ПОЛУЧЕНИЯ СТЕРОИДНЫХ ЭФИРОВ | 1996 |
|
RU2091388C1 |
| ШТАММ Rhodococcus erythropolis ВКПМ Ac-1740 ДЛЯ ПОЛУЧЕНИЯ 9 АЛЬФА-ГИДРОКСИСТЕРОИДОВ | 2007 |
|
RU2351645C1 |
| ШТАММ БАКТЕРИЙ MYCOBACTERIUM NEOAURUM И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ ДЛЯ ПОЛУЧЕНИЯ АНДРОСТ-4-ЕН-3,17-ДИОНА ИЗ СТЕРИНОВ РАСТИТЕЛЬНОГО И ЖИВОТНОГО ПРОИСХОЖДЕНИЯ | 2001 |
|
RU2231553C2 |
| УНИВЕРСАЛЬНОЕ СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ РЕПРОДУКЦИИ ПОЗВОНОЧНЫХ ЖИВОТНЫХ | 1996 |
|
RU2101013C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛЕНАНДРОСТ-4-ЕН-3,17-ДИОНА ИЗ АНДРОСТ-4-ЕН-3,17-ДИОНА, СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛЕНАНДРОСТА-1,4-ДИЕН-3,17-ДИОНА (ЭКСЕМЕСТАНА) С ИСПОЛЬЗОВАНИЕМ ПОЛУЧЕННОГО 6-МЕТИЛЕНАНДРОСТ-4-ЕН-3,17-ДИОНА | 2010 |
|
RU2425052C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНДРОСТ-4-ЕН-3,17-ДИОНА ИЗ СТЕРИНОВ РАСТИТЕЛЬНОГО И ЖИВОТНОГО ПРОИСХОЖДЕНИЯ ИЛИ ИХ ПРОИЗВОДНЫХ | 1998 |
|
RU2205224C2 |
| ШТАММ БАКТЕРИЙ MYCOBACTERIUM SMEGMATIS, ИСПОЛЬЗУЕМЫЙ ДЛЯ ОКИСЛЕНИЯ СТЕРИНОВ РАСТИТЕЛЬНОГО И ЖИВОТНОГО ПРОИСХОЖДЕНИЯ ДО АНДРОСТ-4-ЕН-3,17-ДИОНА | 1997 |
|
RU2126837C1 |
| СПОСОБ ПОЛУЧЕНИЯ НОВЫХ 3β-АЦЕТОКСИ-17α-ГИДРОПЕРОКСИ-16α-МЕТИЛПРЕГНАНОВ ИЗ Δ-20-КЕТОСТЕРОИДОВ И СПОСОБ ПОЛУЧЕНИЯ 3β-АЦЕТОКСИ-17α-ГИДРОКСИ-16α-МЕТИЛПРЕГНАНОВ С ИСПОЛЬЗОВАНИЕМ 3β-АЦЕТОКСИ-17α-ГИДРОПЕРОКСИ-16α-МЕТИЛПРЕГНАНОВ | 2009 |
|
RU2418805C1 |
Изобретение относится к фармацевтической химии, а именно к улучшенному способу получения калийсберегающего диуретика, а именно спиронолактона (верошпирона, альдактона) из доступного сырья - стеаринов растительного и животного происхождения. По описываемому способу спиронолактон 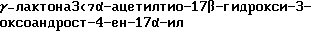 пропионовую кислоту] формулы I
пропионовую кислоту] формулы I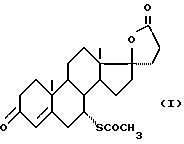
получают из андростендиона или его производного формулы II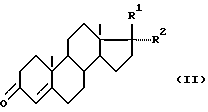
где R1 - карбонитрил, R2 - гидроксил, подвергают защите Δ4-3-кетосистемы, метиленированию по 17-кетогруппе диалкилсульфонийметилидом, генирируемым in situ из триалкилсульфонийгалогенида, с последующим превращением полученного оксиранового цикла в лактонный построением Δ4,6-диеноновой структуры, присоединением тиоуксусной кислоты и выделением целевого продукта. Построение Δ4,6-диеноновой системы осуществляют после предварительного построения лактонового кольца и одновременного декарбоалкоксилирования путем нагревания в апротонном растворителе в присутствии каталитических количеств насыщенных водных растворов солей сильных оснований и сильных кислот, селективной функционализацией 6-го положения стероидной молекулы с помощью реакций галоидирования - дегидрогалоидирования. Затем присоединяют тиоуксусную кислоту и выделяют целевой продукт. Способ позволяет повысить выход основного продукта путем исключения образования побочных продуктов и осмоления реакционной массы в результате проведения реакций в мягких условиях. 8 з.п.ф-лы.
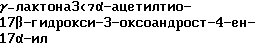 пропионовой кислоты формулы I
пропионовой кислоты формулы I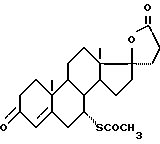
заключающийся в том, что андростендион или его производное формулы II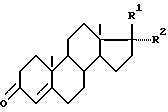
где R1 - карбонитрил, R2 - гидроксил, подвергают защите Δ4-3-кетосистемы, метиленированию по 17-кетогруппе диалкилсульфонийметилидом, генерируемым in situ из триалкилсульфонийгалогенида, с последующим превращением полученного оксиранового цикла в лактонный, построением Δ4,6-диеноновой структуры, присоединением тиоуксусной кислоты и выделением целевого продукта, отличающийся тем, что построение диеноновой системы осуществляют после построения лактонного кольца и одновременного декарбоалкоксилирования путем нагревания в апротонном растворителе в присутствии каталитических количеств насыщенных водных растворов солей сильных оснований и сильных кислот, и последующей селективной функционализацией 6-го положения стероидной молекулы с помощью реакций галоидирования - дегидрогалоидирования.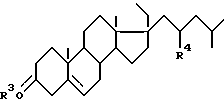
где R3 - ацил, или алкил, или карбоксиацил, или атом Н;
R1 - Н или С2Н5,
а его производное формулы II получают путем взаимодействия андростендиона с ацетонциангидрином.
| Ehlinger T., Magnus P.J | |||
| Am | |||
| Chem | |||
| Soc | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Приспособление для тонкой настройки струнных инструментов | 1926 |
|
SU5004A1 |
| Sturtz G., Yanakej J | |||
| Synthesis | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| US 3738983, 1974 | |||
| US 3682894, 1973 | |||
| US 4057542, 1977 | |||
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
| US 4265816, 1980 | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| US 4211701, 1980 | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| СПОСОБ ВЫЯВЛЕНИЯ СТЕНОЗА ВИСЦЕРАЛЬНЫХ И ПОЧЕЧНЫХ АРТЕРИЙ ПРИ ТРОМБИРОВАННЫХ АНЕВРИЗМАХ БРЮШНОЙ АОРТЫ | 2003 |
|
RU2216273C1 |
| УСТРОЙСТВО ДЛЯ СОЗДАНИЯ ЛЕДЯНОЙ ПЕРЕПРАВЫ | 2005 |
|
RU2281357C1 |
| Способ получения тиоацетил-или меркаптопроизводных стероидных лактонов | 1974 |
|
SU517262A3 |
| GB 1447247, 1976 | |||
| GB 1450425, 1976 | |||
| GB 1450693, 1976 | |||
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
Авторы
Даты
2001-02-27—Публикация
1999-12-08—Подача