Настоящее изобретение относится к новым соединениям, которые способны сохранять, увеличивать или восстанавливать чувствительность клеток к терапевтическим или профилактическим средствам. Данное изобретение относится также к фармацевтическим композициям, содержащим эти соединения. Соединения и фармацевтические композиции по данному изобретению специально предназначены для воздействия на клетки с множественной лекарственной устойчивостью, для предотвращения развития c множественной лекарственной устойчивостью и для лечения злокачественных опухолей с множественной лекарственной устойчивостью.
Главной проблемой, влияющей на эффективность химиотерапевтического лечения, является эволюция клеток, которые под воздействием химиотерапевтического средства приобретают устойчивость к большому количеству неродственных в структурном отношении лекарственных и терапевтических средств. Такая множественная лекарственная устойчивость часто возникает в случае избытка продуцирования P-гликопротеина мембраны 170 кДа (gp-170). Белок gp-170 присутствует в плазматических мембранах некоторых здоровых тканей, помимо линий раковых клеток, и гомологичен бактериальным транспортным белкам (Hait et al. Cancer Communications, vol. 1(1), 35 (1989); West, TIBS, vol. 15, 42 (1990)). Этот белок действует как экспортирующий насос, вызывая лекарственную устойчивость в результате активного вытеснения токсичных химических веществ. Хотя механизм действия этого насоса не известен, существует мнение, что белок gp-170 вытесняет вещества, обладающие определенными химическими и физическими характеристиками, такими как гидрофобность, наличие карбонильных групп или присутствие глутатионового конъюгата (см. West).
Другой белок с множественной лекарственной устойчивостью, MRP (белок, связанный с лекарственной устойчивостью), был недавно обнаружен в клетках H69AR, линии клеток с множественной лекарственной устойчивостью, у которой отсутствует детектируемый P-гликопротеин [S.P.C. Cole et al. Science, 258, p. 1650-54 (1992)]. Лекарственно-устойчивый белок был обнаружен также в других линиях клеток с множественной лекарственной устойчивостью, не имеющих P-гликопротеина, таких как клетки рака груди HL60/ADR и MCF-7 [(E. Schneider et al. Cancer Res., 54, p. 152-58 (1994); и N. Krishnamachary et al. Cancer Res. 53, p. 3658-61 (1993)].
Ген лекарственно-устойчивого белка кодирует мембранный белок 190 кДа, который является еще одним членом суперсемейства АТФ-связывающих кассет. Лекарственно-устойчивый белок подобно P-гликопротеину действует как насос, удаляющий натуральные лекарственные средства из клетки. Возможной физиологической функцией лекарственно-устойчивого белка может быть АТФ-зависимый перенос глутатионовых S-конъюгатов [G. Jedlitschky et al. Cancer Res., 54, p. 4833-36 (1994); I. Leier et al., J. Biol. Chem., 269, p. 27807-10 (1994); и Muller et al., Proc. Nail. Acad. Sci., USA, 91, p. 13033-37 (1994)].
Роль лекарственно-устойчивого белка в области клинической лекарственной устойчивости еще предстоит установить, но вполне вероятно, что лекарственно-устойчивый белок может быть еще одним белком, определяющим широкую устойчивость к противораковым лекарственным средствам.
Разные химические средства использовали для подавления множественной лекарственной устойчивости и восстановления чувствительности к лекарственным средствам. Хотя некоторые лекарственные средства улучшают чувствительность клеток с множественной лекарственной устойчивостью в отношении химиотерапевтических средств, их введение часто сопровождается нежелательными побочными эффектами (см. Hait и др.). Например, хотя циклоспорин A (CsA), широко применяемый иммуносупрессор, может повышать чувствительность определенных раковых клеток в отношении химиотерапевтических средств (Slater et al., Br. J. Cancer, vol. 54, 235 (1986)), концентрации, необходимые для достижения такого эффекта, вызывают значительную иммуносупрессию у больных, иммунные системы которых уже ослаблены химиотерапией (см. Hait и др.). Кроме того, использование CsA часто сопровождается вредными побочными эффектами, включающими нефротоксичность, гепатотоксичность и расстройства центральной нервной системы. Аналогичным образом блокаторы кальциевого переноса и ингибиторы кальмодулина сенсибилизируют клетки с множественной лекарственной устойчивостью, но каждый из них вызывает нежелательные физиологические эффекты (см. Hait et al.; Twentyman et al., Br. J. Cancer, vol. 56, 55 (1987)).
Последние исследования привели к созданию лекарственных средств, которые потенциально обладают гораздо большим клиническим значением в отношении сенсибилизации клеток с множественной лекарственной устойчивостью. Эти средства включают аналоги CsA, которые не оказывают иммуносупрессивного действия, такие как 11-метиллейцинциклоспорин (11-met-leu CsA) (см. Hait et al.; Twentyman et al.), или средства, которые могут быть эффективными при низких дозах, такие как иммуносупрессор FK-506 (Epand and Epand, Anti-Cancer Drug Design 6, 189 (1991)). Публикация PCT WO 94/07858 относится к новому классу средств, модифицирующих множественную лекарственную устойчивость, которые по своей структуре несколько схожи с иммуносупрессорами FK-506 и рапамицином. Несмотря на эти разработки, по-прежнему существует необходимость в более эффективных средствах, которые можно использовать для ресенсибилизации клеток с множественной лекарственной устойчивостью в отношении терапевтических или профилактических средств или предотвращения развития множественной лекарственной устойчивости.
Краткое изложение сущности изобретения
Настоящим изобретением предусматриваются новые соединения, которые неожиданно обладают более высокой способностью по сравнению с ранее описанными модификаторами множественной лекарственной устойчивости (MDR), сохранять, увеличивать или восстанавливать чувствительность к лекарственным средствам в лекарственно-устойчивых клетках, композиции, содержащие эти соединения, и способы их применения. Соединения по настоящему изобретению можно использовать отдельно или в сочетании с другими терапевтическими или профилактическими средствами с целью сохранения, увеличения или восстановления терапевтического или профилактического действия лекарственных средств в клетках, особенно в клетках с множественной лекарственной устойчивостью, или с целью предотвращения образования клеток с множественной лекарственной устойчивостью. В соответствии с одним вариантом осуществления данного изобретения эти новые соединения, композиции и способы успешно используются для усиления схемы химиотерапевтического лечения или профилактики рака и других болезней.
Настоящим изобретением предусматриваются также способы получения соединений по данному изобретению и промежуточных продуктов, полезных при осуществлении этих способов.
Подробное описание изобретения
Данное изобретение относится к новому классу соединений, выраженных формулой (I):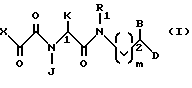
где R1, В и D независимо друг от друга обозначают:
Ar, (C1-C6)-алкил с прямой или разветвленной цепью, (C2-C6)-алкенил или алкинил с прямой или разветвленной цепью, (C5-C7)-циклоалкилзамещенный (C1-C6)-алкил с прямой или разветвленной цепью, (C5-C7)-циклоалкилзамещенный (C3-C6)-алкенил или алкинил с прямой или разветвленной цепью, (C5-C7)-циклоалкенилзамещенный (C1-C6)-алкил с прямой или разветвленной цепью, (C5-C7)-циклоалкенилзамещенный (C3-C6)-алкенил или алкинил с прямой или разветвленной цепью, Ar-замещенный (C1-C6)-алкил с прямой или разветвленной цепью, Ar-замещенный (C3-C6)-алкенил или алкинил с прямой или разветвленной цепью;
где любая из CH2 групп указанных алкильных цепей может быть необязательно замещена гетероатомом, выбираемым из группы, включающей О, S, SO, SO2 и NR, где R выбирают из группы, включающей водород, (C1-C4)-алкил с прямой или разветвленной цепью, (C3-C4)-алкенил или алкинил с прямой или разветвленной цепью и (C1-C4) мостиковый алкил, где мостиковая связь образована между азотом и атомом углерода указанной содержащей гетероатом цепи с образованием кольца и где указанное кольцо необязательно связано с Ar группой;
В и D могут также быть водородом;
J выбирают из группы, включающей (C1-C6)-алкил с прямой или разветвленной цепью, (C3-C6)-алкенил с прямой или разветвленной цепью, Ar-замещенный (C1-C6)-алкил с прямой или разветвленной цепью и Ar-замещенный (C3-C6)-алкенил или алкинил с прямой или разветвленной цепью;
К выбирают из группы, включающей (C1-C6)-алкил с прямой или разветвленной цепью, Ar-замещенный (C1-C6)-алкил с прямой или разветвленной цепью, Ar-замещенный (C2-C6)-алкенил или алкинил с прямой или разветвленной цепью и циклогексилметил;
X выбирают из группы, включающей Ar, -OR2 и -NR3R4;
где R2 имеет те же значения, что и R1; R3 и R4 независимо друг от друга имеют те же значения, что В и D, или R3 и R4, вместе взятые, образуют 5-7-членное гетероциклическое алифатическое или ароматическое кольцо;
где Ar является карбоциклической ароматической группой, выбираемой из группы, включающей фенил, 1-нафтил, 2-нафтил, инденил, азуленил, флуоренил и антраценил;
или Ar является гетероциклической ароматической группой, выбираемой из группы, включающей 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 2-пиридил, 3-пиридил, 4-пиридил, пирролил, оксазолил, тиазолил, имидазолил, пираксолил, 2-пиразолинил, пиразолидинил, изоксазолил, изотриазолил, 1,2,3-оксадиазолил, 1,2,3-триазолил, 1,3,4- тиадиазолил, пиридазинил, пиримидинил, пиразинил, 1,3,5-триазинил, 1,3,5-тритианил, индолизинил, индолил, изоиндолил, 3H-индолил, индолинил, бензо[b] фуранил, бензо[b]тиофенил, 1H-индазолил, бензимидазолил, бензтиазолил, пуринил, 4H-хинолизинил, хинолинил, 1,2,3,4-тетрагидрохинолинил, изохинолинил, 1,2,3,4-тетрагидроизохинолинил, циннолинил, фталазинил, хиназолинил, хиноксалинил, 1,8-нафтиридинил, птеридинил, карбазолил, акридинил, феназинил, фенотиазинил и феноксазинил;
где Ar может иметь один или несколько заместителей, которые независимо друг от друга выбирают из группы, включающей водород, галоген, гидроксил, нитро, -SO3H, трифторметил, трифторметокси, (C1-C6)-алкил с прямой или разветвленной цепью, (C2-C6)-алкенил с прямой или разветвленной цепью, O-[(C1-C6)-алкил с прямой или разветвленной цепью] , O-[(C3-C4)-алкенил с прямой или разветвленной цепью], О-бензил, О-фенил, 1,2-метилендиокси, -NR5R6, карбоксил, N-(C1-C5-алкил с прямой или разветвленной цепью или C3-C5-алкенил с прямой или разветвленной цепью)-карбоксамиды, N,N-ди-(C1-C5-алкил с прямой или разветвленной цепью или C3-C5-алкенил с прямой или разветвленной цепью)-карбоксамиды, морфолинил, пиперидинил, O-М, CH2-(CH2)q-M, O-(CH2)q-M, (CH2)q-O-M и CH=CH-М;
где R5 и R6 независимо друг от друга выбирают из группы, включающей водород, (C1-C6)-алкил с прямой или разветвленной цепью, (C3-C6)-алкенил или алкинил с прямой или разветвленной цепью и бензил; М выбирают из группы, включающей 4-метоксифенил, 2-пиридил, 3-пиридил, 4-пиридил, пиразил, хинолил, 3,5-диметилизоксазоил, 2-метилтиазоил, тиазоил, 2-тиенил, 3-тиенил и пиримидил; и q означает 0-2; и
m означает 0 или 1.
Предпочтительно, чтобы по крайней мере один из В или D независимо от другого был выражен формулой -(CH2)r-(Z)-(CH2)s-Ar, где:
r означает 1-4;
s означает 0-1;
Ar имеет значения, указанные выше для соединений формулы (I); и
каждый Z независимо от других выбирают из группы, включающей CH2, О, S, SO, SO2 и NR, где R выбирают из группы, включающей водород, (C1-C4)-алкил с прямой или разветвленной цепью, (C3-C4)-алкенил или алкинил с прямой или разветвленной цепью и (C1-C4) мостиковый алкил, где мостиковая связь образована между атомом азота и Ar группой.
Предпочтительными Ar группами по данному изобретению являются фенил, 2-пиридил, 3-пиридил, 4-пиридил, имидазолил, индолил, изоиндолил, хинолинил, изохинолинил, 1,2,3,4-тетрагидроизохинолинил и 1,2,3,4-тетрагидрохинолинил, где указанный Ar может иметь один или несколько заместителей, которые независимо друг от друга выбирают из группы, включающей водород, гидроксил, нитро, трифторметил, (C1-C6)-алкил с прямой или разветвленной цепью, O-[(C1-C6)-алкил с прямой или разветвленной цепью], галоген, SO3H и NR3R4, где R3 и R4 независимо друг от друга выбирают из группы, включающей (C1-C6)-алкил с прямой или разветвленной цепью, (C3-C6)-алкенил с прямой или разветвленной цепью, водород и бензил; или где R3 и R4, вместе взятые, могут образовывать 5-6-членное гетероциклическое кольцо.
Примеры некоторых предпочтительных соединений формулы (I) имеют формулу (II) или (III):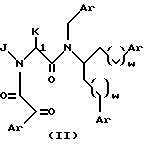
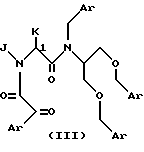
где J и K независимо друг от друга обозначают (C1-C6)- алкил с прямой или разветвленной цепью или Ar-замещенный (C1-C6)-алкил с прямой или разветвленной цепью; каждый Ar независимо от других является одной из предпочтительных арильных групп по данному изобретению, указанных выше; и каждый w означает 1 или 2.
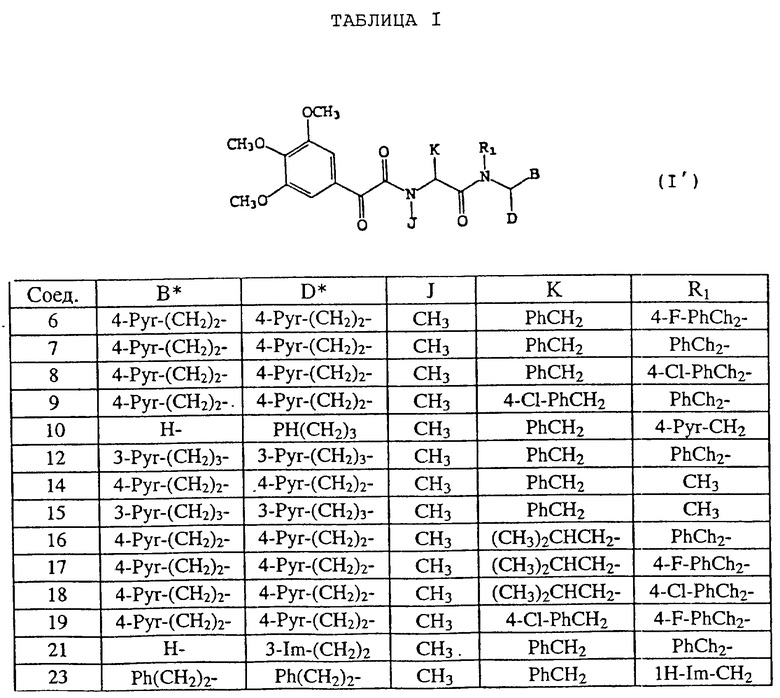
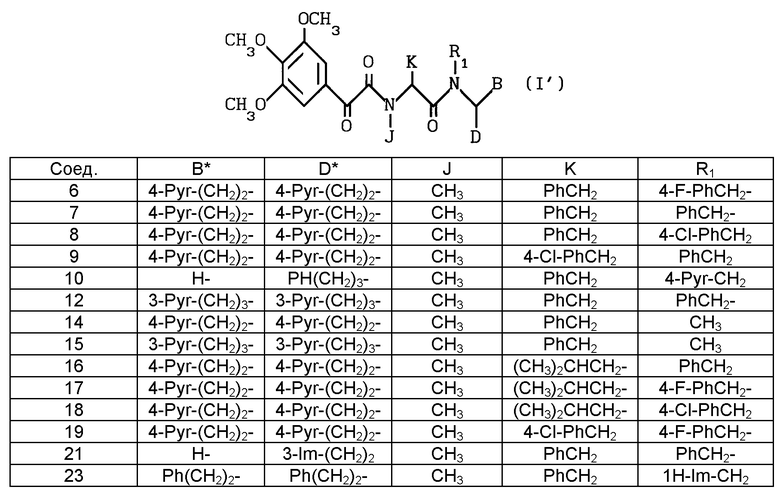
В таблице 1 приведены некоторые примеры предпочтительных соединений формулы (I), где X является 3,4,5-триметоксифенильной группой и m означает O (формула (I')), где В, D, J, K и R1 имеют указанные значения для каждого соединения,
где Pyr - пиридильный радикал, Ph - фенильная группа и Im - имидазолильная группа.
Другое воплощение данного изобретения относится к соединениям формулы (XXXI):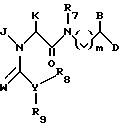 (XXXI)
(XXXI)
где m, В, D, J и K имеют значения, указанные выше для соединений формулы (I);
R7 имеет те же значения, что и R1, указанные выше для соединений формулы (I);
W является О или S;
Y является О или N, где,
когда Y означает О, тогда R8 является одиночной парой (термин "одиночная пара" относится к одиночной паре электронов, такой как одиночная пара электронов, присутствующая в двухвалентном кислороде) и R9 выбирают из группы, включающей Ar, (C1-C6)-алкил с прямой или разветвленной цепью и (C3-C6)-алкенил или алкинил с прямой или разветвленной цепью; и
когда Y означает N, тогда R8 и R9 независимо друг от друга выбирают из группы, включающей Ar, (C1-C6)-алкил с прямой или разветвленной цепью и (C3-C6)-алкенил или алкинил с прямой или разветвленной цепью; или R8 и R9, вместе взятые, образуют гетероциклическое 5-6-членное кольцо, выбираемое из группы, включающей пирролидин, имидазолидин, пиразолидин, пиперидин и пиперазин;
где Ar имеет значение, указанное выше для соединений формулы (I).
Предпочтительно, чтобы W в соединениях формулы (XXXI) был кислородом. Кроме того, предпочтение отдается соединениям формулы (XXXI), где по крайней мере один из В или D независимо от другого выражен формулой -(CH2)r-(Z)-(CH2)s-Ar, где:
r означает 1-4;
s означает 0-1; и
каждый Z независимо от других выбирают из группы, включающей CH2, О, S, SO, SO2 и NR, где R выбирают из группы, включающей водород, (C1-C4)-алкил с прямой или разветвленной цепью, (C3-C4)-алкенил или алкинил с прямой или разветвленной цепью и (C1-C4)-алкил с мостиковой связью, где мостик образован между атомом азота и Ar-группой.
Как указывалось выше, соединения по данному изобретению включают все оптические и рацемические изомеры.
Как указывалось выше, все соединения по данному изобретению включают свои фармацевтически приемлемые производные. "Фармацевтически приемлемое производное" означает любую фармацевтически приемлемую соль, сложный эфир или соль такого эфира соединения по данному изобретению или любое другое соединение, которое при введении нуждающемуся субъекту способно предоставить ему (прямо или косвенно) соединение по данному изобретению, его метаболит или остаток, отличающийся способностью сохранять, увеличивать или восстанавливать чувствительность клеток с множественной лекарственной устойчивостью к терапевтическим или профилактическим средствам или предотвращать развитие множественной лекарственной устойчивости.
Соединения по данному изобретению, выраженные формулами (I) и (I'), можно получить с помощью любого известного метода. Эти соединения предпочтительно синтезируют химическим путем из готовых исходных веществ, таких как альфа-аминокислоты. Предпочтение отдается также модулярным и конвергентным методам синтеза. В соответствии с конвергентным методом, например, крупные части конечного продукта соединяют на последних стадиях синтеза вместо последовательного добавления небольших частей к растущей молекулярной цепи.
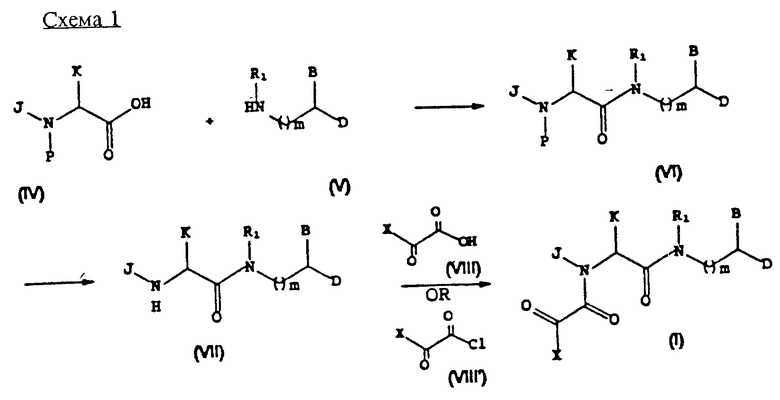
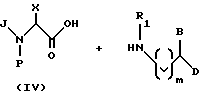
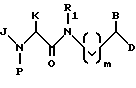
Схема 1 иллюстрирует типичный пример конвергентного процесса синтеза соединений формулы (I) (где m означает 0 или 1). Этот процесс включает связывание защищенной аминокислоты формулы (IV), где P является защитной группой, с амином формулы (V), в результате чего образуется аминоамид формулы (VI). Защищенные альфа-аминокислоты хорошо известны в этой области и многие из них коммерчески доступны. Например, обычные защитные группы и известные способы защиты аминокислот описываются в книге T.W. Greene, P.G.M. Wuts, Protective Groups in Organic Chemistry, 2nd Ed., John Wiley and Sons, New York (1991). Для защиты атома азота в соединениях формулы (IV) предпочтение отдается алкоксикарбонильным группам, причем более предпочтительными являются трет-бутоксикарбонил (Boc), бензилоксикарбонил (Cbz), аллилоксикарбонил (Alloc) и триметилсилилэтоксикарбонил (Teoc).
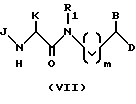
После связывания у соединений формулы (VI) удаляют защитные группы в приемлемых условиях удаления защитных групп (см. Greene, выше), после чего свободную аминогруппу формулы (VII) ацилируют, используя заранее полученный ацилхлорид формулы (VIII') или любую другую активированную форму соединения формулы (VIII). Галоген хлорсодержащей группы в соединении (VIII') может быть заменен другими отщепляемыми группами или активирующими группами, известными в этой области, такими как другие галогены, имидазолильные или пентафторфеноксигруппы.
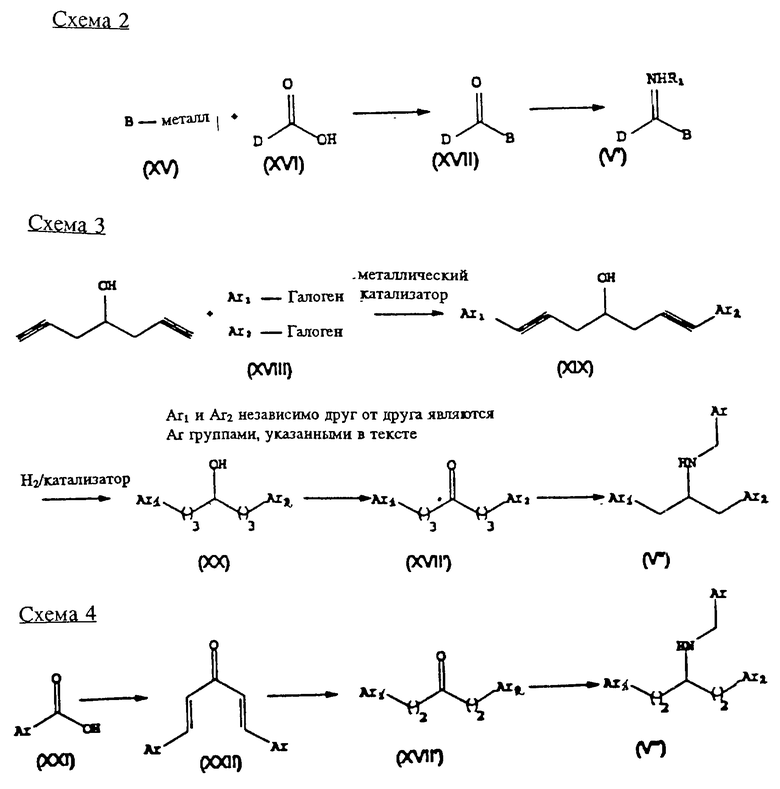
Амины формулы (V), где m означает 0 (формула (V')) можно также получить в соответствии с известными способами, например, так, как показано на схемах 2, 3 и 4. В результате взаимодействия металлорганического реагента формулы (XV) с карбоновой кислотой формулы (XVI) или эквивалентным веществом (например, амидом Вейнреба) получают кетоны формулы (XVII).
Такие кетоны можно легко превратить в амины формулы (V') с помощью любого процесса, хорошо известного в этой области, например, путем восстановительного аминирования (схема 2).
Альтернативно (схема 3) в результате взаимодействия, катализируемого металлическим катализатором, 1,6-гептадиин-4-ол можно связать с ароматическими галогенидами формулы (XVIII), в результате чего получают спирт формулы (XIX). Дальнейшая гидрогенизация дает спирт формулы (XX). Окисление в кетон формулы (XVII') и последующее аминирование позволяют получить необходимый амин формулы (V").
В соответствии с другим воплощением способов по данному изобретению (схема 4) восстанавливают кетодиен формулы (XXII), получаемый из альдегида формулы (XXI), с получением кетона формулы (XVII"). В результате выполнения стандартной редакции аминирования получают амин формулы (V"').
Таким образом, данным изобретением предусматривается также способ получения соединений формулы (I), включающий стадии:
(а) связывания аминокислоты формулы (IV) с амином формулы (V) с получением амида формулы (VI)
(b) удаление защитных групп из амида формулы (VI) с получением аминоамида формулы (VII); и
(с) ацилирование аминоамида формулы (VII) соединением формулы (VIII).
Специалистам в этой области должно быть понятно, что в соответствии со способами, проиллюстрированными на схемах синтеза 1-4, можно легко получить много разных соединений формулы (I). Те же способы можно использовать для синтеза многих других конечных продуктов путем варьирования исходных веществ.
Оптически активные соединения формулы (I) можно также получить, используя оптически активные исходные вещества, в результате чего устраняется необходимость разделения энантиомеров или отделения диастереомеров на последней стадии синтеза.
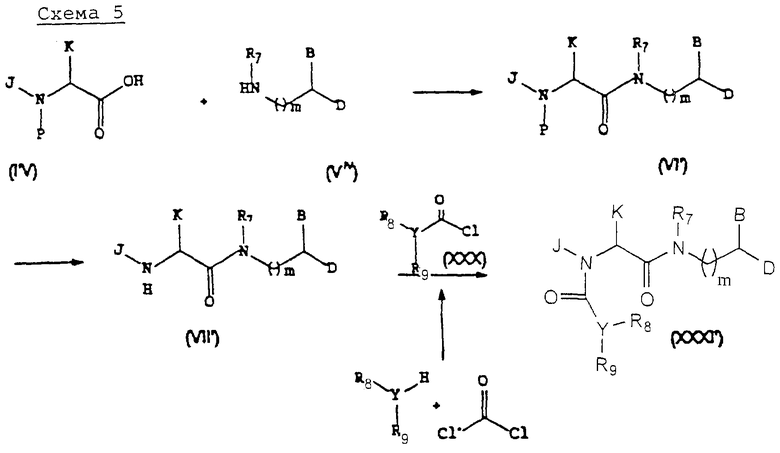
Схема 5 иллюстрирует типичный пример способа получения предпочтительного подкласса соединений формулы (XXXI), где W является кислородом. Как показано на схеме 5, мочевины и карбаматы формулы (XXXI') получают аналогично способам получения соединений формулы (I), изображенным на схеме 1. Так, защищенную аминокислоту формулы (IV) можно связать со вторичным амином формулы (Viv). Удаление защитных групп с последующим ацилированием хлорангидридом формулы (XXX) дает желаемое соединение формулы (XXXI').
Специалистам в этой области должно быть также понятно, что вышеуказанные схемы синтеза не включают полный перечень всех способов, с помощью которых можно синтезировать соединения или промежуточные продукты по данному изобретению.
Специалистам в этой области должны быть очевидны другие способы или модификации вышеуказанных общих схем.
Соединения по данному изобретению можно модифицировать путем присоединения соответствующих функциональных групп с целью усиления специфических биологических свойств. Такие модификации известны в этой области и включают те, которые увеличивают биопроницаемость в данную биологическую систему (например, кровь, лимфатическую систему, центральную нервную систему), увеличивают доступность лекарственного средства при пероральном введении, повышают растворимость, что делает возможным парентеральное введение, изменяют метаболизм и скорость экскреции.
Соединения по данному изобретению отличаются способностью увеличивать, восстанавливать или сохранять чувствительность клеток с множественной лекарственной устойчивостью в отношении цитотоксичных соединений, например, таких, которые применяют в химиотерапии. На основании этой способности соединения по данному изобретению преимущественно используют в виде химиосенсибилизирующих средств с целью увеличения эффективности химиотерапии у лиц, имеющих лекарственно-устойчивые злокачественные опухоли, метастазы или подобные болезни. Кроме того, соединения по данному изобретению способны сохранять чувствительность к терапевтическим или профилактическим средствам в нерезистентных клетках. Поэтому соединения по данному изобретению полезны для лечения или предупреждения множественной лекарственной устойчивости у нуждающихся субъектов. В частности, эти соединения полезны для лечения или предупреждения множественной лекарственной устойчивости, опосредованной P-гликопротеином и лекарственно-устойчивым белком.
Используемый в тексте данной заявки термин "нуждающийся субъект" относится к млекопитающим, включая человека. Термин "клетка" относится к клеткам млекопитающих, включая клетки человека.
Термины "сенсибилизирующее средство", "сенсибилизатор", "химиосенсибилизирующее средство", "химиосенсибилизатор" и "модификатор множественной лекарственной устойчивости" означают соединение, обладающее способностью увеличивать или восстанавливать чувствительность клетки с множественной лекарственной устойчивостью либо сохранять чувствительность нерезистентной клетки к одному или нескольким терапевтическим или профилактическим средствам. Термин "сенсибилизация множественной лекарственной устойчивости", "сенсибилизация" и "ресенсибилизация" относятся к действию такого соединения в отношении сохранения, увеличения или восстановления чувствительности к лекарственным средствам.
Соединения по настоящему изобретению можно использовать в форме фармацевтически-приемлемых солей, получаемых из неорганических или органических кислот и оснований. Такими кислыми солями являются следующие соли: ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфосульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, памоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат и ундеканоат. Основные соли включают соли аммония, соли щелочных металлов, такие как соли натрия и калия, соли щелочноземельных металлов, такие как соли кальция и магния, соли, образуемые с органическими основаниями, такие как соли дициклогексиламина, N-метил-D-глюкамин, и соли аминокислот, такие как аргинин, лизин и подобные. Кроме того, основные азотсодержащие группы можно кватернизировать с помощью таких веществ, как низшие алкилгалогениды, такие как метил, этил, пропил и бутилхлорид, бромиды и иодиды; диалкилсульфаты, такие как диметил, диэтил, дибутил и диамилсульфаты, галогениды с длинной цепью, такие как децил, лаурил, миристил и стеарилхлориды, бромиды и иодиды, аралкилкалогениды, такие как бензил и фенетилбромиды, и другие. В результате этого получают водо- или маслорастворимые или диспергируемые продукты.
Соединения по настоящему изобретению можно вводить перорально, парентерально, путем ингаляции, местного применения, ректально, назально, трансбуккально, вагинально или в виде имплантированных дозированных лекарственных форм, содержащих известные нетоксичные фармацевтически приемлемые носители, адъюванты и связующие. Термин "парентеральный" включает подкожные, внутривенные, внутримышечные, интраартикулярные, внутрисуставные, внутригрудинные, подоболочечные, внутрипеченочные, внутриопухолевые и внутричерепные инъекции или вливания.
Фармацевтические композиции по данному изобретению включают любые соединения по этому изобретению или их фармацевтически приемлемые соли вместе с фармацевтически приемлемым носителем, адъювантом или связующим. Фармацевтически приемлемые носители, адъюванты и связующие, которые можно использовать в фармацевтических композициях по данному изобретению, включают, но не ограничиваются ими, иониты, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, частичные глицеридные смеси насыщенных растительных жирных кислот, вода, соли или электролиты, такие как протаминсульфат, динатрийфосфат, дикалийфосфат, хлорид натрия, соли цинка, коллоидный кремнезем, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натрий карбоксиметилцеллюлоза, полиакрилаты, парафины, блоксополимеры полиэтилена и полиоксипропилена, полиэтиленгликоль и ланолин.
В соответствии с данным изобретением фармацевтические композиции могут быть в форме стерильного инъекционного препарата, например, стерильной инъецируемой водной или масляной суспензии. Эту суспензию можно получить с помощью известных методов, используя приемлемые диспергаторы, смачивающие и суспендирующие агенты. Стерильный инъекционный препарат может также быть стерильным инъекционным раствором или суспензией в нетоксичном пригодном для парентерального введения разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых связующих и растворителей можно назвать воду, раствор Рингера и изотонический раствор хлорида натрия. Помимо этого в качестве растворителя или суспендирующей среды обычно используют стерильные нелетучие масла. С этой целью можно применять любое мягкое нелетучее масло, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, пригодны для получения инъекционных препаратов, так же как и натуральные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в полиоксиэтилированном виде. Эти масляные растворы или суспензии могут также содержать спиртовой разбавитель или диспергатор с длинной цепью, такой как Ph. Helv. или аналогичный спирт.
Фармацевтические композиции по данному изобретению можно вводить перорально в любой пригодной для перорального введения дозированной форме, включающей, но не ограничивающейся ею, капсулы, таблетки, водные суспензии или растворы. В случае таблеток, предназначенных для перорального введения, обычно применяемыми носителями являются лактоза и кукурузный крахмал. Обычно также добавляют такие смазывающие вещества, как стеарат магния. Для перорального введения в виде капсул полезны такие разбавители, как лактоза и сухой кукурузный крахмал. Когда для перорального введения требуются водные суспензии, активный ингредиент соединяют с эмульгирующими и суспендирующими агентами. При желании могут быть добавлены определенные подсластители, ароматизаторы или красители.
Альтернативно фармацевтические композиции по данному изобретению можно использовать в виде суппозиториев для ректального введения. Их можно получить путем смешивания лекарственного средства с приемлемым нераздражающим наполнителем, который является твердым при комнатной температуре и жидким при ректальной температуре, поэтому он плавится в прямой кишке, высвобождая лекарственное средство. Такие вещества включают кокосовое масло, пчелиный воск и полиэтиленгликоли.
Фармацевтические композиции по данному изобретению можно также использовать для местного применения, особенно, когда целью лечения являются легкодоступные участки или органы, включая болезни глаз, кожи или нижнего отдела кишечника. Приемлемые составы для местного применения можно легко приготовить для каждого из этих участков или органов.
Местное применение для нижнего отдела кишечника может осуществляться с помощью составов ректальных суппозиториев (см. выше) или в виде приемлемого состава для клизмы. Кроме того, можно использовать пластыри местного чреcкожного действия.
Для местного применения фармацевтические композиции можно использовать в виде приемлемой мази, содержащей активный компонент, суспендированный или растворенный в одном или нескольких носителях. Носители для местного применения соединений по данному изобретению, включают, но не ограничиваются ими, минеральное масло, жидкий вазелин, белый вазелин, пропиленгликоль, полиоксиэтилен, полиоксипропилен, эмульгируемый парафин и воду. Альтернативно фармацевтические композиции можно получить в виде приемлемого лосьона или крема, содержащего активные компоненты, суспендированные или растворенные в одном или нескольких фармацевтически приемлемых носителях. Приемлемые носители включают, но не ограничиваются ими, минеральное масло, моностеарат сорбита, полисорбат 60, цетиловые сложные эфиры воска, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
Для офтальмологического применения фармацевтические композиции могут быть получены в виде очень тонких суспензий в изотоническом pH-отрегулированном стерильном физиологическом растворе или предпочтительно в виде растворов в изотоническом pH-отрегулированном стерильном физиологическом растворе с консервантом, таким как хлорид бензилалкония или без него. Альтернативно для офтальмологического применения фармацевтические композиции могут быть получены в виде мази на основе вазелина.
Фармацевтические композиции по данному изобретению можно также вводить в виде назального аэрозоля или путем ингаляции. Такие композиции получают в соответствии с методами, хорошо известными в фармации, и они могут представлять собой растворы в физиологическом растворе с использованием бензилового спирта или других приемлемых консервантов, промоторов абсорбции, усиливающих биологическую доступность, фторуглеродов и/или других солюбилизаторов или диспергаторов.
Количество активного ингредиента, которое можно соединить с носителями с целью получения однократной дозы, будет изменяться в зависимости от нуждающегося субъекта и определенного режима введения. Однако следует понять, что специфичная доза и схема лечения для любого нуждающегося субъекта будет зависеть от ряда факторов, включающих активность используемого соединения, возраст, вес тела, общее состояние здоровья, пол и питание нуждающегося субъекта, время введения и скорость выведения соединения, определенные сочетания лекарственных препаратов, назначение лечащего врача и серьезность заболевания, подлежащего лечению. Количество активного ингредиента может также зависеть от терапевтического или профилактического средства, если оно применяется, вместе с которым вводится данный ингредиент. Термин "фармацевтически эффективное количество" относится к количеству, оказывающему эффективное действие по предотвращению множественной лекарственной устойчивости или по сохранению, увеличению или восстановлению чувствительности к лекарственному средству у клеток с множественной лекарственной устойчивостью.
Полезные дозы составляют от около 0,01 до около 100 мг/кг массы тела в день, предпочтительно от около 0,5 до около 50 мг/кг массы тела в день соединения активного ингредиента. Типичный препарат должен содержать от около 5 до 95% активного соединения (в весовом отношении). Такие препараты, предпочтительно, содержат от около 20 до около 80% активного соединения.
Если соединения по данному изобретению вводят в процессе комбинированной терапии вместе с другими средствами, их можно вводить нуждающемуся субъекту последовательно или одновременно. Альтернативно фармацевтические или профилактические композиции по данному изобретению могут содержать соединение по этому изобретению и другое терапевтическое или профилактическое средство.
Например, эти соединения можно вводить отдельно или в сочетании с одним или несколькими терапевтическими средствами, такими как химиотерапевтические средства (например, актиномицин D, доксорубицин, винкристин, винбластин, этопозид, амсакрин, митоксантрон, тенипазид, таксол и колхицин) и/или химиосенсибилизирующее средство (например, циклоспорин A и его аналоги, фенотиазины и тиоксантеры), с целью увеличения чувствительности клеток с множественной лекарственной устойчивостью у нуждающегося субъекта к лекарственному средству или средствам.
Более полному пониманию данного изобретения способствуют приводимые ниже примеры. Эти примеры служат только для иллюстрации и никоим образом не ограничивают объем изобретения.
Примеры
Общие методы
Спектры протонного ядерного магнитного резонанса (1H ЯМР) регистрировали при 500 МГц на спектрометре Bruker AMX 500. Химические сдвиги выражены в частях на миллион (δ) относительно Me4Si (δ 0,0). Аналитическую жидкостную хроматографию высокого разрешения выполняли с помощью жидкостного хроматографа Waters 600 E или Hewlett Packard 1050.
Пример 1
1,5-Ди(пиридин-4-ил)-пент-1,4-диен-3-он (соединение 1)
К раствору 1,3-ацентондикарбоновой кислоты (21,0 г, 0,144 ммоль) в абсолютном этаноле (200 мл) по каплям добавляют 4- пиридинкарбоксальдегид (30,8 г, 0,288 ммоль). В процессе добавления происходит выделение газа. После перемешивания при комнатной температуре в течение 2 ч реакционную смесь обрабатывают концентрированной хлористоводородной кислотой (100 мл) и нагревают до 80oC; на протяжении этого времени медленно образуется желтый осадок. Перемешивая суспензию, добавляют еще 500 мл этанола. После отстаивания суспензии в течение 1 ч при температуре 80oC осадок собирают фильтрованием, промывают этанолом и сушат в вакууме с получением необходимого продукта в виде желтого твердого вещества. Полученный дигидрохлорид перекристаллизовывают из метиленхлорида, получая чистое соединение 1.
Пример 2
1,5-Ди(пиридин-4-ил)-пентан-3-он (соединение 2)
К суспензии соединения 1 (21,3 г, 67,4 ммоль) в 1,4- диоксане (40 мл) добавляют триэтиламин (48,1 мл, 0,346 моль), муравьиную кислоту (6,54 мл, 0,145 моль) и 10% палладия на углероде (0,7 г), и полученную смесь нагревают до температуры кипения с обратным холодильником. После перемешивания при температуре кипения с обратным холодильником в течение 1 ч реакционную смесь охлаждают до комнатной температуры, фильтруют и концентрируют в вакууме. Полученный остаток хроматографируют на силикагеле (элюирование смесью 5% метанола и метиленхлорида) с получением требуемого продукта.
Пример 3
(4-Фторбензил)-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил) этил)-пропил)амин (соединение 3)
В колбу, оснащенную ловушкой Дина-Старка, вводят соединение 2 (12,46 г, 51,91 ммоль), 4-фторбензиламин (5,93 мл, 51,91 ммоль) и бензол (50 мл), и полученную смесь нагревают до температуры кипения с обратным холодильником. После отделения 930 мкл воды реакционную смесь охлаждают и концентрируют. Остаток растворяют в этаноле (50 мл) и добавляют к суспензии борогидрида натрия (2,96 г, 77,8 ммоль) в этаноле (50 мл), смесь нагревают до 80oC и перемешивают в течение 1 ч. Реакционную смесь охлаждают и концентрируют. Остаток растворяют в воде и подкисляют до pH 3,0 путем добавления 6 н раствора хлористоводородной кислоты. Водную фазу промывают этилацетатом (2 раза). Водную фазу подщелачивают гидроксидом натрия до pH 10 и экстрагируют продукт метиленхлоридом (2 раза). Органические фракции собирают, промывают насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Хроматография остатка на силикагеле (элюирование смесью 5% метанола и метиленхлорида) дает соединение 3.
Пример 4
(S)-N-(4-Фторбензил)-2-(N-метил-N-трет-бутилкарбамоил) -амино-3-фенил-N-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил)этил) -пропил)пропионамид (соединение 4)
К раствору соединения 3 (550 мг, 1,66 ммоль) и (L)-BOC-N-метил-фенилаланина (700 мг, 2,5 ммоль) в метиленхлориде (4,0 мл), содержащему диизопропилэтиламин (300 мкл, 1,72 ммоль), добавляют гидрохлорид (3-диметиламинопропил)-3-этил-карбодиимида (480 мг, 2,5 ммоль) и перемешивают реакционную смесь в течение 48 ч. Реакционную смесь разбавляют этилацетатом и водой. Слои разделяют и водную фазу повторно экстрагируют этилацетатом. Органические фракции собирают, промывают насыщенным раствором бикарбоната натрия, водой и насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Хроматография остатка на силикагеле (элюирование смесью 5% метанола и метиленхлорида) дает соединение 4.
Пример 5
(S)-N-(4-Фторбензил)-2-метиламино-3-фенил-N-(3-(пиридин-4-ил) -1-(2-(пиридин-4-ил)этил)пропил)пропионамид (соединение 5)
Соединение 4 растворяют в метиленхлориде (10 мл) и обрабатывают трифторуксусной кислотой (4,0 мл). После перемешивания при комнатной температуре в течение 1,5 ч реакционную смесь концентрируют в вакууме. Остаток нейтрализуют насыщенным раствором карбоната калия и экстрагируют этилацетатом (2 раза). Экстракты соединяют, промывают водой, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме с получением соединения 5.
Пример 6
(S)-N-(4-Фторбензил)-2-(метил-(2-оксо-2-(3,4,5- триметоксифенил)-ацетил)амино)-3-фенил-N-(3-(пиридин-4-ил)-1- (2-пиридин-4-ил)-этил)пропил)пропионамид (соединение 6)
К раствору соединения 5 (500 мг, 0,98 ммоль) и 3,4,5- триметоксибензоилмуравьиной кислоты (294 мг, 1,22 ммоль) в метиленхлориде (4,0 мл), содержащему N,N-диметилформамид (0,4 мл), добавляют гидрохлорид (3-диметиламинопропил)-3-этилкарбодиимида (235 мг, 1,22 ммоль), и перемешивают реакционную смесь в течение 24 ч. Реакционную смесь разбавляют этилацетатом и водой. Слои разделяют и водную фазу повторно экстрагируют этилацетатом. Органические фракции соединяют, промывают насыщенным раствором бикарбоната натрия, водой и насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Остаток хроматографируют на силикагеле (элюирование смесью 5% метанола и метиленхлорида) с получением требуемого продукта.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,48-8,44 (м), 8,38 (двойной дублет), 7,36-7,33 (м), 7,28-7,18 (м), 7,13-7,02 (м), 6,97-6,87 (м), 6,58 (д), 6,00 (двойной триплет), 5,81 (т), 4,97 (широкий синглет), 4,81 (д), 4,23-4,16 (м), 3,93 (с), 3,90 (с), 3,85 (с), 3,76 (с), 3,59 (двойной дублет), 3,28 (дд), 3,20 (с), 3,15 (с), 3,04-2,96 (м), 3,02 (с), 3,01 (с), 2,94 (двойной дублет), 2,63 (двойной триплет), 2,53-2,37 (м), 1,92-1,78 (м), 1,72-1,62 (м), 1,52-1,42 (м).
Пример 7
(S)-N-Бензил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил) - ацетил)амино)-3-фенил-N-(3-пиридин-4-ил)-1-(2-пиридин-4-ил-этил) пропил)-пропионамид (соединение 7)
Соединение 7 получают в соответствии с процедурами по примерам 3-6 путем замены 4-фторбензиламина бензиламином.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,48 (двойной дублет), 8,53 (двойной дублет), 8,43 (двойной дублет), 8,35 (двойной дублет), 7,38 (д), 7,30-7,18 (м), 7,17-7,02 (м), 6,93 (с), 6,89 (д), 6,54 (д), 6,03 (двойной дублет), 5,86 (т), 5,08 (широкий дублет), 4,88 (д), 4,32-4,18 (м), 3,95 (с), 3,89 (с), 3,86 (с), 3,73 (с), 3,63 (двойной дублет), 3,23-3,19 (м), 3,09 (двойной дублет), 3,05 (с), 3,03 (с), 2,97 (двойной дублет), 2,63 (двойной триплет), 2,57-2,37 (м), 2,24 (двойной триплет), 2,06 (м), 1,95-1,76 (м), 1,74-1,63 (м), 1,54-1,44 (м).
Пример 8
(S)-N-(4-Хлорбензил)-2-(метил-(2-оксо-2- (3,4,5-триметоксифенил)-ацетил)амино)-3-фенил-N-(3-(пиридин- 4-ил)-1-(2-(пиридин-4-ил)-этил) пропил)пропионамид (соединение 8)
Соединение 8 получают в соответствии с процедурами по примерам 3-6 путем замены 4-фторбензиламина 4-хлорбензиламином.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,49 (двойной триплет), 8,45 (двойной дублет), 8,40 (двойной дублет), 7,69 (д), 7,31-7,14 (м), 7,12 (с), 7,08-7,03 (м), 6,98 (с), 6,94-6,91 (м), 6,85 (д), 6,02 (двойной дублет), 5,79 (т), 4,99 (широкий дублет), 4,83 (д), 4,22-4,16 (м), 3,96 (м), 3,91 (с), 3,88 (с), 3,87 (с), 3,81 (с), 3,78 (с), 3,61 (двойной дублет), 3,33 (двойной дублет), 3,21 (с), 3,17 (с), 3,04 (с), 3,03 (с), 3,03-3,00 (м), 2,95 (двойной дублет), 2,65 (двойной триплет), 2,56-2,40 (м), 2,28 (двойной триплет), 1,90-1,80 (м), 1,75-1,66 (м), 1,52-1,43 (м).
Пример 9 (S)-N-Бензил-3-(4-хлорфенил)-2-(метил-(2-оксо-2- (3,4,5-триметоксифенил)ацетил)амино)-N-(3-(пиридин-4-ил)-1- (2-(пиридин-4-ил)-этил)пропил)пропионамид (соединение 9)
Соединение 9 получают в соответствии с процедурами по примерам 3-6 путем замены 4-фторбензиламина бензиламином и (L)- BOC-N-метилфенилаланина (L)-BOC-N-метил-4-хлорфенилаланином.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,48 (двойной дублет), 8,45 (двойной триплет), 8,38 (двойной дублет), 7,32-6,87 (м), 6,58 (д), 5,94 (двойной дублет), 5,78 (т), 5,05 (широкий дублет), 4,83 (д), 4,26 (двойной дублет), 4,15 (м), 3,97 (с), 3,89 (с), 3,86 (с), 3,75 (с), 3,57 (двойной дублет), 3,20 (с), 3,15 (с), 3,15-3,09 (м), 3,05-2,96 (м), 3,01 (с), 3,00 (с), 2,91 (двойной дублет), 2,65-2,38 (м), 2,26 (двойной триплет), 1,94-1,47 (м).
Пример 10
(S)-2-(Метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил) -амино)-3-фенил-N-(4-фенилбутил)-N-[(пиридин-4-ил)метил] пропионамид (соединение 10)
Соединение 10 получают в соответствии с процедурами по примерам 3-6 путем замены 4-фторбензиламина 4-фенилбутиламином и соединения 2 4-пиридинкарбоксальдегидом.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,46 (двойной дублет), 8,42 (двойной дублет), 7,30-7,23 (м), 7,18-7,11 (м), 7,11 (с), 7,10 (с), 6,90 (д), 6,77 (д), 5,88 (т), 5,60 (двойной дублет), 4,85 (д), 4,50 (д), 4,28 (д), 3,93 (с), 3,83 (с), 3,81 (с), 3,80 (с), 3,65-3,50 (м), 3,37 (м), 3,20-3,15 (м), 3,08-3,06 (м), 3,06 (с), 3,05 (с), 2,92 (двойной дублет), 2,60 (м), 2,54 (м), 1,60-1,48 (м), 1,38-1,28 (м).
Пример 11
1,7-Ди(пиридин-4-ил)-гептан-4-он (соединение 11)
К раствору 1,7-ди-(пиридин-4-ил)-гептан-4-ола (4,1 г, 15,2 ммоль) в метиленхлориде (50 мл) при температуре 0oC добавляют бромид калия (180 мг) и свободный 2,2,6,6-тетраметил-1- пиперидинилоксирадикал (71 мг). К полученной смеси по каплям добавляют раствор бикарбоната натрия (510 мг) в гипохлорите натрия (65 мл). После окончания добавления реакционную смесь нагревают до комнатной температуры и перемешивают в течение 30 мин. Смесь разбавляют этилацетатом и водой. Слои разделяют и водный слой повторно экстрагируют этилацетатом. Органические фракции соединяют, промывают водой и насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Хроматография остатка на силикагеле (элюирование смесью 5% метанола и метиленхлорида) дает соединение 11.
Пример 12
(S)-N-Бензил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)-ацетил) амино)-3-фенил-N-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил)-пропил) бутил)пропионамид (соединение 12)
Соединение 12 получают в соответствии с процедурами по примерам 3-6 путем замены 4-фторбензиламина бензиламином и соединения 2 соединением 11.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,43-8,38 (м), 8,30 (м), 8,16 (м), 7,53-7,45 (м), 7,34 (м), 7,32 (м), 7,26-7,22 (м), 7,19-7,07 (м), 7,00-6,83 (м), 5,89 (двойной дублет), 5,72 (т), 4,90 (д), 4,72 (д), 4,10 (д), 4,00 (д), 3,93 (с), 3,91 (с), 3,85 (с), 3,74 (с), 3,52 (двойной дублет), 3,16-3,10 (м), 3,04 (с), 2,99 (двойной дублет), 2,93 (с), 2,84 (двойной дублет), 2,67-2,38 (м), 2,30 (м), 2,22 (м), 1,63-1,12 (м), 0,94 (м).
Пример 13
Метил-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил)-этил) пропил)-амин (соединение 13)
К суспензии гидрохлорида метиламина (1,7 г, 25,4 ммоль) и ацетата натрия (2,5 г, 30,48 ммоль) в метаноле (20 мл) добавляют раствор соединения 2 (1,21 г, 5,08 ммоль) в метаноле (5 мл). Полученную смесь обрабатывают раствором цианборогидрида натрия (370 мг, 6,09 ммоль), в метаноле (5 мл) и нагревают до 80oC. После выстаивания в течение 1 ч при 80oC реакционную смесь охлаждают до комнатной температуры и концентрируют в вакууме. Остаток растворяют в метиленхлориде и 2 н растворе гидроксида натрия. Слои разделяют, органическую фазу промывают насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме с получением соединения 13.
Пример 14
(S)-N-Метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил) -ацетил)амино)-3-фенил-N-(3-(пиридин-4-ил)-1-(2- (пиридин-4-ил)-этил)пропил)пропионамид (соединение 14)
Соединение 14 получают в соответствии с процедурами по примерам 4-6 путем замены соединения 3 соединением 13.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,50-8,46 (м), 8,37 (д), 7,32-7,26 (м), 7,21-7,16 (м), 7,10-7,06 (м), 6,97 (двойной дублет), 6,93 (д), 5,93 (д), 5,54 (т), 4,72 (широкий синглет), 4,17 (м), 3,94 (с), 3,92 (с), 3,84 (с), 3,82 (с), 3,51 (двойной дублет), 3,38 (двойной дублет), 3,29 (с), 3,11 (двойной дублет), 3,06 (с), 3,00 (с), 2,97 (двойной дублет), 2,86 (с), 2,82 (с), 2,49 (м), 2,37-2,23 (м), 2,17-1,98 (м), 1,85-1,55 (м).
Пример 15
(S)-N-Метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил) -ацетил)амино)-3-фенил-N-(3-(пиридин-4-ил)-1-(2- (пиридин-4-ил)-пропил)бутил)пропионамид (соединение 15)
Соединение 15 получают в соответствии с процедурами по примерам 13 и 14 путем замены соединения 2 соединением 11.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,44-8,38 (м), 8,37-8,30 (м), 7,50-7,43 (м), 7,38-7,08 (м), 7,04 (с), 7,03-6,98 (м), 6,90-6,86 (м), 5,83 (двойной дублет), 5,74 (т), 4,75 (т), 4,65 (м), 3,94-3,93 (м), 3,92 (с), 3,90 (с), 3,84 (с), 3,83 (с), 3,44 (двойной дублет), 3,32 (двойной дублет), 3,20 (с), 3,01 (двойной дублет), 2,95 (с), 2,91 (с), 2,87 (двойной дублет), 2,59 (с), 2,58-2,37 (м), 1,68-1,00 (м).
Пример 16
Бензил-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил) этил)пропил)-амид (S)-4-метил-2-(метил-(2-оксо-2-(3,4,5- триметоксифенил)-ацетил)амино) пентановой кислоты (соединение 16)
Соединение 16 получают в соответствии с процедурами по примерам 3-6 путем замены 4-фторбензиламина бензиламином и (L)-BOC- N-метилфенилаланина (S)-BOC-H-метиллейцином.
Пример 17
4-Фторбензил-(3-пиридин-4-ил-1-(2-пиридин-4-ил-этил)пропил) амид (S)-4-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил) ацетил)амино)пентановой кислоты (соединение 17)
Соединение 17 получают в соответствии с процедурами по примерам 4-6 путем замены (L)-BOC-N-метилфенилаламина (S)-Boc-N- метиллейцином.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,48 (м), 8,45 (д), 7,32 (м), 7,18 (с), 7,12 (с), 7,09-6,92 (м), 6,84 (д), 5,72 (двойной дублет), 5,48 (двойной дублет), 4,99 (широкий дублет), 4,68 (д), 4,42 (д), 4,36 (д), 4,29 (м), 3,94 (с), 3,91 (с), 3,87 (с), 3,83 (с), 2,96 (с), 2,92 (с), 2,69 (двойной триплет), 2,62-2,55 (м), 2,52- 2,44 (м), 2,12-1,73 (м), 1,63-1,57 (м), 1,48-1,39 (м), 1,23 (м), 1,03 (т), 0,90 (д), 0,69 (д).
Пример 18
4-Хлорбензил-(3-пиридин-4-ил-1-(2-пиридин-4-ил- этил)-пропил)амид (S)-4-метил-2-(метил-(2-оксо-2-(3,4,5- триметоксифенил) ацетил) амино)пентановой кислоты (соединение 18)
Соединение 18 получают в соответствии с процедурами по примерам 3-6 путем замены 4-фторбензиламина 4-хлорбензиламином и (L)-BOC-N-метилфенилаланина (S)-BOC-N-метиллейцином.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,50 (м), 8,47 (д), 7,38 (д), 7,30-7,26 (м), 7,19 (с), 7,13 (с), 7,10 (д), 7,04 (д), 6,98 (д), 6,84 (д), 5,73 (двойной дублет), 5,47 (двойной дублет), 5,03 (широкий дублет), 4,69 (д), 4,42 (д), 4,36 (д), 4,31 (м), 3,95 (с), 3,93 (с), 3,88 (с), 3,84 (с), 2,97 (с), 2,94 (с), 2,70 (двойной триплет), 2,63-2,43 (м), 2,12-1,56 (м), 1,48-1,40 (м), 1,25 (м), 1,04 (т), 0,91 (д), 0,70 (д).
Пример 19
(S)-N-(4-фторбензил)-3-(4-хлорфенил)-2-(метил-(2-оксо-2- (3,4,5-триметоксифенил)ацетил)амино)-N-(3-пиридин-4- ил-1-(2-пиридин-4-ил-этил)пропил)пропионамид (соединение 19)
Соединение 19 получают в соответствии с процедурами по примерам 4-6 путем замены (L)-BOC-N-метилфенилаланина (L)-BOC-N-метил-4- хлорфенилаланином.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,49-8,41 (м), 7,34 (с), 7,28-7,20 (м), 7,10-6,90 (м), 6,64 (д), 5,92 (двойной дублет), 5,74 (т), 4,95 (широкий дублет), 4,74 (д), 4,24-4,13 (м), 3,94 (с), 3,90 (с), 3,86 (с), 3,77 (с), 3,54 (двойной дублет), 3,23-3,17 (м), 2,99 (с), 2,98 (с), 2,90 (д), 2,63 (двойной триплет), 2,59-2,37 (м), 2,28 (двойной триплет), 1,94-1,70 (м), 1,57-1,47 (м).
Пример 20
(4-Хлорбензил)-(3-имидазол-1-ил-пропил)амин (соединение 20)
К раствору 1-(3-аминопропил)имидазола (2,1 г, 16,8 ммоль), диизопропилэтиламина (3,5 мл, 20,0 ммоль) и 4-N,N-диметиламинопиридина (200 мг, 1,7 ммоль) в метиленхлориде (15 мл) при температуре 0oC по каплям добавляют 4-хлорбензоилхлорид (2,1 мл, 16,8 ммоль). Затем реакционную смесь оставляют для нагревания до комнатной температуры. Через 5 ч реакционную смесь разбавляют метиленхлоридом, промывают 1 н раствором гидроксида натрия, насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме с получением белого твердого вещества. Это вещество промывают диэтиловым эфиром с получением N-(3-имидазол-1-ил-пропил)-4-хлорбензамида. К суспензии вышеуказанного амида (1,58 г, 6,0 ммоль) в тетрагидрофуране (30 мл) медленно добавляют алюмогидрид лития (456 мг, 12,0 ммоль), после чего реакция становится экзотермической. Смесь нагревают до температуры 80oC, перемешивают в течение 1 ч, охлаждают до 0oC и гасят путем добавления воды (0,5 мл), 15% гидроксида натрия (0,5 мл) и еще 1,5 мл воды. Реакционную смесь разбавляют этилацетатом, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме с получением соединения 20.
Пример 21
(S)-N-(4-хлорбензил)-N-(3-имидазол-1-ил-пропил)-2-(метил- (2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино) -3-фенил-пропионамид (соединение 21)
Соединение 21 получают в соответствии с процедурами по примерам 4-6 путем замены соединения 3 соединением 20.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 8,48 (м), 7,44 (широкий синглет), 7,37 (широкий синглет), 7,30-7,16 (м), 7,10-7,02 (м), 6,95 (д), 6,83 (м), 5,78 (т), 5,72 (т), 4,77 (д), 4,57 (д), 4,26 (двойной дублет), 3,94 (с), 3,93 (с), 3,88-3,77 (м), 3,80 (с), 3,48 (двойной триплет), 3,42-3,33 (м), 3,19-3,14 (м), 3,13 (с), 3,12 (с), 3,13-2,97 (м), 2,89 (т), 2,80 (м), 2,74 (т), 2,65 (м), 2,08-1,98 (м), 1,90 (м), 1,80-1,60 (м).
Пример 22
N-(1H-Имидазол-2-ил-метил)-N-(1-фенетил-3-фенилпропил)-амин (соединение 22)
К раствору 1,5-дифенилпентан-3-она (5,26 г, 22,1 ммоль), ацетата аммония (8,52 г, 110,5 ммоль) и ацетата натрия (9,06 г, 110,5 ммоль) в метаноле (80 мл) добавляют раствор цианборогидрида натрия (1,67 г, 26,52 ммоль) в метаноле (20 мл), и реакционную смесь нагревают до температуры кипения с обратным холодильником. После перемешивания при температуре кипения с обратным холодильником в течение 30 мин реакционную смесь охлаждают и концентрируют до сухого состояния. Остаток распределяют между метиленхлоридом и 2 н раствором гидроксида натрия. Органическую фазу отделяют, промывают насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Хроматография остатка на силикагеле (элюирование смесью 2-5% метанола и метиленхлорида) дает N-(1-фенетил-3-фенилпропил)амин. К раствору вышеуказанного амина (2,1 г, 8,82 ммоль) в этаноле (50 мл) добавляют 2-имидизолкарбоксальдегид (813 мг, 8,47 ммоль), и реакционную смесь нагревают до 50oC. После перемешивания в течение 2 ч полученный однородный раствор обрабатывают борогидридом натрия (400 мг, 10,58 ммоль) и перемешивают в течение ночи. Реакционную смесь концентрируют до сухого состояния, и остаток распределяют между метиленхлоридом и 2 н раствором гидроксида натрия. Органическую фазу отделяют, промывают насыщенным раствором соли, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Хроматография остатка на силикагеле (элюирование смесью 5% метанола и метиленхлорида) дает соединение 22.
Пример 23
(S)-N-(1H-Имидазол-2-ил-метил)-2-(метил-(2-оксо-2- (3,4,5-триметоксифенил)ацетил)амино)-N-(1-фенетил-3- фенилпропил)-3-фенилпропионамид (соединение 23)
Соединение 23 получают в соответствии с процедурами по примерам 4-6 путем замены соединения 3 соединением 22.
Спектр 1H ЯМР в виде смеси ротомеров (500 МГц, CDCl3) δ 7,40-7,00 (м), 6,95-6,87 (м), 5,95 (т), 5,69 (т), 4,66 (д), 4,46 (д), 4,12 (м), 3,94 (с), 3,92 (с), 3,82 (м), 3,81 (с), 3,80 (с), 3,47 (с), 3,43 (двойной дублет), 3,34 (двойной дублет), 3,22 (с), 3,15 (с), 3,03 (двойной дублет), 3,00 (с), 2,60 (двойной триплет), 2,45-2,22 (м), 1,80-1,78 (м).
Пример 24
Исследование сенсибилизации клеток с множественной лекарственной устойчивостью
Для определения способности соединений по данному изобретению увеличивать антипролиферативную активность лекарственного средства можно использовать линии клеток, которые, как известно, устойчивы к определенному лекарственному средству. Эти линии клеток включают, но не ограничиваются ими, L1210, P388D, CHO и MCF7. Альтернативно устойчивые линии клеток можно вырастить в лабораторных условиях. Линию клеток подвергают воздействию лекарственного средства, в отношении которого она обладает устойчивостью, или испытуемого соединения. После этого измеряют жизнеспособность клеток и сравнивают полученный результат с жизнеспособностью клеток, подвергнутых воздействию этого лекарственного средства в присутствии испытуемого соединения.
Анализы выполняли с использованием лейкозных клеток мышей L1210, трансформированных с помощью ретровируса pHaMDR1/A, содержащего кДНК с множественной лекарственной устойчивостью MDR1, описанных Пастаном и др., Proc. Natl. Acad. Sci. , vol. 85, 4486-4490 (1988). Резистентная линия, маркированная L1210VMDRC. 06, была предоставлена д-ром М.М. Готтесманом из Национального института рака. Эти лекарственно-устойчивые трансфектанты были отобраны в результате культивирования клеток в 0,06 мг/мл колхицина.
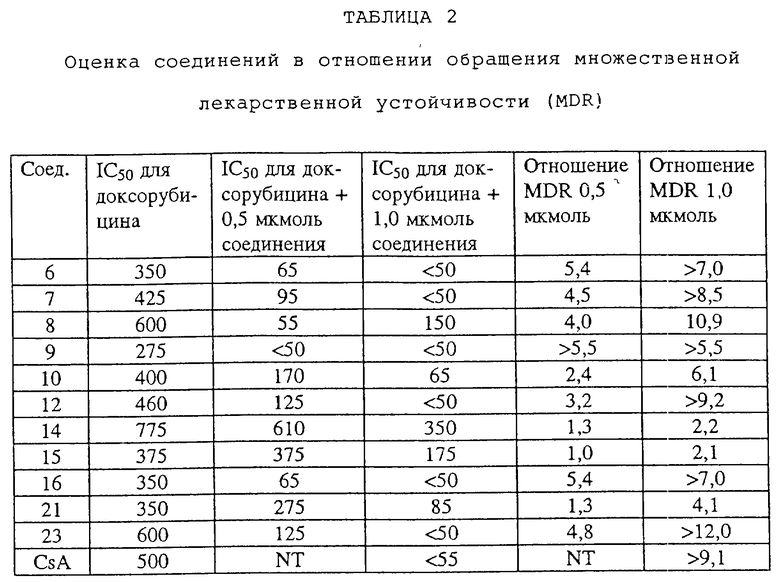
Анализы множественной лекарственной устойчивости выполняли путем культивирования клеток (2·103, 1·104 или 5·104 клеток/лунку) на 96-луночных титрационных микропланшетах и обработки их доксорубицином с разными концентрациями (50 нмоль - 10 мкмоль) в присутствии или отсутствии модификаторов множественной клеточной устойчивости (ингибиторов множественной клеточной устойчивости) по данному изобретению (1, 2,5 или 10 мкмоль), как это описывается в статье Форда и др. Cancer Res., vol. 50, 1748-1756 (1990). После культивирования в течение 3 дней производили количественное определение жизнеспособности клеток, используя красители MTT (Mossman) и XTT для оценки митохондриальной функции. Все анализы повторяли 4 или 8 раз; см. также Mossman T., J. Immunol. Methods, vol. 65, 55-63 (1983).
Результаты определяли путем сравнения IC50 для доксорубицина с IC50 для доксорубицина и ингибитора множественной лекарственной устойчивости. Высчитывали величину отношения множественной лекарственной устойчивости (IC50 доксорубицин/IC50 доксорубицин + ингибитор) и целые числа использовали для сравнения эффективности соединений.
Во всех анализах соединения по данному изобретению тестировали в отношении характерной антипролиферативной или цитотоксической активности. Результаты представлены в таблице 2. Как видно из таблицы 2, соединения обычно вызывали цитотоксичность < 10% при концентрациях 10 мкмоль или выше. В таблице 2 "NT" означает, что данное соединение не испытывали при соответствующей концентрации.
Пример 25
Ингибирование множественной лекарственной устойчивости, опосредованной лекарственно-устойчивым белком
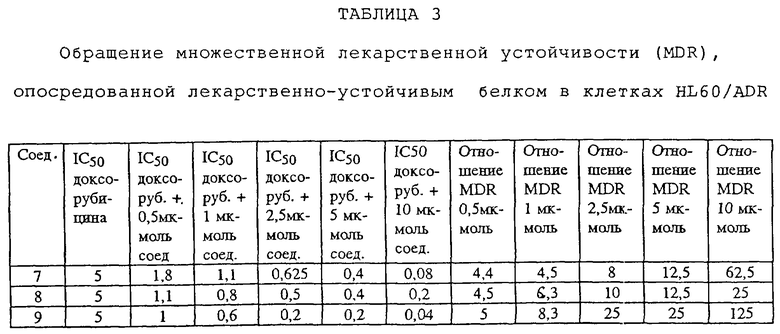
Чтобы показать, что соединения по данному изобретению эффективно воздействуют на множественную лекарственную устойчивость, опосредованную лекарственно-устойчивым белком, помимо множественной лекарственной устойчивости, опосредованной P-гликопротеином, анализировали ингибирование на линии клеток, не экспрессирующих P-гликопротеин.
Клетки HL60/ADR культивировали на 96-луночных титрационных микропланшетах (4·104 клеток/лунку). Затем клетки подвергали воздействию доксорубицина с разными концентрациями (от 50 ммоль до 10 мкмоль) в присутствии или отсутствии разных соединений по данному изобретению при разных концентрациях (0,5 - 10 мкмоль). После культивирования клеток в течение 3 дней производили количественное определение их жизнеспособности, используя метод на основе красителя XTT для оценки митохондриальной функции. Результаты выражали в виде отношения IC50 для доксорубицина к IC50 для доксорубицина и ингибитора множественной лекарственной устойчивости. Значения IC50 выражены в нмолях. Во всех анализах характерная антипролиферативная или цитотоксическая активность ингибиторов множественной лекарственной устойчивости определялась также для клеток HL60/ADR. Результаты этого анализа представлены в таблице 3.
Хотя здесь описано лишь несколько осуществлений данного изобретения, очевидно, что основные положения изобретения могут быть изменены, в результате чего будут получены другие варианты, при осуществлении которых используются продукты, способы и методы данного изобретения. Поэтому следует понимать, что объем данного изобретения должен определяться прилагаемой формулой изобретения, а не типичными вариантами осуществления, приведенными в качестве примеров.
Описываются новые соединения формулы I, где В и D независимо друг от друга обозначают водород или Аr-замещенный (C1-С6)-алкил с прямой или разветвленной цепью; R1 - (C1-С6)-алкил с прямой или разветвленной цепью или Аr-замещенный (C1-С6)-алкил с прямой или разветвленной цепью; J обозначает (C1-С6)-алкил с прямой или разветвленной цепью; К обозначает (C1-С6)-алкил с прямой или разветвленной цепью, фенилзамещенный (C1-С6)-алкил с прямой или разветвленной цепью, где фенил может быть замещен галогеном; Х обозначает фенил, замещенный O-(C1-С6)-алкилом; Аr обозначает фенил, или Аr является гетероциклической ароматической группой, выбираемой из группы, включающей 2-пиридил, 3-пиридил, 4-пиридил и имидазолил, причем Аr может быть замещен галогеном, которые могут быть использованы для подавления множественной лекарственной устойчивости. Описывается также способ их получения, фармацевтическая композиция и способ подавления множественной лекарственной устойчивости. 6 c. и 5 з.п. ф-лы, 3 табл.
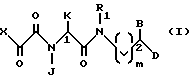
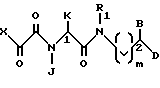
где В и D независимо друг от друга обозначают водород или Ar - замещенный (C1 - C6) - алкил с прямой или разветвленной цепью;
R1 - (C1 - C6) алкил с прямой или разветвленной цепью или Ar - замещенный (C1 - C6) - алкил с прямой или разветвленной цепью;
J - (C1 - C6) - алкил с прямой или разветвленной цепью;
K - (C1 - C6) - алкил с прямой или разветвленной цепью, фенил замещенный (C1 - C6) - алкил с прямой или разветвленной цепью, где фенил может быть замещен галогеном;
X - фенил, замещенный O - (C1 - C6) - алкилом;
Ar - фенил, или Ar является гетероциклической ароматической группой, выбираемой из группы, включающей 2-пиридил, 3-пиридил, 4-пиридил и имидазолил, причем Ar может быть замещен галогеном.
где Pyr - пиридильный радикал, Ph - фенильная группа и Im - имидазолильная группа.
| Способ коррозионных испытаний материалов | 1975 |
|
SU529395A1 |
| EP 0431520 A1, 12.06.1991 | |||
| Сплав на основе никеля | 1974 |
|
SU539976A1 |
| WO 9407858 A1, 14.04.1994 | |||
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ АМИДОВ ЯНТАРНОЙ КИСЛОТЫ | 0 |
|
SU262006A1 |
| RU 2001907 C1, 30.10.1993. | |||
Авторы
Даты
2001-04-20—Публикация
1995-11-13—Подача