Изобретение относится к области биотехнологии, в частности к средствам специфической профилактики чумы плотоядных и сальмонеллеза пушных зверей.
Для профилактики чумы и сальмонеллеза у данного вида пушных зверей используют моновакцины.
Известна вакцина для профилактики чумы плотоядных, содержащая культуральную суспензию аттенуированного штамма "ЭПМ" (Патент РФ N 2067002, A 61 K 39/175, 1996).
Известна поливалентная формолтиомерсаловая вакцина против сальмонеллеза и эшерихиоза молодняка сельскохозяйственных животных и пушных зверей, содержащая взвесь эшерихий и сальмонелл S.typhimurium, S.dublin, S.choleraesuis, инактивированных формалином и тиомерсалом, и адъювант алюмокалиевые квасцы и хлористый кальций (Ветеринарные препараты. Справочник. Под ред. Д.Ф.Осидзе. М.: Колос, 1981, с.223-224).
Недостаток моновакцин заключается в необходимости проведения профилактических обработок против каждой инфекции в отдельности, кроме того, известную вакцину против сальмонеллеза вводят пушным зверям трехкратно. Все это сказывается на затратах труда, растягивает сроки формирования иммунитета у зверей, способствует возникновению стрессовых явлений и осложнений.
Вакцина ассоциированная против чумы и сальмонеллеза лисиц и песцов не известна.
Задачей изобретения является разработка ассоциированной вакцины против чумы и сальмонеллеза пушных зверей, характеризующейся высокой антигенной и иммуногенной активностью.
Технический результат изобретения заключается в получении ассоциированной вакцины против чумы и сальмонеллеза пушных зверей, обладающей широким спектром протективного действия, способной обеспечить длительный и надежный иммунитет против данных инфекций.
Сущность изобретения заключается в следующем: ассоциированная вакцина против чумы и сальмонеллеза лисиц и песцов содержит из антигенов вируса чумы плотоядных (ВЧП) культуральную вирусную суспензию штамма Virus distemper canine ЭПМ с титром инфекционной активности 103 -104 ТЦД 50/0,5 мл, из антигенов сальмонелл - суспензии клеток штаммов Salmonella typhimurium N 3, Salmonella dublin N 6, Salmonella cholerasuis N 9 с концентрацией каждого штамма 10 млрд. кл в 1 мл физиологического раствора, и любой известный стабилизатор, например, на основе сорбита и желатозы.
Входящие в состав вакцины штаммы Salmonella typhimurium N 3, Salmonella dublin N 6, Salmonella cholerasuis N 9 являются известными производственными штаммами, но ранее для изготовления вакцин для пушных зверей не использовались.
Молодняк лисиц и песцов вакцинируют с 45-50-дневного возраста двукратно с интервалом 10-14 дней. Взрослых зверей вакцинируют однократно до гона в декабре-январе. В стационарно неблагополучных по сальмонеллезу хозяйствах рекомендуется вакцинация самок во второй половине беременности, но не позднее чем за 14 дней до щенения. Вакцину вводят внутримышечно в объеме 1 мл.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение ассоциированной вакцины против чумы и сальмонеллеза лисиц и песцов осуществляют путем раздельного приготовления культуральной вирусной суспензии штамма Virus distemper canine ЭПМ и суспензий клеток штаммов Salmonella typhimurium N 3, Salmonella dublin N 6, Salmonella cholerasuis N 9.
Для получения вируссодержащего материала вирус чумы плотоядных выращивают в первично-трипсинизированной культуре клеток эмбрионов японских перепелов в ростовой среде, содержащей 0,5% гидролизат лактальбумина (ГЛА) на растворе Хенкса, 25-50% среды 199 и 8-10% сыворотки крупного рогатого скота с добавлением антибиотиков. Вирус вносят в суспензию клеток и выращивают роллерным способом при 37oC. Через 4-6 часов ростовую среду сливают. Культивирование продолжают в поддерживающей среде, содержащей 60-70% среды 199 и 30-40% ГЛА на растворе Эрла с добавлением антибиотиков. После полного развития цитопатического действия (ЦПД) вируссодержащую культуральную жидкость сливают, замораживают при температуре минус 10-20oC, оттаивают при комнатной температуре и объединяют с бактериальным компонентом.
Для получения бактериального компонента штаммы Salmonella typhimurium N 3, Salmonella dublin N 6, Salmonella cholerasuis N 9 выращивают раздельно в реакторах на бульоне Хоттингера в течение 10-12 часов при температуре 37oC при постоянном перемешивании и непрерывной аэрации. Культивирование прекращают в начале стационарной фазы роста. Выращенные культуры охлаждают до температуры 6-8oC и подвергают проверке. После чего их концентрируют на суперцентрифуге. Бактериальные массы каждого штамма в отдельности разводят стерильным физиологическим раствором до концентрации 10 млрд. микробных клеток в 1 мл по оптическому стандарту ГИСК им. Тарасевича, соединяют в равных объемах и тщательно перемешивают.
К объединенной бактериальной массе добавляют в равном объеме культуральную вирусную суспензию, содержащую не менее 400-500 ТЦД 50/0,5 мл. После тщательного перемешивания добавляют равное по объему количество стабилизирующей среды высушивания. Для лиофилизации вакцины используют стабилизирующую среду высушивания, обычно применяемую при производстве вакцины против чумы плотоядных из штамма ЭПМ, например, на основе сорбита и желатозы. Полученную массу расфасовывают при непрерывном перемешивании в стерильные ампулы или флаконы и лиофилизируют.
Перед применением лиофилизированную ассоциированную вакцину разводят в специальном растворителе, который используется для растворения вакцин против чумы плотоядных.
Получают три серии вакцины. Вакцина ассоциированная против чумы и сальмонеллеза лисиц и песцов имеет следующий компонентный состав, в об.% (табл. 1а).
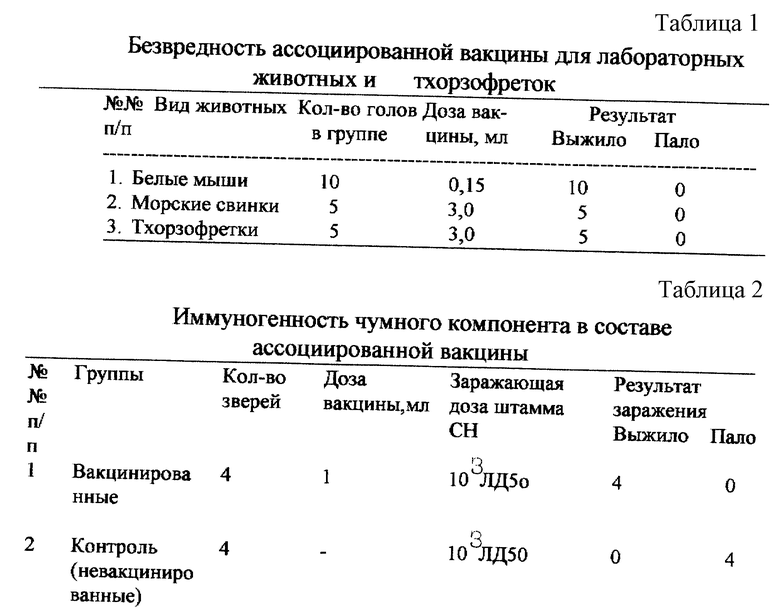
Пример 2. Полученную по примеру 1 ассоциированную вакцину испытывают на безвредность на белых мышах массой 14-16 г, морских свинках массой 300-350 г и тхорзофретках 4-5-месячного возраста при введении различных доз. Обобщенные результаты контроля безвредности представлены в табл. 1.
Испытуемая вакцина безвредна для животных, которые оставались клинически здоровыми в течение 21 дня наблюдения после вакцинации.
Пример 3.
Оценку иммуногенной активности ассоциированной вакцины против чумы и сальмонеллеза лисиц и песцов проводят соответственно на тхорзофретках и морских свинках. Животных иммунизируют однократно внутримышечно в дозе 1,0 мл и через 21 сутки после вакцинации заражают вирулентными штаммами вируса чумы плотоядных и возбудителя сальмонеллеза. Результаты проводимого контроля представлены в табл. 2 и 3.
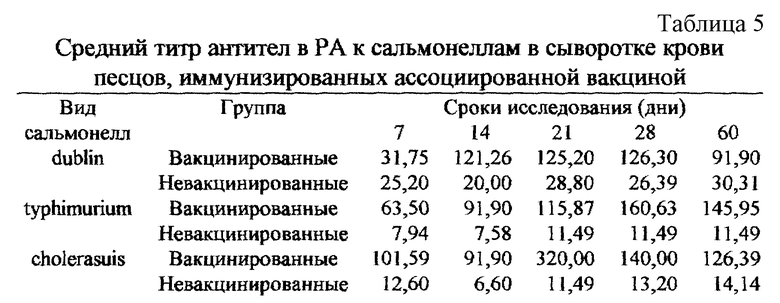
Пример 4. Антигенную активность полученной ассоциированной вакцины оценивают на песцах и лисах путем изучения динамики накопления специфических антител к вирусу чумы плотоядных в реакции непрямой гемагглютинации (РНГА) и к сальмонеллам в реакции агглютинации (РА). Данные исследований представлены в таблицах 4 и 5.
Из табл. 4 и 5 следует, что вакцина ассоциированная против чумы и сальмонеллеза у песцов и лисиц вызывает напряженный иммунитет к вирусу чумы плотоядных и сальмонеллам.
Использование предлагаемой вакцины в ветеринарной практике позволит повысить эффективность проводимых мероприятий по профилактике инфекционных болезней песцов и лисиц.


Изобретение предназначено для специфической профилактики чумы плотоядных и сальмонеллеза лисиц и песцов. Ассоциированная вакцина содержит сбалансированные в антигенном и иммуногенном отношении вирусные и бактериальные антигены. Из антигенов вируса чумы плотоядных она содержит культуральную вирусную суспензию штамма Virus distemper canine ЭПМ с титром инфекционной активности 103-104 ТЦД 50/0,5 мл. Из антигенов сальмонелл - суспензии клеток штаммов Salmonella typhimurium 3, Salmonella dublin 6, Salmonella cholerasuis 9. Концентрация каждого штамма составляет 10 млрд.кл в 1 мл физиологического раствора. Вакцина содержит также стабилизатор. Ассоциированная вакцина характеризуется более высокой антигенной и иммуногенной активностью. 1 з.п. ф-лы, 6 табл.
Культуральная вирусная суспензия штамма Virus distemper canine ЭПМ с титром инфекционной активности 103 - 104 ТЦД 50/0,5 мл - 20 - 25
Суспензия клеток штамма Salmonella typhimurium 3, Salmonella dublin 6, Salmonella cholerasuis 9 с концентрацией каждого штамма 10 млрд.кл в 1 мл физ.р-ра - 20 - 25
Стабилизатор - Остальное
2. Вакцина по п.1, отличающаяся тем, что она содержит стабилизатор на основе сорбита и желатозы.
| ЖИВАЯ КУЛЬТУРАЛЬНАЯ ВАКЦИНА ЭПМ ПРОТИВ ЧУМЫ ПЛОТОЯДНЫХ | 1994 |
|
RU2067002C1 |
| ВАКЦИНА ПРОТИВ ВИРУСНОГО ЭНТЕРИТА, БОТУЛИЗМА, ПСЕВДОМОНОЗА И ЧУМЫ ПЛОТОЯДНЫХ | 1994 |
|
RU2086260C1 |
| US 5000951 A, 19.03.91 | |||
| Система питания для карбюраторного двигателя | 1975 |
|
SU554414A1 |
| Ветеринарные препараты | |||
| Справочник/Под ред.Д.Ф.Осидзе | |||
| - М.: Колос, 1981, с.223-224. | |||
Авторы
Даты
2001-05-10—Публикация
1999-02-11—Подача