Изобретение относится к технологии неорганических продуктов, в частности к способам получения тиосульфатов, и может быть использовано как в химической, так и в металлургической промышленности.
Известен способ получения тиосульфатов путем обработки щелочного серусодержащего раствора кислородсодержащим газом при нормальных условиях [1]. Процесс ведут в присутствии активированного угля при содержании его в растворе 1-150 г/л и при объемном расходе воздуха 1-10 частей на 1 объемную часть раствора. Недостатком способа является малая скорость окисления при атмосферном давлении.
Наиболее близким к предлагаемому способу по технической сущности и достигаемому эффекту является способ получения тиосульфатов путем обработки щелочного раствора серы кислородсодержащим газом при температуре 60-120oC и давлении 0,8-8,0 кг/см2 [2]. По этому способу в автоклав загружают навеску технической молотой серы и водный раствор (суспензию) щелочи натрия или кальция в стехиометрическом соотношении. Перемешивание осуществляют при 100oC в течение 1 часа до получения щелочного раствора серы. Через полученный раствор с температурой 60-120oC продувают кислород, воздух или кислородовоздушную смесь, содержащую 60% кислорода, при удельном расходе ~ 100 л/час и давлении 0,8-8,0 кг/см2. Суммарное время обработки серы составляет 2 часа.
Недостатком способа является большая длительность процесса и необходимость последовательного и раздельного проведения двух реакций.
Цель изобретения - упрощение процесса и сокращение времени обработки.
Поставленная цель достигается путем проведения процесса растворения серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия одновременно с ее окислением до тиосульфата кислородсодержащим газом при повышенных температурах и давлениях.
Сущность метода состоит в следующем. Процесс растворения серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия протекает в кинетической области. Скорость этих процессов сильно зависит от температуры и может замедляться при накоплении растворимых продуктов реакций. С другой стороны, процесс окисления кислородсодержащим газом протекает во внешнедиффузионной области. Скорость протекания этого процесса зависит от вязкости раствора.
При растворении серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия образуются растворы, содержащие сульфиды, полисульфиды и тиосульфат. При проведении растворения серы в щелочном растворе в течение длительного времени (по прототипу) получают обладающие большой вязкостью и богатые по сере "поли" растворы (>100 г/л Sполи).
В предлагаемом способе получают менее концентрированные по сере "поли" растворы (<50 г/л Sполи) за счет постоянного присутствия окислителя в зоне реакции.
Таким образом, уменьшение концентрации серы "поли" в растворе способствует с одной стороны поддержанию высокой скорости растворения серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия, т.к. нет накопления растворимых продуктов реакций, а с другой стороны - увеличению скорости окисления образующихся в растворе сульфидов и полисульфидов до тиосульфата кислородсодержащим газом за счет снижения вязкости раствора.
При получении тиосульфата кальция оптимальными являются следующие условия проведения процесса: температура 85-100oC и давление 1,0- 2,0 кг/см2, при получении тиосульфата натрия, соответственно, температура 70-120oC и давление 1,0-8,0 кг/см2. При температуре ниже указанных значений снижается скорость растворения серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия, что приводит к увеличению времени процесса. Проведение растворения серы при температуре выше указанных значений приводит к увеличению доли серы "моно", которая в дальнейшем может окисляться до сульфатной серы. При парциальном давлении кислорода выше указанных значений происходит окисление тиосульфата до сульфита. При парциальном давлении кислорода менее 1,0 кг/см2 снижается скорость окисления "моно" и "поли" форм серы и увеличивается время процесса, что способствует разложению тиосульфат-иона на сульфитную и элементарную серу. Во всех рассмотренных случаях выход за пределы граничных условий проведения процесса приводит к уменьшению выхода серы "тио". Различие диапазонов температур и давлений, при которых проводится получение тиосульфатов кальция и натрия, обусловлено различной растворимостью соединений кальция и натрия в воде и различной щелочностью получаемых растворов.
Пример 1 (по прототипу).
В автоклав с механическим перемешиванием загружают навеску технической молотой серы и водную суспензию щелочи кальция из расчета массового отношения S:CaO=1,1:1,0. Суспензию перемешивают при температуре 100oC в течение 1 часа, затем в течение еще 1 часа при температуре 85oC подают в автоклав технический кислород при парциальном давлении 1,6 кг/см2. При скачке окислительно-восстановительного потенциала от - 0,4 до - 0,1 В считают процесс завершенным. Концентрация серы "тио" в растворе составляет 107 г/л. Время обработки 2 часа.
Пример 2 (по предлагаемому способу).
Загрузка исходных продуктов в автоклав такая же, как в примере 1. По окончании нагрева суспензии до температуры 85oC в автоклав начинают подавать технический кислород при парциальном давлении 1,6 кг/см2. При достижении eH пульпы<равным приблизительно - 0,1 В, процесс завершают. Концентрация серы "тио" в растворе составляет 118 г/л. Время обработки 65 минут.
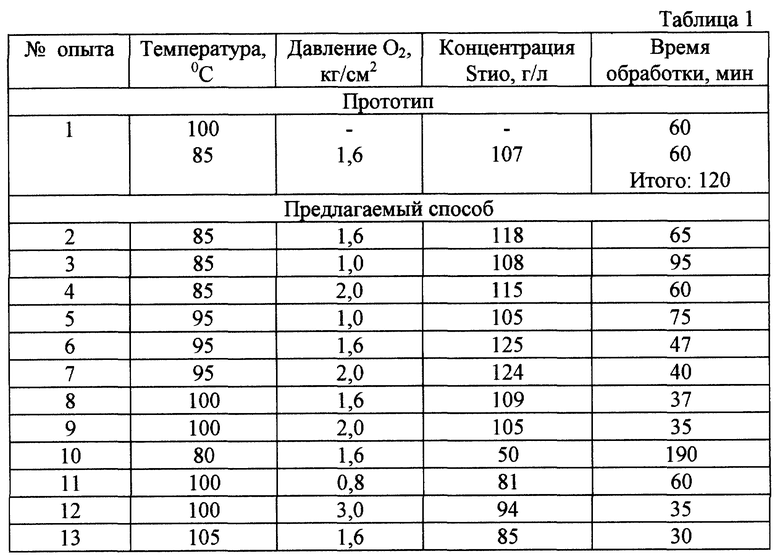
Результаты опытов по получению тиосульфата кальция при различных температурах и давлениях представлены в таблице 1.
При температуре менее 85oC снижается скорость растворения серы в водной суспензии щелочи кальция, время процесса возрастает, выход серы "тио" уменьшается (оп. 10).
При температуре более 100oC при растворении серы в водной суспензии щелочи кальция увеличивается доля серы "моно", которая при окислении переходит в сульфатную и, соответственно, уменьшается выход серы "тио" (оп. 13).
При парциальном давлении кислорода менее 1,0 кг/см2 снижается скорость окисления "моно" и "поли" форм серы и увеличивается время процесса, что в свою очередь способствует разложению тиосульфат-иона на сульфитную и элементарную серу и выход серы "тио" падает (оп. 11).
При парциальном давлении кислорода более 2,0 происходит окисление тиосульфата до сульфита и снижается выход серы "тио" (оп. 12).
Пример 3 (по прототипу).
В автоклав загружают навеску технической молотой серы и водный раствор щелочи натрия в стехиометрическом соотношении. Растворение серы в водном растворе щелочи ведут при температуре 100oC в течение 1 часа, затем при температуре 95oC в течение еще 1 часа подают в автоклав технический кислород при парциальном давлении 1,6 кг/см2. При скачке окислительно-восстановительного потенциала до значения приблизительно 0,1 В заканчивают процесс. Концентрация серы "тио" в растворе составляет 132 г/л. Время обработки 2 часа.
Пример 4 (по предлагаемому способу).
По окончании нагрева смеси серы и водного раствора щелочи натрия, взятых в стехиометрическом соотношении, до температуры 95oC начинают подавать в автоклав технический кислород при парциальном давлении 1,6 кг/см2. При достижении значения окислительно-восстановительного потенциала, равным ~ 0,1 В, процесс завершают. Концентрация серы "тио" в растворе составляет 132 г/л. Время обработки 75 минут.
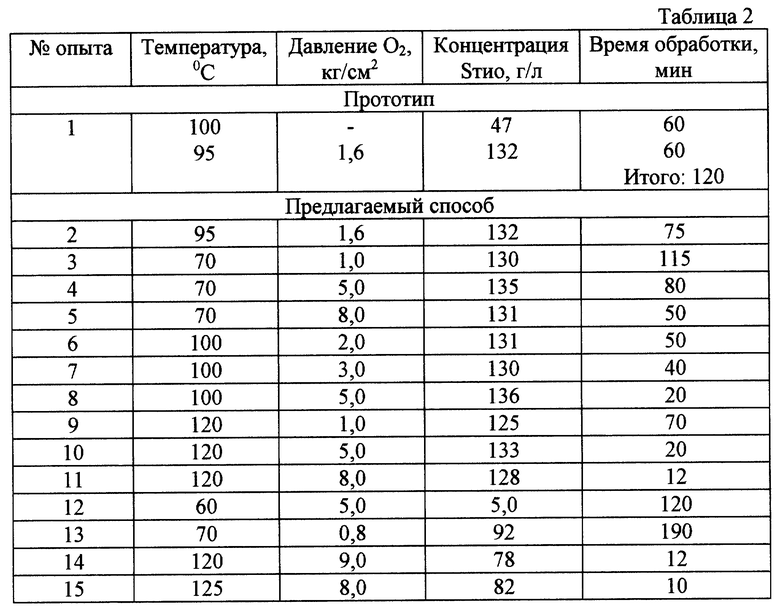
Результаты опытов по получению тиосульфата натрия при различных температурах и давлениях представлены в таблице 2.
При получении тиосульфата натрия выход за пределы граничных условий проведения процесса - температура 70-120oC и давление 1,0-8,0 кг/см2 - приводит к сокращению выхода серы "тио" (оп. 12 - 15), а в случае проведения опытов при температуре менее 70oC, а также опытов при давлении менее 1,0 кг/см2 - также к увеличению и продолжительности времени обработки (оп. 12, 13).
При ведении процесса получения тиосульфатов по предлагаемому способу в непрерывном режиме загрузка реагентов осуществляется в реактор, в котором пульпа находится при повышенной температуре и повышенном давлении. Охлаждения пульпы не будет происходить, т.к. реакция окисления кислородсодержащим газом идет с большим выделением тепла. Поэтому отпадает необходимость в предварительном нагреве исходных реагентов до температуры, при которой ведется процесс получения тиосульфатов.
Таким образом, проведение растворения серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия одновременно с окислением ее до тиосульфата кислородсодержащим газом позволяет упростить известный способ и существенно сократить время обработки серы.
Источники информации
1. Авторское свидетельство СССР N 589901, кл. C 01 B 17/64, 1978.
2. Авторское свидетельство СССР N 833480, кл. C 01 B 17/64, 1981.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОСАЖДЕНИЯ ЦВЕТНЫХ МЕТАЛЛОВ ИЗ РАСТВОРОВ | 2000 |
|
RU2182183C2 |
| Способ получения тиосульфатов | 1979 |
|
SU833480A1 |
| СПОСОБ ПЕРЕРАБОТКИ СУЛЬФИДНОГО СЫРЬЯ, СОДЕРЖАЩЕГО БЛАГОРОДНЫЕ МЕТАЛЛЫ | 2010 |
|
RU2447166C2 |
| СПОСОБ ПЕРЕРАБОТКИ СУЛЬФИДНОГО СЫРЬЯ, СОДЕРЖАЩЕГО ДРАГОЦЕННЫЕ МЕТАЛЛЫ | 2012 |
|
RU2528300C2 |
| СПОСОБ ПЕРЕРАБОТКИ СУЛЬФИДНОГО ПИРРОТИНСОДЕРЖАЩЕГО СЫРЬЯ | 1997 |
|
RU2114195C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИФТОРИРОВАННЫХ СПИРТОВ | 1999 |
|
RU2150459C1 |
| СПОСОБ ПОДГОТОВКИ НЕФТИ И ГАЗОКОНДЕНСАТА | 2013 |
|
RU2541523C2 |
| СПОСОБ ПЕРЕРАБОТКИ СЫРЬЯ, СОДЕРЖАЩЕГО БЛАГОРОДНЫЕ МЕТАЛЛЫ И СУЛЬФИДЫ | 2013 |
|
RU2547056C1 |
| СПОСОБ ПЕРЕРАБОТКИ СВИНЦОВИСТЫХ ШЛАМОВ ЭЛЕКТРОРАФИНИРОВАНИЯ МЕДИ (ВАРИАНТЫ) | 2011 |
|
RU2451759C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАЛЬЦИЕВОГО СУЛЬФИДИЗАТОРА ДЛЯ ОСАЖДЕНИЯ ТЯЖЕЛЫХ ЦВЕТНЫХ МЕТАЛЛОВ ИЗ КИСЛЫХ СУЛЬФАТНЫХ РАСТВОРОВ И ЖИДКОЙ ФАЗЫ ГИДРАТНЫХ ЖЕЛЕЗИСТЫХ ПУЛЬП | 1997 |
|
RU2120484C1 |
Изобретение относится к технологии неорганических продуктов и может быть использовано в химической и металлургической промышленности. Способ получения тиосульфатов заключается в проведении растворения серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия одновременно с окислением ее до тиосульфата кислородсодержащим газом. Получение тиосульфата кальция ведут при температуре 85-100°С и давлении 1,0-2,0 кг/см2, а тиосульфата натрия - при температуре 70-120°С и давлении 1,0-8,0 кг/см2. Способ позволяет упростить процесс и сократить время получения тиосульфатов. 2 табл.
Способ получения тиосульфата кальция или натрия, включающий растворение серы в водной суспензии щелочи кальция или в водном растворе щелочи натрия и окисление полученного раствора кислородсодержащим газом, отличающийся тем, что растворение серы ведут одновременно с процессом ее окисления до тиосульфата при следующих условиях: для получения тиосульфата кальция процесс ведут при температуре 85-100°С, давлении 1,0-2,0 кг/см2, а для получения тиосульфата натрия - при температуре 70-120°С и давлении 1,0-8,0 кг/см2.
| Способ получения тиосульфатов | 1979 |
|
SU833480A1 |
| Способ получения тиосульфата натрия | 1980 |
|
SU947034A1 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОГО ТИОСУЛЬФАТА АММОНИЯ | 1996 |
|
RU2110473C1 |
| Устройство для резки труб | 1984 |
|
SU1177163A2 |
| СПОСОБ ВЫРАБОТКИ КОНСЕРВОВ "КОТЛЕТЫ ДОМАШНИЕ С СОУСОМ КРАСНЫМ С ЛУКОМ И ОГУРЦАМИ" | 2008 |
|
RU2360511C1 |
| US 3473891 А1, 21.10.1969 | |||
| Т.Г | |||
| AXMETOB, В.М | |||
| БУСЫГИН, Л.Г | |||
| ГАЙСИН, Р.Т | |||
| ПОРФИРЬЕВА | |||
| Химическая технология неорганических веществ | |||
| - М.: Химия, 1998, с.219. | |||
Авторы
Даты
2001-05-20—Публикация
1999-07-05—Подача