Изобретение относится к способам подготовки нефти, включает обессоливание и очистку нефти и газоконденсата от сероводорода и меркаптанов, и может быть использовано в газо- и нефтедобывающей и нефтеперерабатывающей промышленности для дезодорации нефти и газоконденсата с одновременной очисткой от солей.
Для обессоливания, то есть очистки от минеральных солей, в основном хлоридов натрия, кальция и магния, нефть и газоконденсат контактируют свежей водой, добавляют деэмульгатор, после содержащую растворенных солей (хлоридов) воду отделяют путем отстаивания и в электродегидраторах.
Для очистки нефтепродуктов от меркаптанов широко применяют способы, основанные на переводе меркаптанов водным раствором щелочи в меркаптиды с последующим окислением меркаптидов кислородом воздуха в дисульфиды в присутствии катализаторов [Сигеру Оаэ. Химия органических соединений серы. - М: Химия, 1975, с. 98-101]. Недостатком этих способов является сложность их реализации, требующих создания специальных многостадийных промышленных установок.
Известны способы демеркаптанизации нефтепродуктов путем обработки растворами гипохлорита натрия, перекиси водорода, надкислотами, диметилсульфоксидом и др. [Сигэру Оаэ. Химия органических соединений серы. - М.: Химия, 512 с; с. 101-103].
Известен способ (патент 3151133 ФРГ) [1] очистки нефти от сероводорода путем окисления 10-50%-ным водным раствором пероксида водорода при температуре от 0 до 60°С и давлении от 0,5 до 2 МПа. При этом водный раствор пероксида водорода берут из расчета не менее 20 мл на 1 г сероводорода и в качестве реактора используют трубопровод, то есть процесс ведут в трубчатом реакторе. Недостатками данного способа являются длительность проведения процесса из-за низкой скорости окисления сероводорода и невысокая степень очистки сырья, особенно при низких температурах, а также большой расход применяемого окислителя.
В патенте РФ 2177494 [2] очистку нефти и газоконденсата от сероводорода и меркаптанов проводят путем обработки 10-50%-ным водным раствором пероксида водорода, взятого в количестве 0,5-3,0 моля на 1 моль сероводородной и меркаптановой серы, в присутствии азотсодержащего основания и/или щелочного реагента, взятых в количестве 0,2-3,0 моля на 1 моль сероводородной и меркаптановой серы, и катализаторов, взятых из расчета 0,1-50 г на 1 т нефти или газоконденсата, при температуре 0-70°С и давлении до 1,0 МПа. В качестве катализаторов используют фталоцианины кобальта (дисульфо-, тетрасульфо-, дихлордиоксидисульфо- и полифталоцианины) в количестве 0,1-2 г на 1 тонну нефти и соединения металлов V1-V111 группы в количестве до 50 г/т. Сырье сначала смешивают с концентрированным водным раствором щелочи и катализаторов, потом в полученную эмульсию вводят раствор пероксида водорода. Аналогичные режимы очистки предложены в патенте РФ 2196804, где предложено применять растворы гидроксидов натрия и калия концентрацией 20-40% [3].
В патенте РФ 2121491 [4] окисление сероводорода и меркаптанов в нефти или газоконденсате пероксидом водорода в присутствии органического амина проводят при 15-65°С и давлении 0,14-2,1 МПа, и сырье дополнительно обрабатывают элементной серой, взятой в количестве 0,15-0,5 молей на 1 моль меркаптановой и сероводородной серы.
Главным недостатком вышеописанных способов является низкая безопасность процессов: концентрированные растворы пероксида водорода (20-50% Н2О2) в случае передозировки в поток нефти или в случае попадания нефти в раствор пероксида могут вызвать пожар и взрыв. Концентрированные растворы пероксида водорода при хранении в присутствии щелочей и катализаторов разлагаются с выделением кислорода. Известно, что при одном и том же соотношении H2S:OH- концентрированные растворы щелочей экстрагируют сероводород хуже, чем разбавленные растворы. Кроме того, щелочной отработанный водный раствор из тяжелых нефтей не отстаивается, происходит образование эмульсии и обводнение сырья. Еще одним недостатком описанных способов является низкая эффективность их при очистке сырья от меркаптанов, для очистки от меркаптанов требуется большой расход реагентов (до 5 молей пероксида водорода, NaOH или аминов на 1 моль меркаптана) и введение катализаторов. Ввиду этих недостатков вышеописанные способы не нашли практического применения.
По технической сущности и достигаемому результату наиболее близким к предлагаемому изобретению является способ, описанный в патенте РФ 2146693 [5], где для очистки от сероводорода нефть или газоконденсат обрабатывают 20-50%-ным водным раствором пероксида водорода в присутствии азотсодержащего основания и/или щелочного реагента. Используют аммиак или органический амин, карбонаты или гидрооксиды натрия и калия в количестве 0,5-5 молей на 1 моль сероводорода. В качестве органического амина применяют этаноламины, алкиламины С1-С4, этилендиамин, полиэтиленполиамин, циклогексиламин, изопропаноламин и их смеси. Водный раствор пероксида водорода берут из расчета 1-5 молей H2O2 на 1 моль H2S. В этом способе катализаторы не применяются.
Недостатками способа являются:
- низкая безопасность процесса: концентрированные растворы пероксида водорода (20-50% H2O2) в случае передозировки в поток нефти или при введении раствора без перемешивания, а также в случае попадания нефти в раствор пероксида водорода могут вызвать пожар и даже взрыв;
- концентрированные растворы NaOH с тяжелыми нефтями образуют эмульсии, которые трудно разделяются, а использование аминов взамен NaOH сильно удорожает стоимость реагентов;
- при одном и том же соотношении H2S:ОН- концентрированные растворы щелочей экстрагируют сероводород из нефти хуже, чем разбавленные растворы;
- большой расход реагентов - до 5 молей на 1 моль сероводорода, так как в концентрированных растворах сероводород окисляется до тиосульфата 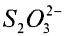 , сульфита
, сульфита  и сульфата
и сульфата 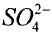 , а в разбавленных растворах - до элементной серы и тиосульфата;
, а в разбавленных растворах - до элементной серы и тиосульфата;
- для очистки от образовавшихся солей (тиосульфатов, сульфитов и сульфатов) нефть после очистки от сероводорода и меркаптанов еще раз контактируют (промывают) чистой водой;
- пероксид водорода в присутствии каталитических количеств ионов железа в растворах NaOH медленно разлагается, поэтому неизбежны дополнительные потери его из-за разложения. Чем выше концентрация щелочей и пероксида водорода, тем больше скорость его разложения.
Задачей настоящего изобретения является снижение затрат на реагенты и повышение безопасности и эффективности процесса, а именно:
- повышение безопасности процесса за счет использования разбавленных, содержащих менее 1,2% H2O2, растворов пероксида водорода;
- снижение затрат на реагенты;
- исключение или уменьшение количества образующейся эмульсии очищенной нефти с отработанными щелочными растворами;
- проведение процессов обессоливания и очистки нефти и газоконденсата от сероводорода и меркаптанов одновременно в одну стадию;
- повышение скорости реакции окисления сероводорода и меркаптанов и степени очистки сырья.
Для получения указанных технических результатов в предлагаемом способе обессоливания и очистки нефти и газоконденсата от сероводорода и меркаптанов исходное сырье контактируют с разбавленным водным раствором щелочных агентов и окисляют образующиеся гидросульфиды и меркаптиды 0,1-1,2%-ным раствором пероксида водорода при температуре 0-65°С. Водный раствор содержит 0,02-1,0% гидрооксида кальция и до 0,95% гидрооксидов щелочных металлов, аммиака, моноэтаноламина, триэтаноламина или их смесей. Гидрооксид кальция находится в полностью растворенном виде или в виде суспензии (известкового молока). Пероксид водорода можно вводить в водный раствор щелочных агентов до контактирования с сырьем, и процессы экстракции сероводорода и меркаптанов из нефтяной фазы в водную фазу и окисления образующихся гидросульфидов и меркаптидов проводить одновременно. Можно также сероводород и метил-, этилмеркаптаны сначала экстрагировать водным раствором щелочных агентов, потом в этом экстракте окислять их путем введения пероксида водорода. На 1 моль сероводорода и подлежащих очистке меркаптанов (например, метил-, этилмеркаптанов) берут 0,3-1,5 моля Ca(OH)2 и 0,5-3,5 моля H2O2. Для приготовления растворов Ca(OH)2 и известкового молока используют негашеную (CaO) или гашенную известь Ca(OH)2. Растворы могут быть приготовлены также путем смешения водных растворов хлористого кальция и едкого натра. В качестве водного раствора хлористого кальция предлагается использовать пластовую воду, содержащуюся в самой сырой нефти. Пластовые воды содержат до 12% NaCl и 1-4% CaCl2.
Отработанный водно-щелочной экстракт хлоридов, сульфидов, меркаптидов и продуктов их окисления утилизируют путем смешения с кислыми (pH ~5) пластовыми водами.
В соответствии с ГОСТ Р 51858-2002 «Нефть. Общие технические условия» в нефти первого вида массовая доля сероводорода не должна превышать 20 ppm (0,0020%), метил- и этилмеркаптанов в сумме - 40 ppm (0,0040%). Массовая доля воды в нефти первой группы не должна превышать 0,5%), а концентрация хлористых солей - 100 мг/дм3. Для нефти второй группы содержание хлоридов не должно быть более 300 мг/дм3.
Отличительными признаками предлагаемого изобретения являются:
1. Использование разбавленных 0,1-1,2%-ных растворов пероксида водорода, которые при контактировании с углеводородами не способны вызвать возгорание. В известном способе используют 20-50%-ные растворы.
2. Использование в качестве щелочного агента или в качестве компонента смеси щелочных агентов гидрооксида кальция и использование известкового молока с содержанием Са(ОН)2 до 1%. В известном способе применяют концентрированные растворы NaOH, KOH, аммиака и аминов.
В отличие от растворов NaOH растворы Са(ОН)2 не образуют с тяжелыми нефтями неразделяющиеся и трудноразделяющиеся эмульсии.
3. Низкие затраты на реагенты. Расходы щелочных агентов и пероксида водорода на 1 моль H2S и RSH С1-С2 в сумме составляют:
В водных растворах H2O2 сероводород в слабощелочной среде окисляется до элементной серы или до тиосульфата S2O3 2-, а в сильнощелочной среде (рН>12) и избытке H2O2 - до сульфата SO4 2- по необратимым реакциям:
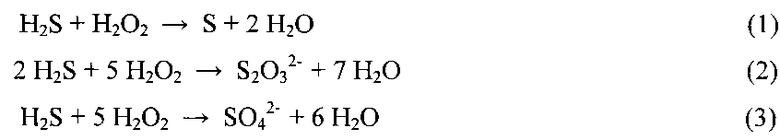
Для окисления до сульфата по реакции (3) расходуется окислителя в два раза больше, чем до тиосульфата по реакции (2). В предлагаемом способе идут реакции (1) и (2), а в известном - реакция (3), соответственно расход H2O2 в известном способе в два раза выше.
В известном способе операции обессоливания нефти (промывки нефти водой) проводят до операции очистки от сероводорода и еще раз после операции очистки для удаления вновь образовавшихся солей (тиосульфатов и сульфатов) [6]. В предлагаемом способе операции обессоливания и очистки от сероводорода совмещены. По крайней мере, нет необходимости проведения второй операции обессоливания.
Сероводород и меркаптаны реагируют с Ca(OH)2 по обратимой реакции с образованием бисульфида и меркаптида кальция:


В реакцию (5) вступают низкомолекулярные меркаптаны C1-C2 и частично C3-C4, которые образуют водорастворимые меркаптиды. Выход сульфидов и меркаптидов зависит от pH водного раствора (экстракта), увеличивается с повышением pH. Растворимость Ca(OH)2 в воде при 20°С равна ~0,15%. pH насыщенного раствора равен 12,4. [Справочник химика. т.111. - М.-Л.: Химия, 1964]. При экстракции из-за образования сульфидов и меркаптидов pH водного раствора снижается до 8-11.
Ввиду ограниченной растворимости Ca(OH)2 в воде, при очистке сырья с высоким содержанием сероводорода и меркаптанов предложено применять известковое молоко, то есть суспензию Ca(OH)2 в его насыщенном растворе с общей концентрацией Ca(OH)2 до 1%. Применение известкового молока не меняет химизм процесса. Образующийся Ca(HS)2 хорошо растворяется в воде, поэтому нерастворенный Ca(OH)2 по мере расходования его по реакциям (4) и (5) переходит в раствор (если избыток его был взят не выше пределов растворимости Ca(HS)2+Ca(OH)2). В присутствии H2O2 идут следующие окислительные реакции:
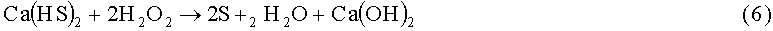

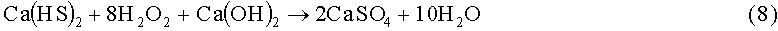

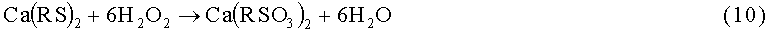
Из-за расходования Ca(OH)2 по реакциям (4) и (5) и образования нейтральных солей по реакциям (7, 8, 10) pH раствора снижается с 12,4 до 8-11.
Минимально необходимый расход Ca(OH)2 по реакциям (4) и (5) составляет 0,5 моля на 1 моль сероводорода и меркаптанов C1-C2 в сумме. Однако часть Ca(OH)2 по реакциям (6, 8 и 9) регенерируется, что позволяет снизить его минимальный расход до 0,3 моля. Для полноты прохождения реакций (4) и (5) берут избыток Ca(OH)2 ~20%.
Часть Ca(OH)2 расходуется на нейтрализацию присутствующих в сырье нафтеновых кислот и углекислого газа. С учетом этих факторов максимальный расход Ca(OH)2 взят равным 1,5 моля на 1 моль сероводорода и меркаптанов C1-C2.
Для создания щелочной среды и поддерживания pH водной фазы не ниже 8-8,5, а также с целью снижения температуры замерзания раствора, в водный раствор Ca(OH)2 могут быть введены дополнительно другие щелочные агенты: NaOH, аммиак и амины. Из аминов на практике могут быть использованы дешевые и доступные моноэтаноламин и триэтаноламин. При введении этих щелочных агентов концентрацию Ca(OH)2 можно снизить до 0,02%. Разбавлять раствор ниже этой концентрации Ca(OH)2 нецелесообразно, так как это приводит к увеличению объема водной фазы. С точки зрения экономики также выгоднее применять более дешевый Ca(OH)2, чем относительно дорогие NaOH, аммиак и амины. Расходы Ca(OH)2 и других щелочных агентов (аминов и аммиака) увеличивать выше 1,5 моль на 1 моль (H2S+RSH) и повысить концентрации их в растворе выше 1% допустимо, но в этом нет необходимости. Концентрация NaOH в водном растворе не должна превышать концентрацию Ca(OH)2, так как это приводит к замедлению скорости окисления, а также может быть причиной образования стойкой эмульсии. Сульфиды натрия NaHS и Na2S окисляются гораздо труднее, чем Ca(HS)2. Использование растворов едкого натра, аммиака и аминов для очистки углеводородного сырья от сероводорода и меркаптанов известно из вышеописанных патентов №2121491, 2146693, 2196804, 2177494 [2-5].
По реакции (9) для окисления 1 моля меркаптанов расходуется 0,5 моля H2O2. Для окисления 1 моля H2S по реакциям 6 и 7 требуется 1 и 2 моля H2O2. Эти реакции идут одновременно. Кроме того, часть H2O2 расходуется на побочные реакции окисления, окисляется также часть меркаптанов C3 и выше. С учетом всех этих факторов расход пероксида водорода взят в пределах 0,5-3,5 моля на 1 моль серы (32 г серы), находящейся в виде сероводорода и меркаптанов C1-C2. Сульфиды и меркаптиды кальция легко окисляются пероксидом водорода: при 0°C окисление сульфидов происходит в течение 5 мин. При повышенном расходе H2O2 до 3,5 моля окисляются также меркаптаны C3 и C4. В известных способах при использовании растворов NaOH образуются сульфиды и меркаптиды натрия, которые трудно окисляются, поэтому процесс окисления вынуждены проводить при температуре выше 40°C [патент 2146693] и в присутствии катализаторов [патенты 2121491, 2177494 и 2196804]. Концентрация H2O2 в водной фазе не превышает 1,2%, контакт ее с нефтью не опасен.
В технологическом плане предлагаемый процесс очистки нефти и газоконденсата может быть оформлен в двух вариантах. В первом варианте стадии контактирования сырья со щелочным раствором и окисления образующихся бисульфидов и меркаптидов совмещены, проводятся одновременно: в поток сырья вводят водный раствор, содержащий расчетные количества щелочных агентов и пероксида водорода. После контактирования (эффективного перемешивания для экстракции H2S и RSH из нефтяной фазы в водную фазу), очищенное сырье отделяют от водно-щелочного экстракта. Окисление бисульфида и меркаптидов кальция начинается при экстракции (контактировании) и заканчивается в отработанной водной фазе после ее отделения от очищенного сырья.
Во втором варианте сначала сырье контактируют со щелочным раствором, затем экстракт отделяют от очищенного сырья, после, растворенные в экстракте бисульфид и меркаптиды кальция, окисляют пероксидом водорода. Процессы экстракции и окисления пероксидом водорода можно проводить при любой температуре в пределах 0-65°C (предпочтительно проводить при 10-30°C). Реакции 6, 7 и 9 заканчиваются за 5-10 мин. Количество водной фазы составляет от 80 до 500 кг на 1 т нефтяной фазы.
При экстракции из нефти или газоконденсата сероводорода и низкомолекулярных меркаптанов разбавленными водными растворами щелочных агентов, присутствующие в сырье неорганические соли, в первую очередь хлориды - NaCl, CaCl2, MgCl2, переходят в водную фазу, происходит очистка от хлористых солей, то есть обессоливание сырья.
Предлагаемый способ проверен в лабораторных условиях. Ниже приведены примеры и результаты опытов.
Примеры конкретного выполнения
Пример 1. Проверка стойкости эмульсии карбоновой нефти Нурлатского месторождения (р. Татарстан) и водных растворов щелочных агентов.
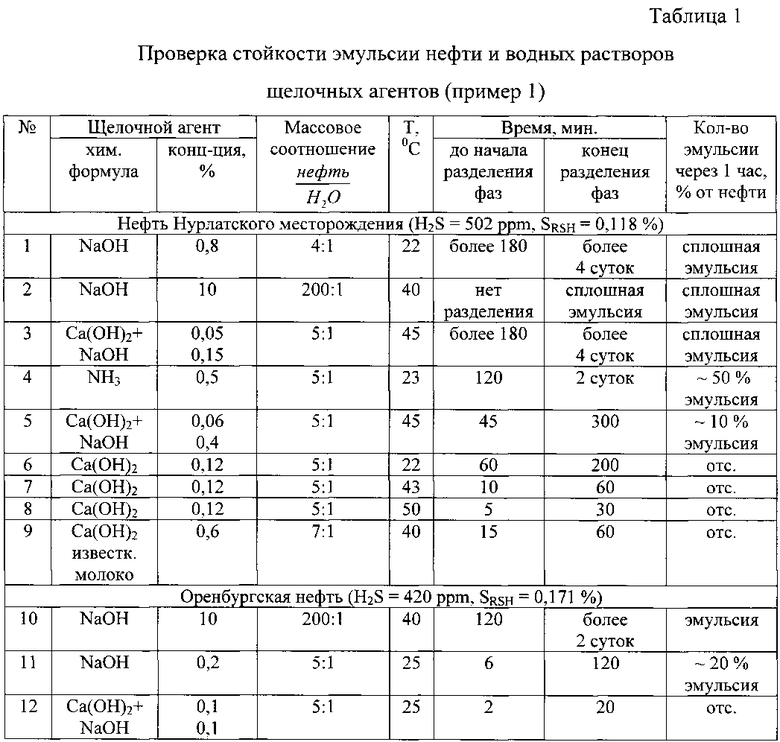
В делительную воронку вместимостью 250 мл берут 100 г (110 мл) тяжелой карбоновой нефти, содержащей 560 ppm сероводородной серы и 0,118% меркаптановой серы, и 25 мл водного раствора щелочных агентов. Воронку закрывают резиновой пробкой, и содержимое перемешивают в течение 3 мин встряхиванием. После воронку ставят в водяной термостат с постоянной температурой. Ведут наблюдения за процессом разделения эмульсии. Результаты наблюдений приведены в табл.1.
Как видно из табл.1, растворы NaOH, которые применяются в известном способе, образуют сплошные, не разделяющиеся эмульсии. Трудно разделяющиеся эмульсии образуют растворы NH3. (Аммиак в водных растворах находится в виде NH4OH). Растворы Ca(OH)2 и известковое молоко при температурах выше 40°C полностью разделяются в течение 30-60 мин. Смешанные растворы NH3 и Ca(OH)2 разделяются труднее, чем растворы Ca(OH)2, а смешанные растворы NaOH и Ca(OH)2 образуют сплошные эмульсии. Этот пример показывает преимущество использования Ca(OH)2 в качестве щелочного агента при экстракции сероводорода и легких меркаптанов из нефтей, образующих стойкие эмульсии с щелочными растворами.
Пример 2. Очистка нефти от сероводорода и меркаптанов. Опыты проводят на нефти месторождений Бузулук Оренбургской обл. и Нурлат республики Татарстан.
2.1. Очистка карбоновой нефти Нурлатского месторождения. Пример расчетов.
Нефть до очистки содержит в расчете на серу (S2-): 550 г/т (ppm) серы H2S и 36 г/т серы меркаптанов (CH3SH+C2H5SH). Содержание хлористых солей до очистки равно 544 мг/л. Берут 100 мл (90 г) нефти с содержанием 586·10-4·0,9=0,0527 г S2-. Для нейтрализации этой S2- требуется
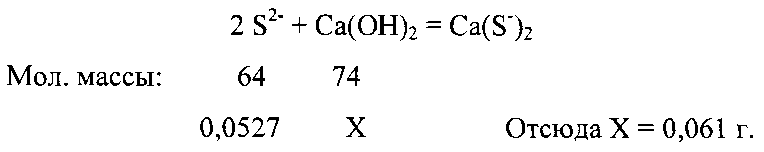
Берут 20%-ный избыток Са(ОН)2, то есть 0,061·1,2=0,073 г.
Для растворения сухого (безводного) Са(ОН)2 и получения 0,14%-ного раствора берут воду в количестве
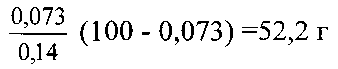
Получают раствор Са(ОН)2 в количестве 52,27 г.
Для окисления 1 моля S2- по реакциям (6-7) требуется 1÷2 моля H2O2, для окисления 0,0527 г S2-, соответственно 0,056÷0,112 г H2O2, или 0,2÷0,4 г. 36%-ного водного раствора пероксида водорода. Раствор пероксида водорода смешивают с раствором извести, получают окислительный водно-щелочной раствор с содержанием 0,11÷0,21% H2O2. Этот раствор в делительной воронке смешивают со 100 мл нефти. Смесь перемешивают встряхиванием в течение 1,5÷2 мин, затем отстаивают до полного отделения водной фазы от нефтяной фазы. При 20°С разделение фаз происходит в течение 1,5÷2 час. При 45÷55°С - за 15÷30 мин. После анализируют обе фазы на содержание сероводородной и меркаптановой серы потенциометрическим титрованием по ГОСТ 17323. Содержание метил- и этилмеркаптанов в нефти определяют хроматографическим методом по ГОСТ Ρ 50802-95. Следующие опыты проводят в тех же условиях, изменяя расходы Са(ОН)2 и пероксида водорода.
2.2. Опыты проводят аналогично п. 2.1, но с использованием легкой нефти Оренбургской области (месторождения Бузулук). Эта нефть содержит 280-400 мг/л хлористых солей.
2.3. Параллельно проводят опыт по известному способу, в котором вместо раствора Са(ОН)2 берут 0,22%-ный раствор NaOH. Эти растворы содержат одинаковое количество ОН- - групп.
Результаты опытов по примеру 2 приведены в табл. 2.
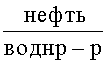
В опытах табл. 2 дополнительно определяют содержание хлористых солей; содержание их в очищенной нефти во всех опытах не превышает 80 мг/л. Как видно из табл. 2, нефть от сероводорода можно очистить, если для экстракции брать не менее 0,6 молей Са(ОН)2 на 1 моль S2- (опыты 3 и 8) и 190-500 л водного раствора Са(ОН)2 на 1 т нефти. Если водной фазы менее 200 л, то требуется более 0,7 моля Са(ОН)2 (опыт 8). Однако в этом случае возникает необходимость очистки экстракта от Ca(SH)2 и Ca(RS)2 (способ очистки описан на примере 4). Удовлетворительная очистка достигается при расходе Са(ОН)2 - 0,4÷0,7 молей и H2O2 - не менее 1 моля (опыты 6, 7 и 11). Увеличение количества водной фазы позволяет уменьшать расходы Са(ОН)2 и H2O2. Сравнение предлагаемого и известного способов (опыты 5, 12 и 13) показывает, что при использовании разбавленных растворов NaOH (опыт 12) степень очистки нефти от H2S находится примерно на одном уровне, а очистка от RSH в предлагаемом способе является намного более эффективной. При использовании раствора NaOH концентрация меркаптанов в нефти снижается на 50 ppm, а в предлагаемом способе, в опытах 5-7 и 10-11, снижается на 300 и более ppm; наряду с меркаптанами C1 и С2 окисляется также часть меркаптанов С3 и выше. В опытах 5-7 содержание метил-, этилмеркаптанов в очищенном сырье не превышает 20 ppm. При использовании концентрированных растворов реагентов по известному способу удовлетворительная очистка не достигается не только по меркаптанам, но и по сероводороду (опыт 13). Очистка нефти до содержания ниже 20 ppm сероводорода достигается только при расходах H2O2 2,8-3,0 моля на 1 моль H2S.
Изменение температуры не влияет на степень очистки нефти: за время контакта нефти с окислительным раствором (15÷120 мин) при 10÷60°С H2O2 расходуется полностью. Окисление гидросульфида и меркаптидов кальция происходит за 5-10 мин.
Пример 3. Опыты проводят как в примере 2, но количество Са(ОН)2 берут не выше 0,5 молей на 1 моль S2-, и для повышения рН в раствор дополнительно вводят другие щелочные агенты. Растворы Са(ОН)2 пониженной концентрации готовят путем разбавления 0,14%-ного раствора. Результаты опытов приведены в табл.3.
Сравнение опытов 5-7 табл.2 и опытов 2, 3 и 5-7 табл.3 показывает, что для очистки нефти от сероводорода вполне возможно использование смесей Ca(OH)2 с другими щелочными агентами. Однако для очистки нефти от меркаптанов эти смеси малоэффективны. При использовании смесей щелочных агентов требуется повышенный расход пероксида водорода.
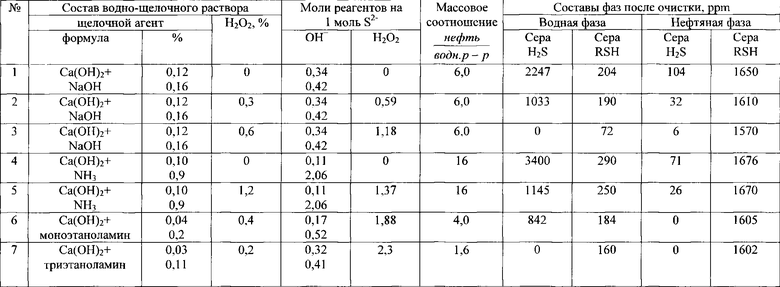
Пример 4. Исходный раствор Ca(OH)2 готовят как в примере 2, но без введения H2O2.. В качестве сырья используют нефть Оренбургского месторождения с содержанием 560 ppm сероводородной и 0,171% меркаптановой серы. Сероводород и низкомолекулярные меркаптаны экстрагируют из нефти путем контактирования щелочного раствора с сырьем. После отстаивания и отделения от очищенного сырья сульфидно-щелочной раствор анализируют на содержание сульфидной и меркаптидной серы и измеряют pH раствора. По результатам анализа в экстракт вводят расчетное количество пероксида водорода. Через 10 мин окисления при 22-25°C раствор анализируют еще раз. Результаты опытов приведены в табл.4.
В опытах 1 и 2 табл.4 для экстракции используют 0,14%-ный раствор Ca(OH)2, а в опытах 3-5 - известковое молоко. В опытах 6 и 7 в экстракты вводят дополнительное количество Ca(OH)2, эти растворы содержат небольшое количество нерастворенной извести. Растворение нерастворенной части извести происходит в процессе окисления.
Как видно из табл.4, при недостатке H2O2 достигается только частичная очистка экстракта от HS- и RS- (опыты 1 и 4). Неполная очистка имеет место также при недостатке щелочи (опыты 2 и 5); при недостатке щелочи окисление прекращается из-за перехода pH раствора в кислую область. Для удовлетворительной очистки требуется расход H2O2 не менее 1,5 моль на 1 моль HS-+RS- (опыты 3 и 7) и pH экстракта к концу процесса окисления более 7. pH экстракта снижается из-за расходования Ca(OH)2 на образование CaS2O3.
Пример 5. Очистка модельного раствора этилмеркаптана в толуоле.
Готовят два образца модельного раствора этилмеркаптана в толуоле с содержанием 388 и 1182 ppm меркаптановой серы. Готовят раствор с концентрацией Ca(OH)2 0,128% и суспензии с содержанием 0,16-0,56% Ca(OH)2. В делительную воронку объемом 100 см3, предварительно заполненную аргоном, берут 50 г модельного раствора, 20-30 г раствора Ca(OH)2 и расчетное количество раствора пероксида водорода. Содержимое воронки перемешивают в течение 1,5 мин и дают отстой до полного разделения фаз. Анализируют толуольную и водную фазы на содержание меркаптанов потенциометрическим методом. Результаты опытов приведены в табл.5.
Как видно из табл.5, экстракционная способность по отношению к этилмеркаптану растворов Ca(OH)2 выше, чем растворов NaOH той же концентрации: коэффициент экстракции при 22°C в опыте 1 Kэ=280:218=1,28; а в опыте 10 Kэ=130:322=0,4.
При одном и том же расходе H2O2 при использовании растворов Ca(OH)2 достигается более глубокая очистка модельного раствора от этилмеркаптана, чем при использовании растворов NaOH (опыты 3 и 11).
При достаточном количестве Ca(OH)2 (более 0,8 молей на 1 моль RSH) степень очистки улучшается с ростом расхода пероксида водорода. Удовлетворительная очистка достигается при расходе 1,5 моля H2O2 на 1 моль RS- (сравнение опытов 6 и 8), для полной очистки требуется не менее 3 молей H2O2 (опыт 9). При одном и том же расходе H2O2 степень очистки повышается с увеличением расхода Ca(OH)2 (опыты 6 и 7).
Пример 6. Очистка нефти Нурлатского месторождения и газоконденсата Карачаганакского месторождения (Казахстан) с использованием растворов, приготовленных из пластовой воды и раствора NaOH.
6.1. Приготовление исходных растворов.
Раствор №1 представляет собой пластовую воду, выделенную из сырой нефти на стадии обезвоживания и содержащую 11,8% NaCl и 3,1% CaCl2.
Раствор №2 представляет собой 0,5-5%-ный раствор NaOH.
Раствор №3 представляет собой 33%-ный водный раствор пероксида водорода.
6.2. Проведение опытов по очистке углеводородного сырья. В делительную воронку объемом 250 мл, предварительно заполненную аргоном, берут пробу 100 г нефти или газоконденсата, вводят расчетное количество воды и расчетные количества растворов №1, №2, №3. Воронку плотно закрывают пробкой, содержимое перемешивают встряхиванием в течение 3-5 мин и дают отстой: в течение 3-5 часов при очистке карбоновой нефти и 30 мин - при очистке газоконденсата. Длительный отстой при очистке нефти необходимо для полного разделения водной фазы от нефти и газоконденсата. Анализируют углеводородную и водную фазы на содержание сероводородной и меркаптановой серы.


При смешении пластовой воды и раствора NaOH происходит реакция:
CaCl2+2NaOH=Ca(OH)2+2NaCl
Так как пластовую воду и, соответственно, CaCl2 берут в избытке, NaOH расходуется полностью. В то же время на общую концентрацию гидроксильных ионов OH- в смеси эта реакция не влияет. В среде нефте-водяной смеси Ca(OH)2 в момент образования реагирует с H2S и NaHS с образованием Ca(HS)2, который легко окисляется пероксидом водорода.
Разбавление пластовой воды чистой водой необходимо для обессоливания углеводородного сырья.
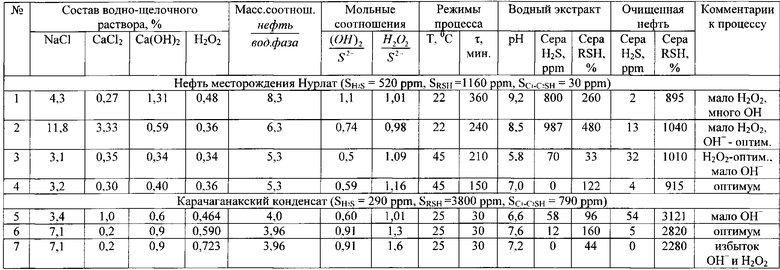
Результаты опытов по примеру 6 приведены в табл.6. В таблице приведены расчетные концентрации Ca(OH)2 при условии полного расходования NaOH на реакцию с CaCl2. Как следует из таблицы эти опыты по сути не отличаются от опытов табл.2, то есть содержащие CaCl2 пластовые воды могут быть использованы в качестве источника Ca(OH)2. В этом случае не требуется приготовление и хранение больших объемов растворов Ca(OH)2 (известкового молока) на нефтепромыслах. Объем растворов NaOH может быть в десять и более раза меньше, чем раствора извести. В зимнее время NaOH можно хранить в виде 18-25%-ных растворов, температура замерзания которых ниже минус 20°C.
В опытах 1-4 концентрация меркаптанов C1-C2 в очищенном сырье не превышала 10 ppm, а в опытах 6 и 7 - 40 ppm.(Норма по ГОСТ Р 51858 - 2002 - 40 ppm). Опыт 7 показывает возможность окисления меркаптанов C3 и выше. В опытах 1,3 и 4-7 концентрация хлоридов в очищенном сырье не превышало 220 мг/дм3. Снижение концентрации хлоридов до 100 мг/дм может быть достигнуто за счет увеличения количества добавляемой воды и улучшения качества сепарации сырья от отработанного водного раствора.
Пример 7. Утилизация отработанных сернисто-щелочных растворов. В отработанный водный раствор из опыта 7 табл.2 с pH 11,8 при перемешивании добавляют пластовую воду с pH 5 до достижения pH 7. Полученную смесь подают на станцию закачки пластовых вод.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Патент ФРГ 3151133, C10G 27/12. Verfahren zur Beseitigung von H2S aus Erdgas, Erdol und deren Gemischen / Schwarzer Hans Dr, Meisel Werner Dipl Ing, assignee Peroxid Chemic GMBH - №19813151133; заявл. 23.12.1981; опубл. 30.06.1983.
2. Патент РФ 2177494, C10G 27/04, 29/22. Способ очистки нефти и газоконденсата от сероводорода и меркаптанов / Шакиров Ф.Г., Мазгаров A.M., Вильданов А.Ф., Хрущева И.К. // заявл. 19.09.2000; опубл. БИ 2001, №36.
3. Патент РФ 2196804. Способ подготовки сероводородсодержащей нефти / Фахриев А.М., Фахриев Р.Ф. // заявл. 25.07.2001; опубл. БИПМ 2003, №2, С 439.
4. Патент РФ 2121491, 6 C10G 27/04, 29/02. Способ очистки нефти и газоконденсата от сероводорода и меркаптанов / Фахриев А М., Фахриев Р.А. // заявл. 02.12.1996; опубл. БИ 1998, №31.
5. Патент РФ 2146693, МПК C10G 27/06, 27/12. Способ очистки нефти и/или газоконденсата от сероводорода / Фахриев А М., Фахриев Р.А. // заявл. 16.03.1998; опубл. БИ 20.05.2000, №8.
6. Сахабутдинов Р.З., Шаталов А.Н., Гарифуллин P.M. и др. Подготовка и очистка нефтей от сероводорода // Казань: Изд-во «Ихлас», 2012, 162 с.
Изобретение относится к подготовке нефти, в том числе очистки от сероводорода и меркаптанов, и может быть использовано в газонефтедобывающей промышленности. Изобретение касается способа включающего стадии обессоливания и очистки от сероводорода и меркаптанов путем контактирования с водными растворами щелочных агентов, окисления образовавшихся гидросульфидов и меркаптидов 0,1-1,2%-ным раствором пероксида водорода, разделения углеводородной и водной фаз, в котором водный раствор содержит 0,02-1,0% гидрооксида кальция, до 0,95% гидроксида натрия, аммиака, аминов или их смесей. Технический результат - проведение дезодорирующей очистки с минимальными потерями углеводородов и с низкими энергетическими затратами непосредственно в промысловых условиях. 10 з.п. ф-лы, 6 табл., 6 пр.
1. Способ очистки нефти и газоконденсата от сероводорода и меркаптанов, включающий стадии обессоливания и очистки от сероводорода и меркаптанов путем контактирования водными растворами щелочных агентов, окисления образовавшихся гидросульфидов и меркаптидов 0,1-1,2%-ным раствором пероксида водорода, разделения углеводородной и водной фаз, отличающийся тем, что водный раствор содержит 0,02-1,0% гидрооксида кальция, до 0,95% гидроксида натрия, аммиака, аминов или их смесей.
2. Способ по п. 1, отличающийся тем, что водный раствор гидроксида кальция представляет собой известковое молоко (суспензию гидроксида кальция в насыщенном водном растворе гидроксида кальция).
3. Способ по п. 1, отличающийся тем, что водный раствор щелочных агентов содержит 0,1-1,2% пероксида водорода и контактирование нефти и газоконденсата с раствором щелочных агентов и окисление образовавшихся гидросульфидов и меркаптидов пероксидом водорода проводят одновременно в одной операции.
4. Способ по п. 1, отличающийся тем, что сначала из нефти или газоконденсата сероводород и низкомолекулярные меркаптаны экстрагируют водным раствором щелочных агентов, после сульфиды и меркаптиды в экстракте окисляют пероксидом водорода.
5. Способ по п. 1, отличающийся тем, что на 1 моль сероводорода и низкомолекулярных меркаптанов С1-С2 берут 0,3-1,5 моля щелочных агентов.
6. Способ по п. 1, отличающийся тем, что на 1 моль сероводорода и меркаптанов С1-С2 берут 0,5-3,5 моля пероксида водорода.
7. Способ по п. 1, отличающийся тем, что в качестве аминных щелочных агентов применяют моноэтаноламин, триэтаноламин и их смеси.
8. Способ по п. 1, отличающийся тем, что процессы контактирования и окисления проводят при температуре 0-65°С, предпочтительно при 10-30°С.
9. Способ по пп. 2 и 3, отличающийся тем, что водный раствор щелочных агентов готовят путем смешения водных растворов хлористого кальция и едкого натра.
10. Способ по п. 9, отличающийся тем, что в качестве водного раствора хлористого кальция используют пластовую воду.
11. Способ по п. 1, отличающийся тем, что водная фаза, содержащий хлориды, сульфиды, меркаптиды и продукты их окисления утилизируют путем смешения с кислыми пластовыми водами.
| СПОСОБ ОЧИСТКИ НЕФТИ И/ИЛИ ГАЗОКОНДЕНСАТА ОТ СЕРОВОДОРОДА | 1998 |
|
RU2146693C1 |
| СПОСОБ ОЧИСТКИ НЕФТИ, ГАЗОКОНДЕНСАТА ОТ СЕРОВОДОРОДА И МЕРКАПТАНОВ | 1996 |
|
RU2121491C1 |
| СПОСОБ ДЕЗОДОРИРУЮЩЕЙ ОЧИСТКИ НЕФТИ И ГАЗОКОНДЕНСАТА ОТ СЕРОВОДОРОДА И НИЗКОМОЛЕКУЛЯРНЫХ МЕРКАПТАНОВ | 2002 |
|
RU2213764C1 |
| WO 9325636 A1, 23.12.1993 | |||
| US 4548708 A, 22.10.1985 | |||
Авторы
Даты
2015-02-20—Публикация
2013-07-09—Подача