Изобретение относится к медицинской микробиологии и может быть использовано в вакцинно-сывороточном производстве для приготовления комбинированной инактивированной вакцины против Ку-лихорадки.
Известна живая вакцина против лихорадки Ку "М-44" (1), содержащая корпускулярный антиген из коксиелл Бернета, находящихся во втором фазовом состоянии. Однако невысокие протективные свойства коксиелл Бернета второй фазы и общие для всех живых вакцин недостатки (опасность контаминации вирусами, наличие тканевых примесей, сложность стандартизации препаратов и др.) ограничивают возможность ее применения.
Известна инактивированная вакцина, содержащая корпускулярный антиген из коксиелл Бернета первой фазы, обработанных трихлоруксусной кислотой (2). Однако она обладает недостаточными протективными свойствами. Хороший защитный эффект обеспечивает лишь 3-кратная иммунизация этим препаратом.
Известна инактивированная вакцина, содержащая корпускулярный антиген Бернета 1-й фазы, обработанный хлороформом и метанолом (3). Однако он также обладает недостаточной протективной активностью.
Наиболее близкой по сущности к предлагаемому изобретению является корпускулярная инактивированная вакцина, описанная в (4). Однако ее применение весьма ограничено, так как иммунизация этим препаратом в количествах, вызывающих надежную защиту лабораторных животных (100 мкг), обуславливает некрозы печени, спленомегалию и гепатомегалию.
Изобретение направлено на усовершенствование вакцины против Ку-лихорадки, при этом обеспечена высокая резистентность в отношении возбудителя Ку-лихорадки при использовании минимальных доз ингредиентов, что обеспечивает наибольшую иммунологическую безопасность.
Сущность изобретения сводится к следующему. Предлагаемая вакцина содержит три ингредиента, мкг:
Корпускулярный антиген из коксиелл Бернета (АГ) - 0,25 - 0,50
Корпускулярный антиген коксиелл Бернета, обработанный хлороформом и метанолом (АГ-ХМ) - 0,15 - 0,30
Экстракт из корпускулярного антигена коксиелл Бернета, полученный путем обработки корпускулярного антигена трихлоруксусной кислоты (АГ-ТХУ) - 5,00 - 10,00
Количественное содержание ингредиентов установлено авторами в результате экспериментальных исследований, исходя из необходимости получить требуемый результат.
В качестве вакцинного штамма применен штамм Луга-1 (коллекция коксиелл Всесоюзного музея риккетсиальных культур Института эпидемиологии и микробиологии им. Гамалеи АМН СССР N 102).
Корпускулярный антиген (АГ) получен из коксиелл Бернета штамма Луга-1. Инактивированные формалином коксиеллы очищали от тканевых примесей дифференциальным центрифугированием и обработкой эфиром. Растворимый антиген (АГ-ТХУ) получали путем обработки (АГ) трихлоруксусной кислотой по методу Brezina, Urvolgyi, 1962 (5). Антиген, лишенный фосфолипидного компонента (АГ-ХМ), оказывающего патогенное действие на лабораторных животных (3), получали путем обработки (АГ) смесью хлороформа и метанола по методу Lukacova M., Schramek S., 1988 (6).
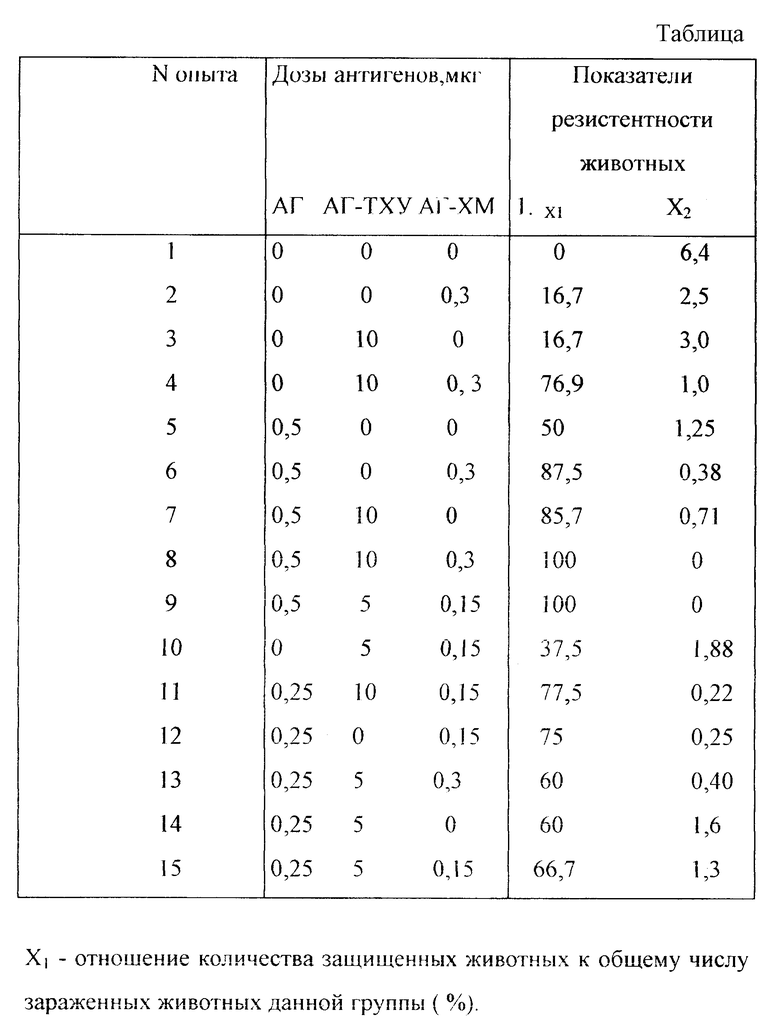
Все указанные ингредиенты были лиофильно высушены и стандартизированы с помощью иммуноферментной тест-системы для обнаружения антигенов коксиелл. С целью оценки протективных свойств каждого из этих препаратов с последующим определением оптимального состава вакцины, обеспечивающей эффективную защиту лабораторных животных при минимальных дозах ингредиентов АГ, АГ-ТХУ, АГ-ХМ, а также их двух и трехкомпонентных сочетаний, ресуспендировали в фосфатно-буферном растворе (pH 7,2 - 7,4) и вводили морским свинкам массой 325 - 350 г подкожно в строго дозированных количествах.
Через 28 - 30 дней после иммунизации животных внутрибрюшинно заражали суспензией коксиелл (штамм Henzerling, 1-я фаза) в дозе 10000 ИД в объеме 1 мл. Контрольная группа животных состояла из интактных морских свинок, зараженных той же дозой возбудителя, что и опытные животные.
О протективных свойствах исследуемых ингредиентов (или их сочетаний) судили по отношению защищенных животных к общему числу животных данной группы. Животное считали защищенным, если в его селезенке на 6 - 7 сутки после заражения (период максимального накопления возбудителя в этом органе) с помощью иммуноферментного анализа (ИФА) не были выявлены коксиеллы. Кроме того, сравнивали уровни резистентности животных, в селезенках которых были обнаружены коксиеллы. Результаты ИФА регистрировали в виде средних значений P-отрицательного логарифма титра при основании 2 в каждой группе животных.
Проводили две серии опытов. В первой из них сравнивали протективную активность однокомпонентных вакцин. С этой целью каждая группа животных, состоящая из 10 морских свинок, была иммунизирована одним из исследуемых ингредиентов. Животные разных групп были инокулированы 100 мкг, 10 мкг и 1 мкг каждого исследуемого антигена.
Установлено, что в селезенках всех неиммунизированных животных (контрольная группа также состояла из 10 морских свинок) были выявлены коксиеллы.
При сравнении одинаковых доз различных коксиеллезных препаратов показано, что наибольшей протективной активностью обладает АГ, затем АГ-ХМ и АГ-ТХУ.
Полученные данные свидетельствуют, что эффективная защита от заражения вирулентной культурой коксиелл возможна при инокуляции достаточно больших доз коксиеллезных монопрепаратов, потенциально вызывающих неблагоприятные поствакцинальные реакции, при этом обладающий наибольшей протективностью АГ обуславливает наибольшее патогенное действие на микроорганизм.
Примеры конкретного содержания ингредиентов усовершенствованной вакцины и показатели резистентности лабораторных животных приведены в таблице.
Источники информации
1. Гениг В. А. Аттенуированный вариант "М" риккетсий Бернета как возможная живая вакцина против Ку-лихорадки // Вестник АМН СССР. - 1960. - вып. 2. - С. 46 - 57.
2. Kazar J. , Brezina R., Palanova A., Turda B., Schramek S. Immunologeniciti and reactogenecity of a Q-fever chemavaccine in persons professionaly exposed to Q-fever in Czechoslovakia.//Bull. Wid. Hlth Org. 60, 1982. - p. 389 - 394.
3. Williams J.C., Cantrell J.L. Biological and immunological properties of Coxiella burnetii vaccines in C 57 Bl/10ScN endotoxinnonresponder mice // Inf. and Immun., 1982, - v. 35. - N 3. - p. - 1091 - 1102.
4. Kazar I., Rehacek I. Fever vaccines : prezent status and application in men. // Zbl. Bacteriol. Microbiol. Hyg., 1987. - v. - A267. - p. 74 - 78.
5. Brezina R., Urvolgyi I., Extract of Coxiella burnetii phase l antigen by means trichloracetic acid // Acta virol., 1961, N 5. - p. 193 - 196.
6. Lukacova M., Schramek S. Kineties of the extracthion of phospholipids from Coxiella burnetii // Acta virol., 1988. - v. 32. - p. 85 - 88.
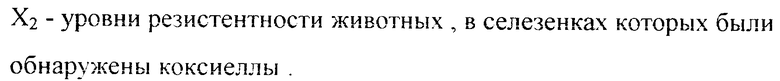
Изобретение относится к медицинской микробиологии и может быть использовано в вакцино-сывороточном производстве. Предлагаемая вакцина содержит три ингредиента: корпускулярный антиген из коксиелл Бернета 0,25 - 0,50 мкг, корпускулярный антиген коксиелл Бернета, обработанный хлороформом и метанолом 0,15 - 0,30 мкг, экстракт из корпускулярного антигена коксиелл Бернета, полученный путем обработки корпускулярного антигена трихлоруксусной кислотой 5,00 - 10,00 мкг. В качестве вакцинного штамма коксиелл Бернета используется штамм Луга-1. Изобретение позволяет получить высокую резистентность в отношении возбудителя Ку-лихорадки, при использовании минимальных доз ингредиентов, что обеспечивает наибольшую иммунобиологическую безопасность. 1 табл.
Инактивированная вакцина против Ку-лихорадки, содержащая корпускулярный антиген из коксиелл Бернета вакцинного штамма, отличающаяся тем, что она дополнительно содержит корпускулярный антиген Бернета, обработанный хлороформом и метанолом, и экстракт из коксиелл Бернета, полученный путем обработки корпускулярного антигена трихлоруксусной кислотой, а в качестве вакцинного штамма - штамм Луга-1 (коллекция коксиелл Всесоюзного музея риккетсиальных культур Института эпидемиологии и микробиологии им.Гамалеи АМН СССР N 102) при следующем соотношении ингредиентов, мкг:
Корпускулярный антиген из коксиелл Бернета штамма Луга-1 - 0,25 - 0,50
Корпускулярный антиген коксиелл Бернета штамма Луга-1, обработанный хлороформом и метанолом - 0,15 - 0,30
Экстракт из корпускулярного антигена коксиелл Бернета штамма Луга-1, полученный путем обработки корпускулярного антигена трихлоруксусной кислотой - 5,00 - 10,00
| RU 2062110 C1, 20.06.1996. |
Авторы
Даты
2001-05-27—Публикация
1999-07-13—Подача