Изобретение относится к области иммунологии и может найти применение в медицине, ветеринарии и биотехнологии при разработке и производстве новых вакцин.
Известны способы получения вакцин, при которых в их состав наряду с антигенами включаются вещества-стимуляторы иммуногенеза-адъюванты или иммуномодуляторы [1].
Наиболее близким по сущности к предлагаемому изобретению является способ получения вакцины, описанный в работе [2].
Указанный способ предусматривает включение в состав вакцины иммуностимулятора (адъюванта)-аминопроизводного фуллерена С60-сер. Указанный способ обеспечивает усиление иммуногенности овальбумина.
Недостатком указанного способа является то обстоятельство, что он не обеспечивает существенного иммуностимулирующего эффекта по отношению к многокомпонентным антигенным смесям, таким как экстракты из микробной биомассы, что было выявлено в наших специальных экспериментах.
Настоящее изобретение направлено на усовершенствование способа получения вакцины, содержащей фуллерен С60-сер в качестве адъюванта, а именно повышение иммуногенной активности вакцины, содержащей фуллерен С60-сер и антигенный экстракт из микробной биомассы. Разработанный способ обеспечивает действие фуллерена по отношению к многокомпонентным антигенным смесям экстракта из микробной массы.
Сущность изобретения сводится к следующему. Вакцину готовят посредством смешивания фуллерена С60-сер с антигенным экстрактом из биомассы микроба, предварительно обработанным периодатом натрия. Обработку антигенного экстракта осуществляют при его концентрации в реагентной смеси 0,5-1,5 мг/мл по содержанию общего белка, концентрации периодата 20-120 мМ и рН среды 5,0-6,0.
Антигенные экстракты из биомассы бактерий являются очень важными объектами научных исследований и практических работ [3, 4]. Необходимость в вакцинах, включающих в свой состав многокомпонентные антигенные экстракты из микробной массы, существует в большинстве областей микробиологии и экспериментальной иммунологии. Особенно важно создание таких вакцин против патогенов, которые не имеют какого-либо одного фактора патогенности или одного (или явно ведущего) протективного антигена. В связи с этим задача обеспечения существенного адъювантного действия фуллерена в отношении природных композиций антигенов (в частности, антигенных экстрактов из биомассы микробов) очень актуальна для научных исследований и практики получения активных иммунных сывороток против микробных патогенов. В перспективе - создание иммуногенных конструкций на основе природных антигенных составов может быть использовано при получении вакцины для людей, например для создания иммунитета против таких сложных патогенов, как Helicobacter pylori, Neisseria meningitidis и других.
Изобретение реализуется следующим образом.
ПРИМЕР 1. Получают вакцину из антигенов Helicobacter pylori (этиологического агента хронических гастритов и язвенной болезни желудка) и аминопроизводного фуллерена.
Получение антигенов Helicobacter pylori: готовят питательную среду для культивирования Helicobacter pylori (H.pylori): к расплавленному колумбийскому агару (Columdia Agar Base) стерильно добавляют лошадиную нормальную сыворотку до конечной ее концентрации 7% и раствор Iso Vitalex (Becton Dickinson Microbiology Systens) до конечной концентрации 1%. Агар разливают в чашку Петри и дают ему застыть.
Посев культуры Н. pylori на поверхность агара производят бактериальной петлей и распределяют нанесенный материал на поверхность агара стерильным стеклянным шпаделем. 4 чашки с посевом помещают в анаэростат системы GasPak 100 с газогенерирующим пакетом типа GasPak и выдерживают в термостате при 37±0,5oС 6 суток. Выросшие колонии H.pylori проверяют микроскопическим методом на чистоту культуры, снимают биомассу культуры стерильным стеклянным шпаделем и эмульгируют в 10 мл стерильного 0,15 М раствора NaCl, содержащего 0,01 М и фосфатного буферного раствора рН 7,2±0,1 (забуференный физиологический раствор - ЗФР). Биомассу осаждают центрифугированием (15 мин при +4oС и 6 тыс./об/мин). Надосадочную жидкость удаляют, а осадок биомассы ресуспендируют в 20 мл 0,1 М глицинового буферного раствора с рН 2,5, выдерживают при постоянном перемешивании на роторной мешалке при скорости вращения 5-10 об/мин. При температуре 20±5oС 10 мин. После этого биомассу культуры осаждают центрифугированием, как описано выше и отсасывают надосадочный слой, содержащий растворимый суммарный антиген H.pylori, осадок культуры удаляют. К надосадочному слою добавляют 1 м раствор NaOH до рН 5,0±0,1. При этом получают 20 мл раствора суммарного антигена H.pylori, содержащего 1,25 мг белка в 1 мл раствора. Его диализуют против 5 л 0,01 М фосфатного буферного раствора рН 5,0±0,1 и доводят общий объем ратвора антигена до 25 мл, добавляя 0,01 М фосфатный буферный раствор рН 5,0±0,1. В результате получают 25 мл суммарного антигена с концентрацией белка 1 мг/мл. Далее готовят четыре варианта вакцины:
10 мл полученного суммарного антигена отбирают для периодатной обработки: к ним добавляют 1,5 мл 800 мМ раствора периодата натрия в дистилированной воде, смесь выдерживают на роторной мешалке 30 мин при условиях, описанных выше. Затем реакционную смесь диализуют против 5 л ЗФР в течение 16 ч при 4±1oС. Диализированный раствор антигена разделяют на две части: к 5 мл его добавляют фуллерен С60-сер до конечной его концентрации 0,5 мг/мл.Получают вакцину по предлагаемому способу, готовую к применению, 5 мл обработанного периодатом антигена используют для иммунизации без фуллерена.
Оставшиеся 15 мл раствора суммарного антигена, необработанного периодатом, диализуют против 2 л ЗФР в течение 16 ч при 4±1oС. Диализованный раствор антигена разделяют пополам: к 5 мл его добавляют фуллерен С60-сер до конечной концентрации 0,5 мг/мл, получают вакцину согласно рототипу. Остальное количество необработанного периодатом антигена используют для иммунизации без фуллерена.
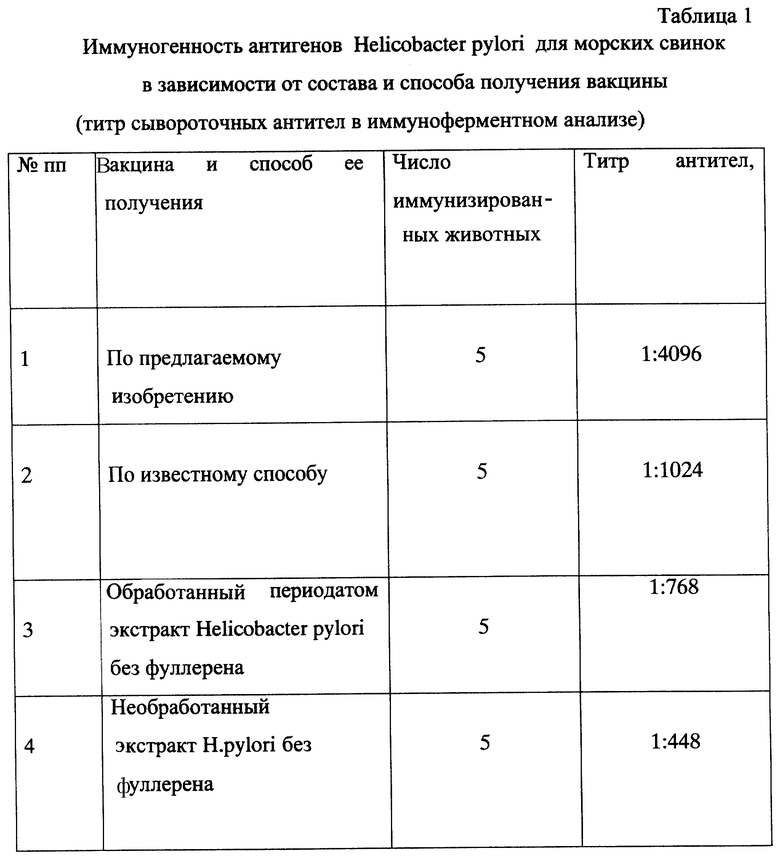
Иммунизаруют морских свинок (5 голов на каждый вариант вакцины). Каждому животному внутрибрюшинно вводят по 1 мл вакцины. Через 30 дней иммунизацию повторяют в тех же дозах. Через 14 дней после 2-й иммунизации получают сыворотку крови и исследуют в иммуноферментном анализе стандартным твердофазным методом в планшетах для иммулогических реакций. В качестве антигена сорбированного в лунках планшета используют суммарный необработанный периодатом антиген H.pylori, детекцию антител производят с помощью меченного пероксидазой белка А золотистого стафилококка - поливидового детектора Ig G.
Результат исследования иммунных сывороток сопоставляют с таковым для смеси 10 нормальных сывороток морских свинок, взятых в одном фиксированном разведении - 1:160 (контроль). Титром антител считают то наибольшее разведение иммунной сыворотки, при котором оптическая плотность продукта реакции еще превышает значение "контроля" в 2,5 раза и более.
Полученные результаты представляют в таблице 1. Из них следует, что предлагаемый способ получения вакцины имеет преимущество перед известным способом ее получения, а также перед нативным необработанным антигеном. Титр антител в крови животных, иммунизированных предлагаемой вакциной, существенно выше, чем при иммунизации другими испытанными вакцинами.
ПРИМЕР 2. Получают вакцину из антигенов Neisseria meningitidis - возбудителя гнойного менингита.
Культуру N. meningitidis серогруппы А выращивают на плотной питательной среде с нормальной лошадиной сывороткой в условиях анаэростата при 37±0,5oС. Микробную массу собирают через 24 ч после посева, суммарный антиген получают и обрабатывают периодатом натрия с помощью операций, описанных в примере 1.
Получают три варианта вакцины (см. табл.1-3):
Первый вариант согласно предлагаемому изобретению: вакцина содержит обработанный периодатом натрия суммарный антиген менингококка серогруппы А в концентрации 1 мг/мл по белку и 0,5 мг/мл фуллерена С60-сер.
Второй вариант согласно прототипу: вакцина содержит 1 мг/мл по белку необработанного антигена и 1 мг/мл фуллерена С60-сер.
Третий вариант: необработанный периодатом антиген без фуллерена.
Вакцины используют для иммунизации кроликов (по 3 кролика на каждый вариант вакцины). Вакцины вводят внутривенно в краевую вену уха в объеме 1,5 мл на кролика. Иммунизацию производят четырехкратно с интервалом 1 неделя. Через 14 дней после четвертой иммунизации получают сыворотку крови для исследования. Определяют титры антител к менингококковым антигенам серогруппы А в ИФА. В качестве антигена используют необработанный периодатом суммарный антиген менингококка серогруппы А. В качестве контрольной сыворотки применяют смесь сыворотки крови от 5 нормальных интактных кроликов в фиксированном разведении 1: 160.Расчет титров антител производят, как указано в примере 1.
Полученные результаты представляют в таблице 2. Из них следует, что предлагаемая вакцина, полученная предлагаемым способом, имеет преимущество - индуцирует существенно более высокие титры противоменингококковых антител, чем другие вакцины. Пример показывает, что изобретение реализуется не только с антигенами Helicobacter pylori, но и с антигенами бактерий другого биологического рода и вида.
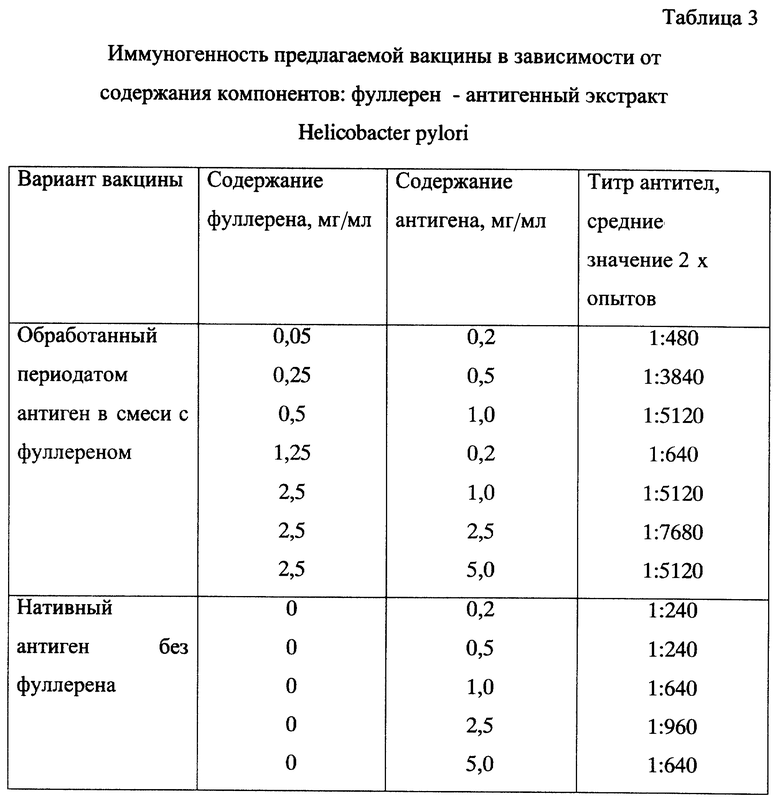
ПРИМЕР 3. Получают серию вариантов вакцин из антигенов H.pylori, варьируя концентрации фуллерена С60-cер от 0,05 до 2,5 мг/мл и концентрации антигена от 0,2 до 5,0 мг/мл и по содержанию белка. Иммунизируют морских свинок, как описано в примере 1. Получают данные, что существенные преимущества предлагаемого способа имеют место, начиная с концентраций антигена 0,5 мг/мл и выше и концентрации фуллерена С60-сер 0,25 мг/мл и выше: индуцируются антитела в титре 1: 3840, что существенно выше, чем при иммунизации нативным антигеном (1: 240), таблица 3. Эффект стимуляции антителегенеза наблюдается при увеличении концентрации фуллерена до 2,5 мг/мл по белку и концентрации антигена 2,5 мг/мл по содержанию белка.
ПРИМЕР 4.Получают антигены H.pylori (см.пример 1), обработанные разными концентрациями периодата натрия и в диапазоне рН 4,0-10,0.
Приготовленными вакцинами иммунизируют морских свинок (по 2 животных на вариант вакцины) в соответствии с условиями примера 1. Получают следующие результаты: эффективна обработка периодатом натрия при его минимальной концентрации в реагентной смеси. 20 мМ и содержании антигена (по концентрации белка) 0,5 мг/мл - титр антител выше в 3,5 раза, чем при использовании вакцины - прототипа с аналогичной концентрацией антигена. Эффективность обработки антигена сохраняется при увеличении концентрации антигена до 1,5 мг/мл и концентрации периодата до 120 мМ, дальнейшее увеличение его концентрации приводит к агрегации антигена и существенному снижению иммуногенности вакцины. Пример обосновывает рабочие концентрации и соотношения периодата и антигена при обработке последнего. Эффективна концентрация периодата 20-120 мМ при содержании антигена в реагентной смеси 0,5-1,5 мг/мл.
Иммуногенность вакцины существенно улучшается по сравнению с известной вакциной, если обработку антигенов периодатом проводят при рН 5,0-6,0. Варианты вакцины, в которых использованы антигенные экстракты, обработанные периодатом при рН среды ниже 5,0 - выше 6,0 существенно не отличаются от известной вакцины по параметру иммуногенности.
Источники информации
1. Петров Р. В. , Хаитов P.M., Атауллаханов Р.И. Иммуногенетика и искусственные антигены. - М.: Медицина 1983/
2. Патент РФ 2129436. Опубл.Б.И.,1999, 12.
3. Goodwin C.S. e.a. J. Infect Dis., 1987, 3 155, 488-494.
4. Kosunn T.U. e.a. Eur. J. Infect, 1983,11: 189-91.

Изобретение относится к области иммунологии и может найти применение в медицине, ветеринарии и биотехнологии. Изобретение направлено на усовершенствование способа получения вакцины, содержащей фуллерен С60-сер в качестве адъюванта. При этом обеспечено существенное (адъювантное) иммуностимулирующее действие фуллерена по отношению к антигенным экстрактам из биомассы бактерий. Способ предусматривает обработку антигенного экстракта из биомассы микроба периодатом натрия при его концентрации 0,5-1,5 мг/мл по содержанию общего белка и концентрации периодата натрия 20-120 мМ/мл в реагентной смеси при рН среды 5,0-6,0. В качестве адъюванта используют фуллерен С60-сер. Способ позволяет значительно повысить иммуногенность вакцины. 1 з.п. ф-лы, 3 табл.
| АДЪЮВАНТЫ | 1997 |
|
RU2129436C1 |
| ИВАНОВ Б.Б., Создание иммунопотенциирующих систем для пептидных экспериментальных вакцин | |||
| Автореф | |||
| дисс | |||
| на соиск | |||
| уч.степ | |||
| канд.биол | |||
| наук | |||
| - М., 1992. | |||
Авторы
Даты
2002-07-10—Публикация
2000-12-07—Подача