Изобретение относится к области биотехнологии и может быть использовано в микробиологической промышленности для производства ферментных препаратов, применяемых в легкой промышленности и в сельском хозяйстве, где требуется гидролиз нативного кератина.
Кератиноподобные белки нерастворимы и устойчивы к деградации обычными протеолитическими ферментами из-за большого количества дисульфидных и водородных связей, гидрофобных взаимодействий. От других белков они отличаются высоким содержанием цистина, количество которого может достигать более 8% от веса белка (1). Кератин входит в состав волос, шерсти, шелка, перьев, рогов, ногтей и копыт.
Кератиназы широко применяются для утилизации перьев на птицеводческих фермах. Полученные с помощью кератиназ гидролизаты перьев используются в птицеводстве и животноводстве, частично заменяя рыбную и мясную муку в кормах. Причем по питательности и усваиваемости ферментативные гидролизаты значительно превосходят муку из перьев и продукты ее обработки химическими и механическими способами (2).
Микробные кератиназы используются для мягчения мяса и рыбы, при получении клея, создании косметических продуктов (питательных кремов, лосьонов); в производстве пищевого и кормового белка. Весьма эффективно применение кератиназ в медицине для приготовления диагностических сред, лечебных сывороток и вакцин, а также при производстве чистящих средств для удаления белковых загрязнений с натуральных тканей (3, 4).
Наиболее широко кератиназы применяются в кожевенной промышленности, прежде всего на стадии обезволаживания. При обработке шкур необходимо удалить верхний слой кожи - эпидермис и шерсть. Для этого разрушают дисульфидные связи в молекулах структурных белков с помощью щелочи, сульфидов и других химических агентов. Применение кератиназ значительно сокращает время и стоимость обезволашивания, упрощает общую схему обработки шкур и позволяет получить более качественные виды кож. Кератиназы используют в комплексе с другими сериновыми протеазами на стадиях замачивания, известкования и мягчения шкур (5). Запатентованы специальные препараты для обезволаживания, состоящие из смеси ферментов, выделенных из плесневых грибов, стрептомицетов и бактерий рода Bacillus.
Кератинолитическая активность обнаружена в ряде микроорганизмов, в частности стрептомицетах (Streptomyces Sp. A11, Streptomyces pactum DSM 40530, Streptomyces fradiae, Streptomyces sp. S. K1-02, Streptomyces ornatus, Streptomyces chromogenes s. graecus ЛИА 0832, Streptomyces lavendulae ВКПМ s-910(6-12)) и грибах (Microsporum canis, Microsporum gypseum, Microsporum fulvum, Dermatophilus congolensis, Aspergillus fumigatus fresenius, Trichophyton mentagrophytes, Trichophyton simii, Trichophyton schoenleinii, Chrysosporum georgiae, Scopulariopsis brevicaulis (13-21).
Недостатками вышеперечисленных продуцентов являются низкая продуктивность и сложность способа культивирования. Кроме того, микроорганизмы рода Microsporum, Dermatophilus и Trichophyton являются патогенными и не могут использоваться для промышленного получения ферментных препаратов.
Известен штамм Bacillus species No АН-101, продуцирующий щелочную кератиназу с оптимальным рН действия 12-13, которая специфично гидролизует кератин человеческого волоса (22). Данный микроорганизм выращивают при 37oС в течение 56 ч на достаточно сложной среде, содержащей растворимый крахмал, желатин, дрожжевой экстракт и набор неорганических солей, рН среды доводят до 9,5 добавлением NaHCO3. Активность кератиназы Bacillus species No АН-101 высока, но недостаточна для промышленного внедрения фермента.
Штаммы Bacillus licheniformis OWU 138В (4) и Bacillus licheniformis OWU 88B (4), выделенные из перьев диких птиц, продуцируют, главным образом, β-кератиназу, избирательно расщепляющую кератин перьев и практически не действующую на кератин шерсти животных.
В патенте не приводится количественная оценка кератинолитической активности штаммов и оптимальные условия действия кератиназы.
Наиболее близким к заявляемому штамму по совокупности существенных признаков и достигаемому результату аналогом является штамм Bacillus licheniformis PWD-1, ATCC No. 53757 (23). При культивировании на среде, содержащей 1% перьевой пудры, при 45oС в течение 96 часов, синтезирует кератиназу в количестве 25 ед/мл. Очищенная кератиназа гидролизует широкий спектр субстратов: казеин, порошок из перьев, эластин, коллаген. Фермент стабилен при рН от 5 до 12 с оптимумом действия на порошок из перьев и казеин - 8,5 и от 10,5 до 11,5 соответственно; оптимальная температура действия - 50-55oС.
Штамм не обладает достаточно высокой кератинолитической активностью, что усложняет процесс получения высокоактивных препаратов.
Задачей, на решение которой направлено изобретение, является получение нового высокопродуктивного штамма-продуцента кератиназы.
Технический результат, который может быть получен при осуществлении изобретения, заключается в повышении кератинолитической активности штамма и сокращении длительности процесса культивирования.
Сущность изобретения - специально селекционированный штамм Bacillus licheniformis - 99 - продуцент кератиназы.
Штамм Bacillus licheniformis - 99 депонирован во Всероссийской коллекции микроорганизмов при Институте биохимии и физиологии микроорганизмов РАН под N ВКМ В-2220 Д.
Штамм Bacillus licheniformis ВКМ В-2220 Д получают с помощью многоступенчатой генетической селекции с применением методов эффективного мутагенеза - ультрафиолетового облучения с одновременным воздействием химических мутагенов из штамма Bacillus licheniformis - 78 ВКМ В-2184Д.
Условия хранения: штамм может храниться в лиофилизированном состоянии в течение нескольких лет или на косяках с агаризованной средой следующего состава: мясопептонный бульон (1 часть), растворимый крахмал - 1,0%; агар-агар - 2,0%; рН среды 7,4-7,6; при 4oС в течение 6 лет с обязательным пересевом не реже одного раза в 2 месяца на эту же среду.
Характеристика штамма
Культурально-морфологические признаки
Клетки представляют собой грамположительные, одиночные подвижные палочки размером 0,6-0,8 и 0,2-0,3 мкм, спорообразующие. В логарифмической фазе роста образуются цепочки из 2-3-х клеток более вытянутой формы, к 56 часам роста (стационарная фаза) цепочки распадаются, клетки утолщаются, появляются споры, имеющие центральное положение и овальную форму.
Мясопептонный агар (t 40oС, 24 часа)
Штамм дает нормальный средний рост, колонии неправильной формы с приподнятым центром, слизистые, гладкие, непрозрачные, 2-5 мм в диаметре, в процессе роста постепенно приобретают светло-коричневый пигмент.
Мясопептонный бульон (t 40oС, 24 часа)
Средний рост клеток, в процессе роста среда мутнеет, к 24 часам роста появляется светло-коричневый оттенок.
Агаризованная среда с казеином или микробными клетками
Нормальный рост и образование зон гидролиза вокруг колоний.
Колонии неправильной формы, слизистые, гладкие, непрозрачные с приподнятым центром, 2-4 мм в диаметре, с ровными краями. К 72 часам роста появляются споры на всей поверхности колонии, цвет спор - светло-коричневый, переходящий к 120-144 часам роста в темно-коричневый.
Физиолого-биохимические свойства
Аэроб.
Температурный диапазон роста - 10-55oС.
Оптимальная температура роста - 40o С.
Растет при значениях рН среды - 5,0-10,0.
Оптимум рН роста - 7,3-7,8
Желатин разжижает. Крахмал, казеин и перьевую пудру быстро гидролизует.
Восстанавливает лакмусовое молоко.
Нитраты восстанавливает до нитритов. Образует тирозиназу (каталазоположительный), образует сероводород. Вызывает гемолиз.
Сбраживает с образованием кислоты арабинозу, ксилозу, фруктозу, маннозу, маннит, сорбит, глицерин, декстрин, гликоген без выделения газа, глюкозу ферментирует анаэробно, утилизирует лимонную кислоту.
Штамм способен расти на средах с аммонийными солями в качестве единственного источника азота, а также на среде, содержащей дрожжевые клетки (прессованные пекарские дрожжи, кормовые дрожжи или белково-витаминный комплекс БВК), как источник углеродного и азотного питания.
На основании указанных свойств штамм ВКМ В-2220 Д идентифицирован по определителю Берги ("Краткий определитель Берги. "Мир", М. , 1980. Под ред. Дж. Хоулта) как штамм Bacillus licheniformis.
Вид Bacillus licheniformis, к которому отнесен штамм, отсутствует в списках патогенных бактерий по Положению Минздрава и в списках патогенных бактерий в Official Journal of the European Communities NC 217/3237, 24.08.92.
Полученный мутант по своим морфологическим свойствам отличается от исходного более слабым спороношением, цветом пигмента спор, а также более коротким циклом роста и образованием меньшего количества биомассы при глубинном культивировании.
Штамм Bacillus licheniformis ВКМ В-2220 Д обладает повышенной способностью к биосинтезу кератиназы и продуцирует не менее шести внеклеточных ферментов, в том числе протеазу и α-амилазу, которые усиливают гидролизующий эффект кератиназного препарата.
При изучении морфологической изменчивости наблюдали выщепление при рассеве штамма на селективных средах 3-5% нетипичных колоний, что свидетельствует о стабильности культуры, а следовательно, о стабильности к продукции кератиназы при длительном культивировании.
Культивирование штамма осуществляют в аэробных условиях при температуре 40oС в течение 48-72 часов, рН среды 7,5-7,8. Для роста культуры и биосинтеза кератиназы источником углерода и азота могут служить крахмал, гидролизованный крахмал, кукурузная, соевая или другая зерновая мука, либо их экстракты, дрожжевые клетки, пептон, дрожжевой экстракт, казеин, перьевая мука, мочевина, аммонийный азот.
Для ферментативной обработки перьевой муки при производстве кормов и при обезволашивании шкур в кожевенном производстве ферментный препарат может быть использован в виде культуральной жидкости или в виде концентрированных препаратов, получаемых известными биохимическими методами, например осаждением этанолом из ультрафильтрата культуральной жидкости.
Кератиназа активна в широком диапазоне рН - от 5,5 до 10,0 с оптимумом при рН 7,5; в диапазоне температуры от 30 до 70oС, с оптимумом при 50oС.
Период полной стабильности фермента при 70oС - 10 мин, при рН 10 и температуре 60oС сохраняет 60% активности.
Возможность использования изобретения иллюстрируется примерами, которые не ограничивают объем и сущность притязаний, связанных с ними.
Пример 1. Посевной материал (инокулюм) получают выращиванием штамма Bacillus licheniformis BKM В-2220 Д на жидкой питательной среде состава: казеин - 1%; мясопептонный бульон и солодовое сусло в соотношении 1: 1, рН среды 7,5. Культивирование проводят в колбах, содержащих 50 мл стерильной среды, на качалке с 240 об/мин при 40oС в течение 24 часов.
Полученный посевной материал в количестве 0,3% к объему среды вносят в качалочные колбы объемом 750 мл, содержащей 50 мл среды состава, г/л: кукурузная мука- 120,0; соевая мука - 10,0; СаСО3 - 2,5; MgSO4•7H2О - 2,5; рН среды 7,5-7,8.
Культивирование штамма осуществляют в аэробных условиях при температуре 40oС и рН среды 7,5-7,8. Каждые 24 часа, начиная с 48 часов роста, отбирают пробы, в которых определяют способность культуральной жидкости гидролизовать кератин, крахмал, казеин.
Активность кератиназы определяют с использованием в качестве субстрата Азо-Кератина. Гидролиз проводят при 50oС и рН 7,5 в течение 30 мин. Реакцию останавливают добавлением 10%-ной ТХУ. В отфильтрованных супернатантах измеряют оптическую плотность при длине волны 450 нм.
За единицу активности кератиназы принимают увеличение оптической плотности на 0,01 за 30 мин при 50oС, рН 7,5.
Максимальная кератинолитическая активность в культуральной жидкости на 72 часа роста составляет 96000 ед/мл.
Пример 2. Способ осуществляют, как в примере 1, но вместо кукурузной муки среда содержит экструдат кукурузной муки в количестве 100,0 г/л и порошок из перемолотых перьев в количестве 10 г/л.
Максимальная кератинолитическая активность в культуральной жидкости на 72 часа роста составляет 117000 ед/мл.
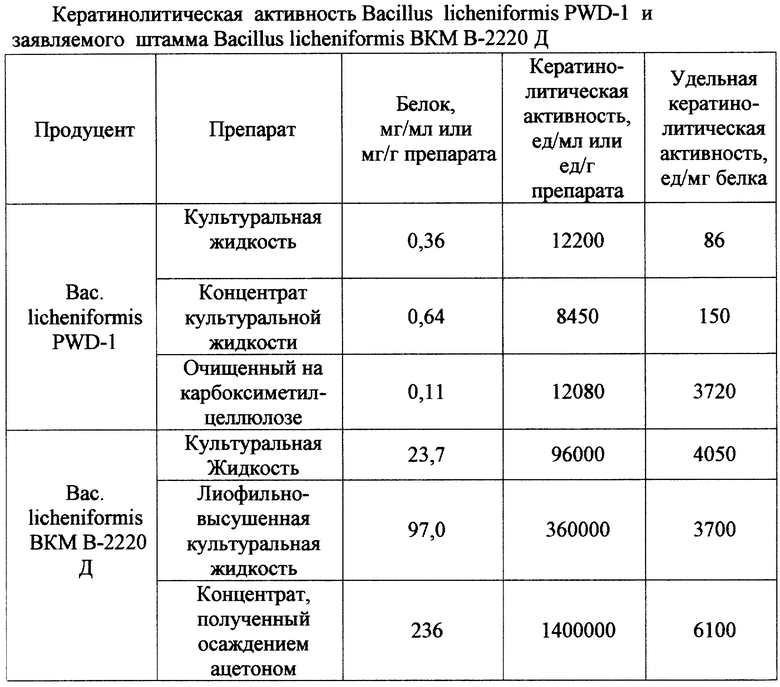
В таблице приводятся сравнительные данные по кератинолитической активности Bacillus licheniformis PWD-1 и заявляемого штамма Bacillus licheniformis ВКМ В-2220 Д при культивировании их в идентичных условиях.
Таким образом, предлагаемый штамм Bacillus licheniformis ВКМ В-2220 Д позволяет значительно повысить кератинолитическую активность в культуральной жидкости и сократить длительность процесса культивирования.
Источники информации
1. Гауровиц Ф. Химия и функции белков. /Под ред. Шпикитера В. О. М. : Мир, 1968. С. 252-257.
2. Dhar SC. , Sreenivasulu. // Leather Science, vol. 31 (10), 1984. P. 261-267.
3. Гребешова Р. Н. , Сальседо-Торрес Л. Э. , Идальго М. А. // Прикладная биохимия и микробиология. 1999, том 35, 2. С. 150-154.
4. Патент США 5877000. Опубл. 02.03.1999 г.
5. Pfleider, E. & R. Reiner. 1988. Microorganisms in processing of leather, p. 730-739. In H. J. Rehm (ed. ), Biotechnology, vol. 6b. Special microbial processes. VCH Verlagsgeselschaft mbH, Weinheim, Germany.
6. Mukhopadhyay RP. , Chandra AL. // Indian J. Exp Biol. 1990, Jun. 28(6). P. 575-577.
7. Bockle B. , Calunsky B. , Muller R. // Appl. Environ Microbiol. 1995, Oct. 61(10). P. 3705-10.
8. Galas E. , Kaluzewska M. // Acta Microbiol Pol. 1992, 41(3-4). P. 169-177.
9. Letourneau F. et al. // Lett Appl Microbiol. 1998, Jan. 26(1). P. 77-80.
10. Патент РФ 2034924. Опубл. 10.05.1995.
11. Авторское свидетельство СССР 1565888. Опубл. 23.05.1990.
12. Авторское свидетельство СССР 1788010. Опубл. 15.01.1993.
13. Mignon B. et al. // Med Mycol. 1998, Dec. 36(6). P. 395-404.
14. Malvivya HK. et al. // Indian J. Exp Biol. 1992, Feb. 30(2). P. 103-106.
15. Hanel H. et al. // Med Microbial Immunol. 1991, 180(1). P. 45-51.
16. Santos RMDB et al. // Curr Microbiol. 1996, Dec. 33(6). P. 364-370.
17. Siesenop U, Bohm KH. // Mycoses. 1995, May-Jun. 38(5-6). P. 205-209.
18. Singh CJ. // Mycopathologia. 1997, 137(1). P. 13-16.
19. Qin Lm, Dekio S, Jidoi J. // Zentral Bakteriol. 1992, Jul. 277(2). P. 236-244.
20. El-Naghy MA et al. // Mycopathologia. 1998, 143(2). P. 77-84.
21. Malvivya HK. et al. // Mycopathologia. 1997, Sep. 119(3). P. 161-165.
22. Takami H et al. // Biosci. Biotech. Biochem. 1992, 56(10), 1667-1669.
23. Патент США 5171682. Опубл. 15.12.1992.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ БАКТЕРИЙ BACILLUS LICHENIFORMIS - ПРОДУЦЕНТ КОМПЛЕКСА ТЕРМОСТАБИЛЬНЫХ АМИЛОЛИТИЧЕСКИХ И ПРОТЕОЛИТИЧЕСКИХ ФЕРМЕНТОВ | 1998 |
|
RU2177995C2 |
| ШТАММ БАКТЕРИЙ BACILLUS LICHENIFORMIS-ПРОДУЦЕНТ ЩЕЛОЧНОЙ ПРОТЕАЗЫ | 2005 |
|
RU2303066C1 |
| ШТАММ БАКТЕРИЙ BACILLUS LICHENIFORMIS ВКМ В-2396 D - ПРОДУЦЕНТ ТЕРМОСТАБИЛЬНОЙ АЛЬФА-АМИЛАЗЫ | 2006 |
|
RU2324734C1 |
| Штамм бактерий Bacillus licheniformis - продуцент кератиназы | 2023 |
|
RU2812484C1 |
| ШТАММ МИЦЕЛИАЛЬНОГО ГРИБА ASPERGILLUS AWAMORI - ПРОДУЦЕНТ ГЛЮКОАМИЛАЗЫ | 2000 |
|
RU2196821C2 |
| ШТАММ МИЦЕЛИАЛЬНОГО ГРИБА ASPERGILLUS AWAMORI - ПРОДУЦЕНТ ГЛЮКОАМИЛАЗЫ | 2002 |
|
RU2245364C2 |
| ШТАММ МИЦЕЛИАЛЬНОГО ГРИБА ASPERGILLUS ORYZAE - ПРОДУЦЕНТ КИСЛОЙ АЛЬФА-АМИЛАЗЫ | 2007 |
|
RU2354697C2 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАТИНАЗЫ ИЗ Penicillium citrinum | 2012 |
|
RU2499833C1 |
| ШТАММ БАКТЕРИЙ BACILLUS MACERANS BKM B-2419D - ПРОДУЦЕНТ ПЕКТАТЛИАЗЫ, ПЕКТИНЛИАЗЫ И ПОЛИГАЛАКТУРОНАЗЫ И КОМПЛЕКСА ЩЕЛОЧНЫХ КАРБОГИДРАЗ, СОДЕРЖАЩЕГО КСИЛАНАЗУ, БЕТА-ГЛЮКАНАЗУ, ГАЛАКТОМАННАНАЗУ, АРАБИНАЗУ, КСИЛОГЛЮКАНАЗУ И АМИЛАЗУ | 2006 |
|
RU2323974C1 |
| СПОСОБ ПРОИЗВОДСТВА ПРОБИОТИЧЕСКОГО ПРЕПАРАТА НА ОСНОВЕ СПОРООБРАЗУЮЩИХ ШТАММОВ Bac. subtilis И Bac. licheniformis | 2010 |
|
RU2432393C1 |
Изобретение относится к биотехнологии и может быть использовано в птицеводстве и животноводстве, а также в кожевенной и пищевой отраслях промышленности. Штамм Bacillus licheniformis-99 получен многоступенчатой генетической селекцией с применением ультрафиолетового облучения с одновременным воздействием химических мутагенов. Штамм депонирован во Всероссийской коллекции микроорганизмов при Институте биохимии и физиологии микроорганизмов им. Г. К. Скрябина РАН под номером ВКМ В-2220 Д. Для роста культуры и биосинтеза кератиназы источником углерода и азота могут служить крахмал, гидролизованный крахмал, кукурузная, соевая или другая зерновая мука, либо их экстракты, дрожжевые клетки, пептон, дрожжевой экстракт, казеин, перьевая мука, мочевина, аммонийный азот. Штамм обладает высокой кератинолитической активностью, что позволяет получать высокоактивные препараты кератиназы. 1 табл.
Штамм бактерий Bacillus licheniformis BKM В-2220Д (Всероссийская коллекция микроорганизмов при ИБФМ им. Г. К. Скрябина РАН) - продуцент кератиназы.
| US 5171682, 15.12.1992 | |||
| US 4959311, 25.09.1990 | |||
| US 5712147, 27.01.1998 | |||
| US 5877000, 02.03.1999 | |||
| ШТАММ STREPTOMYCES ORNATUS - ПРОДУЦЕНТ КЕРАТИНАЗЫ | 1993 |
|
RU2034924C1 |
Авторы
Даты
2002-01-10—Публикация
2000-01-17—Подача