Данное изобретение относится к способу получения производного камптотецина, представленного следующей общей формулой I:
или его фармацевтически приемлемой соли,
где Y и Z - одинаковы или различны и каждая группа представляет собой атом водорода, C1-С6алкил-, C1-С3гидроксиалкилгруппу или обычную защитную аминогруппу, например бензилоксикарбонил-, бензилгруппу и т.д.;
R1 - атом водорода, C1-С6алкил- или гидроксигруппа;
R2 и R3 - одинаковы или различны и каждая представляет собой атом водорода или гидроксигруппу, или они могут связываться, образуя циклический фрагмент - метилендиокси- или этилендиоксигруппу;
R4 - атом водорода или C1-С6алкилгруппа;
R5 - атом водорода, гидроксигруппа, атом фтора, хлора, брома или йода или аминогруппа.
Предпосылки изобретения
Со времени первого выделения камптотецина из древесины и коры Camptotheca acuminata, Wall с сотр. [М.Е. Wall et a., J. Am. Chem. Soc. 88, 3888 (1966)] , было предпринято много попыток синтезировать камптотецин. Однако применение камптотецина в качестве эффективного противоопухолевого препарата было неудачным вследствие его сильной токсичности, показанной в клинических исследованиях в 1970 году. Впоследствии Liu с сотр. в 1985 году сообщали, что комптотецин обладает специфическим методом действия в ингибировании топоизомеразы I. Таким образом, значительный интерес был сосредоточен на данном соединении.
Для того чтобы уменьшить токсичность камптотецина и способствовать усилению его противоопухолевой активности, в последнее время были предприняты различные исследования по созданию производных камптотецина. Среди названных исследований клиническая проверка СРТ-11 (иринотекана), синтезированного в Японии компанией Yakurt-Honsha Co. в 1986 году, показала, что он обладает превосходной противоопухолевой активностью и меньшей токсичностью (Japanese Patent Laid Open Publication No. 64-61482); исследования продолжались другими фармацевтическими компаниями, такими как SmithKline Beecham (топотекан) и Glaxo (MDO-камптотецин и 9-аминокамптотецин). Среди них начаты исследования СРТ-11 и топотекана.
С другой стороны, создатели данного изобретения сообщали в Корейских патентных заявках (Korean Patent Applications No. 95-269 и 96-248) о производных 7-аминоэтилкамптотецина, которые обладают сильной противоопухолевой активностью, слабой токсичностью и обширной областью безопасности, и способе их получения посредством полного (тотального) синтеза.
В вышеупомянутом изобретении описано получение производных камптотецина, которые обладают сильной противоопухолевой активностью. Однако способ получения их является сложным, поскольку принят полный синтез и поскольку используемое промежуточное вещество является новым соединением. Следовательно, имелась определенная необходимость в создании простого и удобного способа получения производных камптотецина для серийного производства.
Таким образом, авторы изобретения предложили удобный способ, с помощью которого производные камптотецина, обладающие превосходной активностью, могут быть получены из соединения общей формулы II, например, (S)-7-метилкамптотецина [S. Sawada et a., Chem. Pharm. Bull., 39 (1991) 2574-2580]. Таким образом, было завершено данное изобретение.
Изложение изобретения
Способ получения производного камптотецина или фармацевтически приемлемой соли его описан более подробно, как это изложено ниже в соответствии с осуществлением на практике данного изобретения.
Способ получения производного камптотецина или его фармацевтически приемлемой соли согласно данному изобретению заключается в получении соединения общей формулы I по реакции Манниха, т.е. соединение общей формулы II реагирует с амином или его солью и с источником формальдегида в присутствии кислоты (схема 1).
Схема 1

где Y и Z - одинаковы или различны и каждая группа представляет собой атом водорода, C1-С6алкил-, C1-С3гидроксиалкилгруппу или обычную защитную аминогруппу, например бензилоксикарбонил-, бензилгруппу и т.д.;
R1 - атом водорода, C1-С6алкил- или гидроксигруппа;
R2 и R3 - одинаковы или различны и каждый представляет собой атом водорода или гидроксигруппу, или они могут связываться, образуя циклический фрагмент - метилендиокси- или этилендиоксигруппу;
R4 - атом водорода или С1-С6алкилгруппа;
R5 - атом водорода, гидроксигруппа, атом фтора, хлора, брома или йода или аминогруппа;
R1, R2, R3, R4, R5 и Y предпочтительно представляют собой-атомы водорода;
Z - изопропильная группа.
Примеры источников формальдегида включают раствор формалина, параформальдегид (полиоксиметилен), триоксан, диметилсульфоксид и т.д.
Применяемый амин включает первичные или вторичные амины, такие как метиламин, этиламин, пропиламин, изопропиламин, бутиламин, пентиламин, гексиламин, бензиламин, изопропилбензиламин, диметиламин, диэтиламин, бензилоксикарбониламин, гидроксиметиламин, гидроксиэтиламин, гидроксипропиламин и тому подобное.
В данной реакции растворителями являются вода, метанол, этанол, диоксан, уксусная кислота, диметилформамид, диметилсульфоксид и тому подобное. Применяемые кислоты включают соляную, серную, уксусную, фосфорную, n-толуолсульфокислоту, метансульфокислоту, трифторметансульфокислоту, трифторид бора, хлорид олова и тому подобные. Реакцию проводят при температуре 20-150oС.
Согласно данному изобретению фармацевтически приемлемые соли соединений, представленных общей формулой I, являются солями неорганических кислот, например гидрохлоридами, сульфатами, фосфатами и т.д. или солями органических кислот, например n-толуолсульфонатами, ацетатами, метансульфонатами, трифторсульфонатами и т.д.
Оптимальный способ осуществления изобретения
Данное изобретение иллюстрируется более подробно с помощью следующих примеров, но формула изобретения этими примерами не ограничивается.
Пример 1. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил]камптотецина
(S)-7-метилкамптотецин (8 г, 0,0221 моль), изопропиламин (3,91 г, 0,0662 моль) и концентрированную соляную кислоту (6,93 мл, 0,0684 моль) прибавляли к диметилсульфоксиду (80 мл). Реакционную смесь перемешивали при 140oС в течение одного часа, затем охлаждали до комнатной температуры и растворитель удаляли отгонкой под пониженным давлением. Таким образом, полученный остаток очищали с помощью "флеш" колоночной хроматографии с метиленхлористый: метанол = 10:1 с получением целевого продукта (6,75 г, 65%) в виде светло-желтого твердого вещества.
1H ЯМР (DMSO-d6, 400 MHz), δ, м.д.:
9,29 (уш. с, 1Н), 8,39 (д, 1Н, J=8,3 Гц), 8,13 (д, 1Н, J=8,3 Гц), 7,83 (т, 1Н, J=7,1 Гц), 7,72 (т, 1Н, J=7,1 Гц), 7,29 (с, 1Н), 6,52 (с, 1Н), 5,43 (с, 2Н), 5,37 (с, 2Н), 3,64-3,60 (м, 2Н), 3,45-3,34 (м, 1Н), 3,20-3,14 (м, 2Н), 1,92-1,82 (м, 2Н), 1,27 (д, 6Н, J=6,4 Гц), 0,87 (т, 3Н, J=8,0 Гц).
Пример 2. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил]камптотецина
(S)-7-метилкамптотецин (8 г, 0,0221 моль) и изопропиламин (3,91 г, 0,0662 моль) добавляли поочередно к смешанному раствору формалина (37%, 9,73 мл, 0,12 моль) и концентрированной соляной кислоты (6,93 мл, 0,0684 моль). Реакционную смесь перемешивали при кипячении в течение 12 часов и затем охлаждали до комнатной температуры. Растворитель удаляли отгонкой при пониженном давлении и таким образом полученный остаток очищали "флеш" колоночной хроматографией (метиленхлористый: метанол = 10: 1) с получением целевого продукта (6,23 г, 60%) в виде светло-желтого твердого вещества. Данные анализа продукта аналогичны примеру 1.
Пример 3. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил]камптотецина
(S)-7-метилкамптотецин (8 г, 0,0221 моль), изопропиламин (3,91 г, 0,0662 моль) и параформальдегид (полиоксиметилен) (5 г) поочередно прибавляли в смешанный растворитель этанола (30 мл), воды (30 мл) и концентрированной соляной кислоты (6,93 мл, 0,0684 моль). Далее реакционную смесь перемешивали при кипячении в течение 20 часов и затем охлаждали до комнатной температуры. Растворитель удаляли отгонкой при пониженном давлении и таким образом полученный остаток очищали с помощью "флеш" колоночной хроматографии (метиленхлористый: метанол = 10:1) с получением целевого продукта (6,35 г, 61,1%) в виде светло-желтого твердого вещества. Данные анализа продукта аналогичны примеру 1.
Пример 4. Гидрохлорид (S)-7-[2-(N-пропиламино)этил]камптотецина
Аналогичную примеру 1 методику применяли для пропиламина (496 мг, 0,0084 моль) и (S)-7-метилкамптотецина (1,005 г, 0,0028 моль) с получением целевого продукта (677 мг, 52%) в виде светло-желтого твердого вещества.
1H ЯМР (DMSO-d6), δ, м.д.: 9,26 (уш.с, 1Н), 8,43-7,7 (м, 4Н), 7,3 (с, 1Н), 6,48 (с, 1Н), 5,42 (с, 2Н), 5,29 (с, 2Н), 3,64-3,37 (м, 2Н), 3,2-3,11 (м, 4Н), 1,92-1,82 (м, 2Н), 1,27-1,11 (м, 8Н), 0,88 (т, 3Н, J=7,2 Гц), 0,81 (т, 3Н, J=7,3 Гц).
Пример 5. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил-10,11-метилендиоксикамптотецина
Аналогичную примеру 1 методику применяли для (S)-7-метил-10,11-метилендиоксикамптотецина (1 г, 0,00248 моль) и изопропиламина (440 мг, 0,0744 моль) с получением целевого продукта (540 мг, 48%) в виде светло-желтого твердого вещества.
1H ЯМР (DMSO-d6), δ, м.д.: 9,21 (уш.с, 1Н), 7,6 (с, 1Н), 7,4 (с, 1Н), 7,21 (с, 1Н), 6,28 (с, 2Н), 5,4 (с, 2Н), 5,32 (с, 2Н), 3,64-3,60 (м, 2Н), 3,45-3,34 (м, 1Н), 3,19-3,10 (м, 2Н), 1,92-1,81 (м, 2Н), 1,27 (д, 6Н, J=7,1 Гц), 0,88 (т, 3Н, J=7,2 Гц).
Пример 6. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил]-10,11-метилен-диоксикамптотецина
Аналогичную примеру 2 методику применяли для (S)-7-метил-10,11-метилендиоксикамптотецина (1 г, 0,00248 моль) и изопропиламина (440 мг, 0,00744 моль) с получением целевого продукта (600 мг, 53%) в виде светло-желтого твердого вещества. Данные анализа продукта аналогичны примеру 5.
Пример 7. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил]-10,11-метилендиоксикамптотецина
Аналогичную примеру 3 методику применяли для (S)-7-метил-10,11-метилендиоксикамптотецина (1 г, 0,00248 моль) и изопропиламина (440 мг, 0,00744 моль) с получением целевого продукта (565 мг, 51%) в виде светло-желтого твердого вещества. Данные анализа продукта аналогичны примеру 5.
Пример 8. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил-10,11-этилендиоксикамптотецина
Аналогичную примеру 1 методику применяли для (S)-7-метил-10,11-этилендиоксикамптотецина (1 г, 0,00239 моль) и изопропиламина (440 мг, 0,00744 моль) с получением целевого продукта (703 мг, 56%) в виде светло-желтого твердого вещества.
1H ЯМР (DMSO-d6), δ, м.д.: 9,20 (уш.с, 1Н), 7,58 (с, 1Н), 7,4 (с, 1Н), 7,23 (с, 1Н), 6,31 (м, 2Н), 5,8 (м, 2Н), 5,4 (с, 2Н), 5,32 (с, 2Н), 3,61-3,3 (м, 2Н), 3,17-3,11 (м, 3Н), 1,96-1,84 (м, 2Н), 1,27 (д, 6Н, J=7,5 Гц), 0,92 (т, 3Н, J=6,8 Гц).
Пример 9. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил-10,11-этилендиоксикамптотецина
Аналогичную примеру 2 методику применяли для (S)-7-метил-10,11-этилендиоксикамптотецина (1 г, 0,00239 моль) и изопропиламина (440 мг, 0,00744 моль) с получением целевого продукта (579 мг, 46%) в виде светло-желтого твердого вещества. Данные анализа продукта аналогичны примеру 8.
Пример 10. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил-10,11-этилендиоксикамптотецина
Аналогичную примеру 3 методику применяли для (S)-7-метил-10,11-этилендиоксикамптотецина (1 г, 0,00239 моль) и изопропиламина (440 мг, 0,00744 моль) с получением целевого продукта (668 мг, 53%) в виде светло-желтого твердого вещества. Данные анализа продукта аналогичны примеру 8.
Пример 11. Гидрохлорид (S)-7-[2-(N-пропиламино)этил-10,11-метилендиокси-камптотецина
Аналогичную примеру 1 методику применяли для (S)-7-метил-10,11-метилендиоксикамптотецина (1 г, 0,00248 моль) и пропиламина (440 мг, 0,00744 моль) с получением целевого продукта (466 мг, 42%) в виде светло-желтого твердого вещества.
1Н ЯМР (DMSO-d6), δ, м.д.: 7,6 (с, 1Н), 7,38 (с, 1Н), 7,21 (с, 1Н), 6,26 (с, 2Н), 5,4 (с, 2Н), 5,29 (с, 2Н), 3,56-3,31 (м, 2Н), 3,18-3,03 (м, 4Н), 1,91-1,81 (м, 2Н), 1,29-1,04 (м, 8Н), 0,87 (т, 3Н, J=6,8 Гц), 0,74 (т, 3Н, J=7,1 Гц).
Пример 12. Гидрохлорид (S)-7-[2-(N-пропиламино)этил]-10,11-этилендиоксикамптотецина
Аналогичную примеру 1 методику применяли для (S)-7-метил-10,11-этилендиоксикамптотецина (1 г, 0,00239 моль) и пропиламина (440 мг, 0,00744 моль) с получением целевого продукта (575 мг, 46%) в виде светло-желтого твердого вещества.
1H ЯМР (DMSO-d6), δ, м.д.: 7,6 (с, 1Н), 7,36 (с, 1Н), 7,20 (с, 1Н), 6,26 (с, 2Н), 5,81 (с, 2Н), 5,41 (с, 2Н), 5,28 (с, 2Н), 3,52-3,41 (м, 2Н), 3,16-3,01 (м, 4Н), 1,93-1,79 (м, 2Н), 1,28-1,02 (м, 8Н), 0,88 (т, 3Н, J=7,1 Гц), 0,78 (т, 3Н, J=7,1 Гц),
Пример 13. Гидрохлорид (S)-7-[2-(N-изопропилбензиламино)этил]камптотецина
(S)-7-метилкамптотецин (8 г, 0,0221 моль), изопропилбензиламин (9,88 г, 0,0662 моль) и концентрированную соляную кислоту (6,93 мл, 0,0684 моль) прибавляли к диметилсульфоксиду (80 мл). Далее применяли аналогичную примеру 1 методику для получения целевого продукта (9,27 г, 75%) в виде светло-желтого твердого вещества.
1H ЯМР (DMSO-d6, 400 MHz) δ, м.д.: 8,38 (д, 1Н, J=8,5 Гц), 8,13 (д, 1Н, J= 8,5 Гц), 7,86 (дд, 1Н, J=8,5; 8,0 Гц), 7,74 (дд, 1Н, J=8,5; 8,0 Гц), 7,52-7,31 (м, 5Н), 7,29 (с, 1Н), 6,52 (с, 1Н), 5,43 (с, 2Н), 5,35 (с, 2Н), 3,66-3,59 (м, 2Н), 3,54 (с, 2Н), 3,45-3,34 (м, 1Н), 3,21-3,16 (м, 2Н), 1,92-1,82 (м, 2Н), 1,26 (д, 6Н, J=6,4 Гц), 0,88 (т, 3Н, J=8,0 Гц).
Пример 14. Гидрохлорид (S)-7-[2-(N-изопропиламино)этил]камптотецина
Pd-C (10%, 500 мл), 4,4% муравьиную кислоту и метанол (100 мл) добавляли к гидрохлориду (S)-7-[2-(N-изопропилбензиламино)этил] -камптотецину (5 г, 0,0089 моль) и реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Далее реакционную массу фильтровали и полученный фильтрат концентрировали под пониженным давлением. Полученный остаток очищали с помощью "флеш" колоночной хроматографии (метиленхлористый: метанол = 10:1) с получением целевого продукта (3,6 г, 86%) в виде светло-желтого твердого вещества. Данные анализа продукта аналогичны примеру 1.
Данное изобретение относится к способу получения производных камптотецина или их фармацевтически приемлемых солей. Особенно 7-замещенные производные камптотецина, которые обладают прекрасной противоопухолевой активностью, могут быть получены легко и экономически выгодно с помощью данного способа.
Настоящее изобретение относится к способу получения производных камптотецина формулы (I), где Y и Z представляют собой водород, алкил, гидроксиалкилгруппу или обычную защитную аминогруппу, R1 - водород, алкил, гидроксигруппа, R2 и R3 - водород, гидроксигруппа, или они могут связываться, образуя циклический фрагмент - метилендиокси- или этилендиоксигруппу, R4 - водород или алкил, R5 - водород, гидроксигруппа, фтор, бром, хлор, йод или аминогруппа. В вышеупомянутом изобретении описан более удобный способ получения, заключающийся в получении соединения общей формулы (I) по реакции Манниха, т.е. соединение общей формулы (II) реагирует с амином или его солью и с источником формальдегида в присутствии кислоты. 4 з.п.ф-лы.
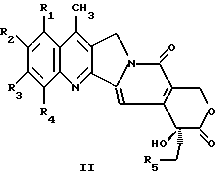



или его солью и с источником формальдегида в присутствии кислоты,
где Y и Z - одинаковы или различны и каждая группа представляет собой атом водорода, C1-С6-алкил-, C1-С3-гидроксиалкилгруппу или обычную защитную аминогруппу, например бензилоксикарбонил-, бензилгруппу и т. д. ;
R1 - атом водорода, C1-С6алкил- или гидроксигруппа;
R2 и R3 - одинаковы или различны и каждая представляет собой атом водорода или гидроксигруппу, или они могут связываться, образуя циклический фрагмент - метилендиокси- или этилендиоксигруппу;
R4 - атом водорода или C1-С6алкилгруппа;
R5 - атом водорода, гидроксигруппа, атом фтора, хлора, брома или йода, или аминогруппа.
| ГЕКСАЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 1992 |
|
RU2071476C1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Способ получения производных 2"окси-3-фенилпропиофенона | 1972 |
|
SU471358A1 |
| Замок двери транспортного средства | 1972 |
|
SU495432A1 |
| ИНЕРЦИОННЫЙ ВИБРАТОР | 0 |
|
SU296597A1 |
| Экономайзер | 0 |
|
SU94A1 |
Авторы
Даты
2002-04-10—Публикация
1998-07-08—Подача