Изобретение относится к области медицинской и ветеринарной микробиологии, а именно к способам приготовления иммунных сывороток, и может быть использовано для контроля качества диагностикума сапного эритроцитарного антигенного и агглютиногенных свойств культур возбудителя сапа.
Известны способы приготовления сывороток, основанные на гипериммунизации животных-продуцентов сывороток микробами сапа или извлеченными из них антигенами (см. Гозарх З. С. Получение противосапной сыворотки по методу Н.В. Колпика // Вестн. современ. ветеринарии, 1928, 15, с.472-475; Мельникова Л. А. , Хасанов Ч.Г. Усовершенствование диагностики сапа // Матер. республик. научно-производств. конференции по актуальным проблемам ветеринарии и зоотехники. - Казань, 1996, с.23).
Общим с заявляемым способом являются последовательность этапов приготовления сыворотки, включающих получение антигена, иммунизацию животных, отбор у животных крови и получение сыворотки.
Однако ни один из указанных способов не получил практического завершения. Цели рассматриваемых работ ограничивались приготовлением сыворотки для лабораторных экспериментов без учета иммуногенности вводимых антигенов либо их комплексов и сравнения эффективности применяемых способов иммунизации животных. В силу отмеченных обстоятельств диагностические сапные сыворотки, которые можно было бы использовать в качестве референс-реагентов для измерения специфической активности диагностических сапных препаратов, отечественной промышленностью не выпускались.
Наиболее близким к заявляемому решению является способ, основанный на внутривенной иммунизации кроликов живой культурой возбудителя сапа (см. Денкевич А.С. Определение сапного микроба методом люминесцентной микроскопии с помощью меченых антител // Труды научн.-исслед. вет ин-та / Казах. акад. сельскохоз. наук, 1961, т.10, с. 272-277).
Способ включает следующие этапы:
выращивания культуры штамма 5584 на плотной питательной среде;
приготовление суспензии живой культуры возбудителя сапа, содержащей микробы в концентрации 2 млрд. микробных тел в одном миллилитре;
внутривенные ежедневные инъекции суспензии кроликам по схеме: (0,2-0,4-0,8 мл), (2,0-2,5-3,0 мл);
отбор крови на 7-10 сутки после последнего введения.
Общим с заявляемым способом является последовательность этапов получения сыворотки, использование кроликов в качестве животного-продуцента сыворотки, введение антигена циклами путем инъекций в ушные вены.
К недостаткам рассматриваемого способа следует отнести применение в качестве антигена живой культуры возбудителя сапа (штамм 5584), что приводит к значительной (до 80%) летальности среди кроликов, взятых в опыт, и низкому выходу конечного продукта. Кроме того, использование в качестве антигенного препарата живой культуры сапных микробов штамма 5584 проведено без экспериментальной проверки его антигенной активности в сравнении с другими штаммами, а сама иммунизация требовала выполнения широкого комплекса мероприятий, предусмотренных специальной техникой безопасности.
Задачей изобретения является разработка способа получения высокоактивной и стабильной при хранении поливалентной сапной сыворотки, пригодной для контроля качества диагностикума эритроцитарного антигенного сапного и агглютиногенных свойств культур возбудителя сапа.
Поставленная задача решается благодаря тому, что в способе получения сапной поливалентной диагностической сухой сыворотки, включающей этапы выращивания культуры, приготовления из нее корпускулярного антигена, иммунизацию животных-продуцентов, получения сыворотки из отобранной крови, розлива сыворотки в ампулы и ее лиофильного высушивания, предусмотрены следующие отличия:
для приготовления сыворотки в качестве производственного используют высоковирулентный штамм Ц-5 Burkholderia (Pseudomonas) mallei;
для иммунизации кроликов используют инактивированный корпускулярный антиген, приготовленный из агаровой культуры штамма Ц-5;
корпускулярный антиген вводят кроликам внутривенно в соответствии с экспериментально отработанной схемой;
консервацию полученной сыворотки производят при помощи лиофилизации согласно отработанному режиму.
Указанные отличия обусловлены следующими причинами.
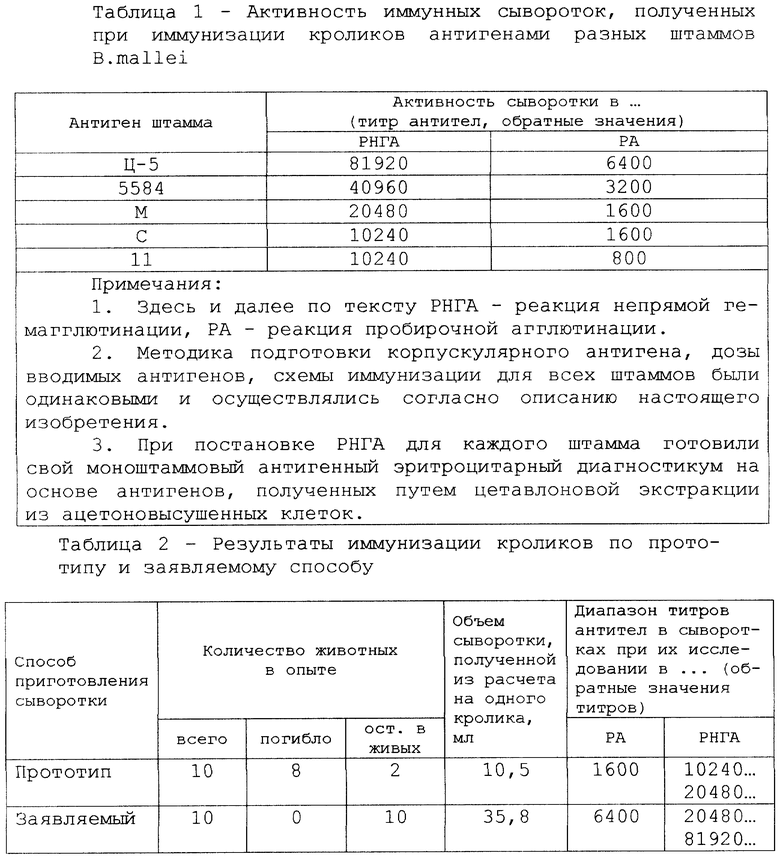
Микробы штамма Ц-5 являются типичными представителями В.mallei и обладают всеми характерными для данного вида бактерий морфологическими, культуральными, антигенными и вирулентными свойствами. По вирулентности для золотистых хомячков они при подкожном заражении превосходят примерно в 5 раз микробов штамма 5584, принятого на отечественных биофабриках в качестве производственного для приготовления сапных диагностических препаратов. По антигенной активности корпускулярный антиген микробов штамма Ц-5 существенно отличается от аналогичных антигенных препаратов, полученных из микробов других штаммов возбудителя сапа (таблица 1).
Инактивация микробной культуры при экспериментально обоснованных условиях позволяет получать стерильный корпускулярный антиген, сохраняющий специфическую антигенную активность и не требующий применения мер специальной техники безопасности при проведении иммунизации.
Отработанная схема иммунизации кроликов не вызывает у них специфических поражений и гибели от анафилактического шока.
Консервация иммунной сыворотки лиофилизацией при выбранном режиме обеспечивает сохранение ее активности в течение 2 лет при условии хранения при температуре 2±2oС и 20-25oС.
Способ включает следующие этапы:
выращивание культуры микробов штамма Ц-5;
приготовление корпускулярного антигена;
иммунизация животных;
получение иммунной сыворотки;
розлив сыворотки в стеклотару и лиофилизация.
Способ выполняется следующим образом:
1. Выращивание культуры сапных микробов.
Исходным материалом служит лиофилизированная сапная культура штамма Ц-5, сохраняемая в ампулах под вакуумом. Для выращивания микробов готовят плотную питательную среду на основе недеионизированного солянокислого гидролизата казеина с содержанием аминного азота 25-35 мг%, глицерина 10 мл/л и агар-агар 1,5%. рН среды 6,8-7,0. Расплавленную питательную среду разливают по 300-500 мл в матрацы. Выращивание микробов осуществляют при температуре 36-38oС в течение двух суток.
2. Получение корпускулярного антигена.
Сформировавшуюся в матраце культуру смывают фосфатным буфером рН 6,9-7,0. Суспензию разводят до концентрации 10 млрд микробов мл по стандарту мутности ГИСК им. Л.А.Тарасовича, после чего инактивируют добавлением фенола с последующим прогреванием. Препарат хранят при 0-4oС до 3 месяцев.
3. Иммунизация животных-продуцентов.
Полученный препарат вводят кроликам внутривенно через день по схеме (0,2-0,4-0,8) мл, перерыв 4 дня, (0,5-1,0-1,5) мл, перерыв 4 дня, (2,0-2,5-3,0) мл.
4. Получение иммунной сыворотки.
Через 10 суток после последнего введения антигена у кроликов производят забор крови. Кровь собирают в стеклянные цилиндры и помещают в термостат для свертывания. Образовавшуюся сыворотку сливают и очищают центрифугированием.
Контроль активности полученной сыворотки определяют в РНГА с диагностикумом эритроцитарным антигенным сапным. Титр антител в иммунной сыворотке должен быть не ниже 1:20480. Полученную сапную поливалентную кроличью сыворотку стерильно разливают по 1,0 мл в ампулы и подвергают лиофилизации на лабораторной коллекторной сушильной установке (СШ-18) при остаточном давлении 50-100 мм рт.ст. в течение 3-4 часов.
После окончания процесса высушивания ампулы отсоединяют и запаивают под вакуумом. Титр антител в сыворотке после регидратации должен быть при исследовании в РНГА не менее 1:10240.
Для сравнения прототипа и заявляемого способа были проиммунизированы кролики и изучены полученные от них сыворотки (таблица 2).
Наблюдения за кроликами показали, что они тяжело переносят иммунизацию по прототипу. У них наблюдались общее истощение, выраженные облитерирующие тромбофлебиты и обширные некрозы ушных раковин. А после второго цикла иммунизации кролики нередко погибали от анафилактического шока.
Общее состояние кроликов, иммунизированных по заявляемому способу, на протяжении всего эксперимента оставалось удовлетворительным. Они сохраняли активность и хороший аппетит, что способствовало достаточно высокому выходу конечного продукта (сыворотки). Из расчета на одного кролика, взятого в работу, было получено в 3 раза больше сыворотки, чем в контроле. А сами сыворотки характеризовались более высоким содержанием специфических антител, чем сыворотки, полученные по прототипу.
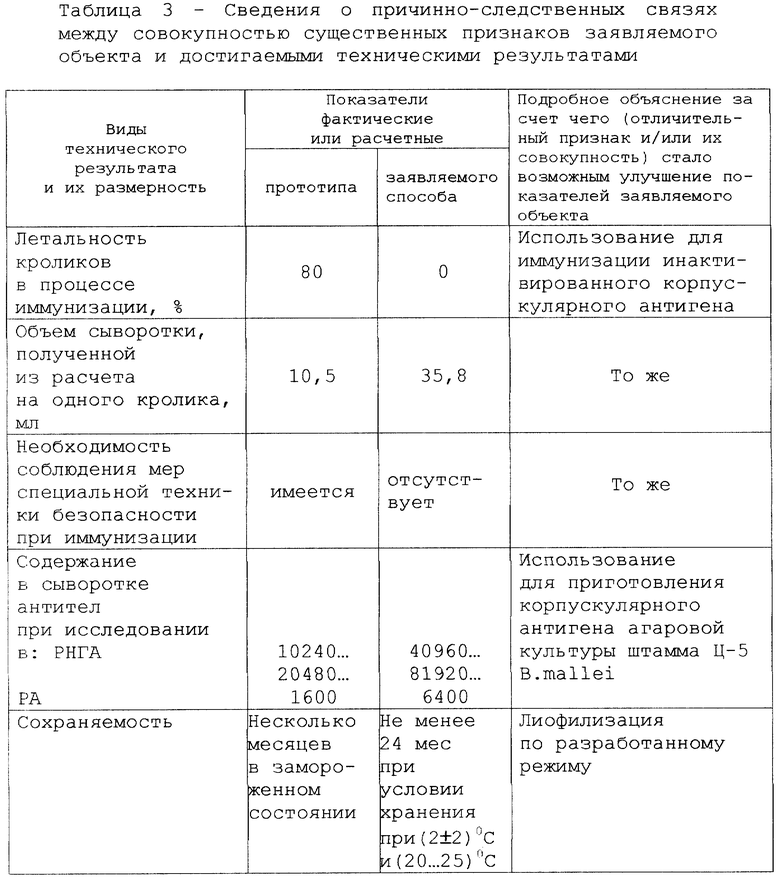
Наличие причинно-следственной связи между совокупностью существенных признаков заявляемого способа и достигаемыми техническими результатами показано в таблице 3.
Предлагаемый способ получения сапной диагностической поливалентной сухой сыворотки имеет следующие преимущества:
не вызывает гибели кроликов от специфических поражений и анафилактического шока, что способствует получению в пересчете на одно животное примерно в 3 раза больше сыворотки, чем в контроле;
обеспечивает получение иммунных сывороток с более высоким титром специфических антител;
обеспечивает после лиофилизации сохранение специфической активности сывороток в течение 2 лет при условии хранения при температуре 2±2oС и 20-25oС;
в процессе иммунизации кроликов и взятия у них крови не требуется соблюдения мер специальной техники безопасности, что существенно облегчает работу.
Высокое содержание специфических антител в получаемых сыворотках и стабильность их свойств при хранении позволили предложить эти препараты для контроля при помощи РНГА качества сапного эритроцитарного антигенного диагностикума. Результаты государственных испытаний позволили сыворотки, получаемые по разработанному способу, рекомендовать для контроля специфической активности сапного эритроцитарного антигенного диагностикума. Способ получения сывороток и сама сыворотка под названием "Сыворотка диагностическая сапная агглютинирующая кроличья сухая" в качестве стандартного образца предприятия (СОП) включены в "Регламент производства сапного эритроцитарного антигенного диагностикума" и "Временную фармакопейную статью", зарегистрированную под номером ВФС 42-3465-99.
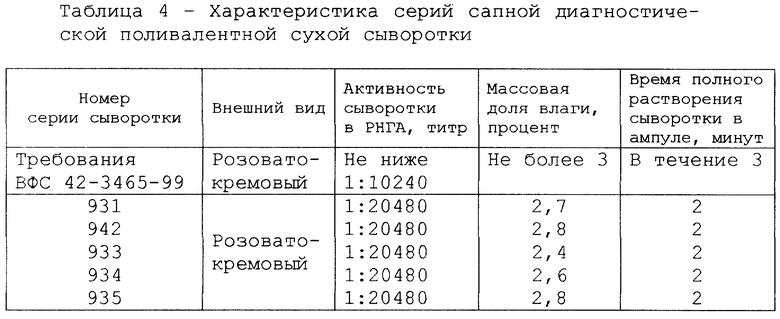
Возможность осуществления предложенного способа может быть продемонстрирована следующим примером. В соответствии с утвержденной нормативно-технической документацией, созданной в НИИ микробиологии МО РФ, АТЛ были приготовлены 5 серий сыворотки. Характеристика серий представлена в таблице 4.
Анализ ее дает основание считать, что все полученные серии сывороток соответствуют требованиям ВФС-42-3465-99. Они характеризуются содержанием специфических антител в высоких титрах. Массовая доля влаги во всех случаях варьирует в оптимальном для биопрепаратов диапазоне от 2,4 до 2,8oС. Время растворения полученных сывороток не превышает 2 минут.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО АНТИГЕННОГО САПНОГО | 2001 |
|
RU2188036C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОТУЛЯРЕМИЙНОЙ ГИПЕРИММУННОЙ СЫВОРОТКИ И СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО ТУЛЯРЕМИЙНОГО ИММУНОГЛОБУЛИНОВОГО СУХОГО | 2002 |
|
RU2240822C2 |
| АНТИГЕННЫЙ ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ САПА У ЛЮДЕЙ И ЖИВОТНЫХ | 2004 |
|
RU2262949C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ АНТИГЕНУ, ОБЩЕМУ ДЛЯ ВОЗБУДИТЕЛЕЙ САПА И МЕЛИОИДОЗА | 1997 |
|
RU2117043C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕННОГО ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА ДЛЯ ОБНАРУЖЕНИЯ АНТИТЕЛ К АНТИГЕНАМ ВОЗБУДИТЕЛЕЙ САПА И МЕЛИОИДОЗА | 2013 |
|
RU2540902C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИЧЕСКОЙ СЫВОРОТКИ | 1997 |
|
RU2135210C1 |
| Способ получения диагностической псевдотуберкулезной сыворотки | 1979 |
|
SU889003A1 |
| ДИАГНОСТИКУМ ПСЕВДОТУБЕРКУЛЕЗНЫЙ ЭРИТРОЦИТАРНЫЙ МОНОКЛОНАЛЬНЫЙ | 2008 |
|
RU2377308C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИЧЕСКОЙ СЫВОРОТКИ | 1991 |
|
RU2010577C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭРИТРОЦИТАРНОГО АНТИГЕННОГО ГИСТОПЛАЗМОЗНОГО И КОКЦИДИОИДОМИКОЗНОГО ДИАГНОСТИКУМА | 2010 |
|
RU2422832C1 |
Изобретение относится к медицине, в частности к микробиологии и касается способов приготовления иммунных сывороток. Сущностью изобретения является применение микробов штамма Ц-5 В. mallei в качестве производственного, из которых после добавления фенола и прогревания готовят корпускулярный антиген, используемый для внутривенной циклической иммунизации кроликов по определенной схеме. Сыворотки получают на 10 день после иммунизации и подвергают лиофилизации. Техническим результатом является разработка способа получения высокоактивной и стабильной при хранении поливалентной сапной сыворотки, пригодной для контроля качества диагностикума эритроцитарного антигенного сапного и агглютиногенных свойств культур возбудителя сапа. 4 табл.
Способ получения сыворотки диагностической поливалентной сапной сухой, включающий выращивание культуры сапных микробов, приготовление из них корпускулярного антигена, иммунизацию животных-продуцентов, получение иммунной сыворотки и ее лиофильное высушивание, отличающийся тем, что в качестве производственного используют микробы штамма Ц-5 В. mallei, а корпускулярный антиген готовят из агаровой культуры, инактивированной добавлением фенола и прогреванием, антиген вводят животным-продуцентам внутривенно через сутки тремя циклами, сыворотки получают на 10 день после иммунизации и подвергают лиофилизации из замороженного состояния при остаточном давлении 50-100 мм рт. ст. в течение 3-4 ч.
| СПОСОБ ПРИГОТОВЛЕНИЯ ПРЕПАРАТОВ ДЛЯ ЦИТОРЕФРАКТОМЕТРИЧЕСКОГО ИССЛЕДОВАНИЯ САПНЫХ МИКРОБОВ | 1998 |
|
RU2149899C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕНА ДЛЯ ДИАГНОСТИКИ САПА В РЕАКЦИИ АГГЛЮТИНАЦИИ | 1997 |
|
RU2111763C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛАТЕКСНОГО ДИАГНОСТИКУМА | 1991 |
|
RU2012888C1 |
| ХРАПОВА Н.П | |||
| Перспективы совершенствования иммуноглобулиновых препаратов для обнаружения и идентификации возбудителей сапа и мелиоизоза | |||
| Медицинская паразитология и паразитарные болезни, 1995, № 4, с | |||
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
Авторы
Даты
2002-08-27—Публикация
2001-01-09—Подача