Изобретение относится к веществам, имеющим гипотензивную активность в сочетании с тромбоцит-антиагрегационной активностью, и к их фармацевтическим композициям.
В особенности изобретение относится к веществам, имеющим улучшенную гипотензивную активность и вызывающим меньше побочных эффектов, в частности, в бронхах, по сравнению с продуктами, представленными на рынке в качестве гипотензивных агентов. Гипотензивная активность сочетается с тромбоцит-антиагрегационной активностью.
Гипотензивные агенты известны в данной области техники. Особенно известны АСЕ-ингибиторы (ингибиторы ангиотензин-конвертирующего фермента), которые используются первыми при выборе мер для лечения сердечно-сосудистых заболеваний, таких как гипертензия, стенокардия, ишемия миокарда, застойная сердечная недостаточность и т.д. АСЕ-ингибиторы действуют на ренин-ангиотензивную систему, которая выделяет ангиотензин II, известный как один из наиболее эффективных гипертензивных агентов. Более точно, эти лекарственные препараты ингибируют активность ангиотензин-конвертирующего фермента, карбоксипептидазы, которая присутствует главным образом в легких, почках и сосудах. Действие этого фермента является неспецифичным. Он инактивирует брадикинин плазмы, который обладает сосудорасширяющей активностью, а также способствует диурезу, в частности натрийурезу. Другими словами, брадикинин плазмы обладает противоположным действием по сравнению с действием ангиотензина II. Следовательно, АСЕ-ингибиторы препятствуют образованию ангиотензина II и в то же время - деградации брадикинина. Следовательно, АСЕ-ингибиторы определенно являются одним из наиболее значительных фармакологических новшеств за последние несколько декад.
Однако введение АСЕ-ингибиторов часто (около 20-30% случаев) сопровождается побочными эффектами в дыхательной системе, такими как кашель, одышка, бронхостеноз. Кроме того, эти лекарственные препараты показывают довольно ограниченный терапевтический профиль, например они не обладают тромбоцит-антиагрегационной активностью, таким образом, при лечении вышеуказанных сердечно-сосудистых заболеваний их часто применяют совместно с другими лекарственными препаратами, имеющими антиагрегационную активность. Например, при лечении инфаркта миокарда и для предотвращения рецидивов по существу используют составную сердечно-сосудистую терапию, включающую, помимо всего прочего, сочетание гипотензивного и антиагрегационного агентов.
Ощущалась необходимость лекарственных препаратов с лучшим терапевтическим профилем и с уменьшенным количеством побочных эффектов, в частности, в дыхательной системе, например в бронхах.
Заявитель обнаружил специфический класс солей АСЕ-ингибиторов, характеризующихся тем, что они обладают, по сравнению с другими солями этих же соединений, улучшенной гипотензивной активностью и вызывают меньше побочных эффектов в бронхах.
Объектом изобретения являются, следовательно, азотные соли АСЕ-ингибиторов, имеющих следующие формулы: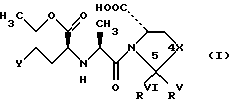
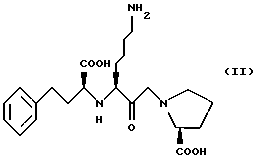
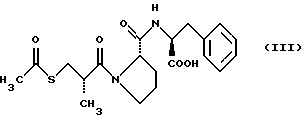
В формуле (I)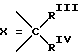
или N-CH3;
Y - СН3, фенил;
RIII - H,
RIII вместе с RIV образует следующее кольцо с углеродом в положении 4: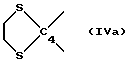
RIII вместе с RV (углероды с положениях 4 и 5) формирует циклогексановые или циклогептановые кольца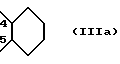
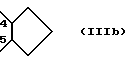
RIV - H или RIV образует с RIII кольцо (IVa);
RV - H или свободная валентность, или RV образует с RIII кольца (IIIа) или (IIIb);
RVI - H или одинарная связь -О, когда RV означает свободную валентность, таким образом формируя кетоновую группу с атомом углерода в положении 5.
Предпочтительные нитраты формулы (I) включают:
когда Х - С(RIII)(RIV), как определено выше, Y - фенил, RIII= RIV=RV=RVI - H, остаток эналаприла;
как в эналаприле, но с RIII, который вместе с RIV образует кольцо (IVa), остаток спираприла;
как в эналаприле, но с RIII, который вместе с RV образует кольцо (IIIb), остаток рамиприла;
как в эналаприле, но с Y - СН3 и RIII, который вместе с RV формирует кольцо (IIIа), остаток периндоприла;
как в эналаприле, но с Х - N-СН3, RV означает свободную валентность и RVI - -О, таким образом формируя с атомом углерода С5 кетоновую группу, остаток имидаприла.
Соединения классов согласно изобретению, которые являются предшественниками солей, используют как отдельные оптически активные изомеры или как их смесь или в форме рацематов.
Предшественник класса II известен как лизиноприл, предшественник класса III - алацеприл. Эти предшественники могут быть получены в соответствии со способами, описанными в "The Mercx Index, Ed. 12".
Соли по изобретению получают согласно следующему способу. Вещество, из которого получают соль, растворяют в органическом растворителе, не содержащем в молекуле свободных гидроксильных групп, и затем добавляют стехиометрическое количество азотной кислоты. Соль отделяют фильтрацией и промывают несколько раз растворителем, например тем, который использовался в реакции. Предпочтительными являются органические растворители, например, такие, как ацетонитрил, этилацетат и другие.
Было обнаружено, что соединения по изобретению улучшают, по сравнению с такими же соединениями и с АСЕ солями в общем, фармакологический профиль вышеуказанных АСЕ-ингибиторов и, дополнительно, показывают более благоприятную общую и региональную толерантность.
Соединения согласно изобретению могут быть использованы в качестве сердечно-сосудистых лекарственных препаратов, в частности, при лечении гипертензии, стенокардии, ишемии миокарда, застойной сердечной недостаточности.
Соли согласно изобретению могут быть изготовлены в виде соответствующих фармацевтических композиций согласно способам, хорошо известным в данной области техники, например тем, которые описаны в Remington's Pharmaceutical Sciences, Ed. 15.
Примеры, приведенные ниже, даны только для иллюстрации изобретения, но не должны восприниматься как ограничивающие его.
ПРИМЕР 1
Синтез (S)-1-[N-[1-(этоксикарбонил)-3-фенилпропил] -L-аланил] -L-пролина(эналаприла) и получение его нитрата в ацетонитриле.
Смесь этил-2-оксо-4-фенилбутирата (2,1 г) и L-аланил-L-пролина (0,4 г) в этаноле/воде 1/1 медленно обрабатывают при комнатной температуре раствором цианоборгидрида натрия (0,4 г) в этаноле/воде 1/1.
В конце реакции продукт абсорбируют на сильнокислотной ионообменной смоле и элюируют водным раствором, содержащим 2% (объем./объем.) пиридина. Фракции, которые содержат продукт, лиофилизируют для получения сырого соединения. Последующая хроматография позволяет выделить требуемый изомер (-) практически чистым (0,24 г).
Этот изомер затем растворяют в ацетонитриле и обрабатывают, помещая реактор в ледяную баню, стехиометрическим количеством концентрированной азотной кислоты, растворенной в ацетонитриле. После охлаждения и фильтрации твердый остаток промывают охлажденным ацетонитрилом и получают 97% чистоты (ВЭЖХ - высокоэффективная жидкостная хроматография) азотную соль эналаприла. Соль 99% чистоты (ВЭЖХ) может быть получена перекристаллизацией из ацетонитрила.
ПРИМЕР 2
Синтез эналаприла и получение нитрата в этилацетате.
Смесь этил-2-оксо-4-фенилбутирата (15 г), L-аланил-L-пролина (9 г), молекулярных сит 3 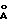 (40 г) и никеля Ренея (10,8 г) в этаноле (300 мл) гидрируют при комнатной температуре под давлением 3 атм до тех пор, пока водород больше не поглощается. После отфильтровывания нерастворившегося вещества при хорошем промывании этанолом растворитель выпаривают под вакуумом, получая смесь диастереомеров, образованную на 85% ожидаемым продуктом (ВЭЖХ). Полученный продукт растворяют в смеси, приготовленной из 200 мл воды и 70 мл метилацетата. Поддерживая раствор в состоянии перемешивания, доводят pH до значения 8,6 посредством 50% NaOH. Органическую фазу отделяют и водную фазу тщательно промывают этилацетатом (3•50 мл). Водную фазу доводят соляной кислотой до pH 4,3, насыщают хлоридом натрия и затем экстрагируют этилацетатом (4•100 мл). После высушивания сульфатом натрия и выпаривания растворителем под вакуумом осадок растворяют в этилацетате, помещая реактор в ледяную баню, и получают соль, обрабатывая стехиометрическим количеством концентрированной азотной кислоты. После перемешивания в течение 2 часов раствор охлаждают, фильтруют, промывают этилацетатом и рекристаллизуют из ацетонитрила, получая 12,5 г азотной соли изомера (-) около 99% чистоты (ВЭЖХ).
(40 г) и никеля Ренея (10,8 г) в этаноле (300 мл) гидрируют при комнатной температуре под давлением 3 атм до тех пор, пока водород больше не поглощается. После отфильтровывания нерастворившегося вещества при хорошем промывании этанолом растворитель выпаривают под вакуумом, получая смесь диастереомеров, образованную на 85% ожидаемым продуктом (ВЭЖХ). Полученный продукт растворяют в смеси, приготовленной из 200 мл воды и 70 мл метилацетата. Поддерживая раствор в состоянии перемешивания, доводят pH до значения 8,6 посредством 50% NaOH. Органическую фазу отделяют и водную фазу тщательно промывают этилацетатом (3•50 мл). Водную фазу доводят соляной кислотой до pH 4,3, насыщают хлоридом натрия и затем экстрагируют этилацетатом (4•100 мл). После высушивания сульфатом натрия и выпаривания растворителем под вакуумом осадок растворяют в этилацетате, помещая реактор в ледяную баню, и получают соль, обрабатывая стехиометрическим количеством концентрированной азотной кислоты. После перемешивания в течение 2 часов раствор охлаждают, фильтруют, промывают этилацетатом и рекристаллизуют из ацетонитрила, получая 12,5 г азотной соли изомера (-) около 99% чистоты (ВЭЖХ).
ПРИМЕР 3
Острая токсичность.
Группа из 10 мышей (вес от 15 до 25 г) получала единичную оральную дозу 100 мг/кг. Все эти животные выживали в течение периода наблюдения (14 дней). Симптомы токсичности не обнаружены.
ПРИМЕР 4
Гипотензивная активность.
Гипотензивную активность соединений по изобретению определяли в соответствии со способом Laubie et al., J. Cardiovasc. Pharmacol 6, 1076, 1984. 6 крыс, весящих от около 200 до 250 г, использовали как экспериментальную группу. Было сформировано четыре группы, каждую из которых обрабатывали внутрибрюшинно как показано ниже:
- малеат эналаприла - 100 μг/кг
- малеат эналаприла - 300 μг/кг
- нитрат эналаприла - 100 μг/кг
- нитрат эналаприла - 300 μг/кг
Дозы относятся к количеству эналаприла (катиона) в соли. Гипотензивный отклик оценивали как процент ингибирования гипертензии, вызванной введением дозы 100 μг/кг внутривенно ангиотензина I, как описано в вышеуказанной статье.
Результаты представлены в табл.1.
ПРИМЕР 5
Фармакологическое воздействие солей по изобретению на бронхоспазм, вызванный введением вещества Р.
Активность оценивали, измеряя усиление бронхоспазма, вызванного веществом Р, в соответствии со способом Subissi et al., Br. J. Phamiacol. 100, 502-6, 1990. Модель, описанная Subissi, предсказывает бронхиальные побочные эффекты вследствие введения АСЕ-ингибиторов.
Четыре группы (6 животных в группе) самок морских свинок, весящих около от 300 до 400 г, анестезировали этилуретаном (200 мг/кг) под искусственным давлением при постоянном положительном давлении. Соединения вводили внутрибрюшинно за 30 минут до вещества Р. Введенные дозы соли были такие же, как в примере 4. Затем измеряли изменения в дыхательном объеме согласно методу Konzett, Arch. Exp. Pathol. Phamiacol. 195, 71, 1940, до и после введения вещества Р (200 μг/кг) с или без тестируемых солей, то есть малеата и нитрата эналаприла.
Результаты представлены в табл.2.
Как видно из данных, нитрат эналаприла обладает лучшим респираторным профилем, чем малеат эналаприла в обеих тестируемых дозах.
ПРИМЕР 6
Тромбоцит-антиагрегационная активность.
Использовалась модель in vivo, описанная Pinon et al., J. Pharm. Methods 12, 79-84, 1984.
Две группы по 6 крыс каждая, весящие около от 200 до 250 г, обрабатывали оральной дозой 10 мг/кг/die малеатом или нитратом эналаприла соответственно (доза относится к количеству катиона эналаприла в соли) в течение пяти дней, тогда как третья группа использовалась в качестве контрольной. Приблизительно 18 часов перед последней обработкой животные голодали. Через час после этой обработки животных анестезировали 10% этилуретаном (1 г/кг внутрибрюшинно), и в левую яремную вену и правую сонную артерию были вставлены катетеры. Затем внутривенно вводили коллаген (тип 6, Sigma) с дозой 2 мг/кг. Три минуты спустя два образца крови, А и В, отобрали из сонной артерии каждого животного.
1,6 мл EDTA/формалинового буфера (24 мМ EDTA тетранатрия, 1,3 мМ КН2РО4, 13,4 мМ Na2HPО4) добавляли к первому образцу (образец А), содержащему 0,4 мл крови.
Второй образец крови (образец В) имел такой же объем, как и предыдущий образец (0,4 мл крови), но вместо буфера к нему добавляли 1,6 мл солевого раствора (физиологический раствор NaCl).
Затем образцы переносили в 5-мл пробирки и оставляли стоять при комнатной температуре в течение 15 минут.
Затем проводили подсчет тромбоцитов под микроскопом. Подсчет тромбоцитов в образцах В и А представляет собой общее число тромбоцитов и общее число агрегированных тромбоцитов соответственно. Результаты, представленные в табл.3, выражены как % агрегации тромбоцитов и относятся к % величине, полученной в контрольной группе.



Изобретение относится к нитрату АСЕ-ингибитора формулы I или II, где Y - фенил, Х - C(RIII)RIV, RIII, RIV, RV и RVI - водород, содержащему стехиометрическое количество азотной кислоты. Соединения I и II имеют улучшенную гипотензивную активность и вызывают меньше побочных эффектов, в частности, в бронхах. 4 з.п.ф-лы, 3 табл.
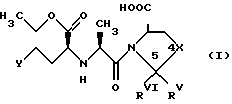
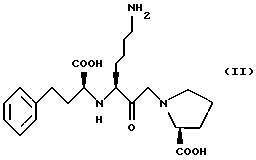
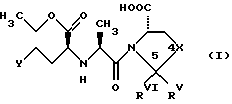
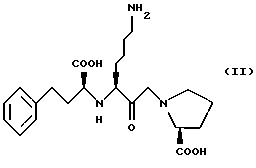
где Y - фенил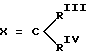
где RIII и RIV водород, RV и RIV - водород, содержащий стехиометрическое количество азотной кислоты.
| Способ получения производных пролина или их фармацевтически приемлемых солей | 1982 |
|
SU1316556A3 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
Авторы
Даты
2002-12-10—Публикация
1998-06-24—Подача