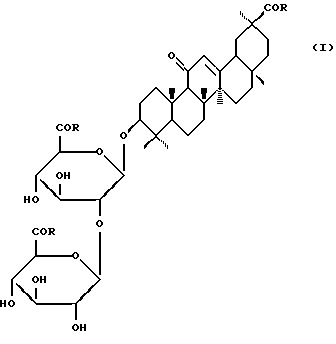
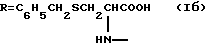
Изобретение относится к новым химическим соединениям, конкретно к гликопептиду глицирризиновой кислоты с S-бензил-L-цистеином [I]: 3-О-{2-О-[N-(β-D-глюкопиранозилуроноил)-L-цистеин(S-бензил)-N-(β-D-глюкопиранозилуроноил)-L-цистеин(S-бензил)]}-(3β,20β)-11-оксо-олеан-12-ен-30-(N-карбонил-L-цистеин(S-бензил)-3-ил формулы (Iб), проявляющему анти-ВИЧ активность.
Указанное соединение и его свойства в литературе не описаны.
В настоящее время во всем мире интенсивно ведутся исследования по поиску средств для борьбы с ВИЧ-инфекцией. Выявлен ряд соединений, ингибирующих репродукцию вируса иммунодефицита человека (ВИЧ): рибавирин, азидотимидин (зидовудин), 2,3-дидезоксинуклеозиды и др. [1,2] . В 1987-88 гг. группой японских ученых была обнаружена способность глицирризиновой кислоты (ГК) - основного биоактивного компонента экстракта корней солодки голой (Glycyrrhiza glabra) и уральской (G1. uralensis) ингибировать ВИЧ in vitro и in vivo [3-5]. ГК была успешно использована в условиях клиники для лечения больных СПИДом [2,3,6]. Основным недостатком ГК является его малая эффективность как ингибитора обратной транскриптазы ВИЧ [7] и высокие дозы препарата, которые вызывают подавление репродукции ВИЧ [8].
Задача, на решение которой направлено заявленное техническое решение, заключается в поиске новых соединений в ряду производных ГК, обладающих анти-ВИЧ активностью.
В заявленном техническом решении синтезировано новое соединение - гликопептид ГК с S-бензил-L-цистеином: 3-O-{ 2-O-[N-(β-D-глюкопиранозилуроноил)-L-цистеин(S-бензил)-N-(β-D-глюкопиранозилуроноил)-L-цистеин(S-бензил)] } -(3β, 20β)-11-оксо-олеан-12-ен-30-(N-карбонил-L-цистеин)(S-бензил)-3-ил формулы (Iб), проявляющий анти-ВИЧ активность.
Биологические свойства данного соединения были изучены в лаборатории ретровирусов Института молекулярной биологии ГНЦ ВБ "Вектор".
Противовирусную активность препарата изучали на традиционной модели первично инфицированных ВИЧ лимфоидных клеток МТ-4. В работе использовали штамм ВИЧ-1/ЭВК. В качестве препаратов сравнения использовали глицирризиновую кислоту в концентрации 100 мкг/мл и один из известных противовирусных препаратов - ингибиторов репликации ВИЧ - азидотимидин (АЗТ) (зидовудин [9] ), облегчающий течение заболевания СПИДом, в концентрации 0,1 мкг/мл. Механизм действия АЗТ связан с подавлением фермента - обратной транскриптазы (ревертазы) ВИЧ, обеспечивающей считывание вирусной ДНК в пораженной клетке с РНК, содержащейся в вирионе (транспортной форме вируса). Однако со временем ВИЧ становится устойчивым к действию ингибиторов обратной транскриптазы, поэтому в последнее время АЗТ и его аналоги стали применять в сочетании с противовирусными, эффективными при ВИЧ-инфекции препаратами другого механизма действия - ингибиторами протеаз. Кроме того, АЗТ является более токсичным препаратом, чем ГК [8].
Цитотоксичность исследуемого соединения оценивали на культуре перевиваемых Т-лимфоцитов человека (линия МТ-4). Препарат растворяли в ДМСО и в соответствующих разведениях вносили в лунки 96-луночных планшетов (по три на каждое разведение) при рассеве клеток.
По окончании инкубации подсчитывали долю жизнеспособных клеток в камере Горяева после окрашивания трипановым синим. Строили дозазависимую кривую и определяли концентрацию препарата, вызывающего гибель 50% клеток, CD50 (токсическая доза).
Для оценки анти-ВИЧ активности соединения клетки МТ-4 (концентрация 2•106 клеток/мл) инфицировали штаммом ВИЧ-1/ЭВК с множественностью заражения 0,2-0,5 инфекционных единиц на клетку. После адсорбции вируса в течение 1 часа при 37oС инфицированные и контрольные клетки (без вируса) разводили ростовой культуральной средой до посевной концентрации 5•105 клеток/мл и вносили в лунки 96-луночных культуральных планшетов. Затем в соответствующие лунки вносили растворы исследуемого соединения (по три лунки на каждое разведение). Конечная концентрация исследуемых препаратов в клеточной суспензии составляла от 0,1 до 100 мкг/мл.
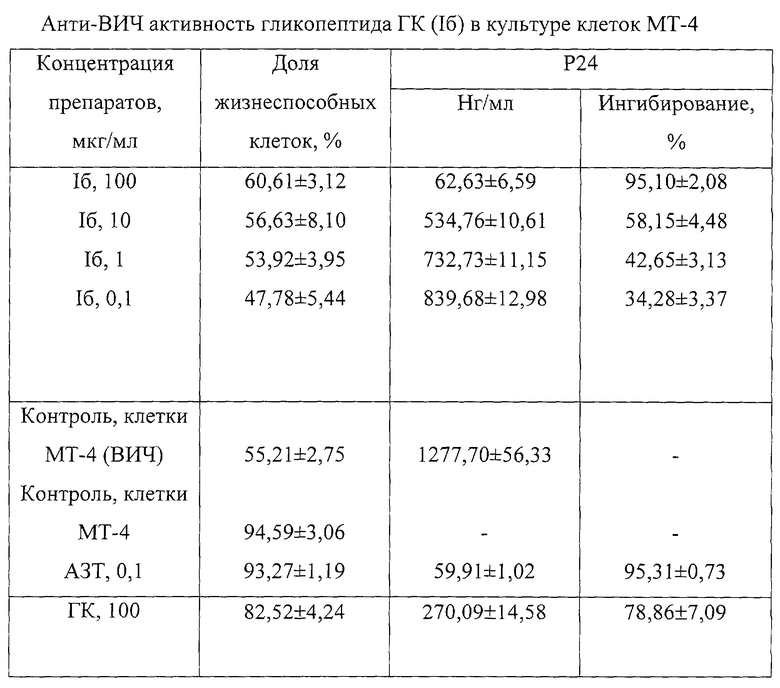
Ингибирующий эффект соединения оценивали на 4-е сутки культивирования измерением количества вирусного антигена - вирусоспецифического белка р24 - иммуноферментным методом. Кроме того, определяли долю жизнеспособных клеток после окрашивания трипановым синим путем подсчета в камере Горяева. На основе полученных экспериментальных данных строили дозазависимые кривые и определяли количественные характеристики ингибирования: ID50 - концентрацию соединения, на 50% подавляющую продукцию вируса или обеспечивающую 50% защиту клеток от гибели вследствие инфекции; ID90 - концентрацию соединения, на 90% подавляющую продукцию вируса или обеспечивающую 90% защиту клеток от гибели вследствие инфекции; IS - индекс селективности - отношение токсичной дозы CD50 к его эффективной дозе ID50. Результаты проведенных исследований приведены в таблице.
Установлено, что для гликопептида (Iб) 50%-ная цитотоксическая доза (СD50) (вызывающая 50% гибель клеток) составила 270 мкг/мл (198 мкМ). Данное соединение является ~ в 50-55 раз менее токсичным веществом, чем АЗТ (CD50= 3,5 мкМ) [8] и проявляет выраженную анти-ВИЧ-1 активность, с высокой эффективностью ингибируя накопление вирусоспецифического белка р24 (ID50=3 мкг/мл, что соответствует 2,2 мкМ). 90%-ное подавление репродукции вируса наблюдается при концентрации гликопептида (Iб) 100 мкг/мл (ID90=100 мгк/мл). В данной концентрации анти-ВИЧ активность (ингибирование р24) препарата (Iб) превосходит анти-ВИЧ эффект ГК и аналогична активности АЗТ в лечебной дозе (0,1 мкг/мл) (см. таблицу). В диапазоне концентраций от 0,1 до 100 мкг/мл данное соединение не является токсичным для клеток (см. таблицу). Кроме того, оказалось, что индекс селективности данного соединения IS=90, что существенно выше такового для ГК (IS=4,4-24). В концентрации 100 мкг/мл гликопептид (Iб) также превосходит ГК по проценту ингибирования вирусоспецифического белка р24 (см. таблицу).
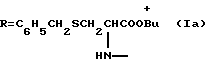
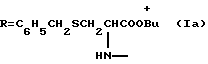
Синтез гликопептида (Iб) проводили путем конденсации ГК (94±2% чистоты) с трет-бутиловым эфиром S-бензил-L-цистеина методом активированных эфиров с помощью N, N'-дициклогексилкарбодиимида (DСС)-N-гидроксисукцинимида (HOSu). Выход карбоксизащищенного гликопептида (Iа) после очистки колоночной хроматографией (КХ) на силикагеле (СГ) составил 60%.
При обработке гликопептида (Iа) раствором СF3СООН в хлористом метилене при 20-22oС получали целевой продукт (Iб) с выходом 53% после очистки КХ на СГ.
Сущность технического решения иллюстрируется следующими примерами.
Пример 1. Синтез гликопептида (Iб).
а) К раствору 1,64 г (2 ммоль) глицирризиновой кислоты в 20 мл диоксана при 0oС прибавили 1,2 г (ммоль) N-гидроксисукцинимида, 1,2 г (ммоль) N,N'-дициклогексилкарбодиимида и перемешивали смесь при 0 - 5oС 2 ч. Отфильтровали осадок дициклогексилмочевины, к фильтрату прибавили 2,12 г (7 ммоль) трет-бутилового эфира S-бензил-L-цистеина и 1,3 мл триэтиламина в 30 мл диоксана. Смесь выдержали с периодическим перемешиванием при 20-22oС 18 ч, разбавили холодной водой и подкислили лимонной кислотой до рН~4. Осадок отфильтровали, промыли водой и высушили. Получили 2,36 г продукта (Iа), который хроматографировали на колонке с СГ, элюируя смесью хлороформа-метанола-воды, 300: 10:1, 200:10:1 и 100:10:1 (v%). Смесью 200:10:1 вымыли 1,58 г (60%) гомогенного по ТСХ карбоксизащищенного гликопептида (Iа). Rf 0,33 (хлороформ-метанол-вода, 45:10:1). [α]
ИК-спектр, ν, см-1: 3200-3600 (ОН, NH); 1740 (COOR); 1670 (С11=О); 1540 (CONH); 1500 (Ph). УФ-спектр, λmax (МеОН), нм (lg ε): 245 (4.40). Спектр ЯМР 13С (DMF-d7, δ, м. д. ): 199,69 (С11); 178,55 (С30); 170,53 (С13); 127,48 (С12); 105,04 (С1'); 104,27 (Cl''); 89,06 (C3); 82,30 (С2'); 169,85 (С6'); 169,79 (С6''); 76,75 (С5'); 76,18 (С5''); 75,17 (C3''); 73,11 (С4'); 72,79 (С4''); 62,03 (С9); 55,37 (С5); 49,0 (С18); 45,64 (С14); 39,84 (С1); 169,93; 170,00; 163,22; 163,03; 162,83; 162,45; 138,94; 138,86; 129,56; 128,98 (С6H5). Спектр ЯМР 1H (DMF-d7, δ, м.д.): 0,78; 0,84; 1,06; 1,08; 1,16; 1,26 (все с, 7 СН3, 21 Н); 1,38; 1,44 (оба с, 9 СН3, 27 Н, трет-бутил); 5,50 (= C12-Н); 7,20-7,40 (м, Н аром.).
Найдено, %: N 2,3. С84Н119N3О19S3. Вычислено, %: N 2,7. М.в. 1570,90.
б) 0,68 г (0,5 ммоль) гликопептида (Iа) обработали раствором СF3СООН в хлористом метилене (2 мл/20 мл) при 20-22oС, упарили досуха и хроматографировали на колонке с СГ, элюируя смесью хлороформ-метанол-вода, 100:10:1, 50: 10: 1, 25: 10:1 (v%). Выход гомогенного по ТСХ гликопептида (Iб) 0,32 г (53%) (аморфное вещество желтоватого цвета), [α]
ИК-спектр, ν, см-1: 3600-3200 (ОН, NH); 1710 (СООН); 1670 (С11=О); 1550 (CONH); 1510 (Ph). УФ-спектр, λmax (МеОН), нм (lg ε): 250 (4,5). Спектр ЯМР 13С (δ, м.д., ацетон-d6): 199,04 (С11); 177,04 (С30); 171,49 (С6'); 170,73 (С6''); 172,99 (С13); 103,20 (С1'); 102,88 (Cl''); 88,10 (C3); 80,08 (С2'); 75,31 (С5'); 74,85 (С5''); 74,10 (C3'); 73,71 (C3''); 72,55 (С2''); 71,69 (С4''); 61,03 (С9); 54,26 (С5); 47,75 (С18); 45,66 (С14); 44,65 (С20); 38,84 (Cl); 36,08; 35,54; 35,33 (CH2 Bzl); 51,27; 50,78; 50,53 (α-CH L-Cys); 169,98; 169,64; 169,32 (COOH L-Cys); 137,78; 137,59; 129,96; 128,91; 128,48; 128,37; 128,13; 127,93; 127,85; 127,70; 127,25; 126,78; 126,46; 126,37 (С6Н5). Спектр ЯМР 1Н (δ, м.д., ацетон-d6): 0,78; 0,84; 1,06; 1,14; 1,36 (21 Н, 7 СН3); 5,54 (=С12-Н); 7,2-7,4 (Н аром.).
Пример 2. Изучение анти-ВИЧ активности соединения (Iб).
Цитотоксичность исследуемого соединения оценивали на культуре перевиваемых Т-лимфоцитов человека (линия МТ-4). Препарат растворяли в ДМСО и в соответствующих разведениях вносили в лунки 96-луночных планшетов (по три на каждое разведение) при рассеве клеток. Посевная концентрация клеток составляла 0,5•106 клеток/мл. Клетки культивировали в 96-луночных планшетах для культур клеток фирмы "Costar" (США) на ростовой питательной среде (среда RPMI-1640 с добавлением 10% сыворотки плода коровы, 0,06% L-глутамина, 100 мкг/мл гентамицина) при 37oС и 5% СО2 в течение 4 суток.
По окончании инкубации подсчитывали долю жизнеспособных клеток в камере Горяева после окрашивания трипановым синим. Строили дозазависимую кривую и определяли концентрацию соединений, вызывающую гибель 50% клеток, CD50.
Для оценки анти-ВИЧ активности соединения (Iб) клетки МТ-4 (концентрация 2•106 клеток/мл) инфицировали штаммом ВИЧ-1/ЭВК с множественностью заражения 0,2-0,5 инфекционных единиц на клетку. После адсорбции вируса в течение 1 ч при 37oС инфицированные и контрольные клетки (без вируса) разводили ростовой культуральной средой до посевной концентрации 5•105 клеток/мл и вносили в лунки 96-луночных культуральных планшетов. Затем в соответствующие лунки вносили растворы исследуемого соединения (по три лунки на каждое разведение) и далее культивировали как описано выше. В качестве препаратов сравнения использовали очищенную глицирризиновую кислоту (95%) (ГК) - нативный гликозид солодкового корня в концентрации 100 мкг/мл и азидотимидин (АЗТ) (зидовудин) - известный анти-ВИЧ препарат в концентрации 0,1 мкг/мл. Конечная концентрация исследуемых препаратов в клеточной суспензии составляла от 0,1 до 100 мкг/мл.
Ингибирующий эффект соединения (Iб) оценивали на 4-е сутки культивирования измерением количества вирусного антигена р24 иммуноферментным методом. Кроме того, определяли долю жизнеспособных клеток после окрашивания трипановым синим путем подсчета в камере Горяева. На основе полученных экспериментальных данных строили дозазависимые кривые и определяли количественные характеристики ингибирования: ID50 - концентрацию соединения, на 50% подавляющую продукцию вируса или обеспечивающую 50%-ную защиту клеток от гибели вследствие инфекции; ID90 - концентрацию соединения, на 90% подавляющую продукцию вируса или обеспечивающую 90%-ную защиту клеток от гибели вследствие инфекции; IS - индекс селективности - отношение токсичной дозы CD50 к его эффективной дозе ID50.
Установлено, что для исследуемого соединения 50%-ная цитотоксическая доза СD50 составила 270 мкг/мл (198 мкМ).
Гликопептид (Iб) проявляет выраженную анти-ВИЧ-1 активность, с высокой эффективностью ингибируя накопление вирусоспецифического белка р24 (ID50=3 мкг/мл, что соответствует 2,2 мкМ). ID90=l00 мкг/мл (90%-ное подавление репродукции вируса). В данной концентрации противовирусная активность препарата аналогична активности АЗТ и превосходит ингибирующий эффект (накопление р24) ГК в равной дозе (100 мг/кг) (см. таблицу). Гликопептид (Iб) является ~ в 50-55 раз менее токсичным веществом для ВИЧ-инфицированных клеток в исследованном диапазоне концентраций (CD50=270 мкг/мл или 198 мкМ) по сравнению с АЗТ (CD50=3,5 мкМ) [8].
Индекс селективности гликопептида (Iб) или химиотерапевтический индекс IS= 90 (по ингибированию р24 ВИЧ-1), что существенно выше такового для глицирризиновой кислоты (IS=4,4-24) [10].
ЛИТЕРАТУРА
1. E. De Clerq. New selective antiviral agents active against the AIDS virus.// Trends Pharmacol. Sci, 1987, v. 8, N 9, р. 339-345.
2. E. De Clerq. Toward improved anti-HIV chemotherapy: therapeutic strategies for interferon with HIV infections. //J. Med. Chem., 1995, v. 38, N 14, p. 2491-2517.
3. A. J.Vlietinck, T. De Bruyne, S.Apers and L.A.Pieters. Plant-Derived Leading Compounds for Chemotherapy of Human Immunodeficiency Virus (HIV) infection. //Planta Medica, 1998, v. 64, p. 97-109.
4. M. Ito, H.Nakashima, M.Baba, R.Pauwels, E. De Clerq, Sh. Shigeta and N. Yamamoto. Inhibitory effect of glycyrrhizin on the in vitro infectivity and cytopathic activity of the human immunodeficiency virus [HIV (HTLV-III/LAV)]. //Antiviral Res., 1987, v. 7, p. 127-137.
5. M. Ito, A. Sato, K.Hirabayashi, F.Tanabe, Sh.Shigeta, M.Baba, E. De Clerq, H. Nakashima and N. Yamamoto. Mechanism of inhibitory effect of glycyrrhizin on replication of human immunodeficiency virus (HIV). // Antiviral Res., 1988, v. 10, p. 289-298.
6. Г. А. Толстиков, Л.А.Балтина, Э.Э.Шульц, А.Г.Покровский. Глицирризиновая кислота. //Биоорганическая химия, 1997, т. 23, 9, с. 691-709.
7. О. А. Плясунова. Скрининг и изучение препаратов - ингибиторов вируса иммунодефицита человека. Дисс. канд. биол. наук. Кольцово, 1992, 55 с.
8. О.А.Плясунова, И.Н.Егоричева, Н.В.Федюк, А.Г.Покровский, Л.А.Балтина, Ю. И. Муринов, Г.А.Толстиков. Изучение анти-ВИЧ активности β-глицирризиновой кислоты. //Вопросы вирусол., 1992, 5 - 6, с. 235-238.
9. М. Д. Машковский. Лекарственные средства. Пособие для врачей. Изд. 14-е, т. 2. Москва: "Новая Волна", 2000, с. 330.
10. О. А.Плясунова. Скрининг и изучение препаратов - ингибиторов вируса иммунодефицита человека. Дисс. канд. биол. наук в форме научного доклада. Кольцово, 1992, 55 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЛИКОПЕПТИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С ГЛИЦИЛ-L-ФЕНИЛАЛАНИНОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ-1 АКТИВНОСТЬ | 2006 |
|
RU2315058C1 |
| АМИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 5-АМИНОУРАЦИЛОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ АКТИВНОСТЬ | 2001 |
|
RU2199547C2 |
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ 3-O-β-D-ГЛЮКУРОНОПИРАНОЗИЛ-β-D-ГЛЮКУРОНОПИРАНОЗИД ОЛЕАН-9( 11),12( 13)-ДИЕН-30-ОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩЕЕ АНТИ-ВИЧ-1 АКТИВНОСТЬ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2475246C2 |
| 3,28-ДИ-О-НИКОТИНАТ БЕТУЛИНА, ПРОЯВЛЯЮЩИЙ ГЕПАТОПРОТЕКТОРНУЮ И АНТИ-ВИЧ АКТИВНОСТЬ | 1999 |
|
RU2174982C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИТЕРПЕНОВЫХ ГЛИКОПЕПТИДОВ | 1994 |
|
RU2083587C1 |
| N'-{N-[3-ОКСО-20(29)-ЛУПЕН-28-ОИЛ]-9-АМИНОНОНАНОИЛ}-3-АМИНО-3-ФЕНИЛПРОПИО НОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2211843C1 |
| ГЛИКОПЕПТИД β-ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С ДИМЕТИЛОВЫМ ЭФИРОМ L-АСПАРАГИНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ АНТИ-СПИД-АКТИВНОСТЬ | 1991 |
|
RU2024544C1 |
| ГЛИКОПЕПТИД β-ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С МЕТИЛОВЫМ ЭФИРОМ ГЛИЦИЛ-L-ВАЛИНА, ПРОЯВЛЯЮЩИЙ АНТИ-СПИД-АКТИВНОСТЬ | 1991 |
|
RU2024542C1 |
| 4-НИТРО-6-ТРИФТОРМЕТИЛ-1,2,3-БЕНЗОТРИТИОЛ-1-ОКСИД В КАЧЕСТВЕ ИНГИБИТОРА РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2007 |
|
RU2366419C2 |
| ГЛИКОПЕПТИД β-ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С ДИБУТИЛОВЫМ ЭФИРОМ L-ГЛУТАМИНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ АНТИ-СПИД-АКТИВНОСТЬ | 1991 |
|
RU2024546C1 |
Описывается новое химическое соединение - производное глицирризиновой кислоты, а именно гликопептид глицирризиновой кислоты с S-бензил-L-цистеином [I] : 3-О-{ 2-O-[N-(β-D-глюкопиранозилуроноил)-L-цистеин(S-бензил)-N-(β-D-глюкопиранозилуроноил)-L-цистеин(S-бензил)]}-(3β,20β)-11-оксо-олеан-12-ен-30-(N-карбонил-L-цистеин(S-бензил)-3-ил, обладающий анти-ВИЧ активностью. Данное соединение превосходит глицирризиновую кислоту (ГK) по ингибированию вирусoспецифического белка р24 (вирусного антигена) при использовании в равных концентрациях (100 мкг/мл) в культуре клеток МТ-4, инфицированных штаммом ВИЧ-1/ЭВК, а также превосходит ГК (IS = 4,4-24) по индексу селективности (IS = 90). В концентрации 100 мкг/мл анти-ВИЧ активность препарата аналогична активности азидотимидина в лечебной дозе, в отличие от последнего препарат менее токсичен для клеток МТ-4. 1 табл. 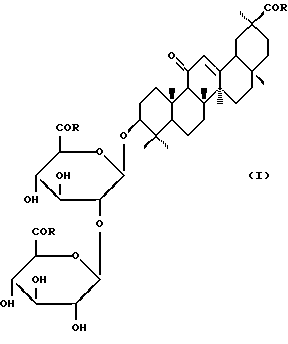
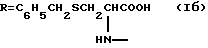
Гликопептид глицирризиновой кислоты с S-бензил-L-цистеином общей формулы I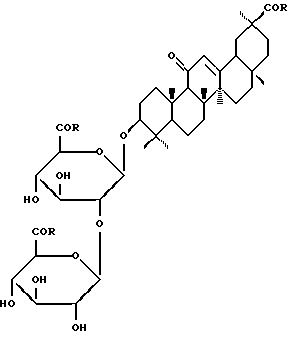
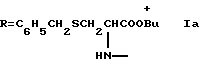
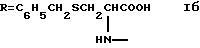
проявляющий анти-ВИЧ активность.
| A.J.Vlietinck | |||
| Planta Medica, 1998, 64, p.97-109 | |||
| M.Jto, A.Sato | |||
| Antiviral Res., 1988, 10, p.289-298 | |||
| Толстиков Г.А | |||
| и др | |||
| Биоорганическая химия, 1997, т | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Счетчик оборотов горизонтального вала машины | 1925 |
|
SU691A1 |
Авторы
Даты
2003-02-10—Публикация
2001-03-30—Подача