Изобретение относится к новому биологически активному химическому соединению, конкретно к 3,28-ди-О-никотинату бетулина (1), формулы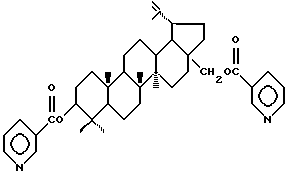
проявляющему гепатопротекторную и анти-ВИЧ активность.
Соединение (1) и его свойства в литературе не описаны.
Номер Государственной регистрации соединения (1) - N 10640198.
В последние годы ведется интенсивный поиск высокоэффективных препаратов на основе доступных природных веществ, обладающих комплексом ценных фармакологических свойств. В связи с этим особый интерес представляет синтез малотоксичных модифицированных аналогов природных соединений, сочетающих различные виды биологической активности.
Наиболее близким по структуре и свойствам к предлагаемому соединению является тритерпеноид лупановой группы - бетулин (2), содержание которого в коре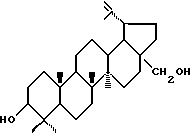
белоствольных берез вида Betula pendula достигает 35- 40%. Известно, что бетулин (2), наряду с гиполипидемическим действием, оказывает желчегонное и гепатопротекторное действия [1] . Бетулин (2) обладает также анти- ВИЧ активностью [2] . В связи с этим поиск новых соединений в ряду лупановых тритерпеноидов, в частности на основе бетулина (2), обладающих более высокой гепатопротекторной и анти-ВИЧ активностью, является актуальным.
В заявленном техническом решении синтезировано новое малотоксичное производное бетулина, а именно 3,28-ди-О-никотинат бетулина (1), проявляющее гепатопротекторную и анти-ВИЧ активность.
При изучении гепатопротекторной активности соединения (1) в качестве референс-препаратов использовали известные препараты карсил и силибор [3]. Однако следует отметить, что достижение хорошего эффекта при применении этих препаратов возможно только при длительном использовании в значительных дозах (не менее 50 мг/кг). Кроме того, карсил, будучи импортным препаратом (Болгария), в настоящее время стал недоступен большой массе больных. Таким образом, весьма актуальной задачей является поиск более эффективного, низкотоксичного и дешевого гепатопротекторного препарата.
В качестве препарата сравнения при изучении анти-ВИЧ активности соединения (1) использовали азидотимидин.
Острая токсичность (LD50) и эффективная доза (ED50) соединения (1) определялись на белых беспородных мышах массой 20-25 г при введении в желудок. Параметры токсичности и единицы действия вычислялись по Литчфильду и Уилкоксону. На основании Постановления Госкомитета стандартов СМ СССР от 10 марта 1976 г. N 579 данное соединение относится к IV классу малоопасных веществ (LD50=6.5 мг/кг). ED50 соединения (1) составила 11.7 мг/кг.
Гепатопротекторное действие соединения (1) оценивали по желчесекреторной и желчевыделительной функциям печени на интактных крысах и у животных с экспериментальным гепатитом, вызванным тетрахлорметаном. В качестве препаратов сравнения с соединением (1) использовали структурный аналог - бетулин (2) и известные фармакологические гепатопротекторные препараты флавоноидной структуры - силибор и карсил. Результаты опытов приведены в табл. 1 и 2.
Установлено, что соединение (1) в дозе 50 мг/кг увеличивает секрецию желчи гепатоцитами крыс во все сроки наблюдения в 1.5-2 раза эффективнее препаратов сравнения - бетулина и силибора. Кроме того, соединение (1) аналогичным образом усиливает желчеобразовательную функцию гепатоцитов крыс (табл. 1). В табл. 2 показано влияние соединения (1) на функциональное состояние печени при CCl4-гепатите у крыс. При гепатите резко угнетается желчеобразовательная и желчевыделительная функции печени по сравнению с интактными животными. Как видно из табл. 2, соединение (1) оказалось более активным даже в более низкой (в 5 раз) дозе (10 мг/кг), чем препарат сравнения - карсил. Соединение (1) повышает функциональную активность гепатоцитов во все сроки опытов, в то время как карсил - только во 2-й и 3-й часы. Кроме того, соединение (1) увеличивает желчеобразование (общий вес желчи) у животных с экспериментальным CCl4-гепатитом активнее карсила более чем в 1.5 раза.
Анти-ВИЧ активность соединения (1) была исследована на традиционной модели высокочувствительной к ВИЧ клеточной линии МТ-4 - перевиваемых лимфоцитов человека, первично инфицированных вирусом иммунодефицита человека 1 типа - штамм ВИЧ-1/ЭВК. В качестве фармакологического аналога использовали известный ингибитор вирусной обратной транскриптазы - азидотимидин (АЗТ), широко применяемый в практике лечения ВИЧ-инфекции, но обладающий высокой токсичностью, малой эффективностью в блокировании репродукции ВИЧ в клетках моноцитов/макрофагов и др. [4].
Эффективность противовирусного действия соединения (1) была оценена с помощью комплекса методов, позволяющих получить достаточно полную информацию об особенностях его анти-ВИЧ действия:
1) определение цитотоксичности препарата;
2) определение степени защиты инфицированных ВИЧ-клеток от гибели вследствие инфекции путем определения их жизнеспособности методом исключения трипановым синим;
3) количественное определение накопления вирусного белка p24 иммуноферментным методом.
Установлено, что соединение (1) эффективно подавляет накопление вирусспецифического белка p24 (ID50=0.02 мкг/мл), не оказывая при этом защитного действия, и в диапазоне концентраций 0.001 - 20.0 мкг/мл не токсично для клеток МТ-4 (IC50 > 20.0 мкг/мл). (табл. 3). Индекс IS соединения (1) > 1000 (подавление накопления антигена p24 > 1000), что свидетельствует о его выраженном анти-ВИЧ действии. Соединение (1) по всем показателям: ID50 (эффективная доза), IC50 (токсичная доза) и IS (терапевтический индекс) имеет значительные преимущества по сравнению с бетулином, у которого ID50=23, IC50=45, IS=1.9[2].
Синтез соединения (1) проводили взаимодействием бетулина с хлорангидридом никотиновой кислоты в среде пиридина - трибутиламина с выходом 93.6%. Аналитически чистый продукт получали путем экстракции бензолом.
Таким образом, предложено новое малотоксичное производное среди тритерпеноидов лупановой группы-3,28-ди-О-никотинат бетулина (1). Соединение (1) малотоксично, обладает выраженной гепатопротекторной активностью, превышающей эффект известных гепатопротекторов силибора и карсила в более низкой дозе, сочетающейся с выраженной анти-ВИЧ активностью.
Сущность изобретения демонстрируется следующими примерами.
Пример 1. Получение диникотината бетулина (1).
К раствору 1 ммоль (0.44 г) бетулина в смеси безводных 5 мл пиридина и 5 мл трибутиламина при перемешивании и охлаждении (0-5oC) добавляли 3 ммоль (0.43 г) свежеприготовленного по методике [5] хлоргидрата хлорангидрида никотиновой кислоты. Температуру доводили до комнатной и перемешивали еще 4 ч. Реакционную массу выливали в 50 мл холодной воды, подкисляли HCl и экстрагировали бензолом. Экстракт промывали водой, 5% раствором HCl, снова водой, сушили Na2SO4 и упаривали в вакууме. Выход 0.59 г (93.6%). Rf=0.55 (элюент хлороформ - метанол = 20:1). Тплпл.=116-118oC. Найдено,%: С-77.54, Н-8.21, N-4.05. C42H56O4N2. Вычислено,%: С-77.26, Н-8.64, N-4.29. УФ-спектр (EtOH), λmax /HM: 263 (Ig ε 4.18). ИК-спектр (υ, см-1, вазелиновое масло): 1730(С= O), 1650(CH-CH2), 1600 (Ar), 1470, 1390, 1330, 1300, 1260, 1220, 1150, 1050, 990, 910 (CH=CH2), 870. Спектр 1H ЯМР (δ, м.д., J/Гц): 0.82, 0.84, 0.91, 0.94, 1.00 (5c, 15H, 5 CH3), 1.00-2.00 (м, CH2, CH), 1.63 (с, 3H, CH3), 2.48 (ддд, 1H, H19,J= 5,7, 10.6, 11.6), 4.05 (д, 1H, H28, J= 11), 4.45-4.53 (м, 2H, H28, H29), 4.60-4.67 (м, 2H, H3, H29), 7.25-7.40, 8.18-8.26, 8.67-8.73, 9.12-9.20 (все м, 8H, H аромат.). Спектр 13С ЯМР ( δ м.д.): 38.3 (C1), 23.7 (C2), 82.2 (C3), 37.6 (C4), 55.6 (C5), 18.1 (C6), 34.6 (C7), 40.9 (C8), 50.2 (C9), 37.0 (С 10), 20.8 (C11), 25.1 (C12), 38.1 (C13), 42.7 (C14), 27.0 (C15), 29.5 (C16), 47.7 (C17), 46.6 (C18), 48.9(C19), 149.8 (C20), 29.8 (C21), 34.0 (C22), 28.0 (C23), 16.0(C24), 16.7(C25), 16.1 (C26), 14.7 (C27), 63.7 (C28), 110.0 (C29), 19.1 (C30), 164.8, 165.8 (-O-C=O), 123.2, 123.2, 126.2, 126.6, 137.0, 137.0, 149.8, 150.8, 153.1, 153.3 (С аромат,),
Пример 2. Изучение гепатопротекторной активности соединения (1).
Опыты проводили на 120 крысах массой 180-200 г. Единицу действия ЕД50= 11.7 мг/кг и токсичную дозу LD50= 6.5 мг/кг определяли по методике [6]. Влияние соединения (1) на функциональное состояние печени оценивали по желчесекреторной и желчевыделительной функции печени по методике [7] на интактных крысах и у животных с экспериментальным CCl4-гепатитом. Секрецию желчи выражали в мг/мин на 100 г массы животного, а желчевыделительную функцию - по общему количеству выделенной желчи за каждый час и в сумме за 4 ч наблюдения на 100 г массы крыс. В качестве препаратов сравнения использовали тритерпеноид лупановой группы - бетулин (2) и известные гепатопротекторы - силибор и карсил.
В первой серии опытов изучали влияние соединения (1) на функциональное состояние печени у интактных животных. В качестве препаратов сравнения использовали тритерпеноид лупановой группы - бетулин (2) и силибор в равных дозах 50 мг/кг, обычно используемой в практике при лечении силибором. Результаты опытов приведены в табл. 1.
В следующей серии опытов изучали влияние соединения (1) на функциональную активность печени крыс при гепатите, вызванном CCl4 по методике [8]. Соединение (1) брали в дозе 10 мг/кг после определения терапевтической дозы ЕД50=11.7 мг/кг, а препарат сравнения карсил в обычно используемой в практике [9] дозе 50 мг/кг. Результаты опытов приведены в табл. 2.
Таким образом, соединение (1) обладает выраженной гепатопротекторной активностью, в более низкой дозе превышающей эффект известных гепатопротекторов - силибора и карсила.
Пример 3. Изучение анти-ВИЧ активности соединения (1).
Анти-ВИЧ свойства представленного соединения (1) были изучены на традиционной модели первично инфицированных ВИЧ лимфоидных клеток МТ-4. В работе использовали штамм ВИЧ-1/ЭВК. Цитотоксичность соединения оценивали в культуре перевиваемых Т лимфоцитов человека линии МТ-4. Препарат растворяли в этиловом спирте и в соответствующих разведениях вносили в лунки 96-луночных культуральных планшетов (по три лунки на каждое разведение) при рассеве клеток. Посевная концентрация составляла 5•105 клеток/мл. Далее клетки культивировали на ростовой среде (среда RPMI-1640 с добавлением 10% сыворотки плода коровы, 0,06% L-глутамина, 100 мкг/мл гентамицина и 60 мкг/мл линкомицина) при 37oC и 5% углекислого газа в течение 4 суток. По окончании инкубации подсчитывали долю жизнеспособных клеток в камере Горяева после окрашивания трипановым синим. Строили дозозависимую кривую и определяли концентрацию соединений, вызывающую гибель 50% клеток - CD50. Для оценки анти-ВИЧ активности соединения клетки МТ-4 инфицировали штаммом ВИЧ-1/ЭВК с множественностью заражения 0.2-0.5 инфекционных единиц на клетку. После адсорбции вируса в течение 1 ч при 37oC инфицированные и контрольные клетки разводили ростовой средой до посевной концентрации 5•105 клеток/мл и вносили в лунки 96-луночных культуральных планшетов. Затем вносили раствор предлагаемого соединения (1) (по три лунки на каждое разведение) и далее культивировали как описано выше. Концентрация соединения составляла от 0.001 до 20 мкг/мл. Ингибирующий эффект соединения (1) оценивали на 4-е сутки культивирования измерением количества вирусного антигена p24 иммуноферментным методом. Кроме того, определяли анти-ВИЧ активность, исходя из степени защиты инфицированных клеток от гибели в результате вирусной инфекции, подсчитывая долю жизнеспособных клеток в камере Горяева после окрашивания трипановым синим. На основе полученных результатов строили дозозависимые кривые и определяли количественные характеристики ингибирования репродукции ВИЧ: ID50 - концентрацию соединения, на 50% подавляющую продукцию вируса или обеспечивающую 50% защиту клеток; IS - индекс селективности: отношение токсичной дозы соединения IC50 к его эффективной дозе ID50. Результаты опытов приведены в табл. 3.
Список литературы
1. Василенко Ю.К., Семенченко В.Ф., Фролова Л.М., Коноплева Г.Е., Парфентьева Е. П. , Скульте И.В. Фармакологические свойства тритерпеноидов коры березы //Эксперим. и клин. фармакол. 1993. Т. 56. N 4. С. 53-55.
2. Fujioka Т., Kashiwada Y., Kilkuskie R. E., Cosentino L. M., Ballas L. M. , Jiang J. B., Janzen W. P., Chen I.-S., Lee K.-H. Anti-AIDs agents, II. Betulinic acid and Platanic acid as anti-HIV principles from Syzigium Claviflorum, and the anti-HIV activity of structurally related triterpenoids//J. Nat. Prod. 1994. V. 57. P. 243-247.
3. Машковский М. Д. Лекарственные средства. М.:Медицина, 1993. Т.П. С. 612.
4. Плясунова О.А., Егоричева И.Н., Федюк Н.В., Покровский А.Г., Балтина Л.А., Муринов Ю.И., Толстиков Г.А. Изучение анти-ВИЧ активности β-глицирризиновой кислоты //Вопросы вирусологии, 1992, N 5-6, С. 235-238.
5. Наумова Б.С., Чекмарева И.Б., Жданович Е.С., Преображенский Н.А. Получение производных никотиновой кислоты //Хим.-фарм. Журнал, 1969. Т.3. N 5. С. 11-12.
6. Беленький М.Л. Элементы количественной оценки фармакологического эффекта. Л.-1963. 186 с.
7. Скакун Н.П., Олейник Л.Н. Сравнительное действие атропина и метацина на внешнесекреторную функцию печени //Журнал фармакол. и токсил. 1967. N 3. С. 334-337.
8. Николаев С.М. Растительные лекарственные препараты при повреждениях гепатобилиарной системы. Новосибирск. 1992. 155с.
9. Насыров X.М., Чепурина Л.С., Киреева Р.М. Изучение гепатопротекторного и желчегонного действия производных глицирризиновой кислоты //Эксперим. и клинич. Фармакология. 1995. N 6. С. 60-63.
| название | год | авторы | номер документа |
|---|---|---|---|
| 3-О-2-ДЕЗОКСИ-α-L-РАМНОПИРАНОЗИД МЕТИЛОВОГО ЭФИРА ГЛИЦИРРЕТОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ГЕПАТОПРОТЕКТОРНУЮ АКТИВНОСТЬ | 1996 |
|
RU2148584C1 |
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ БИСИЗОНИКОТИНОАТ БЕТУЛИНА, ПРОЯВЛЯЮЩЕЕ ПРОТИВОЯЗВЕННУЮ, ПРОТИВОВОСПАЛИТЕЛЬНУЮ И ГЕПАТОПРОТЕКТОРНУЮ АКТИВНОСТЬ | 2013 |
|
RU2538212C1 |
| ГЛИКОПЕПТИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С S-БЕНЗИЛ-L-ЦИСТЕИНОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ АКТИВНОСТЬ | 2001 |
|
RU2198177C2 |
| АМИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 5-АМИНОУРАЦИЛОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ АКТИВНОСТЬ | 2001 |
|
RU2199547C2 |
| ГЛИКОПЕПТИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С ГЛИЦИЛ-L-ФЕНИЛАЛАНИНОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ-1 АКТИВНОСТЬ | 2006 |
|
RU2315058C1 |
| N'-{N-[3-ОКСО-20(29)-ЛУПЕН-28-ОИЛ]-9-АМИНОНОНАНОИЛ}-3-АМИНО-3-ФЕНИЛПРОПИО НОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2211843C1 |
| 3-О-2-ДЕЗОКСИ-α-D-ГАЛАКТО- ИЛИ α-L-РАМНОПИРАНОЗИД МЕТИЛОВОГО ЭФИРА ГЛИЦИРРЕТОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ПРОТИВОЯЗВЕННУЮ АКТИВНОСТЬ И СТИМУЛИРУЮЩИЙ РЕПАРАТИВНУЮ РЕГЕНЕРАЦИЮ КОЖИ | 1996 |
|
RU2148583C1 |
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ 3-O-β-D-ГЛЮКУРОНОПИРАНОЗИЛ-β-D-ГЛЮКУРОНОПИРАНОЗИД ОЛЕАН-9( 11),12( 13)-ДИЕН-30-ОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩЕЕ АНТИ-ВИЧ-1 АКТИВНОСТЬ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2475246C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3β,28-ДИ-O-АЦЕТИЛ-29-НОР-20(30)-ЛУПИНА | 2009 |
|
RU2402562C1 |
| БИС-(2-ЭТИЛГЕКСАНОАТО)БИС(ТРИЭТИЛЕНТЕТРАМИН) КОБАЛЬТ (II), ПРОЯВЛЯЮЩИЙ СВОЙСТВА СТИМУЛЯТОРА ГЕМОПОЭЗА | 1994 |
|
RU2078767C1 |
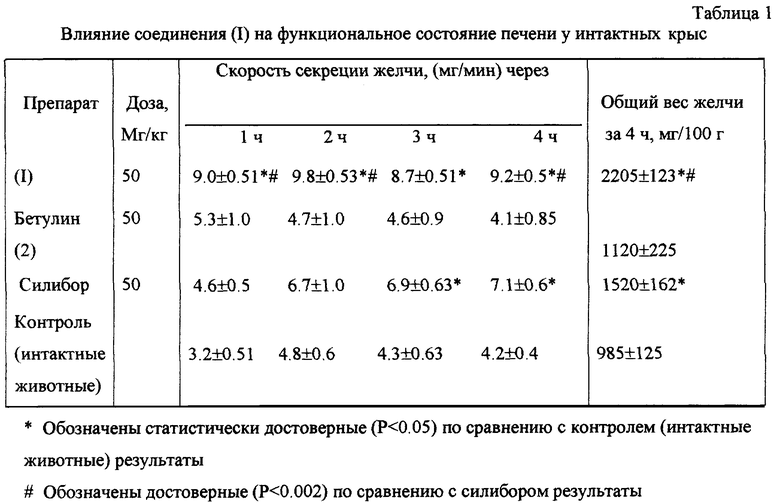
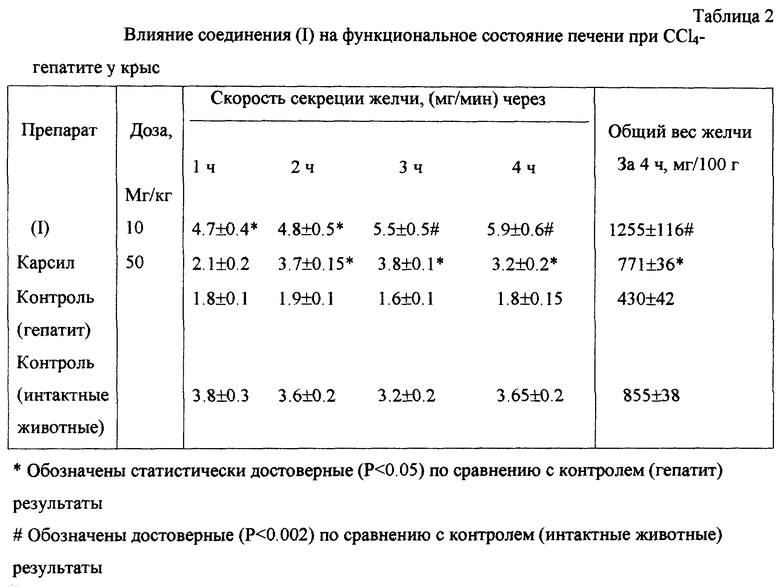

Описывается новое химическое соединение, а именно 3,28-ди-О-никотинат бетулина формулы I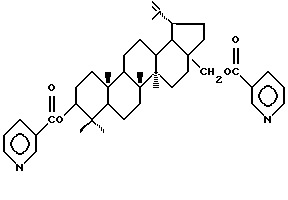
проявляющий гепатопротекторную и анти-ВИЧ активность. Соединение является малотоксичным веществом, обладает выраженной гепатопротекторной активностью, превосходящей эффект бетулина и силибора, сочетающейся с анти-ВИЧ активностью. 3 табл.
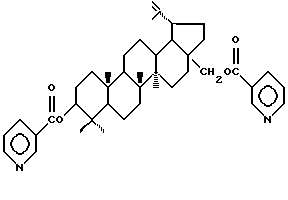
проявляющий гепатопротекторную и анти-ВИЧ активность.
| Эксперими клин | |||
| фармакология | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| Машковский М.Д | |||
| Лекарственные средства | |||
| -М.: Медицина, 1993, т | |||
| II, с.612 | |||
| J | |||
| Nat | |||
| Prod | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| Вопросы вирусологии, 1992, № 5-6, C.235-238 | |||
| Хим.-фарм.журнал, 1969, т.3, № 5, с | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Беленький М.Л | |||
| Элементы количественной оценки фармакологического эффекта | |||
| Приспособление к комнатным печам для постепенного сгорания топлива | 1925 |
|
SU1963A1 |
| Пружинная погонялка к ткацким станкам | 1923 |
|
SU186A1 |
| Журнал фармакол и токсил | |||
| Запальная свеча для двигателей | 1924 |
|
SU1967A1 |
| Растительные лекарственные препараты при повреждениях гепатобилиарной системы, Новосибирск: 1992г., с | |||
| Канатное устройство для подъема и перемещения сыпучих и раздробленных тел | 1923 |
|
SU155A1 |
| Экспер | |||
| и клинич | |||
| Фармакология, 1995, № 6, с.60-63. | |||
Авторы
Даты
2001-10-20—Публикация
1999-11-05—Подача