Область техники, к которой относится изобретение
Изобретение относится к фотокатализатору для получения водорода, к способу его приготовления и к способу получения водорода с его применением, а более конкретно к фотохимической реакции, в ходе проведения которой в присутствии CdZnMS фотокатализатора, предлагаемого в соответствии с настоящим изобретением, из воды эффективно и успешно с экономической точки зрения получают водород.
Предпосылки создания изобретения
Водород обычно применяют при получении аммиака и метанола и его используют в качестве существенного элемента при получении насыщенных соединений. Кроме того, он играет основную роль в процессах гидроочистки, включающих присоединение водорода, десульфуризацию, денитрацию, деметаллирование и особенно гидрогенизацию диоксида углерода, вызывающего глобальное потепление. Более того, водород рассматривают как не загрязняющий окружающую среду источник энергии и замену существующим ископаемым топливам.
Существует множество различных типов известных методов получения водорода, которые включают его извлечение из ископаемых топлив, таких как нефть, модифицирование природного газа, взаимодействие пара с железом при высокой температуре, взаимодействие воды со щелочным металлом, электролиз воды и т. д.
Однако из-за необходимости затрат чрезмерных количеств тепловой или электрической энергии такие технологии с экономической точки зрения считаются неблагоприятными, а при модифицировании, в частности, ископаемых топлив в качестве побочного продукта образуется большое количество диоксида углерода. В случае электролиза воды необходимо разрешать такие проблемы, как кратковременный срок службы электродов и выделение в качестве побочного продукта кислорода. Таким образом, разрешение этих проблем вследствие огромных затрат на технические средства при получении водорода до сих пор оказывалось экономически неэффективным.
Благодаря низкому удельному весу водород способен легко преодолевать силу тяжести, и наибольшая часть водорода содержится в воде или в форме неорганических материалов. По этим причинам в атмосфере находится лишь небольшое количество водорода. Очистка водорода, содержащегося в форме неорганических материалов, также сопряжена с очень большими затруднениями технологического порядка. Даже если очистка водорода с практической точки зрения возможна, то экономически также неэффективна. Таким образом, разработка технологии получения высокочистого водорода из воды имеет очень важное значение для решения неотложной проблемы создания заменяющих источников энергии.
В последнее время разработана технология получения водорода, в которой для разложения воды на водород и кислород применяют фотохимический катализатор. Однако до настоящего времени технике фотохимических катализаторов получения водорода посвящено очень мало публикаций. Типичными примерами публикаций являются выложенные заявки на патенты JP 62-191045 и 63-107815 от имени Sho.
В выложенной заявке на патент JP 62-191045 от имени Sho показано, что водород получают из водного раствора Na2S реакцией фотолиза в присутствии соединения редкоземельного элемента. Соединение редкоземельного элемента в качестве катализатора обладает также тем достоинством, что проявляет оптическую активность при излучении в видимой области спектра.
В выложенной заявке на патент JP 63-107815 от имени Sho описана реакция фотолиза, в ходе проведения которой в качестве фотохимического катализатора для получения водорода из раствора метанола в воде используют композиционный оксид ниобия и щелочно-земельного металла. Точно также достоинство этого фотохимического катализатора заключается в оптической активности при излучении в видимой области спектра.
Однако упомянутой известной технологии свойственны недостатки, состоящие в том, что количество получаемого водорода мало, а производительность составляет всего 10 мл/0,5 г/ч.
В заявках KR 95-7721, 95-30416 и 96-44214 также высказывается и предлагается возможность разрешения вышеописанных проблем.
В заявке KR 95-7721 предлагается фотокатализатор, отвечающий следующей формуле I:
Cs(a)/K4Nb6O17 I
Осуществление этой технологии в присутствии фотокатализатора формулы I оказывает слабое влияние на окружающую среду и позволяет получать водород при комнатной температуре. Однако кислородсодержащие органические соединения, которые при получении водорода действуют как промоторы выделения водорода, создают препятствие для повторного использования этих реагентов.
В заявке KR 95-30416 предлагается фотокатализатор, отвечающий следующей формуле II:
Cs(a)M(c)/S(b) II
Осуществление этой технологии тоже оказывает слабое влияние на окружающую среду и позволяет получать водород при комнатной температуре без кислородсодержащего органического соединения, которое действует как промотор выделения водорода, но создает некоторые проблемы срока службы и стабильности фотокатализатора формулы II. Так, например, когда носитель фотокатализатора пропитывают щелочным металлом, таким как цезий (Cs), значительно увеличивается количество выделяющегося водорода, но стабильность катализатора снижается.
Кроме того, в заявке KR 96-44214 описан фотокатализатор, отвечающий следующей формуле III:
Pt(a)/Zn[M(b)]S III
Осуществление такой технологии точно так же оказывает слабое влияние на окружающую среду. Несмотря на зависимость от доноров электронов и восстановителей, фотокатализатор формулы III превосходит упомянутые ранее известные технические решения по простоте приготовления, стабильности и сроку службы, а также по оптической активности при излучении в видимой области спектра. Но количество получаемого водорода оказывается экономически неэффективным.
В заявке KR 98-37179 предлагается фотокатализатор, отвечающий следующей формуле IV:
Pt(a)/Zn[M(b)]S IV
Осуществление такой технологии также оказывает слабое влияние на окружающую среду, и этот фотокатализатор формулы IV в определенной степени проявляет оптическую активность в видимой области спектра. Такой фотокатализатор намного проще в приготовлении и обусловливает образование намного меньших количеств побочных продуктов. Однако количество получаемого водорода все еще оказывается экономически неэффективным.
Для разрешения упомянутых выше проблем в заявке KR 98-37180 авторами настоящего изобретения был предложен фотокатализатор, отвечающий следующей формуле V:
m(A)/Cd[M(B)]S V
Фотокатализатор формулы V проявляет оптическую активность в видимой области спектра, регулируемую оптическим фильтром, равно как и на солнечном свету. Количество выделяемого водорода намного больше, а срок службы такого катализатора оказывается полубесконечным. Введение различных легирующих металлов и промоторов и применение других, новых методов позволяет этому средству, приготовленному по ранее известному техническому решению, преодолеть ограничения активности источниками света и дает возможность предложить более простой способ приготовления. Подобным же образом срок службы фотокатализатора также становится более длительным, а количество водорода, выделяемое из воды, заметно большим, чем в известных в данной области техники случаях. Однако это средство проявляет ограничение активности по водороду только одним восстановителем.
Для экономически успешного разрешения упомянутых выше проблем в заявке KR 99-22954 авторами настоящего изобретения был предложен фотокатализатор, отвечающий следующей формуле VI:
m(a)/Cd[M(b)]S VI
В соответствии с этим известным техническим решением предлагаются новый CdS фотокатализатор (фотокаталитическая система), его приготовление и строение новой восстановительной системы с сульфитом для экономически эффективного выделения водорода. Однако с экономической точки зрения скорость получения водорода все еще остается неудовлетворительной.
Описание изобретения
Таким образом, целью настоящего изобретения является разрешение вышеупомянутых проблем, с которыми приходится сталкиваться в данной области техники, и создание нового фотокатализатора получения водорода с оптической активностью при излучении как в видимой, так и УФ-областях спектра.
Другой целью настоящего изобретения является создание фотокатализатора с высокой восстановительной активностью на солнечном свету, обеспечивающего высокий выход водорода и обладающего бесконечным сроком службы.
Еще одной целью настоящего изобретения является разработка способа приготовления фотокатализатора с высокой степенью фотокаталитической активности.
Наилучший вариант выполнения изобретения
Фотокатализатор по настоящему изобретению характеризуется следующей общей формулой VII:
m(a)/CdxZnyMzS VII
в которой m обозначает легирующий металлический элемент в качестве акцептора электронов, выбранный из группы, включающей Ni, Pt, Ru, или окисленное соединение этих металлов; а обозначает массовое процентное содержание m, находящееся в интервале 0,10-5,00; М обозначает по меньшей мере один каталитический элемент, выбранный из группы, включающей Мо, V, Al, Ti, Cs, Mn, Fe, Pd, Pt, P, Cu, Ag, Ir, So, Pb, Ga и Re; z обозначает соотношение M/(Cd+Zn+M) в атомных процентах, находящееся в интервале 0,05-20,00, а х и у обозначают Cd/(Cd+Zn+M) в атомных процентах и Zn/(Cd+Zn+M) в атомных процентах, находящиеся в интервале соответственно 10,00-89,95.
Приготовление фотокатализатора по настоящему изобретению характеризуется процессом легирования с осуществлением следующих стадий: растворение Cd-содержащего, Zn-содержащего и М-содержащего соединений в воде в таком количестве, при котором значение М в атомных процентах находится в интервале 0,05-20,00, a Cd/(Cd+Zn+M) в атомных процентах и Zn/(Cd+Zn+M) в атомных процентах находятся в интервале соответственно 10,00-89,95; добавление в этот раствор при перемешивании в качестве реагента H2S или Na2S для осаждения CdZnMS; промывка осадка водой и вакуумная сушка осадка в азотной атмосфере; легирование этого осадка жидким m-содержащим соединением в таком количестве, при котором массовое процентное содержание m находится в интервале 0,10-5,00.
Аналогично ранее известной технологии, до создания настоящего изобретения, водород получают по методу, в котором суспензию фотокатализатора в воде, в которую в качестве электронного донора добавлен Na2S и в качестве восстановителя добавлен NaH2PO2 или NaH2PO2, обрабатывают светом в видимой области спектра, отрегулированным с помощью оптического фильтра, солнечный светом или УФ-облучением.
Настоящее изобретение подробно описано ниже.
Выполняющий функции акцептора электронов легирующий металл m в фотокатализаторе по настоящему изобретению представляет собой элемент, выбранный из группы, включающей Ni, Pt, Ru, или их оксид, который в предпочтительном варианте используют в таком количестве, при котором содержание в массовых процентах находится в интервале 0,10-5,00. Если количество компонента m составляет, например, меньшее 0,10 мас.%, количество выделяющегося водорода уменьшается и уменьшается также стабильность фотокатализатора. С другой стороны, когда количество компонента m превышает 5,00 мас.%, количество выделяющегося водорода уменьшается, а затраты на его получение с экономической точки зрения оказываются неэффективными.
Значения M в фотокатализаторе по настоящему изобретению выбирают из группы, включающей Мо, V, Al, Ti, Cs, Mn, Fe, Pd, Pt, P, Cu, Ag, Ir, Sb, Pb, Ga и Re, a z обозначает M/(Cd+Zn+M) в атомных процентах, находящееся в интервале 0,05-20,00. Если значение В меньше нижнего предельного, фотокатализатор обычно утрачивает активность. С другой стороны, если значение В превышает верхнее предельное, уменьшается количество выделяющегося водорода.
Что касается молярных соотношений между Cd и S и между Zn и S, то в предпочтительном варианте молярное соотношение между Cd и S находится в интервале 1: 0,05-1,4 и между Zn и S - в интервале 1:0,05-1,4, более предпочтительно соответственно 1:0,3-1:0,7. В этом интервале молярных соотношений фотокатализатор по изобретению проявляет повышенную эффективность.
Если при приготовлении фотокатализатора в качестве легирующего элемента m используют платину (Pt), в предпочтительном для Pt варианте обработку УФ-облучением следует проводить в азотной атмосфере и легировать CdZnMS спеканием. В более предпочтительном варианте к осадку CdZnMS добавляют платинохлористоводородную кислоту (H2PtCl6) и обрабатывают УФ-облучением в азотной атмосфере для пропитки носителя таким количеством, при котором значение m(Pt) находится в интервале 0,10-5,00. Приготовленный таким образом осадок промывают водой до тех пор, пока рН промывной воды не достигнет 7, сушат под вакуумом при 105-130oС в течение 1,5-3 ч, подвергают окислительному спеканию при 300-400oС в течение 1,0-6,0 ч и затем восстановительному спеканию при 300-400oС в течение 1,0-6,0 ч.
В случае других легирующих элементов предпочтительный вариант приготовления фотокатализатора включает стадии добавления к полученному осадку CdZnMS m-содержащего соединения, отличного от платины, в таком количестве, при котором значение m достигает интервала 0,10-5,00; добавления при перемешивании 6 или 7 капель концентрированной соляной кислоты; обработки приготовленной суспензии ультразвуком в течение 1,0-5,0 мин; сушки под вакуумом при 110-130oС в течение 1,5-3,0 ч; окислительного спекания при 300-400oС в течение 1,0-6,0 ч и затем восстановительного спекания при 300-400oС в течение 1,0-6,0 ч с получением фотокатализатора.
При приготовлении фотокатализатора, легированного платиной, причина проведения сушки и спекания в окислительных/восстановительных условиях после достижения рН 7 заключается в том, чтобы сохранить в свободном состоянии акцептор электронов, Pt. Хорошо известно, что когда Pt в H2PtCl6 обрабатывают УФ-облучением, Pt активирует поверхность CdZnMS и создает связь с выделившейся S с образованием PtS, вследствие чего в процессе спекания при температуре 300-400oС в окислительных и восстановительных условиях образуется структура вюртцита. В случае спекания этого продукта при температуре 300-400oС в течение 1,0-6,0 ч Pt как акцептор электронов способна переходить в свободное состояние Pt(0). В более предпочтительном варианте его следует спекать при температуре 320-390oС. За пределами этого температурного интервала срок службы и оптическая активность фотокатализатора уменьшаются.
Примеры Cd-содержащих соединений включают CdCl2, CdBr2, CdI2, Cd(CH3CO2)2•xH2O, CdSO4•xH2O и Cd(NO3)2•4H2O, примеры Zn-содержащих соединений включают ZnCl2, ZnBr2, ZnI2, Zr(CH3CO2)2•xH2O, ZnSO4•xH2O и Zn(NO3)2•xH2O, а примеры М-содержащих соединений включают MoCl5, VCl3, VOSO4, VOCl3, Al(NO3)3, AlCl3, TiCl4, Сs2СО3, Ti[ОСН(СН3)2]4, K2Cr2O7,
Cr(СН3СO2)3, Cr(HCO2)3, Cr(NO3)3, H3PO2, МаН2РО2, SbCl3, MnCl3, MnF3, KMnO4, Pb(NO3)2, Pb(CH3CO2)4, RuCl3, FeCl3, IrCl3, Pd(NO3)2, Н2PtCl6,
Cu(NO3)2•3Н2O, AgNO3, Ga(NO3)3, SnCl2, ReCl3 и т.д.
И затем также примеры m-содержащих соединений включают H2PtCl6, RuCl3, NiSO4, Ni(NO3)2, Ni(CH3CO2)2, NiCl2, NiBr2, NiI2 и т.д.
В заявке KR 96-44214, поданной до создания настоящего изобретения, после первичного спекания предусмотрено травление кислотой, а по настоящему изобретению необходима только стадия сушки осадка под вакуумом в азотной атмосфере, благодаря чему по предлагаемому способу приготовления стадии первичного спекания и травления кислотой необязательны.
Однако в соответствии с настоящим изобретением водород получают растворением 0,15-1,00 моль Na2S в качестве донора электронов и 0,15-1,00 моль SO3 2- вместо Н2РО2 - в качестве восстановителя в первично и/или вторично дистиллированной воде или в предварительно обработанной воде и добавлением в нее фотокатализатора по настоящему изобретению. Далее приготовленную таким образом суспензию обрабатывают облучением в видимой области спектра, регулируемым оптическим фильтром, или УФ-облучением с перемешиванием при температуре 5-85oС и под давлением 0,1-5 ат с достижением высокой эффективности при получении водорода.
Более того, важной задачей является поддержание концентрации донора электронов и восстановителя в упомянутых пределах. Когда она ниже нижнего предела, количество выделяющегося водорода уменьшается; когда она избыточна, дополнительное увеличение количества выделяющегося водорода может быть не достигнуто. Оптимальным реакционным условием является температура 10-60oС под давлением от вакуума до 2 ат.
Если в реакционную среду повторно добавлять донор электронов и восстановитель, срок службы фотокатализатора по настоящему изобретению оказывается полубесконечным.
Ниже приведены примеры приготовления в соответствии с изобретением.
ПРИМЕР ПОЛУЧЕНИЯ I
В 250 мл воды, CdSO4•H2O и ZnSO4•7H2O, МоCl5 в качестве промотора и H2S в качестве реагента с достижением такого же состава, как указанный в таблице, подмешивают до тех пор, пока не показывается осадок. Образовавшуюся смесь, в которой осадок представляет собой CdZnMoS, перемешивают. Осадок промывают водой до тех пор, пока рН промывной воды не достигает 7. Промытый таким образом осадок сушат под вакуумом в азотной атмосфере при температуре 130oС в течение 2 ч, получая в виде порошка CdZnMoS.
Ni(NO3)2•6Н2О в этот порошок добавляют таким образом, чтобы добиться содержания Ni в осадке 1 мас.%. Далее с перемешиванием осторожно добавляют 6-7 капель концентрированной соляной кислоты с последующими обработкой полученного продукта ультразвуком в течение 3 мин, сушкой при температуре 130oС в течение 2 ч и наконец окислительным спеканием при температуре 380oС в течение 4 ч и затем восстановительным спеканием при температуре 380oС в течение 4 ч с получением в качестве готового фотокатализатора Ni(1 мac. %)/Cd49,70Zn49,70Mo0,6S.
ПРИМЕР ПОЛУЧЕНИЯ II
Эксперимент примера получения I повторяют, добавляя MoCl5 с тем, чтобы ввести в осадок 1,0 ат.% Мо, с получением таким образом в итоге фотокатализатора Ni(1 мac.%)/Cd49,50Mo1,0S.
ПРИМЕРЫ ПОЛУЧЕНИЯ III-VII
Эксперимент примера получения I повторяют, добавляя MoCl5 с тем, чтобы ввести в осадок 2,0 ат.% Мо, с получением таким образом в итоге фотокатализатора Ni(1 мac.%)/Cd49,00Zn49,00Mo2,0S.
ПРИМЕР ПОЛУЧЕНИЯ VIII
Эксперимент примера получения I повторяют, добавляя MoCl5 с тем, чтобы ввести в осадок 3,0 ат.% Мо, с получением таким образом в итоге фотокатализатора Ni(1 мac.%)/Cd48,50Zn48,50Mo3,0S.
ПРИМЕР ПОЛУЧЕНИЯ IX
К порошку Cd49,70Zn49,70Mo2,0S, полученному в соответствии с примером получения III, добавляют H2PtCl6 в таком количестве, чтобы содержание Pt в этом порошке составляло 1,0 мас.%. Готовый порошок обрабатывают УФ-облучением (ртутная лампа высокого давления мощностью 450 Вт при расстоянии от образца 4 см) в азотной атмосфере в течение 0,5 ч, облученный таким образом осадок промывают промывной водой до тех пор, пока рН промывной воды не достигает 7, промытый осадок сушат при температуре 130oС в течение 2 ч с последующими окислительным спеканием на воздухе при температуре 380oС в течение 4 ч и восстановительным спеканием при температуре 380oС в течение 4 ч, получая в качестве готового фотокатализатора Pt(1 мac. %)/Cd49,00Zn49,00Mo2,0S.
ПРИМЕР ПОЛУЧЕНИЯ Х
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 используют VCl3 и окислительное спекание проводят при температуре 380oС в течение 4 ч, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70V0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XI
Эксперимент примера получения I повторяют, за исключением того, что VCl3 добавляют таким образом, чтобы ввести в осадок 1,0 ат.% V и окислительное спекание проводят при температуре 380oС в течение 4 ч, получая таким образом в итоге фотокатализатор Ni(1 мас.%)/Cd49,50Zn49,50V1,0S.
ПРИМЕР ПОЛУЧЕНИЯ XII
Эксперимент примера получения I повторяют, за исключением того, что VCl3 добавляют таким образом, чтобы ввести в осадок 2,0 ат.% V, с получением в итоге фотокатализатора Ni(1 маc.%)/Cd49,00Zn49,00V2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XIII
Эксперимент примера получения I повторяют, за исключением того, что VCl3 добавляют таким образом, чтобы ввести в осадок 2,0 ат.% V, и окислительное спекание проводят при температуре 380oС в течение 2 ч с получением в итоге фотокатализатора Ni(1 мас.%)/Сd49,00Zn49,00V2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XIV
Эксперимент примера получения I повторяют, за исключением того, что VCl3 добавляют таким образом, чтобы ввести в осадок 2,0 ат.% V, и окислительное спекание проводят при температуре 380oС в течение 4 ч с получением в итоге фотокатализатора Ni(1 мас.%)/Сd49,00Zn49,00V2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XV
Эксперимент примера получения I повторяют, за исключением того, что VCl3 добавляют таким образом, чтобы ввести в осадок 2,0 ат.% V, и окислительное спекание проводят при температуре 380oС в течение 6 ч с получением в итоге фотокатализатора Ni(1 мac.%)/Cd49,00Zn49,00V2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XVI
Эксперимент примера получения XI повторяют, за исключением того, что VCl3 добавляют с тем, чтобы ввести в осадок 3,0 ат.% V, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd48,50Zn48,50V3,0S.
ПРИМЕР ПОЛУЧЕНИЯ XVII
Эксперимент примера получения XI повторяют, за исключением того, что VCl3 добавляют с тем, чтобы ввести в осадок 5,0 ат.% V, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd47,50Zn47,50V5,0S.
ПРИМЕР ПОЛУЧЕНИЯ XVIII
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 используют Со(NO3)2 и в итоге таким образом получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Co0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XIX
Эксперимент примера получения XVIII повторяют, за исключением того, что Со(NO3)2 добавляют с тем, чтобы ввести в осадок 2,0 ат.% Со, получая таким образом в итоге фотокатализатор Ni(1 Мac.%)/Cd49,00Z49,00Co2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XX
Эксперимент примера получения XIX повторяют, за исключением того, что Со(NO3)2 добавляют с тем, чтобы ввести в осадок 5,0 ат.% Со, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd47,50Zn47,50Co5,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXI
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 используют Al(NO3)3 и в итоге таким образом получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Al0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXII
Эксперимент примера получения XIX повторяют, за исключением того, что Al(NO3)3 добавляют с тем, чтобы ввести в осадок 2,0 ат.% Al, получая таким образом в итоге фотокатализатор Ni(l мac.%)/Cd49,00Zn49,00Al2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXIII
Эксперимент примера получения XIX повторяют, за исключением того, что Al(NO3)3 добавляют с тем, чтобы ввести в осадок 5,0 ат.% Al, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd47,50Zn47,50Al5,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXIV
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 используют Cs2CO3 и в итоге таким образом получают фотокатализатор Ni(1 мас.%)Сd49,70Zn49,70Cs0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXV
Эксперимент примера получения XXIV повторяют, за исключением того, что Cs2CO3 добавляют с тем, чтобы ввести в осадок 2,0 ат.% Cs, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd49,00Zn49,00Cs2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXVI
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 используют Ti[OCH(CH3)2] 4 и в итоге таким образом получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Ti0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXVII
Эксперимент примера получения XXVI повторяют, за исключением того, что Тi[ОСН(СН3)2] 4 добавляют с тем, чтобы ввести в осадок 2,0 ат.% Ti, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd49,00Zn49,00Ti2,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXVIII
Эксперимент примера получения XXVI повторяют, за исключением того, что Ti[OCH(CH3)2] 4 добавляют с тем, чтобы ввести в осадок 5,0 ат.% Ti, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd47,50Zn47,50Ti5,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXIX
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют MnF3 и в итоге таким образом получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Mn0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXX
Эксперимент примера получения XXIX повторяют, за исключением того, что MnF3 в качестве промотора добавляют с тем, чтобы ввести в осадок 0,2 ат.% Mn, получая таким образом в итоге фотокатализатор Ni(1 мac. %)/Cd49,90Zn49,90Mn0,2S.
ПРИМЕР ПОЛУЧЕНИЯ XXXI
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют H3PO2 и в итоге таким образом получают фотокатализатор Ni(1 мac.%)/Cd47,00Zn47,00P6,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXXII
Эксперимент примера получения III повторяют, за исключением того, что вместо NiCl2•6H2O используют RuCl3•3H2O с тем, чтобы ввести в осадок 1,0 мас.% Ru, получая таким образом в итоге фотокатализатор Ru (1 мac. %)/Cd47,00Zn47,00P6,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXXIII
Эксперимент примера получения XXXI повторяют, за исключением того, что в качестве промотора используют Н3РО2 с тем, чтобы ввести в осадок 10,0 мас.% Р, получая таким образом в итоге фотокатализатор Ni(1 мас. %)/Cd45,00Zn45,00P10,0S.
ПРИМЕР ПОЛУЧЕНИЯ XXXIV
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют FeCl3 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Fe0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXXV
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют Pd(NO3)2 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Pd0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXXVI
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют H2PtCl6 и в итоге получают фотокатализатор Ni(1 мас.%)/Сd49,70Zn49,70Pt0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXXVII
Эксперимент примера получения I повторяют, за исключением того, что вместо МоСl5 в качестве промотора используют Cu(NO3)2•3H2O и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Cu0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXXVIII
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют AgNO3 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Ag0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XXXIX
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют IrCl3 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Ir0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XL
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют Pb(NO3)2 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Pb0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XLI
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют SnCl2 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70zn49,70Sn0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XLII
Эксперимент примера получения I повторяют, за исключением того, что вместо ModCl5 в качестве промотора используют Ga(NO3)3 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Ga0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XLIII
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют ReCl3 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Re0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XLIV
Эксперимент примера получения I повторяют, за исключением того, что вместо MoCl5 в качестве промотора используют SbCl3 и в итоге получают фотокатализатор Ni(1 мac.%)/Cd49,70Zn49,70Sb0,6S.
ПРИМЕР ПОЛУЧЕНИЯ XLV
Эксперимент примера получения I повторяют, за исключением того, что K2Cr2O7 в качестве промотора добавляют с тем, чтобы ввести в осадок 0,2 ат.% Cr, получая таким образом в итоге фотокатализатор Ni(1 мac. %)/Cd49,90Zn49,90Cr0,2S.
ПРИМЕР ПОЛУЧЕНИЯ XLVI
Эксперимент примера получения XLV повторяют, за исключением того, что добавляют Cd и Zn с тем, чтобы ввести в осадок соответственно 39,90 ат.% Cd и 59,90 ат. % Zn, получая таким образом в итоге фотокатализатор Ni(1 мac. %)/Cd39,90Zn59,90Cr0,2S.
ПРИМЕР ПОЛУЧЕНИЯ XLVII
Эксперимент примера получения XLV повторяют, за исключением того, что добавляют Cd и Zn с тем, чтобы ввести в осадок соответственно 59,90 ат.% Cd и 39,90 ат. % Zn, получая таким образом в итоге фотокатализатор Ni(1 мac. %)/Cd59,90Zn39,90Cr0,2S.
ПРИМЕР ПОЛУЧЕНИЯ XLVIII
Эксперимент примера получения XLV повторяют, за исключением того, что K2Cr2О7 в качестве промотора добавляют с тем, чтобы ввести в осадок 0,5 ат.% Cr, получая таким образом в итоге фотокатализатор Ni(1 мac. %)/Cd49,75Zn49,75Cr0,5S.
ПРИМЕР ПОЛУЧЕНИЯ XLIX
Эксперимент примера получения XLV повторяют, за исключением того, что K2Cr2O7 в качестве промотора добавляют с тем, чтобы ввести в осадок 1,0 ат.% Cr, получая таким образом в итоге фотокатализатор Ni(1 мас. %)/Cd49,50Zn49,50Cr1,0S.
ПРИМЕР ПОЛУЧЕНИЯ L
Эксперимент примера получения XLV повторяют, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd49,90Zn49,90Cr0,2S.
ПРИМЕР ПОЛУЧЕНИЯ LI
Эксперимент примера получения III повторяют, получая таким образом в итоге фотокатализатор Ni(1 мac.%)/Cd49,00Zn49,00Mo2,0S.
СРАВНИТЕЛЬНЫЙ ПРИМЕР ПОЛУЧЕНИЯ I
Эксперимент примера получения XL повторяют с тем, чтобы ввести 0,05 мас. % Ni, получая в итоге фотокатализатор Ni(0,05 мac.%)/Cd49,70Zn49,70Pb0,6S.
СРАВНИТЕЛЬНЫЙ ПРИМЕР ПОЛУЧЕНИЯ II
Эксперимент примера получения XL повторяют с тем, чтобы ввести 7,0 мас.% Ni, получая в итоге фотокатализатор Ni(7,0 мac.%)/Cd49,70Zn49,70Pb0,6S.
СРАВНИТЕЛЬНЫЙ ПРИМЕР ПОЛУЧЕНИЯ III
Эксперимент примера получения XLV повторяют с тем, чтобы ввести 91,80 ат.% Cd и 8,00 ат.% Zn, получая в итоге фотокатализатор Ni(1 мac. %)/Cd91,80Zn8,00Cr0,2S.
СРАВНИТЕЛЬНЫЙ ПРИМЕР ПОЛУЧЕНИЯ IV
Эксперимент примера получения XLV повторяют с тем, чтобы ввести 8,00 ат. % Cd и 91,80 ат.% Zn, получая в итоге фотокатализатор Ni(1 мас. %)/Cd8,00Zn91,80Cr0,2S.
СРАВНИТЕЛЬНЫЙ ПРИМЕР ПОЛУЧЕНИЯ V
Эксперимент примера получения XLVIII повторяют, за исключением того, что после окислительного спекания восстановительное спекание проводят в течение 30 мин при температуре 380oС с получением таким образом в итоге фотокатализатора Ni(1 мac.%)/Cd49,75Zn49,75Cr0,5S.
ПРИМЕРЫ I-XLIX И СРАВНИТЕЛЬНЫЕ ПРИМЕРЫ I-V
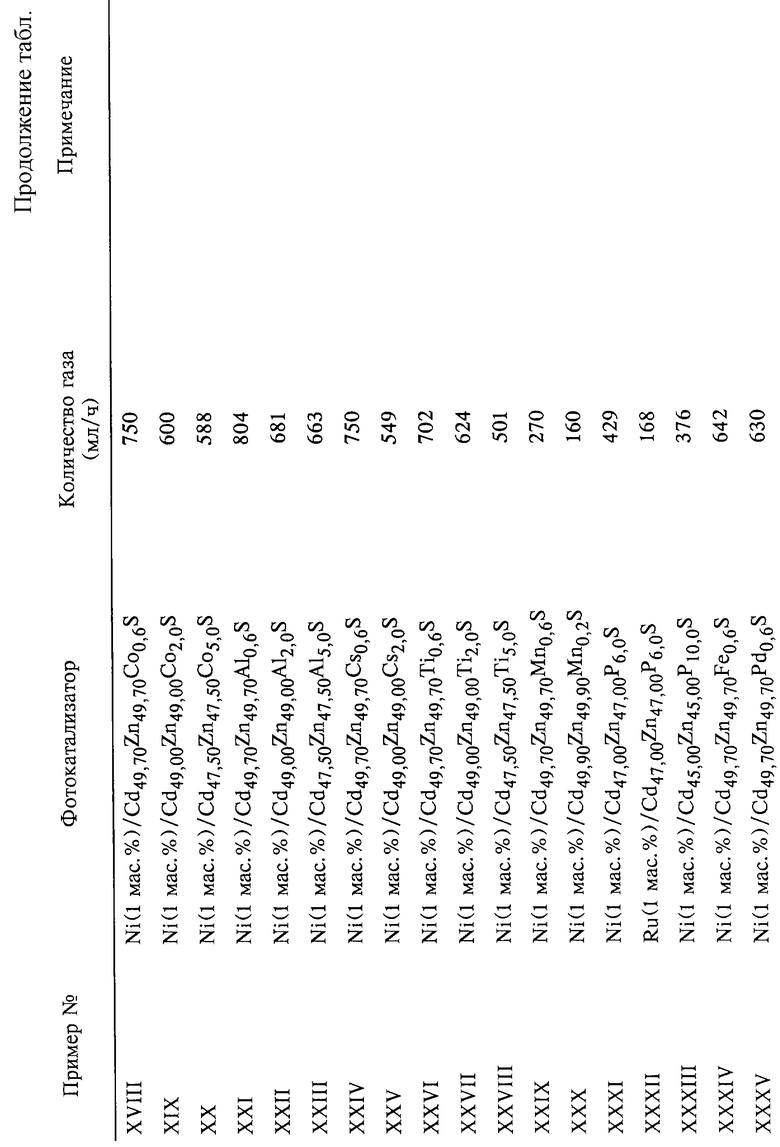
0,5 г фотокатализатора, приготовленного в соответствии с каждым из примеров получения I-XXIII и сравнительными примерами получения I-V, независимо суспендируют в 500 мл воды, которая включает 0,36 М Na2S и 0,36 М Na2SO3, и приготовленную суспензию перемешивают при скорости вращения мешалки 300 об/мин в фотохимическом реакторе замкнутой газоциркуляционной системы. Готовую суспензию облучают в видимой области спектра (Хе лампа мощностью 500 Вт с оптическим фильтром, который пропускает свет с длиной волны более 400 нм, при расстоянии от образца до источника света 4 см) при комнатной температуре и под давлением 1 ат. Количества выделяющегося водорода, который таким образом получают, определенные газовой хроматографией и с помощью бюретки, указаны в таблице.
ПРИМЕР L
Эксперимент примера I повторяют, за исключением того, что вместо Хе лампы мощностью 500 Вт применяют ртутную лампу высокого давления мощностью 450 Вт и таким образом получают результат, отраженный в таблице.
ПРИМЕР LI
Срок службы фотокатализатора, приготовленного в соответствии с примером получения III, определяли следующим образом. 0,5 г фотокатализатора, приготовленного в соответствии с примером получения III, суспендируют в 500 мл воды, которая включает 0,36 моль/л Na2S и 0,36 моль/л Na2SO3, и после этого по прошествии каждого последующего 10-часового периода при общей продолжительности 100 ч в приготовленный по вышеизложенному раствор дополнительно добавляют 0,36 моль/л Na2S и 0,36 моль/л Na2SO3 и измеряют количество полученного водорода. В результате среднее количество газообразного водорода, полученного в ходе проведения описанного эксперимента, составляет 980 мл/ч, что аналогично результату (972 мл/ч), полученному в примере XVII. Таким образом, результат, полученный в ходе проведения этого эксперимента, доказывает, что фотокатализатор обладает полубесконечным сроком службы.
Возможность промышленного применения
Из этих данных очевидно, что CdZnMS фотокатализатор в соответствии с настоящим изобретением включает как фотокаталитическую CdS группу, проявляющую свойства высокой каталитической активности при облучении в видимой области спектра, так и фотокаталитическую ZnS группу, относительное преимущество которой состоит в высокой активности при обработке УФ-облучением, благодаря чему такой фотокатализатор можно применять в сочетании с источниками излучения более широкого диапазона, чем ранее известные фотокатализаторы.
Кроме того, выполнение настоящего изобретения путем внедрения следующих технических приемов, таких как добавление других новых легирующих металлов и различных промоторов, разработка новых способов введения и определение оптимальной продолжительности спекания, позволяет устранить затруднения, связанные с ранее существовавшими ограничениями активности фотокатализаторов в отношении вводимых в реакцию восстановителей.
Более того, благодаря оптимальным составу Cd/Zn и реакционным условиям эти фотокатализаторы обладают также превосходными прогнозируемой долговечностью, равно как и производительностью по водороду.
Сущность изобретения и его преимущества легко понять из вышеприведенного описания. Очевидно, что в предлагаемые способы и композиции можно вносить самые разнообразные изменения, не выходя при этом из сущности и объема изобретения или без ущерба для его материальных преимуществ. Эти способы и композиции в настоящем описании представлены просто с целью иллюстрации предпочтительных вариантов выполнения изобретения.



Изобретение относится к фотокатализатору для получения водорода, к способу его приготовления и к способу получения водорода с его использованием. В заявке описаны фотокатализатор CdZnMS получения водорода из воды, способ его приготовления и способ получения водорода с использованием этого фотокатализатора. Фотокатализатор характеризуется следующей общей формулой: m(a)/ CdxZnyMzS, в которой m обозначает по меньшей мере один легирующий металлический элемент в качестве акцептора электронов, выбранный из группы, включающей Ni, Pt, Ru, или окисленное соединение этих металлов; а обозначает массовое процентное содержание m, находящееся в интервале 0,10-5,00; М обозначает каталитический элемент, выбранный из группы, включающей Мо, V, Al, Cs, Ti, Mn, Fe, Pd, Pt, P, Cu, Ag, Ir, Sb, Pb, Ga и Re; z обозначает М/(Cd+Zn+M) в атомных процентах, находящееся в интервале 0,05-20,00, а х и у обозначают соответственно Cd/(Cd+Zn+M) в атомных процентах и Zn(Cd+Zn+M) в атомных процентах, находящиеся в интервале 10,00-89,95. Фотокатализаторы в соответствии с настоящим изобретением обладают преимуществами, проявляя высокую степень фотокаталитической активности соответственно фотокатализаторов CdS при обработке излучением в видимой области спектра и фотокатализаторов ZnS при обработке УФ-излучением. Таким образом, выполнение настоящего изобретения позволяет применять источники излучения широкого диапазона. Кроме того, установлено, что применение фотокатализаторов по настоящему изобретению дает возможность преодолеть ограничение восстановителями активности во время фотохимической реакции и эти катализаторы обладают намного более длительным сроком службы и увеличенной производительностью по водороду. 3 с. и 7 з.п. ф-лы, 1 табл.
m(a)/CdxZnyMzS,
в которой m обозначает легирующий металлический элемент в качестве акцептора электронов, выбранный из группы, включающей Ni, Pt, Ru, или оксиды какого-либо из этих металлов;
а обозначает массовое процентное содержание m, находящееся в интервале 0,10-5,00;
М обозначает каталитический элемент, выбранный из группы, включающей Мо, V, Al, Cs, Ti, Mn, Fe, Pd, Pt, P, Cu, Ag, Ir, Sb, Pb, Ga и Re;
х обозначает соотношение Cd/(Cd+Zn+M) в атомных процентах, находящееся в интервале 10,00-89,95;
у обозначает соотношение Zn/(Cd+Zn+M) в атомных процентах, находящихся в интервале 10,00-89,95;
z обозначает М/(Cd+Zn+M) в атомных процентах, находящееся в интервале 0,05-20,00 соответственно.
SbCl3, MnCl3, MnF3, KMnO4, Pb(NO3)2, Pb(CH3CO2)4, RuCl3, FeCl3, IrCl3,
Pb(NO3)2, H2PtCl6, Cu(NO3)2•3H2O, AgNO3, Ga(NO3)3, SnCl2 и ReCl3. 5. Способ приготовления фотокатализатора CdZnMS по п.2, в котором m - содержащим соединением является представитель, выбранный из группы, включающей H2PtCl6, RuCl3, NiSO4, Ni(NO3)2, Ni(CН3CO2)2, NiCl2, NiBr2 и Nil2.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| ЭЛЕКТРОНОАКЦЕПТОРНЫЕ КОМПОЗИЦИИ | 1994 |
|
RU2139881C1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| US 4745094 А, 17.05.1988 | |||
| ПЕНОМАТЕРИАЛ НА ОСНОВЕ СОПОЛИМЕРА СТИРОЛА-АКРИЛОНИТРИЛА С ПОЛОЖИТЕЛЬНОЙ АСИММЕТРИЕЙ РАСПРЕДЕЛЕНИЯ | 2009 |
|
RU2493181C2 |
Авторы
Даты
2003-02-27—Публикация
2001-02-21—Подача