Изобретение относится к медицинской промышленности и может быть использовано в производстве пробиотиков.
Известно, что пробиотики, содержащие живые лактобактерии, широко используют для нормализации кишечной и вагинальной микрофлоры человека. В состав нормальной микрофлоры здорового человека входят различные виды лактобактерий, образующие всевозможные сочетания. Многогранно их физиологическое значение, они играют немаловажную роль в защитной функции организма [1]. Несмотря на многочисленные известные варианты лактосодержащих препаратов, отечественная медицинская практика базируется на применении лактобактерина и его аналогов: ацилакта и аципола [2, 3].
При изготовлении указанных препаратов, имеющих аналогичную сферу применения, используют один штамм или ассоциацию штаммов одного вида бактерий, терапевтическая доза которых составляет 107-109 колониеобразующих единиц (КОЕ). Лактобактерин представляет собой монопрепарат, содержащий один штамм лактобактерий вида Lactobacillus plantarum или Lactobacillus fermentum, а ацилакт и аципол - ассоциацию штаммов вида Lactobacillus acidophilus. Способ получения лактобактерина и его аналогов включает культивирование бактерий производственного штамма (штаммов) в жидкой питательной среде с внесением углеводной добавки, в качестве которой применяют растворы глюкозы или лактозы. Полученную бактериальную взвесь смешивают с защитной средой и подвергают лиофилизации. В качестве комплексной защитной среды используют обезжиренное молоко (20-30% от объема бактериальной взвеси) и сахарозо-желатозную среду (10-20% от объема бактериальной взвеси) [4].
К недостаткам способа получения лактобактерина и его аналогов следует отнести использование одного вида лактобактерий, что ограничивает биологический потенциал препарата. К тому же в ациполе и ацилакте неизвестно количественное соотношение составляющих бактериальной композиции, так как данный вид контроля, основанный на выявлении межштаммовых отличий, достаточно сложен и не используется при их изготовлении. Недостатком способа получения лактобактерина и аналогов следует считать использование различных углеводосодержащих растворов, используемых в процессе культивирования и в составе защитной среды для лиофилизации. Недостаток указанного способа заключается также в значительном разведении бактериальной взвеси защитной средой (до 50% от объема бактериальной взвеси), что снижает количество КОЕ в единице объема.
С целью устранения указанных недостатков предлагается способ получения лактобактерина, сущность которого заключается в следующем. Использование сахарозо-желатозной среды в качестве углеводной добавки в процессе культивирования лактобактерий позволяет исключить другие углеводы и унифицировать рабочие растворы, применяемые при накоплении биомассы лактобактерий и в составе защитных сред. Для повышения биологического потенциала препарата получаемую бактериальную взвесь лактобактерий вида Lactobacillus plantarum или Lactobacillus fermentum, как основы лактобактерина, смешивают с культурой одного из штаммов вида Lactobacillus acidophilus, применяемых для изготовления ацилакта или аципола. В получаемой бактериальной композиции возможен раздельный учет КОЕ каждого штамма с помощью простых и общедоступных способов благодаря выраженным межвидовым различиям. Для предотвращения разведения бактериальной взвеси обезжиренное молоко, как компонент защитной среды, предварительно используют в качестве питательного субстрата для накопления биомассы лактобактерий. Это позволяет уменьшить расход бактериальной суспензии для получения 1 дозы сухого препарата.
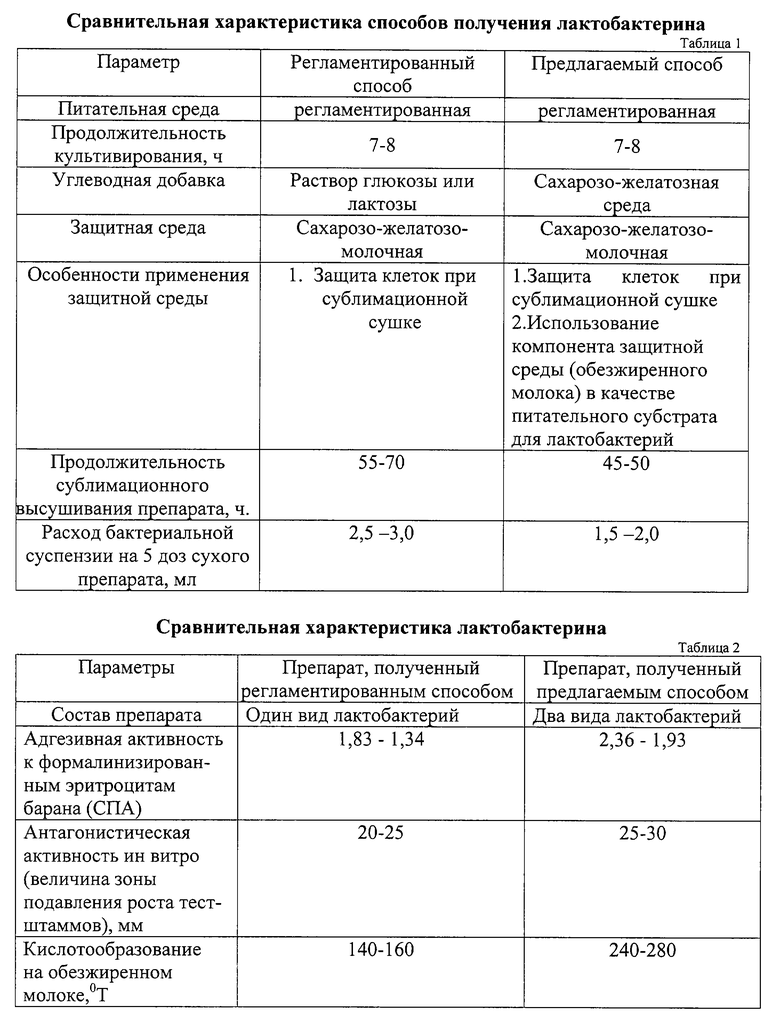
Достигаемый технический результат заключается в оптимизации способа получения препарата и повышении его биологической активности (табл. 1, 2).
При осуществлении способа используют сахарозо-желатозную среду обычного состава, содержащую 40-50% сахарозы по ГОСТ 5833-75 (или сахар рафинированный, ГОСТ 22-94, быстрорастворимый) и 8-10% желатина по ГОСТ 11293-89. Желатин, входящий в состав сахарозо-желатозной среды, при использовании указанной углеводной добавки в процессе культивирования исключает внесение уплотняющего компонента на этапе приготовления питательной среды. Количество вносимой сахарозы аналогично расходу глюкозы или лактозы в процессе культивирования.
Смешивание бактериальных взвесей производят в соотношении, обеспечивающем содержание жизнеспособных бактерий каждого штамма в количестве не менее 107 КОЕ/мл в получаемом сухом препарате и зависящем от величины КОЕ/мл в каждой взвеси. Количество КОЕ в 1 мл взвеси лактобактерий видов Lactobacillus plantarum или Lactobacillus fermentum определяют с помощью стандартного метода высева на плотную среду МРС-4 и подсчета выросших колоний после инкубирования в аэробных условиях [5]. Количество бактерий вида Lactobacillus acidophilus определяют с помощью стандартного метода посева на молоко [6]. Указанные методики позволяют проводить раздельный учет бактериальных компонентов в смешанной взвеси и сухом препарате.
При использовании обезжиренного молока в качестве субстрата для накопления биомассы производственного штамма продолжительность культивирования составляет 2-6 ч при коррекции рН (6,0±4). Указанная продолжительность культивирования обеспечивает накопление биомассы до 107-108 КОЕ/мл и не приводит к образованию сгустка, сохраняя обычную консистенцию молока. Молоко, обогащенное лактобактериями в данной концентрации, при использовании в дальнейшем в качестве компонента защитной среды позволяет получить сухой препарат с обычными физическими свойствами и повышенным содержанием КОЕ в 1 дозе.
Пример 1. Бактериальную взвесь штамма Lactobacillus plantarum 8P-A3 получают путем культивирования в реакторе при 37oС с применением казеиново-дрожжевой среды. Доза посевного материала составляет (10,0±2,5)% от объема питательной среды. В процессе выращивания добавляют сахарозо-желатозную среду и поддерживают рН в пределах 5,5-6,0 с помощью 10%-ного раствора аммиака. Культивирование ведут в течение (7±1)ч до достижения культурой стационарной фазы роста. Содержание жизнеспособных клеток в бактериальной взвеси составляет 109 КОЕ/мл. Бактериальную взвесь штамма Lactobacillus acidophilus К3Ш24 получают аналогичным образом. Содержание жизнеспособных клеток в бактериальной взвеси составляет 108 КОЕ/мл.
Полученные бактериальные взвеси штаммов Lactobacillus plantarum 8P-A3 и Lactobacillus acidophilus К3Ш24 смешивают в соотношении 1:1, добавляют защитную сахарозо-желатозную среду в количестве 15% и обезжиренное молоко в количестве 15% от объема смешанной бактериальной взвеси. Полученную суспензию разливают во флаконы и лиофильно высушивают. В сухом препарате содержание лактобактерий штамма Lactobacillus plantarum 8P-A3 составляет не менее 108KОЕ/доза, a Lactobacillus acidophilus К3Ш24 - не менее 107 КОЕ/доза.
Пример 2. Бактериальную взвесь штамма Lactobacillus fermentum 90 Т-С4, содержащую 108 КОЕ/мл, получают, как описано в примере 1. Бактериальную взвесь штамма Lactobacillus acidophilus NK1 получают путем культивирования бактерий на обезжиренном молоке. Доза посевного материала составляет 5-10% от объема обезжиренного молока. Продолжительность инкубации при 37oС составляет 2-4 ч. Содержание жизнеспособных клеток в обезжиренном молоке составляет 107 КОЕ/мл.
Полученные бактериальные взвеси штаммов Lactobacillus fermentum 90 Т-С4 и Lactobacillus acidophilus NK1 смешивают в соотношении 1:1,5, добавляют защитную сахарозо-желатозную среду в количестве 10% от объема бактериальной взвеси. Полученную суспензию разливают во флаконы и лиофильно высушивают. В сухом препарате содержание лактобактерий каждого штамма составляет не менее 107 КОЕ/доза.
Пример 3. Бактериальные взвеси штамма Lactobacillus plantarum 8P-A3 и Lactobacillus acidophilus 100АШ получают, как описано в примере 1. Бактериальную взвесь штамма Lactobacillus acidophilus 100АШ получают так же, как взвесь штамма Lactobacillus plantarum 8P-A3.
Дополнительно получают бактериальную взвесь штамма Lactobacillus plantarum 8P-A3 путем культивирования бактерий на обезжиренном молоке. Доза посевного материала составляет 5-10% от объема обезжиренного молока. Продолжительность инкубации при 37oС составляет 4-6 ч. Содержание жизнеспособных клеток в обезжиренном молоке составляет 108 КОЕ/мл.
Полученные бактериальные взвеси штаммов Lactobacillus plantarum 8P-A3, Lactobacillus acidophilus 100 АШ и Lactobacillus plantarum 8P-A3 на молоке смешивают в соотношении 1:4:3, добавляют защитную сахарозо-желатозную среду в количестве 10% от объема бактериальной взвеси. Полученную суспензию разливают во флаконы и лиофильно высушивают. В сухом препарате содержание лактобактерий каждого штамма составляет не менее 108 КОЕ/доза.
Предложенный способ получения пробиотика обладает выраженными технологическими и экономическими преимуществами и позволяет получать препарат более высокого качества.
Список литературы
1. A.A. Ленцнер "Лактобациллы микрофлоры человека". Автореферат на соискание ученой степени доктора медицинских наук. 1973 г.
2. "Справочник практического врача. Бактерийные, сывороточные и вирусные лечебно-профилактические препараты...". Под редакцией Н.А.Озерецковского, Г. И. Останина. Санкт-Петербург 1998 г., с. 141-147.
3. В.М.Коршунов, Б.А. Ефимов, А.Р. Пикина "Характеристика биологических препаратов и пищевых добавок для функционального питания и коррекции микрофлоры кишечника". Журн. Микробиол., 2000, 3, С.86-91.
4. Регламент производства Лактобактерина сухого 705-97.
5. ФС 42-3256-96 "Лактобактерин сухой".
6. ФС 42-3946-00 "Ацилакт сухой".
| название | год | авторы | номер документа |
|---|---|---|---|
| МАЗЬ "ЭМУЛАКТ" ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ИНФЕКЦИОННО-ВОСПАЛИТЕЛЬНЫХ ГИНЕКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И ДИСБАКТЕРИОЗОВ | 1999 |
|
RU2183963C2 |
| ЖИДКИЙ СОСТАВ, СОДЕРЖАЩИЙ ЛАКТОБАКТЕРИИ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2023 |
|
RU2824201C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ОСНОВЫ ДЛЯ ЛЕКАРСТВЕННЫХ И КОСМЕТИЧЕСКИХ СРЕДСТВ | 2000 |
|
RU2187994C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКОГО СТИМУЛЯТОРА | 2001 |
|
RU2224018C2 |
| СПОСОБ ПОЛУЧЕНИЯ И КОНТРОЛЯ ПРОБИОТИЧЕСКИХ ПРЕПАРАТОВ | 2006 |
|
RU2332454C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУХОЙ ЛИОФИЛИЗИРОВАННОЙ БИОМАССЫ ЛАКТО- И БИФИДОБАКТЕРИЙ | 2004 |
|
RU2272837C2 |
| ШТАММ Lactobacillus fermentum Z, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРОИЗВОДСТВА ПРОБИОТИЧЕСКИХ МОЛОЧНОКИСЛЫХ ПРОДУКТОВ | 2008 |
|
RU2412239C2 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ УРОГЕНИТАЛЬНЫХ ИНФЕКЦИЙ | 1999 |
|
RU2185842C2 |
| КОНСОРЦИУМ ШТАММОВ ЛАКТОБАКТЕРИЙ И СПОСОБ ПОЛУЧЕНИЯ НА ЕГО ОСНОВЕ БИОЛОГИЧЕСКИ АКТИВНОЙ ДОБАВКИ ИЛИ ЗАКВАСКИ ДЛЯ ПРОИЗВОДСТВА КИСЛОМОЛОЧНЫХ ПРОДУКТОВ | 2008 |
|
RU2376366C2 |
| ШТАММ LACTOBACILLUS BREVIS BA-13, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ПРОБИОТИЧЕСКИХ ПРЕПАРАТОВ И ПРОДУКТОВ ПИТАНИЯ | 2001 |
|
RU2190015C1 |
Изобретение относится к области медицинской промышленности и может быть использовано для производства пробиотиков. Сущностью способа является комплексное применение защитной сахарозо-желатозо-молочной среды не только в процессе лиофилизации, но и при накоплении бактериальной биомассы. Способ включает использование сахарозо-желатозной среды в качестве углеводной добавки при культивировании производственных штаммов, а также предварительное применение обезжиренного молока в качестве субстрата для выращивания лактобактерий с последующим внесением его как компонента защитной среды в состав бактериальной суспензии перед высушиванием. Для повышения биологической активности препарата предлагается дополнительно вводить лактобактерии вида Lactobacillus acidophilus. Техническим результатом является оптимизация способа получения препарата и повышение его биологической активности. 1 з.п.ф-лы, 2 табл.
| СПОСОБ ПРИГОТОВЛЕНИЯ ПРОБИОТИКА НА ОСНОВЕ ЖИВЫХ БИФИДОБАКТЕРИЙ И ЛАКТОБАКТЕРИЙ | 1995 |
|
RU2060673C1 |
| RU 2053781 C1, 10.02.1996 | |||
| КОНЬКОВА Н.К | |||
| и др | |||
| Сравнительная характеристика аминокислотного состава питательных сред и основ, используемых в производстве лактобактерина | |||
| Биотехнология и генетика | |||
| Межвуз | |||
| сб | |||
| - Н | |||
| Новгород, 1991, с | |||
| Аппарат, предназначенный для летания | 0 |
|
SU76A1 |
Авторы
Даты
2003-03-20—Публикация
2001-07-26—Подача