Изобретение относится к медицине, а именно к клинической микробиологии, и может быть использовано при бактериологическом исследовании различных клинических материалов и объектов внешней среды.
Определение лецитиназной активности является одним из диагностических тестов при выделении родов Clostridium, Bacillus, Staphylococcus, Anthracis.
Продукция фермента лецитиназы исследуется на средах с добавлением желточной эмульсии. Желточная эмульсия в качестве компонента входит в состав таких сред, как Baird Parker agar, Cereus Selective agar, Sodium Aside Egg-York Pyruvate agar, желточно-солевой агар [1, 2].
Известен способ получения желточной эмульсии путем смешивания желтка яиц с солевыми растворами с последующей фильтрацией [3].
Недостатками данного способа являются большая вероятность прохождения микроорганизмов через фильтр, возможность бактериального пророста, низкая емкость и необходимость наличия специального оборудования.
Наиболее близким решением задачи того же назначения к заявляемому изобретению по совокупности признаков является способ получения желточной эмульсии, заключающийся в смешивании желтка яиц с физиологическим раствором [4].
К причинам, препятствующим достижению указанного ниже технического результата при использовании известного способа, принятого за прототип, является обсеменение желточной эмульсии микроорганизмами, что ограничивает срок хранения препарата до нескольких дней.
Кроме того, наличие микроорганизмов в желточной эмульсии препятствуют росту изучаемого микроба, определению его свойств и изменяет состав среды. Указанные недостатки известного способа приводят к необходимости приготовления желточной эмульсии непосредственно перед проведением бактериологических исследований, что удлиняет сроки предварительной подготовки к анализу.
Задача предлагаемого изобретения - повышение стабильности и увеличение срока хранения желточной эмульсии.
Указанный технический результат при осуществлении изобретения достигается тем, что после смешивания желтка яиц с физиологическим раствором к смеси добавляют 1,0-2,0% хлороформа, выдерживают при температуре окружающей среды в течение 24 ч, а затем дважды прогревают при 56-58oС в течение 2 ч.
Обработка желточной эмульсии хлороформом, обладающим высокой бактерицидной активностью, и последующее прогревание позволяет получить стерильный препарат с длительным сроком хранения и обеспечивает проявление лецитиназной активности микроорганизмов.
Способ осуществляется следующим образом.
Пример 1. Свежие яйца моют щеткой с мылом, ополаскивают дистиллированной водой, дают обсохнуть, обтирают спиртом. Яйца разбивают, отделяют желтки и к 300 мл желтка добавляют 700 мл физиологического раствора, смесь размешивают до получения гомогенной эмульсии и фильтруют через воронку с 4 слоями стерильной марли. Отфильтрованную эмульсию разливают в стерильные флаконы, добавляют 1% хлороформа, закрывают стерильной ватно-марлевой пробкой и оставляют на сутки при температуре окружающей среды. Затем прогревают на водяной бане при 56-58oС в течение 2 ч, предварительно сняв ватно-марлевую пробку и закрыв флакон стерильной марлей. После чего, флаконы закрывают пробками, предварительно простерилизованными, плотно герметизируют металлическими колпачками и еще раз прогревают при тех же температурах и времени.
Контроль стерильности полученной желточной эмульсии определяют путем посева 0,1 мл желточной эмульсии из разведения 1:10 на стерильный питательный агар с последующей инкубацией посевов при (37±1)oС в течение 48 ч.
Проявление лецитиназной активности определяют путем посева на питательный агар с 5%-ной желточной эмульсией тест-штаммов В. cereus 2010, St. aureus Wood 46, St. aureus 209 "P", St. aureus "Виотко", St. aureus "Лепин", St. aureus ATCC 5538 с последующей инкубацией посевов при температуре (37±1)oС в течение 18-24 ч. При этом вокруг колоний тест-штаммов образуется прозрачный или слегка мутный ореол - зона лецитиназной активности.
Пример 2. Отличается от примера 1 тем, что к отфильтрованной эмульсии добавляют 1,5% хлороформа. Далее согласно примеру 1.
Пример 3. Отличается от примера 1 тем, что к отфильтрованной эмульсии добавляют 2% хлороформа. Далее согласно примеру 1.
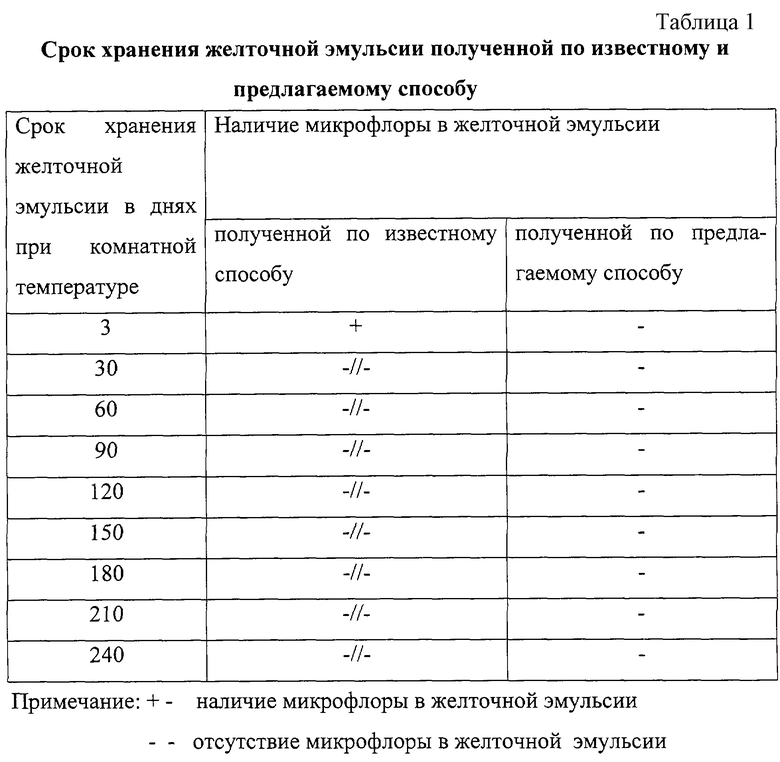
Результаты определения срока хранения желточной эмульсии, полученной по известному и предлагаемому способу, представлены в таблице 1.
Из таблицы 1 видно, что желточная эмульсия, полученная по предлагаемому способу имеет преимущество, так как на протяжении 240 дней хранения сохраняет свою стерильность. Желточная эмульсия, полученная по известному способу, теряет свою стерильность уже после 3-дневного хранения.
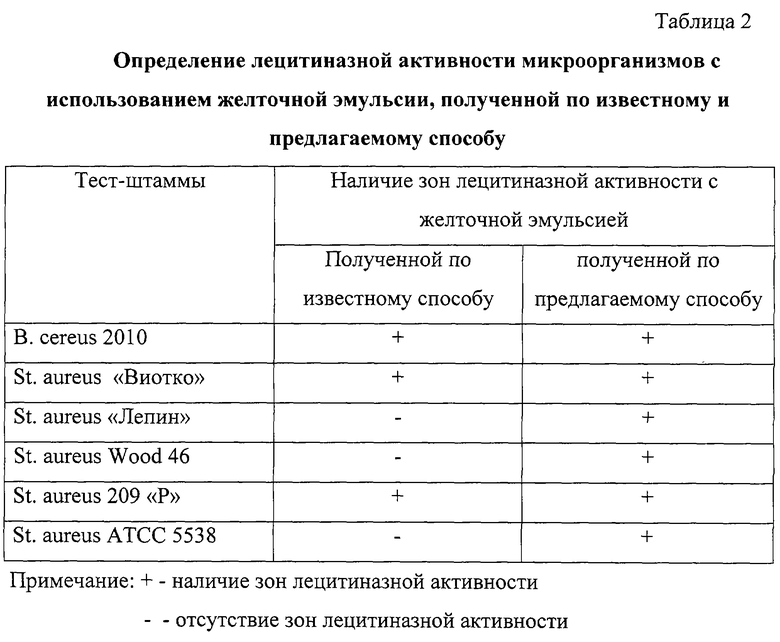
Кроме того, в результате обсемененности желточной эмульсии, полученной по известному способу, некоторые тест-штаммы не проявляют лецитиназной активности. Желточная эмульсия, полученная предлагаемым способом, обеспечивает проявление лецитиназной активности всеми тест-штаммами на протяжении всего срока хранения (таблица 2).
Предлагаемый способ прост в выполнении, легко воспроизводим, не требует специального оборудования и позволяет сократить сроки предварительной подготовки к бактериологическому анализу.
Литература
1. Лабинская А.С. Микробиология с техникой микробиологических исследований. - М.: Медицина, 1979, с. 358.
2. Microbiology Manual MERCK. 1990, s. 51-52; 74-75; 164.
3. The Oxoid Manual FIFTH Edition. 1982, s. 128-129.
3. Санитарная микробиология. / Под. ред. Калины Г.П. - М.: Медицина, 1969, с. 99 (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ BACILLUS CEREUS | 2001 |
|
RU2201965C2 |
| СРЕДСТВО ДЛЯ ПОДАВЛЕНИЯ РОЕНИЯ БАКТЕРИЙ РОДА ПРОТЕЯ | 1998 |
|
RU2145352C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ И ПРЕДВАРИТЕЛЬНОЙ ИДЕНТИФИКАЦИИ E.COLI 0157:H7 | 1998 |
|
RU2157837C2 |
| ТЕСТ-СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ АНТИБАКТЕРИАЛЬНЫХ СУБСТАНЦИЙ В МОЧЕ | 1999 |
|
RU2164946C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ИДЕНТИФИКАЦИИ ЛИСТЕРИЙ | 2001 |
|
RU2201957C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ЛАКТОБАКТЕРИЙ | 2001 |
|
RU2213779C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ПАТОГЕННЫХ ЭНТЕРОБАКТЕРИЙ | 2000 |
|
RU2179582C2 |
| СПОСОБ УСКОРЕННОГО ВЫРАЩИВАНИЯ ЗОЛОТИСТОГО СТАФИЛОКОККА ДЛЯ ДИАГНОСТИКИ ИНФЕКЦИЙ, СВЯЗАННЫХ С ОКАЗАНИЕМ МЕДИЦИНСКОЙ ПОМОЩИ | 2012 |
|
RU2511031C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ГЕМОКУЛЬТУРЫ ПРИ ДИАГНОСТИКЕ БРЮШНОГО ТИФА И ПАРАТИФОВ | 2000 |
|
RU2175671C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ Cl. PERFRINGENS | 2001 |
|
RU2203939C2 |
Изобретение относится к медицине, а именно к клинической микробиологии, и может быть использовано при бактериологическом исследовании различных клинических материалов и объектов внешней среды. Желтки яиц смешивают с физиологическим раствором, к полученной смеси добавляют 1,0-2,0% хлороформа, выдерживают при температуре окружающей среды в течение 24 ч, а затем дважды прогревают при 56-58oС в течение 2 ч. Изобретение обеспечивает стабильность и длительность сроков хранения препарата, что сокращает сроки предварительной подготовки к проведению бактериологического анализа. 2 табл.
Способ получения желточной эмульсии для определения лецитиназной активности микроорганизмов путем смешивания желтков яиц с физиологическим раствором, отличающийся тем, что после смешивания к смеси добавляют 1,0-2,0% хлороформа, выдерживают при температуре окружающей среды в течение 24 ч, а затем дважды прогревают при 56-58oС в течение 2 ч.
| Санитарная микробиология/Под ред | |||
| Г.П | |||
| КАЛИНЫ и Г.Н | |||
| ЧИСТОВИЧА | |||
| - М.: Медицина, 1969, с.99, 167 | |||
| Руководство по микробиологии, клинике и эпидемиологии инфекционных болезней/Под ред | |||
| ЖУКОВА-ВЕРЕЖНИКОВА | |||
| - М.: Медпед, 1962, с.322 | |||
| КОЗЛОВ Ю.А | |||
| Питательные среды в медицинской микробиологии | |||
| - М.: Медпед, 1950, с | |||
| Облицовка комнатных печей | 1918 |
|
SU100A1 |
Авторы
Даты
2003-05-10—Публикация
2001-08-14—Подача