Изобретение относится к способу получения 3-циано-2,4-дигалоген-5-фторбензойных кислот, промежуточным продуктам для осуществления указанного способа и к способу получения этих промежуточных продуктов.
3-Циано-2,4-дигалоген-5-фторбензойная кислота известна из немецкой заявки на патент DE-A-3702393. Ее получают из 3-амино-2,4-дихлор-5-фторбензойной кислоты диазотированием и взаимодействием соли диазония с цианидными солями. Этот способ невыгоден прежде всего при его осуществлении в крупнопромышленном масштабе.
Предметом настоящего изобретения являются
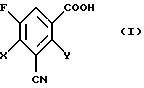
1. Способ получения 3-циано-2,4-дигалоген-5-фторбензойных кислот формулы (I)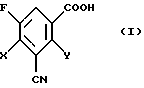
в которой Х и Y независимо друг от друга обозначают галоген,
путем гидролитического расщепления
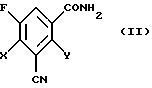
а) амидов 3-циано-2,4-дигалоген-5-фторбензойной кислоты формулы (II)
в которой Х и Y независимо друг от друга обозначают галоген,
или
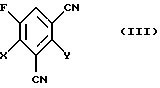
б) 1,3-дициано-2,4-дигалоген-5-фторбензолов формулы (III)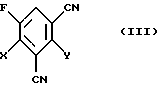
в которой Х и Y независимо друг от друга обозначают галоген,
или
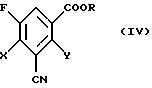
в) эфиров 3-циано-2,4-дигалоген-5-фторбензойной кислоты формулы (IV)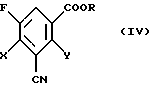
в которой Х и Y независимо друг от друга обозначают галоген и
R обозначает алкил с 1-4 атомами углерода, который необязательно может быть замещен.
2. Новые соединения формул (II)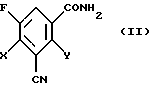
и формулы (IV)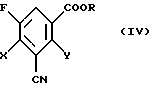
в которой Х и Y независимо друг от друга обозначают галоген и
R обозначает алкил с 1-4 атомами углерода, который необязательно может быть замещен,
за исключением метилового эфира 3-циано-2,4,5-трифторбензойной кислоты.
3. Способ получения амидов 3-циано-2,4-дигалоген-5-фторбензойной кислоты формулы (II)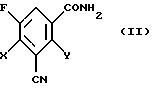
соответственно эфиров формулы (IV)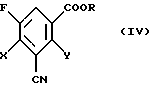
отличие которого состоит в том, что 1,3-дициано-2,4-дигалоген-5-фторбензолы формулы (III)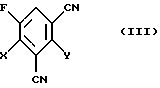
в которой Х и Y имеют вышеуказанное значение,
гидролизуют в присутствии воды или в присутствии спиртов.
4. Новые соединения формулы (III)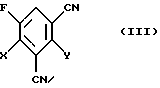
в которой X и Y обозначают неодинаковые остатки, выбранные из группы, состоящей из фтора и хлора, или оба остатка обозначают хлор.
5. Способ получения соединений формулы (III)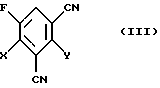
которой Х и Y обозначают неодинаковые остатки, выбранные из группы, состоящей из фтора и хлора,
отличие которого состоит в том, что 1,2,4-трифтор-3,5-дицианбензол(2,4,5-трифторизофталодинитрид) подвергают взаимодействию с галогенидом металла.
1,2,4-Трифтор-3,5-дицианобензол и его получение известны из ЕР-А-307897.
В вышеприведенных формулах Х и Y предпочтительно обозначают фтор или хлор. В соединениях формул (II) и (IV) они особенно предпочтительно обозначают одинаковые остатки фтор или хлор.
В соединениях формулы (III) особенно предпочтителен 2,4-дихлор-5-фторизофталодинитрил.
R предпочтительно обозначает метил, этил, пропил или бензил.
Если в качестве исходного продукта для получения 3-циано-2,4,5-трифторбензойной кислоты согласно способу а) используется 3-циано-2,4,5-трифторбензамид, то реакцию можно наглядно представить в виде следующей схемы:
Используемые в качестве исходных продуктов амиды формулы (II) являются новыми. Их получение описано ниже.
Гидролиз проводится в присутствии кислот и воды. В качестве кислот могут применяться сильные органические и неорганические кислоты, такие как, например, НСl, НВr, серная кислота, метансульфоновая кислота, трифторметансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, и сильнокислотные ионообменники в присутствии воды.
В качестве растворителей может применяться используемая в качестве реагента кислота в избытке или органический растворитель. В качестве органических растворителей могут рассматриваться кислоты, такие как муравьиная, уксусная, пропионовая кислота; эфиры, такие как диметоксиэтан, диоксан; кетоны, такие как ацетон, бутанон.
Компоненты реакции могут смешиваться в любой последовательности. Затем производится нагревание до необходимой температуры.
Температура реакции находится в пределах от 0 до 200oС, предпочтительно от 20 до 150oС.
Реакция может проводиться при нормальном давлении или при повышенном давлении в пределах от 0 до 50 бар, предпочтительно от 0 до 6 бар.
Продукты отфильтровываются из реакционной смеси при необходимости после разбавления водой. В случае применения большого избытка кислоты или растворителя может оказаться целесообразным проведение отгонки и выделение продукта путем экстракции.
Если в качестве исходного продукта для получения 4-хлор-2,5-дифтор-3-цианобензойной кислоты согласно способу 1б) используется 4-хлор-2,5-дифторизофталодинитрил, то реакцию можно наглядно представить в виде следующей схемы:
2,4,5-Трифторизофталодинитрил известен из литературы (ЕР-А-307897).
2,4-Дихлор-5-фторизофталодинитрил является новым. Его получение описано ниже.
Гидролиз проводится с помощью кислот в присутствии воды. В качестве кислот могут применяться сильные органические и неорганические кислоты, такие как, например, HCl, HВr, серная кислота, метансульфоновая кислота, трифторметансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, и сильнокислотные ионообменники в присутствии воды.
В качестве растворителей может применяться используемая в качестве реагента кислота в избытке или органический растворитель. В качестве органических растворителей могут рассматриваться кислоты, такие как муравьиная, уксусная, пропионовая кислота; эфиры, такие как диметоксиэтан, диоксан; кетоны, такие как ацетон, бутанон.
Компоненты реакции могут смешиваться в любой последовательности. Затем производится нагревание до необходимой температуры.
Температура реакции находится в пределах от 0 до 200oС, предпочтительно от 20 до 150oС.
Реакция может проводиться при нормальном давлении или при повышенном давлении в пределах от 0 до 50 бар, предпочтительно от 0 до 6 бар.
Продукты отфильтровываются из реакционной смеси при необходимости после разбавления водой. В случае применения большого избытка кислоты или растворителя может оказаться целесообразным проведение отгонки и выделение продукта путем экстракции.
Если в качестве исходного продукта согласно способу 1в) для получения 3-циано-2,4,5-трифторбензойной кислоты используется метиловый эфир 3-циано-2,4,5-трифторбензойной кислоты, то реакцию можно наглядно представить в виде следующей схемы: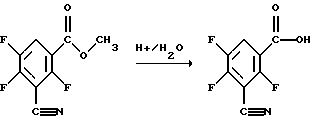
Применяемые в качестве исходных продуктов сложные эфиры формулы (IV) являются новыми. Их получение описано ниже.
Гидролиз проводится в присутствии кислот и воды. В качестве кислот могут применяться сильные органические и неорганические кислоты, такие как, например, HCl, HBr, серная кислота, метансульфоновая кислота, трифторметансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота и сильнокислотные ионообменники в присутствии воды.
В качестве растворителей может применяться используемая в качестве реагента кислота в избытке или органический растворитель. В качестве органических растворителей могут рассматриваться кислоты, такие как муравьиная, уксусная, пропионовая кислота; эфиры, такие как диметоксиэтан, диоксан; кетоны, такие как ацетон, бутанон.
Компоненты реакции можно смешивать в любой последовательности. Затем производится нагревание до необходимой температуры.
Температура реакции находится в пределах от 0 до 200oС, предпочтительно от 20 до 150oС.
Реакция может проводиться при нормальном давлении или при повышенном давлении в пределах от 0 до 50 бар, предпочтительно от 0 до 6 бар.
Продукты отфильтровываются из реакционной смеси при необходимости после разбавления водой. В случае применения большого избытка кислоты или растворителя может оказаться целесообразным проведение отгонки.
Как уже упоминалось, соединения формулы (IV) являются новыми.
Если в качестве исходного продукта для получения соединений согласно способу 3) используется 2,4-дихлор-5-фторизофталодинитрил, то реакцию можно наглядно представить в виде следующей схемы: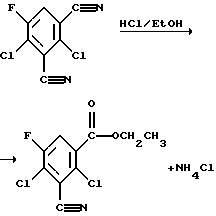
Реакция протекает через образование в качестве промежуточного продукта сложного иминоэфира и его гидролиз водой. В качестве побочной реакции наблюдается образование соответствующего амида. Если не производится добавление воды, то образование амида становится главной реакцией (см. ниже).
2,4,5-Трифторизофталодинитрил известен из литературы (ЕР-А-307897).
2,4-Дихлор-5-фторизофталодинитрил является новым, его получение описано ниже.
Соединение формулы (II) получается путем гидролиза соответствующих динитрилов с помощью кислот в присутствии воды и спиртов.
Взаимодействие проводится в присутствии от 1 до 10 эквивалентов воды и первичных и вторичных алифатических спиртов. Предпочтительны метанол, этанол, пропанол и бутанол. В качестве кислот могут применяться сильные органические и неорганические кислоты, такие как НСl, НВr, серная кислота, метансульфоновая кислота, трифторметансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, и сильнокислотные ионообменники.
На 1 моль динитрила может расходоваться, помимо 1-10 молей спирта, также от 1 до 10 молей воды.
Реакция может происходить как в присутствии растворителей, так и без них. В качестве растворителей можно применять используемый в качестве реагента спирт в избытке или инертный органический растворитель. Инертными органическими растворителями являются все инертные органические растворители, такие как углеводороды, например пентан, гексан, гептан, петролейный эфир, бензин, лигроин, бензол, толуол; галогенированные углеводороды, такие как дихлорметан, хлороформ, хлорбензол, дихлорбензол, трихлорэтан; эфиры, такие как диэтиловый эфир, дибутиловый эфир, этиленгликольдиметиловый эфир, диэтиленгликольдиэтиловый эфир.
Вначале загружают динитрил и спирт, затем к ним прибавляют кислоту, после чего добавляют воду. Однако необходимую для реакции воду можно загружать также сразу непосредственно.
Температура реакции находится в пределах от -20 до 150oС, предпочтительно от 10 до 100oС.
Реакция может проводиться при нормальном давлении или при повышенном давлении в пределах от 0 до 50 бар, предпочтительно от 0 до 6 бар.
Реакционную смесь разбавляют водой и экстрагируют. Если используется спирт в большом избытке или инертный растворитель, растворитель может быть предварительно отогнан. Образовавшийся в качестве побочного продукта реакции амид может быть отделен.
Как уже упоминалось, соединения формулы (II) являются новыми.
Если в качестве исходного продукта для получения соединений согласно способу 3) используется 2,4,5-трифторизофталодинитрил, то реакцию можно наглядно представить в виде следующей схемы: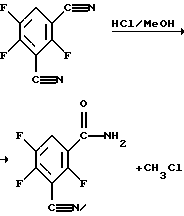
Реакция протекает через образование в качестве промежуточных продуктов сложных иминоэфиров, из которых путем отщепления алкильных остатков образуются амиды.
2,4,5-Трифторизофталодинитрил известен из литературы (ЕР-А-307897).
2,4-Дихлор-5-фторизофталодинитрил является новым, его получение описано ниже по тексту.
Взаимодействие с первичными и вторичными алифатическими спиртами присходит в присутствии кислот. Предпочтительны метанол, этанол, пропанол и бутанол. Особенно предпочтителен метанол. В качестве кислот могут применяться сильные органические и неорганические кислоты, такие как, например, НСl, НВr.
На 1 моль динитрила может расходоваться от 1 до 10 молей спирта.
Реакция может проводиться как в присутствии растворителя, так и без растворителя. В качестве растворителей можно применять используемый в качестве реагента спирт в избытке или инертный органический растворитель. Инертными растворителями являются все инертные органические растворители, такие как углеводороды, например пентан, гексан, гептан, петролейный эфир, бензин, лигроин, бензол, толуол; галогенированные углеводороды, такие как дихлорметан, хлороформ, хлорбензол, дихлорбензол, трихлорэтан; эфиры, такие как диэтиловый эфир, дипропиловый эфир, дибутиловый эфир, этиленгликольдиметиловый эфир, диэтиленгликольдиэтиловый эфир.
Вначале загружают динитрил и спирт, затем прибавляют кислоту.
Температура реакции находится в пределах от -20 до 150oС, предпочтительно от 0 до 100oС.
Взаимодействие может проводиться при нормальном давлении или при повышенном давлении в пределах от 0 до 50 бар, предпочтительно от 0 до 6 бар.
Продукты из реакционной смеси отфильтровывают при необходимости после разбавления водой, водой и экстрагируют. Если используется спирт в большом избытке или инертный растворитель, то растворитель может быть предварительно отогнан.
Соединения формулы (III), в которых Х и Y одновременно не обозначают F, являются новыми. Если в качестве исходного продукта используется 2,4,5-трифтор-изофталодинитрил, то получение соединения согласно способу 5) может быть представлено следующей схемой реакции: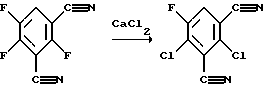
2,4,5-Трифторизофталодинитрил известен из литературы (ЕР-А-307897).
Обмен галогенами происходит в результате реакции с неорганическими хлоридными солями.
В качестве неорганических хлоридных солей могут быть использованы MgCl2, CaСl2. Реакция также может катализироваться, например, солями тетраалкиламмония, краун-эфирми и так далее.
Неорганическая соль применяется в количестве от 0,5 до 10 молей на подлежащий обмену фтор, предпочтительно в количестве от 0,5 до 2 молей.
Реакция может проводиться как в присутствии растворителя, так и без растворителя. В качестве растворителей можно применять все инертные органические растворители, например пентан, гексан, гептан, петролейный эфир, бензин, лигроин, бензол, толуол, дихлорметан, хлороформ, хлорбензол, дихлорбензол, трихлорэтан; эфиры, такие как дибутиловый эфир, этиленгликольдиметиловый эфир, диэтиленгликольдиэтиловый эфир, кетоны, такие как ацетон, метилэтилкетон, циклогексанон, а также N-метилпирролидинон, диметилсульфон, сульфолан.
Вещества смешивают и нагревают до нужной температуры. Последовательность добавления не играет роли. В зависимости от условий проведения реакции на один атом хлора могут быть обменены один или два атома фтора.
Температура реакции находится в пределах от 50 до 350oС. Предпочтительны температуры от 90 до 250oС.
Реакция может проводиться при нормальном давлении или при повышенном давлении. При использовании низкокипящих растворителей предпочтительно проводить реакцию при повышенном давлении. Пределы давлений: от 0 до 100 бар, предпочтительно от 0 до 50 бар (избыточное давление).
Выделение продуктов производится путем отфильтровывания неорганических солей и фракционной перегонки фильтрата. Если применялся смешивающийся с водой растворитель, то реакционную смесь можно выливать на воду и экстрагировать.
3-Циан-2,4-дигалоген-5-фторбензойная кислота может быть использована, например, для получения следующих, известных из патента США US-P-4990517 соединений (VIII):
7-хлор-8-циан-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновая кислота,
метиловый эфир 7-хлор-8-циан-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты,
8-циан-1-циклопропил-6,7-дифтор-1,4-дигидро-4-оксо-3-хинолинкарбоновая кислота,
этиловый эфир 8-циан-1-циклопропил-6,7-дифтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты.
С этой целью, например, 3-циан-2,4,5-трифторбензойную кислоту в форме ее хлорангидрида подвергают взаимодействию с эфиром β-диметиламиноакриловой кислоты формулы (V) и полученный продукт формулы (VI) подвергают дальнейшему взаимодействию с циклопропиламином с получением соединения формулы (VII), получая затем вышеназванное соединение (VIII)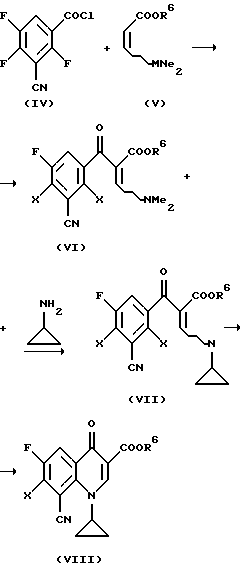
В вышеприведенной схеме символы обозначают следующее:
Х галоген, в частности фтор или хлор,
R6 алкил с 1-4 атомами углерода, в частности метил или этил.
Также возможно проводить реакцию соединения формулы (IV) непосредственно с эфиром 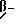 циклопропиламиноакриловой кислоты
циклопропиламиноакриловой кислоты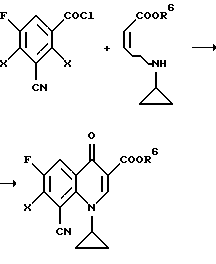
(в формулах X и R6 имеют вышеуказанные значения).
Хлорангидрид 3-циан-2,4,5-трифторбензойной кислоты может быть получен из сложных эфиров формулы (IV) по следующей схеме: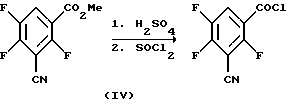
Из соединений формулы (VIII) могут быть получены путем взаимодействия с подходящими аминами антибактриально эффективные соединения.
Если, например, 7-хлор-8-циан-1-циклопропил-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновую кислоту подвергают взаимодействию с 2,8-диазабицикло[4.3.0]нонаном, то ход реакции можно представить следующей схемой: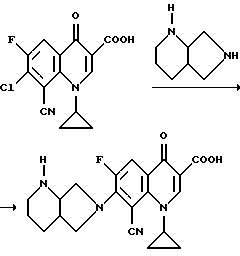
Получение этих соединений описано в неопубликованной заявке на немецкий патент DE-A-19633805 заявителя.
Нижеследующие примеры поясняют изобретение, не ограничивая его объема.
Пример 1 (способ 1а).
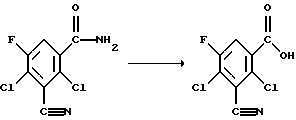
0,4 г (1,72 моля) 3-циано-2,4-дихлор-5-фторбензамида и 5 мл концентрированной соляной кислоты нагревают в течение трех часов с обратным холодильником. После этого упаривают и остаток сушат в эксикаторе над серной кислотой. Выход 370 мг. Чистота 84% (площадь на ЖХВР-хроматограмме) 3-циано-2,4-дихлор-5-фторбензойной кислоты, 12% (площадь на ЖХВР-хроматограмме) 3-циано-2,4-дихлор-5-фторбензамид (исходный материал).
В этом и других примерах аббревиатура ЖХВР обозначает "жидкостую хроматографию высокого разрешения".
Пример 2 (способ 1б).
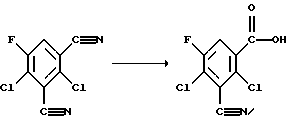
2,5 г (12 молей) 2,4-дихлор-5-фторизофталодинитрила суспендируют в 25 мл метанола, охлаждают до 0oС и насыщают газообразным НСl. Смесь оставляют стоять на 60 часов при -16oС. После этого упаривают. Остаток смешивают с 38 мл концентрированной соляной кислоты и нагревают в течение трех часов с обратным холодильником. Затем выливают на 120 мл воды, осадок отсасывают и сушат в эксикаторе над серной кислотой. Выход 1,86 г. Чистота 87% 3-циано-2,4-дихлор-5-фторбензойной кислоты, 10% 3-циано-2,4-дихлор-5-фтор-бензамида.
Пример 3 (способ 1б).
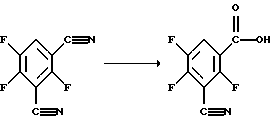
1 г (5,5 моля) 2,4,5-трифторизофталодинитрила, 6,3 мл воды, 6,3 мл ледяной уксусной кислоты и 0,63 мл 96%-ной серной кислоты нагревают в течение 24 часов с обратным холодильником. Затем выливают на 50 мл воды и смешивают с 25 мл дихлорметана. После этого рН водной фазы доводят до значения 9 с помощью 45%-ного NaOH, органическую фазу затем отделяют и дважды экстрагируют дихлорметаном. Экстракты выбрасывают. рН оставшейся водной фазы доводят с помощью концентрированной соляной кислоты до значения 2 и в общей сложности трижды экстрагируют каждый раз 25 мл дихлорметана. Объединенные экстракты сушат сульфатом натрия и упаривают. Остаток 470 мг. Чистота 80% (ГХ/МС-площадь на хроматограмме).
Пример 4 (способ 1в).
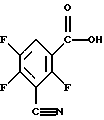
2 г (8,7 моля) этилового эфира 3-циано-2,4,5-трифторбензойной кислоты (чистотой 79%), 10 мл ледяной уксусной кислоты, 10 мл воды и 1 мл 96%-ной серной кислоты нагревают в течение 7,5 часов с обратным холодильником. После этого охлаждают, выливают на 100 мл воды и трижды экстрагируют дихлорметаном. Экстракт смешивают со 100 мл воды и при перемешивании доводят рН водной фазы до значения 8,5. Органическую фазу отделяют, водную фазу дополнительно экстрагируют дихлорметаном. Органические экстракты выбрасывают. К водной фазе добавляют 50 мл дихлорметана и подкисляют серной кислотой. Дихлорметан отделяют и еще раз проводят экстракцию дихлорметаном. Объединенные экстракты затем сушат с помощью Na2SO4 и упаривают. Остаток сушат в эксикаторе над КОН. Выход 1,2 г (81% от теоретического). Чистота 95% (площадь на ЖХВР-хроматограмме). Т. пл. 146oС.
Пример 5 (способ 3).
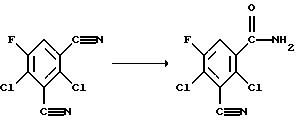
9 г (42 моля) 2,4-дихлор-5-фторизофталодинитрила суспендируют в 90 мл метанола, охлаждают до 5oC и вводят газообразный НСl до насыщения. Образовавшийся раствор перемешивают в течение 24 часов при комнатной температуре. Затем упаривают, остаток смешивают с дихлорметаном и отсасывают. Выход 8,04 г. Чистота 95% (площадь на ЖХВР-хроматограмме). Т. пл. 178oС.
Пример 6 (способ 3).
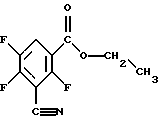
5,52 г (30 молей) 2,4,5-трифторизофталодинитрила (чистотой 86%) загружают в 60 мл сухого этанола и при охлаждении льдом вводят газообразный НСl до насыщения. Перемешивают в течение четырех часов при комнатной температуре, затем добавляют 4,8 мл (0,266 моль) воды и нагревают в течение четырех часов с обратным холодильником. После этого упаривают, остаток распределяют между водой и хлороформом. Органическую фазу отделяют, водную фазу еще дважды экстрагируют хлороформом. Собранные экстракты сушат с помощью Na2SO4 и упаривают. Остаток перегоняют в трубке с шаровым расширением. Т. кип. 220oС (42 мбар). Выход 4,21 г (55% от теоретического). Чистота 79% (площадь на ЖХВР -хроматограмме).
1Н-ЯМР (CDCl3):
8,1 ч/млн (m, 1H, Ar-H),
4,4 ч/млн (t, J=8 Гц, 2Н, -ОСН2-),
1,4 ч/млн (t, J=8 Гц, 3Н, -СН3).
Пример 7 (способ 3).
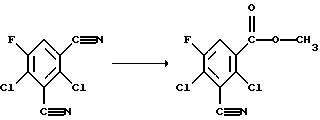
0,5 г (2,3 моля) 2,4-дихлор-5-фторизофталодинитрила растворяют в 10 мл метанола и при хорошем охлаждении при 0oС насыщают газообразным НСl. Затем смесь оставляют стоять на 72 часа при -10oС. После этого добавляют 1 мл 96%-ного водного метанола и в течение трех часов нагревают с обратным холодильником. Затем упаривают в вакууме, остаток распределяют между хлороформом и насыщенным раствором бикарбоната, органическую фазу отделяют, сушат сульфатом натрия и упаривают. Остаток 410 мг. После ЖХВР в нем содержалось 10% исходного материала, 7,5% амида, 76% метилового эфира.
Пример 8 (способ 5).
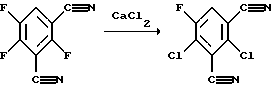
13,5 г (74 моля) 2,4,5-трифторизофталодинитрила, 125 мл сульфолана и 17,7 г свежепульверизованного хлорида кальция нагревают в течение 24 часов до 200oС и затем выливают на 1200 мл воды. Тонкий осадок отсасывают и сушат. Выход 13,8 г.
Для очистки может быть профильтрован через силикагель с толуол/гексаном. Выход 12,8 г. Чистота 96% (площадь на ЖХВР-хроматограмме). Т. пл. 119oС.
Пример 9 (способ 5).
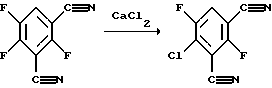
0,55 г (3 моля) 2,4,5-трифторизофталодинитрила, 5 мл сульфолана и 0,37 г (3,3 моля) свежепульверизованного хлорида кальция нагревают в течение 1,5 часов до 200oС, затем выливают на 100 мл воды и дважды экстрагируют эфиром. Экстракт сушат сульфатом натрия и упаривают. Выход 0,56 г. Состав: 75% 4-хлор-2,5-дифторизофталодинитрила, 25% 5-фтор-2,4-дихлоризофталодинитрила (площадь на ЖХВР-хроматограмме).
| название | год | авторы | номер документа |
|---|---|---|---|
| 8-ЦИАН-1-ЦИКЛОПРОПИЛ-7-(2,8-ДИАЗАБИЦИКЛО(4.3.0)-НОНАН-8-ИЛ)-6-ФТОР-1,4-ДИГИДРО-4-ОКСО-3-ХИНОЛИНКАРБОНОВЫЕ КИСЛОТЫ, ИХ ПРОИЗВОДНЫЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2173318C2 |
| КАРБАНИЛИДЫ И СРЕДСТВО ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ И ПАТОГЕННЫМИ ГРИБАМИ НА ИХ ОСНОВЕ | 1997 |
|
RU2194704C2 |
| ПРОИЗВОДНЫЕ N-СУЛЬФОНИЛИМИДАЗОЛА И ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ И ФУНГИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1997 |
|
RU2171806C2 |
| СПОСОБ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ПОЛУЧЕНИЯ ПРОСТЫХ ГИДРОКСИЛАМИНОВЫХ ЭФИРОВ И ИХ СОЛЕЙ | 1993 |
|
RU2119911C1 |
| АМИДЫ ИЗОТИАЗОЛКАРБОНОВОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2214403C2 |
| ОРТОЗАМЕЩЕННЫЕ АМИДЫ 2-МЕТОКСИИМИНОФЕНИЛУКСУСНОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СРЕДСТВО ДЛЯ БОРЬБЫ С ВРЕДОНОСНЫМИ ГРИБАМИ И ИНСЕКТОАКАРИЦИДНОЕ СРЕДСТВО | 1994 |
|
RU2130924C1 |
| ЗАМЕЩЕННЫЕ АРИЛКЕТОНЫ | 2001 |
|
RU2299879C2 |
| Способ получения производных акриловой кислоты | 1985 |
|
SU1395139A3 |
| 2,4,5-ТРИЗАМЕЩЕННЫЕ ФЕНИЛКЕТОЕНОЛЫ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ, СПОСОБ И СРЕДСТВО ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ И ПАУКООБРАЗНЫМИ НА ИХ ОСНОВЕ | 1996 |
|
RU2195449C2 |
| ПРОИЗВОДНЫЕ 3-ГАЛОГЕН-3-ГЕТАРИЛКАРБОНОВОЙ КИСЛОТЫ, ГЕРБИЦИДНОЕ СРЕДСТВО | 1994 |
|
RU2146255C1 |
Изобретение относится к способам получения 3-циано-2,4-дигалоген-5-фторбензойных кислот формулы (I), в которой Х и Y независимо друг от друга обозначают галоген, которые являются промежуточными продуктами для получения эффективных антибактериальных соединений. Способ заключается в гидролитическом расщеплении в присутствии кислоты и воды при температуре 0-200oС амида 3-циано-2,4-дигалоген-5-фторбензойной кислоты формулы (II), или 1,3-дициано-2,4-дигалоген-5-фторбензола формулы (III), или сложного эфира 3-циано-2,4-дигалоген-5-фторбензойной кислоты формулы (IV), в которых Х и Y имеют вышеуказанные значения, a R обозначает алкил с 1-4 атомами углерода, который необязательно может быть замещен. Также изобретение касается новых соединений формулы (Iа), где Х и Y независимо друг от друга обозначают галоген, Z означает группу CN, CONH2 или COOR, где R обозначает алкил с 1-4 атомами углерода, который необязательно может быть замещен, при этом в случае Z=CN, Х и Y обозначают неодинаковые остатки, выбранные из группы, состоящей из фтора и хлора, или оба остатка обозначают хлор, а в случае Z=COOR, R не означает метил и каждый из радикалов Х и У не означает фтор, которые являются промежуточными продуктами для получения соединений формулы (I). Способы могут быть использованы при получении соединений формулы (I) в крупнопромышленном масштабе. 4 с.п. ф-лы.


в которой Х и Y независимо друг от друга обозначают галоген,
отличающийся тем, что амид 3-циано-2,4-дигалоген-5-фторбензойной кислоты формулы (II)
в которой Х и Y имеют вышеуказанное значение,
подвергают гидролитическому расщеплению в присутствии кислоты и воды при температуре 0-200oС.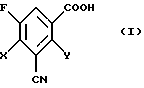
в которой X и Y независимо друг от друга обозначают галоген,
отличающийся тем, что 1,3-дициано-2,4-дигалоген-5-фторбензол формулы (III)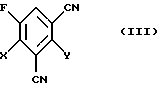
в которой Х и Y имеют вышеуказанное значение,
подвергают гидролитическому расщеплению в присутствии кислоты и воды при температуре 0-200oС.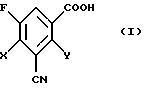
в которой Х и Y независимо друг от друга обозначают галоген,
отличающийся тем, что сложный эфир 3-циано-2,4-дигалоген-5-фторбензойной кислоты формулы (IV)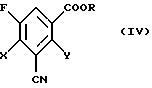
в которой Х и Y имеют вышеуказанное значение;
R обозначает алкил с 1-4 атомами углерода, который необязательно может быть замещен,
подвергают гидролитическому расщеплению в присутствии кислоты и воды при температуре 0-200oС.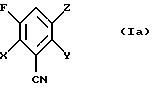
в которой Х и Y независимо друг от друга обозначают галоген;
Z означает группу CN, СОNН2 или COOR, где R обозначает алкил с 1-4 атомами углерода, который необязательно может быть замещен, при этом в случае Z= CN, Х и Y обозначают неодинаковые остатки, выбранные из группы, состоящей из фтора и хлора, или оба остатка обозначают хлор, а в случае Z= COOR, R не означает метил и каждый из радикалов Х и У не означает фтор.
| ЭЛЕКТРОГИДРАВЛИЧЕСКИЙ СЛЕДЯЩИЙ ПРИВОД | 0 |
|
SU307897A1 |
| Бюлер К., Пирсон Д | |||
| Органические синтезы | |||
| - М.: Мир, 1973, ч.2, с.591 | |||
| DE 3702393 А, 11.08.1988 | |||
| Способ получения цианбензойных кислот | 1975 |
|
SU595300A1 |
Авторы
Даты
2003-10-27—Публикация
1998-07-18—Подача