Изобретение относится к способу переработки пироконденсата высокотемпературного гомогенного пиролиза предельных углеводородов усредненного состава от С3Н8 до C5H12 при производстве ацетилена и этилена.
При всем различии технологических процессов пиролиз углеводородов при температуре 1600-2000oС и выше [С.П. Гориславец и др. Пиролиз углеводородного сырья. Изд. "Наукова думка", 1977, с. 197, 292] [Анг. Патент 924591, 1963] до целевых продуктов всегда сопровождается образованием значительного количества пироконденсата. В производстве ацетилена и этилена пироконденсат, так называемая "стабильная ароматика", не находит квалифицированного применения, идет в отвал или, в лучшем случае, его используют как компонент котельного топлива.
Целевая квалифицированная переработка пироконденсата, как отхода производства, не только позволяет значительно повысить экономические, но и улучшить экологические показатели производства. Неквалифицированная переработка таких отходов, обладающих определенной токсичностью (и даже концерогенностью) [Вредные вещества в промышленности. Спр. т.1, изд. "Химия", Л-д, 1976, с. 77, 140 и др.], не способствует охране окружающей среды и безопасности производства.
Известные технические решения по переработке пироконденсата связаны с дробной дистилляцией, селективной экстракцией и фракционной разгонкой компонентов сложной смеси. Примеры решения описаны, например, в монографии [С.П. Гориславец и др. Пиролиз углеводородного сырья. Изд. "Наукова думка", 1977, с. 197, 292]. Однако рациональным такое решение не является. Выделение одного какого-либо компонента не решает проблемы в целом, а выделение каждого из, например, 15 компонентов смеси продуктов пироконденсата представляет только теоретическую ценность. Для практики это чрезвычайно сложное и весьма дорогое решение.
В частности, это продемонстрировано в способе разделения смеси ароматических углеводородов [Авт. св. СССР 422164, С 10 G 25/00. Бюл. 12, опубл. 30.03.74].
Более приемлемым техническим решением является способ совместной переработки пироконденсата и отработанной серной кислоты по [Авт. св. СССР 1772133 А1 С, 10 G 17/06. Бюл. 40, опубл. 30.10.92]. Утилизация отходов производства осуществляется путем сульфирования 85% H2SO4 ароматических продуктов пироконденсата при массовом соотношении 1:1-2 при нагревании до кипения с последующей отгонкой непрореагировавшего бензола с выходом 2-35% с одновременным получением сульфомассы (около 60-70%), которая представляет интерес для применения в производстве бетона.
Однако указанный способ переработки пироконденсата ограниченно решает проблему утилизации отходов производства по ряду причин.
При больших объемах производства пироконденсата реализовать, например, сульфомассу невозможно из-за несоответствия спроса и предложений. Кроме того, переработке подвергается пироконденсат, содержащий в своем составе 52-53% бензола и 0,6-0,7% высших ароматических углеводородов, а остальное приходится на алкилбензолы. Такой состав пироконденсата образуется при малых нагрузках углеводородного сырья при производстве этилена и ацетилена. При оптимальных режимах работы установки гомогенного пиролиза содержание бензола в пироконденсате в 2-3 раза меньше, а высших ароматических углеводородов около 20%. При этом отличительные признаки способа совместной утилизации отходов должны быть иные.
Технические решения, связанные с переработкой других пироконденсатов или углеводородного сырья, не ставят перед собой цели и задачи, аналогичные заявленному. Так, в качестве окислителя для обработки различных фракций широко используется кислород О2 и воздух, например [Авт. св. СССР 1382404 A3, С 10 G 27/06. Бюл. 10, опубл. 15.03.88], перекись водорода Н2O2 [Авт. св. СССР 1540998 А1, С 10 G 17/06. Бюл. 10, опубл. 15.09.90], гидроперекись трет-бутила, но все они посвящены очистке углеводородного сырья от примесей.
Предлагаемый способ переработки пироконденсата решает проблему утилизации отходов путем расширения областей использования товарных продуктов, полученных из пироконденсата, образующихся в оптимальных режимах пиролиза, состава, мас. %: циклопентадиен 1-2, бензол 15-20, толуол 35-40, этилбензол 15-20, стирол 8-15, фенилацетилен 1-3, высшие ароматические углеводороды 12-18.
Задачей предлагаемого изобретения является получение бензола, бензойной кислоты и мастики из сложной смеси продуктов, каким является пироконденсат высокотемпературного пиролиза углеводородов.
Технический результат достигается тем, что пироконденсат первоначально подвергается фракционной разгонке при атмосферном давлении с дефлегматором на три фракции: первая фракция с т.кип. до 80-83oС, вторая фракция с т.кип. от 84 до 165oС и третья с т.кип. более 165oС - кубовый остаток. Химический и хроматографический анализ показывает, что первая фракция в количестве 14-19% от массы пироконденсата является преимущественно бензолом с содержанием основного вещества не ниже 90%. Такой бензол может применяться в качестве растворителя, добавки к моторному топливу и т.п.
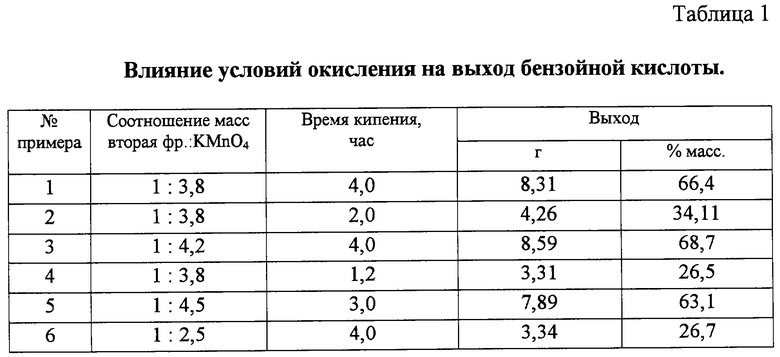
Вторая фракция с т.кип. от 84 до 165oС подвергается окислению перманганатом калия КМnО4 при соотношении (мас.) 1:3,6-4,0 при нагревании в течение 3-4 ч в водном растворе при температуре кипения реакционной массы с получением бензойной кислоты с выходом 63-68% от теории. Бензойная кислота применяется в производстве хлористого бензила, ряда полупродуктов и красителей, используется в качестве консерванта пищевых продуктов.
Физико-химические основы процесса окисления указанной фракции пироконденсата базируются на использовании простого и доступного метода окисления гомологов бензола, содержащих предельную и кратную связь в боковой цепи. Вне зависимости от длины цепи окисление протекает по углероду α-положения по отношению к ароматическому ядру. Использованы водные растворы окислителя КМnO4, обычно применяемые для процесса окисления толуола. Расход окислителя при этом близок к стехиометрии в расчете на каждый компонент второй фракции дистиллята (после отгонки бензола). Брутто-уравнение процесса включает собственно окисление каждого компонента (по своему уравнению), например, для этилбензола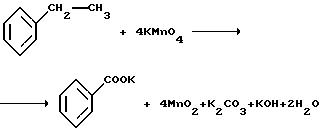
с последующей нейтрализацией раствора соляной кислотой
С6Н5СООК+НСl-->С6H5СООН+КСl
Следует иметь ввиду, что продукты разложения окислителя МnО2 и калевые соли могут использоваться по прямому назначению, последние, например, в качестве калийных удобрений.
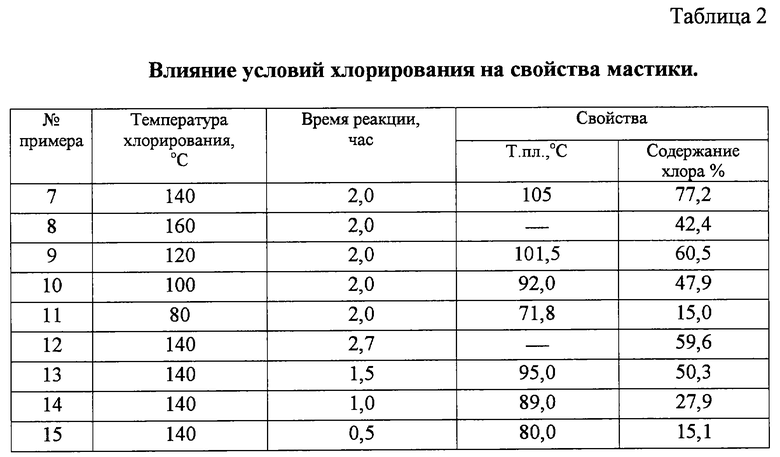
Третья фракция с т. кип. более 165oС - кубовый остаток - подвергается хлорированию молекулярным хлором при температуре 80-140oС в присутствии катализатора FeCl3 в течение 2,0±0,5 ч с получением мастики с содержанием хлора в ней 50-77%. Мастика представляет собой воскообразное вещество от темно-коричневого до черного цвета с т.пл. от 92 до 106oС в зависимости от глубины хлорирования. Мастика близка по показателям и промышленному назначению продукту - мастике "галовакс" (Galowax 1001,США) [Промышленные хлорорганические продукты. Спр. под ред. Л.А. Ошина. Изд. "Химия", М., 1978, с. 530-532] . Она может применяться для пропитки тканей, древесины для придания огнестойкости, в строительном деле, в производстве стройматериалов и резинотехнических изделий.
Физико-химические основы процесса хлорирования указанной фракции пироконденсата базируются на способности органических соединений вступать в реакции замещения под воздействием хлора в присутствии радикальных или ионных активаторов процесса. Так, путем хлорирования торфяного или буроугольного воска в растворе, при температуре 10-12oС в течение 2 ч получают хлорированный воск с содержанием хлора 3,6-6,92% по [Авт. св. СССР 1004451, С 10 G 73/00. Бюл. 10, опубл. 15.03.83]. Указанный выше "галовакс" - это продукт электрофильного ароматического замещения при действии хлора на нафталин в присутствии хлоридов металлов FеСl3 или АlСl3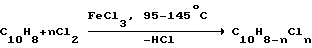 ,
,
где n=3-4.
Третья фракция с т.кип. более 165oС (высшие ароматические углеводороды в количестве 12-20% от пироконденсата) представляет собой смесь полиядерных и конденсированных соединений. На долю нафталина и его различных алкилпроизводных приходится около 50% состава. Реакционная способность таких соединений выше нафталина. Превращение идет с большим выделением тепла и не требует подогрева на начальной стадии. Для съема тепла необходимо кубовый остаток хлорировать в четыреххлористом углероде CCl4 с последующей регенерацией растворителя.
Образующийся на начальной стадии хлорирования и конечной (без растворителя) хлористый водород легко абсорбируется водой и в виде соляной кислоты используется для нейтрализации на стадии выделения бензойной кислоты при окислении второй фракции пироконденсата.
Следует иметь ввиду, что длительное воздействие хлором при температуре ≥140oС на указанные высшие ароматические углеводороды не способствует процессу замещения. Более конкурентоспособными являются процессы деструкции и элиминирования, резко падает содержание хлора в конечном продукте (за счет отщепления НСl) и резко уменьшается т.пл. (разрыв С-С связей).
Изобретение иллюстрируется следующими примерами.
Переработку пироконденсата проводят следующим образом. Навеска пироконденсата подвергается разгонке при атмосферном давлении на фракционной дестиляционной установке с дефлегматором на три фракции: первая фракция с т. кип. до 82-83oС с получением бензола; вторая с т.кип. от 84 до 165oС подвергается окислению (примеры 1-6); третья фракция - кубовый остаток - используется как исходное сырье для процесса хлорирования (примеры 7-15).
Пример 1. В трехгорвый реактор, снабженный обратным холодильником и мешалкой, загружают 10 г второй фракции пироконденсата, 740 мл воды и 38 г мелко растертого перманганата калия (соотношение масс фракции пироконденсата : КМnO4 равно 1:3,8). Кипятят смесь в течение 4 ч. После окончания реакции бесцветный раствор охлаждают, выпавшую двуокись марганца MnO2 отфильтровывают и дважды промывают горячей водой (по 10-15 мл). Фильтраты соединяют, упаривают и подкисляют концентрированной соляной кислотой до кислой реакции на конго. При этом осаждается бензойная кислота. Ее отфильтровывают, промывают ледяной водой и сушат.
Получено 8,31 г бензойной кислоты С6Н5СООН с т.пл 121-122oС (проба смешения температурной депрессии не имеет).
Выход 66,45% от теоретически возможного количества 12,50 г, которое вытекает из расчетной величины мольных долей компонентов смеси второй фракции пироконденсата (0,0582 толуол; 0,0246 этилбензол; 0,0167 стирол; 0,0028 фенилацетилен).
Примеры 2-6. Окисление второй фракции пироконденсата осуществляют аналогично примеру 1, отличающееся меньшим временем контакта реагентов (примеры 2, 4), меньшим количеством окислителя, т.е. меньшим соотношением (пример 6) и большим соотношением, но меньшим временем (пример 5). Следует иметь ввиду, что завершенность реакции по окислителю (обесцвечивание) наблюдается только в примере 6. В примере 5 завершенность реакции по MnO2 наступает при соотношении 1: 3,6, а в примере 3 - при соотношении 1:4,0. При окрашенных растворах реакционная смесь обесцвечивается добавкой небольших количеств этилового спирта. Результаты экспериментов сведены в таблицу 1. Они показывают, что лучшими условиями проведения окисления являются условия примера 1, что с учетом колебаний состава соответствует соотношению вторая фракция : КМnО4, равному 1:3,6-4,0.
Пример 7. В трехгорлый реактор, снабженный обратным холодильником с системой поглощения абгазов, мешалкой и барботером, загружают 50 г третьей фракции пироконденсата (кубовый остаток), 50 мл четыреххлористого углерода CCl4 и 0,5 г хлорного железа FeCl3. При интенсивном перемешивании подают хлор Cl2 из баллона с расходом 0,6-0,7 г/мин в течение 30 мин. По истечении указанного времени обратный холодильник меняют на нисходящий, при температуре 80oС отгоняют четыреххлористый углерод (48-50 мл, который используют в последующих примерах на начальной стадии хлорирования). После удаления CCl4 массу продолжают хлорировать в течение 2 ч при температуре 140oС. После окончания хлорирования реакционную массу продувают азотом для удаления остатков хлористого водорода (поглощается водой в склянке Дрекселя).
Получено 92,5 г (привес 85% от исходной массы) мастики с т.пл. 104-106oС с содержанием общего хлора 72%.
Мастика представляет собой воскообразное вещество черного цвета со слабым запахом хлорорганических продуктов. Не горит и не поддерживает горения, например древесина после пропитки (проверялась методом огневой трубы по ГОСТ 16363-81). Мастика растворима в ацетоне, четыреххлористом углероде, бензоле при слабом нагревании; почти нерастворима в бензине и гексане; нерастворима в воде.
Примеры 8-15. Хлорирование кубового остатка осуществляют аналогично примеру 7, отличающееся большей температурой (пример 8), большим временем контакта реагентов, наблюдается деструкция продукта с активным выделением хлористого водорода (пример 12), меньшей температурой (пример 11) и меньшим временем контакта (примеры 14, 15). Результаты эксперимента отражены в таблице 2. Они показывают, что мастика наиболее близка по своим свойствам к "галоваксу", исходя из температуры плавления и содержания общего хлора, полученная в условиях примеров 9, 10, 13, а также примера 7, что и определяет отличительные признаки изобретения по условиям хлорирования. Оптимальная температура 120±20oС в течение 1,5-2 ч до содержания хлора в мастике 50-77%, причем для съема тепла реакции первоначально хлорируют кубовый остаток в четыреххлористом углероде при 80oС в течение 0,5 ч с последующей регенерацией растворителя.
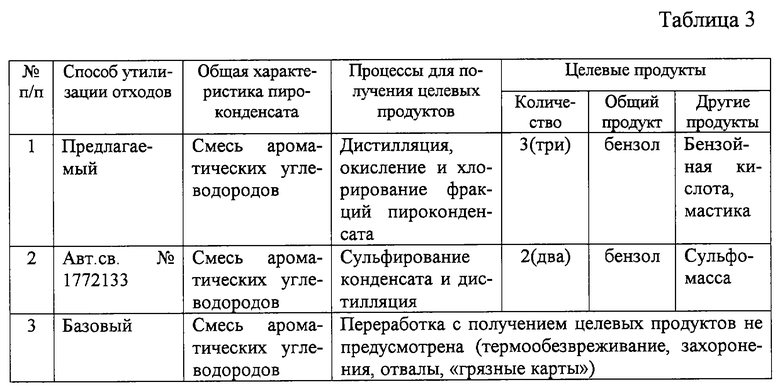
Сравнительные данные по переработке пироконденсата высокотемпературного гомогенного пиролиза предельных углеводородов, заявленного и известного способа, наиболее близкого по целям и задачам, приведены в таблице 3. При определенном различии в составе исходных смесей ароматических углеводородов в обоих случаях использован пироконденсат одного и того же производства, в качестве целевого продукта выделяют бензол с использованием процесса дистилляции. Однако порядок проведения, время и место процесса перегонки в системе мер по утилизации отходов различно. Разнообразны другие целевые продукты переработки и соответственно технические приемы и процессы для их получения. Изложенное отображено в ограничительной и отличительной части формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ ЖИДКИХ ПРОДУКТОВ ПИРОЛИЗА В АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ | 2004 |
|
RU2266944C1 |
| СПОСОБ ОЧИСТКИ БЕНЗОЛА ОТ НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ | 1999 |
|
RU2157360C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИХЛОРЭТАНА | 2004 |
|
RU2264374C1 |
| СПОСОБ АРОМАТИЗАЦИИ НЕАРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2010 |
|
RU2449978C1 |
| Способ переработки рафината каталитического риформинга | 2023 |
|
RU2809282C1 |
| Эмульгатор для буровых растворов | 1988 |
|
SU1578176A1 |
| СПОСОБ ОБРАБОТКИ И УТИЛИЗАЦИИ ПИРОЛИЗНОЙ СМОЛЫ | 2021 |
|
RU2757255C1 |
| СПОСОБ ОЧИСТКИ ОТХОДОВ ХЛОРОРГАНИЧЕСКИХ ПРОИЗВОДСТВ ОТ ПРОДУКТОВ ОСМОЛЕНИЯ | 2006 |
|
RU2313513C1 |
| СПОСОБ ОЧИСТКИ БЕНЗОЛА ОТ НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ И ТИОФЕНА | 1999 |
|
RU2164908C1 |
| РАСТВОРИТЕЛЬ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2000 |
|
RU2180679C2 |
Изобретение относится к комплексной переработке пироконденсата высокотемпературного гомогенного пиролиза предельных углеводородов состава С3-С5. Пироконденсат подвергают фракционированию с отбором первой фракции с т.кип. до 80-83oС, второй фракции с т.кип. от 84 до 164oС и кубового остатка с т. кип. свыше 165oС. Первая фракция является преимущественно бензолом с содержанием основного вещества около 90%, вторую фракцию окисляют перманганатом калия при соотношении по массе 1:3,6-4,0 при нагревании в течение 3-4 ч в водном растворе при температуре кипения реакционной массы с получением бензойной кислоты с выходом 63-68% от теории. Кубовый остаток подвергают хлорированию молекулярным хлором при температуре 80-140oС в присутствии катализатора FeCl3 в течение 1,5-2,0 ч с получением мастики с содержанием хлора 50-77%. Первоначально хлорирование ведут в четыреххлористом углероде 0,5 ч при 80oС, затем отгоняют его и продолжают хлорировать в течение 2 ч при 140oС. Технический результат - утилизация побочных продуктов высокотемпературного пиролиза с получением товарных продуктов. 2 з.п.ф-лы, 3 табл.
| Способ совместной переработки отработанной серной кислоты и пироконденсата, полученных в производстве этилена и ацетилена высокотемпературным пиролизом жидких нефтепродуктов | 1990 |
|
SU1772133A1 |
| Способ получения модифицированного воска | 1981 |
|
SU1004451A1 |
| СПОСОБ ГИДРООЧИСТКИ ПИРОКОНДЕНСАТА ОТ НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ | 1991 |
|
RU2024584C1 |
| Способ очистки меркаптансодержащей углеводородной фракции и катализатор для его осуществления | 1984 |
|
SU1382404A3 |
Авторы
Даты
2003-10-27—Публикация
2002-02-11—Подача