Настоящее изобретение относится к способу получения хинолинкарбальдегида. Более конкретно, оно относится к процессу легкого и эффективного получения 2-циклопропил-4(4-фторфенил)хинолин-3-карбальдегида, который полезен в качестве промежуточного продукта для синтеза ингибитора HMG-CoA peдуктазы как лекарственного средства для понижения холестерина.
Предпосылки изобретения
2-Циклопропил-4-(4-фторфенил)хинолин-3-карбальдегид является промежуточным продуктом синтеза ингибитора HMG-CoA редуктазы. До сих пор в качестве способа окисления 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина в 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегид использовался способ окисления с применением хромовой кислоты или способ, применяющий диметилсульфоксид-дегидратирующий агент (такой, как способ окисления Сверна (Swern)), или способ, использующий нитроксильный радикал - гипохлорит, представленный TEMPO (свободные радикалы 2,2,6,6-тетраметил-1-пиперидинилокси).
Раскрытие изобретения
Однако вышеупомянутые способы имеют проблемы обработки сточной жидкости вследствие образования опасных для окружающей среды ионов хрома или проблемы, связанные, например, с образованием плохо пахнущего диметилсульфида, а в случае нитроксильных радикалов реагент является дорогим, и существует также сложность с химической стабильностью, и такая реакция не может рассматриваться как преимущественная в промышленном отношении.
Соответственно, целью настоящего изобретения является обеспечение способа простого и промышленно благоприятного получения 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида окислением 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина.
Авторы настоящего изобретения изучили различные способы окисления для решения таких проблем и в результате обнаружили способ получения, который свободен от вышеупомянутых проблем, связанных с обработкой сточных жидкостей или плохим запахом, и который обеспечивает хороший выход и благоприятен в промышленном отношении, что привело к настоящему изобретению.
А именно, настоящее изобретение представляет способ получения 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида формулы (III)
характеризующийся окислением 2-циклопропил-4(4-фторфенил)-3-гидроксиметилхинолина формулы (I)
солью гипогалогеновой кислоты в присутствии соли четвертичного аммония формулы (II)
в которой каждый из R1, R2, R3 и R4, которые являются одинаковыми или различными, представляет C1-16 алкильную группу или бензильную группу (бензильная группа может быть замещена C1-4 алкильной группой, C1-4 алкоксигруппой или атомом галогена), и Х- является ионом галогена, ионом сульфата или ионом метансульфоната.
Согласно настоящему изобретению 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегид, который является полезным промежуточным продуктом для синтеза ингибитора HMG-CoA редуктазы, может быть получен с хорошим выходом и выгодно в промышленном отношении.
Наилучший способ осуществления изобретения
Теперь настоящее изобретение будет описано более подробно.
Во-первых, поясняются обозначения для соответствующих заместителей R1, R2, R3, R4 и Х-.
В данном описании "н" обозначает нормальный, "и" - изо, "втор" - вторичный, "трет" - третичный, "ц" - цикло и "о" - орто.
C1-4 алкильная группа включает прямые, разветвленные и циклические алкильные группы и может быть, например, метилом, этилом, н-пропилом, изо-пропилом, ц-пропилом, н-бутилом, изо-бутилом, втор-бутилом, трет-бутилом, ц-бутилом, 1-метил-ц-пропилом и 2-метил-ц-пропилом, предпочтительно метилом и этилом.
C1-16 алкильная группа включает прямые, разветвленные и циклические алкильные группы и может, например, представлять метил, этил, н-пропил, и-пропил, ц-пропил, н-бутил, и-бутил, втор-бутил, трет-бутил, ц-бутил, 1-метил-ц-пропил, 2-метил-ц-пропил, н-пентил, 1-метил-н-бутил, 2-метил-н-бутил, 3-метил-н-бутил, 1,1-диметил-н-пропил, 1,2-диметил-н-пропил, 2,2-диметил-н-пропил, 1-этил-н-пропил, ц-пентил, 1-метил-ц-бутил, 2-метил-ц-бутил, 3-метил-ц-бутил, 1,2-диметил-ц-пропил, 2,3-диметил-ц-пропил, 1-этил-ц-пропил, 2-этил-ц-пропил, н-гексил, 1-метил-н-пентил, 2-метил-н-пентил, 3-метил-н-пентил, 4-метил-н-пентил, 1,1-диметил-н-бутил, 1,2-диметил-н-бутил, 1,3-диметил-н-бутил, 2,2-диметил-н-бутил, 2,3-диметил-н-бутил, 3,3-диметил-н-бутил, 1-этил-н-бутил, 2-этил-н-бутил, 1,1,2-триметил-н-пропил, 1,2,2-триметил-н-пропил, 1-этил-1-метил-н-пропил, 1-этил-2-метил-н-пропил, 2-этил-2-метил-н-пропил, ц-гексил, 1-метил-ц-пентил, 2-метил-ц-пентил, 3-метил-ц-пентил, 1-этил-ц-бутил, 2-этил-ц-бутил, 3-этил-ц-бутил, 1,2-диметил-ц-бутил, 1,3-диметил-ц-бутил, 2,2-диметил-ц-бутил, 2,3-диметил-ц-бутил, 2,4-диметил-ц-бутил, 3,3-диметил-ц-бутил, 1-н-пропил-ц-пропил, 2-н-пропил-ц-пропил, 1-и-пропил-ц-пропил, 2-и-пропил-ц-пропил, 1,2,2-триметил-ц-пропил, 1,2,3-триметил-ц-пропил, 2,2,3-триметил-ц-пропил, 1-этил-2-метил-ц-пропил, 2-этил-1-метил-ц-пропил, 2-этил-2-метил-ц-пропил, 2-этил-3-метил-ц-пропил, н-гептил, н-октил, н-нонил, н-децил, н-андецил, н-додецил, н-тридецил, н-тетрадецил, н-пентадецил и н-гексадецил.
C1-4 алкоксигруппа включает прямые, разветвленные и циклические алкоксигруппы и может, например, представлять метокси, этокси, н-пропокси, и-пропокси, ц-пропокси, н-бутокси, и-бутокси, втор-бутокси, трет-бутокси, ц-бутокси, 1-метил-ц-пропокси и 2-метил-ц-пропокси, предпочтительно метокси и этокси.
Атом галогена может быть, например, атомом фтора, атомом хлора, атомом брома и атомом йода, предпочтительно атомом хлора и атомом брома.
Ион галогена может быть, например, ионом фтора, ионом хлора, ионом брома и ионом йода, предпочтительно ионом хлора и ионом брома.
Соль гипогалогеновой кислоты может конкретно представлять собой гипохлорит натрия, гипохлорит кальция, гипохлорит калия и гипобромит натрия, предпочтительно гипохлорит натрия, гипохлорит кальция и гипохлорит калия.
Предпочтительными R1, R2, R3 и R4 могут быть метил, этил, н-пропил, изо-пропил, н-бутил, н-октил, н-додецил и бензил.
Предпочтительным X- может быть ион хлора и ион брома.
Следующий способ может быть отмечен, как предпочтительный способ настоящего изобретения.
(1) Способ получения 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида формулы [III] , характеризующийся окислением 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина формулы [I], гипохлоритом натрия, гипохлоритом кальция или гипохлоритом калия в присутствии соли четвертичного аммония формулы [II].
Далее будет пояснен конкретный способ получения 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида.
Соль четвертичного аммония добавляют к раствору, включающему 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолин и растворитель для реакции с последующим перемешиванием и к нему добавляют соль гипогалогеновой кислоты с последующим перемешиванием, получая таким образом желаемый 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегид.
Растворитель для реакции не имеет особых ограничений, если он не оказывает влияния на реакцию. Например, могут быть упомянуты нитрилы, такие как ацетонитрил, пропионитрил и бутилонитрил, кетоны, такие как ацетон, метилэтилкетон и мети-лизобутилкетон, ароматические углеводороды, такие как бензол, толуол, ксилол, мезитилен (1,3,5-триметилбензол), хлорбензол и о-дихлорбензол, алифатические углеводороды, такие как н-гексан, циклогексан, н-октан и н-декан, сложные эфиры, такие как метилацетат, этилацетат и пропилацетат, галогенированные углеводороды, такие как дихлорметан, дихлорэтан и хлороформ, простые эфиры, такие как тетрагидрофуран, диэтиловый эфир, трет-бутилметиловый эфир и диметоксиэтан, амиды, такие как N,N-диметилформамид, N, N-диметилацетамид и N-метилпирролидон, мочевины, такие как 1,3-диметилимидазолидинон и тетраметилмо-чевина, предпочтительно сложные эфиры, такие как метилацетат, этилацетат и пропилацетат, галогенированные углеводороды, такие как дихлорметан, дихлорэтан и хлороформ, ароматические углеводороды, такие как толуол и ксилол, и кетоны, такие как ацетон, метилэтилкетон и метилизобутилкетон.
Кроме того, данные растворители для реакции могут использоваться по одному или в сочетании друг с другом.
Количество используемого в реакции растворителя находится в пределах от 1 до 200 частей (вес/вес), предпочтительно в пределах от 2 до 50 частей (вес/вес), от субстрата (2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина).
Соли четвертичного аммония не обязательно могут использоваться по одной, можно использовать сочетание из двух и более из них. Количество соли четвертичного аммония составляет от 0,005 до 5 эквивалентов, предпочтительно от 0,05 эквивалента до 0,5 эквивалента, в расчете на субстрат.
Количество соли гипогалогеновой кислоты составляет от 1,05 до 5 эквивалентов, предпочтительно от 1,1 до 2 эквивалентов, в расчете на субстрат.
Температура реакции составляет в пределах от -20 до 100oС, предпочтительно от 10 до 70oС.
Время реакции меняется в зависимости от используемого растворителя, типа и количества соли четвертичного аммония, температуры реакции и т.д. с точки зрения промышленного процесса, она составляет предпочтительно в пределах 8 часов.
После завершения реакции добавляют воду с последующей экстракцией растворителем для экстракции, таким как этилацетат, дихлорметан или толуол, сушкой и концентрированием при пониженном давлении с получением желаемого 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида.
При необходимости осуществляют перекристаллизацию из растворителя для перекристаллизации, такого как смешанный растворитель метанол/вода или смешанный растворитель толуол/н-гексан, или кристаллы, полученные отгонкой растворителя для экстракции, промываются, например, и-пропиловым эфиром или ц-гексаном, с помощью чего может выделяться 2-циклопропил-4-(4-фторфенил)-хинолин-3-карбальдегид высокой чистоты.
Теперь настоящее изобретение будет описано подробно со ссылкой на примеры, но настоящее изобретение никоим образом не ограничивается такими конкретными примерами.
ВЭЖХ анализ 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида проводили в следующих условиях.
Колонка: Nucleosil 100 5С-18.
Элюент: ацетонитрил/вода (3:2, объем/объем).
Температура 40oС.
Скорость потока 1 мл/мин.
Время удерживания: 30,4 минуты.
ПРИМЕР 1. Окисление спирта в альдегид гипохлоритом натрия в присутствии бромида тетра-н-бутиламмония.
0,15 г (0,47 ммоль) бромида тетра-н-бутиламмония добавляют к смешанному раствору 0,8 г (2,73 ммоль) 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина в этилацетате (7,5 мл) и воде (3,5 мл) с последующим перемешиванием при 15oС.
Затем туда же добавляют 4,2 г (5,41 ммоль) гипохлорита натрия (9,6%) с последующим перемешиванием в течение одного часа и затем добавляют 20 мл воды с последующей экстракцией 20 мл этилацетата.
Водный слой экстрагируют еще раз 20 мл этилацетата.
Органические слои объединяют и промывают 20 мл воды, затем сушат над сульфатом магния и растворитель отгоняют при пониженном давлении.
Остаток растворяют в 32 мл метанола и туда по каплям добавляют 10 мл воды с последующим охлаждением до 0oС.
Полученные кристаллы собирают фильтрованием, получая 0,62 г (выход 78%) 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида в виде слегка желтых кристаллов.
Чистота (ВЭЖХ) 99,6%, точка плавления 152oС.
ПРИМЕР 2.
0,15 г (0,47 ммоль) бромида тетра-н-бутиламмония добавляют к смешанному раствору 2,4 г (8,19 ммоль) 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина в этилацетате (22,5 мл) и воде (10,5 мл) с последующим перемешиванием при 15oС.
Затем туда же добавляют 12,6 г (16,23 ммоль) гипохлорита натрия (9,6%) с последующим перемешиванием в течение 3 часов и затем добавляют 60 мл воды с последующей экстракцией 60 мл этилацетата.
Водный слой экстрагируют еще раз 60 мл этилацетата.
Органические слои объединяют, промывают 60 мл воды, затем сушат над безводным сульфатом магния и растворитель отгоняют при пониженном давлении.
Остаток растворяют в 110 мл метанола и по каплям добавляют 35 мл воды с последующим охлаждением до 0oС.
Полученные кристаллы собирают фильтрованием, получая 2,03 г (выход 85%) 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида в виде слегка желтых кристаллов.
Чистота (ВЭЖХ) 99,8%, точка плавления 152oС.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОПТИЧЕСКИ-АКТИВНЫЙ β-АМИНОАЛКОКСИБОРАНОВЫЙ КОМПЛЕКС, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ОПТИЧЕСКИ АКТИВНОЕ β-АМИНОСПИРТОВОЕ ПРОИЗВОДНОЕ ДЛЯ ЕГО ПОЛУЧЕНИЯ И СПОСОБЫ ПОЛУЧЕНИЯ ОПТИЧЕСКИ АКТИВНЫХ СПИРТОВ С УЧАСТИЕМ КОМПЛЕКСА | 1994 |
|
RU2126412C1 |
| ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ БЕНЗОПИРАНА В КАЧЕСТВЕ ПРОТИВОАРИТМИЧЕСКИХ АГЕНТОВ | 2005 |
|
RU2380370C2 |
| ИНГИБИТОР АТЕРОСКЛЕРОТИЧЕСКОГО УТОЛЩЕНИЯ ВНУТРЕННЕЙ ОБОЛОЧКИ СОСУДОВ | 1992 |
|
RU2114620C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХИНОЛИЛАКРИЛОНИТРИЛА И СООТВЕТСТВУЮЩИХ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ | 2001 |
|
RU2260000C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-((2-ЦИКЛОПРОПИЛ-4-(4-ФТОРФЕНИЛ)-3-ХИНОЛИЛ)ПРОП-2-ЕНАЛЯ И ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ | 1999 |
|
RU2214402C2 |
| ПРОИЗВОДНОЕ БЕНЗИМИДАЗОЛА И СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ ПРОТИВ ВЕЩЕСТВА Р И АНТИГИСТАМИНОВОЙ АКТИВНОСТЬЮ | 1998 |
|
RU2188822C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ БЕНЗОПИРАНА ПРОТИВ АРИТМИИ | 2002 |
|
RU2291867C2 |
| БЕНЗОПИРАНОВОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2366658C2 |
| СПОСОБ ПОЛУЧЕНИЯ 7-ХИНОЛИНИЛ-3,5-ДИГИДРОКСИГЕПТ-6-ЕНОАТА | 2002 |
|
RU2260001C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕВАЛОНОЛАКТОНОВЫХ ПРОИЗВОДНЫХ | 1989 |
|
RU2045529C1 |
Изобретение относится к способу получения 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида формулы (I), который заключается в окислении 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина солью гипогалогеновой кислоты в присутствии соли четвертичного аммония. 2-Циклопропил-4-(4-фторфенил)-хинолин-3-карбальдегид может быть использован в качестве промежуточного продукта в синтезе ингибитора HMG-СоА редуктазы, используемого в качестве лекарственного средства для понижения холестерина. Технический результат: разработан простой, промышленно благоприятный способ получения 2-циклопропил-4-(4-фторфенил)хинолин-3-карбальдегида с высоким выходом. 1 з.п. ф-лы.
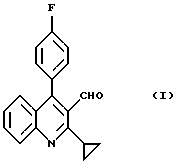

включающий окисление 2-циклопропил-4-(4-фторфенил)-3-гидроксиметилхинолина формулы (I)

солью гипогалогеновой кислоты, отличающийся тем, что процесс ведут в присутствии соли четвертичного аммония формулы (II)
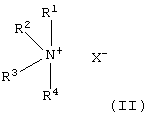
в которой каждый из R1, R2, R3 и R4, которые являются одинаковыми или различными, представляет С1-16алкильную группу;
Х- является ионом галогена, ионом сульфата или ионом метансульфоната.
| JP 08027114 А2, 30.01.1996 | |||
| ИНГИБИТОР АТЕРОСКЛЕРОТИЧЕСКОГО УТОЛЩЕНИЯ ВНУТРЕННЕЙ ОБОЛОЧКИ СОСУДОВ | 1992 |
|
RU2114620C1 |
| DE 3905908 A1, 06.09.1990 | |||
| Система единого времени для управления вторичными часами | 1974 |
|
SU535548A1 |
| US 5102888 A, 07.04.1992. | |||
Авторы
Даты
2003-11-27—Публикация
1999-11-29—Подача