Изобретение относится к медицине, а именно к медицинской микробиологии, и может быть использовано для серологической диагностики хламидийных инфекций человека и животных.
Известен способ получения инфекционных антигенов хламидий из овокультур путем многократного дифференциального центрифугирования гомогенизированной суспензии желточных мешков на солевом растворе с последующей инактивацией возбудителя формалином в конечной концентрации 0,25% (J Clinical micrcob., 1980, 12, 3, 409-412).
Однако известный способ не обеспечивает достаточного качества полученных антигенов. Обработка возбудителя высокой концентрацией формалина существенно снижает специфическую активность поверхностных антигенов хламидий. Как следствие, снижается эффективность их специфического свечения при взаимодействии с гомологичными антителами, уменьшается чувствительность реакции. Жидкие антигены хламидий имеют ограниченный срок годности (9-12 мес).
Наиболее близким аналогом к предлагаемому способу является получение неинфекционных антигенов хламидий из овокультур возбудителя путем центрифугирования при 500 g в течение 10 мин гомогенизированной 20% суспензии желточных мешков на среде 199, после предварительной инактивации 0,05% формалином и 0,1% азида натрия в конечной концентрации в течение 72 часов при температуре от 4 до 6oС с последующей лиофилизацией (Авторское свидетельство SU 1711898, кл. А 61 К 39/02, 39/118, G 01 N 33/531, 1992 г.).
Недостатком данного способа является то, что он не обеспечивает достаточной дисперсности среды, в которой взвешены корпускулы хламидий, и полного освобождения от липидов, что снижает растворимость препарата после лиофильного высушивания и его адгезивные свойства на стекле при приготовлении слайдов для проведения реакции и соответственно специфическую активность.
Техническим результатом изобретения является повышение специфической активности, растворимости и адгезивности на стекле антигенов хламидий.
Сущность изобретения заключается в следующем: 20%-ную инактивированную суспензию, приготовленную из гомогенизированных инфицированных желточных мешков на среде 199 подвергают дифференциальному центрифугированию при 150 g и 500 g в течение 10 мин при температуре (3±1)oС, средний слой (целевой продукт) фильтруют через мембрану с размерами пор 3 мкм под давлением (0,3±0,1) МПа при температуре (13±3)oС, концентрируют, фильтрат стандартизуют, доводя средой 199 до содержания 100 корпускул в поле зрения препарата.
Причинно-следственная связь между существенными признаками и техническим результатом заключается в следующем.
Дифференциальное центрифугирование, проводимое после инактивации суспензии инфицированных желточных мешков куриных эмбрионов, при 150 g и 500 g в течение 10 мин при температуре (3±1)oС повышает степень адгезивности и гомогенности за счет удаления крупнодисперсного дебриса. Мембранное разделение на мембранах с размерами пор 3 мкм при температуре (13±3)oС под давлением (0,3±0,1) МПа повышает растворимость целевого продукта за счет удаления нерастворимых клеточных компонентов и липидов. Фильтрация на мембране с размерами пор 0,2 мкм под давлением (0,3±0,1) МПа при температуре (13±3)oС позволяет провести концентрацию антигенов, что повышает специфическую активность целевого продукта за счет стандартизации до концентрации 100 корпускул в поле зрения.
Все это приводит к повышению специфической активности, растворимости, гомогенности и адгезивных свойств антигенов хламидий.
Изобретение осуществляется следующим образом.
Пример 1. Куриные эмбрионы, инфицированные Chlamydia psittaci (штамм Лори), погибшие на 4-7 сутки после заражения, вскрывают в стерильных условиях. Желточные мешки гомогенизируют, затем на среде 199 готовят 20%-ную маточную суспензию. В суспензию добавляют азид натрия 0,1% и формалин 0,05% и выдерживают в течение 72 часов при температуре от 2 до 8oС. После этого суспензию подвергают дифференциальному центрифугированию при 150 g в течение 10 мин при температуре (3±1)oС. Средний слой вновь центрифугируют при 500 g в течение 10 мин при температуре (3±1)oС. Полученный средний слой подвергают мембранной фильтрации с величиной пор 3 мкм под давлением (0,3±0,1) МПа при температуре (13±3)oС с последующей концентрацией целевого продукта на мембране с порами 0,2 мкм под давлением (0,3±0,1) МПа при температуре (13±3)oС, фильтрат - целевой продукт - стандартизуют методом прямого подсчета и доводят средой 199 до содержания 100 хламидийных корпускул в поле зрения препарата. В пермеате остаются крупнодисперсный дебрис и липиды, являющиеся отходом.
Полученный таким образом хламидийный антиген смешивают со стабилизатором состава, мас. %: среда 199 - 99; сахароза - 1, разливают по ампулам по 0,2 мл, ампулы помещают в металлические кассеты и лиофилизируют на сублимационных установках. Рабочий вакуум в течение цикла не более 13,33 Па. Температура конденсатора в начале высушивания не выше минус 50oС, в течение цикла не выше минус 47oС. Начальная температура материала в период сублимации минус (45±10)oС. Конечная температура досушивания (20±2)oС. По окончании высушивания кассеты с препаратом немедленно закрывают крышками, помещают в эксикатор с сухим силикагелем и герметизируют запайкой.
Пример 2. Получение неинфекционных антигенов из Chlamydia pecorum возбудителя энзоотического аборта овец (штамм ЕАЕ). Способ осуществляется так, как указано в примере 1, но в качестве исходного материала используют желточные мешки куриных эмбрионов, инфицированных штаммом ЕАЕ.
Пример 3. Получение неинфекционных антигенов из Chlamydia trachomatis, возбудителя уретрита (штамм ЛБ-1). Способ осуществляется так, как указано в примере 1, но в качестве исходного материала используют желточные мешки куриных эмбрионов, инфицированных штаммом ЛБ-1.
Пример 4. Получение неинфекционных антигенов из Chlamydia trachomatis возбудителя венерической лимфогранулемы (штамм Л-2). Способ осуществляется так, как указано в примере 1, но в качестве исходного материала используют желточные мешки куриных эмбрионов, зараженных штаммом Л-2.
Пример 5. Получение неинфекционных антигенов из Chlamydia pneunoniae возбудителя респираторной патологии человека (штамм TW-183). Способ осуществляется так, как указано в примере 1, но в качестве исходного материала используют желточные мешки куриных эмбрионов, зараженных штаммом TW-183.
Дополнительная очистка полуфабрикатов антигенов хламидий с помощью мембранной фильтрации в фильтрационных ячейках под давлением, отделяющая антиген от крупнодисперсного дебриса и липидов, с последующей концентрацией позволила не только усилить флуоресценцию корпускул хламидий в темном поле препарата, повысить растворимость, гомогенность и адгезивность на стекле антигенов хламидий, но и оптимизировать условия стандартизации хламидийных корпускул. Стандартизацию проводили методом прямого подсчета в РНИФ до концентрации 100 корпускул в поле зрения, при интенсивности флуоресценции не менее чем +++.
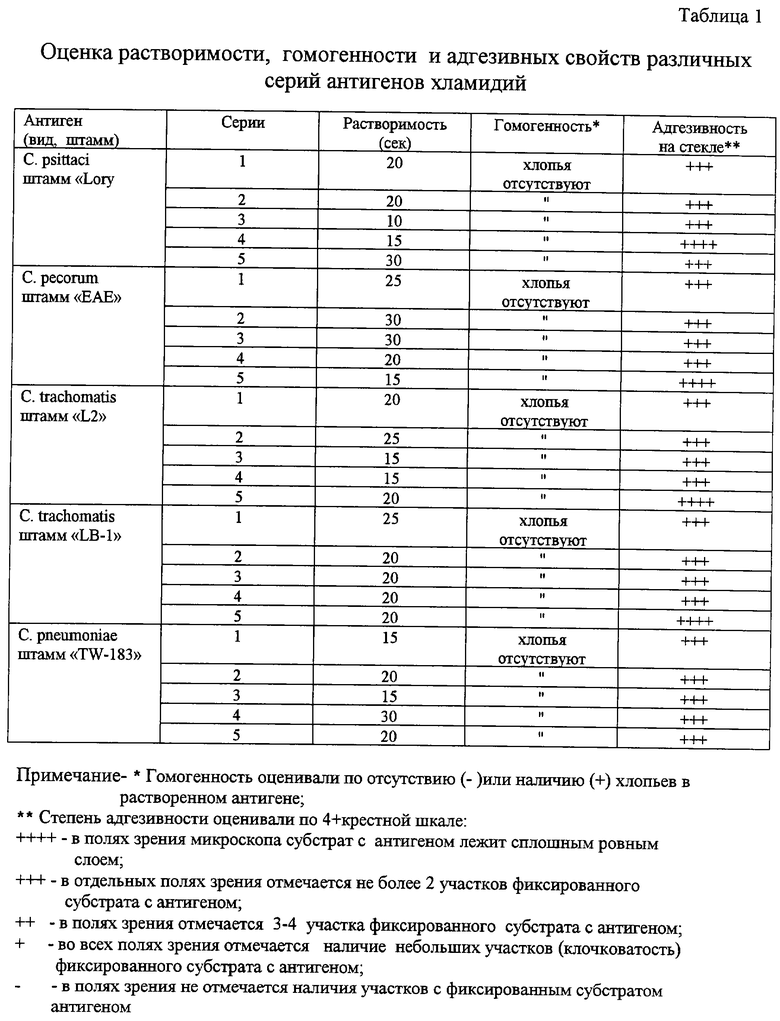
Оценка растворимости, гомогенности и адгезивности различных серий антигенов хламидий представлена в табл 1.
Как видно из материалов, представленных в табл. 1, все серии антигенов обладают хорошей растворимостью в течение 10-30 с, гомогенностью, т.е. при растворении не образуют хлопьев, и высокой степенью адгезивности на стекле (+++, ++++).
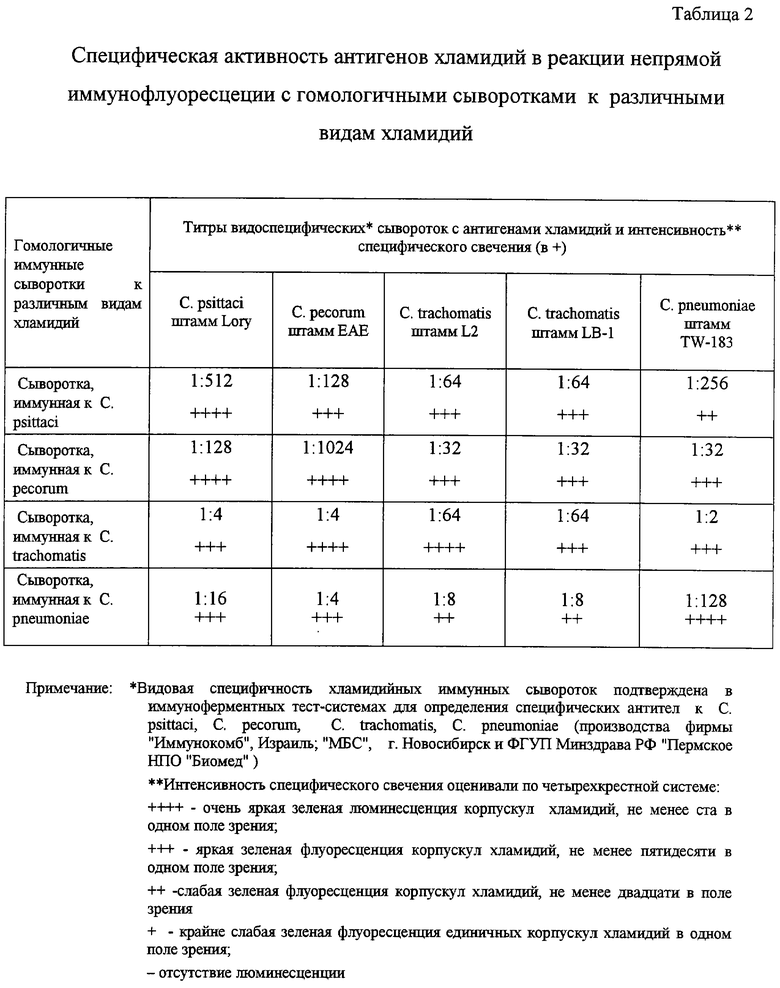
Специфическую активность полученных антигенов хламидий, очищенных с помощью мембранной фильтрации и стандартизованных методом прямого подсчета в реакции непрямой иммунофлуоресценции (РНИФ) определяли путем титрования гомологичных иммунных сывороток в реакции непрямой иммунофлуоресценции (см. табл.2).
Как видно из данных табл. 2, все серии антигенов хламидий обладают выраженной видоспецифической активностью с высокой интенсивностью специфического свечения.
Таким образом, использование предлагаемого способа позволяет повысить специфическую активность хламидийных антигенов, их растворимость и гомогенность, адгезивность на стекле, что способствует стандартизации условий проведения реакции и объективизации получаемых результатов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения хламидиозного антигена для реакции непрямой иммунофлюоресценции | 1989 |
|
SU1711898A1 |
| НАБОР ДЛЯ ВЫЯВЛЕНИЯ ХЛАМИДИЙНОЙ ИНФЕКЦИИ | 1992 |
|
RU2042360C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ ХЛАМИДИЙНЫХ ИНФЕКЦИЙ У ЧЕЛОВЕКА | 2002 |
|
RU2242993C2 |
| ВАКЦИНА ДЛЯ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ХЛАМИДИОЗА КРУПНОГО РОГАТОГО СКОТА | 1991 |
|
RU2092188C1 |
| ВАКЦИНА КУЛЬТУРАЛЬНАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ ХЛАМИДИОЗА (ОРНИТОЗА) ПТИЦ | 2005 |
|
RU2279892C1 |
| ВАКЦИНА ДЛЯ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ХЛАМИДИОЗА СВИНЕЙ | 2002 |
|
RU2247577C2 |
| ВАКЦИНА КУЛЬТУРАЛЬНАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ ХЛАМИДИОЗА СВИНЕЙ | 2002 |
|
RU2233670C2 |
| ВАКЦИНА ДЛЯ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ХЛАМИДИОЗА КРУПНОГО И МЕЛКОГО РОГАТОГО СКОТА | 2005 |
|
RU2301682C1 |
| Штамм хламидий СнLамYDIа рSIттасI, используемый для изготовления биопрепаратов для диагностики и профилактики хламидиоза серебристо-черных лисиц | 1989 |
|
SU1667870A1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ MUS. MUSCULUS L., ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К CHLAMYDIA | 1998 |
|
RU2158760C2 |
Изобретение относится к медицине, а именно к медицинской микробиологии, и может быть использовано для серологической диагностики хламидийных инфекций человека и животных. Сущностью изобретения является дифференциальное центрифугирование инактивированной суспензии из гомогенизированных желточных мешков, инфицированных хламидиями, при 150 g и 500 g в течение 10 мин при температуре (3±1)oС, фильтрация среднего слоя через мембрану с размерами пор 3 мкм под давлением (0,3±0,1) МПа при температуре (13±3)oС, концентрации и стандартизации фильтрата. Техническим результатом является повышение специфической активности, растворимости, гомогенности и адгезивности антигенов хламидий. 2 табл.
Способ получения хламидийного антигена для реакции непрямой иммунофлуоресценции, включающий культивирование хламидий в куриных эмбрионах, гомогенизацию инфицированных желточных мешков, суспендирование корпускул в среде 199 с последующей инактивацией формалином в смеси с азидом натрия в конечной концентрации 0,05% и 0,1% на объем суспензии соответственно, отделением целевого продукта центрифугированием, смешиванием со стабилизатором состава, мас.%: среда 199 - 98-99,5; сахароза 0,5-2, и лиофилизацией, отличающийся тем, что после инактивации проводят дифференциальное центрифугирование при 150 g и 500 g в течение 10 мин при температуре (3±1)°С, средний слой (целевой продукт) фильтруют через мембрану с размерами пор 3 мкм под давлением (0,3±0,1) МПа при температуре (13±3)°С, концентрируют, фильтрат стандартизуют, доводя средой 199 до содержания 100 корпускул в поле зрения препарата.
| Способ получения хламидиозного антигена для реакции непрямой иммунофлюоресценции | 1989 |
|
SU1711898A1 |
| НАБОР ДЛЯ ВЫЯВЛЕНИЯ ХЛАМИДИЙНОЙ ИНФЕКЦИИ | 1992 |
|
RU2042360C1 |
| HANNAL et al | |||
| Chlamidial antigens stabilized with formalin for use in the mucroimmunofluorescence test | |||
| Journal of Clinical Microbiology | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Способ модулирования для радиотелефонии | 1923 |
|
SU409A1 |
Авторы
Даты
2004-02-10—Публикация
2002-07-12—Подача