Изобретение относится к медицине, а именно к способу приготовления вакцины для профилактики хламидиозов у человека.
Известен способ приготовления живой вакцины против хламидиоза (пситтакоза) человека из живой культуры возбудителя пситтакоза (Терских И.И. Орнитоз и другие хламидийные инфекции, М., 1979, с.106-114).
Однако при широком использовании живых вакцин было установлено, что они обладают низкой протективной активностью, имеют ограниченный срок хранения, требующий использования их практически ex temporo после приготовления из-за выраженного снижения активности в 2 и более раз уже в течение первых 7 суток хранения.
Наиболее близким техническим решением к заявляемому является способ приготовления аэрозольной инактивированной тканевой вакцины против хламидиоза человека, включающий репродукцию хламидий орнитоза штамма "В" в первичной культуре клеток куриных фибробластов в течение 72 часов на среде 199 без сыворотки, для приготовления вакцины использовали жидкую фракцию культуры клеток, инфицированных хламидиями, которую предварительно инактивировали при температуре 37°С течение 10 дней в присутствии мертиолята (Терских И.И., Беклешова А.Ю. Вопросы вирусологии, М., 1965, №1, с.99-100., Терских И.И., Ильинский Ю.А., Болотовский В.М. и др. Вопросы вирусологии, М., 1974, №2, с.149-151).
Однако предложеный способ позволял получить вакцину, которая стимулировала гуморальный иммунитет, но устойчивость к заражению хламидиями ограничивалась формированием только местного иммунитета. Кроме этого, предложенный аэрозольный способ иммунизации создавал определенные трудности для применения вакцины по причинам необходимости обеспечения специальным оборудованием и приспособлением для распыления вакцины, а также сложностью дозирования вакцины для каждого вакцинируемого.
Технический результат предлагаемого способа заключается в получении хламидийной вакцины расширенного спектра действия, повышении ее протективной активности при подкожном или внутримышечном способе введения.
Сущность изобретения заключается в следующем. Вакцину готовят из цельноклеточных антигенов хламидий двух видов - хламидий трахоматис (штамм “Л-2”) и хламидий пситтаци (штамм “Лори”), которые культивируют в желточных мешках развивающихся куриных эмбрионов, готовят взвесь инфицированных желточных мешков на стерильном апирогенном 0,9%-ном растворе натрия хлорида, затем инактивируют нейтральным формалином в конечной концентрации 0,4% при температуре от 2 до 8°С в течение 5 суток, очищают дифференциальным центрифугированием и эфирной обработкой, уравновешивают по специфической активности не менее 128 АЕ (антигенных единиц) в мл и сорбируют на геле гидрооксида алюминия, с последующим добавлением консерванта, в качестве консерванта используют мертиолят в конечной концентрации 0,005-0,01%.
Использование для приготовления вакцины двух штаммов хламидий (штамм "Л-2" хламидий трахоматис и штамм "Лори" хламидий пситтаци) расширяет спектр ее действия, предохраняя человека как от антропонозных, так и от зоонозных хламидийных инфекций.
Репродуцирование хламидий в желточных мешках развивающихся куриных эмбрионов является наиболее экономичным способом культивирования.
Проведение инактивации взвеси хламидий на стерильном апирогенном 0,9%-ном растворе натрия хлорида нейтральным формалином в конечной концентрации 0,4% при температуре от 2 до 8°С в течение 5 суток сохраняет антигенную специфическую активность хламидийных корпускул за счет мягких условий инактивации.
Обработка полуфабрикатов дифференциальным центрифугированием и эфиром повышает степень очистки от ткани субстрата культивирования и процент выхода целевого продукта.
Оценку специфической активности антигенов хламидий обоих штаммов проводят в реакции нейтрализации антител (РНАт) и уравновешивают до 128 АЕ (антигенных единиц) в мл, что значительно упрощает технологию приготовления вакцины.
В качестве адъюванта используют гель гидрооксида алюминия, что способствует выработке напряженного иммунитета при отсутствии и местных реакций при подкожном или внутримышечном способе введения.
Мертиолят используют в качестве консерванта в концентрации 0,005-0,01%, что исключает его токсическое действие на организм человека и гарантирует при этом стабильность исходных свойств вакцины в течение не менее 1 года.
В результате предложенный способ расширяет спектр действия вакцины и повышает ее протективную активность при подкожном или внутримышечном способе введения.
Изобретение осуществляется следующим образом
Пример 1. Производственные штаммы хламидий трахоматис штамм Л-2 и хламидий пситтаци штамм Лори культивировали в 7-ми суточных развивающихся куриных эмбрионах. Инкубирование зараженных куриных эмбрионов проводили при температуре 38±1°С и относительной влажности воздуха от 60 до 65%. Максимум специфической гибели инфицированных куриных эмбрионов наступал на 4-5 сутки после заражения. Погибшие куриные эмбрионы вскрывали и извлекали желточные мешки. Инфицированные желточные мешки каждого штамма гомогенизировали отдельно, из гомогенатов готовили 50% взвеси на стерильном апирогенном 0,9% растворе натрия хлорида, содержащие нейтральный формалин в конечной концентрации 0,4%. Полученные полуфабрикаты тщательно перемешивали и ставили в холодильник при температуре от 2 до 8°С на 5 суток до полной инактивации хламидий, после чего полуфабрикаты подвергали центрифугированию при 800 g в течение 2 часов. Осадки ресуспендировали в стерильном апирогенном 0,9%-ном растворе натрия хлорида, содержащем 0,4% нейтрального формалина. К полученным взвесям хламидий трахоматис и пситтаци добавляли эфир наркозный при соотношении объемов 1:1,5. Смеси выдерживали при температуре от 2 до 8°С в течение 18-20 часов, использовали водную фазу, которую подвергали центрифугированию при 1500 g в течение часа. Осадки цельноклеточных антигенов хламидий ресуспендировали в стерильном апирогенном 0,9%-ном растворе натрия хлорида. Специфическую активность полученных антигенов хламидий трахоматис и пситтаци оценивали в РНАт. При специфической активности не менее 128 АЕ (антигенных единиц/мл) проводили сорбцию антигенов в соотношении объемов 1:1 на геле гидрооксида алюминия в течение 2-х часов при температуре от 2 до 8°С. Полноту сорбции определяли в динамике путем титрования надосадочной жидкости в РНАт до 100%-ной сорбции антигена. К сорбированному на геле гидрооксида алюминия антигену добавляли 1%-ный раствор мертиолята в количестве, равном 0,005-0,01 объема полуфабриката, затем стерильным апирогенным 0,9%-ным раствором натрия хлорида доводили до исходного объема полуфабриката сорбированного антигена. Содержимое емкости встряхивали в течение 10±2 мин на шуттель-аппарате, разливали в стерильные ампулы и герметизировали.
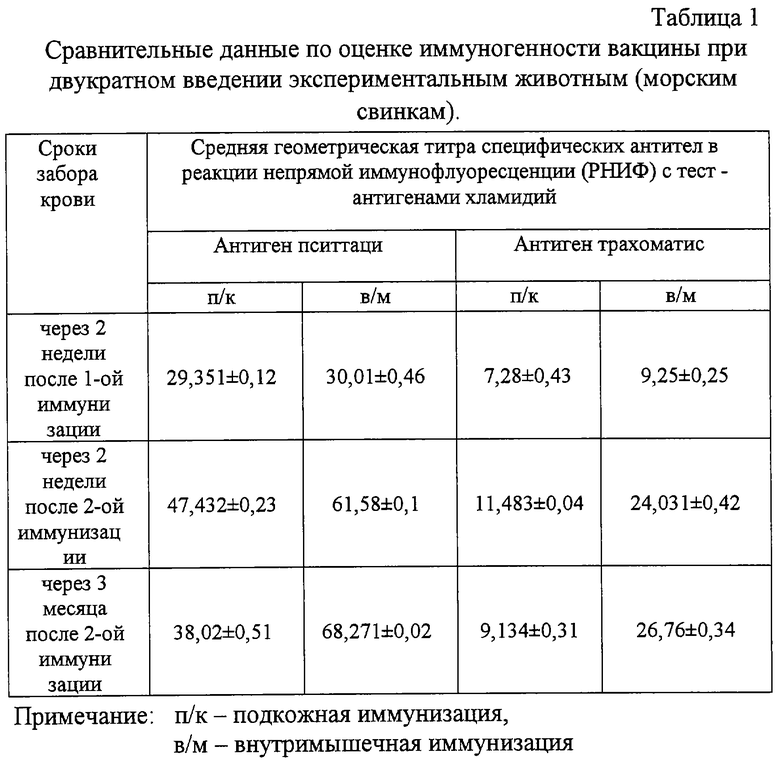
На основании результатов доклинических испытаний, проведенных на лабораторных животных, в соответствии с РД 42-28-8-89 “Доклинические испытания новых медицинских иммунобиологических препаратов”, утвержденных Минздравом РФ от 10.04.89, выявлено, что предложенный способ приготовления позволяет получить вакцину расширенного спектра действия, индуцирующую в организме экспериментальных животных (морских свинок) напряженный иммунитет при двукратной иммунизации подкожно или внутримышечно в отношении 2-х штаммов хламидий - хламидий пситтаци (возбудителя зоонозных хламидиозов) и хламидий трахоматис (возбудителя антропонозных хламидиозов),что отражено в таблице 1.
Кроме этого, полученная предложенным способом вакцина обладает высокой протективной активностью, обуславливающей в эксперименте 100% защиту от развития инфекции у вакцинированных морских свинок при внутрибрюшинном заражении их вирулентной культурой хламидий пситтаци и хламидий трахоматис в дозах 100 и 10000 LD50 (табл.2).

Использование предложенного способа приготовления позволит получить вакцину расширенного спектра действия и повысить ее протективную активность при подкожном или внутримышечном способе введения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ДЛЯ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ХЛАМИДИОЗА КРУПНОГО И МЕЛКОГО РОГАТОГО СКОТА | 2005 |
|
RU2301682C1 |
| ВАКЦИНА ДЛЯ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ХЛАМИДИОЗА СВИНЕЙ | 2002 |
|
RU2247577C2 |
| ВАКЦИНА ДЛЯ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ХЛАМИДИОЗА КРУПНОГО РОГАТОГО СКОТА | 1991 |
|
RU2092188C1 |
| ВАКЦИНА КУЛЬТУРАЛЬНАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ ХЛАМИДИОЗА (ОРНИТОЗА) ПТИЦ | 2005 |
|
RU2279892C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛАМИДИЙНОГО АНТИГЕНА ДЛЯ РЕАКЦИИ НЕПРЯМОЙ ИММУНОФЛУОРЕСЦЕНЦИИ | 2002 |
|
RU2223497C1 |
| ВАКЦИНА КУЛЬТУРАЛЬНАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ ХЛАМИДИОЗА СВИНЕЙ | 2002 |
|
RU2233670C2 |
| ВАКЦИНА КУЛЬТУРАЛЬНАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ ХЛАМИДИОЗА КРУПНОГО И МЕЛКОГО РОГАТОГО СКОТА | 2002 |
|
RU2233174C2 |
| Штамм хламидий СнLамYDIа рSIттасI, используемый для изготовления биопрепаратов для диагностики и профилактики хламидиоза серебристо-черных лисиц | 1989 |
|
SU1667870A1 |
| ВАКЦИНА КУЛЬТУРАЛЬНАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ ХЛАМИДИОЗА (ОРНИТОЗА) ПТИЦ | 1995 |
|
RU2125465C1 |
| Способ получения хламидиозного антигена для реакции непрямой иммунофлюоресценции | 1989 |
|
SU1711898A1 |
Изобретение относится к области медицины и касается способа приготовления вакцины для профилактики хламидиозов у человека. Сущность изобретения состоит в том, что вакцину готовят из цельноклеточных антигенов хламидий трахоматис (штамм “Л-2”) и хламидий пситтаци (штамм “Лори”), культивирование хламидий проводят в желточных мешках развивающихся куриных эмбрионов, взвесь овокультуры хламидий инактивируют нейтральным формалином, очищают дифференциальным центрифугированием и эфирной обработкой, уравновешивают по специфической активности и сорбируют на геле гидрооксида алюминия с последующим добавлением мертиолята в качестве консерванта. Техническим результатом является получение вакцины для профилактики хламидийной инфекции у человека, обладающей повышенной протективной активностью при подкожном или внутримышечном введении. 2 табл.
Способ приготовления вакцины для профилактики хламидийных инфекций у человека, отличающийся тем, что вакцину готовят из цельноклеточных антигенов хламидий двух видов - хламидий трахоматис (штамм “Л-2”) и хламидий пситтаци (штамм “Лори”), культивирование хламидий проводят в желточных мешках развивающихся куриных эмбрионов, взвесь овокультуры хламидий на стерильном апирогенном 0,9%-ном растворе натрия хлорида инактивируют нейтральным формалином в конечной концентрации 0,4% при температуре от 2 до 8°С в течение 5 суток, очищают дифференциальным центрифугированием и эфирной обработкой, уравновешивают по специфической активности не менее 128 АЕ (антигенных единиц) в мл и сорбируют на геле гидрооксида алюминия, с последующим добавлением консерванта, в качестве консерванта используют мертиолят в конечной концентрации 0,005-0,01%.
| ТЕРСКИХ И.И | |||
| и др | |||
| Аэрозольная вакцинация тканевой вакциной против орнитоза, Вопросы вирусологии, 1965, №1, с.99 и 100 | |||
| ВАКЦИНА ДЛЯ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ХЛАМИДИОЗА КРУПНОГО РОГАТОГО СКОТА | 1991 |
|
RU2092188C1 |
| ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ХЛАМИДИОЗА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПУШНЫХ ЗВЕРЕЙ | 1995 |
|
RU2085213C1 |
Авторы
Даты
2004-12-27—Публикация
2002-11-18—Подача