Изобретение относится к медицине, а именно к области фтизиобактериологии, и может быть использовано для определения лекарственной устойчивости микобактерий туберкулеза.
Разработка методов и сред для ускоренного определения лекарственной устойчивости является важной задачей современной фтизиобактериологии, особенно в условиях подъема лекарственной устойчивости, наблюдающегося в последние годы [1, 2]. Общеизвестно, что чем ранее начата адекватная химиотерапия, тем быстрее наступает излечение больного, поэтому клиницисты очень заинтересованы в быстром получении данных о лекарственной устойчивости МБТ, выделенных от пациента.
Учет результатов определения лекарственной устойчивости стандартным непрямым методом абсолютных концентраций на плотной яичной среде Левенштейна - Йенсена производится на 14-21-й день после посева культуры МБТ [3, 4]. Ускоренный метод определения лекарственной устойчивости на плотной яичной среде Попеску по нитратредуктазной активности применим только для Mycobacterium tuberculosis, но не для M.bovis, не имеющего данного фермента [5].
На жидких средах МБТ растут быстрее. Так, бульон Миддлбрука используется для определения лекарственной устойчивости в таких системах, как ВАСТЕС, МВ-ВАСТ, BBL-MGIT. Индикация роста МБТ в этих системах осуществляется радио-, коло- и флюорометрическими методами на 3-10-е сутки после посева культуры [6, 7, 8]. Перечисленные системы, использующие жидкую среду, очень дороги и доступны немногим хорошо оснащенным референс-лабораториям. Так, стоимость 1 флакона со средой МВ-ВАСТ превышает 100 руб., системы BBL-MGIT - около 1 у.е., система ВАСТЕС требует дорогого аппаратурного обслуживания и небезопасна радиологически.
Полужидкие среды используются в практике некоторых фтизиобактериологических лабораторий только для выделения измененных форм МБТ - L-форм [9].
В целях ускоренного определения лекарственной устойчивости штаммов МБТ перспективно использование полужидких сред с добавлением оптимальных количеств ростовых и питательных факторов и противотуберкулезных препаратов.
Прототипом предлагаемой среды является жидкая синтетическая среда Сотона [3], с помощью которой определяют лекарственную устойчивость. Но в практике фтизиобактериологии она, как и другие жидкие среды [3], используется в крайне редких случаях из-за неудобства применения или сложности и трудоемкости считывания результата: 1) визуально - по росту поверхностной пленки на 10-14-21-й день, при этом теряется преимущество среды в скорости роста; 2) по мазку из осадка - процедура, увеличивающая опасность внутрилабораторного заражения и требующая длительного времени.
Таким образом, преимущество предлагаемой среды в сравнении с наиболее близкими: 1) быстрота получения результатов - 3-7 суток; 2) дешевизна; 3) доступность любой фтизиобактериологической лаборатории, так как необходимые для нее ингредиенты постоянно используются в повседневной практике этих лабораторий; 4) безопасность - не требуются дополнительные манипуляции, такие, как высев, микроскопия для верификации роста; 5) простота считывания результата, которое осуществляется визуально.
Задачей предлагаемого изобретения является разработка питательной среды для ускоренного определения лекарственной устойчивости штаммов МБТ к трем основным препаратам - стрептомицину, изониазаду, рифампицину.
Задача решается за счет того, что в жидкую модифицированную среду Сотона добавляют 0,35% питательного агара и 25% лошадиной сыворотки.
Приготовление питательной среды для определения лекарственной устойчивости МБТ.
Основу среды представляет модифицированная жидкая синтетическая среда Сотона [10], в которую добавляют питательный агар и после стерилизации - лошадиную сыворотку. Конечная концентрация агар-агара в предлагаемой среде около 0,08%, то есть среда близка по консистенции к жидкой, что наряду с оптимальной концентрацией вносимой лошадиной сыворотки обусловливает быстрый рост МБТ, а агар-агар не дает инокуляту опускаться на дно, повышая локальную концентрацию микроорганизмов. Это обеспечивает быструю визуализацию роста - начальные его признаки на 3-5-е сутки, отчетливые - на 5-7-е сутки в зависимости от особенностей штамма.
Состав питательной среды, г:
Калий двухосновный фосфорнокислый 0,5
Магнезия сернокислая 0,05
Железо лимоннокислое аммиачное 0,05
Натрий лимоннокислый 2,0
L-аспарагин 4,0
Глицерин, мл 60
Питательный агар 3,5
Дистиллированная вода До 1 л
Смесь подогревают до полного растворения солей, разливают в колбы по 300 мл и стерилизуют в автоклаве при 1 атм (120°С) 30 мин. В остывшую полужидкую основу асептически добавляют 100 мл лошадиной сыворотки (к 300 мл основы, что составляет 25%). Затем полужидкую среду разливают в 4 колбы по 100 мл: 1 - контроль, без противотуберкулезных препаратов; 2 - с 1 мл стрептомицина в концентрации 1000 мкг/мл; 3 - с 1 мл изониазида в концентрации 100 мкг/мл; 4 - с 1 мл рифампицина в концентрации 2000 мкг/мл. Разведения препаратов производят стандартно [3, 4]. Конечные концентрации химиопрепаратов равны: стрептомицина - 10 мкг/мл, изониазида - 1 мкг/мл, рифампицина - 20 мкг/мл, то есть данные концентрации идентичны тем, которые используются в стандартном непрямом методе абсолютных концентраций. Затем среду с противотуберкулезными препаратами и без них разливают асептически по 4 мл. Пробирки должны быть закрыты резиновыми пробками без лунок.
Определение лекарственной устойчивости МВТ.
Готовят суспензию исследуемого штамма МБТ в физиологическом растворе по стандарту мутности 5 ед., разводят ее в 10 раз и вносят в пробирки с полужидкой средой в объеме 0,2 мл. Инокулят засевают поверхностно по стенке пробирки без перемешивания и встряхивания. Посевы инкубируют при 37°С в течение 7 дней. Учет результатов производят визуально. МБТ растут в верхней части среды в виде взвеси или облачка очень мелких и более крупных крошковидных колоний. При чувствительности культуры МБТ к препарату роста нет, среда остается равномерно прозрачной. При резистентности штамма МБТ к противотуберкулезным препаратам результат можно учитывать при появлении первых признаков роста, то есть на 3-5-е сутки, при чувствительности - не ранее 7 суток (срок, при котором наблюдается наибольший процент совпадений результатов, полученных с помощью данной среды и стандартной среды Левенштейна - Йенсена).
Испытание предлагаемой среды проведено на 242 клинических штаммах МБТ, выделенных из патологического материала больных туберкулезом органов дыхания и его внелегочными формами. Лекарственную устойчивость исследовали параллельно на предлагаемой среде и стандартным методом на среде Левенштейна - Йенсена.
Результаты определения скорости роста МБТ на предлагаемой среде по сравнению со средой Левенштейна - Йенсена представлены в табл. 1.

Как видно из приведенных данных, срок начального и отчетливого роста, определяемого визуально, на полужидкой среде в 2,1 и 2,8 раза меньше такового на среде Левенштейна - Йенсена, что делает предлагаемую среду перспективной для ускоренного определения лекарственной устойчивости.
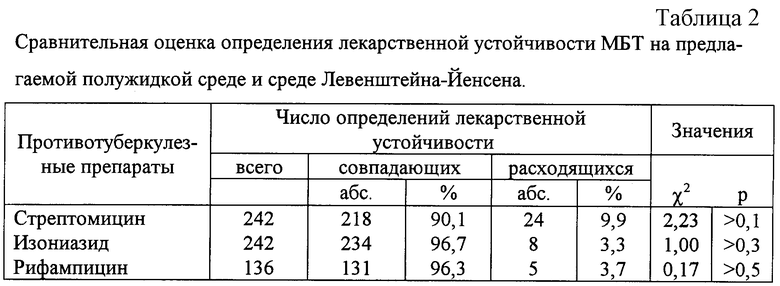
В табл. 2 представлены данные исследования лекарственной устойчивости с помощью предлагаемой среды и стандартным методом на среде Левенштейна - Йенсена. Статистически достоверных различий между ними нет.
Таким образом, проведенные исследования показали, что использование предлагаемой полужидкой среды в 2,1-2,8 раза сокращает сроки роста МВТ в сравнении со средой Левенштейна - Йенсена, используемой для определения лекарственной устойчивости стандартным методом, и дает высокий процент сходимости результатов. Поэтому для ускоренного определения устойчивости МБТ к основным противотуберкулезным препаратам - стрептомицину, изониазиду, рифампицину целесообразно использовать предлагаемую полужидкую среду.
Источники информации
1. Вишневский Б.И., Вишневская Е.Б., Платонова М.В. Лекарственная устойчивость микробактерий туберкулеза при различных локализациях заболевания// Мат. VII съезда Всерос. общ. эпидем., микробиол. и паразитол. - М., 1997, т.2, с.301 и 302.
2. Дорожкова И.Р., Попов С.А., Медведева И.Н. Мониторинг лекарственной устойчивости возбудителя туберкулеза в России за 1979-1998 гг.// Пробл. туб. - 2000, №5, с.19-22.
3. Ященко Т.Н., Мечева И.С. Руководство по лабораторным исследованиям при туберкулезе. - М.: Медицина, 1973.
4. Приказ №558 от 8.06.1978. Об унификации микробиологических методов исследования при туберкулезе. - М., 1978.
5. Патент RU 2099425. Способ определения лекарственной устойчивости микобактерий туберкулеза //Голышевская В.И., Корнеев А.А., Аникин В.А. и др.
6. Siddiqi S.H., Libonati J.P. Middlbrook G. Evaluation of a rapid radiometric method for drug susceptibility testing of Mycobacterium tuberculosis //J.Clin. Med. - 1981, 13, №5, p.908-912.
7. Севастьянова Э.В., Голышевская В.И., Сафонова С.Г. и др. Определение лекарственной устойчивости М. tuberculosis традиционными и современными методами //Тез.докл. IV съезда НМА фтиз. - М. - Йошкар-Ола, 1999, с.218.
8. Иртуганова О.А., Смирнова Н.С., Слогоцкая С.В. и др. Бактериологические методы определения лекарственной устойчивости микобактерий туберкулеза // Туберкулез сегодня: проблемы и перспективы. - М., 2000, с.73-75.
9. L-формы микобактерий туберкулеза/ Под ред. З.Н.Кочемасова. - М.: Медицина, 1980.
10. Щеголева Р.А. Модификация жидкой питательной среды Сотона для выращивания микобактерий туберкулеза. Лаб. дело. - 1989, №5, с.78 и 79.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ УСКОРЕННОГО ОПРЕДЕЛЕНИЯ ЛЕКАРСТВЕННОЙ ЧУВСТВИТЕЛЬНОСТИ M. tuberculosis К ОСНОВНЫМ ПРОТИВОТУБЕРКУЛЕЗНЫМ ПРЕПАРАТАМ | 2010 |
|
RU2470071C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ УСКОРЕННОГО ОПРЕДЕЛЕНИЯ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТИ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2003 |
|
RU2252260C2 |
| СПОСОБ ДИАГНОСТИКИ ЧУВСТВИТЕЛЬНОСТИ MYCOBACTERIUM TUBERCULOSIS К ПРОТИВОТУБЕРКУЛЕЗНЫМ ПРЕПАРАТАМ | 2005 |
|
RU2315113C2 |
| ТЕСТ-НАБОР ДЛЯ ОПРЕДЕЛЕНИЯ ЛЕКАРСТВЕННОЙ ЧУВСТВИТЕЛЬНОСТИ И ПЕРВИЧНОЙ ИДЕНТИФИКАЦИИ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2003 |
|
RU2268298C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОТУБЕРКУЛЕЗНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2549477C1 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА ЛЕГКИХ С ПРЕИМУЩЕСТВЕННО ЭКССУДАТИВНЫМ ТИПОМ ВОСПАЛЕНИЯ | 1990 |
|
RU2008902C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ И НОКАРДИОФОРМНЫХ АКТИНОМИЦЕТОВ | 2006 |
|
RU2322495C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛЕКАРСТВЕННОЙ ЧУВСТВИТЕЛЬНОСТИ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2003 |
|
RU2255977C1 |
| ФАРМАКОЛОГИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВОТУБЕРКУЛЕЗНОГО ДЕЙСТВИЯ | 2008 |
|
RU2412715C2 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2413517C1 |
Изобретение относится к области медицины, а именно к фтизиобактериологии. Сущность изобретения: разработана питательная среда для микобактерий туберкулеза (МБТ) для определения их лекарственной устойчивости на основе модифицированной синтетической среды Сотона, которая дополнительно содержит 0,35% питательного агара и 25% лошадиной сыворотки. Технический результат: среда позволяет получить визуально видимый рост МБТ в 2,1-2,8 раза быстрее (на 3-5-е сутки), чем на известной среде. Предлагаемая среда может быть использована в практике фтизиобактериологических лабораторий для ускоренного получения данных о лекарственной устойчивости клинических штаммов МБТ к изониазиду, стрептомицину, рифампицину. 2 табл.
Питательная среда для ускоренного определения лекарственной устойчивости микобактерий туберкулеза, содержащая солевой состав модифицированной питательной среды Сотона, отличающаяся тем, что она содержит дополнительно 0,35% питательного агара и 25% лошадиной сыворотки при следующем составе компонентов:
Полужидкая основа:
Калия двухосновного фосфорнокислого 0,5 г
Магнезии сернокислой 0,05 г
Железа лимоннокислого аммиачного 0,05 г
Натрия лимоннокислого 2,0 г
L-аспарагина 4,0 г
Глицерина 60 мл
Питательного агара 3,5 г
Дистиллированной воды До 1 л
Лошадиной сыворотки 100 мл/300 мл полужидкой основы
| ЩЁГОЛЕВА Р.А | |||
| Модификация жидкой питательной среды Сотона для выращивания микобактерий туберкулеза./Лабораторное дело, 1989, №5, с | |||
| Парный автоматический сцепной прибор для железнодорожных вагонов | 0 |
|
SU78A1 |
| Руководство по микробиологической диагностике инфекционных болезней./Под ред | |||
| К.И | |||
| Матвеева | |||
| - М.: Медицина, 1973, с | |||
| Клапанный регулятор для паровозов | 1919 |
|
SU103A1 |
Авторы
Даты
2004-04-10—Публикация
2001-07-30—Подача