Избретение относится к технологии производства энантиомеров липоевой кислоты, более конкретно к кристаллической модификации R- или S-липоевой кислоты и способу получения кристаллической липолевой кислоты.
α-Липоевая кислота применяется в промышленности пищевых продуктов и в фармацевических композициях.
Способ получения чистых энантиомеров липоевой кислоты описан, например, в публикации Bulman-Page и др., J. Сhem. Sоc., Сhem. Commun. 1986, 1409 и в заявке ЕР 0586987. Кроме того, ее рацемат может быть получен описанным в заявке ЕР 0586987 способом. Разделение рацемата может осуществляться применением хиральных аминов (см., например, заявку ЕР 0543088). (R)-Липоевая кислота может выделяться также и из естественных источников (см. Reed и др. JACS 1953, том 75, стр. 1267). Кроме того, (R)-липоевая кислота может быть получена описанным в заявке ЕР 487986 способом. Сырой продукт (энантиомер или рацемат) перекристаллизовывается потом из пентана, гексана или циклогексана. Кроме того, он может также перекристаллизовываться из смеси циклогексана и этилацетата в сооотношении 2:1 (см. вышеуказанную заявку ЕР 0595896).
В том случае, если указываются точные условия перекристаллизации и выходы энантиомеров липоевой кислоты, то из циклогексана при температуре от 5 до 10°С получают 40% в пересчете на сырой продукт, и из смеси циклогексана и этилацетата при приблизительно -15°С получают 31% в пересчете на сырой продукт.
Известные до сих пор способы получения кристаллических (R)- или (S)-α-липоевой кислоты дают выход продукта, который не пригоден для технического получения α-липоевой кислоты.
Возможность повышения выхода за счет повторного применения маточного щелока для кристаллизации технически сложна и приводит в общем к повышению количества загрязнений, которые в высшей степени нежелательны для фармацевтического применения или в промышленности пищевых продуктов.
Задачей изобретения является разработка чистой, применяемой в фармацевтической промышленности липоевой кислоты в пригодной для фармацевтического применения форме.
Поставленная задача решается кристаллической модификацией R- или S-липоевой кислоты, для которой линия рефлекции при 2Θ=23° на 2Θ-дифрактограмме является самой интенсивной в диапазоне 15-30°.
Другим объектом изобретения является способ получения кристаллической липоевой кислоты, при котором липоевую кислоту перекристаллизовывают из растворителя или из смеси растворителей при темперратуре от 0 до -20°С и растворитель или смесь растворителей выбирают с диэлектрической постоянной эпсилон от 1,95 до 2,4.
Продукт по изобретению получают с высокой чистотой (примесь <0,1%) и с высоким выходом, равным 75% и более. Он пригоден как для фармацевтического применения, так и для применения в промышленности пищевых продуктов, при которой липоевая кислота применяется в качестве добавки к продуктам питания, а также в пищевых добавках.
Кристаллизаты по изобретению имеют соотношение интенсивности между 2Θ=23° к 2Θ=18,2°, равное минимум 1.
Применение растворителей с диэлектрической постоянной 1,95-2,4 имеет по сравнению с известными решениями то преимущество, что при кристаллизации они дают кристаллизат с высокой чистотой при высоком выходе. В качестве растворителя или компонентов смеси растворителей могут применяться, например, разветвленные или неразветвленные, насыщенные или один или несколько раз ненасыщенные алифатические углеводороды с длиной цепи от С5 до С8, циклоалифатические углеводороды, такие как циклопентан, циклогексан, метилциклогексан, один или несколько раз галогенированные, предпочтительно хлорированные, углеводороды с длиной цепи 1-4 углеродов. Могут также применяться такие смеси растворителей, как технический гексан или гептан, при которых гексан или гептан является главным компонентом. Также могут применяться чистые растворители.
Предпочтительны смеси растворителей из алифатических или ароматических углеводородов.
В качестве растворителей или компонентов растворителей могут применяться одно- или многоядерные ароматы, которые могут быть замещенными. В качестве примера следует при этом привести толуол, о-, м- и п-ксилол, этил-, пропил- и изопропилбензол и мезитилен.
Растворители по изобретению или смеси растворителей должны иметь, кроме того, точку плавления ниже 0°С, предпочтительно ниже -20°С, особенно предпочтительно ниже -40°С. Кроме того, предпочтение отдается растворителям, которые по возможности приемлемы по токсилогическим соображениям, так как получаемая липоевая кислота должна применяться в качестве лекарственного средства или в качестве добавки к пищевым продуктам.
Предпочтительной верхней границей диэлектрической постоянной является величина 2,2, особенно предпочтительно она лежит в пределах 2,0-2,1.
Предпочтительная верхняя граница температурного диапазона кристаллизации составляет около -5°С, особенно предпочтительно, около -10°С.
Способ можно осуществлять при более низких температурах пока растворитель или смесь растворителей не затвердевает. Предпочтительная температурная граница составляет -20°С.
Предпочтительными смесями растворителей являются смеси из толуола или ксилола с С5-С7-алифатами при объемном соотношении от 1:1 до 1:4, особенно предпочтительна смесь из толуола и технического гексана или толуола и технического гептана.
Липоевая кислота перекристаллизовывается из растворителя или смеси растворителей, причем весовое соотношение между липоевой кислотой и растворителем составляет предпочтительно 1:5-1:15, особенно предпочтительно 1:8-1:12.
В случае применения смеси растворителей сначала производят растворение в полярной смеси или в полярном компоненте смеси и потом перед охлаждением до температуры от 0 до -20°С добавляют остаточный неполярный компонент смеси растворителей для перекристаллизации.
Продукт по изобретению имеет в водном растворе (1 г липоевой кислоты в 20 мл 1N NaOH) экстинкцию <0,300 (430 нм) при толщине слоя 1 см.
Пример 1.
10 г сырой (R)-α-липоевой кислоты вводят в 67 мл смеси растворителей толуола и технического гексана в соотношении 1:1 при 50°С. Получают раствор, который отфильтровывают. Фильтрат промывают с помощью 33 мл гексана (технического). Объединенные органические растворы держат 1 час в ледяной воде при 0-5°С и потом 1 час перемешивают при охлаждении при приблизительно до -15°С смесью льда и поваренной соли.
После этого продукт отсасывают и сушат в вакууме при комнатной температуре. Получают 8,1 г (R)-(+)-α-липоевой кислоты.
Пример 2.
10 г сырой (R)-α-липoевой кислоты растворяют в 35 мл толуола при 50°С. К реакционной смеси добавляют 35 мл технического гептана, фильтруют при 50°С на 4 г силикагеля F 60 и к фильтрату добавляют еще 35 мл технического гептана. Раствор охлаждают до температуры 0-5°С, вводят затравку и через 1 час охлаждают со скоростью 5°С/ч до -15°С.
Целевой продукт выделяют отсасыванием на фритте, промывают два раза с помощью 15 мл технического гептана и кристаллизат сушат в потоке азота. Получают 8,0 г (R)-α-липоевой кислоты, Тпл 47,9-48,9°С; [α]
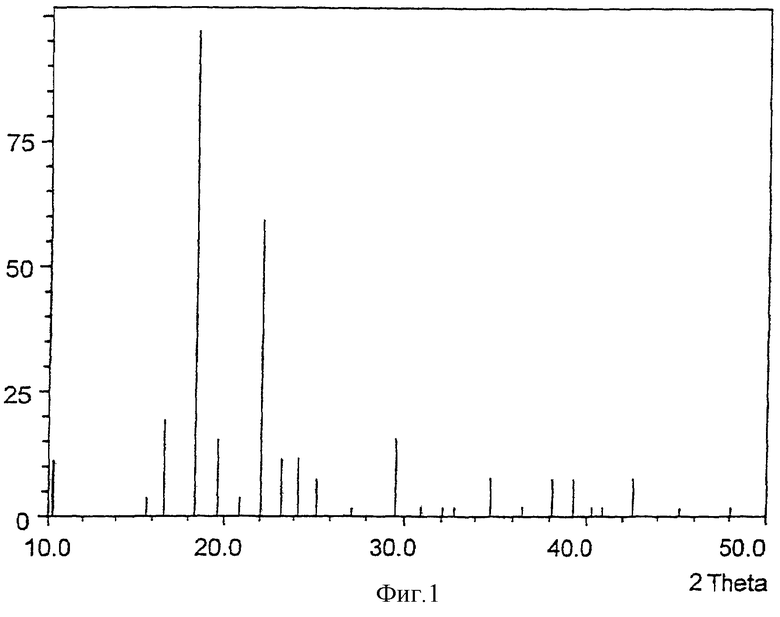
Полученную по изобретению кристаллическую модификацию липоевой кислоты подвергают рентгеновской дифракции с помощью Сu К-альфа-излучения.
Фиг.1 показывает дифрактограмму порошковой (R)-липоевой кислоты, полученной перекристаллизацией из циклогексана согласно вышеуказанному источнику Reed и др.
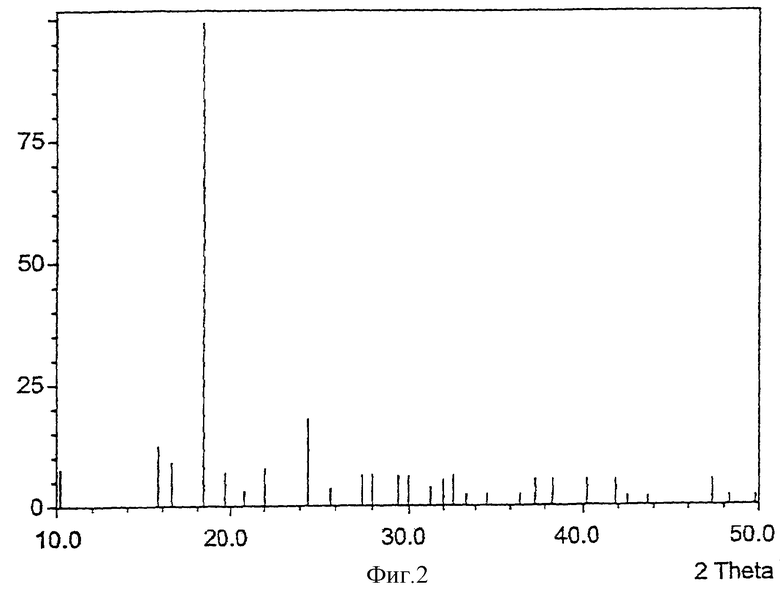
Фиг.2 показывает дифрактограмму порошковой (R)-липоевой кислоты, полученной перекристаллизацией из цикогексана/этилацетата (2:1) согласно вышеуказанной заявке ЕР № 593896.
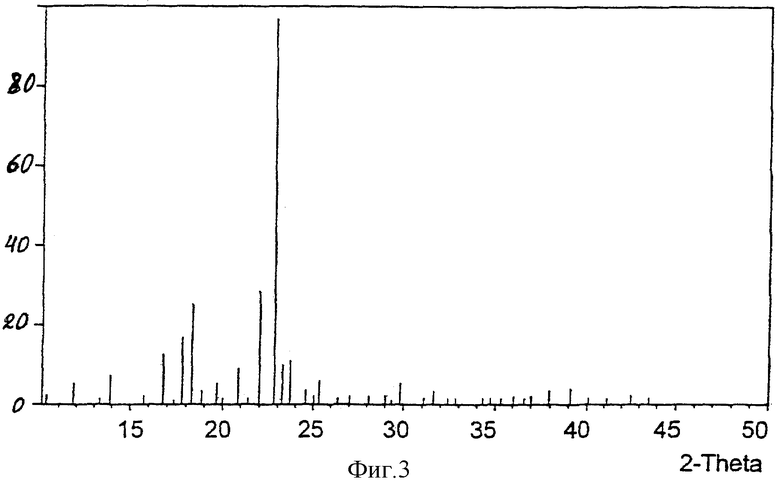
Фиг.3 показывает дифрактограмму порошковой (R)-липоевой кислоты по изобретению.
| название | год | авторы | номер документа |
|---|---|---|---|
| 8-ХЛОР-6-СУЛЬФОНИЛОКСИОКТАНОВЫЕ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ, ИХ ЭФИРЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ, ЭФИРЫ 6,8-ДИХЛОРОКТАНОВОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ 6,8-ДИХЛОРОКТАНОВЫХ КИСЛОТ И СПОСОБ ПОЛУЧЕНИЯ α-ЛИПОЕВОЙ КИСЛОТЫ (ВЫРИАНТЫ) | 1996 |
|
RU2176641C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА АНАЛОГА Y-АМИНОМАСЛЯНОЙ КИСЛОТЫ | 2004 |
|
RU2412162C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОЙ ФОРМЫ 8 СОФОСБУВИРА (ВАРИАНТЫ) | 2019 |
|
RU2745293C1 |
| НОВАЯ КРИСТАЛЛИЧЕСКАЯ ФОРМА СОЕДИНЕНИЯ ТРИЦИКЛИЧЕСКОГО БЕНЗОПИРАНА И СПОСОБ ЕГО ПРОИЗВОДСТВА | 2010 |
|
RU2523279C2 |
| КРИСТАЛЛИЧЕСКИЙ ДИАЦИЛГИДРАЗИН И ЕГО ПРИМЕНЕНИЕ | 2012 |
|
RU2629113C2 |
| СПОСОБ ОЧИСТКИ ПРОИЗВОДНОГО БЕНЗОПИРАНА, ЕГО КРИСТАЛЛИЧЕСКАЯ ФОРМА И СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОЙ ФОРМЫ | 2016 |
|
RU2729074C2 |
| МАЛЕАТ 3-[2-(ДИМЕТИЛАМИНО)МЕТИЛ-(ЦИКЛОГЕКС-1-ИЛ)]ФЕНОЛА И ЕГО КРИСТАЛЛИЧЕСКИЕ ФОРМЫ | 2006 |
|
RU2434845C2 |
| 8-ГАЛОГЕН-6-ГИДРОКСИОКТАНОВЫЕ КИСЛОТЫ, ИХ ЭФИРЫ, СОЛИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2175965C2 |
| ЛЕЧЕНИЕ МИГРЕНИ С ПОМОЩЬЮ ВВЕДЕНИЯ α-ЛИПОЕВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ | 2000 |
|
RU2232577C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА И СПОСОБ ЕЕ ОЧИСТКИ | 2011 |
|
RU2604734C2 |
Настоящее изобретение относится к кристаллической модификации R- или S-липоевой кислоты, для которой линия рефлекции при 2Θ=23° на 2Θ-дифрактограмме является самой интенсивной в диапазоне 15-30°. Также описывается дающий высокий выход способ получения кристаллической липоевой кислоты, при котором липоевую кислоту перекристаллизовывают из растворителя или из смеси растворителей при температуре от 0 до -20°С и растворитель или смесь растворителей выбирают с диэлектрической постоянной эпсилон от 1,95 до 2,4. 2 с. и 3 з.п. ф-лы, 3 ил.
| RU, 96105410, А1, 10.06.1998 | |||
| ЕР, 694542, А1, 31.01.1996 | |||
| DE, 4235912, А1, 28.04.1994. |
Авторы
Даты
2004-04-10—Публикация
1999-07-12—Подача