(54) СПОСОБ ПОЛУЧЕНИЯ СУЛЬФСЖИЛШЫХ СОЕДИНЕНИЙ
-SOg-CHgCH-CHgCHs I
OH
взаимодействием ароматического альдегида с соответствутощим замещенным нитротолуолом при HarpesaifflH в присутствии основного ката1шзатора. Одаако способ получения соединений формулы 1 неизвестен.
Полученные соединения представляют интерес в качестве физиологически активных соединений, а могут найти применение в качестве восстановительного компонента в окислительно-восстановительных системах катализаторов, которые используются для получения гомо- и сополимеров с олефиновой связью.
Предлагается способ получения соединений формулы 1, заключающийся в том, что сульфинов то кислоту подвергают взаимодействию с соответствующим аяьдегадом и образовавшееся при зтом оксисульфонильное соединение подвергают взаимодействию с тиолоь или гщклической мочевиной, или производным мочевины, или соединением общей формулы II
Н2 N-COO-Y-OOC-NHa где У имеет указанное значение, с последующим выделением целевого продукта известным способом.
В качестве сульфиновых кислот общей формулы II можно применять, например, метан-, зтан-, пропан-, бутан-, бензол-, п-толуол-, п-хлорбензол-, 4-метоксибензол-, 3-трифторметилбензол-, 4-нитробензол-, 3-цианбензол-, 4-ацетаминобензол-, 3,4-дихлор-, 2,5-дихлор- или 2,6-дихлорбензол-, 2,3,4--трихлорбензол-, 2,5-даметоксибензол-, 3,4,5-триметоксибензол-, 3-метокси- 5-хлорбензол-, 2-хлор-5-нитробензол-, 2-хлор- 5-трифторметилбензол-, 2-хлор- 6-метилбензол-, 4-гидрокси-5-карбоксибензол-, 2-тиофен-, 2-нафталин- сульфоновые кислоты.
Можно применять также и соли сульфиновой кислоты, ft особенности натриевые и калиевые.
Сульфиновые кислоты можно получать, например, восстановлением соответствующих хлоргидридов сульфоновой кислоты (их получают путем взаимодействия соответствующих замещенных бензолов с хлорсульфокислотой или из соответствующих замещенных анилинов путем модифицированной реакции Зандмейера по Меервейну)или путем непосредственной реакции Зандмейера с получением сульфиновой кислоты. Таким образом получили, например, еще неизвестную 2-хлор-6-метилбензолсульфиновую кислоту (т.пл. ПО С с разложением), исходя из 2-хлор-6- метиланил1ша через 2-хлор-6-метил,бензолсульфохлорид (т. кип. 117t/l,3MMpT.cT.
В качестве альдегидов можно применять, например, формальдегид, ацетальдегид, пропионовый альдегид, Н- или мзо-бутиральдегид, Я- или ызо-валериановый альдегид, капроновьш альдегид.
бензальдегид, хлораль, бромаль, п- и о-хлорбензальдегид, п-бромбензальдегид, п- и о-метоксибензальдегид, 3,4,5-триметоксибензальдегид, о-оксибензальдегид, 2,5- и 3,4-дихлорбензальдегид, п-диметиламинобензальдегид, п-ацетилами-нобензальдегид, толилальдегид, .м-ии-нитробензальдегид, фурфуровый альдегид, фурфурол, акролеин, кретоновый альдегид, пиридил-3- альдегид, глиоксиловую кислоту (также в виде ее солей, в особенности натриевой, калиевой, кальциевой, аммониевой, триэтаноламмониевой и триэтиламмониевой соли).
В качестве тиолов (меркаптанов) можно применять, например, метантиол, этантиол, пропантиол, бутантиол, р-оксизтантиол, бензолтиол, п-хлорбензолтиол, п-оксибензолтиол, 3,4-дихлорбензолтиол, 2-хлор 5- трифторметилбензолтиол, 3-трифторметилбензолтиол, 4-ацетиламинобензолтиол, 4-диметиламинобензолткол, 2,3,4-трихлорбензолтиол, 4-бромбензолтиол, 2,5-диметоксибензод1тиол,
5-хлор-2- метоксибензолтиол, 2-нафталинтиол, 2-хлор-6- метилбензолтиол, 4-метилбензолтиол, фенилметантиол, 3,4-диметилбензолтиол, циклопентантиол, п-меркаптобензойную кислоту, меркаптоуксусную кислоту, метиловый, этиловый и
пропиловый эфиры меркаптоуксусной кислоты.
Тиолы можно получать известными способами, например путем апкшшрования или арилирования сероводорода и путем превращения других серных функций в группу -SH. При алкилировании сероводорода целесообразно замещение второго атома Н легкоотщепляемыми радикалами. Алкилируют, например, тиосульфат натрия, тиомочевину или ксантогенаты и продукты алкшшрования посредством подкисления или гидролиза переводят в
ТИОЛЫ. Ароматические тиолы. предпочтительно получают восстановлением хлорангидридов сульфокислоты.
В качестве циклической мочевины и ее производных можно применять, например,
JfJfV (этиленмочевина)
Н
О
г
(п ропиленмочевина)
S О
ШК хМН
(бутиленмочевина)
О
Л НОон НзССНз
v-f
HN,xNH
О
ии
оО (ацетиленмочевина) - N-снз; Шч Ы-СгНд; II ..Ы- ОНз HNxxN-Ci Hg HNxxN - CHg-CgHs Л Из соединений, содержащих карбоксильные группы, формулы 1 можно получать, соли путем взаимодействия с неорганическими или органическими основаниями. При получении срлей щелочны и щелочноземельных металлов, в особенности солей калия, натрия и кальция, целесообразно применение растворенного в спирте алкоголята. Пример 1. 35г п-толуолсульфинкислого натрия5 00 мл воды, 30 мл муравьиной кислоты S5%-w u} и 20 мл формалъдегада (39%-н« в воде в течение 3 час перемешивают при 40° С. Затем к прозрачному раствору добавляют 16 г зтиленмочевины и перемешивают еще в течение Ш мин при 40°С и еще в течение 2 час при 10°С. Приблизительно через 10 мин после добавки этиленмочевины кристаллизуется продукт в виде бесцветных игольчатых кристаллов. Получают 38,5 г (76% от теоретического) соединения формулы СНз -Шг-/ }ын с Т.ПЛ. i 58°f (разложение). Пример 2. 24 г 3,4-дихлорбензолсульфинккслого натрия, 10 г этиленмочевины, 75 мл воды, 200 мл муравьиной ки«лоть1 (85%-мая) и 15 г о-хлорбенза;п дегида, размеши пя при 40°С, растворяют до прозрачного состояния. По истечении 5 мин начинается кристаллизация. Смесь перемешивают еще в течение получаса при 40° С, охлаждают до 10 С и отсасьтают. Проля тают небольшим количеством воды. Можно перекристаллизовывать из изопропанола. Выход продукта 32 г (77% от теоре;Тического) соединения формулы CH-N NH ClV О СТ.Ш1. 161°С, Пример 3. Юг пропиленмочевины, 40 г глиоксиловой кислоты (45%-ная) в воде, 20мл воды и 10 мл муравьиной кислоты (85%-ная) в течение Зчас перемеиявают при 80-85° С. Затем охлаждают до 40°f и добавляют растаор из 40 г птолуолсульфинкислого натрия (избыток) в 150мл воды и 50мл муравьиной кислоты (85%-ная). Смесь размешивают в течение 5 час при 40° С, добавляют еще 15 мл соляной кислоты (25%-ная) и охлаждают до 10°С. После вьщержки в течение ночк выкристадянзовьшается вещество. Его отсасывают и промывают 100 мл дкдяНой воды. Вещество можно перекристаллизовывать из изопропанола. Выход продукта 30 г- (58% от теоретического) соединения формулы гГЧ И, S02-CH-N N-CH-SOr I Y I 0 ещество хорошо растворяется в водном растворе икарбоната натрия. Пример 4. 25 г 3,4-дихлорбензолсуль.шкислого натрия, 50мл воды, 50мл муравьиное ислоты (85%-ная) и 15 г 50%-ного раствора диксиметилзтиленмочевины в течение 3 час размемвают при 50° С. По истечении 20 мин начинается ристаллизация. После охлаждения до 10 Си выержки в течение ночи отсасывают бесцветные гольчатые кристаллы соединения формулы се ,-so,,-/4-cf Y т. пл. 2102;(разложение) и хорпЕпо промывают дой. Можно nepCKpHCTanjrasoBbmaTb ип лйоксана. .7 Дыход продукта 22,6 г (87,5% кого).
Соедвненн формулы R - 02- СН - $R 2 от теоретичес-Аналогичным способом получают соединения, S5%46 8 приведенные в табл. 1-4. Таблица 1

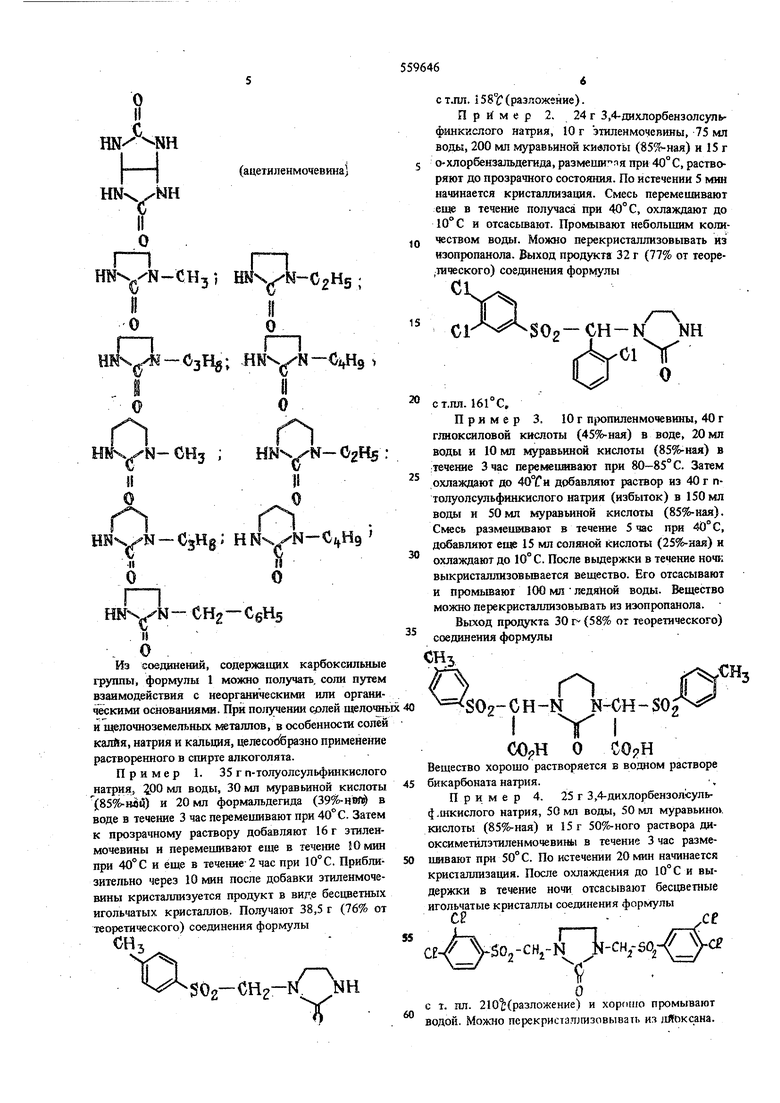
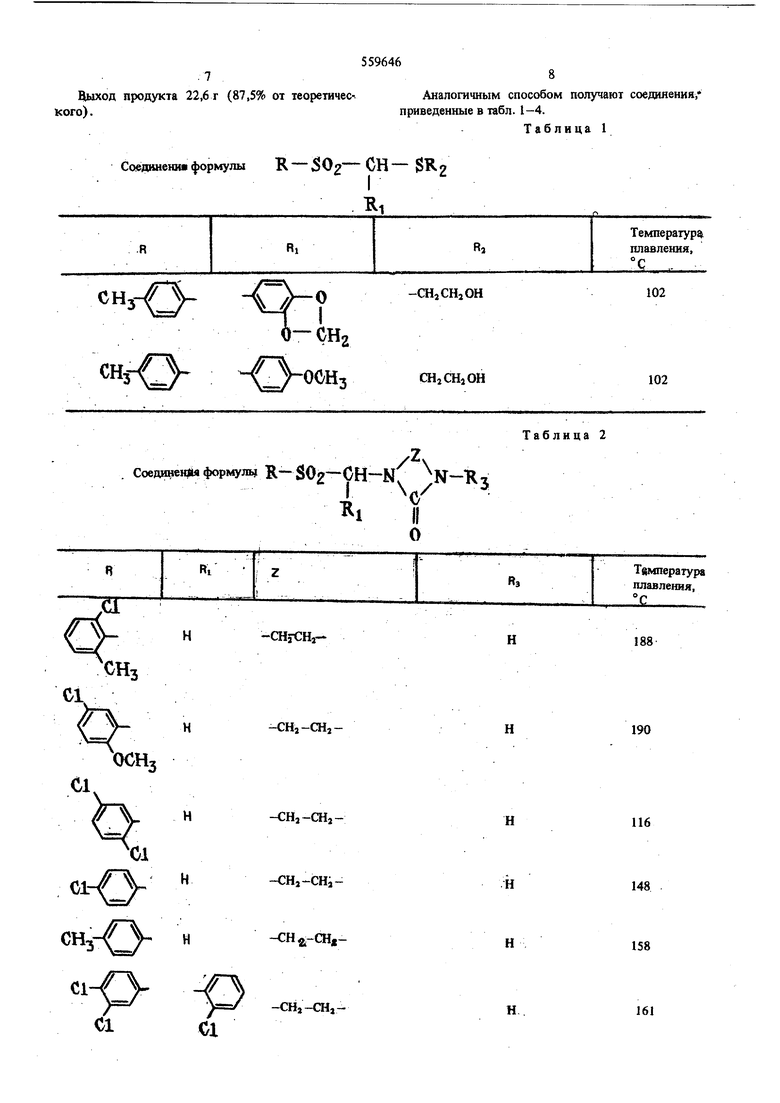
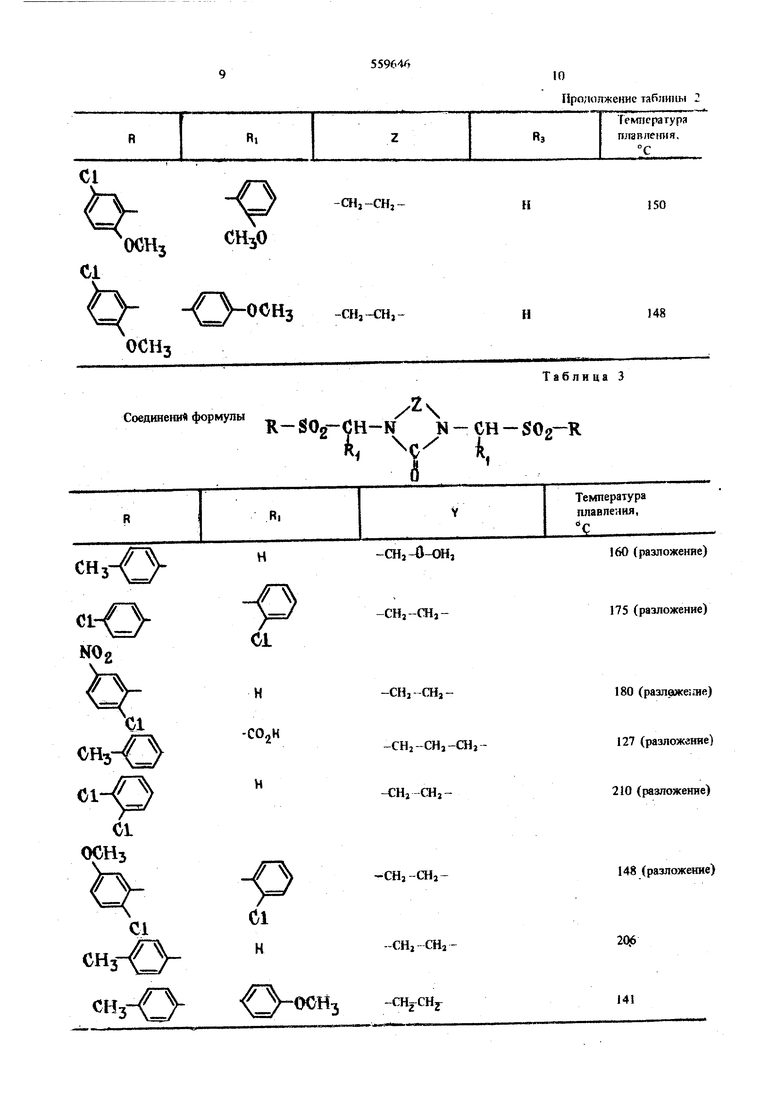
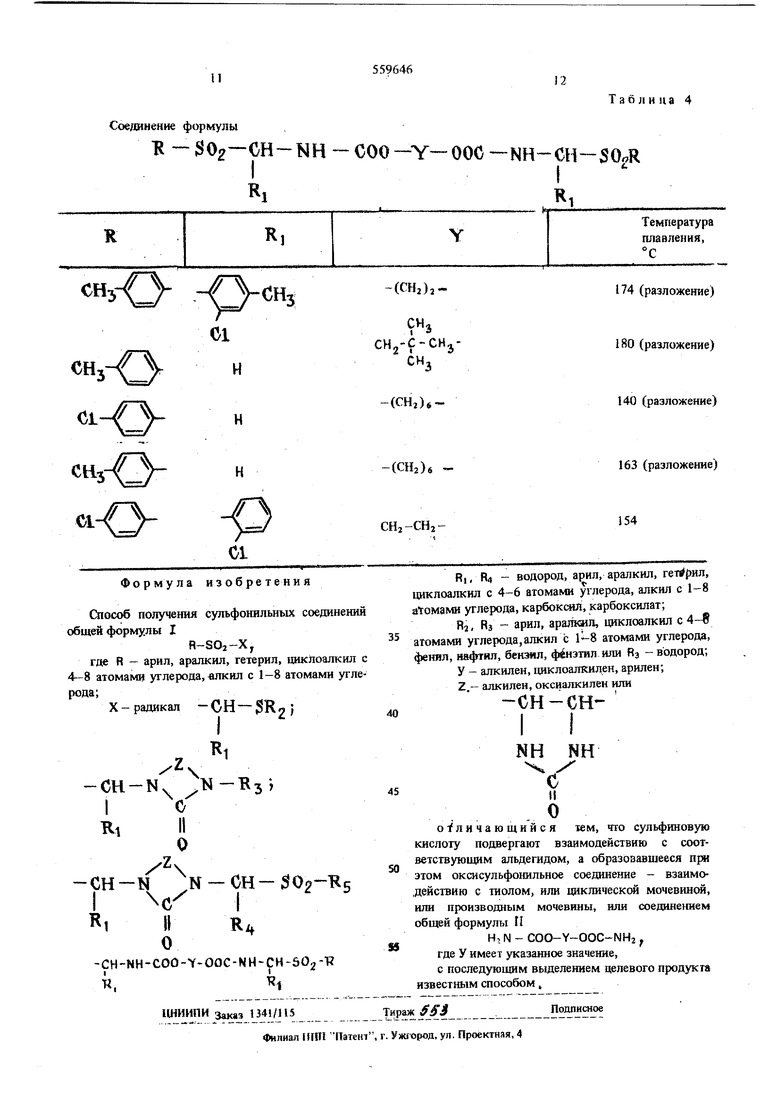

cHj-/.
i //-о
I- СНг
сн,-/3
/л
-осн.
S--S02 CH NN-H-i
1II
102
-сн,сн,он
CHjCHjOH
102
Таблица 2
/2.
О
н
-CHfCHjн
188
С1
-CHj-CHjн
оса
Н
-CHj -СН -
И
-CHj j -
сн,,Cl
ysss/ -CHa-CHjCl
Cl
н
190
н
116
н
148
H
158
H
161
С1
-Ш,-СНз
ООНч 5
н
150
ООН
3 -сн,-сн,148
н
ОСНз
Соединение формулы
сНз-О -ОСНз
Таблица 3
I xj
CH S02-R
V 210 (разложение) -CHi СН2 148 (разложение) -CHj-CHj-CHj CHj-ot cHjr
Таблица 4
Авторы
Даты
1977-05-25—Публикация
1972-06-02—Подача