Данное изобретение относится к новым способам получения промежуточных соединений (в частности, 4-циано-3-нитробензотрифторида), которые могут быть использованы при получении пестицидов.
Пестицидные 4-бензоилизоксазолы, в частности 5-циклопропилизоксазоловые гербициды и промежуточные соединения в их синтезе, описаны в литературе, например в публикациях Европейских патентов №0418175, 0487353, 0527036, 0560482, 0609798 и 0682659.
Известны различные способы получения этих соединений. Данное изобретение направлено на разработку усовершенствованных способов получения пестицидов и промежуточных соединений, которые могут быть использованы при их получении.
Поэтому целью данного изобретения является разработка новых и более экономичных способов получения соединений орто-нитробензонитрила.
Следующей целью данного изобретения является разработка способов получения соединений орто-нитробензонитрила с высоким выходом и/или высокой селективностью.
Дальнейшей целью данного изобретения является разработка способа получения соединений орто-нитробензонитрила, требующих применения небольшого количества соединения меди в качестве катализатора.
Очередной целью данного изобретения является разработка способа получения соединений орто-нитробензонитрила, включающего применение цианистой меди (I) без необходимости применения катализатора.
Следующей целью данного изобретения является разработка способа получения соединений орто-нитробензонитрила, проводимого при более низкой температуре, чем известные способы, и поэтому более легкого для осуществления.
Данное изобретение позволяет достичь этих целей полностью или частично.
Краткое описание изобретения
Данное изобретение, соответственно, предусматривает способ получения соединения орто-нитробензонитрила формулы (I):
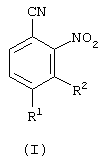
где R1 - C1-4 галоалкил (предпочтительно трифторметил), фтор, хлор или бром;
R2 - водород или C1-4 алкокси;
включающий реакцию соответствующего орто-нитрогалобензола формулы (II):
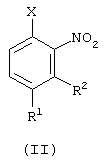
где R1 и R2 имеют вышеуказанные значения, а Х - атом фтора, хлора или брома, с, когда Х - атом фтора:
(a) цианидом щелочного металла в безводном растворителе необязательно в присутствии катализатора; или
когда Х - атом хлора:
(b) цианистой медью (I) и источником бромида, выбираемого из бромистого водорода, брома и бромида тетраалкиламмония; необязательно в присутствии бромида щелочного или щелочноземельного металла; или
(c) цианидом щелочного металла или тетраалкиламмония в присутствии бромистой меди (I) и межфазного катализатора; или
(d) цианистой медью (I) и йодистым литием; или
когда Х - атом брома:
(e) цианистой медью (I) необязательно в присутствии катализатора, выбираемого из бромида щелочного или щелочноземельного металла;
или
(f) цианидом щелочного металла в присутствии каталитического количества цианистой меди (I) и межфазного катализатора.
Некоторые соединения формулы (I) известны, и многие способы их получения и превращения в гербицидные производные 4-бензоилизоксазола описаны в вышеуказанных заявках на Европейские патенты.
Соединения формулы (II) известны или могут быть получены известными способами.
В формулах (I) и (II), а также в приводимых ниже формулах символы предпочтительно имеют следующие значения:
R1 предпочтительно представляет собой трифторметил, фтор или бром; a R2 - водород или метокси.
В особенно предпочтительном варианте осуществления данного изобретения R1 - трифторметил, a R2 - водород.
В соответствии с данным изобретением подразумевается, что термин "алкил", составляющий часть солей тетраалкиламмония, означает алкильную группу с прямолинейной или разветвленной цепью, содержащую от 1 до 6 атомов углерода.
Подробное описание изобретения
Вышеуказанное получение (а) соединений формулы (I) из соединений формулы (II), где Х - атом фтора, осуществляют с применением цианида щелочного металла (например, цианистого натрия или калия). Предпочтительным является цианистый натрий. Количество применяемого цианида обычно составляет 1-2 мольных эквивалента, предпочтительно 1-1,1 мольных эквивалентов.
Подходящими являются многие безводные растворители, например нитрилы, такие как ацетонитрил или бензонитрил; простые эфиры, такие как тетрагидрофуран или диглим (диметиловый эфир диэтиленгликоля); амиды, такие как N,N-диметилформамид или N-метилпирролидон; кетоны, такие как метилизобутилкетон; сложные эфиры, такие как метилбензоат или н-бутилацетат; диметилсульфоксид или сульфолан. Растворитель предпочтительно выбирают из бензонитрила, ацетонитрила, тетрагидрофурана или N,N-диметилформамида.
Реакцию обычно проводят в растворителе, содержащем менее чем примерно 1 об.% воды, предпочтительно менее около 0,5%, еще более предпочтительно менее около 0,1%, обычно приблизительно от 0,005 до 0,05%. Однако следует иметь в виду, что в некоторых случаях допускается несколько большее или меньшее содержание воды в зависимости от природы применяемых растворителей и температуры реакции, получаемого соединения формулы (I) и других условий реакции.
Предпочтительно применяют катализатор, который может быть выбран из солей аммония (таких как хлориды, бромиды или гидросульфаты тетраалкиламмония или триалкилбензиламмония, в которых алкильные группы имеют прямолинейные или разветвленные цепи, содержащие от 1 до 6 атомов углерода, такие как бромид тетраметиламмония); или предпочтительно солей гуанидиния (таких как хлорид гексабутилгуанидиния или хлорид гексаметилгуанидиния). При использовании катализатора его количество обычно составляет от 0,01 до 0,3 мольных эквивалентов, предпочтительно от 0,05 до 0,25 мольных эквивалентов.
Температура реакции обычно составляет от 20°С до температуры кипения растворителя, предпочтительно от 30 до 180°С, более предпочтительно от 60 до 100°С.
Вышеуказанное получение (b) соединений формулы (I) из соединений формулы (II), где Х - атом хлора, осуществляют с применением цианистой меди (I) и источника бромида, выбираемого из бромистого водорода, брома и бромида тетраалкиламмония, необязательно в присутствии бромида щелочного или щелочноземельного металла, предпочтительно бромистого лития. В соответствии с этим способом количество применяемой цианистой меди обычно составляет 0,5-2 мольных эквивалентов, предпочтительно 0,8-1,2 мольных эквивалентов.
Количество источника бромида обычно составляет 0,05-1 мольный эквивалент.
Если в реакционной смеси также присутствует бромид щелочного или щелочноземельного металла, то его количество является каталитическим и обычно составляет 0,01-0,5 мольных эквивалентов, обычно 0,02-0,05 мольных эквивалентов.
Растворитель может быть выбран из нитрилов, таких как ацетонитрил или бензонитрил; кетонов, таких как метилизобутилкетон; простых эфиров, таких как тетрагидрофуран или диглим (диметиловый эфир диэтиленгликоля); сложных эфиров, таких как метилбензоат или н-бутилацетат; диметилсульфоксида или сульфолана. Предпочтительными растворителями являются ацетонитрил, бензонитрил или диглим.
Концентрация соединения формулы (II), применяемого в реакционном растворителе, обычно составляет от 0,1 до 2 мл/ммоль, предпочтительно от 0,2 до 1 мл/ммоль.
Реакционная температура обычно составляет от 100 до 200°С, предпочтительно от 130 до 180°С.
Вышеуказанное получение (с) соединений формулы (I) из соединений формулы (II), где Х - атом хлора, осуществляют с применением цианида щелочного металла (например, цианистого натрия или калия) либо цианида тетраалкиламмония в присутствии бромистой меди (I) и межфазного катализатора.
Цианид щелочного металла предпочтительно представляет собой цианистый калий. Количество применяемого цианида щелочного металла или тетраалкиламмония обычно составляет 1-1,5 мольных эквивалента (предпочтительно 1-1,1 мольных эквивалентов). Количество применяемой бромистой меди (I) обычно составляет 0,01-2 мольных эквивалента (предпочтительно 1 мольный эквивалент). Реакцию осуществляют с применением твердого или жидкого межфазного катализатора. Межфазный катализатор может быть выбран из солей тетраалкиламмония или триалкилбензиламмония (таких как бромид тетраметиламмония или бензилтриметиламмония); солей фосфония (таких как бромид трибутилгексадецилфосфония); солей гуанидиния (таких как бромид гексабутилгуанидиния или гексаметилгуанидиния); а также краун-эфиров (таких как 18-краун-6). Количество применяемого катализатора по переносу фаз обычно составляет 0,05-0,3 мольных эквивалентов. Подходящие для реакции растворители включают нитрилы, такие как ацетонитрил или бензонитрил; простые эфиры, такие как тетрагидрофуран или диглим (диметиловый эфир диэтиленгликоля); кетоны, такие как метилизобутилкетон; или сложные эфиры, такие как метилбензоат. Предпочтительным растворителем является ацетонитрил.
Концентрация соединения формулы (II), применяемого в реакционном растворителе, обычно составляет от 0,1 до 2 мл/ммоль, предпочтительно от 0,2 до 1 мл/ммоль.
Реакционная температура обычно составляет от 100 до 200°С, предпочтительно от 130 до 180°С.
Вышеуказанное получение (d) соединений формулы (I) из соединений формулы (II), где Х - атом хлора, осуществляют с применением цианистой меди (I) и йодистого лития. Обычно в реакции применяют 0,5-2 мольных эквивалентов (предпочтительно 0,8-1,2 мольных эквивалентов) цианистой меди (I). Количество применяемого йодистого лития обычно составляет от 0,05 до 2 мольных эквивалентов, предпочтительно от 0,2 до 0,5 мольных эквивалентов.
Подходящие для реакции растворители включают нитрилы, такие как бензонитрил или ацетонитрил; простые эфиры, такие как диглим (диметиловый эфир диэтиленгликоля); кетоны, такие как метилизобутилкетон; или сложные эфиры, такие как метилбензоат.
Реакционная температура обычно составляет от 100 до 200°С, предпочтительно от 130 до 180°С.
Вышеуказанное получение (е) соединений формулы (I) из соединений формулы (II), где Х - атом брома, осуществляют с применением цианистой меди (I) необязательно в присутствии катализатора, выбираемого из бромида щелочного или щелочноземельного металла, предпочтительно бромистого лития. Обычно в реакции применяют 0,5-2 мольных эквивалентов (предпочтительно 1-1,1 мольных эквивалентов) цианистой меди (I). При использовании катализатора его количество обычно составляет от 0,05 до 2 мольных эквивалентов.
Подходящие для реакции растворители включают нитрилы, такие как ацетонитрил или бензонитрил; простые эфиры, такие как тетрагидрофуран или диглим (диметиловый эфир диэтиленгликоля); кетоны, такие как метилизобутилкетон; сложные эфиры, такие как метилбензоат или н-бутилацетат; амиды, такие как N,N-диметилформамид или N-метилпирролидон; диметилсульфоксид или сульфолан. Предпочтительными растворителями являются ацетонитрил, бензонитрил или тетрагидрофуран.
Температура реакции обычно составляет от 100 до 200°С, предпочтительно от 110 до 160°С (более предпочтительно от 120 до 140°С).
Соединение формулы (II), применяемое в реакции, может содержать часть (обычно до 20%) соответствующего соединения, в котором атом брома замещен атомом хлора. Было установлено, что это не наносит вреда реакции. Поэтому более удобной и простой может оказаться очистка и выделение соединения нитрила формулы (I), чем применение чистого соединения формулы (II). Такое выделение может быть проведено с применением стандартных процедур, известных в данной области, например дистилляцией.
Вышеуказанное получение (f) соединений формулы (I) из соединений формулы (II), где Х - атом брома, осуществляют с применением цианида щелочного металла в присутствии каталитического количества цианистой меди (I) и межфазного катализатора. Предпочтительным цианидом щелочного металла является цианистый калий. Количество применяемой цианистой меди (I) обычно составляет от 0,05 до 0,2 мольных эквивалентов. Количество применяемого цианида щелочного металла обычно составляет 0,5-2 мольных эквивалентов, предпочтительно 0,6-1,3 мольных эквивалентов (более предпочтительно 0,7-1 мольных эквивалентов). Межфазный катализатор может быть выбран из бромидов щелочных или щелочноземельных металлов, предпочтительно бромистого лития; бромидов тетраалкиламмония или триалкилбензиламмония, в которых алкильные группы имеют неразветвленные или разветвленные цепи, содержащие от 1 до 6 атомов углерода (таких как бромид тетраметиламмония или бензилтриметиламмония); солей фосфония (таких как бромид трибутилгексадецилфосфония); солей гуанидиния (таких как бромид гексабутилгуанидиния или гексаметилгуанидиния); а также краун-эфиров (таких как 18-краун-6). Количество применяемого межфазного катализатора обычно составляет 0,05-0,5 мольных аквивалентов (предпочтительно 0,05-0,3 мольных эквивалентов).
Подходящие для реакции растворители включают нитрилы, такие как ацетонитрил или бензонитрил; спирты, такие как н-бутанол; амиды, такие как N,N-диметилформамид или N-метилпирролидон; кетоны, такие как метилизобутилкетон; сложные эфиры, такие как метилбензоат; простые эфиры, такие как тетрагидрофуран или диглим (диметиловый эфир диэтиленгликоля); диметилсульфоксид или сульфолан.
Концентрация соединения формулы (II), применяемого в реакционном растворителе, обычно составляет от 0,1 до 2 мл/ммоль, предпочтительно от 0,2 до 1 мл/ммоль, более предпочтительно от 0,2 до 0,4 мл/ммоль.
Температура реакции обычно составляет от 100 до 200°С, предпочтительно от 110 до 160°С.
В соответствии со следующей целью данного изобретения разработан способ (g) получения соединения формулы (II), где R1 и R2 имеют вышеуказанные значения, а Х - атом брома, включающий реакцию соответствующего соединения формулы (II), где Х - атом хлора, с источником бромида.
Примеры подходящих источников бромида включают бромиды щелочных металлов (такие как бромистый калий или литий); бромиды щелочноземельных металлов (такие как бромистый магний); бромистую медь (I); бромистую медь (II); бромистый цинк; бромистый водород; или бром; или смесь бромистого лития и бромистой меди (I). Предпочтительным источником бромида является смесь бромистого лития и бромистой меди (I); или бромистый магний, или бромистая медь (II). Количество применяемого источника бромида обычно составляет от 1 до 5 мольных эквивалентов. При использовании смеси бромистого лития и бромистой меди (I) обычно применяют 0,1-1 мольных эквивалентов бромистой меди (I) вместе с одним или двумя мольными эквивалентами бромистого лития.
Для получения хороших результатов обычно необходим растворитель. Подходящие для реакции растворители включают нитрилы, такие как ацетонитрил или бензонитрил; простые эфиры, такие как тетрагидрофуран или диглим (диметиловый эфир диэтиленгликоля); кетоны, такие как метилизобутилкетон; сложные эфиры, такие как метилбензоат или н-бутилацетат; N-метилпирролидон; алкановые кислоты, такие как уксусная кислота; диметилсульфоксид и сульфолан.
Температура реакции обычно составляет от 100 до 200°С, предпочтительно от 130 до 180°С. Хорошие результаты могут быть получены при осуществлении данного способа в концентрированной среде.
В соответствии с очередной особенностью данного изобретения способ (е) или (f) может быть соединен со способом (g) для получения соединения формулы (I) исходя из соединения формулы (II), где Х - атом хлора.
Соединения формулы (I), полученные способами в соответствии с данным изобретением, могут быть использованы при получении гербицидно-активных производных 4-бензоилизоксазола, например, согласно следующей реакционной схеме:
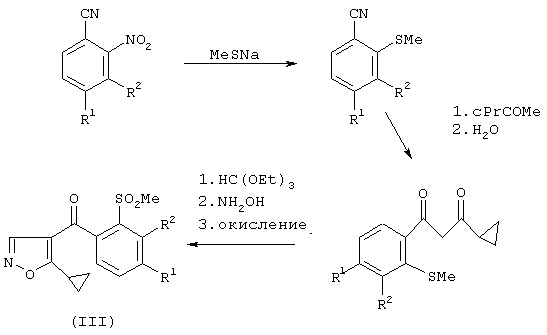
4-Бензоилизоксазолы формулы (III) описаны, к примеру, в публикациях Европейских патентов № 0418175, 0527036 и 0560482.
Данное изобретение проиллюстрировано следующими неограничивающими примерами. Подразумевается, что указанные концентрации ингредиентов в растворителе означают концентрацию соединения формулы (II) в растворителе (т.е. мл растворителя/ммоль соединения формулы (II)).
Пример 1
Получение 4-циано-3-нитробензотрифторида из 4-фторо-3-нитробензотрифторида с применением цианида щелочного металла
(способ (а)):
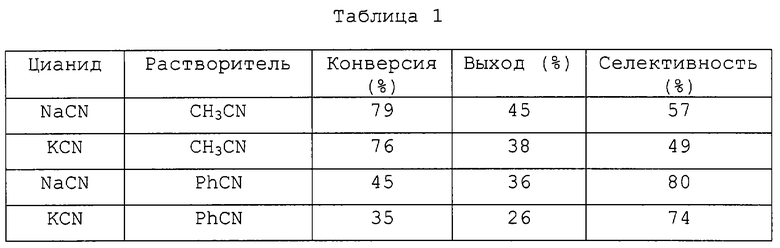
Смесь 4-фторо-3-нитробензотрифторида (1 ммоль) и цианистого натрия или калия (1 ммоль), а также ацетонитрила или бензонитрила (1 мл/ммоль) смешивают при 20°С и подвергают нагреванию в течение 6 часов при 80°С, получая целевой продукт. Результаты представлены в таблице 1, откуда следует, что применение цианистого натрия обеспечивает хорошую селективность.
Пример 2
Получение 4-циано-3-нитробензотрифторида из 4-фторо-3-нитробензотрифторида с применением цианистого натрия: действие температуры, растворителя и катализатора (способ (а)):
Смесь 4-фторо-3-нитробензотрифторида (1 ммоль) и цианистого натрия (1 ммоль), а также N,N-димeтилфopмaмидa, ацетонитрила, тетрагидрофурана или бензонитрила (1 мл/ммоль) перемешивают при 20°С и подвергают нагреванию в течение 6 часов, получая целевой продукт. Результаты представлены в таблице 2, откуда следует, что бензонитрил (PhCN) обеспечивает самую высокую селективность.
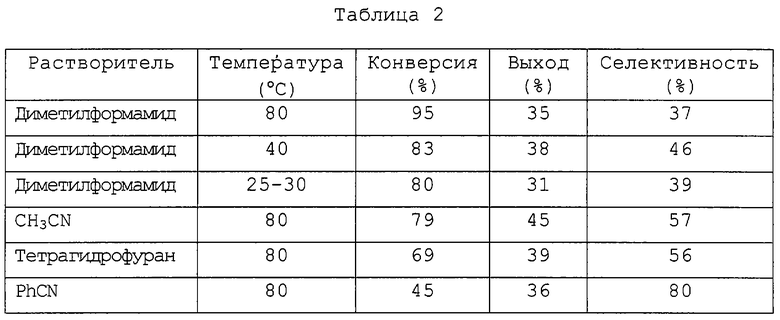
Вышеописанную экспериментальную процедуру повторяют при 80°С, но в присутствии катализатора (0,2 эквивалента) и ацетонитрила, тетрагидрофурана или бензонитрила (1 мл/ммоль). В качестве катализаторов применяют хлорид гексабутилгуанидиния или бромид тетрабутиламмония. Результаты, представленные в таблице 3, показывают, что применение хлорида гексабутилгуанидиния в качестве катализатора обеспечивает очень хорошую селективность, особенно в отношении тетрагидрофурана или бензонитрила.
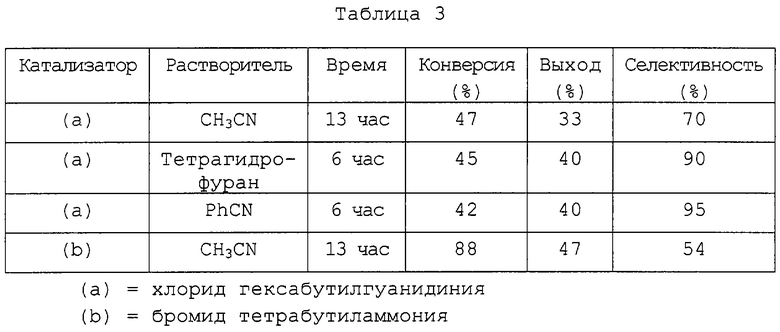
(a)=хлорид гексабутилгуанидиния
(b)=бромид тетрабутиламмония
Пример 3
Получение 4-циано-3-нитробензотрифторида из 4-хлоро-3-нитробензотрифторида с применением цианистой меди (I) и источника бромида (способ (b)):
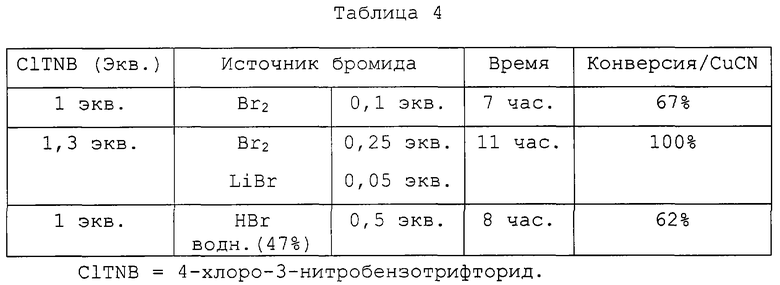
Смесь 4-хлоро-3-нитробензотрифторида (1 или 1,3 эквивалентов), цианистой меди (I) (1 эквивалент) и брома (необязательно в присутствии каталитического количества бромистого лития) или бромистого водорода (47% водн.) перемешивают в бензонитриле (2 эквивалента) при 20°С и подвергают нагреванию при 170°С, получая целевой продукт. Результаты представлены в таблице 4. Селективность в этих реакциях составляет, по меньшей мере, 90%
 .
.
ClTNB=4-хлоро-3-нитробензотрифторид.
Вышеописанную процедуру повторяют, используя 4-хлоро-3-нитробензотрифторид (1 эквивалент), цианистую медь (I) (1 эквивалент) и бромид бензилтриметиламмония (1 эквивалент) в ацетонитриле (1 мл/ммоль) с нагреванием при 160°С в течение 6 часов и получением целевого соединения. Конверсия 4-хлоро-3-нитробензотрифторида составляет 94%, выход продукта - 62%, а селективность - 66%.
Вышеописанный эксперимент повторяют, но со следующими изменениями: цианистую медь (I) (1 эквивалент) и трет-бутиламингидробромид (1 эквивалент) в бензонитриле (2 эквивалента) смешивают при 20°С, а затем подвергают нагреванию до 150°С. После этого в течение часа добавляют 4-хлоро-3-нитробензотрифторид (1,2 эквивалента) и смесь выдерживают при такой температуре в течение 7 часов. Очевидно (таблица 5), что при использовании таких условий реакция протекает с хорошей селективностью.

Пример 4
Получение 4-циано-3-нитробензотрифторида из 4-хлоро-3-нитробензотрифторида с применением цианида щелочного металла, бромистой меди (I) и межфазного катализатора (способ (с)):
Смесь 4-хлоро-3-нитробензотрифторида (1 эквивалент), цианистого калия (1 эквивалент), бромистой меди (I) (1 эквивалент) и четвертичной соли аммония (0,2 эквивалента) смешивают при 20°С, а затем подвергают нагреванию с ацетонитрилом (1 мл/ммоль) при 160°С в течение 6 часов, получая целевой продукт. Таблица 6 показывает результаты, из которых следует, что такие условия обеспечивают хорошую селективность.

Пример 5
Получение 4-циано-3-нитробензотрифторида из 4-хлоро-3-нитробензотрифторида с применением цианистой меди (I) и йодистого лития (процесс (d)):
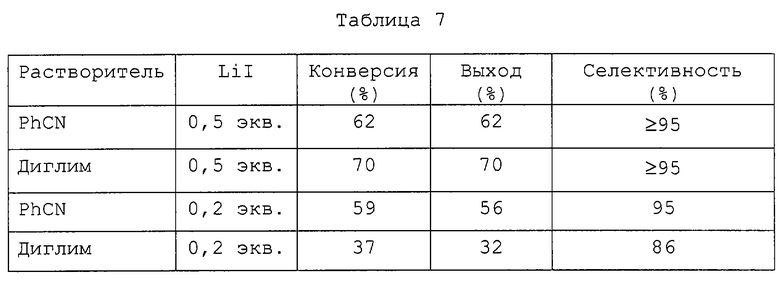
Смесь 4-хлоро-3-нитробензотрифторида (1 эквивалент), цианистой меди (1 эквивалент) и йодистого лития (0,2 или 0,5 эквивалента) нагревают с бензонитрилом или диглимом (диметиловый эфир диэтиленгликоля) (1 мл/ммоль) в течение 6 часов при 160°С, получая целевой продукт. Йодистый литий выбирают из-за его растворимости в органических растворителях. Таблица 7 показывает результаты, из которых следует, что особенно хорошую селективность обеспечивает применение 0,5 эквивалента йодистого лития.
Пример 6
Получение 4-циано-3-нитробензотрифторида из 4-бромо-3-нитробензотрифторида с применением цианистой меди (I) необязательно в присутствии бромистого лития (способ (е)):
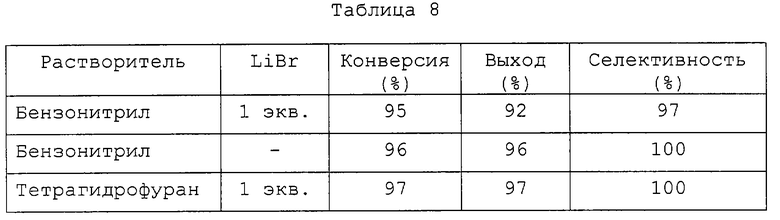
Смесь 4-бромо-3-нитробензотрифторида (1 эквивалент) и цианистой меди (I) (1 эквивалент) необязательно в присутствии бромистого лития (1 эквивалент) и бензонитрила или тетрагидрофурана (1 мл/ммоль) подвергают нагреванию при 130°С в течение 6 часов, получая целевой продукт. Результаты (таблица 8) показывают, что такие условия с применением катализатора или без него обеспечивают отличные выход и селективность.
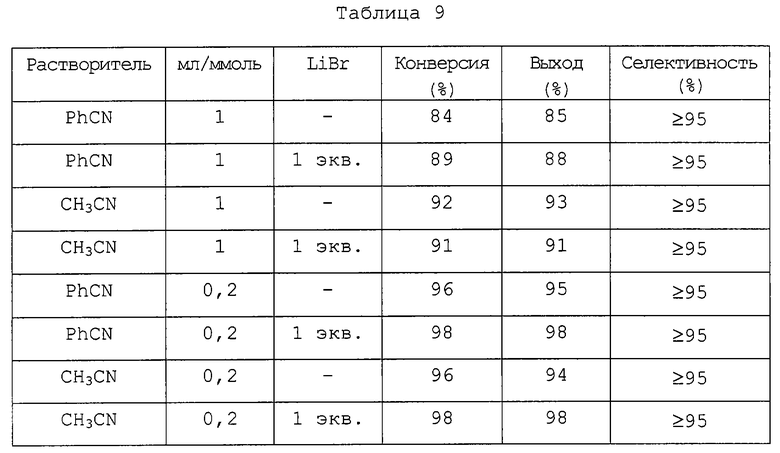
Вышеуказанный эксперимент повторяют, применяя бензонитрил или ацетонитрил (1 мл/ммоль) при 110°С. Бромистый литий улучшает растворимость цианистой меди (I) в органическом растворителе, однако отличные результаты получают (таблица 9) как с применением бромистого лития, так и без него.
Пример 7
Крупномасштабное получение 4-циано-3-нитробензотрифторида из смеси 4-бромо-3-нитробензотрифторида и 4-хлоро-3-нитробензотрифторида с применением цианистой меди (I) (способ (е)):
Смесь 4-бромо-3-нитробензотрифторида (0,2 эквивалента, 1,7 моль, содержащую 12% 4-хлоро-3-нитробензотрифторида) и цианистой меди (I) (1 эквивалент) нагревают до 130°С, а затем в течение 4 часов при 130°С добавляют оставшийся 4-бромо-3-нитробензотрифторид (0,8 эквивалента). После нагревания еще в течение 2 часов при 130°С охлажденную смесь экстрагируют (толуол), промывают (водный бромистый натрий, а затем бисульфит натрия) и выпаривают, получая целевой продукт. Конверсия и выход целевого продукта (в расчете на содержание 4-бромо-3-нитробензотрифторида) составляют 100%. 4-Хлоро-3-нитробензотрифторид остается неизменным.
Пример 8
Получение 4-циано-3-нитробензотрифторида из 4-бромо-3-нитробензотрифторида с применением цианида щелочного металла и каталитического количества цианистой меди (I) в присутствии межфазного катализатора (способ (f)):
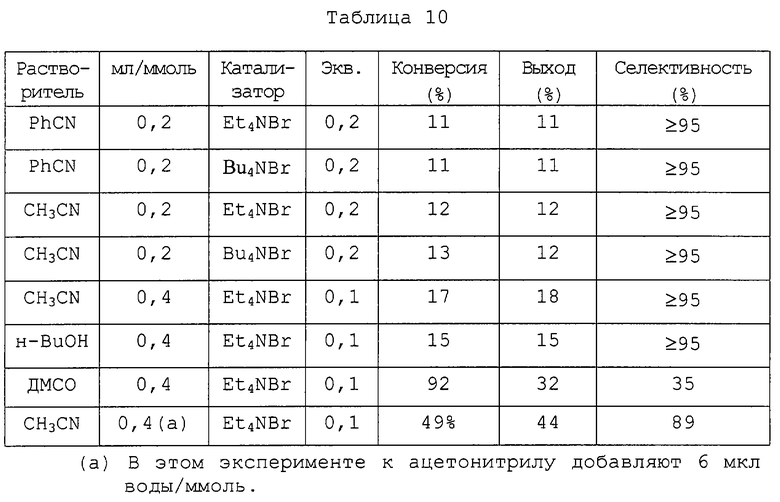
Смесь 4-бромо-3-нитробензотрифторида (1 эквивалент), цианистого калия (0,9 эквивалента), цианистой меди (I) (0,1 эквивалента) и межфазного катализатора (бромид тетраэтиламмония или тетрабутиламмония) подвергают нагреванию с бензонитрилом, ацетонитрилом, н-бутанолом или диметилсульфоксидом при 110°С в течение 6 часов. Результаты (таблица 10) показывают, что отличная селективность может быть получена в результате применения бензонитрила, ацетонитрила или н-бутанола при концентрации, составляющей 0,2 мл/ммоль или 0,4 мл/ммоль. При наличии, помимо ацетонитрила (0,4 мл/ммоль), небольшого количества воды (6 мкл/ммоль) выход целевого продукта повышается до 44%, при этом селективность остается на высоком уровне.
Пример 9
Получение 4-циано-3-нитробензотрифторида из 4-бромо-3-нитробензотрифторида с применением цианида щелочного металла и каталитического количества цианистой меди (I) в присутствии бромистого лития в качестве межфазного катализатора (способ (f)):
Смесь 4-бромо-3-нитробензотрифторида (1 эквивалент, 0,02 моль), цианистого калия (1,2 эквивалента, 0,024 моль), цианистой меди (I) (0,1 эквивалента, 0,002 моль) и бромистого лития (0,25 эквивалента, 0,005 моль) подвергают нагреванию в 6 мл ацетонитрила при 110°С в течение 18 часов, после чего исходный 4-бромо-3-нитробензотрифторид оказывается израсходованным. Охлажденную смесь экстрагируют (метил трет-бутиловый эфир), промывают (вода), сушат (сульфат магния) и выпаривают, получая целевой продукт.
Конверсия составляет 99%, а выход продукта - 89,7% при чистоте, составляющей 93,8%.
Пример 10
Получение 4-бромо-3-нитробензотрифторида из 4-хлоро-3-нитробензотрифторида с применением различных источников бромида (способ (g)):
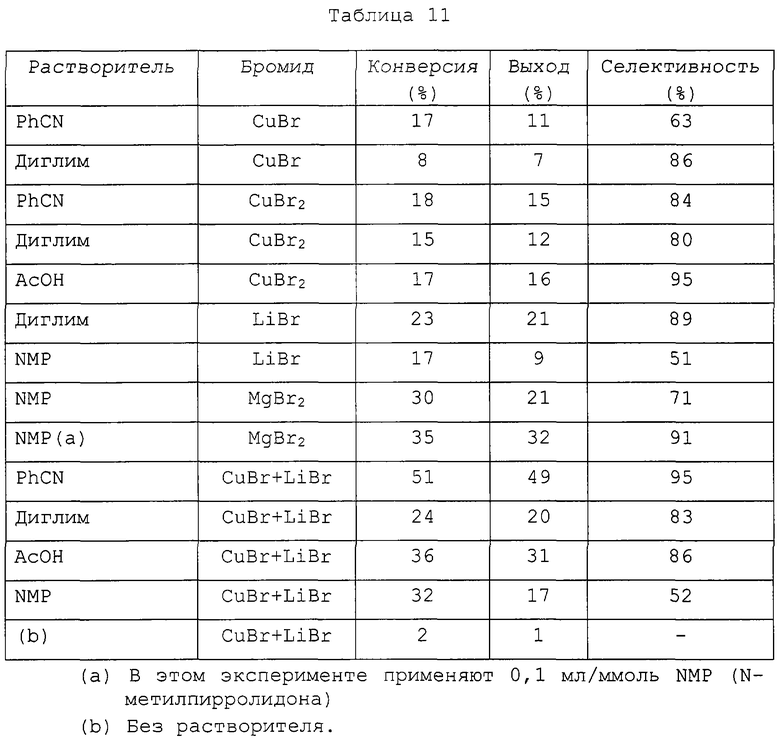
Смесь 4-хлоро-3-нитробензотрифторида (1 эквивалент) и источника бромида (бромистая медь (I), бромистая медь (II), бромистый литий или магний) (1 эквивалент) или смесь бромистой меди (I) (1 эквивалент) и бромистого лития (1 эквивалент) подвергают нагреванию в течение 6 часов при 160°С с бензонитрилом, диглимом (диметиловый эфир диэтиленгликоля), уксусной кислотой или N-метилпирролидоном (1 мл/ммоль), получая целевой продукт. Таблица 11 показывает, что хорошая селективность может быть получена в различных условиях и что смесь бромистой меди и бромистого лития обеспечивает особенно хорошие результаты. Для сравнения в отсутствие растворителя были получены плохие результаты.
 .
.
Пример 11
Получение 4-бромо-3-нитробензотрифторида из 4-хлоро-3-нитробензотрифторида с применением смеси бромистой меди и бромистого лития (способ (g)):
Процедуру, описанную выше в примере 10, повторяют, применяя смесь бромистой меди (I) (1 эквивалент) и бромистого лития (1 эквивалент) с различными концентрациями бензонитрила (0,02, 0,04, 0,1, 0,5, 1 или 2 мл/ммоль). Таблица 12 показывает, что хорошую селективность получают, применяя все вышеуказанные условия, но когда бензонитрил присутствует в количестве 0,04 мл/ммоль, выход и селективность особенно высоки.
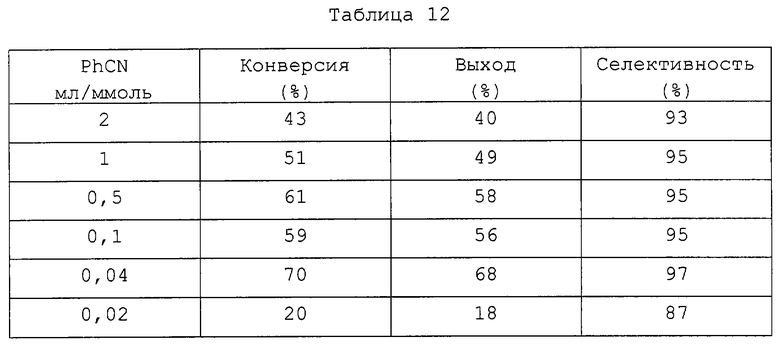
Вышеописанную реакцию повторяют, но вместо бензонитрила применяют диглим (диметиловый эфир диэтиленгликоля), имеющий различные концентрации (0,01, 0,02, 0,04, 0,08, 0,1, 0,5, 1 или 2 мл/ммоль). Таблица 13 показывает, что оптимальную конверсию, выход и селективность обеспечивает концентрация, составляющая 0,02-0,04 мл/ммоль.
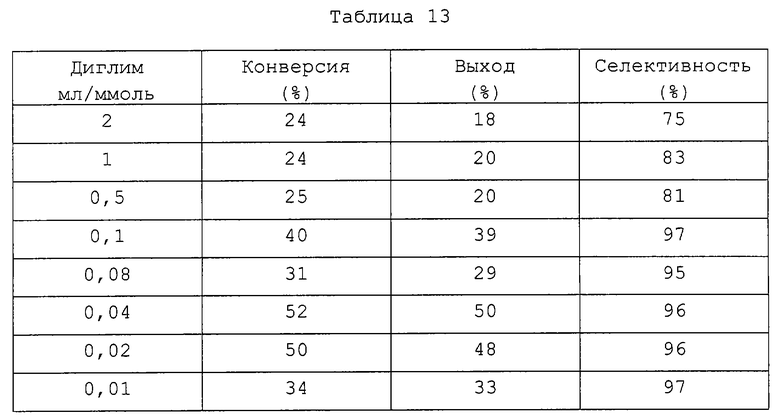
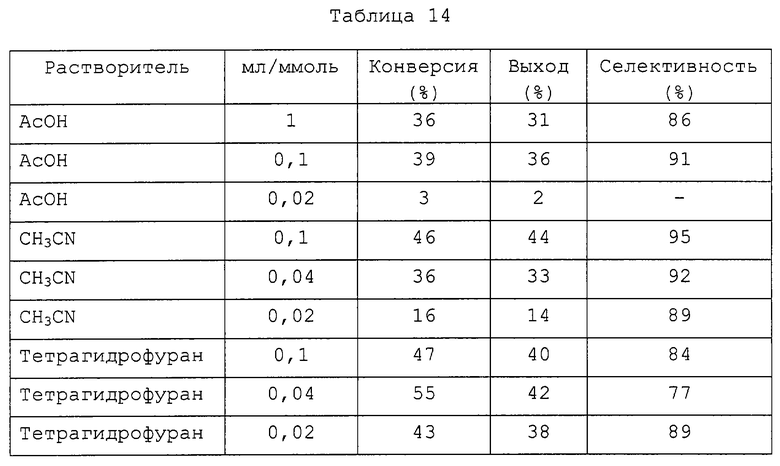
Вышеописанную реакцию повторяют, но вместо бензонитрила применяют уксусную кислоту, ацетонитрил или тетрагидрофуран в различных концентрациях (0,02, 0,04, 0,1 и 1 мл/ммоль). Таблица 14 показывает результаты, из которых следует, что оптимальная концентрация зависит от растворителя и что наилучшие результаты получают при высокой концентрации.
Пример 12
Получение 4-бромо-3-нитробензотрифторида из 4-хлоро-3-нитробензотрифторида с применением различных соотношений смеси бромистой меди (I) и бромистого лития (способ (g)):
Смесь 4-хлоро-3-нитробензотрифторида (1 эквивалент), бромистой меди (I) (1 эквивалент) и бромистого лития (2 эквивалента) в бензонитриле (4 эквивалента) подвергают нагреванию при 180°С в течение 5 часов. Охлажденную смесь экстрагируют толуолом, промывают водным раствором бромистого натрия и раствором бисульфита натрия, а затем выпаривают, получая целевой продукт. Конверсия (в расчете на 4-хлоро-3-нитробензотрифторид) составляет 84%, выход - 78%, а селективность - 93%.
Вышеописанную реакцию повторяют, применяя бромистую медь (I) (0,1 эквивалента) и бромистый литий (2 эквивалента), при этом конверсия составляет 83%, а селективность - 90%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-АМИНОМЕТИЛПИРИДИНА И 2-ЦИАНОПИРИДИНА | 2001 |
|
RU2266900C2 |
| Способ получения нитриловКЕТОКАРбОНОВыХ КиСлОТ | 1977 |
|
SU799653A3 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ЦИАНОПИРИДИНОВ | 2000 |
|
RU2222530C2 |
| Способ получения 2-/2',2',2'-тригалогенэтил/-4-галогенциклобутан-1-онов | 1978 |
|
SU917695A3 |
| Способ получения пестицидных производных | 1999 |
|
RU2223950C2 |
| Способ получения нитрилов кетокарбоновых кислот | 1977 |
|
SU745361A3 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 1997 |
|
RU2175958C2 |
| РЕАКЦИИ СОЧЕТАНИЯ, КОТОРЫЕ МОГУТ БЫТЬ ИСПОЛЬЗОВАНЫ ПРИ ПОЛУЧЕНИИ ПРОИЗВОДНЫХ (1Н-ТЕТРАЗОЛ-5-ИЛ)БИФЕНИЛА | 2005 |
|
RU2426728C2 |
| СПОСОБ ГИДРОЦИАНИРОВАНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С НЕНАСЫЩЕННОЙ ЭТИЛЕНОВОЙ СВЯЗЬЮ | 1996 |
|
RU2186058C2 |
| СПОСОБ СТЕРЕОСЕЛЕКТИВНОГО ПОЛУЧЕНИЯ АСИММЕТРИЧНО АЛКИЛИРОВАННЫХ ПРОИЗВОДНЫХ ОКСИНДОЛА | 1991 |
|
RU2072354C1 |
Настоящее изобретение относится к новым способам (вариантам) получения промежуточных соединений (в частности, 4-циано-3-нитробензофторида), которые могут быть использованы при получении пестицидов. Способы (варианты) получения соединения формулы (I):
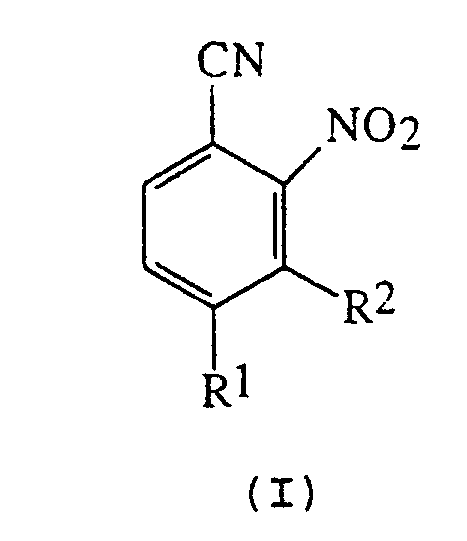
где R1 означает C1-4 галогеналкил; R2 означает водород или C1-4 алкокси; включают взаимодействие соответствующего орто-нитрогалогенбензола формулы (II):
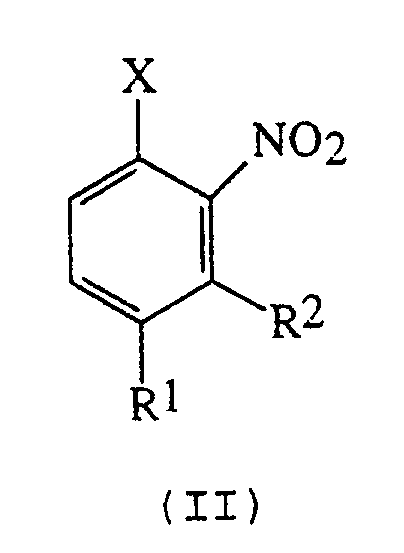
где R1 и R2 имеют вышеуказанные значения, а Х представляет атом фтора или брома, (a) с цианидом щелочного металла в безводном растворителе необязательно в присутствии катализатора в том случае, когда Х - атом фтора; или (b) с цианидом щелочного металла в присутствии каталитического количества цианистой меди (I) и межфазного катализатора в том случае, когда Х - атом брома, или взаимодействие соответствующего орто-нитрогалогенбензола формулы (II) с цианистой медью (I) необязательно в присутствии катализатора, выбираемого из бромида щелочного или щелочноземельного металла. Способ позволяет получать соединения орто-нитробензонитрила с высоким выходом и/или высокой селективностью. 17 з.п. ф-лы, 14 табл.
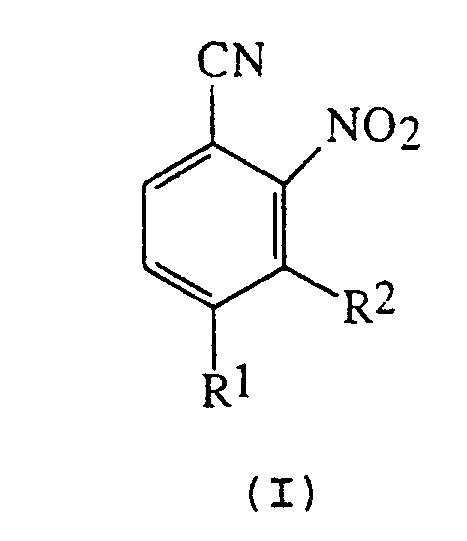
где R1 означает C1-4 гaлoгенaлкил;
R2 означает водород или C1-4алкокси,
включающий взаимодействие соответствующего ортонитрогалогенбензола формулы (II)
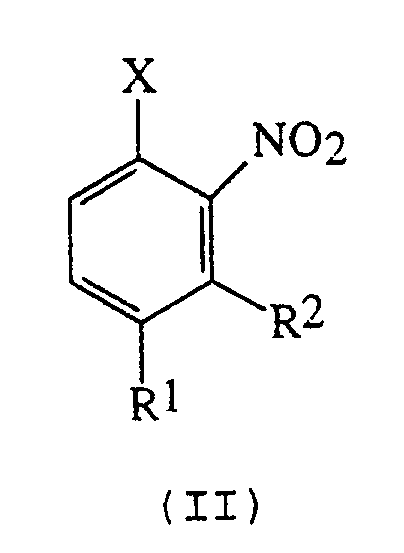
где R1 и R2 имеют вышеуказанные значения;
Х представляет атом фтора или брома,
(a) с циaнидoм щелочного металла в безводном растворителе необязательно в присутствии катализатора, в том случае, когда Х - атом Фтора; или (b) с цианидом щелочного металла в присутствии каталитического количества цианистой меди (I) и межфазного катализатора в том случае, когда Х - атом брома.
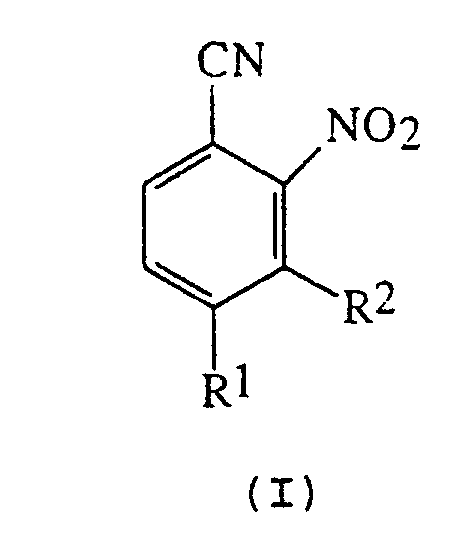
где R1 означает C1-4 гaлoгенaлкил;
R2 означает водород или C1-4 алкокси,
включающий взаимодействие соответствующего орто-нитрогалогенбензола формулы (II)
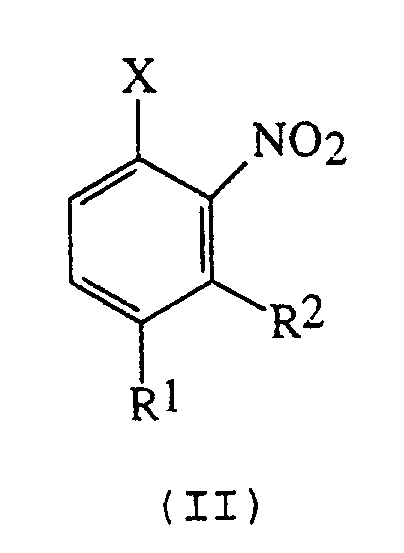
где R1 и R2 имеют вышеуказанные значения;
Х представляет атом брома,
с цианистой медью (I) необязательно в присутствии катализатора, выбираемого из бромида щелочного или щелочноземельного металла.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| EP 0758643 A2, 19.02.1997 | |||
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US 4886936 A, 12.12.1989 | |||
| СПОСОБ УПРАВЛЕНИЯ ЗАДЕРЖКАМИ РАСПРОСТРАНЕНИЯ СИГНАЛОВ | 1997 |
|
RU2195076C2 |
| Высокоуглеродистая сталь для инструмента холодной высадки | 1956 |
|
SU110559A1 |
| Механический тормоз | 1977 |
|
SU635303A1 |
| BACON and HILL | |||
| Metal Ions and Complexes in Organic Reactions | |||
| Part I | |||
| Substitution Reactions between Aryl Halides and Cuprous Salts in Organic Solvents | |||
| Journal of The Chemical Society | |||
| Прибор для заливки свинцом стыковых рельсовых зазоров | 1925 |
|
SU1964A1 |
| J.MARCH | |||
| Advanced Organic Chemistry, 1992, p.659 | |||
| US 3890326 A, 17.06.1975 | |||
| Сборно-разборный стеллаж | 1974 |
|
SU608713A1 |
| Способ получения гадоид замещенных 4-трифторметил-4"-нитродифениловых эфиров | 1974 |
|
SU559640A3 |
Авторы
Даты
2004-09-20—Публикация
1999-10-11—Подача