Изобретение может найти применение в фармакологии и для получения новых фотолюминесцентных препаратов.
Известен способ получения 2-(2'-тиенил)бензимидазола (Perry R., Wilson D. // J. Org. Chem 1993. Vol. 58. P. 7016-7021).
В реакционный сосуд, работающий под давлением, помещают 967 мг (8,94 ммоль) о-фенилендиамина, 1877,4 мг (8,94 смоль) 2-иодтиофена, 94 мг (0,13 ммоль) PdCl2 и 27 мл диметилацетамида. Затем из реактора аргоном удаляют кислород, после чего заполняют его оксидом углерода под давлением 35 дюймoв/м2 и выдерживают при температуре 120° С до растворения всех компонентов. Даже давление снижают до атмосферного и приливают в реактор 1,4 мл (12,0 ммоль) 2,6-лутидина. Затем в реакторе вновь создают давление CO и содержимое выдерживают 19 ч при 145° С. После чего от реакционной массы отделяют катализатор, а фильтрат концентрируют в вакууме, остаток растворяют в 25 мл горячего этанола, добавляют 2 мл NH4OH и 25 мл воды, и оставляют на ночь. Выпавшие кристаллы отделяют, промывают холодным водным раствором этанола и высушивают. Выход 588 мг (32%). Из фильтрата путем хроматографирования через слой селикагеля, элюент толуол:этилацетат (1:1), получено еще 104 мг (6%) продукта.
Наиболее близким является способ получения 2-(2'-фурил)-, 2-(2'-тиенил) и 2-(1'-метил-2-пирролил)бензимидазолов (Ельчанинов М.М., Олейникова Л.Я., Симонов А.М. // ХГС. 1979. №8. С.1047-1049, и Ельчанинов М.М., Симонов А.М., Олейникова Л.Я. // ХГС. 1980. №1. С.71-73).
Смесь 4,32 г (40 ммоль) о-фенилендиамина в 75 мл изопропилового спирта, 16 г (80 ммоль) ацетата меди в 200 мл воды и 40 ммоль соответствующего альдегида нагревают при 80-90° С 2 ч. Реакционную массу охлаждают, осадок медной соли отделяют, суспендируют ее в 150 мл изопропилового спирта и через суспензию пропускают сероводород в течение часа. Отфильтровывают сульфид меди, фильтрат упаривают вдвое, остаток разбавляют 250 мл воды, выпавший продукт отфильтровывают и сушат. Выход 67-90%.
Однако эти способы не являются достаточно общими, продолжительны во времени, имеют большую себестоимость, экологически небезопасны и не имеют преимуществ в сравнении с предлагаемым, с точки зрения технологичности и чистоты.
Задача изобретения – расширение ассортимента целых продуктов при упрощении и экологическом очищении процесса получения известных и новых 2-гетарилимидазолов.
Задача решается так, что конденсированные 2-гетарилимидазолы общей формулы

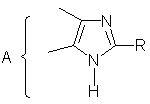
в отличие от структурного аналога, получают с использованием диамина общей формулы
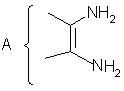
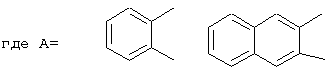
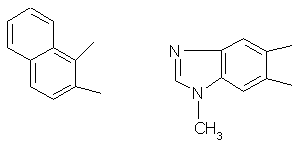
R=2-фурил, 2-тиенил, 2-(1-метл)пирролил 3-(1-метил)индолил,
и альдегидов в присутствии ацетата или сульфата меди путем кипячения в 50%-ной уксусной кислоте с последующим разложением медной соли, действием на ее суспензию в 50%-ной уксусной кислоте тиосульфата натрия при 100° С.
Эти условия значительно повышают экологическую чистоту и технологичность процесса в связи с тем, что ранее для разложения медной соли применялся длительный барботаж сероводорода через ее суспензию в спирте (Ельчанинов М.М., Олейникова Л.Я., Симонов А.М. // ХГС, 1979. №8. С.1047-1049).
Сероводород, как известно, - высокоопасное вещество 2 класса с очень низкой (0,008 мг/м3) предельно допустимой концентрацией, выбрасывался в атмосферный воздух.
Пример. Получение конденсированных 2-гетарилимидазолов (общая методика).
К нагретому до кипения раствору 40 ммоль диамина в 75 мл 50%-ной уксусной кислоты прибавляют 16 г (80 ммоль) ацетата ((СН3СОО)2Cu· Н2О) или 20 г (80 ммоль) сульфата (CuSO4·5Н2О) меди в 200 мл воды и 40 ммоль соответствующего альдегида в 50 мл 50%-ной уксусной кислоты. Полученную смесь нагревают до кипения в течение 1-2 ч. Затем реакционную массу охлаждают, осадок медной соли целевого продукта отделяют и суспендируют в 150 мл 50%-ного водного раствора уксусной кислоты. Суспензию нагревают до кипения и порциями в течение 0,5 ч вносят 20 г (80 ммоль) тиосульфата натрия (Na2S2O3·5Н2О) и после прибавления всего тиосульфата смесь выдерживают при слабом кипении еще 0,5 ч, после чего осадок сульфида меди отделяют. Сырой продукт реакции выпадает из маточного раствора при нейтрализации последнего концентрированным раствором аммиака. Выход 60-90%.
Предлагаемый метод позволяет синтезировать соединения, обладающие биологической активностью. Так, например, 2-(2'-фурил)- (1а) и 2-(2'-тиенил)бензимидазол (1б) обладают фунгицидной активностью (Preston P.N. // Chem Rews. 1974. Vol. 74. №3. P.311; Ельчанинов М.М. и др. // Авт. свид. №1032755, 1983).
Кроме того они являются синтонами для получения большой серии препаратов с фунгицидной и антимикробной активностью (Ельчанинов М.М. и др. // Авт. свид. №614630, 1978; Симонов А.М. и др. // Авт. свид. №677338, 1979; Олейникова Л.Я. и др. // Авт. свид. №704064, 1979; Симонов А.М. и др. // Авт. свид. №723853, 1979) и люминофоров (Печкин А.А. // Дисс. к.х.н., Новочеркасск, 2000, с. 92.).
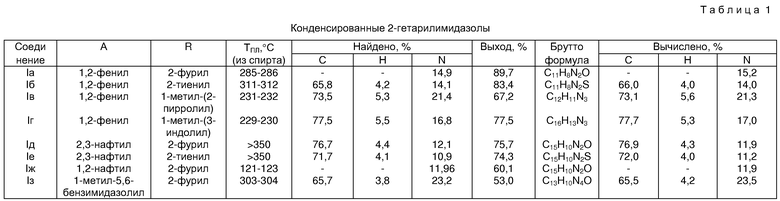
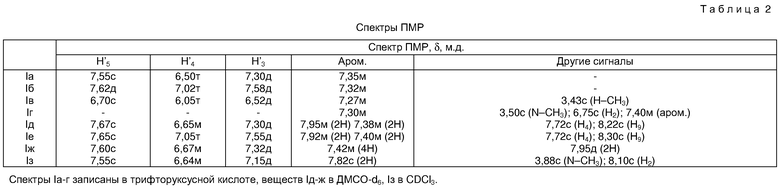
Физико-химические константы соединений представлены в таблицах 1 и 2.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ ПОКРЫТИЙ СПОСОБОМ АВТОФОРЕЗА | 2006 |
|
RU2298572C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4(5)-(2-ГЕТАРИЛ) И 4(5)-(2-ГЕТАРИЛ)-2-(2'-ГЕТАРИЛ)-ИМИДАЗОЛОВ | 2009 |
|
RU2400480C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ГЕТАРИЛПРОИЗВОДНЫХ БЕНЗОТИАЗОЛА И БЕНЗОКСАЗОЛА | 2008 |
|
RU2371442C1 |
| Способ получения 5-замещенного оксазолидин-2,4-диона | 1982 |
|
SU1264841A3 |
| Способ получения 5-замещенных оксазолидин-2,4-дионов | 1982 |
|
SU1151207A3 |
| Способ получения замещенных 2-аминобута-1,3-диен-1,1,3-трикарбонитрилов | 2022 |
|
RU2792619C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4-ДИАРИЛ(ГЕТАРИЛ)МАЛЕИМИДОВ | 2005 |
|
RU2278855C1 |
| Способ получения 1,3-бис- и 1,4-бис(4,5-ди[тиофен-3-ил]-1Н-имидазол-2-ил)бензолов | 2016 |
|
RU2614447C1 |
| Способ получения 5-замещенных оксазолидин-2,4-дионов или их фармацевтически приемлемых солей с щелочными металлами или кислотно-аддитивных солей в виде рацемата или оптически активного энантиомера | 1981 |
|
SU1194275A3 |
| НОВЫЕ ТИАЗОЛИДИНДИОНЫ И СОДЕРЖАЩИЕ ИХ ЛЕКАРСТВЕННЫЕ СРЕДСТВА | 1994 |
|
RU2122002C1 |
Изобретение относится к способу получения конденсированных 2-гетарилимидазолов общей формулы
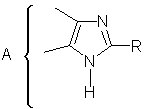
с использованием диамина общей формулы
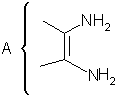
где А=
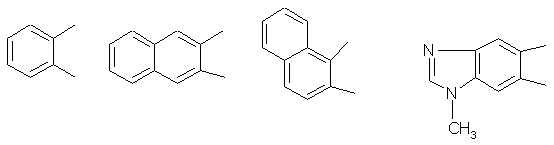
R=2-фурил, 2-тиенил, 2-(1-метил)пирролил, 3-(1-метил)индолил, и альдегидов в присутствии ацетата или сульфата меди, отличающийся тем, что взаимодействие происходит при кипячении в 50%-ной уксусной кислоте с последующим разложением медной соли, действием на ее суспензию в 50%-ной уксусной кислоте тиосульфата натрия при 100°С. Технический результат – повышение технологичности процесса. 2 табл.
Способ получения конденсированных 2-гетарилимидазолов общей формулы
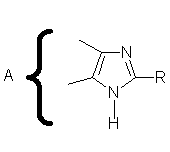
с использованием диамина общей формулы
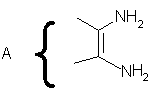
где А=
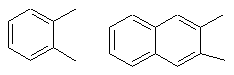

R=2-фурил, 2-тиенил, 2-(1-метил)пирролил, 3-(1-метил)индолил, и альдегидов в присутствии ацетата или сульфата меди, отличающийся тем, что взаимодействие происходит при кипячении в 50%-ной уксусной кислоте с последующим разложением медной соли, действием на ее суспензию в 50%-ной уксусной кислоте тиосульфата натрия при 100°С.
| ЕЛЬЧАНИНОВ М.М | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Химия гетероциклических соединений | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
| ЕЛЬЧАНИНОВ М.М | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Химия гетероциклических соединений | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Способ получения 2-гетерилзамещенных бензимидазола | 1975 |
|
SU541846A1 |
| Привод поворота планшайбы делительного стола | 1974 |
|
SU511187A1 |
Авторы
Даты
2004-10-10—Публикация
2002-12-17—Подача