Изобретение относится к области биологически активных соединений, касающихся фторированных производных бенз[4,5]-имидазо[1,2-b][1,3]-тиазолов, являющихся ингибиторами вируса кори. Изобретение может быть использовано в молекулярной биологии, вирусологии и медицине, а также в научных исследованиях.
Соединения бензимидазольного ряда занимают важное место среди лекарственных препаратов. Так, широко применяются спазмолитик дибазол, нейролептики пимозид, дроперидол, антигистаминный препарат астемизол и др. [1]. В то же время известно, что фторсодержащие соединения бензимидазольного ряда обладают более выраженной биологической активностью по сравнению с нефторированными аналогами [2].
Известны производные 5,6-дихлорбензимидазола, используемые в фармацевтических препаратах для лечения вируса герпеса (WO 96/01833, МПК С 07 Н 19/04, опубл. 25.01.1996).
Известны производные бензимидазола, обладающие антивирусной активностью, в частности, в отношении вируса герпеса (патент США №5998605, МПК С 07 Н 19/052, опубл. 07.12.1999).
Известны фторированные производные бензимидазола, обладающие активностью в отношении вируса герпеса (патент США №5840743, МПК С 07 D 405/04, А 61 К 31/215, опубл. 24.11.1998).
Однако вышеуказанные соединения не обладают активностью в отношении вируса кори.
Наиболее близким аналогом (прототипом) является рибавирин - 1-(β-d-рибофуранозил-1)-1,2,4-триазол-3-карбоксамид [3], используемый для лечения тяжелых случаев коревой инфекции. Проходя через клеточные мембраны, рибавирин метаболизирует, превращаясь в моно- и трифосфат. Монофосфат является конкурентным ингибитором инозинмонофосфат дегидрогеназы, что приводит к торможению синтеза РНК и ДНК вируса кори, слабо действуя на клетки хозяина.
Однако эффективность действия рибавирина на вирус кори недостаточна.
Техническим результатом предлагаемого изобретения является применение синтезированных соединений фторированных производных бензимидазола, действие которых более эффективно в отношении вируса кори, которые способны проникать внутрь клетки и обладают избирательной активностью в подавлении репродукции вируса.
Согласно изобретению предлагается применение фторированных производных бензимидазола - 2-ароил-3-метил-6,7-дифторбенз[4,5]-имидазо[2,1-b][1,3]-тиазолы общей формулы (1)
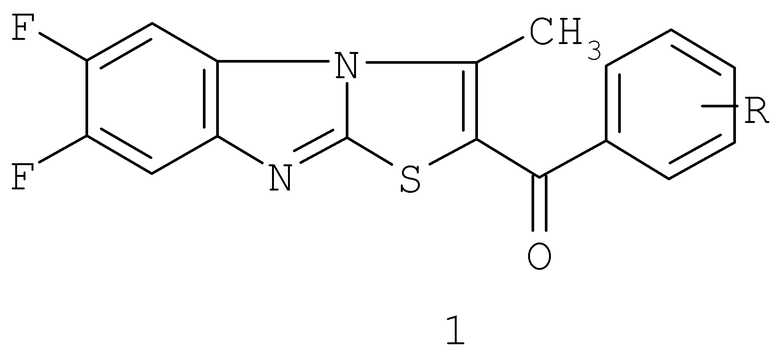
в качестве ингибиторов репродукции вируса кори.
На фиг.1 приведены данные по цитотоксичности и противовирусной активность соединения 1а при внесении в культуральную жидкость после адсорбции вируса кори.
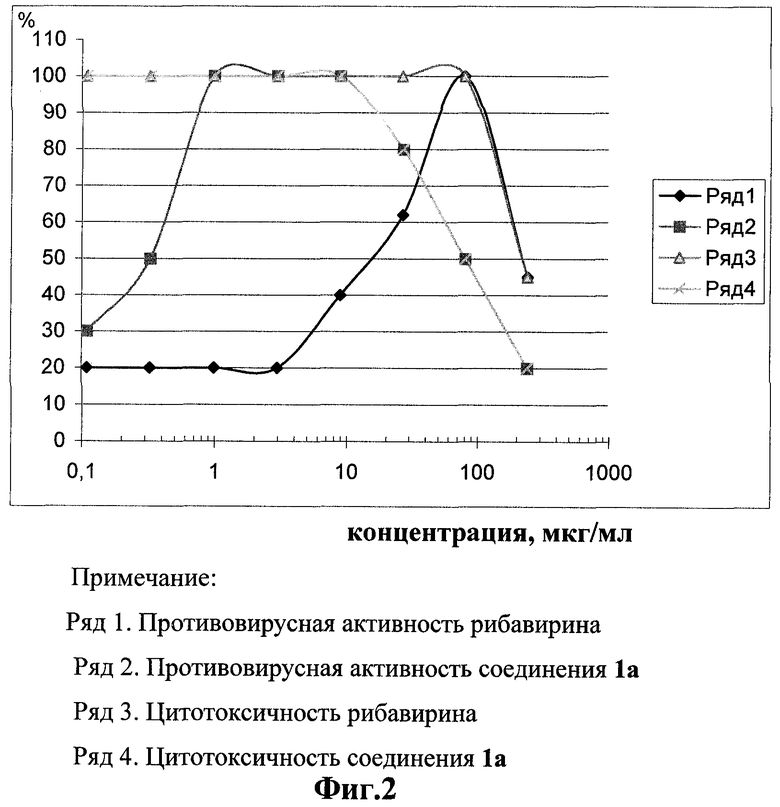
На фиг.2 приведены данные по цитотоксичности и противовирусная активность в отношении вируса кори соединения 1а и рибавирина.
Пример 1. Описание синтеза заявляемых соединений
Новые производные 2-ароил-3-метил-6,7-дифторбенз[4,5]-имидазо[2,1-b][1,3]-тиазолов синтезированы, как описано в [4].
2-Ароил-3-метил-6,7-дифторбенз[4,5]-имидазо[2,1-b][1,3]-тиазолы, подходящие для использования в качестве ингибиторов вируса кори, имеют общую формулу (1) и содержат в качестве фрагментов R атом водорода, ацилированную аминогруппу, атом или атомы галогена, гидроксигруппу, ацилированную гидроксигруппу, нитрогруппу, метальную группу, метоксигруппы или фенил.
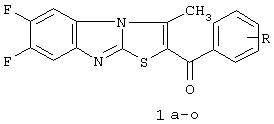
R=Н (1a), NHCOCH3 (1б), 4-Сl (1в), 4-Вr (1г), 4-ОН (1д), 4-ОСОСН3 (1е), 4-NО2 (1ж), 3-NO2 (1з), 2-СН3 (1и), 2,4-Сl2 (1к), 3,4-Cl2 (1л), 2,4-(ОСН3)2 (1м), 3,4(ОСН3)2 (1н), 4-Рh(1о).
Синтез исходного 2-меркапто-5,6-дифторбензимидазола (III) был осуществлен по схеме 1. При восстановлении 2-нитро-4,5-дифторанилина (I) [5] водородом в присутствии катализатора Ni-Ra образуется диамин (II), конденсацией которого с сероуглеродом в этаноле в присутствии триэтиламина получен бензимидазол (III).
Схема 1
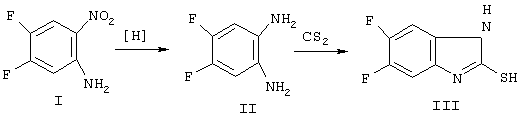
Реакцией 2-меркапто-5,6-дифторбензимидазола (III) с алифатическими кетонами, такими как: ацетон, метилэтилкетон, ацетилацетон, бензоилацетон, ацетоуксусный эфир, в уксусной кислоте в присутствии каталитических количеств серной кислоты мы получили соответствующие 2-R-3-метил-6,7-дифтор-бензимидазо[2,1-b]тиазолы (IVa-д) с выходами 30-40%. Алициклические кетоны, такие как: циклопентанон, циклогексанон, циклогептанон, в реакции с тиолом (III) в аналогичных условиях (АсОН-Н2SO4) образуют тетрациклические соединения (Va-в) с выходами 45-60% (схема 2).
Схема 2
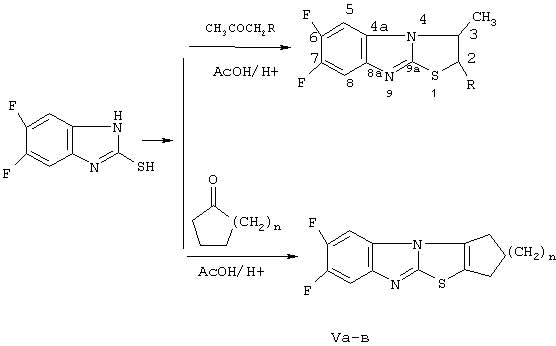
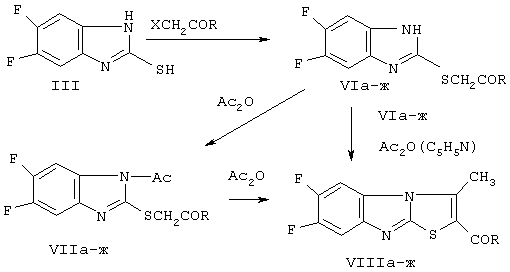
По реакции тиола (III) с α-галогенкетонами при комнатной температуре в этаноле в присутствии триэтиламина получены замещенные 2-фенацилтио-5,6-дифторбензимидазолы (VIa-ж) (схема 3).
Схема 3
Пример 2. Исследование биологической активности заявляемых соединений
Ингибирование репродукции вируса кори исследовали в первично инфицированных клетках почки зеленой мартышки Vero в присутствии экспериментального препарата, конечная концентрация которого в культуральной среде составляла 0,1-400 мкг/мл, на протяжении одного пассажа - в течение 5 суток. Об ингибировании исследуемым соединением репродукции вируса в культуре чувствительных клеток судили по снижению вирус-индуцированного цитопатического действия в присутствии препарата по сравнению с контролем. В качестве препарата сравнения использовали рибавирин (прототип).

Из полученных экспериментальных данных, приведенных в таблице, видно, что выраженное противовирусное действие в отношении вируса кори (значительно выше, чем у рибавирина) проявило соединение 1a (R=Н), менее активно - соединение 1б (R=NHCOCH3), остальные соединения 1в-о оказались слабоактивными или неактивными.
Пример 3. Оценка цитотоксичности фторированных производных бенз[4,5]-имидазо[1,2-b][1,3]-тиазолов
Цитотоксичность соединений оценивали путем добавления разведении каждого препарата в среде DMEM к монослою клеточной культуры Vero в лунки 96-луночного планшета ("Cel-Cult", England), до конечных концентраций 0,1-400 мкг/мл (по три лунки на каждую дозу) с последующим культивированием при 37°С в СО2-инкубаторе в течение 5 суток. Контролем служили клетки без добавления исследуемого соединения. Жизнеспособность клеток оценивали по оптической плотности (при 570 нм) после окрашивания раствором кристаллического фиолетового (1,3 г красителя, 50 мл этанола, до 700 мл H2O, 300 мл 40% формалина) в течение 1,5 ч при комнатной температуре. Токсичность различных доз соединений определяли по жизнеспособности клеток относительно контроля, по полученным результатам рассчитывали дозу, на 50% снижающую жизнеспособность клеток (CD50). Данные представлены в таблице.
Пример 4. Исследование влияния фторированных производных бенз[4,5]-имидазо[1,2-b][1,3]-тиазолов на репродукцию вируса кори в культуре клеток Vero.
Исследование противовирусной активности экспериментальных препаратов в отношении вируса кори проводили на перевиваемой линии чувствительных клеток почки зеленой мартышки Vero. Для заражения использовали коммерческую вакцину кори, полученную в ГНЦ ВБ “Вектор” (сер.276 от 08.02.01). Множественность заражения составляла 0,2-0,5 инфекционных единиц на клетку. В лунки 96-луночного планшета ("Cel-Cult", England) помещали суспензию клеток Vero с посевной концентрацией 150 тыс.кл./мл, инкубировали 2 суток при 37°С в СО2-инкубаторе. После формирования монослоя из лунок планшета удаляли культуральную жидкость, вносили вирус (15 мкл) и одновременно такой же объем ростовой среды с исследуемым соединением до конечной концентрации 0,1-400 мкг/мл (по три лунки на каждую дозу). Контролем служили инфицированные клетки Vero без добавления препарата (вместо препарата вносили такое же количество среды DMEM без добавок) и неинфицированные клетки.
Адсорбцию вируса проводили в течение 1,5 ч при 37°С в СО2-инкубаторе. Затем в лунки вносили питательную среду DMEM с добавлением 2% фетальной сыворотки КРС, предварительно инактивированной прогреванием при 56°С в течение 30 мин, 100 мкг/мл гентамицина, 100 мкг/мл линкомицина с исследуемым соединением до конечной концентрации 0,1-400 мкг/мл. В контрольные лунки вносили питательную среду со всеми добавками, но без препарата. Через 5 суток культивирования удаляли культуральную жидкость, вносили по 30 мкл раствора кристаллического фиолетового в каждую лунку, выдерживали 1,5 ч при комнатной температуре и измеряли оптическую плотность на спектрофотометре при длине волны 570 нм. Относительную степень защиты инфицированных клеток рассчитывали по формуле
Защита (%)=(А-O)/(В-O)·100%,
где А - % жизнеспособности инфицированных клеток в присутствии соединения на 5 сутки культивирования, В - % жизнеспособности в контроле клеток, О - % жизнеспособности инфицированных клеток без добавления соединения (контроль вируса).
По полученным данным строили график зависимости защиты клеток от возрастающих доз соединения (для соединения 1а и рибавирина, см. фиг.2) и находили дозу препарата, на 50% защищающую клетки (ED50). Терапевтический индекс, или индекс селективности (IS), определяли как отношение концентрации соединения, токсичной для 50% клеток (СD50), к концентрации, на 50% защищающей клетки от гибели (ЕD50):
IS=CD50/ED50.
Пример 5. Исследование влияния соединения 1а на репродукцию вируса кори при внесении в культуральную среду после адсорбции вируса
Исследование проводили на перевиваемой линии чувствительных клеток почки зеленой мартышки Vero. После формирования монослоя из лунок планшета удаляли культуральную жидкость, вносили вирус (15 мкл), множественность заражения составляла 0,2-0,5 инфекционных единиц на клетку. Адсорбцию вируса проводили в течение 1,5 ч при 37°С в СО2-инкубаторе. Затем в лунки вносили питательную среду DMEM с добавлением 2% фетальной сыворотки КРС, 300 мг/мл L-глютамина, 100 мкг/мл гентамицина, 100 мкг/мл линкомицина с исследуемым соединением до конечной концентрации 0,1-400 мкг/мл. Контролями служили инфицированные (контроль вируса) и не инфицированные (контроль клеток) клетки Vero. Через 5 суток культивирования удаляли культуральную жидкость, вносили по 30 мкл раствора кристаллического фиолетового в каждую лунку, выдерживали 1,5 ч при комнатной температуре и измеряли оптическую плотность на спектрофотометре при длине волны 570 нм.
По полученным данным строили график зависимости защиты клеток от возрастающих доз соединения (фиг.1) и находили дозу препарата, на 50% защищающую клетки (ED50). Терапевтический индекс, или индекс селективности (IS), определяли как отношение концентрации соединения, токсичной для 50% клеток (СD50), к концентрации, на 50% защищающей клетки от гибели (ED50):
IS=CD50/ED50.
Как видно из данных, представленных на фиг.1, CD50=81 мкг/мл, ED50=0,7 мкг/мл, IS=115,7. Таким образом, эффективная доза соединения 1а при внесении его одновременно с вирусом (см. таблицу) ниже эффективной дозы этого соединения при добавлении после адсорбции вируса в 2,1 раза.
Пример 6. Исследование токсичности соединения 1а на нелинейных мышах
Исследование проводили на нелинейных белых мышах массой 20-21 г. Соединение 1а растворяли в диметилсульфоксиде (ISN) до концентрации 20 мг/мл. Затем из этого раствора готовили раствор соединения 1а в стерильном физиологическом растворе в концентрации 8 мг/мл (максимально возможная концентрация), 4 мг/мл, 2 мг/мл, 1 мг/мл. По 0,5 мл каждого раствора вводили мышам внутрибрюшинно, используя по 4 животных на каждое разведение. Наблюдение вели в течение 7 суток. Через 7 суток после внутрибрюшинного введения раствора, содержащего препарат 1а, ни в одной группе мыши не погибли, что свидетельствует о невысокой токсичности этого соединения in vivo.
Таким образом, показано, что соединения 1а и 1б при умеренной цитотоксичности в культуре клеток Vero обладают выраженной противовирусной активностью относительно вируса кори (терапевтические индексы равны 245,5 и 8 соответственно).
Соединение 1а по своим противовирусным свойствам значительно превосходит препарат сравнения рибавирин. Представляется перспективной разработка лекарственного препарата на основе соединения 1а для терапии инфекций, вызванных вирусом кори.
Список научно-технической и патентной информации
1. Машковский М.Д. Лекарственные средства. М.: Медицина, 1993, т. 1, 2.
2. Bouzard D. // Antibiotics and Antiviral Compounds. Chemical Synthesis and Modification. Eds. R.Krohn, H.A.Kirst, H.Maag. Weinheim. - N. Y.: VCH Publishers Inc., 1993. P.187-203.
3. Mason W.H. Measles. // Adolesc. Med. 1995. V. 6. P.1-14.
4. Котовская С.К., Перова Н.М., Баскакова З.М., Романова С.А., Чарушин В.Н., Чупахин О.Н. // ЖОрХ. 2001. Т. 37. С.598-603.
5. Котовская С.К., Чарушин В.Н., Чупахин О.Н., Кожевникова Е.О. // ЖОрХ. 1998. Т. 34. Вып.3. С.399-404.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2`-АМИНО-2`-ДЕЗОКСИНУКЛЕОЗИДЫ - ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСОВ КОРИ И МАРБУРГ | 2003 |
|
RU2264409C2 |
| N'-{N-[3-ОКСО-20(29)-ЛУПЕН-28-ОИЛ]-9-АМИНОНОНАНОИЛ}-3-АМИНО-3-ФЕНИЛПРОПИО НОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2211843C1 |
| ГЛИКОПЕПТИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С S-БЕНЗИЛ-L-ЦИСТЕИНОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ АКТИВНОСТЬ | 2001 |
|
RU2198177C2 |
| ГЛИКОПЕПТИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С ГЛИЦИЛ-L-ФЕНИЛАЛАНИНОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ-1 АКТИВНОСТЬ | 2006 |
|
RU2315058C1 |
| 2-[6-МЕТИЛ-3-(ТИЕН-2-ИЛ)-5-ФЕНИЛ-5,6-ДИГИДРО-4Н-[1,2,4,5]ТЕТРАЗИН-1-ИЛ]-БЕНЗОТИАЗОЛ С ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСОВ КОКСАКИ В3 | 2023 |
|
RU2836398C1 |
| 4-НИТРО-6-ТРИФТОРМЕТИЛ-1,2,3-БЕНЗОТРИТИОЛ-1-ОКСИД В КАЧЕСТВЕ ИНГИБИТОРА РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2007 |
|
RU2366419C2 |
| УСНИНОВАЯ КИСЛОТА И ЕЕ ОКИСЛЕННОЕ ПРОИЗВОДНОЕ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПРОДУКЦИИ ВИРУСА ГРИППА | 2011 |
|
RU2464033C1 |
| 3,28-ДИ-О-НИКОТИНАТ БЕТУЛИНА, ПРОЯВЛЯЮЩИЙ ГЕПАТОПРОТЕКТОРНУЮ И АНТИ-ВИЧ АКТИВНОСТЬ | 1999 |
|
RU2174982C2 |
| 2',3'-ДИДЕГИДРО-2',3'-ДИДЕЗОКСИТИМИДИН-5'[(ЭТОКСИКАРБОНИЛ)(ЭТИЛ)ФОСФОНАТ]- ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2000 |
|
RU2188203C2 |
| N'-{N-[3-ОКСО-ЛУПАН-28-ОИЛ]-9-АМИНОНОНАНОИЛ}-3-АМИНО-3-ФЕНИЛ-ПРОПИОНОВАЯ КИСЛОТА И ЕЕ СОЛИ КАК ПРОТИВОВИРУСНЫЕ И ИММУНОСТИМУЛИРУЮЩИЕ АГЕНТЫ | 2006 |
|
RU2317996C1 |
Изобретение относится к области молекулярной биологии, вирусологии и медицины. 2-Ароил-3-метил-6,7-дифторбенз[4,5]-имидазо[2,1-b][1,3]-тиазолы общей формулы (1а-о)
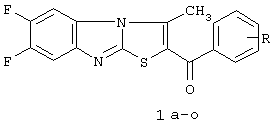
в которой R является водородом, бромом, хлором гидрокси, группой NHCOCH3, -ОСОСН3, нитро, метилом, метокси или фенолом, являются эффективными ингибиторами вируса кори. Соединения 1а и 1в обладают способностью ингибировать репродукцию вируса кори в перевиваемой культуре клеток почки зеленой мартышки Vero. Антивирусная активность соединения 1а в отношении вируса кори значительно превосходит активность рибавирина. Изобретение расширяет арсенал средств указанного назначения. 1 табл., 2 ил.

Применение фторированных производных 2-ароил-3-метил-6,7-дифторбенз[4,5]-имидазо[2,1-b][1,3]-тиазолы общей формулы (1 а-о)
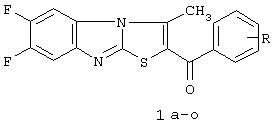
где R=Н (1a), NHCOCH3 (1б), 4-Сl (1в), 4-Вr (1г), 4-ОН (1д), 4-ОСОСН3 (1е), 4-NO2 (1ж), 3-NO2 (1з), 2-СН3 (1и), 2,4-Cl2 (1к), 3,4-Сl2 (1л), 2,4-(ОСН3)2 (1м), 3,4(ОСН3)2 (1н), 4-Рh (1о),
в качестве ингибиторов репродукции вируса кори.
| ПРОТИВОВИРУСНОЕ СРЕДСТВО | 1991 |
|
RU2005475C1 |
| СРЕДСТВО ОТ ПРОСТУДЫ | 2000 |
|
RU2163121C1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| УСТРОЙСТВО ПОГЛОЩЕНИЯ УДАРОВ ДЛЯ АВТОТРАНСПОРТНОГО СРЕДСТВА | 2013 |
|
RU2609632C2 |
| КОТОВСКАЯ С.К | |||
| и др | |||
| Фторсодержащие гетероциклы IV | |||
| Синтез производных бензимидазола | |||
| Журнал органической химии, 2001, т.37, вып.4, с.598-603 | |||
| КОТОВСКАЯ С.К | |||
| и др | |||
| Фторсодержащие гетероциклы II | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Журнал органической химии, 1998, т.34, вып.3, с.399-404. | |||
Авторы
Даты
2004-10-20—Публикация
2003-08-07—Подача