Изобретение относится к медицине, а именно к лечению бруцеллеза.
Известен способ лечения бруцеллеза антибиотиками. Недостатком этого способа является снижение эффективности в лечении данной инфекции ранее применяемых антибиотиков, связанное с их низкой способностью проникать внутрь клетки и с развивающейся резистентностью бруцелл к ним. Кроме того, при бруцеллезе наблюдается выраженное угнетение клеточного иммунитета и неспецифической резистентности организма, что приводит к накоплению в фагосомах жизнеспособных бруцелл, способных к размножению и к развитию хронического инфекционного процесса. Длительный курс антибиотикотерапии еще более усиливает иммунодепрессию.
Известен способ лечения бруцеллеза, в котором антибиотики применяются в сочетании с иммуномодуляторами (Таран И.Ф., Швецова Н.М., Сафронова В.М. Влияние иммуномодуляторов на развитие инфекционного и вакцинального процессов, а также на эффективность лечебных препаратов при бруцеллезе. ЖМЭИ. - 1993. - №6.-С.88-89; Thornes R.D. The energy of chronic human brucellosis. J. Irish Med. Assoc. - 1977. - V. 70.- P. 480-483).
Такой способ позволяет воздействовать на иммунную систему макроорганизма. Применяемые иммуномодуляторы активизируют фагоцитарные клетки и стимулируют неспецифическую резистентность организма, но, однако, зачастую и при комплексном применении антибиотиков и иммуномодуляторов наблюдается недостаточная эффективность проведенной терапии, возникают рецидивы и переход болезни в хроническую форму.
Технической задачей изобретения является снижение обсемененности возбудителем организма животных или людей за счет доставки к клеткам-мишеням антибиотиков в максимальной терапевтической дозе с пролонгацией их действия, а также за счет активации иммунной системы организма.
Сущность изобретения заключается в том, что заявляемый способ основан на пероральном применении липосомальных форм ликопида или левамизола в сочетании с азитромицином или рифампицином для лечения бруцеллезной инфекции.
Липосомальные формы лекарств в настоящее время применяются для лечения инфекционных заболеваний. Липосомы позволяют доставлять лекарство к клеткам-мишеням, способствуют преодолению мембранно-клеточных барьеров. Использование их в качестве носителей лекарств обеспечивается уникальностью их совокупных свойств, таких как отсутствие токсичности, иммуногенности и аллергических реакций организма, в ответ на введение липосом, а также их биосовместимость, биодеградируемость и способность пролонгировать действие иммобилизованных в них веществ с доставкой последних внутрь клеток [4]. В макроорганизме липосомальные антибиотики захватываются клетками мононуклеарной фагоцитарной системы, а в органах, содержащих большое количество макрофагов, создается повышенная концентрация препарата, причем на более длительный промежуток времени, чем при использовании свободного антибиотика.
В настоящее время липосомальные формы антибиотиков применяются при лечении бруцеллезной инфекции (Тихонов Н.Г., Ротов К.А. Перепелкин А.И. Липосомальный гентамицин в лечении экспериментального бруцеллеза. // Проблемы биологической и экологической безопасности: Междунар. конф. - Оболенск, 2000.- С. 95-96; Vitas A.I., Diaz R.., Gamazo C. Protective effect of liposomal gentamicin against systemic acute murine brucellosis. // Chematherapy. - 1997.- V.43, №3. - P. 204-210).
Технический результат заявляемого способа, а именно увеличение эффективности лечения бруцеллеза, обеспечен за счет применения дополнительно в лечении бруцеллеза иммобилизованных в липосомы ликопида или левамизола, что является существенным отличительным признаком и критерием патентоспособности “новизна”.
Заявляемый способ осуществлялся следующим образом.
Проводили изучение действия антибактериальных (азитромицина, рифампицина) и иммуномодулирующих (ликопида, левамизола) средств, эффективных при бруцеллезной инфекции и различающихся механизмом действия, на результаты лечения бруцеллеза.
Применение ликопида, левамизола и липосом при лечении бруцеллеза известно, но только в заявляемом способе используются ликопид или левамизол, иммобилизованные в липосомальные везикулы для лечения хронической бруцеллезной инфекции.
В лечении инфекционных заболеваний липосомальные формы лекарств используются в инъекционной форме. При длительно протекающих хронических инфекциях пероральное применение лекарственных средств является более предпочтительным, чем парентеральное. В заявляемом способе липосомальные формы иммуномодуляторов применяются перорально.
Липосомы готовили из фосфатидилхолина, холестерина и дицетилфосфата (“Sigma”, США) в молярных соотношениях 7:2:1. Для получения “пустых” липосом использовали метод “выпаривания в обращенной фазе” [5]. Иммуномодуляторы включали в липидные везикулы путем “замораживания-оттаивания” [6]. Липосомы с иммобилизованным веществом отделяли от свободного препарата диализом против фосфатно-солевого буфера, рН 7,4. Количество связанного иммуномодулятора определяли методом серийных разведении [3] после разрушения липосом 1% раствором дезоксихолата натрия при 70±1°С. Для лечения использовали липосомы с высоким содержанием антибиотика, включение которого в липосомальные везикулы составляло 72±3,3%. Электронно-микроскопический контроль образования липосом осуществляли при исследовании как нативных препаратов липосом, так и их ультратонких срезов [1].
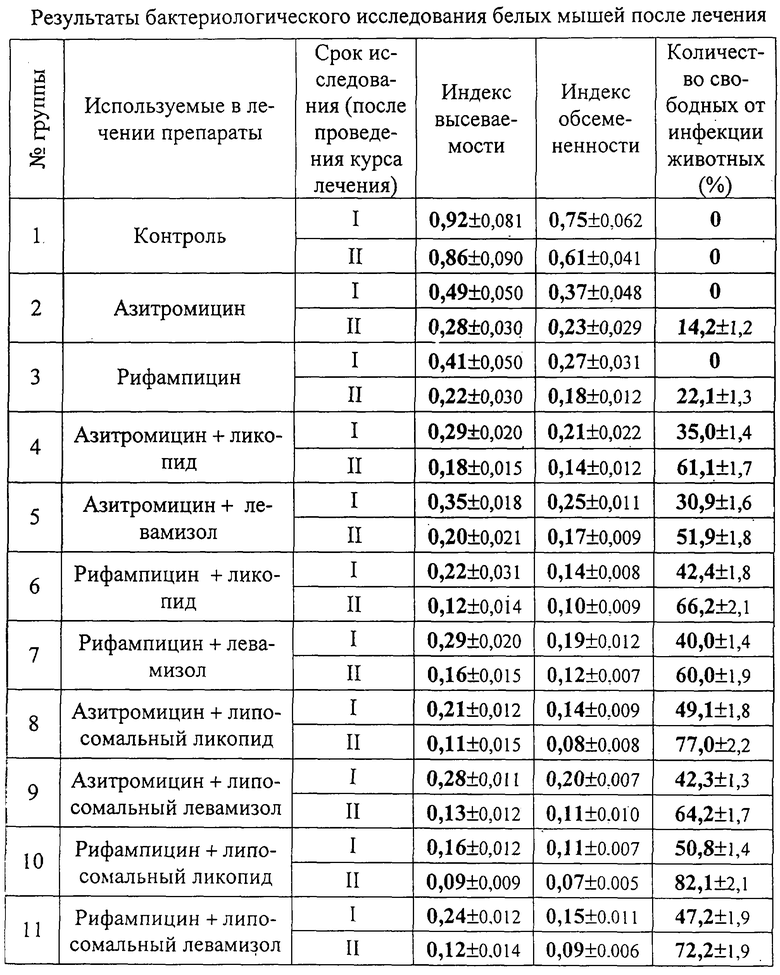
Эффективность липосомальных форм иммуномодуляторов в комплексном лечении бруцеллеза изучали на белых мышах, чувствительность которых к бруцеллам наиболее близка к чувствительности организма человека. Это позволяет экстраполировать полученные в опытах на клинические условия. Хроническую бруцеллезную инфекцию моделировали путем подкожного введения белым мышам высоковирулентного штамма Brucella melitensis 565 в дозе 0,5·105 микробных клеток в 0,5 мл 0,9% хлорида натрия, рН 7,2. Лечение начинали с 21 суток после инфицирования и проводили 2 курсами с интервалом 10 суток. Животным 1 группы (контрольная) - лечение не проводили; биологическим моделям 2 и 3 групп вводили только антибиотик; 4, 5, 6 и 7 групп - антибиотик и иммуномодулятор в свободной форме; 8, 9, 10 и 11 групп - антибиотик в комплексе с иммуномодулятором, иммобилизованным в липосомы (таблица).
Антибиотики вводили перорально в субтерапевтических дозах: азитромицин (“Сумамед”, Плива, Республика Хорватия) курсовой дозой 2,7 мг/мышь в течение 3 суток; рифампицин (ЗАО “Брынцалов А”, Москва) курсовой дозой 5 мг/мышь в течение 10 суток. Применяемые иммуномодуляторы левамизол и ликопид имеют разный механизм действия, но оба оказывают активизирующее влияние на систему фагоцитоза, гуморальный и клеточный иммунитет, неспецифическую резистентность организма [2, 7]. Свободные и липосомальные иммуномодуляторы вводили перорально однократно в начале каждого курса лечения: левамизол (“Декарис”, Гедеон Рихтер А.О., Будапешт, Венгрия) по 50 мкг/мышь, ликопид (ЗАО Пептек, Москва) по 100 мкг/мышь.
Животных исследовали через 14 суток после окончания каждого курса лечения, поскольку на 10-12 сутки после завершения антибиотикотерапии в случае сохранения жизнеспособных бруцелл в клетках ретикулоэндотелиальной системы белых мышей происходит выход микробов в кровяное русло и наблюдается активизация инфекции. О степени элиминации бруцелл из организма экспериментальных животных судили по данным бактериологического анализа, который проводили путем посева гомогенизированных паховых, аксиллярных, подчелюстных, парааортальных лимфоузлов и селезенки, взятых от умерщвленных животных, на агар Альбими, рН 7,2. Критерием интенсивности бактериальной обсемененности организма мышей служили: индекс высеваемости - частное от деления количества органов с положительными высевами на количество всех исследованных органов; индекс обсемененности - отношение суммы баллов, характеризующих рост, к сумме возможного максимального количества баллов; количество свободных от инфекции животных.
Статистическую обработку полученных результатов проводили общепринятыми методами с определением средних арифметических, средней ошибки средних арифметических, достоверности различий. Различия считали достоверными при р<0,05.
По данным эксперимента, представленным в таблице 1, следует, что у животных 1 (контрольной) группы продолжался генерализованный инфекционный процесс на протяжении всего эксперимента. Во 2 и 3 группах биологических моделей, подвергшихся только антибиотикотерапии в субтерапевтических дозах, бактериологические индексы были снижены в оба срока исследования, но оставались достаточно высокими. Свободных от инфекции животных после 1 курса лечения не было, а после 2 курса 14,2±1,2% зверьков, леченных азитромицином, и 22,1±1,3% мышей, получавших рифампицин, освободились от бруцелл.
Проведение лечения экспериментальной бруцеллезной инфекции белых мышей с использованием азитромицина или рифампицина в субтерапевтических дозах в комплексе со свободными формами ликопида или левамизола (4-7 группы) приводило к более выраженному снижению всех бактериологических показателей по сравнению с результатами лечения в режиме антибактериальной монотерапии. При этом бактериологические индексы достоверно снижались, а количество освободившихся от инфекции мышей значительно увеличивалось.
Результаты экспериментов показали, что пероральное введение липосомальных форм иммуномодуляторов белым мышам с экспериментальной бруцеллезной инфекцией способствовало более выраженному снижению интенсивности обсемененностн возбудителем организма биологических моделей и в значительной степени повышало эффективность этиотропного лечения бруцеллеза. Использование в комплексном лечении экспериментального бруцеллеза липосомальных форм как ликопида, так и левамизола существенно влияло на интенсивность элиминации бруцелл из организма биологических моделей. Наблюдалось более выраженное снижение индексов высеваемости и обсемененности и увеличение количества свободных от инфекции животных после окончания лечения, чем после проведенного лечения с использованием свободных форм ликопида или левамизола.
Липосомальный ликопид способствовал увеличению количества свободных от бруцелл мышей на 16,0±1,0%, а липосомальный левамизол - на 12,2±0,9% по сравнению с результатами терапии с применением азитромицина или рифампицина и интактных ликопида или левамизола.
Таким образом, установлено, что при лечении экспериментальной бруцеллезной инфекции липосомальные формы иммуномодуляторов (левамизола или ликопида) имеют преимущество перед их свободными формами при пероральном пути их введения в организм биопробных животных.
Источники информации
1. Закревский В.И., Ефременко В.И., Мельников В.А с соавт. Приготовление липосом, содержащих биологически активные вещества. Методические рекомендации. - Волгоград, 1982. - 23 с.
2. Иванов В.Т., Хаитов P.M., Андронова Т.М., Пинегин Б.В. // Иммунология. - 1996. - №2. - С.4-6.
3. Инструкция по определению чувствительности возбудителей опасных инфекционных заболеваний к антибиотикам и химиопрепаратам. - М., 1990. - 36 с.
4. Швец В.И., Краснопольский Ю.М. Липиды в лекарственных препаратах // Вестн. Акад. мед.наук СССР. - 1990. - №6. - С. 19-28.
5. Cafiso D.С.. Petty H.R., McConnell H. Preparation of unilamellar lipid vesicles at 37°C by vaporization method.// Biochim. et biophys acta. - 1981. - Vol.649. - P. 129-131.
6. Pica U. Liposomes with a large trapping capability prepared by freezing // Arch. Biochem. and Biophys. - 1981. - Vol.212. - P. 186-194.
7. Symoens J., De Cree J., Van Bever W.T.M., Janssen P.A.J. // A. Ph. A. Acod. Pharm. Sci. - 1979. - V.2. - P. 407-464.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ БРУЦЕЛЛЕЗА | 2002 |
|
RU2234311C1 |
| СПОСОБ КОНТРОЛЯ ЭФФЕКТИВНОСТИ АНТИБИОТИКА ПРИ ЛЕЧЕНИИ БРУЦЕЛЛЕЗА | 2001 |
|
RU2206898C2 |
| СПОСОБ ПРОФИЛАКТИКИ БРУЦЕЛЛЕЗА КРУПНОГО РОГАТОГО СКОТА | 2008 |
|
RU2378011C1 |
| СПОСОБ ЛЕЧЕНИЯ БРУЦЕЛЛЕЗА КРУПНОГО РОГАТОГО СКОТА | 2013 |
|
RU2540428C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ БРУЦЕЛЛЕЗА | 2002 |
|
RU2230572C1 |
| СПОСОБ ПРОФИЛАКТИКИ БРУЦЕЛЛЕЗА | 2002 |
|
RU2238759C2 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ХРОНИЧЕСКИМ БРУЦЕЛЛЕЗОМ | 2008 |
|
RU2367490C1 |
| АНТИБАКТЕРИАЛЬНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПТИЦ, СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЦЫПЛЯТ ПРИ ЗАБОЛЕВАНИЯХ БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ, СПОСОБ ЛЕЧЕНИЯ РЕСПИРАТОРНОЙ БОЛЕЗНИ ТЕЛЯТ БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ, СПОСОБ ПРОФИЛАКТИКИ ТУБЕРКУЛЕЗА У КРУПНОГО РОГАТОГО СКОТА | 1999 |
|
RU2158587C1 |
| СПОСОБ ИММУНИЗАЦИИ ЖИВОТНЫХ ПРОТИВ БРУЦЕЛЛЕЗА | 2013 |
|
RU2554055C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМ С ИНКАПСУЛИРОВАННЫМ ДОКСИЦИКЛИНОМ ГИДРОХЛОРИДОМ И ПОВЕРХНОСТНО ЛОКАЛИЗОВАННЫМИ МОНОКЛОНАЛЬНЫМИ АНТИТЕЛАМИ | 2015 |
|
RU2582969C1 |
Изобретение относится к медицине, к инфекционным болезням и может быть использовано для лечения бруцеллеза. Используют антибиотик и иммунокорректор, при этом иммунокорректор иммобилизован в липосому и его вводят перорально. Данное изобретение способствует ускорению элиминации бруцелл из организма. 1 табл.
Способ лечения бруцеллеза, включающий применение антибиотика в сочетании с иммунокоррекцией, отличающийся тем, что иммунокоррекцию проводят иммобилизованным в липосому иммуномодулятором перорально.
| ТИХОНОВ Н.Г | |||
| И ДР | |||
| Липосомальный гентамицин в лечении экспериментального бруцеллеза | |||
| Проблемы биологической и экологической безопасности | |||
| Международная конференция | |||
| - Оболенск, 2000, с | |||
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| МАРКОВА И.В | |||
| и др | |||
| Фармакология | |||
| Издание второе, переработанное и дополненное | |||
| - СПб.: Фолиант, 2001, с | |||
| Замкнутая радиосеть с несколькими контурами и с одной неподвижной точкой опоры | 1918 |
|
SU353A1 |
| ШВЕЦ В.И | |||
| и др | |||
| Липиды в лекарственных препаратах | |||
| Вестник Академии медицинских наук СССР, 1990, №6, с | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| RU 94023720 A1, 10.01.1996 | |||
| RU 94027343 A1, 27.09.1996 | |||
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ТОНЗИЛЛИТА | 2000 |
|
RU2163130C1 |
| ПРЕПАРАТ АБАКТАН ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ ЖИВОТНЫХ | 1997 |
|
RU2111744C1 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА ОРГАНОВ ДЫХАНИЯ С ВЫРАЖЕННОЙ ЭКССУДАТИВНОЙ РЕАКЦИЕЙ У ДЕТЕЙ | 2000 |
|
RU2189234C2 |
| ГЕТЕРОВЕЗИКУЛЯРНЫЕ ЛИПОСОМЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2120795C1 |
| ЭЛЕКТРОДНЫЙ УЗЕЛ ДЛЯ УСТРОЙСТВ ЭЛЕКТРОТЕРАПИИ | 2002 |
|
RU2328321C2 |
Авторы
Даты
2004-11-10—Публикация
2002-12-15—Подача